初三化学模拟试卷(含答案)

上海市黄浦区2009初三化学模拟考
(满分60分)
相对原子质量(原子量):H-1O-16 F-19 Na-23P-31 Cl-35.5
六、单项选择题: (本题共20分)
27.不属于化学研究范畴的是
A.研制新型的高能催化剂
B.设计开发新的电脑程序
C.生产无毒高效的新农药
D.制造符合环保的新材料
28.生活中的常见现象,属于化学变化的是
A.酒精挥发 B.石灰浆变硬 C.冰受热熔化D.用木炭消除冰箱中的异味
29.人们常用的物质中属于纯净物的是
A.铝合金门窗B.新鲜牛奶C.医用酒精D.体温计中的水银
30.关于元素符号书写正确的是
A.钡Ba
B.铝AL
C. 汞hg
D.硅SI
31.氢气是清洁的燃料,它由氢分子构成。能表示两个氢分子的化学符号是
A.2H2B.H2 C.2H D.2H2O
32.“民以食为天”,在这些可食用的物质中不属于有机物的是
A.食盐B.酒精C.淀粉D.葡萄糖
33.几种物质的化学式、俗名和名称相对应的是
A.CO 水煤气一氧化碳B.CuSO4·5H2O 胆矾硫酸铜
C.CaO 消石灰氧化钙D.NaOH 火碱氢氧化钠
34.C1O2是一种高效自来水消毒剂,关于C1O2说法错误的是
A. 该物质由氯元素和氧元素组成B.该物质读做氧化氯
C. 该物质是一种氧化物D.氯氧元素质量比是35.5:32
35.下列各组物质中,属于同素异形体的是
A.冰与干冰
B.汞与水银
C.石墨与碳60
D.氧气与液氧
36.MgFe2O4是一种磁信息材料的主要成份,广泛应用于电子计算机。其中铁元素的化合价是
A. +1
B. +2
C. +3
D. +4
37.合理利用资源是当今世界所关注的话题。下列做法不合理的是
A. 设计雨水回收系统
B. 建风力发电站
C. 使用太阳能路灯
D. 深埋废弃金属
38.实验室中装有浓硫酸的试剂瓶应贴有的图标是
药品橱柜甲乙丙丁
常见药品木炭粉、硫磺等铜片、锌粒等烧碱溶液、石灰水等浓硫酸、盐酸等现实验需用磷酸(H3PO4),能从下列橱柜中找到的是
A.橱柜甲
B.橱柜乙
C.橱柜丙
D.橱柜丁
40.以下装置分别用于气体的发生和收集,现用该套装置可制取的气体是
A. O2
B. H2
C. CO2
D. 无法确定
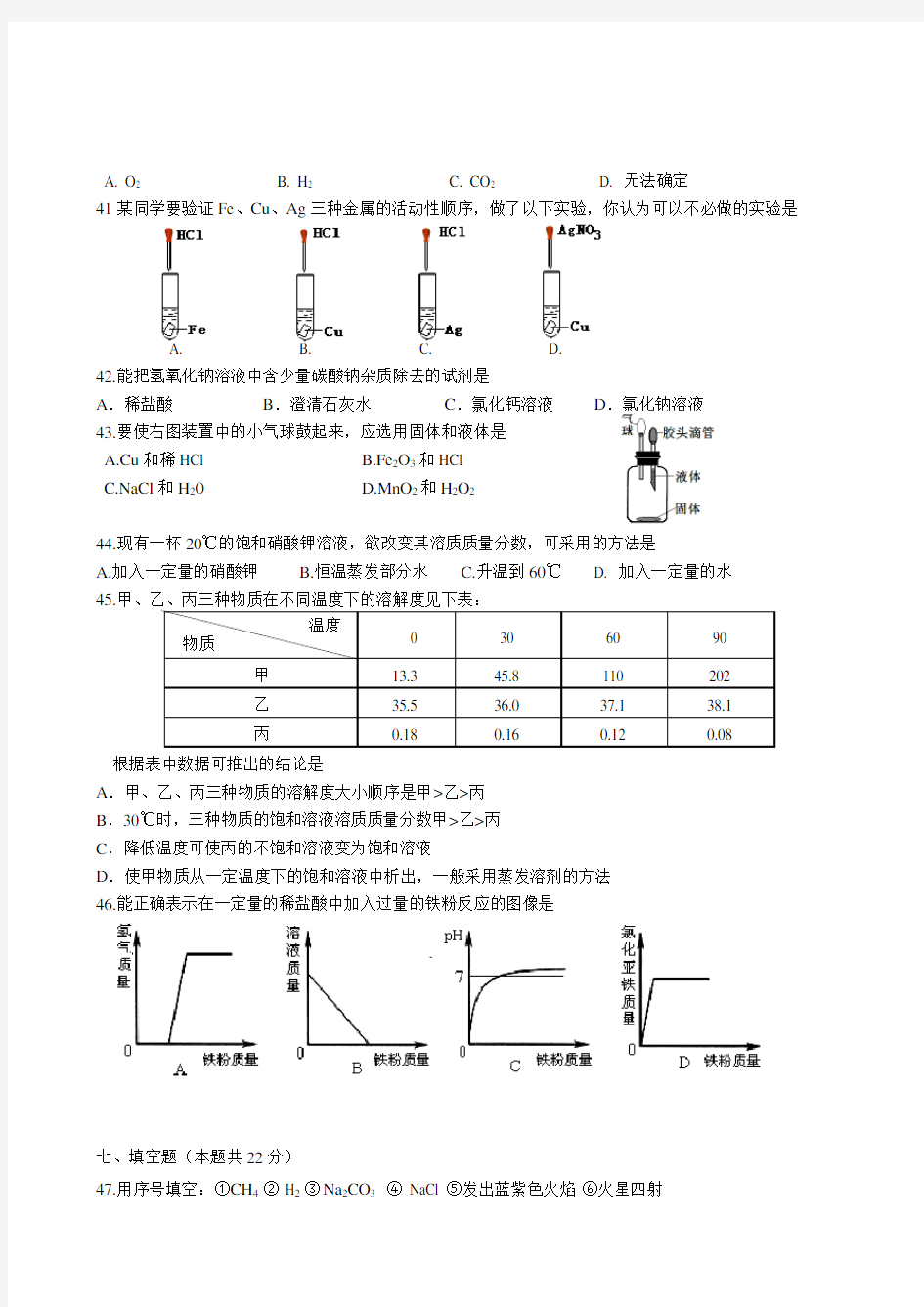
41某同学要验证Fe、Cu、Ag三种金属的活动性顺序,做了以下实验,你认为可以不必做的实验是
A. B. C. D.
42.能把氢氧化钠溶液中含少量碳酸钠杂质除去的试剂是
A.稀盐酸B.澄清石灰水C.氯化钙溶液D.氯化钠溶液
43.要使右图装置中的小气球鼓起来,应选用固体和液体是
A.Cu和稀HCl
B.Fe2O3和HCl
C.NaCl和H2O
D.MnO2和H2O2
44.现有一杯20℃的饱和硝酸钾溶液,欲改变其溶质质量分数,可采用的方法是
A.加入一定量的硝酸钾
B.恒温蒸发部分水
C.升温到60℃
D. 加入一定量的水
45.甲、乙、丙三种物质在不同温度下的溶解度见下表:
温度
物质0 30 60 90
甲13.3 45.8 110 202
乙35.5 36.0 37.1 38.1
丙0.18 0.16 0.12 0.08 根据表中数据可推出的结论是
A.甲、乙、丙三种物质的溶解度大小顺序是甲>乙>丙
B.30℃时,三种物质的饱和溶液溶质质量分数甲>乙>丙
C.降低温度可使丙的不饱和溶液变为饱和溶液
D.使甲物质从一定温度下的饱和溶液中析出,一般采用蒸发溶剂的方法
46.能正确表示在一定量的稀盐酸中加入过量的铁粉反应的图像是
七、填空题(本题共22分)
47.用序号填空:①CH4② H2③Na2CO3 ④ NaCl ⑤发出蓝紫色火焰⑥火星四射
(1)厨房中调味品之一食盐的化学式是_______(2)我国“西气东输”的气体是______。
(3)细铁丝在氧气中燃烧的现象是:______,生成一种黑色固体。
48.根据右图信息,按要求回答:
(1)A、B两瓶溶液溶质的化学式分别是__________;________,它们分别
属于_______、________类别。(填写“酸、碱、盐、氧化物或单质”)
(2)用铂丝蘸取少量A 瓶中的溶液,放在酒精灯的火焰上,透过钴玻璃观察,
火焰颜色呈______色。
A B
(3)B瓶溶液长期放置后浓度会变稀,这是因为该物质具有______性,若用量筒量取50mL密度为ρg/mL 该硫酸溶液,则量筒内溶液的溶质质量为__________________克(只要求列式)。
49.某品牌牙膏中的主要活性成分是单氟磷酸钠(Na2PO3F)。它是由_______种元素组成。单氟磷酸钠(Na2PO3F)摩尔质量是____________,1mol Na2PO3F中含有_________个氧原子。
50.某同学在化学课外兴趣活动中得知:金属钾能与水发生剧烈反应,反应的化学方程式为:
2K + 2H2O→2KOH + H2↑,请分析:
(1)该反应属于___________反应类型。反应中_________作还原剂。
(2)反应后的溶液中加入硫酸铜溶液会出现________现象。
51.某化工厂为综合利用生产过程中的副产品CaSO4,与相邻化肥厂联合设计了制备(NH4)2SO4的工艺流程(如图所示)
已知:上述流程中,沉淀池中发生的主要化学反应为:
CO2+2NH3+CaSO4+H2O→+(NH4)2SO4,
(1)根据质量守恒定律,,可以推测内的物质是_________。
(2)根据实验室制取CO2不能使用硫酸的原理,判断该厂得到的副产品CaSO4固体溶于少量水中易形成_____液。(填“悬浊液、乳浊液或溶液”)。
(3)制得(NH4)2SO4是一种常用化肥,请任意列举一种与这种物质具有相同肥效的物质是________。(4)通过操作a将沉淀池中反应产物进行分离,其中操作a的名称是____________。
(5)煅烧炉中发生的化学反应方程式为_________。该反应产生可循环使用的物质是_______。
三.实验题(本题共18分)
52.根据实验回答:
(1)写出图中a、b仪器名称:a_______________ ;b_________________。
(2)图A中的操作错误是。
(3)用图B的方法测定空气中氧气的体积分数结果偏低,改进的措施是。
(4)图C称量氢氧化钠固体的方法有处错误。
53.如图所示,进行中和反应实验:
(1)在A的实验中,滴入酚酞试液后,溶液由无色变为色。
(2)B中发生中和反应的化学方程式是_________________。
(3)写出C的溶液中溶质可能存在的几组情况。(用化学式表示)
(4)使10 ml氢氧化钠恰好中和,需滴加溶有0.01mol硫酸的稀硫酸溶液,求该10 ml氢氧化钠溶液中含氢氧化钠多少克?(列式计算)
54.某兴趣小组同学通过查找资料得知:草酸(H2C2O4)受热会分解。于是同学们对草酸受热分解的产物作如下探究:
(1)猜想与假设:第一种:草酸分解产物是CO2和H2;
第二种:草酸分解产物是CO2、CO和H2O;
第三种:草酸分解产物是CO2和H2O。
(2)设计如下实验装置:(图中铁架台略去,假设每步都反应完全)
①装置图方框内的仪器未画完整,请画完整(直接画在答题卡的图上)。
②按装置进行实验,看到无水硫酸铜由白变蓝,洗气瓶中澄清石灰水变浑浊。在尖嘴管口点燃剩余气体,火焰上方罩一个烧杯,有白色固体生成,证明燃烧气体中含有CO;换一个干、冷烧杯罩在火焰上方,内壁无现象,证明燃烧气体中无_________气体。
(3)结论与思考:
①第_______种猜想是正确的,请写出草酸受热分解的化学反应方程式:。
②碱石灰的作用是。
③若撤去方框内的仪器,整套装置也能证明产物中有CO2,方法是:。
上海市黄浦区2009初三化学模拟考评分参考
(满分60分)
本卷中的化学方程式,如果条件或↓或↑没有标明、没有配平,整卷共扣一分。
六、选择题(本题共20分)(每题只有一个正确答案)
题号27 28 29 30 31 32 33 34 35 36
答案 B B D A A A D B C C
题号37 38 39 40 41 42 43 44 45 46 答案 D A D C B B D D B D
七、填空题(本题共22分)(每空一分)
47.⑴④⑵①⑶⑥
48.⑴KCl H2SO4盐酸⑵吸水 50×ρ×98%
49.四 144g/mol 1.806×1024
50.⑴置换金属钾(或K)⑵蓝色(絮状)沉淀
51.⑴碳酸钙(或CaCO3)⑵悬浊液⑶铵态化肥均可⑷过滤
⑸CaCO3CaO + CO2↑二氧化碳(或CO2)
高温
三、实验题(本题共18分)(每空一分,其中53题⑶、⑷分别为2分)
52.⑴烧杯水槽⑵缺少玻璃棒搅拌⑶改用红磷燃烧(或合理给分)⑷2处53.⑴红⑵2NaOH +H2SO4→Na2SO4 + 2H2O
⑶只有Na2SO4(1分);Na2SO4与H2SO4(1分)
⑷设10ml氢氧化钠溶液中溶质为n mol
2NaOH +H2SO4→Na2SO4 + 2H2O
n 0.01
2 = 1
n 0.01
n=0.02 mol (1分) m=0.02 mol×40 g/mol=O.8 g(1分)
54.⑵实验
①作图
②涂有澄清石灰水氢气(或H2)
⑶结论与思考
①二H2C2O4→H2O+ CO2↑+ CO↑
②吸收二氧化碳气体和干燥气体,避免对氢气、一氧化碳检验产生干扰
③实验后,在干燥管内,滴加盐酸看是否有气体产生。(或合理给分)
