酵母双杂交

附件1:
大学生科研兴趣培养计划项目申报书
项目名称
项目负责人
学院
联系电话
申报日期
四川农业大学制表
项目名称
起止时间年月至年月
负
责
人
姓名年级所在学院、专业联系电话E-mail
项
目
组
成
员
导师姓名职务/职称通讯地址电话E-mail
一.立题依据
玉米是世界上第三大粮食作物,我国的种植面积约2530万hm2,2009-2010年度中国玉米产量1.655亿吨[1],成为世界上第二大玉米生产国。1996年前,我国玉米的种植面积仅小于水稻和小麦,居第三位;1996年后,玉米总产量和单位面积产量超过小麦居禾谷类作物第二位,同年玉米增产总额在谷类作物增产总额中占40.5%,远高于水稻的26%和小麦的22 %[2]。玉米不仅是重要的粮饲作物,还是重要的工业原料。世界上以玉米淀粉为工业原料的工业制品己超过500余种,并广泛应用于食品、医药、化工等行业[3]。
淀粉是玉米籽粒中的主要积累物质,以淀粉粒的形式存在于植物体中,占籽粒总重的70%左右,淀粉也是构成植物王国的主要成分。玉米淀粉是人类淀粉主要来源之一,也是工业淀粉和以淀粉为原料的深加工产业的主要原料。美国淀粉加工业95%的淀粉都是玉米淀粉。全世界淀粉产量为3600万吨,其中的80%以上都是玉米淀粉[4]。因此玉米淀粉生产工业在整个玉米加工业中占有十分重要的地位,加强高淀粉玉米育种具有显著的社会效益和经济效益。
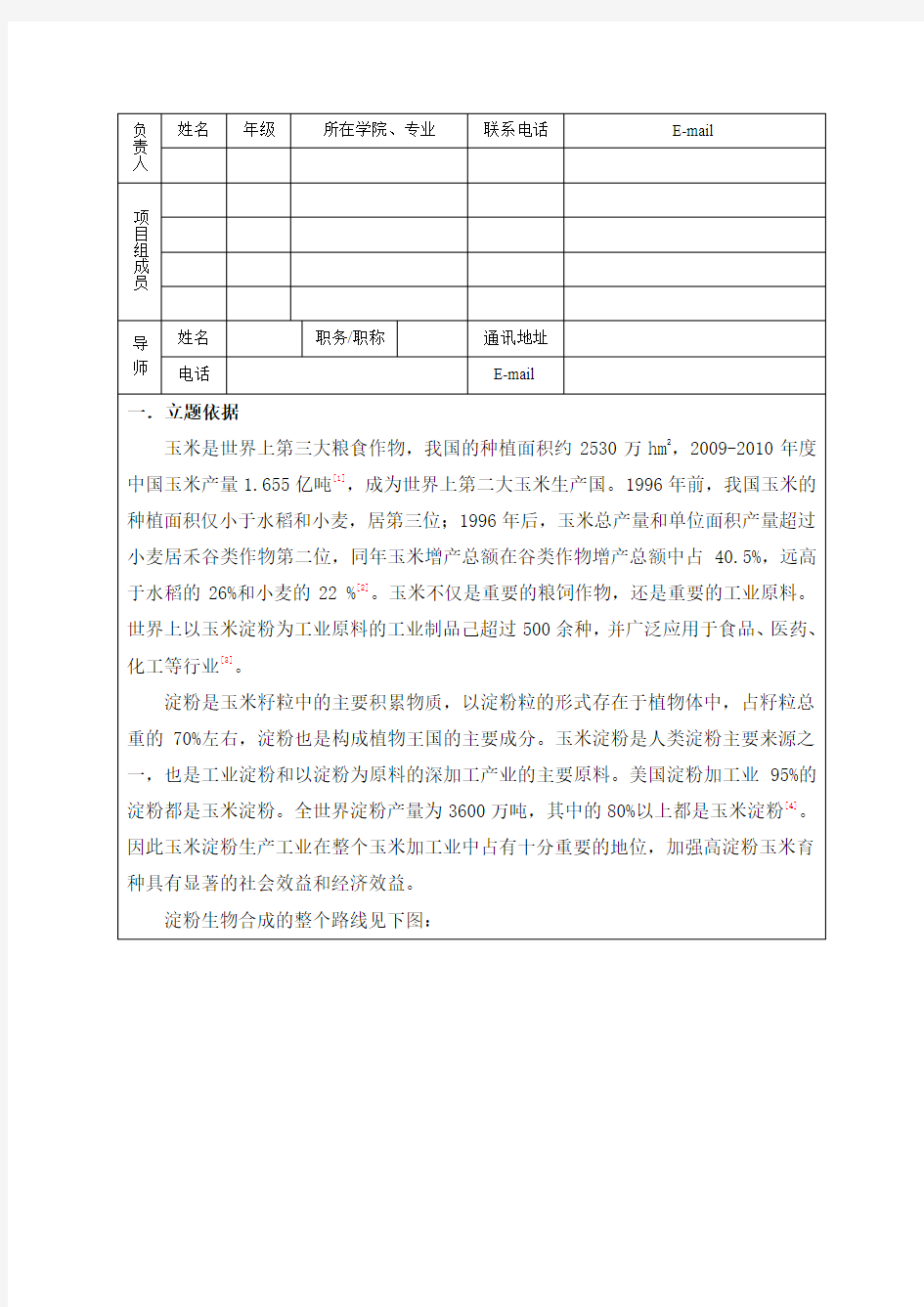
淀粉生物合成的整个路线见下图:
碳源来自叶片通过光合作用合成的蔗糖,然后蔗糖运输到淀粉合成器官-胚乳细胞又转化为1-磷酸-葡萄糖(G-1-P),如图所示,1-磷酸-葡萄糖穿过细胞膜,进入细胞溶质和造粉体中,依靠腺昔二磷酸葡萄糖焦磷酸化酶(ADP-glucose pyrophosphorylase,ADPGPPase),淀粉合成酶(Starch synthase,SS)和淀粉分支酶(Starch branching enzyme,SBE)催化淀粉生物合成[5,6]。研究表明ADP-葡萄糖是在细胞溶质中合成并通过在造粉体中的腺昔酸转置于造粉体中的。
在植物体内,淀粉合成的直接前体是腺苷二磷酸葡萄糖(Adenosine diphos-phate glucose,ADPG)。ADPG由ADPGPPase催化合成,一般认为是植物淀粉生物合成的主要限速步骤。叶绿体中的ADPGPPase可利用光合作用产生的葡萄糖-1-磷酸合成ADPG,ADPGPPase是一个别构酶,被3-磷酸甘油酸(3-PGA)、二价阳离子Mg2+、Mn2+变构激活,被无机磷(Pi)抑制;同时ADPGPPase活性还受氧化还原势的修饰,还原力强时,二硫键断开,酶被激活。在某些储藏器官中,特别是禾谷类作物的籽粒中还存在定位于胞质的ADPGPPase,但区别于叶绿体中的ADPGPPase,其酶活性对3-PGA和无机磷不敏感。这可能是由于单子叶植物的进化引起的,胞质内激活子不敏感的ADPGPPase是为适应胚乳发育的调控需要,同时为了协调光合作用与淀粉合成途径保留着的造粉体内激活敏感的ADPGPPase;也可能由于位于胞质的ADPGPPase可减少造粉体中ATP的产生和PPi循环。在玉米胚乳细胞中,ADPGPPase活性主要位于细胞质中,只有少部分(10%)位于造粉体内[7]。植物的ADPGPPase是由大、小亚基组成异四聚体,根据其在细胞内的分布,分为胞质型(cytosolic)和质体型(plastidia1)两种[8]。因此,在植物细胞内
AGPase存在着4种亚基:即胞质型小亚基(cytosolic small subunit,SSUⅠ)、质体型小亚基(plastidial small subunit,SSUⅡ)、胞质型大亚基(cytosolic large subunit,LSUⅠ)和质体型大亚基(plastidial large subunit,LSUⅡ[9]。小亚基起催化作用,而大亚基则发挥别构效应[10]。大亚基为调节亚基,而小亚基为催化亚基[11]。小亚基行使AGPase的代谢功能,大亚基则承担AGPase 小亚基代谢活性的调控,变构因子诱导的变构调控是AGPase主要的调控形式);许多单子叶和双子叶植物AGPase 组成亚基不同“等型体”(isoformas )的编码基因cDNA和gDNA已分别从中克隆,其中绝大多数AGPase小亚基由单个基因编码,大亚基则是由多个基因编码的。不同物种间编码亚基的基因在表达数目和模式方面存在相当大的差异,即使同一物种,不同组织器官大小亚基表达也具有特异性。迄今为止,在已研究的植物种类中,包括拟南芥、马铃薯、大麦、水稻以及小麦等,它们的AGPase的大亚基同属多基因编码。
国内外有关AGPase的研究较少,关于AGPase的作用模式了解不够深入。在玉米中AGPase的亚细胞定位鲜有报到,通过酵母双杂交系统研究体内AGPase亚基的组成形式更是种创新。由于AGPase组成模式及组织表达特异性研究对淀粉合成代谢网络机制的研究有很重要意义,因此有必要要进行此次研究。
本实验的目的及拟解决的问题:体外克隆表达编码玉米AGPase的六个基因,利用酵母双杂交系统研究其组成模式,并通过酶联免疫技术对玉米中AGPase进行亚细胞定位。此研究将深入阐述AGPase的功能特性,为进一步从生理学和细胞生物学角度深入解析淀粉合成代谢网络机制做好基础,同时也为高淀粉含量玉米品种的选育提供参考。
参考文献:
[1]中国行业研究网. https://www.360docs.net/doc/a414834714.html,/doc/70300/475123.html. 2009-10-8.
[2]刘纪麟. 玉米育种学[M]. 北京: 中国农业出版社, 2000.
[3]杜何为,黄敏,张祖新. 玉米DNA的小量快速提取[J]. 玉米科学,2004, 12(2): 114-115.
[4]尤新编著.玉米深加工技术[M].北京:中国轻工业出版社,2000.
[5]Mu-Forster C, Huang RM, Powers JR, et al. Physical association of starch biosynthetic enzymes with starch granules of maize endosperm: Ganrule-ass.
Ociated forms of starch synthase I and starch branching enzyme. Plant Physiol, 1996, 111: 821-829.
[6]Myers AM, Morell MK, James MG,et al. Rccent Progress toward understanding biosnythesis of the amylopectin cystal. Plant Physiol, 2007, 122: 989-997.
[7]Sikka, Choi SB, Kavakli IH, et al. Subcellula: compartmentation and allosteric regulation of the rice endosperm ADP glucose pyrophosphorylase. Plant Sci, 2006, 161: 461-468.
[8] Morell MK, Bloom M, Knowles V, Preiss J. Subunit structure of spinach leaf ADPglucose pyrophosphorylase [J].Plant Physiol, 2004, 85: 182-187.
[9] Tetlow I J,Morell M K,Emes M J.Recent developments in understanding the regulation of starch metabolism in higher plants[J]. J Exp. Bot, 2004, 55(406): 2131-2145.
[10] Johnson PE,Patron NJ, Bottrill AR, et a1. A low-starch barley mutant,Risaφ16, lacking the cytosolic small subunit of ADP-Glucose pyr0phosphorylase,reveals the importance of the cytosolic isoform and the identity of the plastidial small subunit [J]. Plant Physiol, 2006, l31: 684-696.
[11]Smith AM, Denyer K, Martin C. The synthesis of the starch granule. Annu Rev Plant Physiol Plant Mot Biel, 2005,48: 67-87.
二、项目方案
1 试剂材料
菌种与质粒:大肠杆菌、酵母菌、T克隆载体、PET表达载体、质粒pGADT-7、pGBKT-7、pGADT7-T、pGBKT7-53、pGBKT7-Lam pMD18-T。
玉米骨干自交系R-08
各类PCR引物
DNA 主要试剂和药品:限制性内切酶、yDNA/EcoRI+Hind1IMarker, DL2000Marker,T
4
连接酶, TaKaRa Taq酶、碱性磷酸酶CIP ;PC R纯化试剂盒和DNA胶回收试剂盒;酵
母双杂交试剂 ;尼龙膜;小鼠抗BD 的单克隆抗体;其余试剂和药品均为国产分析纯试剂和药品。
常用培养基:LB 培养基、BG-11培养基、YPD 培养基、SD 培养基。
常用溶液:碱变性法提取质粒用液、植物DNA 提取用液、琼脂糖凝胶电泳用液、SDS-PAGE 凝胶电泳用液、Western 印迹法用液、酵母双杂交试剂、蛋白分离纯化等。 常用仪器:台式高速离心机、台式高速冷冻离心机、PCR 仪、多用电泳仪、电子分析天平、水浴恒温振荡器、超声破碎仪、凝胶成像分析系统、分光光度计、核酸蛋白质分析仪、发酵系统、微孔板阅读仪、蛋白电泳系统。
2 技术路线
从玉米胚乳和叶片中克隆AGPase 基因。使用clontech 公司的酵母双杂交试剂盒,将这些基因构建到酵母双杂交表达载体中。利用酵母双杂交,筛选阳性菌株,克隆鉴定,并通过测定β-半乳糖苷酶活性来确定起结合的强弱程度。同时将六个基因进行原核表达,分离纯化蛋白,免疫制备抗体。植物组织蛋白提取,进行免疫印记反应。
2.1 酵母双杂交技术路线
植物RNA 提取
六个目的片段获得
转化酵母AH109菌株
转化酵母Y187菌株 三个片段连接文库载体
目的片段转化T 载体克隆
阳性菌株鉴定
三个片段连接到诱饵载体 酵母双杂交
2.2 免疫印记技术路线
3.研究方案:
3.1 酵母双杂交试验
3.1.1酵母感受态细胞制备(按照clontech 公司YeastmakerTM transformation system2 protocol 操作):
a 将酵母菌 Y178菌种划线接种于YPDA 平板上, 30℃培养2~3d 后,长出白色克隆。
b 挑取1个克隆,接种于3mlYPD 液体培养基中,30℃,250rpm 震荡培养8~12h ,OD 600达到0.15-0.3之间,室温下700g 离心5min ,去上清,用100mlYPDA 重悬沉淀。
c 30℃,250rpm 震荡培养3~5h ,当OD 600达到0.4~0.5时,室温下700g 离心5min 。
d 加入3ml l.l*TE/LiAc 溶液重悬沉淀,重悬液按1.5ml 的量分装于2个1.5ml 离心管中,高速离心15Sec ,每份沉淀用600ulTE/LIAc 溶液重悬,制成感受态细胞。
3.1.2 BD 载体构建:
不同玉米组织进行酶联免疫印记检测
导入免疫动物制备抗体
表达产物蛋白检测提取
目的片段连接到PET 表达载
连接到T 载体克隆
六个基因PCR 目的片段
a 经植物RNA提取,用反转录试剂盒,合成cDNA。设定特定引物,以cDNA为模板,特异引物体外PCR扩增,获得目的基因。
b 将获得的特异片段回收,克隆到pMD18-T载体中,形成pMD18-T-CP克隆,挑出阳性克隆,菌落PCR验证后,提出质粒。
c 用特异限制性内切酶切pMD18-T-CP和载体pGBKT7,酶切产物电泳,回收目的片断和载体,再连接转化,构建诱饵载体pGBKT7-CP,PCR检测后,送上海生工测序。
3.1.3 AD载体构建方法与BD载体构建方法雷同,只是将最后pGBKT7换为pGADT7。3.1.4 BD载体和AD载体共转化酵母(按照Yeastmaker TM Transformation System2 protocol操作):
a 于1.5 ml预冷的离心管加入1ug质粒DNA和20u1变性的Herring testes carrier DNA(10mg/ml)。
b 再加入50ul酵母感受态,轻混匀后,加入500ulPEG/LiLc溶液,轻轻震荡混匀。
c 30℃每10min摇匀一次培养30min后,加入20ulDMSO,混匀后42℃水浴15min,每15min摇匀一次,高速离心15sec,去上清。
d 加入lmlYPD Plus Liquid Medium高速离心15Sec,去上清,加入1ml0.9%NaCI溶液,涂布于营养缺陷平板SD/-TrP上,30℃培养。
3.1.4 β-半乳糖普酶分析:
a 准备新鲜的Z-bufer/X-Gal浸润Whatman#4滤纸;用灭菌的干燥滤纸平铺在SDIHis-Leu-Trp+3AT平板上。
b 在平板的不同位置打孔以确定菌落和滤纸的相对位置。
c 当滤纸在平板上完全浸润的时候小L的用镊子拿出粘有菌落滤纸,转移到含有液氮的培养皿中。
d 用液氮完全浸泡滤纸,直到全部冷冻,拿出滤纸。室温融化。反复冻融,使细胞壁破裂。
e 小心地将经过冻融处理的滤纸放在预先浸润的滤纸上,菌落面向上。
f 注意:在两层滤纸之间不能有气泡:将滤纸放在室温或30℃下培养,不时地检查菌落是否变蓝;CG1945菌株产生α-半乳糖着酶变蓝的时间变化很大,往往是30 min到8h,延长培养时间容易产生假阳性的菌落。在平板上确定变蓝菌落的位置,挑取该克隆进行下一步的研究。
3.2免疫印记
3.2.1原核表达蛋白(带组氨酸标签)纯化:
a 将构建的六种各原核表达载体分别转化大肠杆菌,隔夜培养,挑出6-10个单菌落接种到3ml含抗生素的LB液体培养基中,37℃,200rpm培养。
b 从隔夜培养物中吸取lml集6000g离心30s,菌体加入用80ul样品缓冲液制样,进行小样检测。
c 将表达蛋白的小样的相应菌样集中继续扩大到50ml体系中培养。将培养12h左右的菌接种到1000ml含抗生素的LB液体培养基中,37℃200rpm培养3h。
d 待菌长至对数生长中期,加入1M的IPTG使其终浓度为lmM,诱导培养4h.5000rpm 离心集菌。
e 按照3ml裂解缓冲液:1g菌体的比例,用裂解缓冲液Buffer L (50mNaH
2PO
4
,
300mMNaCl, 20mM咪哇,PH8.0)重悬菌体。
f 冰浴条件下对菌体超声破碎。4℃条件下30000g离心30min,收集上清。
g 上清与Ni-NTA填料4℃结合1h以后,分别用含有20,50,100mM咪唑清洗溶液洗杂蛋白。
h 洗到基线后,用含有30mM咪唑洗脱液收集目的蛋白。用PEM(80mM Pipes)溶液透析或用超滤管浓缩,快速置换溶液,-80℃保存。
3.2.2 抗体纯化(参照抗体技术试验指南美E.哈洛等著,沈关心等译):
a 按照说明书准备好Protein A Sepharose CL-4B (Phannacia) 4 ml,与兔抗CMV CMV MP粗血清 (以 pH8.0 Tris-HCI调pH至8.0)5ml混合轻轻搅拌2hr,装柱。
b 10倍柱体积100m mol/L。10m mol/L Tris-HC1 pH 8.0依次洗柱。
c 以1/2柱体积0.1mol/L Glycine, pH 3.0洗脱抗体,按每管lml收集于加入200ul
1 mol/L pH8.0 Tri s-HCI的1.5ml eppendof管中,检测蛋白浓度。
d 合并浓度0.1 mg以上的抗体。SDS-PAGE电泳检测纯度。
4.时间安排
2010年1月-2月:前期准备,主要是实验室发芽试验,还包括药品的购买,引物合成。
2010年3月:但材料长到四叶期后,提取RNA,反转录cDNA,PCR体外扩增完成六个AGPase基因目的条带的克隆。
2010年4月-7月:分两部分试验,一部分做抗体,一部分做酵母双杂交。团队分工协作,分两组,一组将六个基因到入T载体克隆,最后在PET中表达,分离蛋白后再制备抗体;一组将六个基因经T载体克隆后,三个导入诱饵载体,三个连接到文库载体,进行表达,提取六个载体。
2010年8月-9月:大田取材,玉米种子和叶片提取蛋白,将得到的抗体进行免疫印记;另外将得到的载体做酵母双杂交,阳性克隆检测。
2010年10月-12月:结果处理分析,完成文章撰写。
三、可行性分析
1.玉米所的试验设备完全满足此次试验过程所用到的仪器设备。目的基因体外克隆,目的基因表达量情况分析,蛋白分离纯化,无菌操作等所用仪器设备都完好在用。2.有关试验技术条件成熟,本团队已发表相关文章做理论基础。本试验所用到的原核表达和酵母双杂交及免疫印迹等试验技术成熟。
3.试验思路明确,方案详细。经过大量文献查找,团队反复论证研究,目标明确,具体实施计划周密。
4.团队动手能力强,积极性高,能团结协作完成此研究。此次试验团队有五人构成,四个是本硕连读,一个已在实验室做了相应试验。
5.经费充足。学校和课题组对项目都有经济支持。
三、预期研究成果
1,通过酵母双杂交研究,解析在体内条件下,玉米AGPase基因表达亚基结合模式。2,通过酶联免疫印记,明确AGPase的亚细胞分布。
3,发表SCI论文一篇。
四、经费预算
常用药品:玉米所实验室提供。
特殊药品(内切酶等):800.00元
常用提取试剂盒:1000.00元
抗体制备:4200.00元
版面费:2000.00元
导师意见:
签名:
年月日学院推荐意见:
签名盖章:
年月日
学校评审意见:
负责人(签字):
(公章):
年月日
1
1
酵母双杂交技术
酵母双杂交系统 1.原理 酵母双杂交系统的建立得力于对真核细胞调控转录起始过程的认识。研究发现,许多真核生物的转录激活因子都是由两个可以分开的、功能上相互独立的 结构域(domain)组成的。例如,酵母的转录激活因子GAL4,在N端有一个由147个氨基酸组成的DNA结合域(DNA binding domain,BD),C端有一个由113 个氨基酸组成的转录激活域(transcription activation domain,AD)。GAL4分子的DNA结合域可以和上游激活序列(upstream activating sequence,UAS)结合,而 转录激活域则能激活UAS下游的基因进行转录。但是,单独的DNA结合域不 能激活基因转录,单独的转录激活域也不能激活UAS的下游基因,它们之间只 有通过某种方式结合在一起才具有完整的转录激活因子的功能。 2.试验流程 酵母双杂交系统正是利用了GAL4的功能特点,通过两个杂交蛋白在酵母细 胞中的相互结合及对报告基因的转录激活来捕获新的蛋白质,其大致步骤为: 2.1、视已知蛋白的cDNA序列为诱饵(bait),将其与DNA结合域融合,构建 成诱饵质粒。 2.2、将待筛选蛋白的cDNA序列与转录激活域融合,构建成文库质粒。2.3、将这两个质粒共转化于酵母细胞中。 2.4、酵母细胞中,已分离的DNA结合域和转录激活域不会相互作用,但诱 饵蛋白若能与待筛选的未知蛋白特异性地相互作用,则可激活报告基因的转录;反之,则不能。利用4种报告基因的表达,便可捕捉到新的蛋白质。 3.特点 优点 蛋白--蛋白相互作用是细胞进行一切代谢活动的基础。酵母双杂交系统的建立 为研究这一问题提供了有利的手段和方法。 缺点 尽管该系统己被证实为一种非常有效的方法,但它也有自身的缺点和问题。1、它并非对所有蛋白质都适用,这是由其原理所决定的。双杂交系统要求两种杂 交体蛋白都是融合蛋白,都必须能进入细胞核内。因为融合蛋白相互作用激活 报告基因转录是在细胞核内发生的。2、假阳性的发生较为频繁。所谓假阳性,即指未能与诱饵蛋白发生作用而被误认为是阳性反应的蛋白。而且部分假阳性 原因不清,可能与酵母中其他蛋白质的作用有关。3、在酵母菌株中大量表达外源蛋白将产生毒性作用,从而影响菌株生长和报告基因的表达。 使用酵母双杂交技术应注意的问题 真正明了酵母双杂交技术的主要原理及筛选方法是进行酵母双杂交实验的前提,构建成功的诱饵质粒及大量的材料准备是进行酵母双杂交实验的保证。只 有明了双杂交的原理,才有可能设计实验进程、才能有目的的进行材料准备, 并能对实验结果作出预测与分析,尤其要对具体实验中各种选择性压力培养基 的使用目的要十分清楚。大量的材料准备、较长的实验流程是酵母双杂交有别
酵母双杂实验步骤
2.1.1酵母双杂交 2.1.1.1Gateway入门克隆 设计Gateway引物时,在上游引物的5'端加上B1序列:GGGG-ACA-AGT-TT G-TAC -AAA-AAA-GCA-GGC-TNN-,下游引物的5'端加上B2序列:GGGG-ACC-ACT-TT G-T AC-AAG-AAA-GCT-GGG-TN-。其中,5'-GGGG序列是保护碱基,防止引物的重要部分被降解,下划线加粗的部分是在整个的Gateway克隆中可以保存下来的序列,3'端的碱基N是为了保证经过入门载体构建目的载体时阅读框的正确性,一般建议为C。 通过PCR扩增获得带有att B位点的基因片段,扩增体系和条件见3.2.2.2,其中将退火温度改为65℃。获得扩增产物后对其进行回收纯化,测定纯化后DNA 的质量和浓度后进行下一步的BP反应,反应体系如下: att B-PCR产物(≥10 ng/μL)1-7μL pDONR221 (150 ng/μL)1μL TE buffer, pH 8.0 补足8μL 将上述混合物加入离心管中,加入2μL BP反应酶,加入之前需将其在涡旋仪上轻轻振荡两次,所有组分混匀离心后,25℃反应1h,加入1μL蛋白酶K后,混匀离心,37℃反应10min终止BP反应,将BP反应产物参照3.2.2.6进行转化,由于pDONR221载体为Kan抗性,所以选用含有50μg/mL Kan抗生素的LB平板进行阳性克隆筛选,参照3.2.2.7检测阳性克隆,然后根据3.2.2.8中的方法提取重组质粒,测定质量和浓度后送至测序公司进行测序。 进行BP反应时,需注意以下几项: (1)对于BP反应来说,最高效的是采用线性的att B-PCR产物和超螺旋的att P 入门载体; (2)为了提高BP反应的效率,可以将建议的25℃反应1h适当延长至4-6h,可 以将效率提高2-3倍,或者延长至过夜反应,可以将效率提高5-10倍,对 于长片段克隆来讲,适当的延长反应时间是非常必要的; (3)提高体系中PCR产物的量可以增加反应效率,但每10μL体系中PCR产物 最好不要超过250ng。 2.1.1.2诱饵载体构建 重组的入门载体测序正确后,通过LR反应来构建酵母双杂交的诱饵载体,LR反应体系如下: 入门载体(50-150 ng)1-7μL pDEST32 (150 ng/μL)1μL TE buffer, pH 8.0 补足8μL
酵母双杂交H2Y和Y187系统protocol
目录 (一)介绍 4 (二)试剂盒物品清单 7 (三)额外附加物品列表9 (四)酵母菌株11 (五)酵母载体14 (六)方法简述:单杂交文库的构建和筛选16 方法简述:双杂交文库的构建和筛选17 (七)构建用于酵母单杂交的报告质粒载体18 (八)构建用于酵母双杂交的DNA-BD融合载体19 (九)构建生成cDNA文库21 (十)构建和筛选酵母单杂交和双杂交文库(简述)27 (十一)酵母单杂交文库的构建和筛选28 (十二)酵母双杂交文库的构建和筛选30 方法A:通过酵母配对(Yeast Mating)来筛选目的蛋白30 方法B:通过共转化的方法筛选目的蛋白35 (十三)分析阳性相互作用结果38 (十四)问题解决指南44 (十五)参考文献47 (十六)相关产品50 附录A: 双链 cDNA合成的典型结果51 附录B: 酵母感受态的制备—LiAc 法52 附录C:单杂交对照载体信息53 附录D:双杂对照载体信息54 表格列表 Table I. BD Matchmaker酵母菌株的基因型11 Table II. BD Matchmaker酵母菌株的表型11 Table III.单杂交系统的载体14 Table IV.双杂交系统的载体15 Table V.各BD-Matchmaker DNA-BD 载体的比较19 Table VI. RNA起始浓度和PCR扩增循环数之间的关系24 Table VII.单杂交共转化的对照实验的设置29 Table VIII.单杂共转化对照实验:期望的结果29 Table IX.双杂交转化的对照实验的设置33 Table X.双杂交配对筛选的对照实验的设置 Table XI.双杂交共转化的对照实验的设置 Table XII.双杂交共转化的对照实验:期望的结果 Table XIII.用于PCR筛选菌落的Assembling Master Mixs
酵母双杂交系统及其应用
酵母双杂交系统及其应用 Y east Two-hybrid System and Its Application 1.酿酒酵母(Saccharomyces cerevisiae)的生物学特性 (1)单细胞真核生物 尽管酵母细胞比较简单,但它们具有所有真核生物细胞的主要特征,如含有一个独立的细胞核、多条线性染色质包装成染色体、细胞质包含了全部的细胞器和细胞骨架结果(如肌动蛋白纤维)。 (2)与其它真核生物相比,它们的基因组较小,基因数目也较少; 1996年已完成酵母全基因组测序( 1.5 x 107 bp),是第一个被测序的真核生物。大约有6000个基因。目前已经建立了一个6000个菌株的文库,每一个菌株中只删除了一个基因。其中5000多株在单倍体状态时能够存活,表明大多数酵母基因时非必需的。 (3)易于培养和操作,可以在实验室快速繁殖 在指数生长期每90分钟繁殖一代,从单个细胞可以繁殖称克隆群体。 (4)单倍体和双倍体的存在使酿酒酵母便于进行遗传分析 酿酒酵母可以以单倍体状态和双倍体状态生长。单倍体和双倍体之间的转换是通过交配和孢子形成来实现的。 有两种单倍体细胞类型,分别为a型和α型。在一起生长时,这些细胞因交配而形成a/α双倍体细胞。在营养匮乏时,a/α双倍体发生减数分裂,产生一个子囊的结构,每个子囊含有4个单倍体孢子(两个a-孢子和两个α-孢子)。但当生长条件改善时,这些孢子可以出芽并以单倍体细胞的形式生长或交配而重新形成双倍体。 一个酵母细胞可同时兼容几种不同质粒 bud,芽, 蓓蕾starvation,饥饿, 饿死 ascus,n.[微生物]子囊meiosis,n.减数分裂, 成熟分裂 haploid,n.[生物]单倍体, 仅有一组染色体的细胞adj.单一的 diploid,adj.双重的, 倍数的, 双倍的n.倍数染色体 ascospore,n.[植]囊孢子 rupture,v.破裂, 裂开, 断绝(关系等), 割裂。n.破裂, 决裂, 敌对, 割裂 spore,n.孢子vi.长孢子germinate,v.发芽, 发育, 使生长
!!酵母双杂交操作步骤(中文翻译)
各种SD培养基: 1)SD/-ade(腺嘌呤)/-leu(亮氨酸)/-trp(色氨酸)/-his (组氨酸)(1000 ml)(? “四缺”) 酵母氮源(YNB):6.7g ; -ade/-leu/-trp/-his DO supplement 0.60g (购买来就配好的) ; 葡萄糖20g (即2%) 2)SD/-leu/-trp/-his (1000 ml) 酵母氮源(YNB):6.7g ; -leu/-trp/-his DO supplement 0.62g ; (购买来就配好的) 葡萄糖 20g. (即2%) 3)SD/-leu/-trp (1000 ml) (?“二缺”) 酵母氮源(YNB):6.7g ; -ade/-leu/-trp/-his DO supplement 0.64g (购买来就配好的); 葡萄糖 20g (即2%) 4)SD/-leu (1000 ml) 酵母氮源(YNB):6.7g ; -leu DO supplement 0.69g ; (购买来就配好的) 葡萄糖 20g (即2%) 5)SD/-trp (1000 ml) 酵母氮源(YNB):6.7g ; -ade/-leu/-trp/-his DO supplement 0.74g ; (购买来就配好的) 葡萄糖 20g (即2%) 注意:YNB有两种,一种含有硫酸胺,另外一种不含硫酸胺。我们这用的是含硫酸铵的。(买来就加进去了的)。如果不含硫酸铵,那么要在终浓度0.17%的YNB中再加入0.5%的硫酸铵,即最终在1000 ml溶液中加入总量为6.7g的YNB与硫酸铵。 实际配制的方法是: 1.配制40%的葡萄糖贮存液(贮存在4℃),过滤除菌,待高压灭菌的溶液温度降至55℃ 以下时,再将50ml葡萄糖贮存液加入。(李博士经验这一步不高压,过滤即可使用)2.酵母氮源6.7g,加DO supplement 在920ml水中溶解,调PH至5.8(李博士的经验大 约加10M NaOH 200ul即可),之后补水至950 ml。 3.高压完后待温度降至55℃以下,加入50 ml40%葡萄糖。
文库构建及酵母双杂交技术
第四章基因文库构建及酵母双杂交技术 1 基因组文库的构建 基因组文库(genomic library)将某种生物细胞的整个基因组DNA切割成大小合适的片断,并将所有这些片断都与适当的载体连接,引入相应的宿主细胞中保存和扩增。 理论上讲,这些重组载体上带有了该生物体的全部基因,称为基因文库。 1. 1构建基因文库的载体选用 载体能够容载的DNA片断大小直接影响到构建完整的基因文库所需要的重组子的数目。
第四章基因文库构建及酵母双杂交技术1.1.1对载体的要求:载体容量越大,所要求的DNA片断数目越少,所需的重组子越少。 1.1.2目前常用的载体: 载体系列(容量为24 kp )、cosmid载体(容量为50 kb )、YAC(容量为1 Mb )、BAC (容量为300 kb) 1.2 基因文库构建的一般步骤 1.2.1染色体DNA大片段的制备:断点完全随机,片断长度合适于载体连接。不能用一般的限制性内切酶消化法,使用物理切割法或不完全酶切法。 1.2.2载体与基因组DNA大片段的连接:直接连接、人工接头或同聚物加尾。
噬菌体载体构建基因组文库
第四章基因文库构建及酵母双杂交技术2 cDNA文库的构建 cDNA克隆的基本过程是通过一系列,酶酶催作用,使poly(A) mRNA转变成双链cDNA群体并插入到适当的载体分子上,转化大肠杆菌寄主细胞,构建包含所有基因编码序列的cDNA基因文库。 2.1高质量mRNA的制备 应用Promega PolyAT tract mRNA Isolation System 分离Poly(A)RNA。将Biotinylated Oligo(dT)引物与细胞总RNA共温育,加入与微磁球相连的Streptavidin,用磁场吸附与PMP相连的SA-Biotinylated Oligo(dT)-mRNA。
(完整版)酵母双杂交原理
酵母双杂交系统原理 酵母双杂交系统(Yeast Two-hybrid System)由Fields和Song等首先在研究真核基因转录调控中建立。典型的真核生长转录因子,如GAL4、GCN4、等都含有二个不同的结构域: DNA 结合结构域(DNA-binding domain)和转录激活结构域(transcription-activating domain)。前者可识别DNA上的特异序列,并使转录激活结构域定位于所调节的基因的上游,转录激活结构域可同转录复合体的其他成分作用,启动它所调节的基因的转录。二个结构域不但可在其连接区适当部位打开,仍具有各自的功能。而且不同两结构域可重建发挥转录激活作用。酵母双杂交系统利用杂交基因通过激活报道基因的表达探测蛋白-蛋白的相互作用。主要有二类载体: a 含DNA -binding domain的载体; b 含DNA-activating domain的载体。上述二类载体在构建融合基因时,测试蛋白基因与结构域基因必须在阅读框内融合。融合基因在报告株中表达,其表达产物只有定位于核内才能驱动报告基因的转录。例如GAL4-bd具有核定位序列(nuclear-localization sequence),而GAL4-ad没有。因此,在GAL4-ad氨基端或羧基端应克隆来自SV40的T-抗原的一段序列作为核定位的序列。 双杂交系统的另一个重要的元件是报道株。报道株指经改造的、含报道基因(reporter gene)的重组质粒的宿主细胞。最常用的是酵母细胞,酵母细胞作为报道株的酵母双杂交系统具有许多优点: 〈1〉易于转化、便于回收扩增质粒。〈2〉具有可直接进行选择的标记基因和特征性报道基因。〈3〉酵母的内源性蛋白不易同来源于哺乳动物的蛋白结合。一般编码一个蛋白的基因融合到明确的转录调控因子的DNA-结合结构域(如GAL4-bd,LexA-bd);另一个基因融合到转录激活结构域(如GAL4-ad,VP16)。激活结构域融合基因转入表达结合结构域融合基因的酵母细胞系中,蛋白间的作用使得转录因子重建导致相邻的报道基因表达(如lacZ),从而可分析蛋白间的结合作用。 酵母双杂交系统能在体内测定蛋白质的结合作用,具有高度敏感性。主要是由于:①采用高拷贝和强启动子的表达载体使杂合蛋白过量表达。②信号测定是在自然平衡浓度条件下进行,而如免疫共沉淀等物理方法为达到此条件需进行多次洗涤,降低了信号强度。③杂交蛋白间稳定度可被激活结构域和结合结构域结合形成转录起始复合物而增强,后者又与启动子DNA结合,此三元复合体使其中各组分的结合趋于稳定。④通过mRNA产生多种稳定的酶使信号放大。同时,酵母表型,X-Gal及HIS3蛋白表达等检测方法均很敏感。 酵母双杂交筛选原理 双杂交系统的建立得力于对真核生物调控转录起始过程的认识。细胞起始基因转录需要有反式转录激活因子的参与。80年代的工作表明, 转录激活因子在结构上是组件式的(modular), 即这些因子往往由两个或两个以上相互独立的结构域构成, 其中有DNA结合结构域(DNA binding domain, 简称为DB,?BD)和转录激活结构域(activation domain, 简称为AD), 它们是转录激活因子发挥功能所必需的。单独的DB虽然能和启动子结合, 但是不能激活转录。而不同转录激活因子的DB和AD形成的杂合蛋白仍然具有正常的激活转录的功能。如酵母细胞的Gal4蛋白的DB与大肠杆菌的一个酸性激活结构域B42融合得到的杂合蛋白仍然可结合到Gal4结合位点并激活转录。 Fields等人的工作标志双杂交系统的正式建立。他们以与调控SUC2基因有关的两个蛋白质Snf1和Snf2为模型, 将前者与Gal4的DB结构域融合, 另外一个与Gal4的AD结构域的酸性区域融合。由DB和AD形成的融合蛋白现在一般分别称之为“诱饵”(bait)和“猎物”或靶蛋白(prey or target protein)。如果在Snf1和Snf2之间存在相互作用, 那么分别位于这两个融合蛋白上的DB和AD就能重新形成有活性的转录激活因子, 从而激活相应基因的转
酵母双杂交系统
酵母双杂交技术的研究与应用 摘要:酵母双杂交系统是在20世纪90年代初发展起来的利用遗传学方法在酵母真核细胞体内研究蛋白质之间相互作用的一种高度灵敏的分子生物学技术,它可以有效分离新基因或新的能与一种已知蛋白相互作用的蛋白质及其编码基因,被广泛应用于蛋白质组学、细胞信号转导和功能基因组学等领域,已成为分子生物学研究领域的重要实验手段之一,获得了许多有价值的重要发现。 关键词:酵母双杂交系统;蛋白质组学;功能基因组学Abstract:Yeast two-hybrid system is a highly sensitive molecular biology technique,which uses genetic methods to study protein-protein interaction in eukaryotic yeast cells,developed in the early 1990s.It can effectively separate new genes or new protein which has interaction with a known protein and protein-coding genes, is widely used in the field of proteomics, cellular signal transduction and functional genomics, has become one of the important experimental methods in the molecular biology areas, gained a lot of valuable important discovery. Key words:Yeast two-hybrid system;Proteomics;Functional Genomics.
酵母双杂交操作步骤(中文翻译)
(酵母菌储存在-70℃中,引物和质粒DNA储存在-20℃中) 概念: 1. 次序转化:指的是先将一种质粒转化进酵母中(常是DNA-BD/bait plasmid),在选择培养基中选择出阳性克隆,之后再将另外一个质粒(AD fusion library)转化进去。优点:就是比共转化使用更少的质粒DNA,也就是节约质粒DNA。 2. 共同转化:将两种质粒一起转化进酵母中。优点:比次序转化更容易操作。 pGBKT7----的选择物是:kanamycin(卡那霉素)? pGADT7----的选择物是:ampicillin (氨苄西林) ? 各种SD培养基: 1) SD/-ade(腺嘌呤)/-leu(亮氨酸)/-trp(色氨酸)/-his (组氨酸)(1000 ml)(?“四缺”) 酵母氮源(YNB):6.7g ; -ade/-leu/-trp/-his DO supplement 0.60g (购买来就配好的); 葡萄糖 20g (即2%) 2) SD/-leu/-trp/-his (1000 ml) 酵母氮源(YNB):6.7g ; -leu/-trp/-his DO supplement 0.62g ; (购买来就配好的) 葡萄糖 20g. (即2%) 3) SD/-leu/-trp (1000 ml) (?“二缺”) 酵母氮源(YNB):6.7g ; -ade/-leu/-trp/-his DO supplement 0.64g (购买来就配好的); 葡萄糖 20g (即2%) 4) SD/-leu (1000 ml) 酵母氮源(YNB):6.7g ; -leu DO supplement 0.69g ; (购买来就配好的)
酵母双杂交系统及其应用
酵母双杂交系统及其应用 Yeast Two-hybrid System and Its Application 1. 酿酒酵母(Saccharomyces cerevisiae)的生物学特性 (1)单细胞真核生物 尽管酵母细胞比较简单,但它们具有所有真核生物细胞的主要特征,如含有一个独立的细胞核、多条线性染色质包装成染色体、细胞质包含了全部的细胞器和细胞骨架结果(如肌动蛋白纤维)。 (2)与其它真核生物相比,它们的基因组较小,基因数目也较少; 1996 年已完成酵母全基因组测序(1.5 x 10 7 bp ),是第一个被测序的真核生物。大约有6000个基因。目前已经建立了一个6000 个菌株的文库,每一个菌株中只删除了一个基因。其中5000 多株在单倍体状态时能够存活,表明大多数酵母基因时非必需的。 (3)易于培养和操作,可以在实验室快速繁殖 在指数生长期每90 分钟繁殖一代,从单个细胞可以繁殖称克隆群体。 (4)单倍体和双倍体的存在使酿酒酵母便于进行遗传分析 酿酒酵母可以以单倍体状态和双倍体状态生长。单倍体和双倍体之间的转换是通过交配和孢子形成来实现的。 有两种单倍体细胞类型,分别为a 型和α型。在一起生长时,这些细胞因交配而形成a/ α双倍体细胞。在营养匮乏时,a/ α双倍体发生减数分裂,产生一个子囊的结构,每个子囊含有4 个单倍体孢子(两个a-孢子和两个α-孢子)。但当生长条件改善时,这些孢子可以出芽并以单倍体细胞的形式生长或交配而重新形成双倍体。一个酵母细胞可同时兼容几种不同质粒bud,芽, 蓓蕾starvation ,饥饿, 饿死ascus,n.[微生物]子囊meiosis,n.减数分裂, 成熟分裂 haploid,n.[生物]单倍体, 仅有一组染色体的细胞adj.单一的diploid ,adj.双重的, 倍数的, 双倍的n.倍数染色体ascospore,n.[植]囊孢子rupture,v.破裂, 裂开, 断绝(关系等), 割裂。n.破裂, 决裂, 敌对, 割裂 germinate,v.发芽, 发育, 使生长 spore,n.孢子vi. 长孢子
酵母双杂交试验流程
4月4日划线配培养基TE/LIAC PEG/LIAC 配置培养基(YPD YPDA)取酵母细胞划线30°生长3天。 需要用品:三角瓶灭菌封口膜酵母提取物蛋白胨 注:以下所有涉及菌的操作均需在超净台中完成。 4月6号星期三 (1)选择2-3mm的单克隆(枪头吸取)放入3-5ml的YPDA液体培养基,30°摇菌200rpm,8h 7号下午开始,过夜培养,次日若菌液浓度达到标准,可先置于4度冰箱保存。 需要用品:200ul灭菌枪头、50ml三角瓶、YPDA液体培养基、摇床。 4月7号星期四 (2)吸取2.5-10ul酵母培养液,加入25mlYPDA液体培养基,摇菌16-20h直到OD值0.15-0.3。 下午4点开始8号8点结束 Tips:由于第一次活化的菌夜浓度不一,此处建议设置梯度,分别取2.5、5、10 ul酵母培养液,加入25ml YPDA液体培养基(转化5个以下质粒的话,25ml菌量就够后续使用)。 4月8号星期五 (3)将菌液转移至灭菌的50ml离心管中,用天平配平后,室温下700g离心5分钟。 (4)弃掉上清,加入50ml新鲜的YPDA液体重悬菌体(由于离心转速较低,沉淀易悬起来,故倒掉上清液时要小心操作)。 (5)30°震荡培养,直到OD值达到0.4-0.5 (3-5h)。8号8点开始下午一点结束进行以下操作之前,配置好TE/LiAc溶液,并准备好冰浴。 (6)将上述菌液转移至一个灭菌的50ml离心管中,用天平配平后,室温下700g离心5分钟。(7)弃掉上清,用30ml无菌水重悬菌体(小心操作)。 (8)再次用天平配平后,室温下700g离心5分钟,弃去上清,加入1.5ml 1.1xTE/LIAC重悬菌体。(9)将上述溶液转移到灭菌的1.5mlEP管中,高速离心15s。 (10)弃去上清,加入600ul 1.1x TE/LIAC,感受态细胞制备完成,置于冰上待用。 需要物品:50ml灭菌离心管、50ml 三角瓶、1.5ml EP管、5ml灭菌枪头、1ml灭菌枪头、灭菌ddH2O、YPDA液体培养基、1.1x TE/LIAC。 1.1x TE/LIAC10ML 10xTE 1.1ml 10xliac 1.1ml Dh2O8.8ml
蛋白的酵母双杂交操作手册大全
蛋白的酵母双杂交实验 ——以钓饵蛋白筛选cDNA 文库研究蛋白相互作用 第一部分 系统简介 1. 实验原理 蛋白的酵母双杂交实验是以酵母的遗传分析为基础,研究反式作用因子之间的相互作用 对真核基因转录调控影响的实验。很早就已知道,转录活化蛋白可以和DNA 上特异的序列结合而启动相应基因的转录反应。这种DNA 结合与转录激活的功能是由转录活化蛋白上两个相互独立的结构域即DNA 结合结构域(Binding Domain, BD)和转录活化结构域(Activation Domain, AD)分别来完成的,并且这两个结构域对于基因的转录活化都是必须的。目前酵母双杂交实验采用的系统有LexA 系统和Gal4系统两种。在LexA 系统中,DNA 结合结构域由一个完整的原核蛋白LexA 构成,转录活化结构域则由一个88个氨基酸的酸性的大肠杆菌多肽B42构成,它在酵母中可以活化基因的转录; 在 Gal4系统中,BD 和AD 分别由Gal4蛋白上不同的两个结构域(1-147aa 与768-881aa)构成。在利用GAL4系统筛选cDNA 文库或研究蛋白间的相互作用时,DNA 结合结构域与靶蛋白即“诱饵”相结合,转录活化结构域与文库蛋白或要验证的蛋白相结合。一般情况下,单独的BD 可以与GAL4上游活化序列(GAL UAS )结合但不能引起转录,单独的AD 则不能与GAL UAS 结合,只有当BD 与AD 分别表达的融合蛋白由于相互作用而导致两者在空间上相互靠近时,BD 与AD 才能与GAL UAS 结合并且引起报道基因的转录。在BD 与AD 要导入的酵母菌AH109中,通过基因工程的方法在GAL4 UASs 和启动子的下游构建了3个报道基因——ADE2,HIS3,MEL1(或LacZ ),因此可以通过营养缺陷筛选和酵母菌表型的改变来筛选或验证两个蛋白之间是否存在相互作用。GAL4系统的原理如图所示: 图一:酵母双杂交系统工作原理 Kan r Amp r pGBKT7-bait pACT2-cDNA
热—酵母双杂交
酵母双杂交 酵母双杂交系统由Fields和Song等首先在研究真核基因转录调控中建立i 。 典型的真核生长转录因子,如GAL4 GCN4等都含有二个不同的结构域:DNA 结合结构域(DNA-binding domain)和转录激活结构(transcription-activating domain)。前者可识别DNA上的特异序列,并使转录激活结构域定位于所调节的基因的上游,转录激活结构域可同转录复合体的其他成分作用,启动它所调节的基因的转录。 基本原理 二个结构域不但可在其连接区适当部位打开,仍具有各自的功能。而 且不同两结构域可重建发挥转录激活作用。酵母双杂交系统利用杂交基因通过激活报道基因的表达探测蛋白—蛋白的相互作用。主要有二类载体:a 含DNA -binding domain 的载体;b 含DNA-activating domain 的载体。 上述二类载体在构建融合基因时,测试蛋白基因与结构域基因必须在阅读 框内融合。融合基因在报告株中表达,其表达产物只有定位于核内才能驱 动报告基因的转录。例如GAL4-bd具有核定位序列(nuclear-localization sequenee),而GAL4-ad没有。因此,在GAL4-ad氨基端或羧基端应克隆来自SV40的T-抗原的一段序列作为核定位的序列。目前研究中常用bin di ng-doma in 基因有:GAL4(1-147); LexA (E coli 转录抑制因子)的DNA-bd 编码序列。常用的activating-domain 基因有:GAL4(768-881)和 疱疹病毒VP16的编码序列等。 双杂交系统的另一个重要的元件是报道株。报道株指经改造的、含报道基因(reporter gene)的重组质粒的宿主细胞。最常用的是酵母细胞,酵母细胞作为报道株的酵母双杂交系统具有许多优点:〈1〉易于转化、便 于回收扩增质粒。〈2〉具有可直接进行选择的标记基因和特征性报道基因。 〈3〉酵母的内源性蛋白不易同来源于哺乳动物的蛋白结合。一般编码一个蛋白的基因融合到明确的转录调控因子的DNA-结合结构域(如GAL4-bd,LexA-bd);另一个基因融合到转录激活结构域(如GAL4-ad,VP16)。激活
酵母双杂交实验流程
模块七蛋白质之间的相互作用 1. 实验目的 本实验以重组质粒和酵母细胞为材料,学习检测蛋白质相互作用的基本原理和技术方法。主要介绍酵母双杂交的基本原理与操作技术;让学生了解和掌握酵母双杂交系统的应用;掌握酵母感受态的制备的基本原理和主要的操作步骤。 2. 实验原理 1989年Fields和Song等人根据当时人们对真核生物转录起始过程调控的认识(即细胞内基因转录的起始需要转录激活因子的参与),提出并建立了酵母双杂交系统。该系统作为发现和研究活细胞体内的蛋白质与蛋白质之间的相互作用的技术平台,近几年得到了广泛的运用和发展。 相比于其它蛋白质筛选系统,酵母双杂交系统具有以下优点:(1)检测在真核活细胞内进行,在一定程度上代表细胞内的真实情况。(2)作用信号是在融合基因表达后,在细胞内重建转录因子的作用而给出的,省去了纯化蛋白质的繁琐步骤。(3)检测结果是基因表达产物的积累效应,因而可检测存在于蛋白质之间的微弱或暂时的相互作用。(4)酵母双杂交系统可采用不同组织、器官、细胞类型和分化时期材料构建cDNA文库,能分析细胞质、细胞核及膜结合蛋白等多种不同亚细胞部位及功能蛋白。(5)通过mRNA产生多种稳定的酶使信号放大。同时,酵母表型、X-Gal 及HIS3 蛋白表达等检测方法均很敏感。 酵母双杂交系统也具有一定的局限性。首先,经典的双杂交系统分析蛋白间的相互作用定位于细胞核内,因而限制了该系统对某些细胞外蛋白和细胞膜受体蛋白的研究。酵母双杂交系统的另一个局限性是“假阳性”。在酵母双杂交系统建立的初期阶段,由于仅仅采用β-半乳糖苷酶这一单一的报告基因体系,这种报告基因的表达往往不能十分严谨地被控制,因此容易产生假阳性。由于某些蛋白本身具有激活转录的功能或在酵母中表达时发挥转录激活作用,使DNA结合结构域融合蛋白在无特异激活结构域的情况下也可被激活转录。另外某些蛋白表面含有对多种蛋白质的低亲和力区域,能与其他蛋白形成稳定的复合物,从而引起报告基因的表达,产生“假阳性”结果。产生“假阴性”结果的原因可能有许多蛋白质间的相互作用依赖于翻译后加工如糖基化、磷酸化和二硫键形成,还有些蛋白的正确折叠和功能有赖于某些非酵母蛋白的辅助等。 现在的酵母双杂交系统大都采用多种报告基因,如AH109酵母株含有三类报告基因—ADE2、HIS3、MEL1/lacZ,这三类报告基因受控于三种完全不同、异源性的GAL4-反应元件和三类启动子元件-GAL1、GAL2以及MEL1(如图6-1-1)。通过这种方法就消除了两类最主要的假阳性,一类是融合蛋白可以直接与GAL4结合位点结合或者是在结合位点附近结合所带来的假阳性;另一类是融合蛋白和某种转录因子结合后再结合到特定的TA TA盒上所带来的假阳性。ADE2一种报告基因就已经能够提供较强的营养选择压力,这时选择性地使用HIS3报告基因,一来可以降低假阳性率;二来可以控制筛选的严格性(如果需要筛选与诱饵蛋白具有较强结合的蛋白,就可以同时使用ADE2、HIS3两种报告基因;如果只需要筛选与诱饵蛋白具有中等强度或较弱结合的蛋白,就可以使用ADE2或HIS3两者中的一种)。MEL1和lacZ分别编码α-半乳糖苷酶和β-半乳糖苷酶,可以作用于相应的底物
酵母双杂交操作手册 by shenao
酵母双杂交操作手册 by shenao Y2H所需材料: PJ69-4A PJ69-4α or AH109 Y187 pGBKT7 DNA-BD Vector (bait) pGADT7 AD Vector (prey) pGBKT7-53 Control Vector pGBKT7-Lam Control Vector pGADT7-T Control Vector pCL1 Control Vector 3' DNA-BD & AD Sequencing Primers Herring testes carrier DNA Yeast extract,Dextrose(glucose); SD base; DO Supplement; Peptone,with DMF) TE buffer DMSO PEG/LiAc (10X) TE/LiAc buffer (10X) X-a- gal( Yeast Phenotypes –––Ade, His, Leu, Requires adenine (Ade), histidine (His), leucine (Leu), or tryptophan (Trp) in the –or Trp medium to grow; is auxotrophic for at least one of these specific nutrients. Expresses the ADE2 reporter gene; i.e., does not require Ade in the medium to +Ade grow. +His Expresses the HIS3 reporter gene; i.e., does not require His in the medium to grow.
酵母杂交系统
一、酵母单杂交系统 酵母单杂交系统(yeast-one-hybrid system):用酵母细胞检测蛋白质与DNA之间相互作用的一种系统。 酵母单杂交技术最早是1993年由Li等从酵母双杂交技术发展而来,通过对报告基因的表型检测,分析DNA与蛋白之间的相互作用,以研究真核细胞内的基因表达调控。由于酵母单杂交方法检测特定转录因子与顺式作用元件专一性相互作用的敏感性和可靠性,现已被广泛用于克隆细胞中含量微弱的、用生化手段难以纯化的特定转录因子。 酵母单杂交(Yeast one-hybrid)是根据DNA结合蛋白(即转录因子)与DNA顺式作用元件结合调控报道基因表达的原理,克隆与靶元件特异结合的转录因子基因(cDNA)的有效方法。其理论基础是:许多真核生物的转录激活子由物理和功能上独立的DNA结合区(DNA-binding domain BD)和转录激活区(Activation domain AD)组成,因此可构建各种基因与AD的融合表达载体,在酵母中表达为融合蛋白时,根据报道基因的表达情况,便能筛选出与靶元件有特异结合区域的蛋白。理论上,在单杂交检测中,任何靶元件都可被用于筛选一种与之有特异结合区域的蛋白。 二、酵母双杂交系统 酵母双杂交系统(yeast two-hybrid system):将待研究的两种蛋白质的基因分别克隆到酵母表达质粒的转录激活因子(如GAL4等)的DNA结合结构域基因和GAL4激活结构域基因,构建成融合表达载体,从表达产物分析两种蛋白质相互作用的系统。 酵母双杂交系统(Yeast two-hybrid system)的建立是基于对真核生物调控转录起始过程的认识。细胞起始基因转录需要有反式转录激活因子的参与。反式转录激活因子,例如酵母转录因子 GAL4在结构上是组件式的(modular),往往由两个或两个以上结构上可以分开,功能上相互独立的结构域(domain)构成,其中有DNA结合功能域(DNA binding domain,DNA-BD)和转录激活结构域(activation domain,DNA-AD)。这两个结合域将它们分开时仍分别具有功能,但不能激活转录,只有当被分开的两者通过适当的途径在空间上较为接近时,才能重新呈现完整的GAL4转录因子活性,并可激活上游激活序列(upstream activating sequence,UAS)的下游启动子,使启动子下游基因得到转录。 双杂交系统的建立得益于对真核生物调控转录起始过程的认识。细胞起始基因转录需要有反式转录激活因子的参与。80年代的工作表明,转录激活因子在结构上是组件式的(modular),即这些因子往往由两个或两个以上相互独立的结构域构成,其中有DNA结合结构域(DNA binding domain,简称为DB)和转录激活结构域(activation domain,简称为AD),它们是转录激活因子发挥功能所必需的。单独的DB虽然能和启动子结合,但是不能激活转录。而不同转录激活因子的DB和AD形成的杂合蛋白仍然具有正常的激活转录的功能。如酵母细胞的Gal4蛋白的DB与大肠杆菌的一个酸性激活结构域B42融合得到的杂合蛋白仍然可结合到Gal4结合位点并激活转录。 在酵母双杂交系统中,“诱饵”蛋白X克隆至DNA-BD载体中,表达DNA-BD/X融合蛋白;待测试蛋白Y克隆至AD载体中,表达AD/Y融合蛋白。一旦X与Y蛋白间有相互作用,则DNA-BD 和AD也随之被牵拉靠近,恢复行使功能,激活报告重组体中LacZ和HIS3基因的表达。
酵母双杂交实验步骤
LexA酵母双杂交系统简介 一、LexA酵母双杂交系统的设计原理 报告质粒p8op-LacZ的GAL4 UAS编码序列被完全去除,因此在缺乏LexA融合激活剂的情况下,报告基因LacZ的转录活性为零,该基因的筛选标志为URA3,可以作为有自主复制能力的质粒存在于酵母EGY48菌株中,也可以被整合到EGY48基因组DNA上。 质粒pLexA的筛选标志为HIS3,在双杂交系统中用于表达DNA-BD(202个氨基酸残基组成的LexA蛋白)与目标蛋白(钓饵,Bait)的融合蛋白,该融合体的表达受酵母强启动子ADH1的调控,选择与报告基因的操纵子LexA×8结合。 质粒pB42AD的筛选标志为TRP1,在其供外源基因插入的多克隆位点(EcoR I与Xho I)上游,含有SV40核定位(SV40 nuclear localization)、HA(血凝素)及AD(来自于的88个氨基酸残基组成的B42蛋白)等几种编码序列,共同组成可以启动报告基因转录表达的激活成份。在酵母EGY48的基因组中还整合有另一个报告基因Leu,它与LacZ报告基因具有相同的操纵子-LexA,但两者启动子不同。 根据双杂交系统的原理,如果某一复合物同时具有DNA-BD和AD的活性,即可激活报告基因的转录和表达。分别将待测蛋白X、Y的编码序列插入pLexA质粒载体和pB42AD质粒载体的多克隆位点中,然后共同转入含有报告基因的酵母菌株,如果蛋白X与Y能相互作用,则启动报告基因的转录和表达,通过检测报告基因的表达情况,就可以间接反映蛋白X、Y是否具有相互作用以及作用的强弱。 如果将蛋白Y换为取自组织或血液的cDNA文库,则可用X从该文库中筛选出能与其相互作用的蛋白,并且可以获得编码这些蛋白的cDNA。 二、商品化酵母双杂交系统的组成 1. 载体质粒:pLexA、pB42AD、p8op-LacZ、pB42AD-DNA文库 2. 酵母菌株:EGY48、EGY48(p8op-LacZ)、YM4271(EGY48的伴侣菌株) 3. 大肠杆菌菌株: KC8株 4. 对照质粒:
酵母双杂交实验流程(精).doc
模块七蛋白质之间的相互作用 1.实验目的 本实验以重组质粒和酵母细胞为材料, 学习检测蛋白质相互作用的基本原理和 技术方法。主要介绍酵母双杂交的基本原理与操作技术 ; 让学生了解和掌握酵母双 杂交系统的应用 ; 掌握酵母感受态的制备的基本原理和主要的操作步骤。 2.实验原理 1989 年Fields 和Song 等人根据当时人们对真核生物转录起始过程调控的认 识(即细胞内基因转录的起始需要转录激活因子的参与,提出并建立了酵母双杂交系 统。该系统作为发现和研究活细胞体内的蛋白质与蛋白质之间的相互作用的技术平 台 ,近几年得到了广泛的运用和发展。 相比于其它蛋白质筛选系统,酵母双杂交系统具有以下优点:(1 检测在真核活细 胞内进行 ,在一定程度上代表细胞内的真实情况。(2 作用信号是在融合基因表达后, 在细胞内重建转录因子的作用而给出的 ,省去了纯化蛋白质的繁琐步骤。(3 检测结果是基因表达产物的积累效应,因而可检测存在于蛋白质之间的微弱或暂时的相互 作用。(4 酵母双杂交系统可采用不同组织、器官、细胞类型和分化时期材料构建cDNA 文库 ,能分析细胞质、细胞核及膜结合蛋白等多种不同亚细胞部位及功能蛋白。(5 通过mRNA 产生多种稳定的酶使信号放大。同时,酵母表型、X-Gal 及 HIS3 蛋白表达等检测方法均很敏感。 酵母双杂交系统也具有一定的局限性。首先 , 经典的双杂交系统分析蛋白间的 相互作用定位于细胞核内,因而限制了该系统对某些细胞外蛋白和细胞膜受体蛋白 的研究。酵母双杂交系统的另一个局限性是“假阳性”。在酵母双杂交系统建立的 初期阶段 ,由于仅仅采用β-半乳糖苷酶这一单一的报告基因体系,这种报告基因的表 达往往不能十分严谨地被控制,因此容易产生假阳性。由于某些蛋白本身具有激活 转录的功能或在酵母中表达时发挥转录激活作用, 使DNA 结合结构域融合蛋白在 无特异激活结构域的情况下也可被激活转录。另外某些蛋白表面含有对多种蛋白
(发展战略)酵母双杂交系统的发展和应用
酵母双杂交系统的发展和应用 随着对多种重要生物的大规模基因组测序工作的完成,基因工程领域又迎来了一个新的时代---功能基因组时代。它的任务就是对基因组中包含的全部基因的功能加以认识。生物体系的运作与蛋白质之间的互相作用密不可分,例如:DNA合成、基因转录激活、蛋白质翻译、修饰和定位以及信息传导等重要的生物过程均涉及到蛋白质复合体的作用。能够发现和验证在生物体中相互作用的蛋白质与核酸、蛋白质与蛋白质是认识它们生物学功能的第一步。 酵母双杂交技术作为发现和研究在活细胞体内的蛋白质与蛋白质之间的相互作用的技术平台,在近几年来得到了广泛运用。酵母双杂交系统是在真核模式生物酵母中进行的,研究活细胞内蛋白质相互作用,对蛋白质之间微弱的、瞬间的作用也能够通过报告基因的表达产物敏感地检测得到,它是一种具有很高灵敏度的研究蛋白质之间关系的技术。大量的研究文献表明,酵母双杂交技术既可以用来研究哺乳动物基因组编码的蛋白质之间的互作,也可以用来研究高等植物基因组编码的蛋白质之间的互作。因此,它在许多的研究领域中有着广泛的应用。本文就酵母双杂交的技术平台和应用加以介绍。 酵母双杂交系统的建立是基于对真核生物调控转录起始过程的认识。细胞起始基因转录需要有反式转录激活因子的参与。反式转录激活因子,例如酵母转录因子GAL4在结构上是组件式的(modular),往往由两个或两个以上结构上可以分开,功能上相互独立的结构域(domain)构成,其中有DNA结合功能域(DNA binding domain,DNA-BD)和转录激活结构域(activation domain,DNA-AD)。这两个结合域将它们分开时仍分别具有功能,但不能激活转录,只有当被分开的两者通过适当的途径在空间上较为接近时,才能重新呈现完整的GAL4转录因子活性,并可激活上游激活序列(upstream activating sequence, UAS)的下游启动子,使启动子下游基因得到转录。 根据这个特性,将编码DNA-BD的基因与已知蛋白质Bait protein的基因构建在同一个表达载体上,在酵母中表达两者的融合蛋白BD-Bait protein。将编码AD的基因和cDNA文库的基因构建在AD-LIBRARY表达载体上。同时将上述两种载体转化改造后的酵母,这种改造后的酵母细胞的基因组中既不能产生GAL4,又不能合成LEU、TRP、HIS、ADE,因此,酵母在缺乏这些营养的培养基上无法正常生长。当上述两种载体所表达的融合蛋白能够相互作用时,功能重建的反式作用因子能够激活酵母基因组中的报告基因HIS、ADE、LACZ、MEL1,从而通过功能互补和显色反应筛选到阳性菌落。将阳性反应的酵母菌株中的AD-LIBRARY 载体提取分离出来,从而对载体中插入的文库基因进行测序和分析工作。在酵母双杂交的基础上,又发展出了 酵母单杂交、酵母三杂交和酵母的反向杂交技术。它们被分别用于核酸和文库蛋白之间的研究、三种不同蛋白之间的互作研究和两种蛋白相互作用的结构和位点。 基于酵母双杂交技术平台的特点,它已经被应用在许多研究工作当中。
