免疫组化与病理诊断

免疫组化与病理诊断
免疫组织化学(Immunohistochemistry,IHC)是临床病理诊断中常用的技术和手段。从20世纪70年代开始,免疫组化技术就已经应用于病理诊断,对诊断肿瘤、肿瘤分类、判断预后产生了巨大的影响,同时也扩展了人们对于各种疾病及肿瘤形成过程的认识,提高了病理诊断与研究水平。本文重点讨论了免疫组化技术在临床上的应用与常见的免疫组化指标在临床上的意义。
1. 什么是免疫组化?
2. 什么是病理诊断?
3. 免疫组化技术在临床上的应用
4. 病理诊断中免疫组化的局限性
5. 临床上常用指标的意义
1、什么是免疫组化?
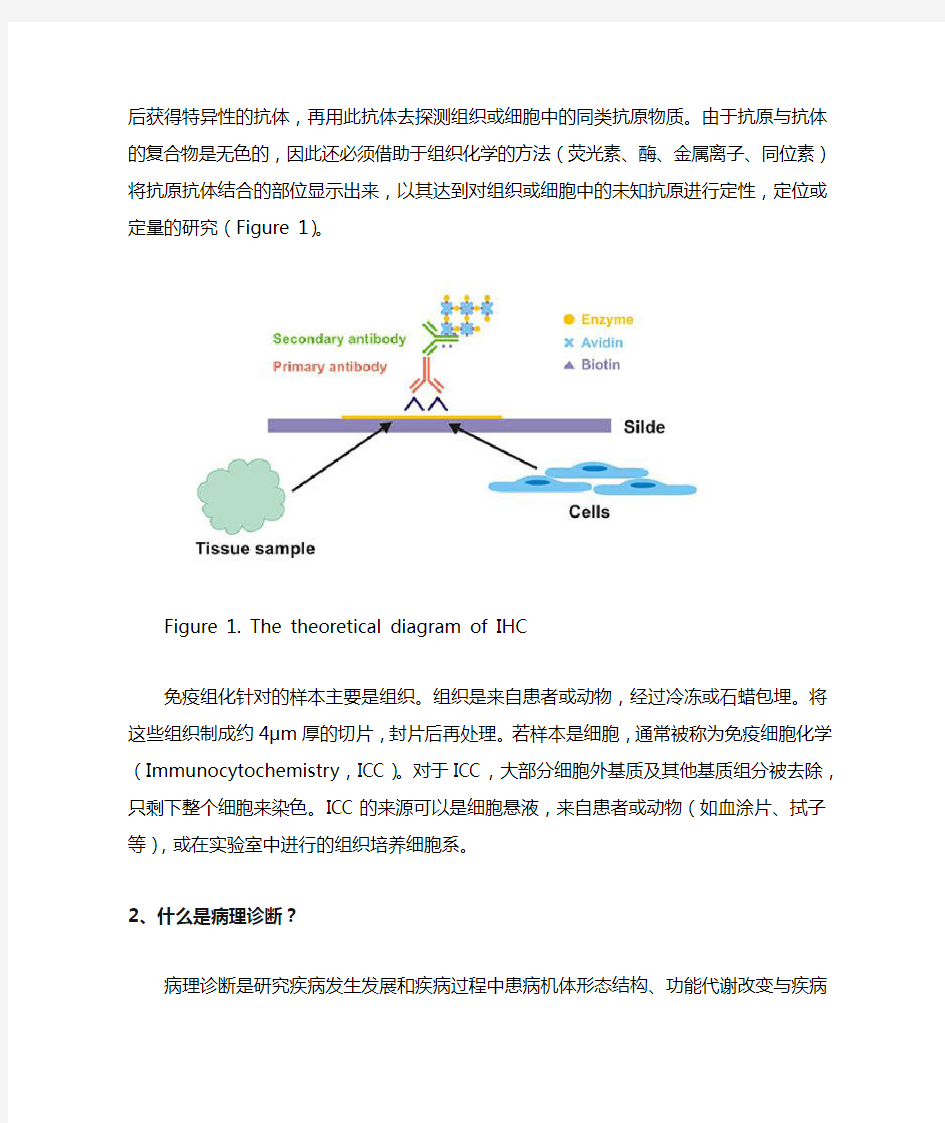
在了解免疫组化在临床上的应用之前,我们先来了解下什么是免疫组化。免疫组化,是应用免疫学基本原理——抗原抗体反应,即抗体和抗原之间的结合具有高度的特异性,先将组织或细胞中的某种化学物质提取出来,以此作为抗原或半抗原。然后通过免疫动物后获得特异性的抗体,再用此抗体去探测组织或细胞中的同类抗原物质。由于抗原与抗体的复合物是无色的,因此还必须借助于组织化学的方法(荧光素、酶、金属离子、同位素)将抗原抗体结合的部位显示出来,以其达到对组织或细胞中的未知抗原进行定性,定位或定量的研究(Figure 1)。
Figure 1. The theoretical diagram of IHC
免疫组化针对的样本主要是组织。组织是来自患者或动物,经过冷冻或石蜡包埋。将这些组织制成约4μm厚的切片,封片后再处理。若样本是细胞,通常被称为免疫细胞化学(Immunocytochemistry,ICC)。对于ICC,大部分细胞外基质及其他基质组分被去除,只剩下整个细胞来染色。ICC 的来源可以是细胞悬液,来自患者或动物(如血涂片、拭子等),或在实验室中进行的组织培养细胞系。
2、什么是病理诊断?
病理诊断是研究疾病发生发展和疾病过程中患病机体形态结构、功能代谢改变与疾病转归,从而为疾病的诊断、治疗与预防提供必要的理论基础和实践依据。
病理诊断是对手术切下或尸体解剖取下的肿瘤标本进行固定染色后,在显微镜下进行组织学检查,以便于诊断疾病。样本更多源于活人。尽管各种影像学技术飞速发展,但是病理诊断仍然是肿瘤各种检查方法中最可靠的,病理诊断被喻为“金标准”,也是疾病的最终诊断。如果将病理诊断和生化免疫等检验诊断进行比较,病理诊断就好像警察办案获得的指纹、脚印、DNA等实际证据。因其通过显微镜观察疑似病变组织的细胞形态和结构,可直接看出组织发生了怎样的病理变化,能较准确地对疾病做出判断,尤其在肿瘤性质的诊断上更为常用。而免疫组化,就是病理诊断中最常用的检测技术。
3、免疫组化技术在临床上的应用
目前免疫组化技术应用于临床主要有以下几个方面:
?肿瘤良恶性的判断:对于反应性增生还是肿瘤性增生,可用免疫球蛋白(Ig)的轻链抗体检测B淋巴细胞增生的单克隆或多克隆性来区别。
?确定肿瘤分期:肿瘤分期是判断预后的一个指标,与是否浸润、有无淋巴管或血管侵袭密切相关,而通过免疫组化方法可以判断肿瘤是否浸润、有无淋巴管或血管侵袭。
?细胞属性的判定:通过特定抗体标记出细胞内相应的抗原成分,来判定细胞的属性,确定肿瘤的来源。
?确定来源不明的转移瘤的原发部位:对于来源不明的转移瘤,用免疫组化技术有助于确定恶性肿瘤的组织学来源,进一步确定原发部位。如角蛋白抗体(CK20)在胃肠道癌、胆管癌、胰腺癌中阳性,而在肺癌、乳腺癌、肾癌中阴性。
?对“未分化”恶性肿瘤的分类:未分化恶性肿瘤包括癌或肉瘤,在HE切片上由于肿瘤的“未分化”而缺少肿瘤细胞的起源特征不能分类,初步区分组织学类型用非特异性抗体,在其基础上再选用特异性抗体做进一步鉴定。
?进一步分类不同器官与组织交界处肿瘤:由于重叠的特征,在一些组织器官交界处的肿瘤,仅凭组织学基础对肿瘤进行分类很困难。
如发生于组织交界处的肿瘤有睾丸胚胎癌与精原细胞癌,两者较难区别,且治疗与预后显著不同,但用免疫组化检测角蛋白就较易于区别:角蛋白阴性则为精原细胞癌,而角蛋白阳性则为胚胎癌。
?及时准确的发现微小转移灶:在常规组织切片中,辨别单个或几个转移性肿瘤细胞很难,淋巴结内窦性组织细胞增生与某些癌的早期转移有时也不易区别,而采用免疫组化方法,有助于及时准确的发现微小(癌)转移灶。
4、病理诊断中免疫组化的局限性
但是,随着免疫组化的广泛应用,发现免疫组化技术存在一些局限性。在肿瘤诊断中评估免疫组化的局限性主要在抗体特异性和解释方面。在免疫组化操作过程中中都必须有适当的阳性与阴性对照,作为技术完整性质量控制,如对照组被忽略或不理想时,免疫组化染色的结果要谨慎对待,免疫组化的正确结果,不仅要依靠技术步骤上规范化操作,而且有赖于正确的解释,在报告免疫组化染色结果时不应孤立地解释,应考虑到诊断与鉴别诊断、所应用的抗体特性、所研究组织性质,同时还要注意假阳性与假阴性结果的干扰。深入研究免疫组化原理和技术,必须熟悉各种抗体真阳性反应部位,实现实验室间免疫组化标准化,使免疫组化在病理诊断中发挥最大的辅助作用。
5、临床上常用免疫组化指标的意义
大家都知道病理检查是临床诊疗的金标准,尤其对于肿瘤患者,更是一封判决书。其中免疫组化(IHC)的结果对肿瘤的诊断和治疗及预后分析尤为重要。本文就目前开展的系列检查及意义进行了整理。
5.1 恶性肿瘤的Ki-67 和p53 常规检查
目前的研究表明,大部肿瘤的复发、转移取决于Ki-67值和p53值,而与肿瘤的组织的分型关系不是十分密切,如中分化腺癌,如果Ki-67 和p53 值超过50%,预后不佳。相反,如肿瘤的组织分型为低分化腺癌,而Ki-67 和p53 值较低,预后也会较中分化或高分化癌的预后稍好。
5.2 耐药预后标记全套4 项:P-gp,GSTπ,TOPOⅡ,Ki-67
P-糖蛋白(P-gp)--药泵作用--胞膜/胞浆--阳性率越高,对下列药物耐药性越强:阿霉素、柔红霉素、表阿霉素、米托蒽醌、长春花碱、长春新碱、紫杉醇及泰素帝。
谷光甘肽S 转移酶(GST π)--解毒作用--胞浆--阳性率越高,对下列药物耐药性越强:阿霉素、顺铂、氮芥、环磷酰胺及瘤可宁。
拓扑异构酶Ⅱ(TOPOⅡ)--靶点作用--胞核--阳性率越高,对下列药物越有效:蒽环类抗生素和鬼臼毒素类,如VP-16、替尼泊苷、玫瑰树碱、新霉素、柔红霉素、表阿霉素、阿霉素、VM26。阳性率高者对VP-16 尤其有效。
Ki-67--细胞增殖标志--胞核--阳性率越高,肿瘤增殖越快,恶性程度越高。
5.3 乳腺癌五项(ER、PR、C-erbB-2(Her-2)、Ki-67、p53)
乳腺癌耐药预后标记,全套7 项:P-gp,GSTπ,TOPOⅡ,Ki-67,ER,PR,HER2。
雌激素受体(ER)--性激素作用--胞核--阳性率越高,肿瘤对内分泌治疗越有效,预后越好。
孕激素受体(PR)--性激素作用--胞核--阳性率越高,肿瘤对内分泌治疗越有效,预后越好。
C-erbB-2--癌基因产物--胞浆--阳性率越高,肿瘤恶性程度越高。
p53 一种抑癌基因,分野生型(Wtp53)和突变型(Mtp53)。野生型Wtp53 因微量免疫组化难以检测,突变型Mtp53 能够被免疫组化测定,突变后则丧失了启动细胞凋亡的能力。突变型p53 高表达,细胞的高度增生、分化程度差分化、恶性程度越高、预后不良,公认预后差指标之一。
5.4 垂体腺瘤功能六项检查
LH(促黄体生成素),FSH(卵泡刺激素),ACTH(促肾上腺皮质激素),TSH(促甲状腺素),PRL(泌乳素)、GH(生长激素)。根据某一种抗体阳性表达进行术后药物治疗。
?DOG1 可以表达于部分CD117 阴性的GIST 中(6%)
?DOG1 在胃部GIST、上皮样GIST、PDGFRA 突变的病例中,表达率高
病理科免疫组化在临床上的应用及其意义
病理科免疫组化在临床上得应用及其意义 免疫组化技术就是以免疫学得抗原抗体反应为其理论基础发展起来得一门方法学,在生物学领域尤其就是在医学得基础与临床研究中发挥重要得作用,对疾病尤其就是肿瘤得诊断、鉴别诊断及发病机制得研究提供了强有力得手段、免疫组化技术就是20世纪70年代初Sterb Berger 在酶标法得基础上发明得,80年代在外国开始应用于临床研究与诊断,90年代初在我国逐渐开始应用于疑难病例得诊断与鉴别诊断。随着新技术得不断发展,抗体种类从研发开始得十几种发展到目前数百种抗体应用于临床科研得各个领域,我国在临床病理诊断上可用抗体293种。由于抗体较昂贵,所以各院根据活检量与病种不同选择不同得抗体,这些抗体对大部分疑难病例得诊断起到重要得辅助作用、对病人得预后及指导治疗具有重要得意义。 一、目前常用得抗体分四大类 1。上皮性标记物:CKhigh(AE3), CK low,CK-pan,CK19,CK7, CK20,EMA,CEA,-CA 15-3,SCLC , E—Caldeherin,CA125, Tg(甲状腺球蛋白) ,TTF—1?AFP。这些抗体阳性,表明肿瘤组织起源于上皮组织,如果就是恶性肿瘤,就就是癌2?.间叶组织标记物:SMA ,Desmin,Vimentin,Lysozyme,AACT, CD68 MyoD1,CD117,这些抗体阳性,表明肿瘤组织起源于间叶组织,如果就是恶性肿瘤,就就是肉瘤、3?、神经及神经内分泌标记物:CgA ,Synaptophysin,NSE,S-100:NF (神经纤维丝蛋白),GFAP,CD99,CD56、 4淋巴细胞标志物: T cell标记物:CD3, CD45RO, CD43,CD5, CD8,CD4,ALK,GranmB , CD56 。?Bcell标记物:CD—20 ,CD79a,CD23, CD10,Kappa ,Lambda CD21CD38 ,CyclinD1 ,Bcl—2。?其它:LCA,CD15,CD30,MPO,CD34,TdT,这些抗体用于淋巴瘤33个亚型得诊断与鉴别诊断。? 二、目前开展得系列检查与意义 1。乳腺癌五项(ER、PR、C—erbB-2(Her-2)、Ki—67、P53) ER、PR阳性,90%得病人对三苯氧胺类药物疗效好。C-erbB-2阳性(2+—3+)可服用抗Her—2基因药物。如果ER与PR均阴性,C-erbB-2强阳性预示预后不好。 Ki—67就是细胞生长指数,代表细胞周期中除G0期以外得细胞生长速度。Ki—67值越高表明肿瘤细胞生长越快,预后越不好。P53就是广谱致癌基因,在许多肿瘤中都有表达,表达值越高预后越不好。据报道,国际上目前有抗P53基因阳性得药物用于治疗肿瘤。 2。垂体腺瘤功能六项检查 LH( 促黄体生成素),FSH(卵泡刺激素),ACTH(促肾上腺皮质激素),TSH( 促甲状腺素),PR L(泌乳素)GH(生长激素) 。根据某一种抗体阳性表达进行术后药物治疗。 3.恶性肿瘤得Ki—67与P53常规检查 目前得研究表明,大部肿瘤得复发、转移取决于Ki—67值与P53值,而与肿瘤得组织得分型关系不就是十分密切,如中分化腺癌,如果Ki-67与P53值超过50%,预后不佳,相反,如肿瘤得组织分型为低分化腺癌,而Ki-67与P53值较低,预后也会较中分化或高分化癌得预后稍好。4?.GIST(胃肠道间质瘤)与EGIST(胃肠道外间质瘤)得诊断?GIST就是90年代新发现得肿瘤,过去均诊断为平滑肌瘤或平滑肌肉瘤,现在经过一组免疫组化可将其诊断,GIST得生物学形为一般无良性,因为小于2cm得GIST偶而也有转移。其良恶性程度取决于肿瘤得大小与核分裂像,国际确定GI ST侵袭行为危险性得推荐方案如下: 危险程度大小核分裂数?很低〈2cm <5/50HPF?低2-5cm〈5/50HPF 中等<5cm5-10cm 6—10/50HPF〈5/50HPF?高〉5cm>10cm不计>5/50HPF不计>10/50HPF?GIST得免疫组化结果为:CD117(+)、CD34(±)、S—100(±)Actin(±)、Desmin(—)、CD117阳性可用格林卫治疗,且效果较好。
免疫组化原理
免疫组织化学的概念: 免疫组化是利用抗原与抗体特异性结合的原理,通过化学反应使标记抗体的显色剂(荧光素、酶、金属离子、同位素) 显色来确定组织细胞内抗原(多肽和蛋白质),对其进行定位、定性及定量的研究,称为免疫组织化学。 免疫组化实验中常用的抗体为单克隆抗体和多克隆抗体。 免疫组化实验所用的组织和细胞标本有哪些? 实验所用主要为组织标本和细胞标本两大类,前者包括石蜡切片(病理大片和组织芯片)和冰冻切片,后者包括组织印片、细胞爬片和细胞涂片。 其中石蜡切片是制作组织标本最常用、最基本的方法,对于组织形态保存好,且能作连续切片,有利于各种染色对照观察;还能长期存档,供回顾性研究;石蜡切片制作过程对组织内抗原暴露有一定的影响,但可进行抗原修复,是免疫组化中首选的组织标本制作方法。 石蜡切片为什么要做抗原修复?有哪些方法? 石蜡切片标本均用甲醛固定,使得细胞内抗原形成醛键、羧甲键而被封闭了部分抗原决定簇,同时蛋白之间发生交联而使抗原决定簇隐蔽。所以要求在进行IHC染色时,需要先进行抗原修复或暴露,即将固定时分子之间所形成的交联破坏,而恢复抗原的原有空间形态。 常用的抗原修复方法有微波修复法,高压加热法,酶消化法,水煮加热法等,常用的修复液是pH6.0的0.01 mol/L的柠檬酸盐缓冲液。 免疫组化常用的染色方法有哪些? 根据标记物的不同分为免疫荧光法,免疫酶标法,亲和组织化学法,后者是以一种物质对某种组织成分具有高度亲合力为基础的检测方法。这种方法敏感性更高,有利于微量抗原(抗体)在细胞或亚细胞水平的定位,其中生物素——抗生物素染色法最常用。 抗体的保存: 抗体储存容器应由不吸附蛋白质的材料制成,常用的有聚丙烯,聚碳酸酯和硼硅酸玻璃。如储存的抗体中蛋白浓度很低(10-100mg/L),就应另加隔离蛋白以减少容器对抗体蛋白的吸附,隔离蛋白常用0.1%-1.0%的牛血清白蛋白。绝大多数已稀释的抗体应存在4℃-8℃条件下,以免冻融对抗体蛋白产生有害效应。抗体原液和已分离的免疫球蛋白组分应保存于-20℃条件下,并避免反复冻融。冷冻的抗体溶液应置于室温中缓慢地解冻,应绝对避免用高温快速解冻。被细菌污染的抗体常会出现假阳性结果,应将污染的抗体溶液及其他试剂弃之。为防止细菌污染,可于抗体溶液中加入0.01%叠氮钠。抗体经真空冷冻干燥后置-20℃以下可保存3-5年。保存稀释后的单抗应加入0.1%叠氮钠浓度。大多数稀释抗体可进行冷冻保存,少数抗体可能会丢失抗原活性。大多数单抗,只要蛋白浓度适当,可在4℃下保存数月。 多聚赖氨酸溶液(Poly-L-Lysine Solution) Cat.No.: SGP8920 Size: 10ml Conc.: 0.1% w/v, in water Storage: 18-26℃ Thimerosal, 0.01%, added as preservative 多聚赖氨酸溶液是广泛应用的组织切片与玻片黏合剂,该多聚阳离子分子与组织切片上的阴离子相互作用会产生较强的黏合力。 适用组织学,免疫组织化学,冰冻切片,细胞涂片,原位杂交等使用的玻片的防脱片处理,以防实验操作过程中组织掉片。也可用于细胞培养,增加细胞贴壁能力。 [使用说明] 免疫学 操作步骤(可直接在玻片上涂布) 1.灭菌的ddH2O 1:10稀释该多聚赖氨酸溶液。
病理科为什么要做免疫组化
龙源期刊网 https://www.360docs.net/doc/af10287442.html, 病理科为什么要做免疫组化 作者:郑宏 来源:《学习与科普》2019年第15期 随着医学技术的快速发展,免疫组化也被越来越多的应用到了病理科检查里面。但是,很多病人在接受免疫组化时心里都是充满了疑惑的,其既不知道免疫组化是什么,也不明白自己为什么要接受免疫组化。甚至还有一部分病人认为医生让自己接受免疫组化就是为了挣钱,导致了医患矛盾的出现,对治疗工作的顺利展开造成了极大的阻碍。所以,接下来本文就对免疫组化及其原理进行了简单介绍,然后阐述了病理科为什么要安排病人进行免疫组化检查。 一、什么是免疫组化? 所谓免疫组化实际上就是应用抗原抗体反应这一原理,通过化学反应来让标记抗体的显色剂显色对组织细胞里多肽和蛋白质等抗原进行定位、定性以及相对定量研究的一种新细胞化学技术。按照标记物种类的不同,免疫组织化学技术主要分为免疫荧光法、免疫酶法、免疫铁蛋白法、免疫金法及放射免疫自显影法等几种。 免疫组化的基本原理就是抗原抗体反应。抗原和抗体结合的时候会出现非常大的特异性,免疫组化就是通过此原理的有效利用,先完成细胞或者组织里面的相应化学物质制取,将其当成抗原或者半抗原,然后再利用免疫动物完成特异性抗体的获取,最后再通过这个特异性抗体去探测细胞或者组织里面是否有同类抗原存在。又因为抗原、抗体以及其复合物都是没有颜色存在的。所以,还需要通过组织化学的方法完成抗原抗体结合部位的着色,从而更加准确的完成对人体里面未知抗原的定位、定性以及定量研究工作,为后续的判断工作提供更有力的支持和保障,有效避免判断失误的情况发生。 二、病理科安排病人做免疫组化的原因? 在最近这几年,随着各种特异性抗体的产生,通过传统的检查技术已经没有办法完成病情的准确判断了。以肿瘤研究为例,在免疫组化技术出现以前,对肿瘤的诊断和分类还局限于细胞水平,而引入免疫组化技术后,则使研究的深度提高到了生物化学水平、分子水平。同时免疫组化这一新的细胞化学技术还拥有特异性强、敏感性高、定位准确以及形态功能相结合等优点,可以帮助医生更为精准的完成病情判断,从而为后续治疗工作的展开提供更为强有力的依据。 首先,通过免疫组化可以让医生完全肿瘤来源的准确确认。我们身体器官以及组织里面的细胞,由于起源都是一样的,所以它们的形态结构也十分相似,很多时候根据形态根本没有办法准确的完成区分工作。仅仅通过肉眼进行分辨的话,会有极大可能因为主观性或者疏忽导致病情判断错误的情况出现,影响到后续的治疗工作,甚至有可能会对人们的身体健康造成更为恶劣的影响。而免疫组化这种方法则会对相应的细胞组织进行染色处理,将其情況更为直观的
免疫组化技术(原理、分类、步骤及主要试剂、设备准备)
免疫组化技术 免疫组化技术
业精于勤而荒于嬉 行成于思而毁于随
免疫组化技术
原理
抗原抗体反应,即抗原与抗体特异性结合的原理,通过化学反应使标记抗体的显色剂 (荧光素、酶、金属离子、同位素) 显色 来确定组织细胞内抗原(多肽和蛋白质),对其进行定位、定性及定量的研究。 众所周知,抗体与抗原之间的结合具有高度的特异性。免疫组化正是利用这一特性,即先将组织或细胞中的某些化学物质提取 出来,以其作为抗原或半抗原去免疫实验动物,制备特异性抗体,再用这种抗体(第一抗体)作为抗原去免疫动物制备第二抗体,并 用某种酶(常用辣根过氧化物酶)或生物素等处理后再与前述抗原成分结合,形成抗原 - 一抗 - 二抗复合物,将抗原放大,由于抗 体与抗原结合后形成的免疫复合物是无色的,因此,还必须借助于组织化学方法将抗原抗体反应部位显示出来(常用显色剂 DAB 显示 为棕黄色颗粒) 。通过抗原抗体反应及呈色反应,显示细胞或组织中的化学成分,在显微镜下可清晰看见细胞内发生的抗原抗体反应产 物,从而能够在细胞或组织原位确定某些化学成分的分布、含量。组织或细胞中凡是能作抗原或半抗原的物质,如蛋白质、多肽、氨 基酸、多糖、磷脂、受体、酶、激素、核酸及病原体等都可用相应的特异性抗体进行检测。
分类(常用)
1、免疫荧光方法
最早建立的免疫组织化学技术。它利用抗原抗体特异性结合的原理,先将已知抗体标上荧光素,以此作为探针检查细胞或组织内 的相应抗原,在荧光显微镜下观察。当抗原抗体复合物中的荧光素受激发光的照射后即会发出一定波长的荧光,从而可确定组织中某 种抗原的定位,进而还可进行定量分析。由于免疫荧光技术特异性强、灵敏度高、快速简便,所以在临床病理诊断、检验中应用比较 广。
2、免疫酶标方法
免疫酶标方法是继免疫荧光后, 60 年代发展起来的技术。 于 基本原理是先以酶标记的抗体与组织或细胞作用, 然后加入酶的底物, 生成有色的不溶性产物或具有一定电子密度的颗粒,通过光镜或电镜,对细胞表面和细胞内的各种抗原成分进行定位研究。免疫酶标 技术是目前定位准确、对比度好、染色标本可长期保存,适合于光、电镜研究等。免疫酶标方法的发展非常迅速,已经衍生出了多种 标记方法,目前在病理诊断中广为使用的当属 PAP 法(过氧化物酶-抗过氧化物酶) 、ABC 法(卵白素-生物素-过氧化物酶复合物) SP 、SP 、即用型二步法(聚合物链接)等。 法(链霉菌抗生物素蛋白-过氧化物酶) 链霉菌抗生物素蛋白-过氧化物酶)
3、免疫胶体金技术
免疫胶体金技术是以胶体金这样一种特殊的金属颗粒作为标记物。胶体金是指金的水溶胶,它能迅速而稳定地吸附蛋白,对蛋白 的生物学活性则没有明显的影响。因此,用胶体金标记一抗、二抗或其他能特异性结合免疫球蛋白的分子(如葡萄球菌 A 蛋白)等作为 探针,就能对组织或细胞内的抗原进行定性、定位,甚至定量研究。由于胶体金有不同大小的颗粒,且胶体金的电子密度高,所以免 疫胶体金技术特别适合于免疫电镜的单标记或多标记定位研究。由于胶体金本身呈淡至深红色,因此也适合进行光镜观察。如应用银 加强的免疫金银法则更便于光镜观察。
4、免疫铁蛋白法 5、放射免疫自显影法
标本
1、组织标本:石蜡切片 石蜡切片(病理切片和组织芯片) 、冰冻切片 石蜡切片 2、细胞标本:组织印片、细胞爬片、细胞涂片
---------------------------------------------------------------------------------华中科技大学同济医学院
1
常见肿瘤病理诊断中免疫组化抗体选择
泌尿与男性生殖系统肿瘤 1.前列腺癌:CK、P63、34?E12、PSA、P504S(9AMAC)、AR 2.前列腺增生/腺瘤:CK、P63、34BE12、P504S 3.肾癌:CK、EMA、Inhibin、Melan-A、CK7、Vimentin、PAX2、CD10 4.肾母细胞瘤:WT-1、CK、P53、Ki-67 5.膀胱尿路上皮癌:CK7、CK20、P53、Ki-67、P63 6.精原细胞瘤:CK、PLAP、CD117、LCA、OCT3/4 淋巴造血系统肿瘤 7.胸腺肿瘤:CK、CD3、CD5、CD20、TdT、EBV* 8.霍奇金淋巴瘤:CD30、CD15、ALK-1、EMA、CD3、CD20、EBV*、PAX-5 9.非霍奇金淋巴瘤:CD3、CD20、CD45RO、CD79α、TdT、CD43 10.间变大细胞淋巴瘤:CD30、CD15、ALK-1、EMA、CD3、CD20、EBV* 11.弥漫性大B细胞淋巴瘤:CD3、CD20、CD45RO、CD79α、CD43、CD30、Ki-67 12.小B细胞淋巴瘤:CD3、CD5、CD10、CD20、CD23、CD79α、CyclinD1、TdT 13.T细胞淋巴瘤:CD3、CD20、CD43、CD45RO、CD79α、TdT、TiA-1、Perforin 14.套细胞淋巴瘤:CD3、CD5、CD20、CD79α、CyclinD1、TdT、Bcl-2、Ki-67 15.T/NK细胞淋巴瘤:CD3、CD20、CD45RO、CD79α、CD56、TiA-1、Perforin、粒酶B 16.淋巴上皮病变/癌:CK、EMA、S-100、Ki-67、P53、EBV*、P63、CD30、CD20 17.Burkitt淋巴瘤:CD3、CD20、CD79α、CD10、Bcl-2、Bcl-6、Ki-67、EBV*、TdT 18滤泡性淋巴瘤:CD3、CD20、CD45RO、CD79α、CD10、Bcl-2、Bcl-6、Ki67 19.脂膜炎样T细胞淋巴瘤:CD2、CD3、CD7、CD20、CD43、Perforin、TiA-1、EBV* 20.浆细胞瘤:CD3、CD20、CD38、CD138、CD79α、EMA、κ*、λ* 21.坏死性淋巴结炎:CD3、CD20、CD45RO、CD79α、CD43、CD68、Mac387、CD163 22.粘膜相关淋巴瘤:CK、CD3、CD5、CD10、CD20、CD23、CD43、CD79a、CyclinD1 23.血管免疫母细胞性淋巴瘤:CD3、CD20、CD45RO、CD43、CD79α 24.组织细胞肉瘤:S100、CD10、CD21、CD35、CD68、Lysozyme、MPO、CD33、CD34、CD11c、CD14、CD45R O 25.朗格罕氏细胞增生症/肉瘤:S100、CD1α、CD68、CD35、HMB45、CK、EMA、Ki67、CD45 26.指状突树突细胞肉瘤/肿瘤:S100、CD1α、CD68、CD21、CD35、CD3、CD20、CD30、CK、EMA、Ki67、C D45 27.滤泡树突细胞肉瘤/肿瘤:CD21、CD35、S100、CD1α、CD68、CD3、CD23、EMA、VIM、MPO、CD34、CD7 9α、CK、HMB45 28.肥大细胞肿瘤:CD117、CD45、CD33、CD68、CD15、CD3、CD20 消化系统肿瘤 29.胃癌:CK7、CK20、Villin、CEA、P53、Ki-67、CDX-2、GST-π、AB/PAS** 30.肠癌:CK7、CK20、Villin、CEA、P53、Ki-67、CDX-2、GST-π、AB/PAS** 31.肝细胞癌:AFP、CD34、CEA、CK8/18、CK19、Ki-67、P53、HbsAg、Hepatocyte 32.肝胆管细胞癌:CK7、CK20、Villin、AFP、CD34、CEA、CK8/18、CK19、Ki-67、Hepatocyte、HbsAg 33.食道癌:P53、Ki-67、CDX-2、GST-π、P63 34.胰腺癌:CEA、P53、Ki-67、CDX-2、GST-π、Villin、CK7、CK20、 35.胰岛细胞瘤:CD56、Syn、CgA、Ki-67、Insulin、CK8/18、CK19 39.肝炎病毒:HbsAg、HbcAg、HCV 涎腺肿瘤 37.涎腺粘液性囊腺癌:CK、P63、SMA、Vimentin、Myosin-heavy chain
病理科免疫组化在临床上的应用及其意义
病理科免疫组化在临床上的应用及其意义 免疫组化技术是以免疫学的抗原抗体反应为其理论基础发展起来的一门方法学,在生物学领域尤其是在医学的基础和临床研究中发挥重要的作用,对疾病尤其是肿瘤的诊断、鉴别诊断及发病机制的研究提供了强有力的手段。免疫组化技术是20世纪70年代初Sterb Berger在酶标法的基础上发明的,80年代在外国开始应用于临床研究和诊断,90年代初在我国逐渐开始应用于疑难病例的诊断和鉴别诊断。随着新技术的不断发展,抗体种类从研发开始的十几种发展到目前数百种抗体应用于临床科研的各个领域,我国在临床病理诊断上可用抗体293种。由于抗体较昂贵,所以各院根据活检量和病种不同选择不同的抗体,这些抗体对大部分疑难病例的诊断起到重要的辅助作用。对病人的预后及指导治疗具有重要的意义。 一、目前常用的抗体分四大类 1.上皮性标记物:CK high(AE3),CK low ,CK-pan,CK19,CK7,CK20,EMA,CEA,-CA15-3,SCLC , E-Caldeherin, CA125, Tg(甲状腺球蛋白) ,TTF-1 AFP。这些抗体阳性,表明肿瘤组织起源于上皮组织,如果是恶性肿瘤,就是癌 2.间叶组织标记物:SMA ,Desmin,Vimentin,Lysozyme,AACT , CD68 MyoD1,CD117,这些抗体阳性,表明肿瘤组织起源于间叶组织,如果是恶性肿瘤,就是肉瘤。 3.神经及神经内分泌标记物:CgA ,Synaptophysin,NSE,S-100:NF (神经纤维丝蛋白),GFAP,CD99,CD56。 4淋巴细胞标志物: T cell标记物:CD3, CD45RO , CD43, CD5, CD8,CD4,ALK,GranmB , CD56 。 B cell标记物:CD-20 ,CD79a ,CD23,CD10 ,Kappa ,Lambda CD21 CD38 ,CyclinD1 ,Bcl-2。 其它:LCA,CD15,CD30,MPO ,CD34,TdT,这些抗体用于淋巴瘤33个亚型的诊断和鉴别诊断。 二、目前开展的系列检查和意义 1.乳腺癌五项(ER、PR、C-erbB-2(Her-2)、Ki-67、P53) ER、PR阳性,90%的病人对三苯氧胺类药物疗效好。C-erbB-2阳性(2+-3+)可服用抗Her-2基因药物。如果ER和PR均阴性,C-erbB-2强阳性预示预后不好。 Ki-67是细胞生长指数,代表细胞周期中除G0期以外的细胞生长速度。Ki-67值越高表明肿瘤细胞生长越快,预后越不好。P53是广谱致癌基因,在许多肿瘤中都有表达,表达值越高预后越不好。据报道,国际上目前有抗P53基因阳性的药物用于治疗肿瘤。 2.垂体腺瘤功能六项检查 LH(促黄体生成素),FSH(卵泡刺激素),ACTH(促肾上腺皮质激素),TSH(促甲状腺素),PRL(泌乳素)GH(生长激素)。根据某一种抗体阳性表达进行术后药物治疗。 3.恶性肿瘤的Ki-67和P53常规检查 目前的研究表明,大部肿瘤的复发、转移取决于Ki-67值和P53值,而与肿瘤的组织的分型关系不是十分密切,如中分化腺癌,如果Ki-67和P53值超过50%,预后不佳,相反,如肿瘤的组织分型为低分化腺癌,而Ki-67和P53值较低,预后也会较中分化或高分化癌的预后稍好。 4.GIST(胃肠道间质瘤)和EGIST(胃肠道外间质瘤)的诊断 GIST是90年代新发现的肿瘤,过去均诊断为平滑肌瘤或平滑肌肉瘤,现在经过一组免疫组化可将其诊断,GIST的生物学形为一般无良性,因为小于2cm的GIST偶而也有转移。其良恶性程度取决于肿瘤的大小和核分裂像,国际确定GIST侵袭行为危险性的推荐方案如下: 危险程度大小核分裂数
免疫组织化学(傅琦博)-免疫组织化学
免疫组织化学 傅琦博 引言 酶工程是生物工程的重要组成部分,近几十年来,随着研究手段的更新和技术水平的提高,产生了一门以研究酶在细胞内的存在及其动态,以阐明组织细胞的结构和功能为主要内容的科学——酶组织化学。酶组织化学是利用酶化学反应的产物可在光学显微镜或电子显微镜下被识别的特性,借以从形态学角度判定酶在组织细胞内的存在的部位的一门技术,其基础是组织化学。它具有将形态学、生物化学和生理学联系起来的特点,在生物学、生物化学、医学生物领域内日益发挥着重要的作用。研究组织细胞内特定酶分布的酶组织化学方法大致分为:(1)利用酶的活性反映的方法;(2)利用抗原抗体反应(免疫应答)证实酶的存在部位的方法。后者也被称之为免疫组织化学。 免疫组织化学概述 免疫组织化学简称免疫组化,是应用免疫学及组织化学原理,对组织切片或细胞标本中的某些化学成分,进行原位的定性、定位或定量的研究。这种技术称为免疫组织化学技术。免疫组化是利用抗体与抗原的结合具有高度特异性的特点,采用一直的抗体检测组织或细胞的抗原物质,以期确定组织或细胞是否存在未知抗原,并进行定性、定位或定量的研究。抗原与抗体结合形成的免疫复合物是无色的,故必须借助组织化学方法,将抗体抗原反应部位显示出来。它的主要研究方法是免疫组织染色法(简称免疫染色法),食用该方法检测细胞内物质,必须具备两个条件:①作为检测对象的物质须具有抗原性,能制作出与之相应的特异、高效价的抗体;②在免疫反应发生之前,目标物质要保持抗原性,同时还要保持在组织细胞内的稳定状态。要检测抗原,就要用与之相应的抗体进行免疫反应,同时要用可视的标记标出抗原或抗体,采用这种方法的免疫染色法称为标识抗体法或标识抗原法,常用的表示抗体法有直接法、间接法、补体结合法以及多重染色法等。直接法是标识要检出的抗原的抗体,然后进行反应的方法,其特异性高,但检出的敏感度不如间接法,标识抗体的食用范围手局限。间接法是以未标识的第一抗体进行反应,接着标识以第一抗体为抗原所制作的抗体(即第二抗体)进行重叠反应,间接的证明抗原,这种方法的缺点是容易出现非特异性反应,但敏感度较高,标识抗体的用途也广;补体结合法是将间接法中的第二抗体作为标识抗补体抗体食用;多重染色法则是在同一标本上检出多种抗原物质的方法,可以用反复进行的重复标记的直接法,也可以用酶标记的重复进行的间接法。此外,还有后标识抗体的免疫染色法,此法先采用未标识的抗体进行反应,反应结束后,通过免疫化学反应或其他化学反应,用适当的标记物质来识别已与组织细胞内抗原发生结合的抗体。 免疫组织化学技术的发展 免疫组织化学技术是形态学研究领域一门新兴方法学。自它问世以来发展迅猛,用“日新月异”一词形容它毫不过分。酶标免疫组织化学技术是由Nakane 等人于60 年代末期创立的最早的免疫酶组织化学技术,之后Sternberger 等人于70 年代初期便在此基础上建立了非标记抗体酶法(又称间接法) 和PAP 法(过氧化酶抗过氧化酶法) 。80 年代初期美籍华人Hsu 又建立了卵白素生物素复合物法(ABC法) ,自此之后,免疫金银染色法、免疫电镜等技术相继问世。80 年代末期人们又发现链霉菌抗生物素蛋白(或译成链霉菌亲合素,St reptavidin) 与生物素结合力极强,遂用它标记过氧化酶建立起了SP 法,或称LSAB 法(链霉菌亲合素生物素过氧化酶法) 。由于链霉菌亲合素不与人组织中的内源性生物素起非特异性结合反应,故背景染色更加清晰,且敏感性比ABC 法高4~8 倍,比PAP 法高8~16 倍。进入90 年代,免疫组织化学又向基因水平深入发展,与分子生物学技术的结合日益紧密。如原位杂交后信 号的放大与显示便是采用了免疫组织化学显色技术,因而又可称之为原位杂交免疫组织化学技术。而图象分析、流式细胞仪的运用,是免疫细胞化学定量分析技术提高到更精确的水平。现就该技术的发展及其应用作一概述。 1利用免疫荧光标记技术可以分辨出标记抗原抗体所在的位置及其性质, 并可利用荧光定量技术计算抗原(或抗体) 的含量, 以达到对定性、定位、定量测定的目的[2 ]。如黄祥瑞等人(1999) 利用免疫荧光细胞化学技术研究西藏环状病毒细胞生物学特性和敏感细胞范围(CPE) , 成功地观察到该病毒的细胞病变效应特异荧光发生的部位、细胞数量和病毒的形态发生。辛德毕斯热是由辛德毕斯病毒Sindbis V irus (SiN ) 引起的人兽共患虫媒病毒病, 1974 年南非发生辛德毕斯热大流行。1991年梁国栋等通
免疫组织化学技术在病理诊断中的应用题库2-0-8
免疫组织化学技术在病理诊断中的应用题 库2-0-8
问题: [单选,A2型题,A1A2型题]下列标记可用来鉴别上皮样淋巴瘤和上皮样肉瘤的是() A.CK B.calretinin C.LCA D.CgA E.CD68 CK为上皮性标志物;calretinin为间皮细胞肿瘤标志;CgA为神经内分泌标志物;CD68为组织细胞标志物。LCA为淋巴细胞标志物,因此可用来鉴别上皮样淋巴瘤和上皮样肉瘤。
问题: [单选,A2型题,A1A2型题]AFP为下列哪种肿瘤的标记物?() A.宫内膜癌 B.黑色素细胞瘤 C.肝细胞癌 D.乳腺癌 E.鼻咽癌 AFP为肝细胞癌和内胚窦瘤的标志物;HMB45和S-100为黑色素细胞的标志物;ER和PR为乳腺癌和子宫内膜癌的分化标志物。
问题: [单选,A2型题,A1A2型题]关于小圆细胞肿瘤的描述,下列错误的是() A.是一类细胞形态为小圆形的细胞 B.常规诊断基本可以明确诊断 C.免疫组化诊断胚胎性横纹肌肉瘤首选Desmin D.原始间叶性肿瘤诊断困难,可采取排除法 E.免疫组化诊断尤因肉瘤首选CD99 小圆细胞恶性肿瘤是病理学从镜下形态的分类,不能说明肿瘤的组织来源,需要免疫组化进一步诊断。 (吉林快3 https://www.360docs.net/doc/af10287442.html,)
问题: [单选,A2型题,A1A2型题]下列免疫组化结果有助于诊断皮肤Merkel瘤的是()。 A.Vimentin(+),CK(+),NSE(-) B.Vimentin(-),CK(-),NSE(+) C.Vimentin(-),CK(+),NSE(-) D.Vimentin(-),CK(+),NSE(+) E.Vimentin(+),CK(-),NSE(+) 皮肤Merkel瘤可同时表达CK、NSE,而Vimentin常呈阴性反应。
免疫组化技术总结(较好)
个人免疫组化感悟(Jane) 1、方法操作不难,最大的难处是出现异常结果时如何解决? 这就需要掌握免疫组化实验原理,每一步知道为什么这样做,这样你才敢大胆地改革先前的不对的方法步骤。如抗体孵育条件主要是抗体浓度、温度、时间,这三者一般是相互成反比的(相对),其中浓度是最重要的先决条件,温度决定反应的速度、时间决定反应的量。就拿温度来说,可以有4度、室温、37度,我推荐4度最佳,反应最温和,背景较浅;而37 度反应速度较快,时间较短;室温我不太提倡,除非你每次都把环境温度控制在一定的范围,否则,尽量选择前两者。 2、免疫组化最大的优势是定位和定性。 相比于其他蛋白检测方法,免疫组化具有定性灵敏度高、定位较直接准确,是定位检测分析首选方法。尤其对于有些因子的转位研究十分有用。 3、免疫组化结果定量分析的前提是高质量的染色切片。 免疫组化结果也能定量分析,但必须是背景染色浅而特异性染色较深的情况下,分析最为准确,这种原则可能也是我们日常审稿时判定研究结果的必备条件。 4、免疫组化实验一定要设置阳性对照和阴性对照。 阳性对照一般是用肯定表达这种抗原的切片来做;阴性对照一般是用PBS或非一抗替代一抗来进行反应,其余步骤均一致。前者是排除方法和实验系统有无问题;后者是排除有无一抗外的非特异性染色。 5、免疫组化的应用广泛,是当前实验研究的最重要方法之一。 如今发SCI论文时,明显感觉仅靠量化的数据来发文章很难,加一些形态学数据或图片,老外十分欢迎,可能是怕你学术造假吧。当然也不能做假阳性或假阴性结果。 6、免疫组化技术掌握与否的鉴定标准是同一切片或不同切片中不同抗原均从摸索浓度或条件而做出优良的染色切片。 我在平时带教中就发现许多研究生把我已经摸索很成熟的反应条件、浓度、方法步骤,重复运用于同一性质的切片和同一种抗体,做出来后就觉得自己已经掌握了免疫组化方法,更换一种抗体后,居然连二抗的种属来源都拿错了。 失败往往促进你去思考试验原理和过程,成功有时也加快你自傲。 7、实验方法需要动手+动脑。 如今我还不敢说我在免疫组化什么都知道。我只所以今天敢在这里说这说那,这是因为我经过
免疫组化的在病理中的临床意义
1 3、意义:标记物--作用--阳性部位--临床意义 耐药性越强:阿霉素、柔红霉素、表阿霉素、米托蒽醌、长春花碱、长春新碱、紫彬醇、泰素帝。 性越强:阿霉素、顺铂、氮芥、环磷酰胺、瘤可宁。 蒽环类抗生素和鬼臼毒素类,如VP16、替尼泊苷、玫瑰树碱、新霉素、柔红霉素、表阿霉素、阿霉素、VM26。阳性率高者对VP16尤其有效。 预后越好。 预后越好。 C-erbB-2--癌基因产物--胞浆--阳性率越高,肿瘤恶性程度越高。ER、PE阳性而C-erbB-2也阳性者,用三苯氧胺治疗效果不好。 Ki-67为细胞增值的一种标记,在细胞周期G1、S、G2、M期均有表达,G0期缺如,其和许多肿瘤分化程度、浸润、转移、预后密切相关。PCNA(增埴细
胞核抗原)。 P53在免疫组化中均为突变型,阳性率越高,预后约差。野生型半衰期很短 于乳腺癌、非小细胞肺癌、胃癌、大肠癌、肝癌、喉癌等多种恶性肿瘤的检测。几乎所有的研究都表明,nm23蛋白高表达患者淋巴结转移率相对较低,存活期相对较长。 胞之间连接的破坏,主要用于肿瘤侵袭和转移方面的研究。 判断的指标之一。 CK18,低分子量角蛋白,主要标记各种单层上皮包括腺上皮,而复层鳞状上皮常阴性,主要用于腺癌诊断。 阳性反应 弱阳性或阴性。 乳腺癌、肺癌、子宫内膜和卵巢非黏液性肿瘤常阴性。
道上皮细胞、胰腺和胆管上皮细胞以及肾实质的上皮细胞中(特别是近曲小管)。Villin在胃肠道癌、胰腺癌、胆囊癌和胆管癌组织中有很高的表达率,具有明显腺样结构的肿瘤上没有villin表达,则这个肿瘤为胃肠道、胰腺、胆囊或胆管来源的可能性极低。 乳腺癌也经常成为女性患者未知原发部位转移癌要鉴别排除的一种疾病。因为在转移癌组织上观察到明显的villin免疫组化阳性染色,则这个肿瘤就极不可能为乳腺来源。其他villin免疫组化染色通常为阴性表达的肿瘤还有:如卵巢浆液性癌、尿道移行细胞癌和前列腺癌。间皮瘤也经常为villin阴性表达,因此在一些情况下Villin还可以作为鉴别间皮瘤和腺癌使用抗体的一种。 但是也有一些非胃肠道来源的肿瘤可表达villin,如子宫内膜样腺癌、卵巢粘液性癌、肾细胞癌和小部分肺癌。也有一些专家报道Villin在部分宫颈内膜腺癌病例中表达。 肝癌的诊断:Villin免疫组化染色可以显示出毛细胆管结构,因此它也可能在表达部分肝癌的管状结构上很有用。多克隆CEA是用于此目的的第一种试剂,而且CD10 (CALLA)在表达肝癌的该结构上也非常有用。多克隆CEA、villin和CD10 (CALLA)在肝癌病例上的表达,相互之间并没有任何的冲突,因此如果怀疑肝癌的可能性,建议将这三种抗体共同使用以协助疑难病例的诊断。Villin在神经内分泌肿瘤上的应用:Villin在神经内分泌肿瘤的研究上也很有帮助。众所周知,类癌和胰腺的胰岛细胞肿瘤具有相相似的形态学特征,仅在形态学上区分这两种肿瘤几乎是不可能的。Villin在这种情况下特别有用,因为据文献报道在85%的胃肠道类癌病例中有villin的表达,但在胰岛细胞肿瘤上
免疫组织化学及其应用
免疫组织化学及其应用 浙江大学病理学与法医学研究所 周韧 1.免疫组织化学的历史、现状和发展 1.1.历史 ●人类的历史有多长,医学的历史也就有多长.医学的任何一个进步都是建立在当 时科学与技术发展的相应水平上的. ●医学的目的: 解除人体的病痛 ●核心: 诊断和治疗。 任何疾病的有效治疗均来源于正确的诊断。●疾病的诊断手段准确性,首推病理诊断准确性高,即病理组织学诊断。更准确、 更可信、更有权威性。 ●免疫组织化学(以下简称免疫组化)已成为病理诊断中的一种常用手段。 病理诊断发展过程的主要事件 年代作者事件 1632年 Severino 肿瘤切开后观察的书 1661年 Malpighi 放大镜观察后的报告 1761年 Morgagni 肿瘤与外科方面的书 1829年 Horner 首篇病理论文 1832年Hodgkin 报告7例尸检结果的论文 1858年Virchow 发表《细胞病理学》 1863年 Paget 发表《外科病理学》 1897年 Mallory和Wright 发表组织学技术的书 1914年 Mallory 发表《细胞组织学原则》 1919年 Ewing 发表《肿瘤病》 1924年 McFarland 发表《外科病理学》 1926年 Karsner 发表《人体病理学》 1928年 Papanicolaou 发表细胞学方面的书 1951年电镜应用于病理诊断 1974年免疫组化用于病理诊断 ●诊断病理学开始于19世纪 ●20世纪的第二个25年中达到光学显微镜诊断的辉煌。随之而起的电子显微镜 ●20世纪第三个25年中成为诊断病理的发展高峰。
●进入20世纪最后25年,取而代之的便是免疫组化了。 1.2.免疫组织化学的发展 1.2.1.免疫学的发展 1.2.2.单克隆技术的出现 ●病理诊断的确立:是找到“特征性”形态表现。 常规苏木素伊红(HE)染色 几百种的“特殊染色” ●免疫组织化学产生: 抗原抗体结合原理 ●从组织细胞水平进行抗原抗体反应,于是就了免疫组织化学技术。 主要的发展过程 年代研究者事件 1941年 Coons 实用免疫荧光技术 1948年 Fagraeus 进一步发展免疫荧光技术 1970年 Sternberger 抗体酶标记技术 1974年 Taylor 证实组织中的浆细胞免疫 1975年 Kohler和Milstein 单克隆抗体技术 1981年 Hsu ABC法 90年代以来 SP法,原位杂交及原位PCR免 疫组化法
免疫组化在血液肿瘤病理诊断中地应用及意义(一)
免疫组化在血液肿瘤病理诊断中的应用及意义(一) IHC方法相对简单,但从取材到发报告之间环节较多,任何环节的疏忽都可能造成检测结果偏差,甚至导致漏诊、误诊。除IHC染色常规注意事项外,血液肿瘤标本的检测还有其特殊性。 1.标本的前期处理 血液系统疾病病理诊断标本,主要是淋巴结、脾脏和骨髓组织。与其它组织相似,造血细胞表面抗原不同其稳定性会有差异,从而对固定剂的耐受性不同。组织固定的原则,是采用10%中性福尔马林作为固定剂,固定时间最好不超过24小时。 (1)淋巴结:取材后迅速固定,待组织表面变硬即可修块。以淋巴结大小为直径,厚度不超过3mm,以使组织得到充分的固定。如淋巴结中有淤血、坏死成分,应尽量除去。组织制片中的每个步骤都应严格掌握,以免破坏组织的抗原活性。(2)脾脏:脾脏组织较大,应注意多点取材;脾脏又是贮血器官,含血量多,取材时应尽量除去积血;取材大小以2×2×7.5px 为宜,取材后尽快固定。在多块标本中,病理医师应根据HE切片,挑出病变明显的1~2 块作IHC 染色。(3)骨髓组织:特点为组织小,主要为骨质,造血细胞充斥于骨小梁之间。在组织制片的每个步骤都应相应缩短时间。骨髓组织制片需要脱钙,酸性脱钙液对抗原活性有影
响,常规采用的2%硝酸,脱钙不应超过3小时。EDTA脱钙液偏碱性,比较温和,效果较好,只是时间长,约需24~48小时。(4)骨髓涂片:某些情况下当骨髓组织取材不好,如太小或组织为骨皮质、血凝块等不能进行石蜡包埋制片时,可用骨髓涂片代替。但注意骨髓涂片不能太厚,最好不混血。涂片稍干后用甲醇:丙酮(1:1)固定90秒后染色。涂片不能在室温下久存。(5)外周血涂片:某些特殊情况不能采用穿刺骨髓取材时,可用外周血涂片代替。前提是外周血有核细胞总数必须较多,结果才相对可靠,固定同骨髓涂片。(6)组织印片:当疾病诊断和分型必需的标记物不能用于石蜡切片时,可用组织印片来补救。将新鲜软组织取材后,按取材大小平放于干净的载玻片上,轻压,然后垂直取下标本,组织表面的细胞即印在玻片上,风干,固定同骨髓涂片。组织印片与冰冻切片相似,由于形态不好,除特殊情况外,临床上尽量不用。 2.IHC所采用的检测系统IHC染色方法很多,如免疫荧光、免疫酶标、免疫金标。免疫酶标是以酶标记的抗体与组织或细胞作用后,加入酶的底物生成有色产物,通过光镜对细胞表面或细胞内抗原进行定位。免疫酶标以其标记酶不同又分为标记过氧化物酶(HRP)法,如ABC、SP及相应二步法;标记碱性磷酸酶(AP)法,如SAP及相应的二步法。葡萄糖氧化酶(GOD)分子量较大,具有较多的氨基酸,在标记时易形成广泛的聚合,影响酶活
石蜡切片病理、免疫组化及免疫荧光方案
石蜡切片病理、免疫组化及免疫荧光方案 石蜡标本固定、脱水、包埋方法 大鼠自心脏灌注4%多聚甲醛内固定1-2h后取材:取脑出血血肿处脑组织(厚度约3mm),置于塑料盒中并浸泡在4%多聚甲醛中固定,室温中固定时间12-48h,固定好的组织脱水前应流水冲洗30min-1h左右除去固定液,取固定好的脑组织标本脱水、包埋。具体步骤按以下方法进行:此方法参考《组织病理学技术》周庚寅北京大学出版社 2006年 ?70%: 1h-2h ?80%: 1h-2h ?90%: 1h-2h ?95%: 1h-2h ?95%: 1h-2h ?无水Ⅰ:30min-60min ?无水Ⅱ:30min-60min ?二甲苯及水水酒精 1:1混合液 30min ?二甲苯Ⅰ:30min ?二甲苯Ⅱ:30min ?石蜡Ⅰ: 1h ?石蜡Ⅱ: 1h ?石蜡Ⅲ: 1h 包埋:在病理科包埋方法基础上灵活改进:在包埋铁模具上进行,融蜡-放置组织于中央-扣包埋盒4℃冷却10min-撬蜡。 注意事项: 1、固定液的种类:10%中性甲醛,4%的多聚甲醛最合适,在37°或室温中固定12-48h能很 好保存抗原和抗体的反应能力,实验室用的更多的是在4℃冰箱中固定24h-3d。有人建议中性甲醛40摄氏度固定2~3小时,流水冲洗20min-30min,这样可以缩短制片的时间。 2、熔蜡温度65 ℃左右; 3、严格按照预定实验步骤进行,保证脱水及透明完全,透明后见云雾状说明脱水不完全, 需退回无水酒精中返工。 4、经一级二甲苯透明后检查组织是否透明,二级二甲苯透明时间以具体时间而定。 5、注意及时更换梯度酒精及二甲苯(1月)。 组织石蜡切片摘自《免疫组织化学实验技术及应用》 P12 化学工业出版社2006 1.载玻片的处理:采用现成的APES处理过的硅化载玻片。 2.石蜡切片注意事项:1、用于免疫组化的蜡温应为56~58℃,切片水温为 40℃左右,应先置于冷水中(冷水中可参入酒精有利快速展片-见相关方 法),然后再移入热水中,这样可以使切片顺利展平;2、烤片时要注意:一般在62℃烤片30-60min,抗原较强的组织可在60摄氏度烤3~8h,抗 原较弱的组织可于37℃的恒温箱内过夜;3、切片如需长期保存,可置 于4℃或室温下,千万不可脱蜡后4℃保存,因脱蜡后失去了对抗原决定 族的保护。
免疫组织化学
免疫组织化学得基本知识 1免疫组织化学得概念: 免疫组化就是利用抗原与抗体特异性结合得原理,通过化学反应使标记抗体得显色剂 (荧光素、酶、金属离子、同位素) 显色来确定组织细胞内抗原(多肽与蛋白质),对其进行定位、定性及定量得研究,称为免疫组织化学、 2免疫组化实验所用得抗体有哪些??免疫组化实验中常用得抗体为单克隆抗体与多克隆抗体、单克隆抗体就是一个B淋巴细胞克隆分泌得抗体,应用细胞融合杂交瘤技术免疫动物制备、多克隆抗体就是将纯化后得抗原直接免疫动物后,从动物血中所获得得免疫血清,就是多个B淋巴细胞克隆所产生得抗体混合物、?3免疫组化实验所用得组织与细胞标本有哪些? 实验所用主要为组织标本与细胞标本两大类,组织标本包括石蜡切片(病理大片与组织芯片)与冰冻切片,细胞标本包括组织印片、细胞爬片与细胞涂片、其中石蜡切片就是制作组织标本最常用、最基本得方法,对于组织形态保存好,且能作连续切片,有利于各种染色对照观察;还能长期存档,供回顾性研究;石蜡切片制作过程对组织内抗原暴露有一定得影响,但可进行抗原修复,就是免疫组化中首选得组织标本制作方法。?4石蜡切片为什么要做抗原修复?有哪些方法? 石蜡切片标本均用甲醛固定,使得细胞内抗原形成醛键、羧甲键而被封闭了部分抗原决定簇,同时蛋白之间发生交联而使抗原决定簇隐蔽。所以要求在进行IHC染色时,需要先进行抗原修复或暴露,即将固定时分子之间所形成得交联破坏,而恢复抗原得原有空间形态。?常用得抗原修复方法有微波修复法,高压加热法,酶消化法,水煮加热法等,常用得修复液就是pH6、0得0、01 mol/L得柠檬酸盐缓冲液、 5免疫组化常用得染色方法有哪些??根据标记物得不同分为免疫荧光法,免疫酶标法,亲与组织化学法,后者就是以一种物质对某种组织成分具有高度亲合力为基础得检测方法。这种方法敏感性更高,有利于微量抗原(抗体)在细胞或亚细胞水平得定位,其中生物素——抗生物素染色法最常用。 6抗体交叉反应得原因: 指抗体除与其相应得抗原发生特异性反应外还与其它抗原发生反应、产生得原因有以下几个方面:
