初三化学酸碱盐归纳总结

初中化学酸碱盐归纳总结
一、酸和碱
1.盐酸、硫酸属于酸,酸在水溶液中能解离出H+和酸根离子。 酸→H ++酸根离子
2.氢氧化钠、氢氧化钙属于碱,碱在水中能解离出金属离子和OHˉ。 碱→金属离子+O Hˉ
3.
二、酸
(1)与酸碱指示剂的反应: 使紫色石蕊试液变红色,不能使无色酚酞试液变色 (2)酸能使多种活泼金属反应,生成盐和氢气。即金属 + 酸 → 盐 + 氢气
F e+2H Cl=F eCl 2+H 2↑ Zn+H 2SO 4=Zn SO 4+H 2↑
2Al+6H Cl =2A lCl 3+3H 2↑ 2Al+3H 2S O4=A l2(S O4)3+3H2↑
(3)酸能使某些金属氧化物反应,生成盐和水。即碱性氧化物 + 酸 → 盐 + 水 铁锈+盐酸:Fe 2O 3+6H Cl====2Fe Cl 3+3H 2O(黄色溶液); 铁锈+硫酸Fe2O 3+3H 2SO 4====F e2(SO 4)3+3H 2O
(4)碱能与某些非金属氧化物反应,生成盐和水。即碱 + 酸 → 盐 + 水
Na OH +CO 2=Na 2C O
3+H 2O C a(OH)2+ CO 2=CaC O3↓+H2O +CO 2↑ (5)盐 + 酸 → 另一种盐 + 另一种酸(产物符合复分解条件)
HCl + AgNO 3=A gCl ↓+H NO 3 H 2SO 4+BaCl 2=BaSO 4↓+H Cl
CaCO 3 + 2HCl = CaCl 2 + H 2O + CO2↑ 三、碱
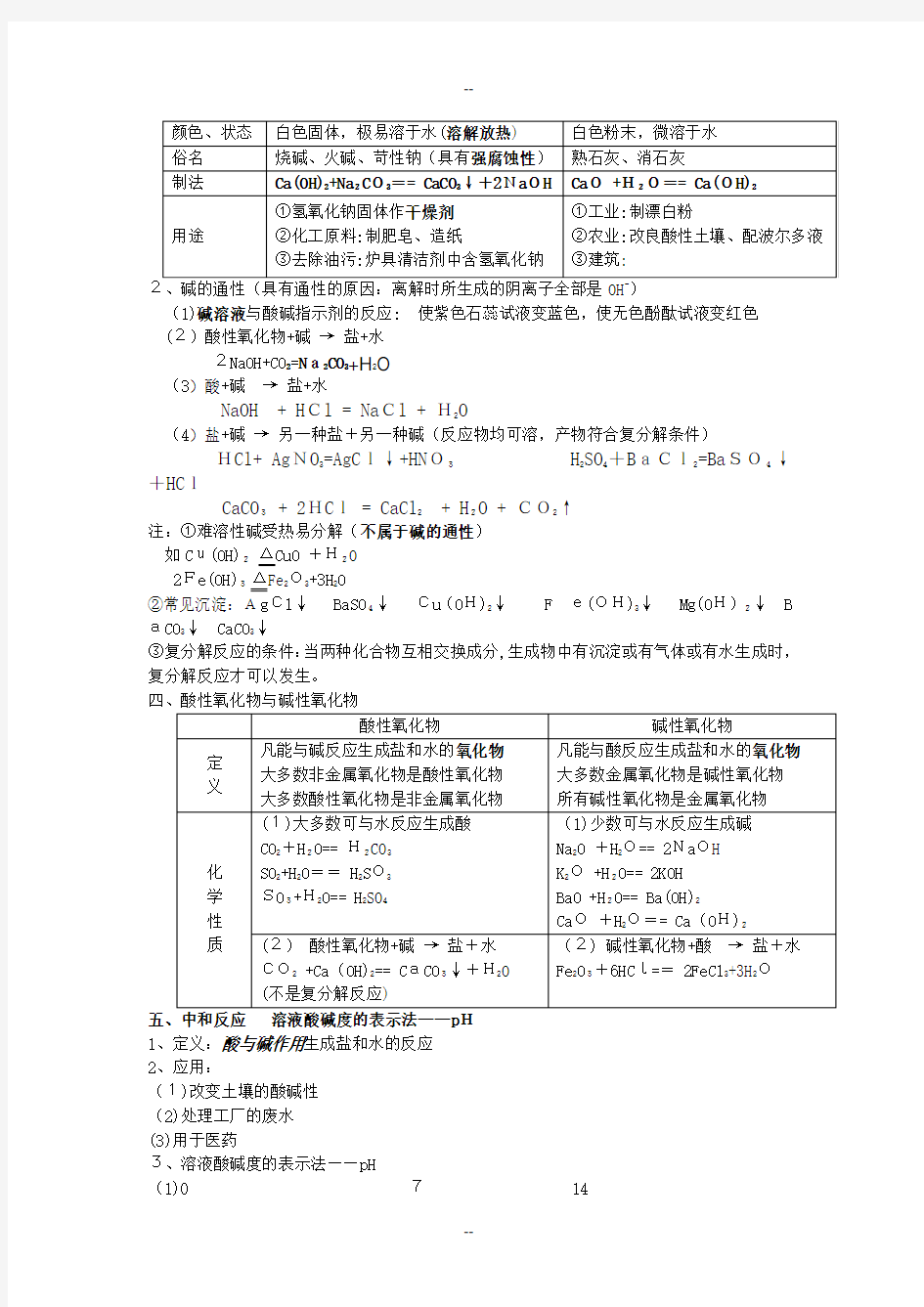
1
2、碱的通性(具有通性的原因:离解时所生成的阴离子全部是OH)
(1)碱溶液与酸碱指示剂的反应: 使紫色石蕊试液变蓝色,使无色酚酞试液变红色(2)酸性氧化物+碱→盐+水
2NaOH+CO2=Na2CO3+H2O
(3)酸+碱→盐+水
NaOH + HCl = NaCl + H
2
O
(4)盐+碱→另一种盐+另一种碱(反应物均可溶,产物符合复分解条件)
HCl+ AgNO
3=AgCl↓+HNO
3
H
2
SO
4
+BaCl
2
=BaSO
4
↓
+HCl
CaCO
3 + 2HCl = CaCl
2
+ H
2
O + CO
2
↑
注:①难溶性碱受热易分解(不属于碱的通性)
如Cu(OH)2ΔCuO +H2O
2Fe(OH)3ΔFe2O3+3H2O
②常见沉淀:AgCl↓BaSO4↓Cu(OH)2↓ F e(OH)3↓Mg(OH)2↓ B aCO3↓ CaCO3↓
③复分解反应的条件:当两种化合物互相交换成分,生成物中有沉淀或有气体或有水生成时,复分解反应才可以发生。
五、中和反应溶液酸碱度的表示法——pH
1、定义:酸与碱作用生成盐和水的反应
2、应用:
(1)改变土壤的酸碱性
(2)处理工厂的废水
(3)用于医药
3、溶液酸碱度的表示法——pH
(1)0 714
(2)pH的测定:最简单的方法是使用pH试纸
用玻璃棒(或滴管)蘸取待测试液少许,滴在pH试纸上,显色后与标准比色卡对照,读出溶液的pH(读数为整数)
(3)酸雨:正常雨水的pH约为5.6(因为溶有CO2)pH<5.6的雨水为酸雨
电离时阳离子唯一是H+的叫酸。
3.电离时阳离子唯一是OHˉ的叫碱。
常见的酸和碱
一、酸碱指示剂
1.酸碱指示剂(简称:指示剂)能跟酸或碱的溶液起作用而显示不同的颜色。常见的有:石蕊溶液、酚酞溶液。
2.变色规律:
3.二氧化碳通入紫色的石蕊试液中,(1)溶液由紫色变成红色。(2)二氧化碳溶于水生成了碳酸,是碳酸改变了溶液的颜色。
4.用酸碱指示剂检验溶液的酸碱性的方法:(1)取少量该溶液,滴入几滴石蕊试液,若溶液呈现红色,则说明该溶液为酸性溶液。(2)取少量该溶液,滴入几滴石蕊试液,若溶液呈现蓝色;或者滴入几滴无色的酚酞试液,若溶液呈现红色,则说明该溶液为碱性溶液。
二、几种常见的酸
1.盐酸是HCl的水溶液。纯净的浓盐酸是无色。盐酸具有挥发性,浓盐酸在空气里会形成白雾,这是因为从浓盐酸里挥发出来的氯化氢气体跟空气里的水蒸气接触,形成盐酸小液滴的缘故。(强调闻气味的方法。)
2.用途:盐酸(HCl)重要化工产品。用于金属表面除锈、制造药物(如盐酸麻黄素、氯化锌)等;人体胃液中含有盐酸,可帮助消化。硫酸(H2SO4)重要化工原料。用于生化肥、农药、火药、染料以及冶炼金属、精炼石油和金属除锈等浓硫酸有吸水性,在实验室中常用它作干燥剂
3.浓硫酸:无色液体无味;(1)有吸水性,在实验室中常用它作干燥剂。(2)浓硫酸具有强腐蚀性,使用时必须十分小心。它能夺取纸张、木材、布料、皮肤(都由含碳、氢、氧等元素的化合物组成)里的水分,生成黑色的炭。(3)稀释浓硫酸的正确操作:将浓硫酸沿着烧杯壁缓慢地注入盛有水的烧杯里,用玻璃棒不断搅动。
(4)如果不慎将浓硫酸沾到皮肤或衣服上,应立即用大量水冲洗,然后涂上3%~5%的碳酸氢钠溶液。
4.酸有一些相似的化学性质
(1)能使酸碱指示剂显示不同的颜色
酸溶液使使紫色的石蕊试液变红色,可使无色的酚酞试液不变色;(2)能与多种活泼金属反应,生成氢气。(注意:实验室制取氢气不使用硝酸)
(3)能与某些金属氧化物反应,生成水。
铁锈+盐酸:(黄色溶液);
铁锈+硫酸:
(4)酸与碱反应(写化学方程式)
⑴盐酸中和氢氧化钠:(中和反应)
如图所示,在烧杯中加入10 mL氢氧化钠溶液,滴入几滴酚酞溶液。再用滴管慢慢滴入稀盐酸,并不断搅拌溶液,至溶液颜色恰好变成无色为止。
①.中和反应:酸与碱作用生成盐和水的反应。
②.盐:在水溶液中能解离出金属离子和酸根离子的化合物。
③.改变土壤的酸碱性
根据土壤情况,可以利用中和反应,在土壤中加入酸性或碱性物质,以调节土壤的酸碱性,利于植物生长。于是人们将适量的熟石灰加入土壤,以中和酸性。
④.处理工厂的废水:工厂生产过程中的污水,需进行一系列的处理。例如,硫酸厂的污水中含有硫酸等杂质,可以用熟石灰进行中和处理。
⑤.用于医药:人的胃液里含有适量盐酸,可以帮助消化,但是如果饮食过量时,胃会分泌出大量胃酸,反而造成消化不良。在这情况下,
可以遵医嘱服用某些含有碱性物质的药物,以中和过多的胃酸。
⑵氢氧化铜和硫酸:
(5)酸与盐反应
如何区别物质里含碳酸根离子和碳酸氢根离子?
取少量未知物,加入少量稀盐酸,看能否生成使澄清石灰水变浑浊的气体。加热或使用澄清石灰水。加热时,碳酸氢钠分解为碳酸钠、水和二氧化碳气体。使用澄清石灰水时,碳酸钠与氢氧化钙发生化学反应,生成一种难溶物。(此方程式为制备氢氧化钠反应原理)
三、几种常见的碱
1.潮解:氢氧化钠暴露在空气中时容易吸收水分,表面潮湿并逐渐溶解,这种现象叫做潮解。溶解时放热。
2.氢氧化钠用途:可用作气体的干燥剂。
(1).氢氧化钠有强烈的腐蚀性,俗名叫做苛性钠、火碱、烧碱。使用时要十分小心。
(2).若不慎将碱液沾到皮肤上,要用较多的水冲洗,再涂上硼酸溶液。氢氧化钠的用途:是一种重要的化工原料,广泛用于肥皂、石油、造纸、纺织和印染等工业。氢氧化钠能与油脂反应,在生活中可用来去除油污,如炉具清洁剂中就含有氢氧化钠。
3.生石灰与水发生化学反应:
反应放出大量的热,这些热量可以将鸡蛋煮熟4.氢氧化钙俗称熟石灰或消石灰,对皮肤、衣服等也有腐蚀作用,使用时应注意安全。
[总结]1.碱有腐蚀性,使用时应十分小心。
5.可作为干燥剂的有:浓硫酸、氢氧化钠。
6.检验二氧化碳的反应,写出化学方程
式:氢氧化钙能与空气中的二氧化碳反应,生成坚硬的碳酸钙。将氢氧化钙、粘土和沙子混合,用来作建筑材料,就是利用氢氧化钙的这一性质。②氢氧化钠在空气中不仅吸收水分潮解(物理变化),同时还会发生下列反应:
(化学变化)。所以,氢氧化钠必须密封保存。这两个反应都是非金属氧化物与碱的反应,都生成水.氢氧化钠与二氧化硫
反应的化学方程式:(化学名称:亚硫酸钠) 7.碱有一些相似的化学性质:
(1)碱能使酸碱指示剂显示不同的颜色。(2)碱能与某些非金属氧化物反应,生成水
8.溶液的导电性
蒸馏水和乙醇溶液、蔗糖溶液不导电,而盐酸、硫酸、硝酸、氢氧化钠溶液、氢氧化钙溶液、氯化钠溶液均能导电。
9.金属能导电的原因是:金属中存在着能自由移动的电子,电子带负电,在电场的作用下,电子定向运动产生电流。
10.盐酸、硫酸、硝酸在水溶液中都解离出H+和酸根离子,即在不同的酸溶液中都含有相同的H+,所以酸有一些相似的性质。我们把在水溶液中能解离出唯一的阳离子(H+)的化合物叫做酸。
11.氢氧化钠、氢氧化钙这些碱,在水溶液中都能解离出金属离子和O H-,即在不同的碱溶液中都含有相同的OH-,所以碱具有一些相似的性质。我们把在水溶液中能电离出唯一的阴离子(OH-)的化合物叫做碱。
四、溶液的酸碱度表示法——pH
1.溶液的酸碱度常用pH来表示,pH范围通常在0~14之间。pH<7 溶液呈酸性;pH>7溶液呈碱性;pH=7溶液呈中性
2.测定pH最简便的方法是:使用pH试纸。(我们测得值一般为整数) 测定方法:在白瓷板或玻璃片上放一小片pH试纸,将被测液滴到试纸上,把试纸显示的颜色与标准比色卡比较,即可得出被测液的pH。3.pH应用
(1).化工生产中许多反应必须在一定pH溶液里才能进行。(2).在农业生产中,农作物一般适宜在pH为7或接近7的土壤中生长(3).测定雨水的pH(因溶解有二氧化碳,正常雨水的pH约为5.6,酸雨的pH小于5.6),可以了解空气的污染情况。
(4).测定人体内或排出的液体的pH,可以了解人体的健康状况
五、盐的性质及及用途
1.氯化钠、NaCl、俗名为食盐。盐是一类物质的总称,食盐属于这类物质中的一种。
2.食盐的用途
(1).食盐是一种重要的调味品。
(2).医疗上用氯化钠配制生理盐水。0.9%
(3).农业上可以用氯化钠溶液来选种。
(4).食盐可以用来腌渍蔬菜、鱼、肉、蛋等,腌制成各种风味独特的食品。
(5).公路上的积雪也可以用氯化钠来消除。
3.粗盐提纯
(1)粗盐中含有较多的可溶性杂质(氯化镁、氯化钙)和不溶性杂质(泥沙等)。
(2)粗盐提纯:溶解、过滤、蒸发、计算产率。
(3)过滤应注意:①叠好的滤纸放入漏斗后,应紧贴漏斗壁,中间不要有气泡。否则过滤速度过慢。②滤纸的边缘要比漏斗口稍低;倾倒液体时,使液体沿着玻璃棒流下,液面要低于滤纸的边缘。③盛有待过滤液的烧杯口紧靠玻璃棒中部;玻璃棒下端紧靠三层滤纸一边,防止滤纸破损,滤液浑浊,漏斗下端紧靠烧杯内壁,防止液滴飞溅。④过滤时最好先让上层滤液滤过,然后再将混有大量沉淀的溶液倒入漏斗,以免沉淀先行进入漏斗后可能堵塞滤纸纤维的间隙,使过滤速度过慢。
(4)一种新的操作——蒸发,在蒸发时应注意什么问题呢?
蒸发一般是用加热的方法,使溶剂不断挥发的过程。蒸发时应注意:①蒸发皿应放在铁圈上,用酒精灯加热。停止加热后,不要立即把蒸发
皿直接放在实验台上,以免烫坏实验台。
②蒸发溶液时要注意倒入蒸发皿里的溶液以不超过蒸发皿容积的2/3为宜,防止加热至沸腾时易进溅。
③在加热过程中,用玻璃棒不断搅动,防止由于局部温度过高,造成液滴飞溅。
④当蒸发皿中出现较多量的固体时,即停止加热。
⑤在溶解、过滤、蒸发操作中都用到了玻璃棒,分别起什么作用?
溶解:玻璃棒起搅拌作用,目的是加速溶解。过滤:玻璃棒起引流作用。蒸发:玻璃棒起搅拌作用,防止局部受热时液滴飞溅。
(5)实验探究:粗盐的初步提纯
①.溶解②.过滤
仔细观察滤纸上剩余物及滤液的颜色,如滤液仍浑浊,应再过滤一次。如果两次过滤后滤液仍浑浊,应如何检查实验装置并找出原因?
过滤后滤液浑浊的原因:a过滤时滤纸破损。b倾倒液体时,液面超过滤纸边缘。③.蒸发把所得澄清滤液倒入蒸发皿。把蒸发皿放在铁架台的铁圈上,用酒精灯加热,同时用玻璃棒不断搅拌。待蒸发皿中出现较多固体时,停止加热。利用蒸发皿的余热使滤液蒸干。
④.计算产率
用玻璃棒把固体转移到纸上,称量后,回收到教师指定的容器中。将提纯后的氯化钠与粗盐作比较,并计算精盐的产率。
4.实验过程中可能出现的误差:
(1)溶解搅拌时液滴溅出,产率降低.
