2020高考化学第二轮复习 实验专题1 常见仪器 精品

2020高考化学实验专题1:常见仪器
1.下列仪器不允许用酒精灯加热的是
A.表面皿
B.蒸馏烧瓶
C.蒸发皿
D.坩埚
2.下列仪器:①集气瓶;②量筒;③烧杯;④表面皿;⑤蒸发皿;⑥容量瓶;⑦烧瓶,能用酒精灯加热的是
A.②③⑤
B.③⑥⑦
C.①③④
D.③⑤⑦
3.下列盛放物质的方法,错误的是
A.把汽油放在带橡皮塞的玻璃瓶中
B.把硝酸银溶液放在棕色玻璃瓶中
C.把氢氧化钠溶液放在带橡皮塞的玻璃瓶中
D.把氢氟酸放在玻璃瓶中
4.准确量取2
5.00毫升高锰酸钾溶液,可选用的仪器是
A.50毫升量筒
B.10毫升量筒
C.50毫升酸式滴定管
D.50毫升碱式滴定管
5.下列叙述仪器“0”刻度位置正确的是
A.在量筒的上端
B.在滴定管上端
C.在托盘天平刻度尺的正中
D.在托盘天平刻皮尺的右边
6.下列盛放试剂的方法正确的是
A.氢氟酸或浓硝酸存放在带橡皮塞的棕色玻璃瓶中
B.汽油或煤油存放在带橡皮塞的棕色玻璃瓶中
C.碳酸钠溶液或氢氧化钙溶液存放在配有磨口塞的棕色玻璃瓶中
D.氯水或硝酸银溶液存放在配有磨口塞的棕色玻璃瓶中
7.下列实验中用错试剂的是
A.用稀盐酸清洗做焰色反应的镍铬丝
B.用酒精萃取碘水中的碘
C.用稀硝酸洗去残留在试管壁上的铜
D.用碱石灰吸收氨气中的水蒸气
8.下列盛放试剂的方法正确的是
A.氯氟酸或浓硝酸存放在带橡皮塞的棕色玻璃瓶中
B.汽油或煤油存放在带橡皮塞的棕色玻璃瓶中
C.碳酸钠溶液或氢氧化钙溶液存放在配有磨口塞的棕色玻璃瓶中
D.氯水或硝酸银溶液存放在配有磨口塞的棕色玻璃瓶中
9.在实验室中进行下列实验,括号内的实验用品都能用到的是
A.硫酸铜晶体里结晶水含量的测定(坩埚、温度计、硫酸铜晶体)
B.蛋白质的盐析(试管、醋酸铅溶液、鸡蛋白溶液)
C.钠的焰色反应(铂丝、氯化钠溶液、稀盐酸)
D.肥皂的制取(蒸发皿、玻璃棒、甘油)
10.下列仪器:①漏斗②容量瓶③蒸馏烧瓶④天平⑤分液漏斗⑥滴定管⑦燃烧匙。常用于物质分离的是
A.①③④
B.①②⑥
C.①③⑤
D.③④⑦
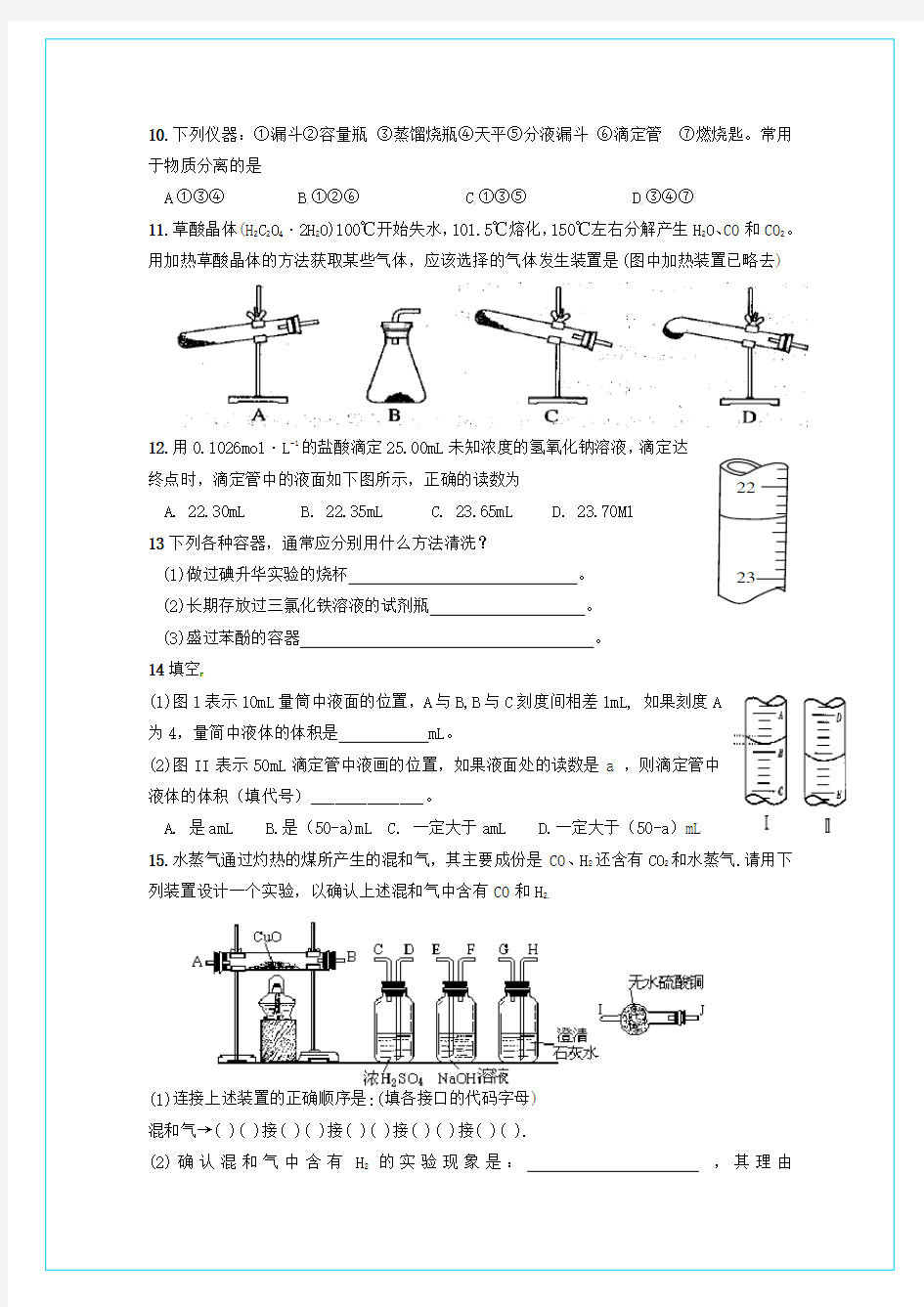
11.草酸晶体(H2C2O4·2H2O)100℃开始失水,101.5℃熔化,150℃左右分解产生H2O、CO和CO2。用加热草酸晶体的方法获取某些气体,应该选择的气体发生装置是(图中加热装置已略去)
12.用0.1026mol·L-1的盐酸滴定25.00mL未知浓度的氢氧化钠溶液,滴定达
终点时,滴定管中的液面如下图所示,正确的读数为
A. 22.30mL
B. 22.35mL
C. 23.65mL
D. 23.70Ml
13下列各种容器,通常应分别用什么方法清洗?
(1)做过碘升华实验的烧杯。
(2)长期存放过三氯化铁溶液的试剂瓶。
(3)盛过苯酚的容器。
14填空
(1)图1表示10mL量筒中液面的位置,A与B,B与C刻度间相差1mL, 如果刻度A
为4,量简中液体的体积是 mL。
(2)图II表示50mL滴定管中液画的位置,如果液面处的读数是a ,则滴定管中
液体的体积(填代号)______________。
A. 是amL
B.是(50-a)mL
C. 一定大于amL
D.一定大于(50-a)mL
15.水蒸气通过灼热的煤所产生的混和气,其主要成份是CO、H2还含有CO2和水蒸气.请用下列装置设计一个实验,以确认上述混和气中含有CO和H2.
(1)连接上述装置的正确顺序是:(填各接口的代码字母)
混和气→( )( )接( )( )接( )( )接( )( )接( )( ).
(2)确认混和气中含有H2的实验现象是:,其理由
22
23
是: .
16.某化学课外小组所做实验的示意图如下:
上图中“→”表示气体流向,M 是一种纯净而干燥的气体,Y 为另一种气体,E 内有棕色气体产生。实验所用的物质,只能由下列物质中选取:
Na 2CO 3、Na 2O 2、NaCl 、Na 2O 、CaCl 2、(NH 4)2CO 3、碱石灰等固体及蒸馏水。据此实验,完成下列填空:
(1) A 中所用装置的主要仪器有 [ (2) B 中所选的干燥剂是 其作用是 。
(3) C 中发生的主要反应的化学方程式是
(4) 制取Y 气的D 装置所用的主要仪器是
制取Y 气的化学方程式是 。
(5) 当F 中充有一定量气体后,D 停止送气,A 停止加热,并立即关闭两个活塞,这时若将F 浸入冰水中,可看到F 中的现象是 ,其原因是
17. (1)右图是用KMnO 4 与浓盐酸反应制取适量氯气的简易..
装置。装置B 、C 、D 的作用分别是:
B ;
C ;
D 。
(2)在实验室欲制取适量NO 气体。
①下图中最适合完成该实验的简易..
装置是________(填序号);
A B C Ⅰ A B C A B C D A B C D I II III IV
②根据所选的装置完成下表(不需要的可不填): 应加入的物质 所起的作用
A B C D
稀NaOH
溶液
A
B
C
D
③简单描述应观察到的实验现象______________________________________________。
18.氢化钙固体登山运动员常用的能源提供剂。某兴趣小组长拟选用如下装置制备氢化钙。 无水氯化钙
a b
浓硫酸 NaOH 小苏打
溶液 饱和溶液
c d e f g h 锌粒 盐酸
i
钙 j k H 2O 2溶液 MnO 2 l
请回答下列问题:
(1)请选择必要的装置,按气流方向连接顺序为________(填仪器接口的字母编号)
(2)根据完整的实验装置进行实验,实验步骤如下:检查装置气密性后,装入药品;打开分液漏斗活塞_________(请按正确的顺序填入下列步骤的标号)。
A.加热反应一段时间
B.收集气体并检验其纯度
C.关闭分液漏斗活塞
D.停止加热,充分冷却
(3)实验结束后,某同学取少量产物,小心加入水中,观察到有气泡冒出,溶液中加入酚酞后显红色,该同学据此断,上述实验确有CaH 2生成。
① 写出CaH 2与水反应的化学方程式 __________________;
②该同学的判断不正确,原因是_______________________。
(4)请你设计一个实验,用化学方法区分钙与氢化钙,写出实验简要步骤及观察到的现象_____________。
(5)登山运动员常用氢化钙作为能源提供剂,与氢气相比,其优点是____________。
19.硫酸亚铁铵[(NH 4)2SO 4·FeSO 4·6H 2O]为浅绿色晶体,实验室中常以废铁屑为原料来制备,其步骤如下:
步骤1:将废铁屑放入碳酸钠溶液中煮沸除油污,分离出液体,用水洗净铁屑。
步骤2:向处理过的铁屑中加入过量的3mol·L -1H 2SO 4溶液,在60℃左右使其反应到不再产生气体,趁热过滤,得Fe SO 4溶液。
步骤3:向所得FeSO 4溶液中加入饱和(NH 4)2SO 4溶液,经过“一系列操作”后得到硫酸亚铁铵晶体。
请回答下列问题:
