western blot,WB,蛋白质印迹法,免疫印迹试验

Western Blot步骤
Western Bolt基本步骤
组织细胞裂解提蛋白→蛋白定量→配试剂→配胶→上样→电泳→电转→封闭→敷一抗→洗→敷二抗→洗→显影
一、组织细胞裂解提蛋白
1. 把组织剪切成细小的碎片。
2. 融解RIPA裂解液,混匀。取适当量的裂解液,在使用前数分钟内加入PMSF,使RIPA与PMSF的比例为100:1(现在EP管里配好再分别加)。
3. 按照每20毫克组织加入150-250微升裂解液的比例加入裂解液。(如果裂解不充分可以适
当添加更多的裂解液,如果需要高浓度的蛋白样品,可以适当减少裂解液的用量。)
4. 用玻璃匀浆器匀浆,直至充分裂解。
5. 充分裂解后,14000g,4℃,离心15分钟,取上清,即可进行后续的PAGE、Western和
免疫沉淀等操作。
6. 以上步骤确保于冰上进行,特别是匀浆时。
7. 如果组织样品本身非常细小,可以适当剪切后直接加入裂解液裂解,通过强烈vortex使
样品裂解充分。然后同样离心取上清,用于后续实验。直接裂解的优点是比较方便,不必使用匀浆器,缺点是不如使用匀浆器那样裂解得比较充分。
二.蛋白定量
配液(按照BCA蛋白浓度测定试剂盒说明书进行)
1、蛋白标准品的准备
a.取0.8ml蛋白标准配制液加入到一管蛋白标准(20mg BSA)中,充分溶解后配制成25mg/ml
的蛋白标准溶液。配制后可立即使用,也可以-20oC长期保存。
b.取适量25mg/ml蛋白标准,稀释至终浓度为0.5mg/ml(50倍)。例如取20μl 25mg/ml蛋
白标准,加入980μl稀释液即可配制成0.5mg/ml蛋白标准。蛋白样品在什么溶液中,标准品也宜用什么溶液稀释。但是为了简便起见,也可以用0.9% NaCl或PBS稀释标准品。稀释后的0.5mg/ml蛋白标准可以-20oC长期保存。
2.BCA工作液配制根据样品数量,按50体积BCA试剂A加1体积BCA试剂B(50:1)配制适量BCA工作液,充分混匀。例如5ml BCA试剂A加100μl BCA试剂B,混匀,配制成5.1ml BCA 工作液。BCA工作液室温24小时内稳定。(需根据以下加样量计算所需工作液量,尽量算多点。标准物8孔,检测物X个,每孔需200ul,所以共需工作液(8+X+2)×200ul。)加样
1.加标准品于96孔板,依次加0,1,2,4,8,12,16,20ul形成梯度,随后每孔中加入PBS使最后每孔总量为20ul。如下
蛋白定量标准品ul 0 1 2 4 8 12 16 20 PBS ul 20 19 18 16 12 8 4 0 蛋白定量工作液ul 200 200 200 200 200 200 200 200
2. .(另排)再96孔板中加入10ul总蛋白,每孔加入10ulPBS,再每孔加入工作液200ul。
如下
总蛋白ul 1 1 1 1 1 1
PBS 19 19 19 19 19 19
工作液200 200 200 200 200 200
全部吹打混匀(不要产生气泡)后放入水浴(37℃30min)或60℃温箱30min,根据蛋白浓度决定,浓度越高需要的温度越高时间越长
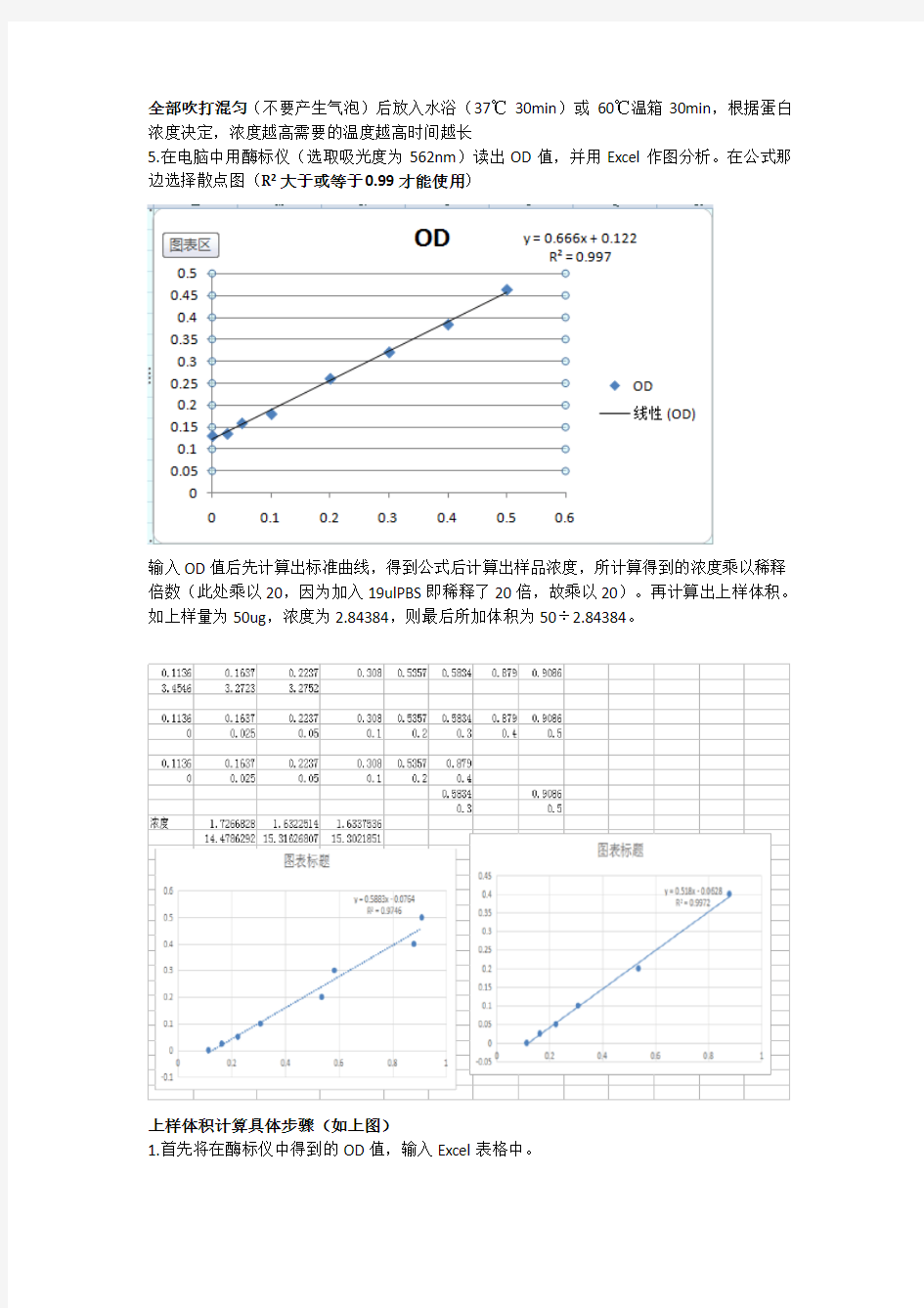
5.在电脑中用酶标仪(选取吸光度为562nm)读出OD值,并用Excel作图分析。在公式那边选择散点图(R2大于或等于0.99才能使用)
输入OD值后先计算出标准曲线,得到公式后计算出样品浓度,所计算得到的浓度乘以稀释倍数(此处乘以20,因为加入19ulPBS即稀释了20倍,故乘以20)。再计算出上样体积。如上样量为50ug,浓度为2.84384,则最后所加体积为50÷2.84384。
上样体积计算具体步骤(如上图)
1.首先将在酶标仪中得到的OD值,输入Excel表格中。
2.将浓度梯度OD值单独列出,并在其下方一行分别输入0,0.025,0.05,0.1,0.2,0.3,0.4,0.5.选定两行后绘制浓度梯度曲线(插入→插入散点图→点选图表上的点后右键→添加趋势线→点选趋势线后右键→设置趋势线格式→选择“显示公式”及“显示R平方值”)
3.R平方值需大于0.99公式才可使用,若R平方值需小于0.99,则需踢除趋势线上较偏离的点,直至R平方值大于0.99。
4.将加入总蛋白的样品的OD值带入X中,Y为浓度,上样体积为上样量÷(浓度×稀释倍数(此处为2)),如上样量为50ug,浓度为2.84384,则最后所加体积为50÷2.84384。
三.蛋白的处理
1.测量好蛋白浓度,再做WB时每次都加30ug蛋白(质量可变,可设定质量梯度),蛋白上样缓冲液Loading buffer 以5分1比例加入,算好体积并加好蛋白上样缓冲液后分装到小管,要多加一些,建议总上样量的2倍
2.煮蛋白,将机器预热到100℃后煮5min
3.放-80℃冻存
四.配液、配胶
5×电泳液:Tris 7.5g,甘氨酸36g,SDS 2.5g,定容至500ml母液,使用时稀释至1×,每个电泳槽2块胶时需1000ml电泳液,4块胶时需至少1500ml电泳液。
10×电转液:甘氨酸72g,Tris 15.4g,定容至500ml母液,4℃保存,使用时稀释:100ml 10×电转液+150ml甲醇,定容至1000ml,每个电转槽需至少1500ml电转液。
TBST:NaCl 8g,Tris 3g,加DDH2O至900ml-950ml溶解后,调PH 7.4,定容至1000ml,最后加TWEEN20 1ml。
10%封闭液:5g脱脂奶粉,加TBST定容至50ml,每个培养皿需50ml。
抗体稀释液:5g BSA,加TBST定容至100ml,可多配一点4℃保存。
胶配方:
30%丙烯酰胺=29g丙烯酰胺+1g亚甲基双丙烯酰胺,DDH20定容至100ml
1.5M Tris 计算方式:Tris分子量×1.5=1L溶液中所需Tris的质量。1.0M Tris 计算方式相同。
五.电泳
胶转到电泳夹子中,夹子要夹紧尽量不要漏电泳液,将夹子放入电泳槽中,黑对黑,红对红,加入电泳液后拔出梳子加样本,最左及最右尽量不要加样本。Marker加5ul并加入6ul 5×蛋白(根据Marker说明书,此处为直接加Marker 5ul)。将电泳槽放入冰块中,80V,3h(时间不定,看实际情况),使loading buffer跑到指示线即可。
六.电转
电泳结束后取出胶切掉无用部分。PVDF膜先用甲醇先泡1min,裁剪滤纸,滤纸大小>膜>胶,用一大托盘,里面倒入电转液,将胶、海绵、滤纸、甲醇浸泡过的PVDF膜放入电转液中,需完全浸湿。搭建三明治结构:夹子黑面(负极)在下,白面(正极)在上,在黑面上依次放置海绵、3层滤纸、胶、PVDF膜、3层滤纸、海绵,每放一层需倒入少许电转液以避免产生气泡,将夹子夹紧,务必保证每层之间没有气泡,需在PVDF膜上标记以确定蛋白面。将三明治结构放入电转槽中,黑对黑,红对红,电转槽中倒入电转液,电转液需没过三明治结构,将电转槽放入冰块中,200mA,2h(需根据蛋白分子量调整)。
七.封闭
将电转好的PVDF膜取出,放于封闭液中,保鲜膜覆盖,在摇床上40转左右,2小时。封闭后,将PVDF膜取出,在TBST中清洗3遍,摇床140转左右,每遍6min。根据Maker将所需要的区段及Actin抗体所显影区段分别裁剪下来。
八.敷一抗,洗一抗
根据抗体说明书使用抗体稀释液稀释一抗,4℃敷一抗摇床慢速至少过夜。
需稀释后一抗3ml,将PE手套裁剪,包裹所需PVDF区段,封口机封口,仅留上端开口,将
一抗加入,完全排出气泡后,用封口机封闭,4℃敷一抗摇床慢速至少过夜。Actin抗体同上。
敷一抗结束后用TBST洗3遍,摇床140转左右,每遍6min。
九.敷二抗,洗二抗
根据抗体说明书使用抗体稀释液稀释二抗,敷二抗摇床40转左右,1小时。
需稀释后二抗2ml,取一个培养皿,其上放置一张封口膜,需完全覆盖培养皿底部,其上按PVDF膜区段大小滴入二抗,将敷二抗PVDF膜蛋白面朝下放于二抗上,完全排出气泡,保鲜膜覆盖后放于摇床40转左右,1小时,Actin同上。结束后用TBST洗3遍,摇床140转左右,每遍6min。
十.显影
配置ECL试剂盒,A液:B液1:1。需提前开启设备降温,将PVDF膜蛋白面朝上放于暗盒板上,显影液滴在PVDF膜蛋白面上,孵育30s后将膜上多余显影液吸干,仅保持膜上湿润,使用电脑可直接读取条带。
(完整版)WesternBlot(免疫印迹法)实验方法步骤
Western Blot(免疫印迹法)实验方法步骤 发布日期:2008-8-25 热门指数:4360 Western Blot(免疫印迹法) 主要包括以下4个基本步骤: n 样品制备 n 电泳分离 n 蛋白的膜转移 n 免疫杂交与显色――蛋白检测 溶液和试剂 n 1X 磷酸盐缓冲液(PBS) n Modified RIPA buffer Tris-HCl: 50 mM, pH 7.4 ; NP-40: 1% ;Na-deoxycholate: 0.25% ;NaCl: 150 mM ;EDTA: 1 mM ;P MSF: 1 mM ;Aprotinin, leupeptin, pepstatin: 1 microgram/ml each ;Na3VO4: 1 mM ;NaF: 1 mM n 1X SDS 样品缓冲液 62.5 mM Tris-HCl (pH 6.8 于25°C), 2% w/v SDS, 10%甘油,50 mM DTT, 0.01% w/v溴酚蓝 n 转移缓冲液 25 mM Tris base, 0.2 M 甘氨酸, 20%甲醇(pH 8.3) n 10X Tris缓冲盐(TBS) 准备1L 10X TBS: 24.2 g Tris base, 80 g NaCl;用1N HCl调pH为7.6 n 脱脂奶粉或BSA n 甲醇 n TBS/T缓冲液 1X TBS, 0.1% Tween-20 n 封闭缓冲液(TBS/T)
1X TBS, 0.1% Tween-20加5% w/v脱脂奶粉或BSA n 一抗的稀释 1X TBS, 0.1% Tween-20 加5% BSA (多抗)或5%脱脂奶粉(单抗) Note:一般来说, BSA被推荐用于多克隆抗体,脱脂奶粉用于单克隆抗体,这样可得到较高的信噪比。抗体的稀释度参考抗体说明书或根据实验确定。 n 预染的蛋白质Marker,可用于监测转膜的效率 样品制备 原始样品可为细胞、组织、培养上清、免疫沉淀或亲和纯化的蛋白,以下为定性检测目的蛋白时细胞样品的处理方法,其余的样品制备方法参阅相关文献。 1.培养细胞或药物处理。 2.弃培养基,用1X PBS漂洗细胞2次,去尽残留培养基。 3.加入1X SDS样品缓冲液(6-well plate, 100 μl /w或75 cm2plate, 500-1000 μl/瓶),刮落细胞,转移到Ep管。注意:冰上操作。 4.超声10~15秒剪切DNA以减低样品粘性。 5.煮沸样品5 minutes。 6.离心12000g, 5 min,取上清。 7.电泳分离:上样15μl~20 μl 至SDS-PAGE 胶(10 cm x 10 cm)电泳。 如要定量检测某蛋白的表达水平,应用RIPA裂解液(1 ml per 107cells/100 mm dish/150 cm2flask)裂解细胞,收集裂解液至离心管中,在振荡器上混匀4~15min,14000g离心15min(4℃),弃沉淀,用B radford法或其它蛋白质测定方法测定上清中蛋白浓度以调整上样体积和上样量,进行Western杂交时还需设置内或外参照,通常用beta-actin。 注意:一般上样20~30 μg已足够,如待检蛋白为低丰度蛋白,可加大上样量至100μg,但电泳条带易拖尾,可制备亚细胞组份或采用更敏感的检测方法。 电泳分离(参照SDS-PAGE电泳方法) 转膜 杂交膜的选择是决定Western blot成败的重要环节。应根据杂交方案、被转移蛋白的特性以及分子大小等因素,选择合适材质、孔径和规格的杂交膜。用于Western blot的膜主要有两种:硝酸纤维素膜(NC) 和PVDF膜。NC膜是蛋白印迹实验的标准固相支持物,在低离子转移缓冲液的环境下,大多数带负电荷的蛋白质会与膜发生疏水作用而高亲和力的结合在一起,但在非离子型的去污剂作用下,结合的蛋白还可以被
蛋白印迹分析
【实验目的】 了解蛋白质印迹法的基本原理及其操作和应用。 【实验原理】 蛋白质印迹法又称为免疫印迹法,这是一种可以检测固定在固相载体上蛋白质的免疫化学技术方法。待测蛋白既可以是粗提物也可以经过一定的分离和纯化,另外这项技术的应用需要利用待测蛋白的单克隆或多克隆抗体进行识别。 如图所示,可溶性抗原,也就是待测蛋白首先要根据其性质,如分子量,分子大小,电荷以及其等电点等采用不同的电泳方法进行分离;通过电流将凝胶中的蛋白质转移到聚偏二氟乙烯膜上;利用抗体(一抗)与抗原发生特异性结合的原理,以抗体作为探针钓取目的蛋白。值得注意的是在加入一抗前应首先加入非特异性蛋白,如牛血清白蛋白对膜进行“封阻”而防止抗体与膜的非特异性结合。 经电泳分离后的蛋白往往需再利用电泳方法将蛋白质转移到固相载体上,我们把这个过程称为电泳印迹。常用的两种电转移方法分别为: 1.半干法: 凝胶和固相载体被夹在用缓冲溶液浸湿的滤纸之间,通电时间为10分钟~30分钟。 2.湿法:凝胶和固相载体夹心浸放在转移缓冲溶液中,转移时间可从45分钟延长到过夜进行。 由于湿法的使用弹性更大并且没有明显浪费更多的时间和原料,因此我们在这里只描述湿法的基本操作过程。 对于目的蛋白的识别需要采用能够识别一抗的第二抗体。该抗体往往是购买的成品,已经被结合或标记了特定的试剂,如辣根过氧化物酶。这种标记是利用辣根过氧化物酶所催化的一个比色反应,该反应的产物有特定的颜色且固定在固相载体上,容易鉴别。因此可通过对二抗的识别而识别一抗,进而判断出目标蛋白所在的位置。其他的识别系统包括碱性磷酸酶系
统和125I标记系统。 【实验操作】 ⒈.蛋白质的分离 根据目的蛋白的性质,利用电泳方法将其进行分离。为提高电转移的效率,通常采用SDS/PAGE技术。 分离实验结束后,首先将样品墙的上边缘用小刀去除,然后在胶板的右上角切一个小口以便定位,小心放入转移缓冲溶液中待用。 ⒉.电转移 ⑴准备PVDF膜
蛋白质免疫印迹技术的实验研究
万方数据
万方数据
万方数据
蛋白质免疫印迹技术的实验研究 作者:张燕婉, 叶珏, 时那, 孟宪敏, 王来元, ZHANG Yan-wan, YE Jue, SHI Na, MENG Xian-min, WANG Lai-yuan 作者单位:中国医学科学院,阜外心血管病医院中心实验室,北京,100037 刊名: 实验技术与管理 英文刊名:EXPERIMENTAL TECHNOLOGY AND MANAGEMENT 年,卷(期):2008,25(10) 被引用次数:21次 参考文献(9条) 1.郭尧君蛋白质电泳实验技术 2006 2.Nieman T Detection based on solution-phase chemiluminescence systems 1989 3.李晓军,秦浚川,武建国蛋白印迹技术研究进展[期刊论文]-临床检验杂志 2004(3) 4.Towbin H;Staehelin T;Gordon Electrophoretic franker of proreins from polyacrylamide gels to nitrocellulose sheets.Procedure and some appHcations 1979(76) 5.Hauri H P;Bucher K Immunoblotting with monodonal antibodities:Importance of the blocking solution 1986(159) 6.高红,王贵新,王维林,张可仞用蛋白印迹技术初步评价肝母细胞瘤血管内皮生长因子表达的意义[期刊论文]-中华小儿外科杂志 2006(2) 7.Towbin H;Gordon J Immunoblotting and dot immunobinding:current status and outlook 1984(72) 8.Tovey ER;Baldo BA Characterisation of allergens by protein blotting 1987(08) 9.沈关心;龚非力抗体技术实验指南 2006 本文读者也读过(1条) 1.段勇.黄韬.袁育林.刘华.李娅.金克炜.DUAN Yong.HUANG Tao.YUAN Yulin.LIU Hua.LI Ya.JIN Kewei蛋白质免疫印迹技术检测肺癌组织上皮钙粘蛋白的表达[期刊论文]-检验医学2009,24(1) 引证文献(7条) 1.秦双立,徐玥蛋白质印迹法在氟中毒研究中的应用[期刊论文]-山东化工 2015(13) 2.马瑛,马明,沈辉,骆新荣,高庆华不孕奶牛宫颈黏液相关ASA免疫印迹分析[期刊论文]-中国奶牛 2013(06) 3.程娜娜,韩榕He-Ne激光和增强UV-B辐射对拟南芥叶片微管蛋白的影响[期刊论文]-激光生物学报 2013(04) 4.刘娇,华碧春,黄智锋蛋白表达检测技术在中药肝损伤机制研究中的应用进展[期刊论文]-浙江中医药大学学报2013(04) 5.韩继美胶体金免疫层析法对AFP、CEA和FN的快速检测[学位论文]硕士 2009 6.黄斌芳c-Jun基因启动子区的遗传变异与肺癌易感性的研究[学位论文]硕士 2012 7.程娜娜He-Ne激光和增强UV-B辐射对拟南芥叶片微管结合蛋白MAP65-1的影响[学位论文]硕士 2014 引用本文格式:张燕婉.叶珏.时那.孟宪敏.王来元.ZHANG Yan-wan.YE Jue.SHI Na.MENG Xian-min.WANG Lai-yuan 蛋白质免疫印迹技术的实验研究[期刊论文]-实验技术与管理 2008(10)
免疫印迹实验报告——wester blot
Western blot实验报告 摘要:目的:学习并掌握western blot分离蛋白及观察方法 方法:western blot 结果:见后文 结论:western blot能很好地分离蛋白 关键词:western blot、分离、小鼠组织、蛋白 Western blot test report Abstract: objective: Learn and master the western blot protein isolated and observation method Methods: western blot:,sds-page and electric transfer Results: see below Key words: Western blot、separate、mouse tissues、protein 前言:免疫印迹又称Western印迹(Western blotting),与DNA的Southern印迹技术相对应,两种技术均把电泳分离的组分从凝胶转移至一种固相载体(通常为NC膜),然后用探针检测特异性组分。不同的是,Western blotting所检测的是抗原类蛋白质成分,所用的探针是抗体,它与附着于固相载体的靶蛋白所呈现的抗原表位发生特异性反应。该技术结合了凝胶电泳分辨力高和固相免疫测定特异敏感等诸多优点,具有从复杂混合物中对特定抗原进行鉴别和定量检测,以及从多克隆抗体中检测出单克隆抗体的优越性。该技术的灵敏度能达到标准的固相放射免疫分析的水平而无需对靶蛋白进行放射性标记。目前,Western blotting广泛用于蛋白质研究、基础研究和临床医学的研究。 免疫印迹可分成两个步骤:蛋白质由凝胶转移至固相基质;特异性抗体检测。 蛋白质转移通常由电泳实现,现常用的方法有二:1 半干法:将凝胶和固相基质似三明治样夹在缓冲液湿润的滤纸中间,通电10-30分钟可完成转移;2 湿法:将凝胶和固相基质夹在滤纸中间,浸在转移装置的缓冲液中,通电45分钟或过夜课完成转移。本试验采用湿法转移。免疫印迹用膜通常有硝酸纤维素膜和尼龙膜两种。大多数应用前者。本实验也用硝酸纤维素膜进行转移。 1 试剂与仪器 1.1 试剂(所有试剂均供两组用) 1.1.1 8%电泳分离胶的配制 H2O 6.9ml
蛋白质印迹法
蛋白印迹法(Western-blot) 一、基本原理 细胞色素P450是一组含亚铁血红素,结构与功能相关的超家族基因编码的同工酶,因还原型P450与一氧化碳有特殊的亲和力,且形成的复合物在波长450nm处有一特异吸收峰而得名。已知的细胞色素P450超家族中,主要有CYP1、CYP2、CYP3三个基因家族,是生物体参与内外源性化合物生物转化酶系的主要成员,并与肿瘤的发生密切有关。其中CYP1家族中的CYP1A1与多种前致癌物、致突变物的代谢活化及肿瘤的发展密切相关,所以对CYP1A1的研究有重要的意义。 本实验采用蛋白免疫印迹(western blotting , WB)技术分析小鼠肝,肾两个器官中的CYP1A1的含量。WB的原理如下。 Western blotting 常用十二烷基硫酸钠-聚丙烯酰胺电泳(SDS—PAGE)法分离蛋白质。SDS是一种阴离子去污剂,它能与绝大多数蛋白质结合。无论与SDS结合前蛋白质的等电点是多少,结合后蛋白质将带上等量的负电荷,通常SDS与蛋白质结合的比例为1.4:1g 。同时结合后蛋白质的分子构象发生改变,行成长椭圆棒状,其短轴大约为18nm,其长轴与分子量有关(一定范围内成正比),此时蛋白质的电泳迁移率仅与蛋白质的分子量有关。另外,SDS—PAGE过程中还加入了二硫苏糖醇和?-巯基乙醇等强还原剂,破坏二硫键使得蛋白质的原有空间结构充分破坏,因此SDS—PAGE能将不同分子量的蛋白质分离开。
分离后的蛋白质带有负电荷,因而用电转移的方法能有效地将蛋白质转移至固相载体上(如硝酸纤维素膜)。用于承载蛋白质的各种膜均具有一个特点,它们都能与蛋白质发生非特异的共价结合,因而结合较为牢固,不易被后续的洗膜等操作洗脱. Western blotting所用的探针为针对靶蛋白某段氨基酸序列的抗体。能直接与靶蛋白发生抗原抗体结合的抗体称为第一抗体(简称一抗),通常由于较难大量获得该抗体,使得对其进行标记很困难。为此人们设计了能与一抗结合的抗体,成为第二抗体(简称二抗)。二抗是将一抗的FC段作为抗原的,而每一物种的抗体FC段氨基酸序列都较为保守,这使得二抗能够大量生产,因而对二抗进行标记也就较为容易了。二抗与一抗能通过抗原抗体特异性结合后,以一定的方法对二抗上的标记进行检测便可检出靶蛋白。 二、器材 电热水浴箱、玻璃匀浆器、冷冻离心机、滤纸、水平摇床、电转移装置、醋酸纤维素膜(NC膜)、电泳仪、试管、微量移液器、Tip头、Epp管(2ml、5 ml、1.5 ml) 三、试剂配制: 1)、1.5M Tris—Hcl, pH8.8:18.16g Tris溶于60 ml ddH2O,用浓盐酸调节PH至8.8,定容至100 ml,4℃保存。 2)、1.0M Tris—Hcl, pH6.8:12.12g Tris溶于60 ml ddH2O,用浓盐酸调节PH至6.8,定容至100 ml,4℃保存。 3)、10%SDS:10g SDS溶于90 ml ddH2O,轻柔搅拌,溶解后加水
免疫印迹介绍及实验过程
免疫印迹 免疫印迹 免疫印迹(immunoblotting)又称蛋白质印迹(Western blotting),是根据抗原抗体的特异性结合检测复杂样品中的某种蛋白的方法。该法是在凝胶电泳和固相免疫测定技术基础上发展起来的一种新的免疫生化技术。由于免疫印迹具有SDS-PAGE 的高分辨力和固相免疫测定的高特异性和敏感性,现已成为蛋白分析的一种常规技术。免疫印迹常用于鉴定某种蛋白,并能对蛋白进行定性和半定量分析。结合化学发光检测,可以同时比较多个样品同种蛋白的表达量差异。 免疫印迹法的基本原理 将混合抗原样品在凝胶板上进行单向或双向电泳分离, 然后取固定化基质膜与凝胶相贴。在印迹纸的自然吸附力、电场力或其它外力作用下, 使凝胶中的单一抗原组份转移到印迹纸上, 并且固相化。最后应用免疫覆盖液技术如免疫同位素探针或免疫酶探针等, 对抗原固定化基质膜进行检测和分析。 免疫印迹法的基本步骤 免疫印迹法(以抗原分析为例)基本上可分为抗原分离、抗原印迹和抗原检定三个步骤。在每一步中因采用的具体实验方法不同, 可构成多种免疫印迹分析系统。 免疫印迹法的优点 免疫印迹法是一项分析抗原、抗体的技术。它具有下列优点: 1、湿的固定化基质膜柔韧, 易于操作; 2 、固定化的生物大分子可均一的与各种免疫探针接近, 不会象凝胶那样受孔径阻隔; 3、免疫印迹分析只需少量试剂; 4、孵育、洗涤的时间明显减短; 5、可同时制作多个拷贝, 用于多种分析和鉴定; 6、结果以图谱形式可长期保存; 7、免疫探针可通过降低PH值等方法, 象抹去录音磁带一样将探针抹掉, 再换用第二探针进行分析检测。免疫印迹法的应用范围及优点不仅局限于此, 它必将随着这一方法的深入研究而不断发展和完善。 免疫印迹 免疫印迹又常称Western blot,是一综合性的免疫学检测技术。它利用SDS-PAGE技术将生物样品中的蛋白质分子按分子量的大小在凝胶上分离开,然后用电转移的方法将蛋白转移到固相膜上(NC、尼龙或PVDF膜),最后进行免疫学检测。由于免疫学检测敏感性高,并且通过SDS-PAGE样品中的待检蛋白得到了浓缩,因此,Western blot的灵敏度特别高,可达到放射免疫的分析水平。而使用一般的免疫学检测技术(如ELISA、放射免疫沉淀)检测时,由于要求被检测蛋白可溶、要求抗体效价高、亲和力高和特异性强,往往并不容易达到目的。而Western blot却没有这些缺点。因此,Western blot广泛应用于生物样品中是否存在某一蛋白质(抗原)的检测。也可用于粗略测定抗原蛋白的相对含量和抗原多肽链的相对分子量。
(完整版)蛋白免疫印迹(westernblot)实验
蛋白免疫印迹(western blot)实验 实验步骤: 一、试剂准备 1. SDS-PAGE试剂:见聚丙烯酰胺凝胶电泳实验。 2. 匀浆缓冲液:1.0 M Tris-HCl(pH 6.8) 1.0 ml;10%SDS 6.0 ml;β-巯基乙醇 0.2 ml;ddH2O 2.8 ml。 3. 转膜缓冲液:甘氨酸 2.9 g;Tris 5.8 g;SDS 0.37 g;甲醇200 ml;加ddH2O定容至1000 ml。 4. 0.01 M PBS(pH7.4):NaCl 8.0 g;KCl 0.2 g;Na2HPO4 1.44 g;KH2PO4 0.24 g;加ddH2O至1000 ml。 5. 膜染色液:考马斯亮兰 0.2 g;甲醇80 ml;乙酸2 ml;ddH2O118 ml。包被液(5%脱脂奶粉,现配):脱脂奶粉1.0 g 溶于20 ml的0.01 M PBS中。 6. 显色液:DAB 6.0 mg;0.01 M PBS 10.0 ml;硫酸镍胺 0.1 ml;H202 1.0 μl。【晶莱生物】 二、蛋白样品制备 1.单层贴壁细胞总蛋白的提取 (1)倒掉培养液,并将瓶倒扣在吸水纸上使吸水纸吸干培养液(或将瓶直立放置一会儿使残余培养液流到瓶底然后再用移液器将其吸走)。 (2)每瓶细胞加3 ml 4℃预冷的PBS(0.01M pH7.2~7.3)。平放轻轻摇动1 min洗涤细胞,然后弃去洗液。重复以上操作两次,共洗细胞三次以洗去培养液。将PBS弃净后把培养瓶置于冰上。 (3)按1ml裂解液加10 μl PMSF(100 mM),摇匀置于冰上。(PMSF要摇匀至无结晶时才可与裂解液混合。) (4)每瓶细胞加400 μl含PMSF的裂解液,于冰上裂解30 min,为使细胞充分裂解培养瓶要经常来回摇动。 (5)裂解完后,用干净的刮棒将细胞刮于培养瓶的一侧(动作要快),然后用枪将细胞碎片和裂解液移至1.5 ml离心管中。(整个操作尽量在冰上进行。) (6)于4℃下12000 rpm离心5 min。(提前开离心机预冷) (7)将离心后的上清分装转移倒0.5 ml的离心管中放于-20℃保存。
蛋白质印迹(Western blotting)方法原理和优化
蛋白质印迹(Western blotting)方法原理和优化 已有2975 次阅读2008-6-19 10:43 |个人分类:生活点滴 蛋白质印迹(Western blotting)方法原理和优化 抽滤 抽滤是一种直接将蛋白质转移到膜上的方法。利用真空使溶解的样品滤过膜,蛋白质吸附到膜上,同时样品中其它成分被真空抽走。另外,也可直接将样品点在膜表面使之干燥。随后可对固定在膜上的蛋白质进行分析。 点印记和狭缝印记是抽滤方法的两种变型,用多支管装置将样品加到膜上成点状或狭缝图样。这些方法可用于快速定性筛选大量样品或定量分析类似样品,尤其是测试复杂分析中实验参数的适用性。 另一种抽滤方法的变型是格栅免疫印迹,这种方法适用于高度平行的样品分析,当样品量及其优先并且不能用常规方法如ELISA进行分析时使用。格栅免疫印迹可用于表征变态反应原-特异性抗体应答,只需最小量的病人血清。 当准备抽滤印迹膜时,要考虑以下方面: 去污剂可以抑制蛋白吸附到膜上。用于样品溶解和漂洗的缓冲液所含去污剂不应超过0.05%,并且仅当必要时才能加入。 样品体积应足以覆盖每个孔中的膜面积,但所含蛋白量不应超过膜的结合能力。 含较多颗粒的样品可能堵塞膜孔,而高黏度样品将降低流速。所以在结合前先通过预过滤或离心除去颗粒,只将上清加到膜上。而粘性样品要用缓冲液稀释。 Western印迹 Western印迹含一系列步骤,包括: ?? 用聚丙烯酰胺凝胶分离蛋白样品。 ?? 将胶上的蛋白转移到膜上。 ?? 鉴定膜上特定蛋白。 下面将从理论和实践方面讨论Western印迹方法。 用1-D或2-D凝胶分离复杂蛋白质混合物 印迹前分离复杂蛋白质混合物的最常见方法是一维(1-D)SDS-PAGE电泳,它根据蛋白质的分子量进行分离。有时用非变性电泳分离天然蛋白质。尽管这种方法通常缺乏变性电泳的分辨率,但当蛋白须保留生物活性时非常有用。 二维(2-D)凝胶电泳用于分析细胞、组织、和体液蛋白质的组成,是现代蛋白质组学的关键技术。2-D免疫印迹可提供分子量和等电点信息,并可用于区分翻译后修饰产生的不同蛋白质形式。有些情况下只进行1-D电泳分离也可用免疫印迹对蛋白分型。 分子量标准 在凝胶中加入分子量标准或标记物可以在电泳分离后估计感兴趣蛋白质的大小。有两种类型的分子量标准:未染色和预染色。未染色分子量标准通常由天然或重组的纯化蛋白混合物组成。在凝胶或膜上显示其位置需要染色步骤。预染标准允许在电泳过程中监测蛋白分离,也可以在随后的印迹步骤中指示转移效率。然而,它们比较昂贵且加入染料会影响蛋白迁移率。预染标准在确定分子量时可能不够精确,并且蛋白质上附加的染料在转移时会影响它们吸附到膜上的能力。 聚丙烯酰胺浓度 凝胶中聚丙烯酰胺浓度可以是均一浓度或是梯度浓度。最常见的聚丙烯酰胺浓度为10%,最适合分离10-150KD范围内的蛋白质。若要分析未知蛋白或许要更宽的分离范围,推
蛋白质免疫印迹(Western Blot )实验步骤和原理及注意事项
蛋白质免疫印迹(Western Blot )实验步骤和原理及注意事项 1.收集蛋白样品(Protein sample preparation) 可以使用适当的裂解液。收集完蛋白样品后,为确保每个蛋白样品的上样量一致,需要测定每个蛋白样品的蛋白浓度。根据所使用的裂解液的不同,需要采用适当的蛋白浓度测定方法。因为不同的蛋白浓度测定方法对于一些去垢剂和还原剂等的兼容性差别很大。BCA法。 2. 电泳(Electrophoresis) (1) SDS-PAGE凝胶配制 (2) 样品处理 在收集的蛋白样品中加入适量浓缩的SDS-PAGE蛋白上样缓冲液。例如2X或5X的SDS-PAGE蛋白上样缓冲液。使用5X的SDS-PAGE蛋白上样缓冲液可以减小上样体积,在相同体积的上样孔内可以上样更多的蛋白样品。 100℃或沸水浴加热3-5分钟,以充分变性蛋白(根据蛋白分子的大小,煮沸时间可适当变化,一般不低于5min。煮沸只是变性蛋白,而不是分解,一般加了抑制酶不会分解。煮沸对于SDS-PAGE凝胶电泳是必须的,只有煮沸,才能消除蛋白质的立体二级结构,伸展为一维线性结构,所以一般来讲二聚体都会解体,才能完全按照分子量跑电泳,加的蛋白Marker才有指示分子量的意义。蛋白样品变性后与SDS充分结合,SDS使每个氨基酸带相同的电荷,使整个蛋白呈线性结构. 抗体因为要是线性表位结合的,100度煮10min 后13000,离心5分钟,取上清电泳,因为沉淀会导致拖尾.也可以取上清到另一管,4度可以放一周备再次电泳)。 (3)电泳
i.清洗玻璃板:一只手扣紧玻璃板,另一只手蘸点洗衣粉轻轻擦洗。 两面都擦洗过后用自来水冲,再用蒸馏水冲洗干净后立在筐里晾 干。 ii.灌胶与上样 (1)玻璃板对齐后放入夹中卡紧。然后垂直卡在架子上准备灌胶。 (操作时要使两玻璃对齐,以免漏胶。) (2)配10%分离胶,加入TEMED后立即摇匀即可灌胶。灌胶时,可用10 ml枪吸取5 ml胶沿玻璃放出,待胶面升到绿带中间线高度时即可。然后胶上加一层水,液封后的胶凝的更快。(灌胶时开始可快一些,胶面快到所需高度时要放慢速度。操作时胶一定要沿玻璃板流下,这样胶中才不会有气泡。加水液封时要很慢,否则胶会被冲变型。) (3)当水和胶之间有一条折射线时,说明胶已凝了。再等3 min使胶充分凝固就可倒去胶上层水并用吸水纸将水吸干。 (4)配4%的浓缩胶,加入TEMED(TEMED,中文名为四甲基乙二胺,是一种无色透明的液体,有微腥臭味,可以用于配制SDS-PAGE胶。TEMED可以催化APS产生自由基,从而加速聚丙烯酰胺凝胶的聚合,可作为一种促凝剂使用)后立即摇匀即可灌胶。将剩余空间灌满浓缩胶然后将梳子插入浓缩胶中。灌胶时也要使胶沿玻璃板流下以免胶中有气泡产生。插梳子时要使梳子保持水平。由于胶凝固时体积会收缩减小,从而使加样孔的上样体积减小,所以在浓缩胶凝固的过程中要经常在两边补胶。待到浓缩胶凝固后,两手分别捏住梳子的两边竖直向上轻轻将其拔出。
蛋白印迹实验报告
蛋白印迹实验报告 篇一:实验十二Western印迹鉴定目标蛋白 实验十二Western印迹鉴定目标蛋白 实验目的 1.了解Western blot的原理及其意义,掌握Western blot的操作方法; 2.应用Western blot 技术分析鉴定经SDS-PAGE分离后转移到尼龙膜上的重组蛋白。 实验原理 Western印迹法简称蛋白质印迹法。蛋白质样品经SDS-PAGE电泳后,凝胶所含的样品蛋白质区带通过电泳方法转移、固定到载体(如尼龙膜、硝酸纤维素膜)上,固相载体以非共价键的形式与蛋白质结合,从而固定住蛋白质;以膜上的蛋白或多肽为抗原,与相应的第一抗体起免疫反应,再和酶标记或同位
素标记的第二抗体反应,用适当的溶液漂洗去未结合抗体后,置含底物的溶液中温育,或通过放射自显影显出谱带,即可检测出样品中的特异蛋白组分。 试剂与器材 试剂 1.转移缓冲液:甘氨酸(39 mmol/L),Tris 碱(48mmol/L),SDS (%),200ml 甲醇(20%),定容至1,000mL; 2.封闭液:5% 脱脂奶粉,% 叠氮钠,溶于PBST溶液中; 3.丽春红S(Ponceaus)染液:丽春红S溶于1mL 冰乙酸中,加水至100mL; 洗膜液:PBS 缓冲液含% Tween 20; 5.DAB浓缩显色液(50X):DAB (二氨基联苯胺)是根过氧化物酶的底物之一,临用前稀释。 6.5 x PBS:在1600mL蒸馏水中溶解Na 2HPO4 , Na H2PO4, 40g Na Cl,
用/L NaOH调pH至,加水定容至2升。高压灭菌20 分钟,室温保存。用前稀释至1x 。 7.SDS-PAGE电泳用溶液和试剂。 器材 电泳装置一套; 2.电转移膜装置 3.抗体-酶反应摇床 操作方法 〈一〉电转移 1.将蛋白质样品进行SDS-PAGE,待溴酚蓝跑出胶后停止电泳(1)。 2.载手套切6-8张定性滤纸和一张尼龙膜,它们的大小应与凝胶的大小相同。在尼龙膜的一(左)角作一记号(或剪角),与滤纸和海棉(纤维)垫浸泡于转移缓冲液中。 3.剥胶,并将凝胶裁成合适大小,切角以做记号(2)。 4.按下图示制备“夹心饼”,打开电极板,在一边放上一块纤维垫,再依次往上叠加3-4张滤纸,将凝胶轻放于滤
实验报告三 免疫印迹
实验三:免疫印迹 1 原理 免疫印迹又称Western印迹(Western blotting),与DNA的Southern印迹技术相对应,两种技术均把电泳分离的组分从凝胶转移至一种固相载体(通常为NC膜),然后用探针检测特异性组分。不同的是,Western blotting所检测的是抗原类蛋白质成分,所用的探针是抗体,它与附着于固相载体的靶蛋白所呈现的抗原表位发生特异性反应。该技术结合了凝胶电泳分辨力高和固相免疫测定特异敏感等诸多优点,具有从复杂混合物中对特定抗原进行鉴别和定量检测,以及从多克隆抗体中检测出单克隆抗体的优越性。该技术的灵敏度能达到标准的固相放射免疫分析的水平而无需对靶蛋白进行放射性标记。目前,Western blotting广泛用于蛋白质研究、基础研究和临床医学的研究。 免疫印迹可分成两个步骤:蛋白质由凝胶转移至固相基质;特异性抗体检测。 蛋白质转移通常由电泳实现,现常用的方法有二:1 半干法:将凝胶和固相基质似三明治样夹在缓冲液湿润的滤纸中间,通电10-30分钟可完成转移;2 湿法:将凝胶和固相基质夹在滤纸中间,浸在转移装置的缓冲液中,通电45分钟或过夜课完成转移。本试验采用湿法转移。免疫印迹用膜通常有硝酸纤维素膜和尼龙膜两种。大多数应用前者。本实验也用硝酸纤维素膜进行转移。 转移结束后,蛋白质的检测可分成三个步骤进行:首先,将膜同特异性抗体孵育数小时或过夜,然后将膜同可特异性识别上述抗体(一抗)的第二抗体(二抗)孵育,通常二抗连接有如辣根过氧化物酶等标记物。目的蛋白可由该酶催化的显色反应在膜上形成有色产物加以检测。本实验用的是酶标抗IgG,故不加一抗。 2 试剂与仪器 2.1 试剂(所有试剂均供两组用) 2.1.1 转移缓冲液 Tris 3.025g 甘氨酸14.413g 甲醇20mL 加蒸馏水约800mL,调pH至8.3,定容1000mL 2.1.2 Tris缓冲盐溶液(TBS)
免疫印迹(WB)实验操作具体步骤及详细说明
免疫印迹(WB)实验操作具体步骤及详细说明 一、试剂和溶液 转印缓冲液:0.025M Tris base , 0.187 M 甘氨酸, 25%甲醇氨基黑溶液:0.1% 酸性黑10B 1×TBST:25mM Tris-HCl ( pH 8.0 ) , 0.2 M NaCl , 0.1%Tween 20 封闭液:TBST 配制的5%牛奶抗体稀释液:TBST 配制的5%牛奶显色系统:ECL 显色 二、实验步骤 1.电泳:将裂解液进行SDS-PAGE 电泳,80v,30 分钟,120v,90 分钟; 2.转膜:PVDF 膜在甲醇中浸泡约30 秒左右,滤纸浸泡在转印缓冲液预湿, 半干法转印到PVDF 膜上,10v,150 分钟; 3.染色:氨基黑染色5 分钟,甲醇褪去背景色,观察条带; 4.膜活化:将PVDF 膜置于甲醇活化1min,用纯水洗膜2 次后再用TBST 洗 涤3 次; 5.封闭:将膜条置于5%牛奶或2% BSA 中,室温混摇2h; 6.一抗孵育:将待检抗体用3%牛奶或2% BSA 稀释到合适浓度(参照抗体说 明书,根据客户预实验结果,稀释度上下浮动一个数量级都为正常),将膜放入对应的已稀释待检样品中,置4℃混摇孵育过夜; 7.洗涤:取出膜放在TBST 中洗涤3×5min; 8.二抗孵育:将膜取出放入稀释好的HRP 标记的二抗(参照二抗说明书进行 稀释)中,室温混摇2h; 9.洗涤:取出膜放在TBST 中洗涤3×5min; 10.ECL 显色:将膜取出放入混匀的ECL 显色液中,孵育3min,将膜取出贴在
有荧光角标的胶片上,迅速用保鲜膜包好; 11.曝光:把底片放在暗盒中,根据荧光强度分别对X 光胶片作不同时间段的曝 光,曝光结束后,将底片取出,1min 显影,30s 清洗,1min 定影,30s 清洗,晾干; 12.结果分析:用扫描仪将曝光后的X 光胶片扫描,做后续结果分析。
westernblotting蛋白质印迹实验的流程
细胞总蛋白的提取 (1)离心后,弃去上清液,将收集的细胞用手指轻弹重悬于剩余的少量上清液中,转移至1.5ml离心管内,用1×PBS溶液洗涤2次,每次加入1mL PBS溶液,1000r/min,4℃离心5min,弃上层液体。洗涤两次后,将上清液完全去除,用手指轻弹细胞团,使其分散重悬(若不分散,则无法与裂解液充分混匀)。 (2)每管加入细胞团等体积的含蛋白酶抑制剂cocktail的RIPA细胞裂解液;如需检测磷酸化蛋白,则需另加入磷酸酶抑制剂。使细胞裂解液与细胞充分混匀,冰上裂解30min。如暂不提取蛋白,也可在洗涤细胞2次后加入含蛋白酶抑制剂cocktail和磷酸酶抑制剂的1×PBS约100μL,1000r/min,4℃离心5min后,完全弃上层液体,置于-80℃冰箱保存备用。 (3)冰上超声处理细胞,每次超声2s,间隔3s,约10-20次。 (4)13000r/min,4℃离心15min,收集上清溶液至另一干净并预冷的1.5mL离心管中,于-80℃冰箱保存备用。 2. BCA法测定蛋白质浓度 (1)配制工作液 根据标准品及待测样品的个数,按BCA试剂A和试剂B体积比为50:1配制足量BCA 工作液,充分混匀,置于常温备用。 (2)配制标准品 取原标准品BSA(2mg/mL)约100μL,取出50μL,用ddH2O按对数法稀释成如下浓度:1mg/mL、0.5mg/mL、0.25 mg/mL、0.125 mg/mL、0.0625 mg/mL;设置96孔板第一横排第一孔为空白孔,第二横排第一、二孔加入20μL 1×PBS,从第三横排起,
按浓度梯度由低到高依次取20μL标准品至96孔板中,每一浓度做2个平行孔。 (3)稀释待测样品 取5μl待测蛋白样品,用ddH2O稀释到50μL,分别取20μL至96孔板中,每一浓度做2个平行孔; (4)分别加入200μL BCA工作液到蛋白标准品及待测样品中,轻轻混匀,并去掉每孔中的气泡,置于温箱37℃孵育30min。 (5)将96孔板取出后用酶标仪测定OD570nm值。 (6)根据标准品的OD570nm值绘制标准曲线,并根据标准曲线计算得到待测样品的蛋白质浓度。 蛋白质变性 (1)根据预计将要上样的蛋白质样品质量(25μg-50μgμg,是蛋白质而定),取适量体积的蛋白质样品于预冷的EP管中,加入5×SDS上样缓冲液(体积约为蛋白质样品体积的25%),通过调节上样缓冲液的体积将各样品混合液的终体积调节至相仿。用封口膜将离心管封口,7000r/min离心点离样品混合液3s,使其混合均匀。 (2)将放置样品混合液的架子置于盛有适量dd H2O的磁盘中,用电磁炉加温至100℃,煮沸5min。点离样品,使其混合均匀。 2.34.54. SDS-PAGE分离蛋白质 根据将要检测的蛋白质大小,首先确定配制10%的分离胶(10ml): dd H2O 4ml
蛋白免疫印迹杂交(Western Blot)技术手册
蛋白免疫印迹杂交(Western Blot)技术手册 蛋白免疫印迹杂交(Western Blot WB)是将蛋白样本通过聚丙烯酰胺电泳按分子量大小分离,再转移到杂交膜(blot)上,然后通过一抗/二抗复合物对靶蛋白进行特异性检测的方法。WB是进行蛋白质分析最流行和成熟的技术之一。本指南讨论Western Blot操作方法及常见问题分析,有助于成功完成WB。 A 蛋白样本提取制备 1 细胞或组织裂解 2 蛋白酶和磷酸酶抑制剂 3 蛋白定量 4 电泳上样样品的准备 B 电泳 1 PAGE胶的制备 2 蛋白分子量Marker 3 阳性对照 4 内参对照 5 上样与电泳 C 转膜与显色(Western Blot) 1 胶中蛋白的检测 2 蛋白转膜 3 膜上蛋白的检测:丽春红 4 膜的封闭 5 一抗的孵育 6 二抗的孵育 7 显色 D 常见问题分析与解决方案 附录1 WB实验试剂配制方法 附录2 SDS-PAGE胶的配制
WB概述: 检测原理:
A 蛋白样本提取制备 蛋白样品制备是Western Blotting的第一步,更是决定WB成败的关键步骤, 总体原则和注意事项: 1:尽可能提取完全或降低样本复杂度只集中于提取目的蛋白 (通过采用不同提取方法或选择不同的试剂盒产品) 2:保持蛋白的处于溶解状态(通过裂解液的PH 盐浓度 表面活性剂、还原剂等的选择) 3:提取过程防止蛋白降解、聚集、沉淀、修饰等,(低温操作,加入合适的蛋白酶和磷酸酶抑制剂) 4:尽量去除核酸,多糖,脂类等干扰分子(通过加入核酸酶或采取不同提取策略) 5:样品分装,长期于-80℃中保存,避免反复冻融。 A-1 细胞或组织裂解 A-1-1 细胞裂解 裂解液Lysis buffer或商品化蛋白抽提试剂盒的选择* 目的蛋白分布定位推荐裂解液Lysis buffe 推荐试剂盒 全细胞NP-40 or RIPA(附录1)全蛋白抽提试剂盒 细胞质(可溶蛋白)Tris-HCl(附录1)胞浆蛋白和核蛋白抽提试剂盒 线粒体蛋白提取试剂盒 细胞质(细胞骨架等不溶蛋白)Tris-Triton(附录1)蛋白分级抽提试剂盒 细胞质(磷酸化蛋白)磷酸化蛋白抽提试剂盒 细胞膜NP-40 or RIPA(附录1)膜蛋白抽提试剂盒 蛋白分级抽提试剂盒 细胞核RIPA(附录1)核蛋白抽提试剂盒 线粒体RIPA(附录1)线粒体蛋白抽提试剂盒 亚细胞定位蛋白抽提试剂盒细胞裂解操作方法: 1 培养的细胞经预冷的PBS漂洗2次,裂解液中加入蛋白酶和磷酸酶抑制剂(种类与量见本节2) 2 吸净PBS,加入预冷的裂解液,((1 ml per 107 cells/100mm dish/150cm2 flask; 0.5ml per 5x106 cells/60mm dish/75cm2 flask). 3 用细胞刮子刮取贴壁细胞,将细胞及裂解液温和地转移至预冷的微量离心管中, 44℃摇动30 min 54℃离心12,000 rpm,20 min(根椐细胞种类不同调整离心力) 6 轻轻吸取上清,转移至新预冷的微量离心管中置于冰上,即为蛋白样本,弃沉淀. A-1-2 组织裂解 1 用灭菌的预冷的工具分离目的组织,尽量置于冰上以防蛋白酶水解, 2 将组织块放在圆底的微量离心管或Eppendorf管中,加入液氮冻结组织于冰上均质研磨,长期可保存于 -80°C, 3 每约5 mg加入约300 μl 预冷的裂解液lysis buffer,冰浴匀浆后置于4℃摇动2小时,裂解液体积与组 织样本量有适当比例,(最终的蛋白浓度至少达到0.1 mg/ml, 理想的蛋白浓度应为1-5 mg/ml). 4 4℃离心12,000 rpm,20 min,轻轻吸取上清,转移至新预冷的微量离心管中置于冰上,即为蛋白样本, 弃沉淀,
蛋白检测篇1-Western Blot
编号:1-1 主题:Western Blot(蛋白质印迹法) 概述: 蛋白质印迹法(免疫印迹试验)即Western Blot,它是分子生物学、生物化学和免疫遗传学中常用的一种实验方法。其基本原理是通过特异性抗体对凝胶电泳处理过的细胞或生物组织样品进行着色,通过分析着色的位置和着色深度获得特定蛋白质在所分析的细胞或组织中表达情况的信息。 目的: 获得特定蛋白质在所分析的细胞或组织中的表达情况的信息。 原理: 与Southern或Northern杂交方法类似,但Western Blot采用的是聚丙烯酰胺凝胶电泳,被检测物是蛋白质,“探针”是抗体,“显色”用标记的二抗。经过PAGE分离的蛋白质样品,转移到固相载体(例如硝酸纤维素薄膜)上,固相载体以非共价键形式吸附蛋白质,且能保持电泳分离的多肽类型及其生物学活性不变。以固相载体上的蛋白质或多肽作为抗原,与对应的抗体起免疫反应,再与酶或同位素标记的第二抗体起反应,经过底物显色或放射自显影以检测电泳分离的特异性目的基因表达的蛋白成分。 步骤: 1.提取组织或细胞蛋白; 2.测定蛋白质浓度;
3.电泳: 电泳条件为:恒压100V,待染料前沿移行到距离凝胶底部2-3mm时方可停止(约120min); 4.电转膜仪转膜: 转膜条件为:恒流250mA ,2h(时间可根据目的蛋白分子量适当调整); 5.封闭:5%脱脂牛奶室温封闭1h; 6.加一抗:一抗封膜之后室温条件下摇1h然后放入4℃冰箱中过夜; 7.收一抗,PBST洗膜3次,10min/次; 8.二抗孵育: 室温孵育1h,所用二抗的比例和种属见步骤9)表格。 9.洗膜:PBST洗膜2次,PBS洗膜一次,10min/次。 10.显色 流程图:
蛋白质印迹法western blot应用介绍
蛋白质印迹法(western blot技术) 威斯腾生物技术中心 2014.9.1
?Western Blot介绍 ?Western Blot一般流程 ?Western Blot常见问题分析
Western Blot 介绍 蛋白质印迹的发明者一般认为是美国斯坦福大学的乔治·斯塔克(George Stark)。在尼尔·伯奈特(Neal Burnette)于1981年所著的《分析生物化学》(Analytical Biochemistry)中首次被称为Western Blot。 蛋白免疫印迹( Western Blot) 是将电泳分离后的细胞或组织总蛋白质从凝胶转移到固相支持物NC膜或PVDF 膜上,然后用特异性抗体检测某特定抗原的一种蛋白质检测技术,现己广泛应用于基因在蛋白水平的表达研究、抗体活性检测和疾病早期诊断等多个方面。
Western Blot流程
(1)贴壁细胞蛋白样品收集 A 收集培养瓶或六孔板中的培养液转移至离心管中。 B 加入PBS 冲洗2-3遍,再将PBS 转移至离心管中,离心收集细胞。 C 将细胞培养瓶或六孔板臵于冰上,然后将离心好的离心管中的液体小心倾尽并放臵于冰中,加入含PMSF 的RIPA 裂解液200μl于离心管中并移至对应的培养瓶中,摇晃培养瓶使裂解液与贴壁的细胞充分接触,冰上裂解30min 。 D 裂解结束后用细胞刮将贴壁的细胞刮下并转移至1.5 ml EP 管中,再用超声破碎仪破碎细胞后,4℃下12000rpm 离心15min ,吸取上层液体于新的离心管中,弃掉沉淀。收集蛋白样品 (Protein sample preparation) 分多次将细胞收至一个管中
WB免疫印迹实验常见问题全汇总
【干货收藏贴】WB常见问题精品全集锦 做了很久的WB(western blot ),走了很多弯路,但是WE想要做好并不难,总结WB实验中可能会遇到的问题,分析可能的原因及对应的解决方案,这就是实验成功的基石。 以下,我们先解决很多技术菌的疑惑,然后再着手汇总实验中常见问题和可能原因分析以及给出建议解决方案。 WB常见问题分析 1. 为什么我的细胞提取液中没有检测到目的蛋白? 原因有很多: a)细胞中不表达这种蛋白质,换一种细胞; b)细胞中的蛋白质被降解掉了,可加入蛋白酶抑制剂,抑制蛋白酶活性; c)抗体不能识别目标蛋白,多看看说明,是否有问题; d)酶降解可能是没有保持低温操作,样品保存不当,样品放置时间过长。 2. 我做的蛋白质分子量很小(10KDa ),请问怎么做 WB ? a)可以选择PSQ膜,同时缩短转移时间。也可以将两张膜叠在一起,再转移。其他按步骤即可; b)也可选择孔径0.22um的PVDF膜或者NC膜,转膜时间缩短,另外可采用 Tricin e-SDS-PAGE 体系。 3. 我的目的带很弱,如何加强? a)可以加大抗原上样量,这是最主要的; b)也可以将一抗稀释比例降低; c)还可以延长曝光时间。 4. DAB好还是ECL好? DAB有毒,但是比较灵敏,是 HRP最敏感的底物; ECL结果容易控制,但被催化时灵敏度差一点,但如果达到阀值,就特别灵敏,可以 检测pg级抗原。 5. 胶片是一片空白,是怎么回事? 如果能够排除下面的几个问题那么问题多半出现在一抗和抗原制备上。 a)二抗的HRP活性太强,将底物消耗光; b)ECM 底物中H2O2,不稳定,失活; c)ECL底物没覆盖到相应位置; d)一抗选择不当二抗失活; e)二抗失活。 6. 磷酸化抗体的检测样本制备时是否一定要加NaF等?
