实验一_电位滴定法测定食醋中醋酸的含量

实验一电位滴定法测定食醋中醋酸的含量
一、实验目的
1、掌握电位滴定的基本操作和滴定终点的计算方法;
2、学习食用醋中醋酸含量的测定方法;
3、学会电位滴定曲线的绘制,熟练使用pH计。
二、实验原理
1、原理:在酸碱电位滴定过程中,随着滴定剂的
不断加入,被测物与滴定剂发生反应,溶液pH值
不断变化,在化学计量点附近发生pH突跃。因此,
测量溶液pH值的变化就能确定滴定终点。
2、确定终点的方法
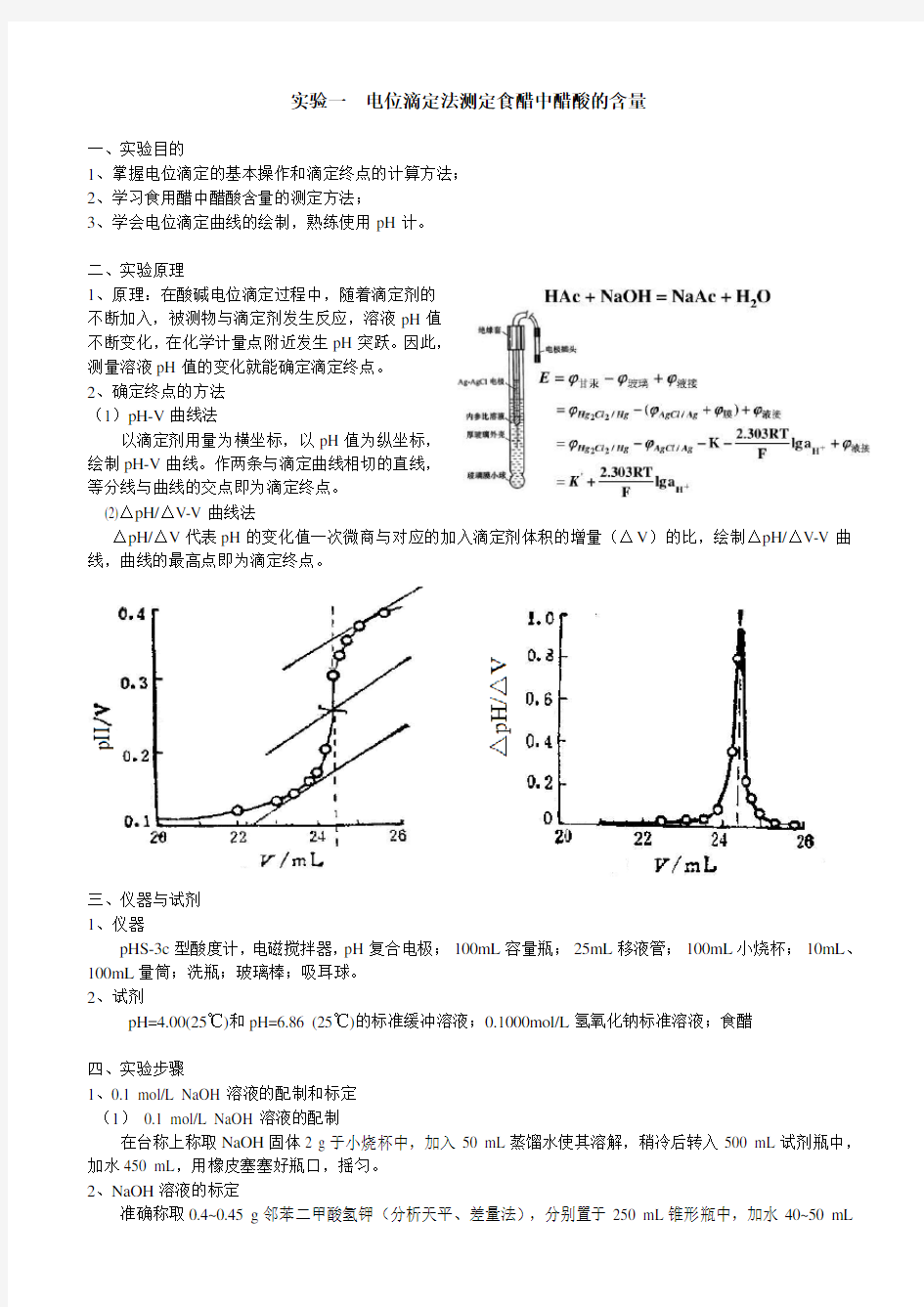
(1)pH-V曲线法
以滴定剂用量为横坐标,以pH值为纵坐标,
绘制pH-V曲线。作两条与滴定曲线相切的直线,
等分线与曲线的交点即为滴定终点。
(2)△pH/△V-V曲线法
△pH/△V代表pH的变化值一次微商与对应的加入滴定剂体积的增量(△V)的比,绘制△pH/△V-V曲线,曲线的最高点即为滴定终点。
三、仪器与试剂
1、仪器
pHS-3c型酸度计,电磁搅拌器,pH复合电极;100mL容量瓶;25mL移液管;100mL小烧杯;10mL、100mL量筒;洗瓶;玻璃棒;吸耳球。
2、试剂
pH=4.00(25℃)和pH=6.86 (25℃)的标准缓冲溶液;0.1000mol/L氢氧化钠标准溶液;食醋
四、实验步骤
1、0.1 mol/L NaOH溶液的配制和标定
(1)0.1 mol/L NaOH溶液的配制
在台称上称取NaOH固体2 g于小烧杯中,加入50 mL蒸馏水使其溶解,稍冷后转入500 mL试剂瓶中,加水450 mL,用橡皮塞塞好瓶口,摇匀。
2、NaOH溶液的标定
准确称取0.4~0.45 g邻苯二甲酸氢钾(分析天平、差量法),分别置于250 mL锥形瓶中,加水40~50 mL
溶解后,用NaOH溶液滴定,记录滴定过程中NaOH体积和对应pH,以此绘制滴定曲线。
3、酸度计的安装与校正
(1)开机预热30min,连接复合电极,安排好滴定管和酸度计的位置
(2)用标准缓冲溶液校准仪器(测定前要开动搅拌器):将搅拌棒放入标准缓冲溶液中,把电极插入溶液中使玻璃球完全浸没在溶液中,开动搅拌器,注意观察磁棒不要碰到电极。
(3)pH6.86标准缓冲溶液定位:先将斜率旋钮顺时针调到最大,调节pH量程至6,按下读数开关,将定位旋钮调至pH至标准缓冲溶液pH值。
(4)pH4.00标准缓冲溶液调斜率:调节pH量程至4,按下读数开关,将斜率旋钮调至pH至标准缓冲溶液pH值。
注意事项:以上校正完成后,定位和斜率旋钮位置不能再变动!在将电极插入待测溶液前,要用蒸馏水冲洗干净,用滤纸吸干水分,再放入溶液中;测定应在搅拌的情况下进行;测定前必须根据测量pH范围选择合适的量程。
4、食醋PH的测定
直接移取20mL食醋于100mL烧杯中,用PH计测定其PH值。
5、电位滴定法测定食醋中醋酸含量
准确移取20.00 mL食醋于100mL容量瓶中定容,再丛中移取15mL于烧杯中,加水35mL后,用NaOH 溶液滴定,记录滴定过程中NaOH体积和对应pH,以此绘制滴定曲线
6、取40—50ml去离子水,进行空白实验。
五、实验记录与处理
1、醋酸的PH值
编号 1 2 3 4 5 6
pH值
2、样品分析
V NaOH/mL pH △pH △V △pH/△V
3、数据处理
(1)绘制pH-V曲线和△pH/△V-V曲线,分别确定滴定终点V。
(2)计算HAc的含量。
六、问题与讨论
1、计算NaOH滴定HAc时化学计量点的电动势,与实验结果比较,是否有差异?其原因是什么?
2、与容量分析法相比较,电位滴定分析法有哪些优缺点?
乙酸的电位滴定分析及其解离常数的测定
实验七乙酸的电位滴定分析及其解离常数的测定 目的要求 1.学习电位滴定的基本原理和操作技术; 2.运用pH- V 曲线和(△pH/△V)-V曲线与二级微商法确定滴定终点; 3.学习滴定弱酸解离常数的方法; 基本原理 乙酸HOAc为一弱酸,其pKa=4.74,当以标准碱溶液滴定乙酸试液时,再化学计量点附近可以观察到pH的突跃。 以玻璃电极和饱和甘汞电极插入试液即组成如下工作电池; Ag,AgCl‖HCl(0.1 mol·L)|玻璃膜|HOAc试液‖KCl(饱和)|Hg2Cl2,Hg 该工作电池的电动势在酸度计上反映出来,并表示为滴定过程中的pH,记录加入标准碱溶液的体积V和相应的被滴定溶液的pH,然后由pH-V曲线或(△pH/△V)-V 曲线求得终点是消耗的标准碱溶液的体积。也可用二级微商法,于△2p H/ △V2处确定终点。根据标准碱溶液的浓度、消耗的体积和试液的体积,即可求得试液中乙酸的浓度和含量。, 根据乙酸的解离平衡 HOAc = H++ OA C- 其解离常数Ka =[H+][OA C-]/[HOAc] 当滴定分数为50%时,[OA C-]= [HOAc]此时 Ka =[H+],即pKa = pH 因此在滴定分数为50%处的pH,即为乙酸的pKa 一仪器 1.酸度计pHS-3C型 2.复合电极 3.容量瓶100mL 4.吸量管5mL、10ml 5. 微量滴定管10ml 二试剂 1. 1.000 mol·L -1草酸标准溶液 2.0.010 mol·L-1 NaOH 标准溶液(浓度已标定) 3.乙酸试液(浓度约1mol·L-1) 三实验步骤 1. 按照仪器操作步骤调试仪器,将选择开关置于pH档。 2. 将pH=4.00 (20℃)的标准缓冲溶液置于100ml小烧杯中,放入搅拌子,并使电极浸入标准缓冲溶液中,开动搅拌器,进行酸度计定位,再以pH=6.88(20℃)的标准缓冲溶液校核,所得读数与测量温度下的缓冲溶液的标准值之差应在-0.005~+0.005单位之内 3. 将待定的乙酸溶液装入微量滴定管中,使液面在0.00ml处。 4. 吸取乙酸试液10.00ml,置于100ml容量瓶中,稀释至刻度,摇匀。吸取稀释后的乙酸溶液10.00ml,置于100ml烧杯中,加水至约30ml。 5. 开动搅拌器,调节至适当的搅拌速度,进行粗测,即测量在加入乙酸溶液0ml、1ml、2ml、···、8ml、9ml、10ml时的各点pH。初步判断发生pH突跃时需要的乙酸体积范围(△V e x) 6. 重复4、5操作,然后进行细测,即在化学计量点附近取较小的等体积增量,以增加测
电位滴定法测定食醋中醋酸的含量
电位滴定法测定食醋中醋酸的含量 一、实验目的 1 通过醋酸的电位滴定,掌握电位滴定的基本操作、PH的变化及指示剂的选择。 2 学习食用醋中醋酸含量的测定方法。 二、实验原理 食用醋的主要酸性物质是醋酸(HAC),此外还含有少量其他的弱酸。醋酸的解离常数Ka=×10-5,用NaOH标准溶液滴定醋酸,化学计量点的PH为,可选用酚酞作指示剂,滴定终点时溶液由无色变为微红色。两者的反应方程式为:HAc + NaOH = NaAc + H2O。然而在本实验滴定过程中,由于食用醋的棕色无法使用合适的指示剂来观察滴定终点,所以它的滴定终点用酸度计来测量。 本实验选用邻苯二甲酸氢钾(KHP)作为基准试剂来标定氢氧化钠溶液的浓度。邻苯二甲酸氢钾纯度高、稳定、不吸水、而且有较大的摩尔质量。标定时可用酚酞作指示剂 三、主要试剂和仪器 1 仪器:pHS-2C型酸度计、天平、电子分析天平、电磁搅拌器、容量瓶(150ml)、锥形瓶(250ml)、吸量管( ,25ml)、碱式滴定管、烧杯(250ml)、量筒(50ml) 2 试剂:NaOH、KHC8H4O4基准物质、食用醋、酚酞、去离子水 四、实验内容和步骤 1 酸度计的安装与校正
(1)开机预热30min,连接复合电极,安排好滴定管和酸度计的位置 (2)用标准缓冲溶液校准仪器(测定前要开动搅拌器):将搅拌棒放入标准缓冲溶液中,把电极插入溶液中使玻璃球完全浸没在溶液中,开动搅拌器,注意观察磁棒不要碰到电极。 (3)标准缓冲溶液定位:先将斜率旋钮顺时针调到最大,调节pHl量程至6,按下读数开关,将定位旋钮调至pH至标准缓冲溶液pH值。 (4)标准缓冲溶液调斜率:调节pH量程至8,按下读数开关,将斜率旋钮调至pH至标准缓冲溶液pH值。 (5)标准缓冲溶液定位:再调节pH量程至6,按下开关读数,将定位旋钮调至pH至标准缓冲溶液pH值。 注意事项:以上校正完成后,定位和斜率旋钮位置不能在变动! ○1在将电极插入待测溶液前,要用蒸馏水冲洗干净,用滤纸吸干水分,再放入溶液中 ○2测定应在搅拌的情况下进行 ○3测定前必须根据测量pH范围选择合适的量程 2 粗配氢氧化钠溶液 用天平称量克氢氧化钠于100ml烧杯中,加蒸馏水溶解,搅拌,可加热加速溶解。等放至室温后转移到带胶塞的试剂瓶中,共加500ml蒸馏水稀释。 3 氢氧化钠的标定(常量法)
食用醋酸总酸量的测定-实验报告模板
山东轻工业学院实验报告 成绩 课程名称基础化学实验1 指导教师实验日期 院(系)专业班级实验地点 学生姓名学号同组人无 实验项目名称食用醋酸总酸量的测定 一、实验目的 1.学习碱溶液浓度的标定方法。 2.进一步练习滴定操作及天平减量法称量。 3.学会用标准溶液来测定未知物含量。 4.熟悉移液管、吸量管和容量瓶的使用,巩固滴定操作。 二、实验原理 1.常用于标定碱的基准物质有邻苯二甲酸氢钾、草酸等。本实验选用邻苯二甲酸氢钾作基准物,其反应为KHC8H4O4+NaOH=KNaC8H4O4+H2O 由于产物是弱碱,可选用酚酞作指示剂。 2.醋酸(CH3COOH,简记为HAc)为一元弱酸,解离常数K a=1.8×10-5,可用NaOH标准溶液直接滴定,滴定时用酚酞作指示剂。食用醋酸中酸的主要成分为醋酸,但也可能含有少量其他的酸,所以测定的是总酸量,测定结果用C HAc(g·L-1)表示。 三、主要试剂 NaOH(AR),邻苯二甲酸氢钾(AR),酚酞指示剂,食用醋酸 四、实验步骤(可用简洁的文字、箭头或框图等表示,自己整理,更富有创意) 1.0.2mol·L-1NaOH溶液浓度的标定 减量法准确称取已烘干的邻苯二甲酸氢钾三份,每份重1~1.5g,分别放入三个已编号的250mL的锥形瓶中,各加水50mL,温热使之溶解,冷却后,加入1~2滴酚酞指示剂,用0.2mol·L-1NaOH溶液滴定至呈现微红色(30s不褪色),即为终点。 2.醋酸总酸量的测定 用一清洁的25mL移液管吸取25.00mL试液于250mL锥形瓶中,加入酚酞指示剂1~2滴,用0.2mol·L-1NaOH溶液滴定至溶液恰好出现微红色,于半分钟内不褪色,即为终点。平行测定3次。根据NaOH标准溶液的浓度和滴定时消耗的体积,计算醋酸中的总酸量。
醋酸的电位滴定
醋酸的电位滴定 一、实验目的 1、掌握电位滴定法操作和确定终点的方法。 2、掌握醋酸电位滴定曲线的绘制及醋酸离解常数pK a 的测定方法。 二、实验原理 复合玻璃电极作为指示电极和参比电极组成原电池,用NaOH 标准溶 液滴定时HAc 溶液,pH 值随加入滴定剂体积的变化而变化;计量点 附近,pH 值突变,以此判断滴定终点。 内差法计算示例: 已知:V NaOH (ml) Δ2pH /ΔV 2 - V 7.95 444 8.00 -548 则:7.9544407.958.00444(548) ep V --=--- V ep = 7.97 ml 三、实验步骤 1、安装好电位滴定装置; 2、用混合磷酸盐调节定位旋钮,用饱和酒石酸氢钾调斜率; 3、精密吸取醋酸溶液10.00 ml ,加水至20 ml ,安装好电极,用NaOH 标准溶液滴定HAc ,记录滴定过程中的V 及对应的pH 值。 四、数据处理要求 电位滴定数据表 () NaOH V mL pH pH ? V ? pH V ?? ()NaOH V mL ()pH V ??? ()V mL 22pH V ?? 2. 作pH-V ,/pH V V ??- ,22/pH V V ??- 图,标出终点; 3.用内插法求出HAc 滴定的终点体积及HAc 的百分含量(g/100 ml ); 4、求HAc 的K a 值。 五、注意事项 1、小心使用玻璃电极,避免碰撞、摩擦,测定溶液时,玻璃球要浸没颈部; 2、更换被测溶液时需冲洗电极并吸干; 3、滴定临近半化学计量点和终点时应小体积滴入; 4、滴定管尖悬挂的滴定剂注意用玻棒引入烧杯中。 六、思考题 p85 1
蟾蜍坐骨神经干动作电位传导速度和兴奋性不应期的测定实验报告
实验二蟾蜍坐骨神经干动作电位传导速度和兴奋性不应期的测定 一、蟾蜍坐骨神经干动作电位引导及传导速度测定 实验目的:加强理解兴奋传导的概念,掌握测定神经干动作电位传导速度的方法。 熟悉仪器设备的操作。 实验原理:通过测出示波器上动作电位传导的距离和传导所需的时间,计算传导速度,可以了解神经的兴奋状态。 1.潜伏期法:测量第一个通道动作电位潜伏期的时间t,输入刺激电极到第一个引导电极间的距离s,v=s/t。 2.潜峰法:测量两个通道的动作电位波峰间的时间差和两对引导电极间的距离,v=(s2-s1)/(t2-t1)。 实验步骤:1.制备坐骨神经-腓神经标本,放入神经屏蔽盒。 2.连接仪器,引导动作电位波形。 3.剪裁编辑图形,计算传导速度。 实验结果:1.(见图) 2.计算 S=10mm,t=0.33ms,v=10mm/0.33ms=33m/s 分析讨论: 1.我们通过对潜伏期法和潜峰法测定结果的比较,结合神经干的特性进行分析:动作电位的起点本质是神经干中传导速度最快的一类神经纤维传导兴奋到达记录点引起的,潜伏期法测量的速度本质是此类神经纤维的传导速度。而潜峰法的形成本质是各种神经纤维兴奋相互叠加后最强的部分。如果采用潜峰法
测量,由于“迁延效应”代表的时间不够准确,不能代表神经干的传导速度,故应该采用潜伏期测量才更准确。 2,.兴奋以局部电流的方式沿着神经干表面传导,兴奋传播过程中造成引导电极下电位改变,故可记录到双相动作电位.通过两对引导电极可观察到兴奋由一对引导电极下传至另一对引导电极下所需时间,根据兴奋传播的距离和所需时间即可计算出传导速度. 实验结论:本实验中测出神经干动作电位的传导速度为33m/s。由实验可知,神经纤维在静息状态下受到有效刺激可产生动作电位,同一条神经干中不同的神经纤维兴奋性不完全相同,且在一次兴奋后兴奋性发生改变,兴奋以一定的速度在神经干表面传导,神经兴奋的传导依赖于神经纤维的完整性。 二、兴奋性不应期的测定 实验目的:了解测定不应期的方法和原理,并加深对兴奋性在兴奋过程中的变化过程的理解。 实验原理:神经纤维受到适宜刺激后,产生兴奋,即动作电位。一次兴奋产生后,必须经绝对不应期、相对不应期、超常期等变化后,兴奋性才能恢复。本实验中先给一个条件刺激,再用另一个检验刺激在兴奋的不同时期给予刺 激,检查神经对检验性刺激反应的兴奋阈值及所引起动作电位的幅度。即可观察到神经组织兴奋性的变化过程。 实验步骤: 1.制备坐骨神经-腓神经标本,并浸在任氏液中,待其兴奋性稳定后实验。 2.连接仪器,设置实验参数,观察并测量神经干的不应期。 实验结果:(见图) 分析讨论:
【免费下载】乙酸的电位滴定分析及其解离常数的测定
[HAc][H +] [Ac -]K a =实验四 乙酸的电位滴定分析及其解离常数的测定 一、目的要求1.学习电位滴定的基本原理及操作技术2.运用pH-V 曲线和(ΔpH-ΔV )-V 曲线与二级微商法确定滴定终点。。3.学习测定弱酸离解常数的方法。二、实验原理乙酸HAc 是一弱酸,其p K a = 4.74,当以标准碱溶液滴定乙酸试液时,在化学计量点附近可以观察到pH 的突跃。以玻璃电极与饱和甘汞电极插入试液即组成如下的工作电池: Ag,AgCl ︱HCl(0.1 mol·L -1)︱玻璃膜︱HAc 试液︱KCl(饱和)︱Hg 2Cl 2,Hg 该工作电池的电动势在酸度计上反映出来,并表示为滴定过程中的pH ,记录加入标准碱溶液的体积V 和相应的被滴定溶液的体积。也可用二级微商法,于Δ2pH-ΔV 2=0处确定 终点。根据标准碱溶液的浓度、消耗的体积和试液的体积,即可求得试液中乙酸的浓度或含量。 根据乙酸的解离平衡:HAc(aq) H +(aq ) + Ac - (aq)其解离常数 当滴定分数为50﹪时,[Ac -] = [HAc],此时K a = [H +],即p K a = pH 因此在滴定分数为50﹪处的pH ,即为乙酸的p K a 。三、仪器和试剂1.酸度计2.玻璃电极3.甘汞电极4.容量瓶 50ml 100ml 5.吸量管6.微量滴定管7.0.1000mol/L 邻苯二甲酸氢钾标准溶液8.0.1mol/LNaOH 9. 0.1mol/LHAc 10. pH=4.00、pH=6.88标准缓冲溶液(20℃) 四、操作步骤1.调试仪器:接通电源,将选择开关置于pH 档,连接好电极,调节温度档于室温。 2.将pH=6.88(20℃)的标准缓冲溶液置于50mL 的烧杯中,放入磁力子,开动搅拌器,
药物分析实验报告
实验四苯甲酸钠的含量测定 一、目的 掌握双相滴定法测定苯甲酸钠含量的原理和操作 二、操作 取本品1.5g,精密称定,置分液漏斗中,加水约25mL,乙醚50mL和甲基橙指示液2滴,用盐酸滴定液(0.5mol/L)滴定,随滴随振摇,至水层显持续橙红色,分取水层,置具塞锥形瓶中,乙醚层用水5mL洗涤,洗涤液并入锥形瓶中,加乙醚20mL,继续用盐酸滴定液(0.5mol/L)滴定,随滴随振摇,至水层显持续橙红色,即得,每1mL的盐酸滴定液(0.5mol/L)相当于72.06mg的C7H5O2Na。 本品按干燥品计算,含C7H5O2Na不得少于99.0% 三、说明 1.苯甲酸钠为有机酸的碱金属盐,显碱性,可用盐酸标准液滴定。 COO Na +H C l COOH +N aC l 在水溶液中滴定时,由于碱性较弱(Pk b=9.80)突跃不明显,故加入和水不相溶混的溶剂乙醚提除反应生成物苯甲酸,使反应定量完成,同时也避免了苯甲酸在瓶中析出影响终点的观察。 2.滴定时应充分振摇,使生成的苯甲酸转入乙醚层。 3.在振摇和分取水层时,应避免样品的损失,滴定前,使用乙醚检查分液漏斗是否严密。 四、思考题 1.乙醚为什么要分两次加入?第一次滴定至水层显持续橙红色时,是否已达终点?为什么? 2.分取水层后乙醚层用5mL水洗涤的目的是什么? 实验五阿司匹林片的分析 一、目的 1.掌握片剂分析的特点及赋形剂的干扰和排除方法。 2.掌握阿司匹林片鉴别、检查、含量测定的原理及方法。 二、操作 [鉴别] 1.取本品的细粉适量(约相当于阿司匹林0.1g),加水10mL煮沸,放冷,加三氯化铁试液1滴,即显紫堇色。 2.取本品的细粉(约相当于阿司匹林0.5g),加碳酸钠试液10mL,振摇后,放置5分钟,滤过,滤液煮沸2分钟,放冷,加过量的稀硫酸,即析出白色沉淀,并发生醋酸的臭气。 [检查] 游离水杨酸 取本品的细粉适量(约相当于阿司匹林0.1g),加无水氯仿3mL,不断搅拌2分钟,用无水氯仿湿润的滤纸滤过,滤渣用无水氯仿洗涤2次,每次1mL,合并滤液和洗液,在室温下通风挥发至干;残渣用无水乙醇4mL溶解后,移至100mL量瓶中,用少量5%乙醇洗涤容器、洗液并入量瓶中,加5%乙醇稀释至刻度,摇匀,分取50mL,立即加新制的稀硫酸铁铵溶液[取盐酸液(1mol/L)1mL,加硫酸铁铵指示液2mL后,再加水适量使成100mL] 1mL,摇匀;30秒钟内如显色,和对照液(精密称取水杨酸0.1g,置1000mL量瓶中,加冰醋酸1mL,
电位滴定法测氯化银的Ksp 备注版
电位滴定法测定AgCl的K sp 一、实验目的 1.掌握电位滴定法测量离子浓度的一般原理; 2.学会用电位滴定法测定难溶盐的溶度积常数。 二、实验原理 当银丝电极插入含有Ag+的溶液时,其电极反应的能斯特响应可表示为: (α代表活度,当溶液浓度很小时可用浓度代替。) 如果与一参比电极组成电池可表示为: (汞活泼性比银大开始时汞会把银离子置换出来所以汞是负极银是正极。Ej表示液体接界电位,一般很小,可以忽略。并且,盐桥是减弱液接电位的有效手段。) 进一步简化为: 式中包括和r(Ag+)常数项。银电极不仅可指示溶液中Ag+的浓度变化,而且也能指示与Ag+反应的阴离子的浓度变化。例如,卤素离子。 本实验利用Cl-与银离子生成沉淀的溶度积K sp非常小,在化学计量点附近发生电位突跃,从而通过测量电池电动势的变化来确定滴定终点。在终点时: 其中X-为Cl-、I-,代入终点时的滴定电池方程: 用该式即可计算出被滴定物质难溶盐的K sp。 通常的电位滴定使用甘汞或AgCl/Ag参比电极,由于它们的盐桥中含有氯离子会渗漏于溶液中,不适合在这个实验中使用,故可选用甘汞双液接硝酸盐盐桥,或硫酸亚汞电极。 注:当盐桥溶液不影响测定的时候选用单盐桥,否则必须选择双盐桥。 外盐桥的作用:(1)防止参比电极内盐桥的物质渗入的待测溶液中干扰测定 (2)防止待测溶液中有害物质进入内盐桥影响其电极电位
三、仪器和药品 仪器:pH/mV计,电磁搅拌器,银电极,双液接饱和甘汞电极,分析天平,容量瓶(250mL,1000mL),烧杯(150mL,250mL) 药品:AgNO3(分析纯,s),KNO3(分析纯,s),KCl(分析纯,s),K2CrO4(分析纯,s),Ba(NO3)2(分析纯,s) 四、实验内容 1.硝酸银标准溶液,0.100mol?L-1 溶解17.00g AgNO3于1000mL去离子水中,将溶液转入棕色试剂瓶中置暗处保存。准确称取1.8638g基准KCl,置于小烧杯中,用去离子水溶解后转入250mL容量瓶中,加水稀释至刻度,摇匀。准确移取25.00mL KCl标准溶液于锥形瓶中,准确移取25.00mL去离子水(加几滴15% K2CrO4和几滴Ba(NO3)2,在不断摇动下,用AgNO3溶液滴定至呈现砖红色即为终点)。根据KCl标准溶液浓度和滴定中所消耗的AgNO3体积(mL),计算AgNO3的浓度。 2.将银电极用蒸馏水冲洗干净,并浸泡在蒸馏水中。烧杯及搅拌磁子都要用清洗干净。 3.根据滴定终点的电动势计算AgCl的K sp。 按图示安装仪器 电位滴定装置 1-银电极;2-双盐桥饱和甘汞电极;3-滴定管;4-滴定池(100mL烧杯);5-搅拌子;6-磁力搅拌器。
实验报告神经干动作电位妇人实验报告_0986文档
2020 实验报告神经干动作电位妇人实验报告_0986文档 EDUCATION WORD
实验报告神经干动作电位妇人实验报告_0986文档 前言语料:温馨提醒,教育,就是实现上述社会功能的最重要的一个独立出来的过程。其目的,就是把之前无数个人有价值的观察、体验、思考中的精华,以浓缩、系统化、易于理解记忆掌握的方式,传递给当下的无数个人,让个人从中获益,丰富自己的人生体验,也支撑整个社会的运作和发展。 本文内容如下:【下载该文档后使用Word打开】 1.捣毁脑脊髓 2.分离坐骨神经 3.安放引导电极 4.安放刺激电极 5.启动试验系统 6.观察记录 7.保存 8.编辑输出 1.观察神经干双相动作电位引导(单通道,单刺激) 如图,观察到一个双相动作电位波形。 2.神经干双相动作电位传导速度测定(双通道,单刺激) (1)选择“神经骨骼肌实验”―“传导速度测定”
(2)改变单刺激强度 (3)传导速度=传导距离(R1--R2-)/传导时间(t2-t1) 如图所示,两个波峰之间的传导时间△t=(t2-t1)=0.66ms 实验中,我们设定在引导电极1和3之间的距离△R=(R1--R2-)=1cm 故传导速度v=△R/△t=1cm/0.66ms=15.2m/s 3.神经干双相动作电位不应期观察 由上图可知,当刺激间隔时间为 4.61ms时,两双相动作电位开始融合,此时为总不应期;当刺激间隔时间为1.05ms时,双相动作电位完全融合,此时为绝对不应期。 故相对不应期=总不应期?C绝对不应期=4.61ms?C1.05ms=3.56ms 4.普鲁卡因对神经冲动传导的阻滞作用 如图所示,在两通道之间滴加普鲁卡因后,两双相电位间的波峰间隔时间为 1.03ms,由引导电极之间的间隔距离1cm,得此时传导速度: V1=1cm/1.03ms=9.71m/s 5.机械损伤对坐骨神经干双向动作电位的影响 由图可知,当剪断两引导电极之间的神经干时,第二通道的双相动作电位消失。故机械损伤对神经动作电位传导的阻滞作用比局麻药强。 6.实验注意事项 a)牛蛙腓肠肌后的神经干分支较难找,可以适当剪开周围软
实验5 电位滴定法测定醋酸的含量
实验5 电位滴定法测定醋酸的含量 一、实验目的 1、熟悉电位滴定的基本原理和操作技术; 2、学习运用二级微商法确定滴定的终点。 二、实验原理 醋酸为有机酸(5108.1-?=a K ),与NaOH 的反应为:O H NaAc NaOH HAc 2+→+。用与已知浓度的NaOH 滴定未知浓度的HAc 溶液在终点时产生pH (或mV )值的突跃,因此根据滴定过程中pH (或mV )值的变化情况来确定滴定的终点,进而求得各组份的含量。 滴定终点可由电位滴定曲线(指示电极电位或该原电池的电动势对滴定剂体积作图)来确定,也可以用二次微商曲线法求得。二次微商曲线法是一种不需绘图,而通过简单计算即可求得滴定的终点,结果比较准确。这种方法是基于在滴定终点时,电位对体积的二次微商值等于零。 例:用下表的一组终点附近的数据,求出滴定终点 滴定剂 的体积 V/mL 电动势 V E △E △V V E ?? 2 2V E ?? 24.10 24.20 24.30 24.40 24.50 24.60 0.183 0.194 0.233 0.316 0.340 0.351 0.011 0.039 0.083 0.024 0.011 0.10 0.10 0.10 0.10 0.10 0.11 0.39 0.83 0.24 0.11 +2.8 +4.4 -5.9 -1.3 表中V V E V E V E ?? ?? ????-??? ????=??12 22 加入△V 为等体积,在接近滴定终点时。 从表中2 2V E ??的数据可知,滴定终点在24.30mL 与24.40mL 之间。 设: (24.30+X )mL 时为滴定的终点 02 2=??V E 即为滴定终点。
醋酸电位滴定的△2pH
-150 -100-50 05010015027.227.4 27.6 27.8 28.0 V/mL △2p H /△V 2 醋酸电位滴定的△2pH/△V 2-V 11 20.00,27.60,0.10()0.1027.60 0.13820.00 HAc NaOH NaOH HAc HAc NaOH NaOH HAc NaOH NaOH NaOH HAc HAc V mL V mL c mol L c V c V n n c V c mol L V --===??=?=??∴= ==? 02468 10120 5 10 1520 25 30 35 V NaOH /mL p H 醋酸电位滴定的pH-V 27.60 024681012141625 26 27 28 2930 △pH/△V V
五、数据记录与处理 1.标准曲线法 序号 1# 2# 3# 4# 5# 6# pF= 6 5 4 3 2 ? -mV 405 355 306 250 196 282 y = 52.3x + 93.2R 2 = 0.9993 150 200250300350 4004501 2 3 4 5 6 7 pF -E /m V 200 3004005006007008009000.0 3.0 6.0 9.012.015.0 V/mL E /m V 11.95 0200400600800 100011.2 11.411.611.812.012.212.412.6 V/mL △E /△V
y = 0.0827x + 0.0025 R 2 = 0.9997 0.00 0.020.040.06 0.080.100 0.2 0.4 0.6 0.8 1 1.2 c Mg /μg?mL -1 A
食醋中醋酸含量的测定
醋酸是一种弱酸,如果用强碱氢氧化钠溶液来滴定,在滴定终点突变点前的pH会维持在4~6之间,因此变色范围在4~6之间的指示剂不适合,例如甲基橙就不适合。应该选择酚酞作为指示剂。 2.实验原理 2 1 食醋中的酸性物质主要是醋酸,可以用酸碱中和反应原理,以已知浓度的氢氧化钠溶液进行中和滴定。反应方程式为:CH3COOH+NaOH=CH3COONa+H2O 2 2 NaOH在称量过程中不可避免地会吸收空气中的二氧化碳,使得配制的NaOH溶液浓度比真实值偏高,最终使实验测定结果偏高,因此,为得到更准确的数据,必须将NaOH 溶液以标准酸溶液邻苯二甲酸氢钾(KHC8H4O4)标定。标定时遵守酸碱中和反应原理,其中参加反应的NaOH与KHC8H4O4的物质的量之比为1∶1。 3.实验用品 31试剂 醋精、糯米甜醋、白醋、陈醋、自制家醋、邻苯二甲酸氢钾、氢氧化钠、活性炭、酚酞。 32仪器 烧杯、容量瓶、玻璃棒、锥形瓶、25mL酸式滴定管、25mL碱式滴定管、漏斗、滤纸、铁架台、托盘天平、25mL移液管、婆梅氏重表、分析天平、洗耳球。 4.实验操作 42食醋的中和滴定 421用移液管准确量取上述滤液各25mL,转移到250mL容量瓶中加蒸馏水到刻度线,配制成稀醋酸溶液。 422将上述各种稀醋酸溶液注入酸式滴定管中并调整液面在“0”刻度线或以下,读取刻度。 423用托盘天平准确称取200g NaOH固体,配制成500mL溶液。 424将上述NaOH溶液注入碱式滴定管中,并调整液面读取刻度。 425根据不同食醋的特点,分别从酸式滴定管中放入约20mL、10mL、5mL溶液于锥形中,滴加2~3滴酚酞指示剂,读取滴定管中刻度。 426左手控制碱式滴定者,右手不断摇晃锥形瓶,当锥形瓶里溶液呈浅红色,且在半分钟内不再褪色,停止滴定,读取滴定管刻度。
实验六 磷酸的电位滴定
实验六磷酸的电位滴定 应化1101 夏海琴2014.11.13 一、实验目的 1. 掌握酸度计测量溶液pH和雷磁ZDJ-4A自动电位滴定仪的操作要点。 2. 了解电位滴定法的基本原理。 3. 学习使用Excel或Origin软件处理NaOH滴定磷酸的数据和绘图。更直观地观察滴定曲线中的两个突跃,学会计算相应的两级解离常数。 4. 掌握用三切线法及一级、二级微商来处理实验数据和分析实验结果。 二、实验原理 电位滴定法是根据滴定过程中,指示电极的电位或pH产生“突变”,从而确定滴定终点的一种分析方法。 在以NaOH滴定H3PO4时,将饱和甘汞电极及玻璃电极插入待测溶液中,使之组成原电池: Ag | AgCl,HCl (0.1 mol/L) | 玻璃膜| 被测试液|| KCl ( >3.5 mol/L),HgCl2 | Hg H+盐桥 玻璃电极甘汞电极 被测试液 由于玻璃薄膜上的阳离子能与溶液中的H+产生离子交换而产生电势,因而称玻璃电极为指示电极,甘汞电极为参比电极,当NaOH溶液不断滴入试液中,溶液H+的活度随着改变,电池的电势也不断变化,可用能斯特(Nernst)公式表示为E电池= ΔEθ– 0.059V lgαH+ 或E电池= ΔEθ + 0.059V pH 此处ΔEθ = Eθ(HgCl2/Hg) - Eθ(AgCl/Ag)。 以滴定体积V NaOH为横坐标,相应的溶液的pH为纵坐标,绘制NaOH滴定H3PO4的滴定曲线,曲线上呈现出两个滴定突跃,以“三切 线法”作图,可以较准确地确定两个突跃范围内各自的滴定 终点,即在滴定曲线两端平坦转折处作AB及CD两条切线, 在“突跃部分”作EF切线与AB、CD两线相交于Q,P两 点,在P、Q两点作PG,QH两条线平行于横坐标。然后在 此两条线之间作垂直线,在垂线一半的J点处,作JJ'线平行 于横坐标,J'点称为拐点,即为滴定终点。此J'点投影于pH 与V坐标上分别得到滴定终点时的pH和滴定剂的体积V,见图8-1。图8-1 三切线法作图 如要求更准确的确定滴定终点,可用一级微商法(d pH/dV-V)和二级微商法(d2pH/dV2-V)。表8-1为数据处理示例。如用三切线法求得第一个终点时,
冰醋酸含量测定报告
冰醋酸含量测定报告 Prepared on 22 November 2020
冰醋酸的成分含量测定方法 实验目的:主要是为了测定供应商提供的冰醋酸的浓度含量是否达到标准要求(CH3COOH%>=98%)。 实验器材:烧杯三个(50ml)锥形瓶两个(带活塞1个)(250ml)酸式滴定管1个100g的精密电子秤一个 .滴管2个 实验原料:100ml的冰醋酸(无色透明液体,具有很强的挥发性,刺激性气味)的氢氧化钠(L的NaoH是无色透明液体,有腐蚀性)酚酞指示剂(主要是为了测 定溶液的碱性)蒸馏水(500ml以上)(注意不能用自来水) 实验原理:主要是通过冰醋酸与氢氧化钠的中和反应,酚酞试剂遇碱变色的原理.往稀释的冰醋酸溶液中滴入的NaOH溶液,直至溶液变成微红色。(通过化学反应, 可知1摩尔的醋酸消耗1摩尔的氢氧化钠。测出消耗多少体积的氢氧化钠, 就可以算出消耗多少摩尔的氢氧化钠,进而计算出消耗多少质量的醋酸,通 过反应消耗醋酸的质量与样品的质量百分比,就求出样品中醋酸的含量百分 比。) 化学反应式: NaOH + CH3COOH = CH3COONa + H2O 计算公式:CH3COOH%={N(NaOH)*V(NaOH)*样品重(g)*1000}*100% 实验步骤:1.先在实验室充分准备好此次实验的器材和实验的原料。(拿一个250ml的锥形瓶(带活塞)到车间的助剂室提取100ml的冰醋酸,并立即盖好塞子。 贴上标签)其他的材料均可在实验室提取。 2. 分别给烧杯编上(1、2、3)号,锥形瓶((装有样品醋酸的为1)、装稀 释的醋酸为2),滴定管(1、2) 3.开电子秤(待电子秤显示数据),接着把烧杯1放到电子称上面称量,调 零。并关闭好各个电子称的各个门。 4.把装有醋酸的锥型瓶半倾,将滴管1伸进醋酸溶液的中间吸取溶液,接着将 滴管1取出,并盖好锥形瓶1瓶子。 5.先打开电子称的顶门,将滴管1伸入电子秤上空中,滴2-3滴()左右的醋 酸溶液,关好电子秤的顶门,待秤上读数稳定,读取读数,并记录读数g。 6.把滴定管放到烧杯2中,迅速打开电子秤的侧门,将烧杯1取出,并用蒸馏 水进行稀释(将蒸馏瓶嘴贴着烧杯1口环绕注入蒸馏水),导入锥形瓶2 中,25ml左右一次,进行四次,共100ml, 7.关闭电子秤,将其他器材与移到滴定管旁边。并在滴定管下方放一张白纸, 防止滴定管漏出的NaOH溶液腐蚀试验台。 8.用滴管2吸取酚酞试剂,往锥形瓶2滴入1—2滴酚酞试剂。 9.倒入适量的氢氧化钠溶液到烧杯3.在将烧杯3的氢氧化钠溶液缓慢的倒入滴 定管中,使得滴定管的液面升到刻度10ml左右。 10.将烧杯3沾取滴定管口溢出的NaOH溶液,读取滴定管的数据,并记录V2. 11.将锥形瓶2放到滴定管的正下方,左手控制滴定管的旋转开关(主要是为 了控制滴定管的滴定速度。)一滴,一滴的放,右手拿着锥形瓶2.晃动锥形
醋酸电离常数的测定实验报告
醋酸电离常数的测定实验报告 篇一:实验四醋酸解离常数的测定 实验四醋酸解离常数的测定 (一) pH法 一. 实验目的 1. 学习溶液的配制方法及有关仪器的使用 2. 学习醋酸解离常数的测定方法 3. 学习酸度计的使用方法二. 实验原理 醋酸(CH3COOH,简写为HAc)是一元弱酸,在水溶液中存在如下解离平衡: HAc(aq) + H2O(l) ? H3O+(aq) + Ac- (aq) 其解离常数的表达式为 [c (H3O+)/cθ][c(Ac-)/ cθ] Kθa HAc(aq) = —————————————c(HAc)/ cθ 若弱酸HAc的初始浓度为C0 mol?L-1,并且忽略水的解离,则平衡时: c(HAc) = (C0 – x)mol?L-1 c (H3O+) = c(Ac-)= x mol?L-1 x Kθa HAc = ———— C0– x 在一定温度下,用pH计测定一系列已知浓度的弱酸溶液的pH。根据PH = -㏒[c (H3O+)/cθ],求出c (H3O+),
即x,代入上式,可求出一系列的Kθa HAc,取其平均值,即为该温度下醋酸的解离常数。 实验所测的4个p Kθa(HAc),由于实验误差可能不完全相同,可用下列方式处理,求p Kθa(HAc)平均和标准偏差s: n ∑ Kθai HAc i=1 θ Ka HAc = ———————— n S = 三.实验内溶(步骤) 1.不同浓度醋酸溶液的配制 2.不同浓度醋酸溶液pH的测定四.数据记录与处理 温度_18_℃ pH计编号____标准醋酸溶液浓度_0.1005_mol?L-1 实验所测的4个p Kθa(HAc),由于实验误差可能不完全相同,可用下列方式处理,求p Kθa(HAc)平均和标准偏差s: n ∑ Kθai HAc i=1 Kθa HAc = ————————
磷酸的电位滴定实验报告doc
磷酸的电位滴定实验报告 篇一:磷酸的电位滴定分析 磷酸的电位滴定分析 一、实验目的 1. 学习电位滴定的基本原理和操作技术 2. 掌握电位滴定确定终点的方法(pH~V曲线、dpH/dV~V 曲线、d2pH/dV2~V曲线制作或 内插法)二、实验原理 1. 磷酸的分步电离 H3PO4 H2PO4- H2PO4- +H+HPO42- +H+PO43- +H+ pKa1=2.12pKa2=7.20pKa3=12.36 HPO42-2. 分步滴定条件 c0Ka1?10?8;Ka1/Ka2?104 3. 电位滴定工作电池 -1 玻璃电极(指示电极) 甘汞电极(参比电极)(pH复合电极:由玻璃电极和参比电极组合而成的电极) 4. 电位滴定确定终点的方法 三、实验内容 1.NaOH溶液的配制与标定 (1)0.1mol·L-1NaOH的配制 1.0gNaOH?溶解????稀释????定容???250mL
(2)NaOH溶液的标定(电位滴定法) 10mLH2C2O4标液(100mL烧杯) ②细测 HO记录V(NaOH)、pH值 2.磷酸试样溶液的测定(电位滴定法) 10mL磷酸试液(100mL烧杯) HO~25mL NaOH滴定搅拌 记录V(NaOH) 、pH值 四、结果计算 1. NaOH溶液浓度标定结果 (1)制作滴定曲线确定终点体积 (2) NaOH浓度计算 滴定反应: H2C2O4+2NaOH=Na2C2O4+2H2O 等物质的量关系:?cV?H2C2O4?n(H2C2O4)?n(2NaOH)? ∴c(NaOH)/mol?L ?1 11 n(NaOH)??cV?NaOH22 ? 2?cV?H2C2O4V(NaOH) 2.磷酸试样溶液分析结果
醋酸含量的测定
醋酸含量的测定 The Standardization Office was revised on the afternoon of December 13, 2020
食醋中醋酸含量的测定 【实验目的】 1. 了解基准物质邻苯二甲酸氢钾()的性质及其应用。 2. 掌握NaOH标准溶液的配制、标定及保存要点。 3. 掌握强碱滴定弱酸的滴定过程、突跃范围及指示剂的选择原理。 【实验用品】 仪器:50mL碱式滴定管,移液管,250mL容量平,250mL锥形瓶,分析天平,托盘天平。 试剂:邻苯二甲酸氢钾(),L ,NaOH溶液,%酚酞指示剂。【实验步骤】 溶液的标定 (1)在电子天平上,用差减法称取三份邻苯二甲酸氢钾基准物分别放入三个250mL锥形瓶中,各加入30-40mL去离子水溶解后,滴加1-2滴%酚酞指示剂。 (2)用待标定的NaOH溶液分别滴定至无色变为微红色,并保持半分钟内不褪色即为终点。 (3)记录滴定前后滴定管中NaOH溶液的体积。计算NaOH溶液的浓度和各次标定结果的相对偏差。 2. 食醋中醋酸含量的测定 (1)用移液管吸取食用醋试液一份,置于250mL容量瓶中,用水稀释至刻度,摇匀。
(2)用移液管吸取稀释后的试液,置于250mL锥形瓶中,加入%酚酞指示剂1-2滴,用NaOH标准溶液滴定,直到加入半滴NaOH标准溶液使试液呈现微红色,并保持半分钟内不褪色即为终点。 (3)重复操作,测定另两份试样,记录滴定前后滴定管中NaOH溶液的体积。测定结果的相对平均偏差应小于。 (4)根据测定结果计算试样中醋酸的含量,以g/L表示。 【实验研讨】 1. 醋酸是一种有机弱酸,其离解常数Ka = ×,可用标准碱溶液直接滴定,反应如下: 化学计量点时反应产物是NaAc,是一种强碱弱酸盐,其溶液pH在左右,酚酞的颜色变化范围是8-10,滴定终点时溶液的pH正处于其内,因此采用酚酞做指示剂,而不用甲基橙和甲基红。 2. 食用醋中的主要成分是醋酸(乙酸),同时也含有少量其他弱酸,如乳酸等。凡是CKa >的一元弱酸,均可被强碱准确滴定。因此在本实验中用NaOH滴定食用醋,测出的是总酸量,测定结果常用: 3. 食用醋中约含3%-5%的醋酸,可适当稀释后再进行滴定。白醋可以直接滴定,一般的食醋由于颜色较深,可用中性活性炭脱色后再行滴定。 4. 是标定NaOH的基准物质,因此称取时要用电子天平,并要用差减法,使其称量结果尽量精确。而称量NaOH就不需要十分准确,用托盘天平即可。
醋酸的电位滴定
醋酸的电位滴定(间接电位法) 专业:能源化学工程年级:2011级姓名:翟裕学号:2011115287 实验时间:2013年11月14号 一.实验原理 等当点时,PH值突跃 二.记录及实验结果 1.实验数据记录 /mL PH ΔPH/ΔV Δ2PH/ΔV2 V NaOH 0.00 3.52 0.109 -0.009 10.00 4.61 0.055 12.00 4.72 0.013 0.093 15.00 5.00 0.043 0.200 17.00 5.40 0.140 0.410 18.00 5.81 0.280 0.620 18.50 6.12 4.93 2.10 18.60 6.33 -12.0 0.90 18.70 6.42 17.0 2.60 18.80 6.68 27.0 5.30 18.90 7.21 6.00 5.90 19.00 7.80 -29.0 3.00 19.10 8.10 -20.0 1.00 19.20 8.20 3.30 1.33 19.30 8.33 -6.30 0.70 19.40 8.40 33.3
4.00 19.50 8.80 -24.0 1.60 19.60 8.96 -3.10 0.825 20.00 9.29 -0.221 0.670 21.00 9.96 -0.380 0.290 22.00 10.25 -0.079 0.133 25.00 10.65 2.拟合滴定曲线 醋酸电位滴定曲线 0.00 2.004.006.008.0010.0012.000.00 5.00 10.0015.0020.0025.0030.00 V/mL P H 3.实验数据处理与分析结果 (1)计算终点时消耗的NaOH 溶液的体积数( V NaOH ) 内插法: ???? ???? ? ? -?-+ =???? ??????? ? ? ?????? ? ? ???2 202222-1 1 21 21p V V pH V pH V H V V V 终点
食醋中总酸量的测定实验报告 (1)
食醋中总酸量的测定 孟娟 2012级化学3班14小组41207149 一、实验目标 1.初步学会用传感器技术测定食醋中的总酸量; 2.会组织中学生用传感器技术测定食醋中的总酸量教学过程。 二、实验原理 1.食醋中的主要成分是醋酸,此外还含有少量的乳酸等有机酸,醋酸是弱酸,用传统的pH试纸或酸度计测定食醋中的总酸量,总是要比实际浓度低,误差很大。本实验将使用传感器技术来测定食醋中的总酸量,该方法不怕待测物中的颜色干扰,测定既快又不用加指示剂。 传感器简介:传感器是一系列根据一定的物理化学原理制成的物理化学量的感应器具,它能把外界环境中的某个物理化学量的变化以电信号的方式输出,再经数据模拟装置转化成数据或图表的形式在数据采集器上显示并储存起来。中学化学教学中进行科学探究常用到的传感器有温度传感器、pH传感器、溶解氧传感器、电导率传感器、光传感器、压力传感器、色度传感器等。传感器技术的特点:便携,实时,准确,综合,直观。 pH传感器是用来检测被测物中氢离子浓度并转换成相应的可用输出信号的传感器,通常由化学部分和信号传输部分构成。pH传感器利用能斯特(NERNST)原理。 待测的食醋中醋酸及其他有机酸可换算为醋酸总量,都可以被标准的强碱NaOH溶液标定: NaOH+CH3COOH=CH3COONa+H2O C待测V待测=C标准V标准 2.当溶液中的电解质含量恒定时,电导率亦恒定,当生成难电离物质时,电导率下降,pH传感器就是把电信号转化为化学信息来测定其中的总酸度的。三、仪器与药品 pH传感器、数据采集器、自动计数器、50mL酸式滴定管、电磁搅拌器、铁架台、250mL烧杯、量筒 有色食醋原液、0.1mol/L NaOH溶液、蒸馏水 四、实验操作过程 1.准备阶段:pH传感器的标定 (1)在采集器3号传感器接口上连接好pH传感器,然后按下采集器电源开
瑞士万通电位滴定仪905-Titrando-操作规程
电位滴定仪905 Titrando 操作规程 一、软件使用简介 瑞士万通tiamo软件操作主要由以下几步: 1、动软件,进入仪器硬件自检程序。 2、确定硬件连接信息、滴定剂信息。 3、操作硬件进入工作状态,使滴定管路充满滴定剂。 4、建立方法并保存。 5、准备样品,调用方法开始实验。 6、查看滴定报告。 二、具体操作 (一)、配置信息设置 1、连接仪器和电脑,接通电源并打开电脑,双击”tiamo”软件图标。 2、程序进入仪器自检程序,稍等几秒,操作界面打开。 3、点击“配置”,操作进入配置界面。 4、双击滴定剂表格,进入滴定剂属性设置页面,需要进行三处设置。 ①溶液标签页:溶液名称。 ②溶液标签页:浓度。 请注意:这里的浓度指的是滴定液的理论浓度!
③滴定度标签页:滴定度。 请注意:这里的滴定度指的是滴定液的实际浓度与其理论浓度的比值。 注意:如果您刚刚更换过滴定液,请将这三处改为新换滴定液的名称、浓度和滴定度。这三处涉及到方法的正确执行以及结果的准 确计算,请认真修改,确保没有错误。 确认无误后,单击下方的“OK”关闭该对话框。 5、在电极信息框内选择实验所连接的电极种类。 6、如果本次实验结果要在下次实验中做为一个常数进行计算,则需要在 公共变量信息框内添加变量信息。 点击“编辑”----“新建”,输入名称和单位,确定后点击“OK”关闭对话框。 (二)、准备仪器工作状态 1、进入人工控制操作页面。 2、点击“准备”仪器进入清洗准备的工作状态,然后按“开始”按 钮,界面跳出一个对话框: 检查滴定头是否放在烧杯里,如果是,则点击“Yes”确认,仪器开 始执行清洗—充液程序。 (三)、编辑方法 1、点击“方法”,进入方法编辑界面。
