高中化学常见离子检验大全

高中化学常见离子检验
大全
Coca-cola standardization office【ZZ5AB-ZZSYT-ZZ2C-ZZ682T-
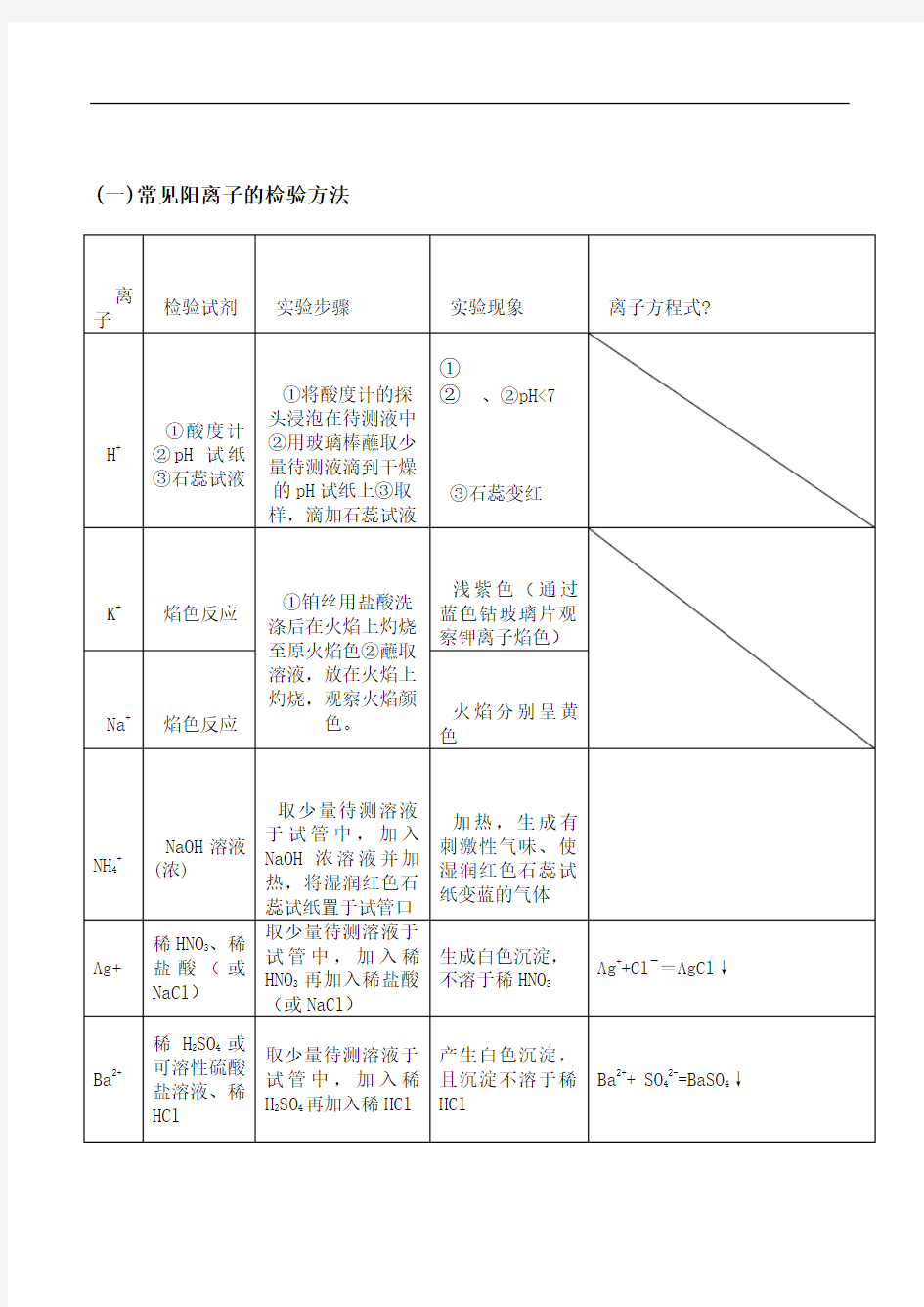
(一)常见阳离子的检验方法
Fe3+KSCN溶液
取少量待测溶液于
试管中,加入KSCN
溶液
变为血红色溶液Fe3++3SCN-=Fe(SCN)3
加苯酚
取少量待测溶液于
试管中,加苯酚
溶液显紫色
6C6H5OH + Fe3+ ?
[Fe(C6H5O)6]3- + 6H+淀粉KI溶
液
滴加淀粉KI溶液溶液显蓝色2Fe3++2I-=2Fe2++ I2
加NaOH溶
液
加NaOH溶产生红褐色沉淀Fe3++3OH-=Fe(OH)3↓
离子检验试剂实验步骤实验现象离子方程式?
Fe2+
①KSCN溶
液,新制的
氯水
取少量待测溶液于
试管中,加入KSCN
溶液,新制的氯水
加入KSCN溶液
不显红色,加入
少量新制的氯水
后,立即显红
色。
2Fe2+ + Cl22Fe3+ + 2Cl-
Fe3++3SCN-=Fe(SCN)3
②NaOH溶
液
取少量待测溶液于
试管中,加入NaOH
溶液并露置在空气
中
开始时生成白色
沉淀,迅速变成
灰绿色,最后变
成红褐色沉淀。
Fe2++2OH - =Fe(OH)2↓
4Fe(OH)2十O2+2H2O=4Fe(OH)3
③酸性高锰
酸钾(无其
它还原性物
质)
取少量待测溶液于
试管中,加入酸性
高锰酸钾溶液
加入酸性高锰酸
钾溶液紫色褪去
5Fe2+ + MnO4-+8H+
5Fe3+ +Mn2++4 H2O
④铁氰化钾
K3[Fe(CN)6]
取少量待测溶液于
试管中,加入铁氰
化钾溶液
产生蓝色沉淀
3 Fe2++2[Fe(CN)6] 3- ═
Fe2 [Fe(CN)6] 3↓
Al3+NaOH溶液取少量待测溶液于
试管中,逐滴加入
NaOH溶液至过量
加入适量NaOH
溶液后生成白色
沉淀,该沉淀溶
于过量NaOH溶
液中
Al3++3OH-=Al(OH)3↓
Al(OH)3+OH-=AlO2-+ 2H2O
Cu2+NaOH溶液取少量待测溶液于
试管中,加入NaOH
溶液
加入适量NaOH
溶液后生成蓝色
沉淀
Cu2++2OH-=Cu(OH)2↓
Mg2+NaOH溶液取少量待测溶液于
试管中,加入NaOH
溶液
加入适量NaOH
溶液后生成白色
沉淀,该沉淀不
溶于过量NaOH
溶液中
Mg2++2OH-=Mg(OH)2↓
(仅用于鉴别Mg2+和Al3+)
(二)常见阴离子的检验方法
注意:
1.若SO
42-与Cl-同时检验,需注意检验顺序。应先用Ba(NO
3
)
2
溶液将SO
4
2-检出,
并滤去BaSO
4,然后再用AgNO
3
检验Cl-。
2.检验SO
32-的试剂中,只能用盐酸,不能用稀硝酸。因为稀硝酸能把SO
3
2-氧化
成SO
4
2-。
3.若Ag+和Ba2+同时检验,也需注意检验顺序,应先用盐酸将Ag+检验出并滤去沉淀,然后再用稀硫酸检验Ba2+。
4.若Ag+和Ba2+同时检验,也需注意检验顺序,应先用盐酸将Ag+检验出
5.若CO
32-和HCO
3
-同时检验,应先用足量的BaCl
2
溶液将CO
3
2-检出,静置,取上层
清夜用Ba(OH)
2或Ca(OH)
2
检出HCO
3
-
