(完整word版)热重分析

第三节 热重分析(TG )
一、基本原理
热重法是在程序控温下,测量物质的质量随温度(或时间)的变化关系的一种技术,简称TG 。如熔融、结晶和玻璃化转变之类的热行为,试样确无质量变化,而分解、升华、还原、解吸附、吸附、蒸发等伴有质量改变的热变化可用TG 来测。如果在程序升温的条件下不断记录试样的重量的变化,即可得到TG 曲线。
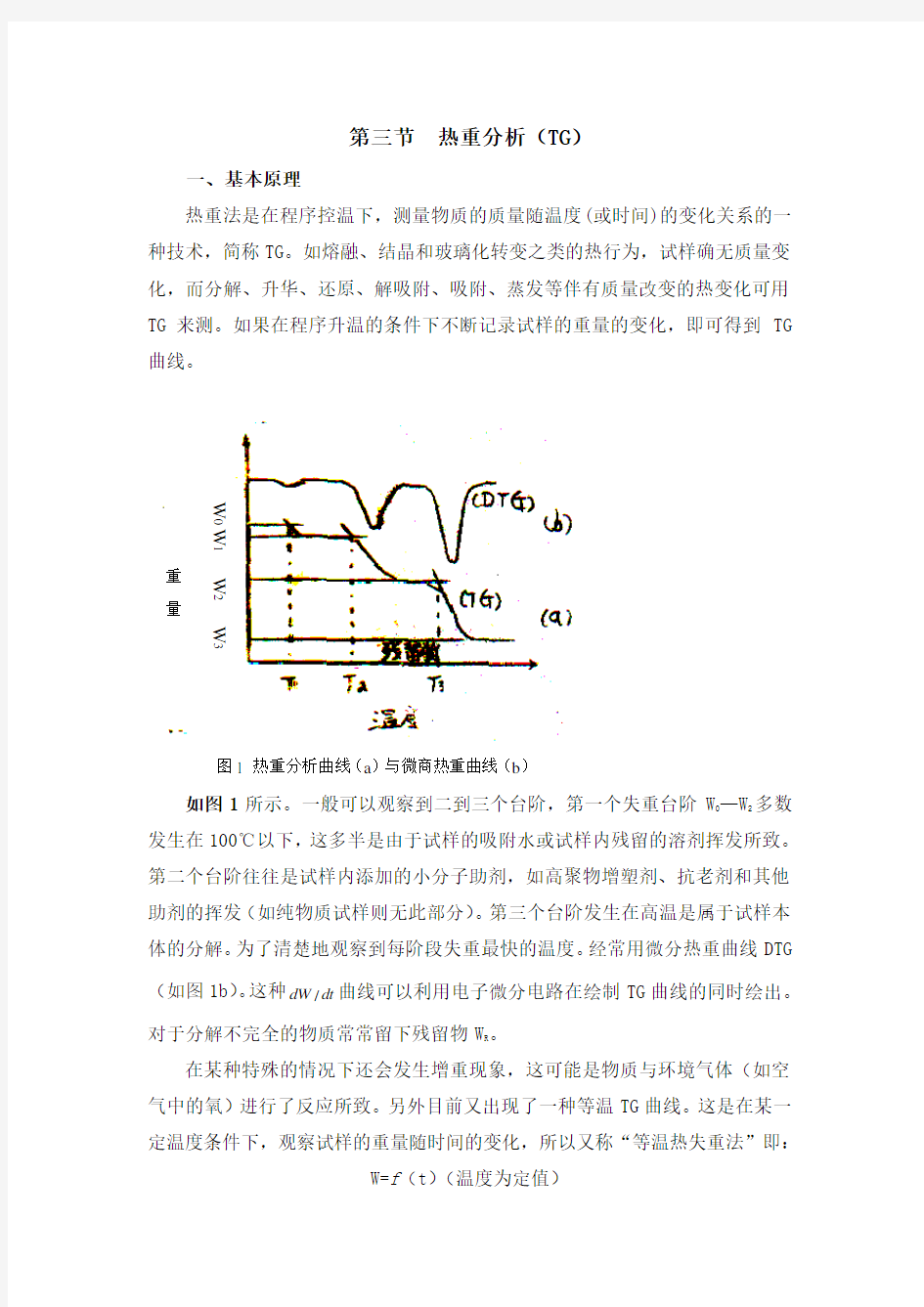
如图1所示。一般可以观察到二到三个台阶,第一个失重台阶W 0—W 2多数
发生在100℃以下,这多半是由于试样的吸附水或试样内残留的溶剂挥发所致。第二个台阶往往是试样内添加的小分子助剂,如高聚物增塑剂、抗老剂和其他助剂的挥发(如纯物质试样则无此部分)。第三个台阶发生在高温是属于试样本体的分解。为了清楚地观察到每阶段失重最快的温度。经常用微分热重曲线DTG (如图1b )。这种/dW dt 曲线可以利用电子微分电路在绘制TG 曲线的同时绘出。对于分解不完全的物质常常留下残留物W R 。
在某种特殊的情况下还会发生增重现象,这可能是物质与环境气体(如空气中的氧)进行了反应所致。另外目前又出现了一种等温TG 曲线。这是在某一定温度条件下,观察试样的重量随时间的变化,所以又称“等温热失重法”即:
W=f (t )(温度为定值)
W 0 W 1 W 2 W 3
重
量
图1 热重分析曲线(a )与微商热重曲线(b )
微量天平
计算机
温度程序器
试样和坩埚
炉子
图2-1 热天平方块图
它能提供很多有用的信息,如在某温度下物体的分解速度或某成分的挥发速度等。
二、基本结构
热重法的仪器称为热天平,给出的曲线为热重曲线。热重曲线以时间t 或炉温T 为横坐标,以试样的质量变化(损失)为纵坐标。热天平的基本单元是微量天平、炉子、温度程序器、气氛控制器以及同时记录这些输出的仪器。热天平的示意图如图2-1所示。通常是先由计算机存储一系列质量和温度与时间关系的数据完成测量后,再由时间转换成
温度。
三、影
响因素
虽然由于技术的进步,在设计TG 仪器时进行了周密的考虑,尽量减少各种因素的影响,但是客观上这些因素还不同程度在存在着,为了数据的可靠性,有必要分述如下:
1.坩埚的影响
坩埚是用来盛装试样的,坩埚具有各种尺寸、形状并由不同材质制成。坩埚和试样间必须无任何化学反应。一般来说坩埚是由铂、铝、石英或陶瓷制成的。石英和陶瓷将与碱性试样反应而改变TG 曲线,聚四氟乙烯在一定条件下与之生成四氟化硅。铂对某些物质有催化作用,而且不适合于含磷、硫和卤素的高聚物。因此坩埚的选择对实验结果尤为重要。
2.挥发物冷凝的影响
样品在升温加热时,分解或升华产生的挥发物可能会产生冷凝的现象,而使实验结果产生偏差。为此试样用量尽可能少,并使气体流量合适。
3.升温速率的影响
由于试样要从外面炉体和容器等传入热量,所以必然形成温差。升温速率过快,有时会掩盖相邻的失重反应,甚至把本来应出现平台的曲线变成折线,同时TG 曲线有向高温推移的现象。但速度太慢又会降低实验效率。一般以5℃/min 为宜,有时需要选择更民的速度。
4.气氛的影响
在静态气氛下,对于可逆的分解反应,升温时,分解速率增大,样品周围的气体浓度增大。随着气体浓度的增大,反应向相反方向进行,正反应的分解速率降低,将严重影响实验结果。实际中通常采用动态气氛以获得重现的结果。
5.样品量的影响
样品量大,对热传导和气体扩散不利。因此在热重分析中,样品用量在满足仪器灵敏度的前提下尽量少。
6.样品粒度的影响
样品粒度对热传、气体扩散影响较大。样品粒度不同,会导致反应速率和TG曲线形状的改变。样品粒度越小,反应速率越快,起始温度和终止温度降低,
图2
反应区间变窄,所以尽量用小颗粒的样品。
四、温度标定
为了消除仪器的测量误差,需对热分析仪进行温度标定。常用于标定的标准物质有磁性物质。
铁磁性材料变成顺磁性,测得的磁力降为零的这一点的温度定义为居里点。当在恒定磁场下加热铁磁性材料通过其居里点时,磁学质量降到零,天平表现出表观质量变化。这种变化用于TG的温度标定。
五、热重分析曲线的处理与计算的国际标准方法(ISO)
由热重法记录的质量变化对温度的关系曲线称为热重曲线(TG),微商热重曲线(DTG)表示质量随时间的变化率。
在TG 曲线中,水平部分表示质量恒定,曲线斜率发生变化部分表示质量变化,如图2中Ⅰ、Ⅱ、Ⅲ段,分别发生了不同的失重反应。DTG 曲线的峰顶,为失重速率的最大值,与TG 曲线的拐点对应。DTG 曲线的峰的数目与TG 线的台阶数相等,峰面积与失重量成正比。
例如:
含水草酸钙分步失重的定量测定:
图2是含水草酸钙CaC 2O 4·H 2O 热失重曲线。此图的三步失重测定值是12%、32%、62%。
理论反应过程如下: 第一步失水:
CaC 2O 4·H 2O= CaC 2O 4+H 2O 失重量(失水)=
224218
100%100%12.3%146
H O CaC O H O
Mr Mr ??=
?= 第二步草酸钙分解: CaC 2O 4=CaCO 3+CO 此步失重量=
24228
100%100%19.2%146
CO CaC O H O
Mr Mr ??=
?= 至此总失重量=12.3%+19.2%=31.5% 第三步碳酸钙分解: CaCO 3=CaO +CO 2↑ 此步失重量=
224244
100%100%30.1%146
CO CaC O H O
Mr Mr ??=
?= 图2
图 3
图4 增重曲线的处理
5
总失重量=12.3%+19.2%+30.1%=61.6% 由此可见,热失重测得的结果七反应过程吻合。 又如
橡胶中炭黑含量的测定:
在橡胶中加入炭黑可提高橡胶制品的拉伸强度等性能。加到橡胶中炭黑的量会影响橡胶制品的物理性质,可作热天平来测定炭黑的含量。
测定方法是:称取数毫克试样,在氮气氛中加热,到600℃左右除炭黑以外的有机物已分解。有机物分解后通入氧气,炭黑燃烧掉,从TG 失重即可测量炭黑的含量。见
图3。
或从理论上来说,热重曲线的分析
可按下列方法进
行:
1.增重曲线如图4所示,增重百分
数为
100m o
G o
W W W W -=
? 式中:W m ——水平线上最大的重量; W 0——原始重量。
2.失重曲线 如图5所示。
B A
L O
W -W W 100W =
? 式中:W B ——损失前试样的重量; W A ——损
失后试样的重量
100m o
G o
W W W W -=
? 1=B1A1W W 100W O
-?
组分2=B2A 2O
W W 100W -?
组
分
残留物=A 2O
W 100W ?
图6 分解温度的定点法
3.分解温度的确定
如图6所示。T 1为分解开始的温度,由曲线的直线部分延长线交点为定点;T 2为分解过程的中间温度,为失重前的水平延线与失重后的水平延线距离的中点线与失重曲线的交点为定点;T 3为分解的最终温度,其定点方法如T 1。
六、应用
7
10
9
1.聚合物热稳定性的评价凭价聚合物热稳定性最简单、方便的方法,是做不同材料的TG 曲线并画在一张图上比较。如图7测定了五种聚合物的热重曲线,由图可知, PMMA 、PE 、PTFE 都可以完全分解,但热稳定性依次增加。PVC 稳定性较差,第一步失重阶段是脱HCl ,发生在200~300℃,脱HCl 后分
子内形成共轭双键,热
稳定性提高(TG 曲线下降缓慢),直至较高温度约420℃时大分子链断裂,形成第
二次失重。PMMA 分解温度低是分子链中叔碳和季碳原子的键易断裂所致,PTFE 是由于链中C-F 键键能大,故热稳定性大大提高。聚酰亚胺PI 由于含有大量的芳杂环结构,需850℃才分解40%左右,热稳定性较强。
图8是六种聚合物在N 2中先快速升至340℃,再以慢速升温得到的TG 曲线,其热稳定性的相对次序:
PMMA 在比较热稳定性时,除了失重的温度外,还需比较失重速率,如比较图9三条TG 曲线,显然c 的热稳定性比a 、b 强,而a 与b 虽然失重的起始温度相同,但a 的斜率大于b ,说明a 的失重速率大于b ,所以a 的 热稳定性最差。 2.组成的剖析 (1)添加剂的分析 TG 用于分析聚合物中各种添加剂和杂质有独到之处,即快速简便。图10 是玻璃钢成分分析 8 曲线,有三个拐点,分别对应失水(100℃附近失水2%),和在400~600℃之间的两步分解(树脂共失重80%),最后不分解的是玻璃,失重率为18%。 图11是用SiO 2和炭黑填充的聚四氟乙烯的TG 曲线,先在N 2中加热至600℃,再切换成空气继续加热到700℃,烧掉炭黑,就能分别对炭黑和SiO 2进行定量。 图12是填充了油和炭黑的乙丙橡胶的TG 和DTG 曲线。首先在N 2中测定乙丙共聚物和油的含量(升温到400℃左右),再切换成空气烧掉炭黑(升温到600℃左右),从而又可获得炭黑的含量和残渣量。 (2)共聚物和共混物的分析 共聚物的热稳定性总是介于两种均聚物热稳定性之间,而且随组成比的变化而变化。如图13所示,为苯乙烯均聚体与α-甲基苯乙烯的共聚物(包括无规和本体共聚)的热稳定的实验。 11 12 结果可以看到,无规共聚物TG 曲线b 介于a 和d 之间,且只有一个分解过程;嵌段共聚物c 曲线也介于a 和d 均聚物之间,但有二个分解过程,因此该热重分析能快速、方便、判断是无规共聚还是嵌段共聚物。 有些共聚物还可以通过TG 曲线获得组成比,如图14是乙烯-乙酸乙烯酯的共聚体TG 曲线,初期失重,是释放乙酸,每摩尔乙酸乙烯酯释放一摩尔乙酸,共聚物中乙酸乙烯酯的含量,可通过下式 求得: 表1 EVA 的TG 和化学分析结果的比较 乙酸乙烯/%(化学分析 ) 乙酸的失重/%(1b) 乙酸乙烯/%(1℃) 绝对偏差 4.3 8.3 11.2 14.9 27.1 31.1 3.2 5.8 7.6 10.2 18.9 21.7 4.6 8.3 10.9 14.6 27.1 31.1 0.3 0.0 O .3 0.3 0.0 0.0 由表1可见,热重分析结果与化学分析结果比较接近,说明热重法是可信的。 从共混物的TG 曲线(图15)可见,各组分的失重温度没有太大变化,各组分失重量是各组分纯物质的失重乘以百分含 量叠加的结果。 13 14 15 3.用热重法研究聚合物固化 对固化过程中失去低分子物的缩聚反应,可用热重法砌究。如图16是酚醛树脂固化TG曲线,在140~240℃一系列等温固化过程中,固化程度随固化温度的提高而增加,而在260℃时固化程度反而下降。这是利用酚醛树脂固化过程中生成水,测定脱水失重量最多的固化温度,其固化程度必然最佳,从而确定240℃为该树脂最佳固化温度。另外还可以从图中看出,不同固化温度的酚醛树脂,相同固化时间,其热稳定性的优劣次序,自上而下热稳定性逐渐提高。 4.用热重法研究聚合物中添加剂的作用 16 (1)聚合物中常用的添加增塑剂,其用量和品种不同,对材料作用效果不同。 图17和图18是测定PVC中邻苯二甲酸二辛酯(DOP)增塑剂的含量,也可以确定PVC的组成比。两种材料虽然同是PVC,但软硬不同,用途不同,增塑剂含量 差别很大,前者为29%后者为8%。 (2)发泡剂的性能和用量直接影响泡沫材料的性能和制造工艺条件。 图19是两种PE泡沫塑料的TG曲线,两种泡沫材料所用发泡剂相同(CBA)但用量不同,分别为5.5%和14.5%。除测定发泡剂含量外,还可以获得适宜的发泡成型温度条 件,图中可见,在200*(2左右的温度是该发泡剂发泡成型的最佳温度。 (3)阻燃剂在聚合物材料中有特殊效果,阻燃剂的种类和用量选择适当,可大大改善聚合物材料的阻燃性能。图13-20是不含和含阻燃剂的聚丙烯TG曲线。加阻燃剂的聚丙烯从分解温度看明显高于不加阻燃剂的,加阻燃剂的PP热稳定性大大提高,而阻燃剂的用量却只有0.5%。 13.3.5研究聚合物的降解反应动力学 13.3.5.1化学反应动力学的基本概念. 化学反应动力学是研究化学反应的速度随时间、浓度、温度变化的关系,最终求出活化能,反应级数并对该反应机理进行解释。 化学反应速度与浓度的关系,即质量作用定律: 口=Kc“ (13.1) 或础:K(1一z)” (13—2)式中K——反应速度常数,它是温度的函数,如果温度不变,K是常数; C——反应物浓度; .17——反应产物浓度; 恕—一是反应级数; 钞——反应速度。 反应速度常数K与温度的关系是阿伦尼鸟斯(Arrhenius)方程: K=Ae—E/RT (13.3) 上式取对数得:. P 1 InK=lnA一嚣‘寺 (13—4)式中E——活化能; A——频率因子; R——气体常数其值为8.31J/kmol。 InK对{作图为一直线,可获得斜率簧,截距lnA,其中E、咒、A称为动力学参数。 另一重要概念在热重法计算时称失重率,即变化率a,以下式表示: Am口。—Am—oo 式中Am。。——最大失质量; Am T(£)时的失质量。 图13.21所示中 Am。m0一优 △优∞。m0一优∞式中m0——初始质量; m是T(£)时的质量; m。。——最终时剩余量,优。。=0叫完全分解。 热分析动力学基本关系式为: 譬=K(1一口)” (13-5] K=Aexp(一E/RT) 华=Ae—E/RT(1一口)” 把升温速率≯:面dT代人上式得到 啬=令e—E/RT(1一扩 把上式变量分离可写成下式 ’不d巧a=拿e—E/RTdT 上面两式是热重动力学微商法和积分法的最基本式,由此出发可以导出各种动力学式。下面介绍几种方法。 13.3.5.2 Newkirk法 它采用一条TG曲线求得分解反应的速率常数,如图13-22所示,失重曲线上点1和点2作切线可得到反应速率面dal和面da2,以及对应样品剩余质量为(1一a1)和(1一口2)。如果是一级反应竹:1,则可以由警=K(1一a)式代人已知值求出各反应速率常数K1,Ka;然后由InK:lnA一吾{式作K的对数与{的图象是一条直线,从斜率和截距可求得E和A。
