高中化学必修一硫教案

一、二氧化硫和三氧化硫
(一)、硫俗称硫磺。
1、硫的物理性质:淡黄色固体,难溶于水,可溶于酒精,易溶于CS2,熔沸点都很低。
用何种方法除去沾在试管上的硫单质?(用CS2洗涤,加热升华法)
2、硫的化学性质
①氧化性:与绝大多数金属反应
Fe+S △
FeS Cu+S
△
Cu2S (与变价金属生成低价金属) 2Na+S==Na2S (研磨并轻微爆炸)
Hg+S==HgS (除去有毒的Hg的方法)
与非金属反应:H2+S △
2S
②还原性:与氧气发生反应S+O2点燃SO2
③自身氧化还原反应3S+6NaOH===2Na2S+Na2SO3 +3H2O
(二) 二氧化硫
1、物理性质:二氧化硫是一种无色、有刺激性气味、有毒、比空气重、容易液化、易溶于水的气体。
2、化学性质
可逆反应:在同一条件
....下,既能向正反应方向进行,同时
..又能向逆反应方向进行的反应,叫可逆反应。
(1) 酸性氧化物------亚硫酐
①二氧化硫与水反应:SO2 + H2OH2SO3(亚硫酸)
②二氧化硫与碱的反应
SO2 + 2 NaOH == Na2SO3 + H2O ;SO2 + NaOH == NaHSO3
[SO2 + 2 NaOH == Na
2SO
3
+ H
2
O;Na
2
SO
3
+ H
2
O + SO2== 2NaHSO
3
]
不能用澄清的石灰水来鉴别SO2 与CO2
③与碱性氧化物反应SO2+CaO==CaSO3
(2) 二氧化硫的氧化性:SO2+2H2S === 3S↓+ 2H2O
(3) 二氧化硫的还原性
①与卤素单质反应:
S O2+B r2+2H2O=H2S O4+2H B r
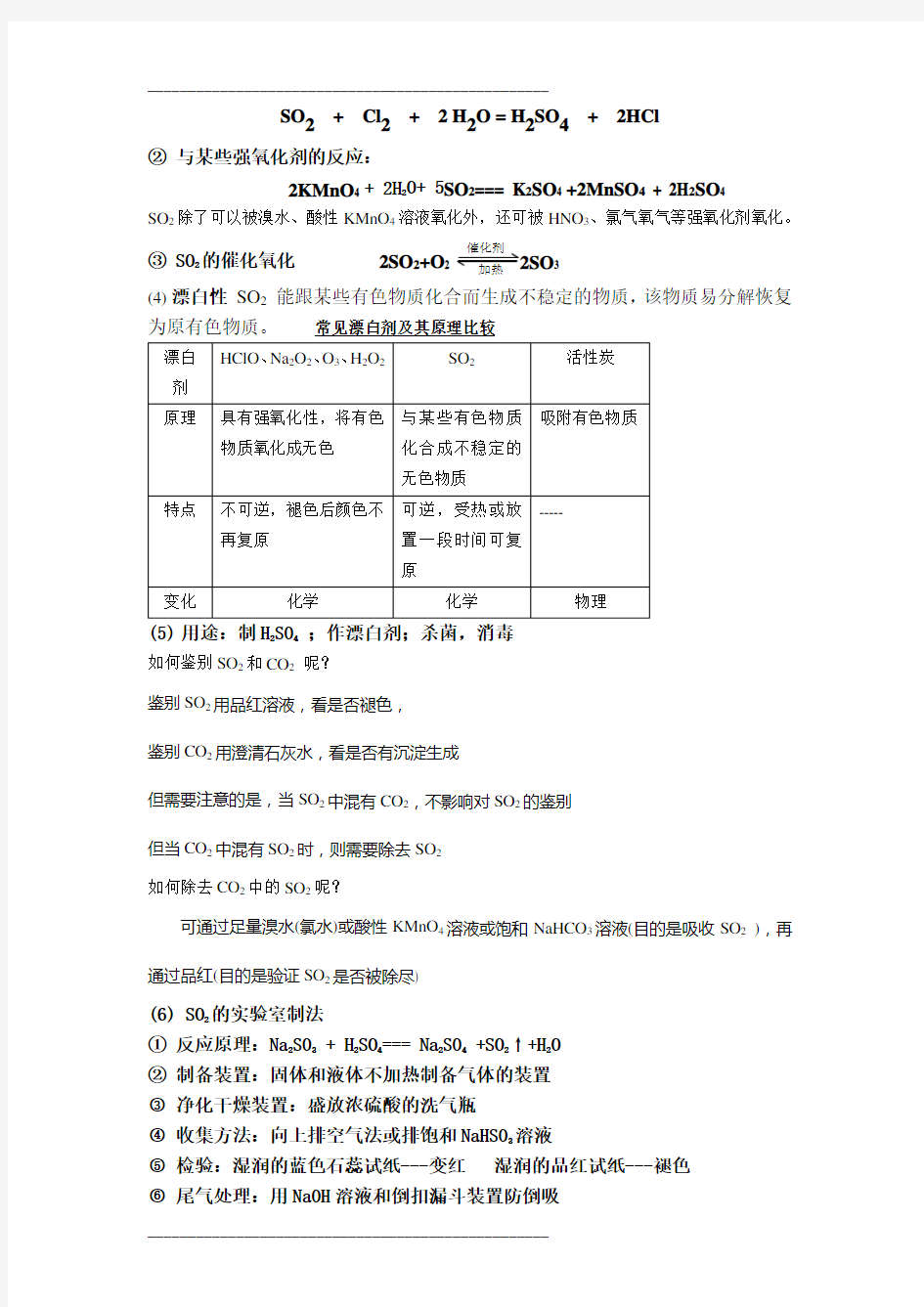
S O2+C l2+2H2O=H2S O4+2H C l
②与某些强氧化剂的反应:
2KMnO4 + 2H2O+ 5SO2=== K2SO4 +2MnSO4 + 2H2SO4
SO2除了可以被溴水、酸性KMnO4溶液氧化外,还可被HNO3、氯气氧气等强氧化剂氧化。
③ SO
2的催化氧化2SO2+O2 催化剂
加热
2SO3
(4)漂白性SO2能跟某些有色物质化合而生成不稳定的物质,该物质易分解恢复为原有色物质。常见漂白剂及其原理比较
(5)用途:制H
2SO
4
;作漂白剂;杀菌,消毒
如何鉴别SO2和CO2呢?
鉴别SO2用品红溶液,看是否褪色,
鉴别CO2用澄清石灰水,看是否有沉淀生成
但需要注意的是,当SO2中混有CO2,不影响对SO2的鉴别
但当CO2中混有SO2时,则需要除去SO2
如何除去CO2中的SO2呢?
可通过足量溴水(氯水)或酸性KMnO4溶液或饱和NaHCO3溶液(目的是吸收SO2),再通过品红(目的是验证SO2是否被除尽)
(6) SO
2
的实验室制法
①反应原理:Na
2SO
3
+ H
2
SO
4
=== Na
2
SO
4
+SO
2
↑+H
2
O
②制备装置:固体和液体不加热制备气体的装置
○3净化干燥装置:盛放浓硫酸的洗气瓶
○4收集方法:向上排空气法或排饱和NaHSO
3
溶液
○5检验:湿润的蓝色石蕊试纸---变红湿润的品红试纸---褪色○6尾气处理:用NaOH溶液和倒扣漏斗装置防倒吸
(7) SO
2
的污染
酸雨:空气中SO
X 和NO
X
随雨水下降成为酸雨,pH<5.6
(三) 三氧化硫
1、物理性质:又名硫酸酐,是一种无色易挥发的晶体,溶沸点都很低。
2、化学性质:具有酸的氧化物的通性,与水反应放出大量的热,具有较强的氧化性。
(1) 与水反应:SO3 + H2O==H2SO4 (放出大量的热)
(2) 与碱性氧化物反应:SO3 + CaO==CaSO4
(3) 与碱反应:SO3 +C a(O H)2 == CaSO4 +H2O
(四) 硫化氢
1、H
2
S的物理性质:
无色、有臭鸡蛋气味的气体,密度比空气大,能溶于水,有剧毒。
2、实验室制法:
由强酸制弱酸的原理
FeS + H
2SO
4
== FeSO
4
+ H
2
S ↑
FeS + 2HCl == FeCl2 + H2S ↑
FeS + 2H+== Fe2++ H2S ↑
要制得干燥的H2S应怎么办?
H2S是酸性、有强还原性的气体,可选用P2O5和中性干燥剂。
用湿润的Pb(CH
3COO)
2
试纸Pb(CH
3
COO)
2
+ H
2
S == PbS↓ + 2CH
3
COOH 试纸变黑
3、化学性质(1) 可燃性
2H
2S + 3O
2
点燃
2H
2
O + 2SO
2
2H
2
S + O
2
点燃
2H
2
O +S
当火焰罩上蒸发皿时,有淡黄色粉末出现时,是由于H2S不完全燃烧生成S之故。
(2)还原性:H2S + X2 ==2HX +S↓(X=Cl、Br、I)
单质氧化性:Cl2>Br2 >I2>S
离子还原性:Cl― (3) 不稳定性:H 2S △ H 2 ↑+S (4) H 2 S气体的水溶液----氢硫酸 氢硫酸是一种易挥发的二元弱酸,其酸性比碳酸还要弱,具有酸的通性。 现有氢硫酸(H2S)、亚硫酸(H2SO3)、亚硫酸钠(Na2SO3)三瓶溶液,它们在空气中易变质。 (1) 分析变质的原因 均有强还原性,能被空气中的氧气氧化。 2H2S+O2==2S↓+2H2O 2H2SO3+ O2==2H2SO4 2Na2SO3 +O2==2Na2SO4 (2) 设计实验证明是否发生变质 H2S :观察是否有浑浊 H2SO3:加BaCl2溶液,是否有白色沉淀 Na2SO3:先加盐酸酸化,再加入BaCl2溶液,看是否有白色沉淀生成 (3) 设计实验证明溶液已完全发生变质 H2S :加入硫酸铜溶液,看是否有黑色沉淀 H2SO3:加入品红溶液,看是否褪色 Na2SO3:加入酸性高锰酸钾溶液,看溶液是否褪色 1 、NO和NO2的生成 N2 + O2放电或高温2NO 2NO + O2== 2NO2 实验室制法:Cu+4HNO3(浓)==Cu(N O3)2+2NO2↑+2H2O 3Cu+8HNO3(稀)==3Cu(NO3)2 +2NO↑+4H2O 2、物理性质: NO是一种无色、无味、难溶于水的有毒气体。 NO2是一种红棕色、有剌激性气味的有毒气体,密度比空气大,易液化,易溶于水 可用什么样的方法收集NO和NO2呢 NO与空气密度相近且与空气中的氧气反应,但NO不溶于水,因此可用排水法收集。NO2溶于水,密度比空气大,故用向上排空气法收集。 3、化学性质 (1)NO与氧气反应:2NO+O2==2NO2 (2) NO2的聚合反应:2NO22O4 NO2在通常状况下,能自身相互结合生成无色的N2O4气体,且在加热时气体颜色加深。NO 仅能与氧气反应,但NO2的N处于中间价态,有弱还原性和强氧化性。NO2具有较强的氧化性,可使湿润的KI淀粉试纸变蓝。 (3) NO2的氧化性:
