杂环化合物和生物碱

13 杂环化合物和生物碱Heterocyclic Compounds and Natural Bases
杂环化合物是由碳原子和非碳原子共同组成环状骨架结构的一类化合物。这些非碳原子统称为杂原子,常见的杂原子为氮、氧、硫等。环状有机化合物中,构成环的原子除碳原子外还含有其它原子,且这种环具有芳香结构,则这种环状化合物叫做杂环化合物。组成杂环的原子,除碳以外的都叫做杂原子。前面学习过的环醚、内酯、内酐和内酰胺等都含有杂原子,但它们容易开环,性质上又与开链化合物相似,所以不把它们放在杂环化合物中讨论。本章将主要讨论的是环系比较稳定、具有一定程度芳香性的杂环化合物,即芳杂环化合物。
杂环化合物种类繁多,在自然界中分布很广。具有生物活性的天然杂环化合物对生物体的生长、发育、遗传和衰亡过程都起着关键性的作用。例如:在动、植物体内起着重要生理作用的血红素、叶绿素、核酸的碱基、中草药的有效成分——生物碱等都是含氮杂环化合物。一部分维生素、抗菌素、植物色素、许多人工合成的药物及合成染料也含有杂环。杂环化合物的应用范围极其广泛,涉及医药、农药、染料、生物膜材料、超导材料、分子器件、贮能材料等,尤其在生物界,杂环化合物随处可见。
13.1 杂环化合物Heterocyclic Compounds
分子中由碳原子和氧、硫、氮等其它原子形成的比较稳定的环状结构的化
合物称为杂环化合物。杂环中除碳原子以外的其它原子称为杂原子。最常见的杂原子有氧、硫、氮等。例如:
S N
H N N
N
O
呋喃噻吩吡咯吡啶嘧啶
furan thiophene pyrrole pyridine pyrimidine
前述章节中,我们遇到的内酯、交酯、内酰胺、内酐、环醚以及环状半缩醛等,虽然也有环状结构,但它们的环容易形成,也容易破裂,其性质与相应的脂肪族化合物相类似,因此不把它们列入杂环化合物之列,本章主要讨论环比较稳定且具有芳香性的杂环化合物。
杂环化合物可以含一个或多个相同的或不相同的杂原子,环的数目也可以是一个或多个。杂环化合物的种类繁多,数量庞大,其数量占已知有机物总数的三分之一左右。杂环化合物在自然界的分布极广,其中很多有重要的生理作用,如血红素、叶绿素、维生素、花色素、抗菌素、核酸、生物碱等都是含有杂环结构的化合物。杂环化合物也是合成许多染料、药物的原料。治疗癌症的一些有效药物也是杂环化合物的衍生物。因此,杂环化合物无论在理论研究或实际应用方面都很重要。
13.1.1杂环化合物的分类Classification of Heterocyclic Compounds
按照杂环的结构,杂环化合物大致可分为单杂环和稠杂环两大类。单杂环中最常见的为五员杂环和六员杂环;稠杂环中普遍存在的是苯环与单杂环稠合和杂环与杂环稠合。根据所含杂原子的种类和数目,单杂环和稠杂环又可分为多种。
常见杂环化合物的分类和名称见表13.1。
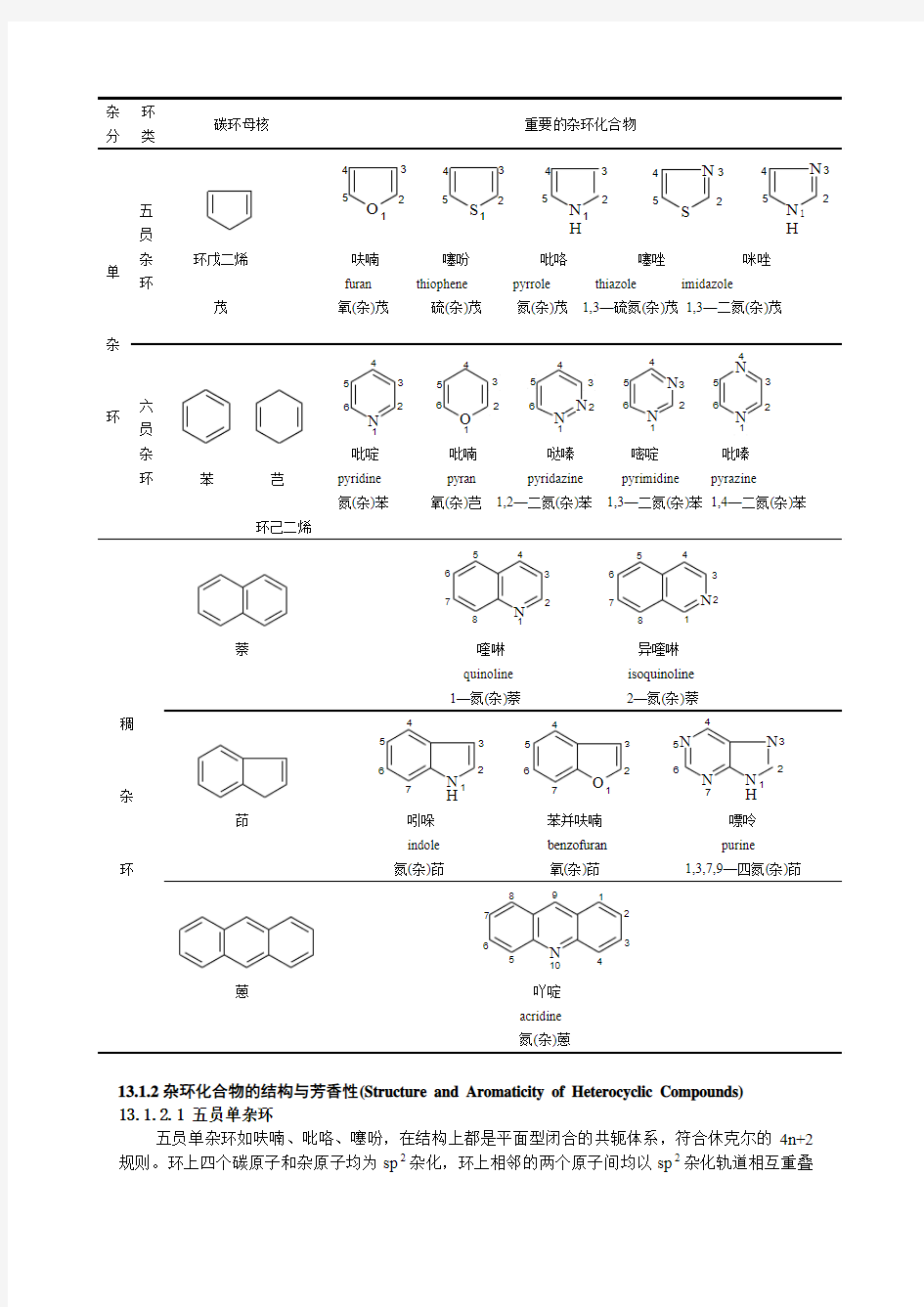
表13.1 常见杂环化合物的结构、分类和名称
杂环
分类
碳环母核重要的杂环化合物
单杂环
五
员
杂
环
环戊二烯
茂
N
N
O S N
N
S1
2
3
4
5
H
1
2
3
4
5
1
2
3
4
5
1
2
3
4
H
2
3
4
5
5
呋喃噻吩吡咯噻唑咪唑
furan thiophene pyrrole thiazole imidazole
氧(杂)茂硫(杂)茂氮(杂)茂1,3—硫氮(杂)茂1,3—二氮(杂)茂
六
员
杂
环
苯芑
环己二烯
N
N
N
11
2
4
1
62
33
4
2
3
5
吡啶吡喃哒嗪嘧啶吡嗪
pyridine pyran pyridazine pyrimidine pyrazine
氮(杂)苯氧(
杂)芑1,2—二氮(杂)苯1,3—二氮(杂)苯1,4—二氮(杂)苯
稠
杂
环
萘
N
N
1
2
3
4
6
5
7
81
2
3
4
6
5
7
8
喹啉异喹啉
quinoline
isoquinoline
1—氮(杂)萘2—氮(杂)萘
茚
O
N
N
N
N
N
H1
2
3
4
5
6
7H1
2
3
4
5
6
7
1
2
3
4
5
6
7
吲哚苯并呋喃嘌呤
indole benzofuran purine
氮(杂)茚
氧(杂)茚1,3,7,9—四氮(杂)茚蒽
N
1
2
3
4
5
6
7
89
10
吖啶
acridine
氮(杂)蒽
13.1.2杂环化合物的结构与芳香性(Structure and Aromaticity of Heterocyclic Compounds)
13.1.2.1 五员单杂环
五员单杂环如呋喃、吡咯、噻吩,在结构上都是平面型闭合的共轭体系,符合休克尔的4n+2规则。环上四个碳原子和杂原子均为sp2杂化,环上相邻的两个原子间均以sp2杂化轨道相互重叠
形成σ键,组成一个五员环状平面结构。环上的每个原子还剩下一个未参与杂化的p 轨道,碳原子的p 轨道各有一个p 电子,而杂原子的p 轨道有两个p 电子,这五个p 轨道都垂直于环的平面,以“肩并肩”的形式重叠形成大π键,组成一个含有五个原子六个π电子的环状闭合共轭体系,符合休克尔规则,具有芳香性,属于芳香杂环化合物。如图13.1所示:
呋喃 吡咯 噻吩
13.1 呋喃、吡咯、噻吩分子中p 轨道重叠示意图
它们分子中键长数据如下:
O N S H
0.144nm
0.135nm 0.137nm
0.143nm
0.137nm 0.138nm 0.142nm
0.137nm 0.171nm
呋喃 吡咯 噻吩
图13.2 呋喃、吡咯、噻吩分子的键长
已知典型的键长数据为:
C -C 0.154nm C -O 0.143nm C -N 0.147nm C -S 0.182nm C =C 0.134nm C =O 0.122nm C =N 0.128nm C =S 0.160nm 由此可见:
① 五员杂环分子中的键长有一定程度的平均化,但不象苯那样完全平均化;此外,由于杂原子的电负性比碳原子大,它们的电子云密度比碳高,即环上电子云分布不象苯环那样完全平均化。因此五员单杂环的芳香性和稳定性比苯差,表现出某些共轭二烯烃的性质,例如能发生加氢反应生成饱和化合物,也可以象共轭二烯烃那样发生Diels-Alder 反应等。五员单杂环的芳香性随着杂原子电负性的增加而减小,由于杂原子的电负性为O>N>S ,所以芳香性的大小次序为苯>噻吩>吡咯>呋喃。
② 五员杂环分子中由于杂原子上的孤电子对参与了环的共轭,这些杂环中的杂原子相当于取代苯中的致活基团,使环上碳原子电子云密度比苯环上碳原子的电子云密度大,所以属富电子杂环,它们在亲电取代反应中的活性比苯大,亲电取代反应的活性次序为吡咯>呋喃>噻吩>苯。在呋喃、吡咯、噻吩的闭合共轭体系中,杂原子的两个α位碳原子上的电子云密度要比两个β位上的相对高些,它们的亲电取代反应主要发生在α位碳原子上。 13.1.2.2 六员单杂环
六员单杂环的典型结构可以吡啶来说明。吡啶的结构与苯很相似,相当于苯中的一个碳原子被氮原子代替,在吡啶分子中,碳原子为sp 2杂化,氮原子为不等性sp 2杂化,氮原子的孤电子对在sp 2杂化轨道上。环上所有原子的p 轨道各有一个电子,所有p 轨道相互平行且垂直于环的平面,形成有六个π电子的环状、平面、闭合的共轭体系,所以吡啶环也有芳香性。
图13.3 吡啶分子中p 轨道重叠示意图
由于吡啶分子中氮原子上的孤电子对不参与共轭,而氮原子的电负性大于碳原子,氮原子类似于苯环上的硝基等吸电子基团,其吸电子的诱导效应使吡啶环中碳原子的电子云密度降低,尤其α、γ位更甚,所以吡啶的亲电取代反应比苯困难,且主要进入β位。但吡啶可以发生亲核取代反应,主要进入α及γ位。
13.1.3杂环化合物的化学性质Chemical Property of Heterocyclic Compounds 13.1.3.1 亲电取代反应
五员杂环属于富电子体系,亲电取代反应容易进行,一般在较缓和的条件下弱的亲电试剂就可以取代环上的氢原子。而六员杂环吡啶是缺电子体系,较难发生亲电取代反应,一般要在较强烈的条件下才能发生反应。
① 卤代反应
五员杂环化合物可以直接发生卤代反应,卤原子主要取代α位上的氢:
O
+Cl 2
O
Cl +HCl
-40o C
吡咯极易发生卤代,如在碱性介质中与碘作用,生成的不是一元产物而是四碘吡咯:
N H
N I
I
I
I
H
+
I 2
Na OH
Na I ++H 2 O
吡啶的卤代反应不但需要催化剂,而且要在较高的温度下才能进行:
N
+Cl 2
N
Cl HCl
+3
100o
C
② 硝化反应
五员杂环的硝化反应一般不用硝酸作硝化剂(吡咯、呋喃在酸性条件下易氧化导致环的破裂或聚合物的生成),而是用温和的硝化剂(乙酰基硝酸酯)在低温下进行:
C +
S
+S
NO 2+CH 3COONO 2CH 3COOH
10C
_(CH 3CO)2O
吡啶的硝化反应要在浓酸和高温条件下才能进行:
N
N
NO 2浓H 2SO
4
。
HNO 3+
H 2O
③ 磺化反应
由于吡咯、呋喃在酸性条件下易氧化导致环的破裂或聚合物的生成,所以不能直接用硫酸进行磺化,一般采用吡啶与三氧化硫的加合物作磺化剂:
O
N SO 3
O
SO 3H
N
+_
噻吩对酸比较稳定,在室温时能与浓硫酸发生磺化反应:
S
S
SO 3
H
H 2SO 4H 2O
+浓 ()
吡啶在催化剂和加热条件下才能发生磺化反应:
N
N
SO 3H
++C
。4
H 2O
H 2SO 4(浓 )
④ 傅-克酰基化反应
五员杂环化合物都可以发生傅-克酰基化反应,而吡啶一般不反应:
O
+O
COCH 3
+CH 3COOH
(CH 3CO)2O
BF 3
13.1.3.2 加成反应
无论是富电子或缺电子的杂环化合物都比苯容易发生加成反应,如它们都可以进行催化氢化反应:
O
O
+H 2
Ni
13.1.3.3 吡咯和吡啶的酸碱性
吡咯由于其氮原子上的孤电子对参与共轭,使氮原子的电子云密度降低,N —H 键的极性增强,所以它的碱性(pKb=13.6)不但比苯胺(pKb=9.4)弱得多,而且显微弱的酸性(pKa=15),能与氢氧化钾作用生成吡咯钾盐:
N N H
+
KOH ( 固 )
K
+_
+
H 2O
吡啶显弱碱性(pKb=8.64),能与各种酸形成盐:
N
N +HCl
HCl
.
13.1.4杂环化合物及其衍生物选述Introduction of Heterocyclic Compounds and their Derivatives
呋喃及其衍生物
呋喃存在于松木焦油中,是无色而有特殊气味的气体。沸点320C ,不溶于水而溶于乙醇、乙醚等有机溶剂。它遇盐酸浸湿的松木片显绿色,被称为松木片反应。用此反应可以检查呋喃的存在。呋喃是有机合成的原料。
① α- 呋喃甲醛
α- 呋喃甲醛(最早是由米糠与稀酸共热制得的,故又称糠醛改为:又称糠醛),通常利用含有多聚戊糖的农副产品如米糠、玉米芯、高梁杆、花生壳等作原料来制取:
O
CHO
稀H ++
OH HO (C 5H 8O 4)n +nH 2H OH
HO HC
CH HC
C
H 3nH 2O
多聚戊糖 戊醛糖 糠醛
纯粹的糠醛是无色而有特殊气味的液体,沸点1620C ,微溶于水,易溶于乙醚和乙醇等有机溶剂。在(空气中改为:光、热及空气中)被氧化聚合(为改为:呈)黄色、棕色以至黑褐色(的物质)。在醋酸存在下与苯胺呈鲜红色反应,可用于糠醛与戊糖的鉴别。
糠醛是一个不含α-氢原子的不饱和醛,化学性质很活泼,容易发生氧化、还原、歧化和聚合等反应,是有机合成工业的重要原料,广泛应用于油漆、树脂、医药和农药等工业。
② 呋喃类药物
呋喃坦丁、呋喃唑酮和呋喃西林是一类5-硝基呋喃甲醛的衍生物。它们都是人工合成的广谱抗菌药物,其结构式如下:
O
O 2N
CH N N
N O
O 2N
CH N N
O
O
O
O
呋喃坦丁
呋喃唑酮
O
O 2N
CH
呋喃西林
呋喃坦丁又名呋喃妥因。它是鲜黄色晶体,味苦,熔点约2580C (分解),难溶于水及有机溶剂,可溶于N ,N-二甲基甲酰胺中。由于它的分子中含有酰亚胺结构,故显弱酸性,能与碱生成盐。它主要用于抑制和杀灭大肠杆菌、金葡萄球菌、化脓性链球菌和伤寒杆菌等,常用于治疗泌尿系统的炎症。
呋喃唑酮又名痢特灵。它是黄色粉末,熔点254~2580C (分解),难溶于水及有机溶剂,呈弱酸性。大肠杆菌、炭疽杆菌、痢疾杆菌和伤寒杆菌等对其最为敏感,故常用于治疗肠道感染和菌痢
等。
呋喃西林又名呋喃新。它是柠檬黄色结晶粉末,难溶于水及醇。主要对葡萄球菌、痢疾杆菌和枯草杆菌等有杀灭和抑制作用。由于它的毒性较大,已很少内服,多作为外用消炎药。
吡咯及其衍生物
N N N
N
2
CH 2H H C
23CH CH 2O O
CH CH 2
CH 2
CH 2
CH 2
COOH
HOOC 卟吩
叶绿素 血红素 (叶绿素a :R 为-CH 3叶绿素b :R 为-CHO)
吡咯存于煤焦油和骨焦油中,是无色油状液体,沸点131℃,难溶于水,易溶于乙醇、乙醚和苯等有机溶剂。在空气中它被逐渐氧化呈褐色并发生树脂化。
吡咯蒸气遇浸过盐酸的松木片显红色,这个特性反应可用来检验吡咯及其低级同系物。 吡咯的衍生物广泛分布在自然界中,其中最重要的是卟啉化合物。这类化合物有一个基本结构称卟吩环,是由四个吡咯和四个次甲基交替相连而成的复杂大环,环上的原子都在一个平面上,形成了共轭体系,具有芳香性。含有卟吩环结构的化合物叫卟啉化合物。重要的天然色素如叶绿素、血红素等都含有卟吩环。
① 叶绿素
叶绿素存在于植物的叶和绿色的茎中。植物在进行光合作用时,通过叶绿素将太阳能转变为化学能而贮藏在形成的有机化合物中。叶绿素在植物内具有重要的生理意义。
叶绿素有多种,量重要的是叶绿素a 和叶绿素b ,可以用色谱法把它们分开。在大多数植物中,它们的比例为3∶1。叶绿素a 比叶绿素b 更为重要。叶绿素a 与叶绿素b 的结构基本相同,只是在Ⅱ环3位上叶绿素a 是甲基(-CH 3),而叶绿素b 则是醛基(-CHO )。
叶绿素a 和叶绿素b 在物理性质方面有所不同,a 是蓝黑色粉末,分子式为C 55H 72O 5N 4Mg ,熔点117~120℃,其乙醇溶液是蓝绿色,并有深红色萤光;叶绿素b 为黄绿色粉末,分子式为C 55H 70O 6N 4Mg ,熔点120~120℃,其乙醇溶液显绿色或黄绿色,有红色萤光。它们都易溶于乙醇、乙醚、丙酮、氯仿等,难溶于石油醚。
叶绿素有旋光性。由于分子中有两个酯键,容易水解生成相应的酸和醇。若用硫酸铜的酸性溶液小心处理叶绿素,则铜可取代镁,其他部分的结构不变,仍显绿色,但比原来的绿色更稳定。因此常用来浸制植物标本。
②血红素
血红素存在于高等动物的体内,是重要的色素之一。它与蛋白质结合形成血红蛋白,存在于红血球中。血红蛋白在高等动物体内起着输送氧气和二氧化碳的作用。
血红蛋白可与氧气配价结合,形成鲜红色的氧合血红蛋白。血红蛋白与氧结合并不稳定,这与氧气的分压有关,因此在缺氧的地方可以放出氧气。由于这一特性,血液可在肺中吸收氧气,由动
脉输送到体内各部分,在体内微血管中,氧的分压低而释放出氧,为组织吸收。一氧化碳与血红蛋白配合的能力比氧大200倍,因此在一氧化碳存在时,血红蛋白失去了输送氧气的能力。这就是一氧化碳使人中毒的原因之一。对血红素的研究使人们对卟吩族色素以及生命现象中最重要的呼吸作用有了进一步的了解。
噻吩的衍生物
生物素和先锋霉素是噻吩的重要衍生物,其结构如下:
O C
CH 2O
CH 3
S
CH 2O C
NH N
S
O
COONa
HOOC(CH 2)
生物素 先锋霉素Ⅰ
生物素又名维生素H ,是人体必须的维生素之一,广泛存在于动植物体内,如谷物、蔬菜和肉类中。生物素是无色针状晶体,熔点232~2330C ,溶于水和乙醇。在中性或酸性条件下稳定,遇强碱或氧化剂易分解。在动物的生理过程中参与CO 2的固定及羧化过程。人体缺乏它会导致身体疲乏,食欲不振,贫血和皮肤发炎、脱屑等。
先锋霉素是由孢头菌素C 合成的一类广谱抗生素。目前人工合成的先锋霉素类药物有十余种,其中先锋霉素Ⅰ又叫头孢金素,是白色结晶粉末,味苦,易溶于水,难溶于有机溶剂。它的抗菌谱广,主要用于对青霉素耐药的金葡萄球菌和一些格兰氏阴性杆菌引起的严重感染,如尿道和肺部的感染、败血症、脑膜炎及腹膜炎等。
咪唑、吡唑和噻唑
咪唑、吡唑和噻唑都有含有两个杂原子的五员环,它们的结构式如下:
N N N N N S
1
2345
H
12
345
H
1
2345
咪唑 吡唑 噻唑
这些杂环化合物与吡咯、吡啶相似,具有闭合的六个π
电子的共轭体系,π电子数符合休克尔规则,都是非苯芳香环。咪唑、吡唑都是无色晶体。咪唑熔点88~89℃,沸点255℃。吡唑熔点70℃,沸点188℃。易溶于水和乙醇。而噻唑是无色液体,沸点117℃。
咪唑和吡唑环上都有两个氮原子,然而只有一个氮原子上有氢,这个氢原子能快速地在两个氮原子之间移动,故有互变异构现象:
N N CH 3
N N
CH 3
N N CH 3
N N
CH 3
12
3
45
H
1
2
3
45
H
12
345
H
1
2
3
4
5H
3―甲基吡唑 5―甲基吡唑 4―甲基咪唑 5―甲基咪唑 在吡唑中3-位和5-位的取代物实际上是一种,在咪唑中4-位和5-位的取代物实际上也是一种。若这两个杂环氮原子上的氢被其它基团取代后,上述互变异构现象就消失了。
下面,就咪唑、吡唑和噻唑三者的酸碱性、环的稳定性及亲电取代反应等三方面作简要介绍。 13.1.4.1 酸碱性
吡唑与吡咯在酸碱性方面比较,有着明显的不同,吡咯显弱酸性,而吡唑则显弱碱性。这是因为在吡唑分子中除含有亚氨基(—NH —)外,还有一个叔胺结构的氮原子(—N==)。咪唑的碱性
(Kb=1.2×10-7)较其同系物吡唑(Kb=3.0×10-
12)为强,吡唑能与硫酸、盐酸、硝酸等反应成盐,但在水中很易水解,而咪唑由于碱性较强,故可生成稳定的盐。咪唑、吡唑与吡咯一样,与氮相连的氢原子可以被钾置换生成钾盐。
噻唑的碱性很弱,水溶液呈中性,与酸作用生成稳定的盐。这是由于氮上未共用电子对能接受质子的缘故。
13.1.4.2 环的稳定性
吡唑、咪唑对酸较稳定,可用硝酸、硫酸进行硝化、磺化。对氧化剂相当稳定,不被高锰酸钾溶液所氧化。环上有支链时可被氧化为羧基而环系不受影响。例如:
N
N CH 3
N
N HOOC
N
N
KMnO 4
N N HOOC
HOOC
H H H
H
噻唑的化学性质比较稳定,在一定条件下,它与酸不起作用,也不受还原剂的影响,在缓和条件下氧化,环系也不受影响,强烈条件下则引起环破裂。
13.1.3.3 取代反应
咪唑、吡唑可以发生硝化、磺化等亲电取代反应,但需较强烈的条件,取代基进入4-位:
N
N N
N C
H 3N N
N
N O 2N
H
H
H
H
噻唑的亲电取代反应更难发生,往往需要在强烈的条件下才能进行。例如:
N S
N
S
3H
以上所述性质说明,吡唑、咪唑有较强的芳香性,这与它们的结构密切相关。这两个环的结构特点是第二个氮原子除以一个π电子参与环的共轭体系外,尚有一对未共用电子对,所以较易和质子结合成盐,具弱碱性;同时该氮原子的存在,通过吸电子的诱导效应降低了环上的电子云密度,使环较稳定,以致亲电取代需要较强烈的反应条件。噻唑的芳香性也比呋喃、噻吩强,环上增加一个电负性较强的氮原子,有助于环的稳定。
吡啶及其衍生物
吡啶最初发现于骨焦油中,在煤焦油中含量较多。它是具有特殊臭味的无色液体,沸点115.3℃。能与水混溶,又能溶于乙醇、乙醚、苯、石油醚等许多极性或非极性有机溶剂中,并能溶解氯化铜、氯化锌、氯化汞、硝酸银等许多无机盐。吡啶是一种叔胺,显弱碱性。工业上用稀硫酸提取煤焦油的轻馏分,然后用氢氧化钠中和,使吡啶等碱性物质游离,再进行分馏提纯。吡啶是良好的溶剂,又是合成某些杂环化合物的原料。
吡啶的衍生物在自然界中分布广泛,如维生素PP 、维生素B 、辅酶I 及辅酶Ⅱ等都含有吡啶环。
① 维生素PP
维生素PP 是属B 族维生素,包括β-吡啶甲酸及β-吡啶甲酰胺两种。结构如下:
N
COOH
N
CONH 2
β-吡啶甲酸(烟酸,尼克酸) β-吡啶甲酰胺(烟酰胺)
熔点 230~237℃ 熔点 128~131℃
二者的生理作用相同,参与生物机体的氧化还原过程,促进组织代谢,能降低血液中胆固醇的含量。维生素PP 也叫抗癞皮维生素,因为体内缺乏它时会引起癞皮病。
二者都是白色结晶,对酸、碱等都比较稳定。β-吡啶甲酰胺加氢氧化钠液液与之共煮,则产生氨气,而β-吡啶甲酸无此反应。
维生素PP 存在于肝脏、肉类、谷物、米糠、花生、酵母、蛋黄、鱼、蕃茄等内,现在多用合成品。
维生素B 6 维生素B 6也是吡啶的衍生物,它由下列三种物质组成:
N
CH 2OH CH 2OH
O
H C H 3N
CH 2OH
O
H C
H 3CHO
N
CH 2OH O
H C
H 3CH 2NH 2
吡哆醇 吡哆醛 吡哆酸
维生素B 6存于蔬菜、鱼、肉、蛋类、豆类、谷物等中。为白色结晶,溶于水及乙醇。耐热,在酸和碱中较稳定,但易被光所破坏。动物机体中缺乏维生素B 6时,蛋白质代谢就不能正常进行。
嘧啶及其衍生物 嘧啶又称1,3-二氮苯,无色晶体,熔点22℃,沸点124℃,易溶于水,它的碱性比吡啶还弱。
由于氮原子具有吸电子效应,能使另一个氮原子上的电子云密度降低,因此碱性也随之减弱(即结合质子的能力减弱)。亲电取代反应比吡啶困难,而亲核取代反应则比吡啶容易。能分别与酸或碱形成盐。
嘧啶很少存于自然界中,但它的重要衍生物胞嘧啶、尿嘧啶和胸腺嘧啶普遍存在于动植物中,都是核酸的组成部分。这三种嘧啶都存在烯醇式和酮式的互变异构现象:
N
N OH
NH 2
N N
NH 2
O
H
胞嘧啶(4―氨基―2―羟基嘧啶),Cytosine 简写为C
N
N OH
OH N N O
O H
H
尿嘧啶(2,4―二羟基嘧啶),Uracil 简写为U
N N
OH
C
H 3N N O
O
C
H 3H H
胸腺嘧啶(5―甲基―2,4―二羟基嘧啶),Thymine 简写为T 在生物体中哪一种异构体占优势主要取决于体系的pH 值。在生物体中嘧啶碱主要以酮式异构体存在。
维生素B 1又名硫胺素。它存在于米糠、麸皮、酵母、花生和豆类中。药用硫胺素是其盐酸盐,结构式为:
N N
C
H 3CH 2NH 2
N S
CH 3
CH 2CH 2OH
+
Cl
盐酸硫胺素是白色晶体,味微苦,熔点248℃(分解),易溶于水,对酸稳定,热或碱能使其分解。维生素B 1能维持心脏、神经和消化糸统的正常功能,能促进碳水化合物代谢。缺乏维生素B 1能导致脚气病、多发性神经炎、食欲不振和消化不良等。
7.嘌呤及其衍生物
嘌呤是嘧啶和咪唑稠合而成的化合物,又名1,3,7,9-四氮茚。嘌呤有两种互变异构体:
N
N N N
N
N
N N
H
13
4
65
78
9H
9-氢嘌呤 7-氢嘌呤
嘌呤为无色晶体,熔点216℃,易溶于水,溶液呈中性,但它却能与酸或碱作用生成盐。嘌呤本身很少存于自然界中,可它的羟基和氨基衍生物却广泛存在。其衍生物重要的有黄嘌呤和尿酸,它们存在于有机体中,并且有显著的生理作用。
嘌呤衍生物中还有腺嘌呤和鸟嘌呤,它们也是核酸的组成部分。鸟嘌呤又称2-氨基-6-羟基嘌呤,也存在着烯醇式和酮式两种互变异构体。
N
N N N
NH 2
N
N N
N
OH
N
H 2N
N N N
N
H 2O
H H H
腺嘌呤(6-氨基嘌呤) 鸟嘌呤(2-氨基-6-羟基嘌呤) Adenine ,简写为A Guanine ,简写为G
吲哚及其衍生物, 吲哚存在于煤焦油中,某些植物的花中也含有吲哚,蛋白质腐烂时生成吲哚和β-甲基吲哚,因此它们存在于粪便中。粪便的恶臭就是由于它们的存在而产生。但吲哚的稀溶液很香,是化妆品常用的香料。
N N CH 3
H
H
吲哚 β-甲基吲哚
吲哚是苯环和吡咯环稠合而成的杂环化合物,具有闭合的共轭体系。它是一种无色片状结晶,熔点为52℃,沸点254℃,微溶于冷水而溶于有机溶剂和热水中。化学性质与吡咯相似,但稍比吡咯的化学稳定性强,与温和的氧化剂不发生作用,而高锰酸钾可以引起环系破裂。吲哚碱性极弱,在空气中颜色变深,并逐渐变成树脂状物质。它很容易发生亲电取代反应,但只得到β-取代物。松木片反应呈红色。
吲哚的衍生物在自然界中分布很广,例如β-吲哚乙酸、色氨酸、5-羟色胺、靛蓝等。β-吲哚乙酸是一种植物生长调节剂,用来刺激植物的插枝生长及促进无子果实的形成;色氨酸是蛋白质的组分;5-羟色胺存在于人和哺乳动物的脑中,是保持思维正常活动不可缺少的物质;靛蓝是人类最早使用的天然染料之一。
N CH 2COOH N CH 2COOH
CH NH 2
2CH 2NH 2
H H
H
β-吲哚乙酸 色氨酸 5-羟色胺
N O N O
H
H C C
靛蓝
.苯并吡喃及其衍生物
苯并吡喃是苯环与吡喃环稠合而成的杂环化合物,广泛存在于天然产物中。许多天然色素是它的衍生物,有些中草药的有效成份以它为基本结构。
O
O
1
2
3
4
657
8
1
2
3
4
65
7
8
苯并吡喃 2-苯基苯并吡喃(花色素母体)
*(1)花色素
植物的花果之所以具有五颜六色,主要是由花色素引起的。花色素常与糖结合成苷,这种苷称为花色苷。花色苷与酸一起加热时,水解而生成糖和花色素的钅羊 盐。研究各种植物中的花色素后发现,花色素具有2-苯基苯并吡喃的骨架,在3-,5-,7-,3′-、4′-、5′-等处常带有羟基,由于苯环上羟基的位置与数目以及与之成苷的糖不同,形成不同的花色苷。植物界最常见的是天竺葵素、青芙蓉素、飞燕草素三种,它们在苯环上的羟基数目不同。
O OH OH
O H OH
Cl
O OH OH O
H OH
OH Cl
O OH
OH
O
H OH OH
OH Cl
+++
氯化天竺葵素 氯化青芙蓉素 氯化飞燕草素
花色苷的一种极为有趣的现象是颜色与介质的pH 值密切相关。同一种花色苷,在不同的PH 值中能显示不同颜色。例如青芙蓉素二葡萄糖苷在pH7~8时呈淡紫色,当pH <3时呈红色,pH >11时则呈蓝色。故同一种花由于种植的土壤酸碱性不同,或是同一种花由于本身的汁液不同,而呈现不同的颜色。
O
O
O
O
OH
OH
C 6H 11O 5
C 6H 11O 5
O
O O
O
H OH
C 6H 11O 5
C 6H 11O 5
O O
O
O O
H O
C 6H 11O 5
C 6H 11O 5
O +(淡紫色)
(红色)
(蓝色)
pH7~8pH>11pH<3
黄酮色素 苯并-γ-吡喃酮又称色酮,为白色固体。2-苯基苯并-γ-吡喃酮则称为黄酮,是黄酮素母体。
O O O
O
O
O
γ-吡喃酮 色酮 黄酮
黄酮的多羟衍生物统称黄酮色素,是存在于植物的根、茎、叶和花中的黄色或棕色色素,例如茶树等植物中的槲皮素,就是黄酮的五羟基衍生物。黄酮素的许多衍生物都可以入药,如董苓背有镇静解热作用,杜鹊素(二氢黄酮衍生物)是治疗老年慢性支气管炎的中草药。
喹啉 喹啉是苯环与吡啶环稠合而成的化合物,存在于煤焦油中,也可用合成方法制得,有些生物碱中也含有喹啉环。
喹啉为无色油状液体,放置一段时间逐渐变黄色。沸点238℃,熔点-15℃,易与水蒸气一同挥发,具有特殊气味。微溶于水,易溶于乙醇、乙醚、氯仿等有机溶剂。是一种高沸点溶剂。
喹啉具有闭合的共轭体系,由于氮原子上还有一对P 电子未参与环上共轭体系,所以喹啉与吡啶相似,具有弱碱性,但碱性比吡啶弱。它可以与无机酸成盐,也可以与碘甲烷生成季铵盐。
喹啉环中含有氮原子的吡啶环,电子云密度低于相并联的苯环,因此喹啉发生亲电取代时,反应
在苯环的5-位或8-位上进行:
N
N NO 2
N
NO 2
N Br
N
Br
N
SO 3H
N
SO 3
H
1
4
657
8
+
+
+
但是,当喹啉进行亲核取代反应时,取代基则进入含氮原子的吡啶环的邻位或对位(2-位或4
-位):
N
N
NH 2
NaNH 2
二甲苯100。
C
当喹啉被高锰酸钾氧化时,因苯环破裂而生成2,3—吡啶二甲酸。若强热此二元羧酸则脱羧生成烟酸:
N
N
COOH COOH
N
COOH KMnO 4+H 2SO 4
200。C 300。
C ~
喹啉 2,3—吡啶二甲酸 烟酸
喹啉与还原剂(锡和盐酸、钠和乙醇等)作用或催化加氢可生成四氢喹啉(吡啶环还原),它是比喹啉更强的碱,具有芳香仲胺的性质。如在更强烈的条件下(铂催化加氢或氢碘酸等)苯环可再加氢,生成强碱性的十氢喹啉:
N
N H N H
Na C 2H 5OH
,H 2
喹啉用于制造药物、染料和试剂,还用于保护解剖标本等。喹啉可以用合成法制取:
NH 2
CH 2CH 2CH 2OH
OH OH
N
+
13.2 生物碱( Natural Base)
13.2.1 生物碱概述(Introduction of Natural Bases)
生物碱是指一类含氮的碱性有机化合物。由于是从生物体(主要是植物)内取得,所以称为生物碱。它们多是含氮杂环衍生物,但也有少数非杂环的生物碱。
生物碱在植物界分布很广,动物体中的含量则很少。不同的植物所含生物碱差异也很大。在双子叶植物的罂粟科、茄科、毛艮科、豆科中含量比较丰富,而在裸子植物、蔷薇植物、隐花植物中的含量则极少。生物碱大都与有机酸(苹果酸、柠檬酸、草酸、琥珀酸、醋酸、乳酸等)或无机酸(磷酸、硫酸、盐酸)结合成盐存在于植物体内,但也有少数以游离碱、苷或酯的形式存在。
生物碱对植物本身有什么作用当前还不清楚,但许多生物碱对人和动物有强烈的生理作用。例如当归、甘草、贝母、黄麻、黄连等许多药物中的有效成份都是生物碱。
有关生物碱的研究已有约两个世纪的历史,并从各种植物中分离提取了几千个品种,且大多数生物碱的结构已经测定,并用人工合成加以证实。目前,中草药的研究和生物碱的研究正相得益彰,既促进了中药的发展,又促进了有机合成药物的发展,为生命科学开拓了广阔的前景。
13.2.2 生物碱的一般性质(General Properties of Natural Bases)
1.生物碱的物理性质
生物碱大多数是无色结晶固体,少数为非结晶体和液体。一般都有苦味,有些极苦而辛辣,还有些能刺激唇舌,使之有焦灼感。大多数生物碱分子中含有手性碳原子,具有旋光性;不溶或难溶于水,能溶于乙醇、乙醚、丙酮、氯仿和苯等有机溶剂中。但也有例外,如黄麻碱、烟碱、咖啡因等可溶于水。
2.生物碱的化学性质
生物碱一般呈碱性,能与无机酸或有机酸结合成盐,这种盐一般易溶于水。
(1)生物碱的沉淀反应
一般生物碱的中性或酸性水溶液均可与数种或某种沉淀试剂反应,生成沉淀。沉淀试剂的种类很多,大多数为重金属盐类或分子较大的复盐,例如碘化汞钾(K2HgI4)、碘化铋钾(BiI3·KI)、磷钨酸(H3PO4·12WO3·2H2O)、磷钼酸(Na3PO4·12MoO3)、硅钨酸(12WO3·SiO2·4H2O)、碘-碘化钾、鞣酸、氯化汞(HgCl2)、10%苦味酸、AuC13盐酸溶液、PtC14盐酸溶液等,其中最灵敏的是碘化汞钾和碘化铋钾。
利用生物碱的沉淀反应,可以检验生物碱的存在。
(2)生物碱的颜色反应
生物碱还可以和生物碱显色剂发生显色反应。显色剂的种类也很多,随生物碱的结构不同而有所区别。常用的显色剂有:钒酸-硫酸试剂、钼酸-硫酸试剂、甲醛-硫酸试剂、钼酸钾、纯硝酸、浓盐酸和氯化镁等。
13.2.3 生物碱的一般提取方法
(General Extraction Methods of Natural Bases)
从植物中提取生物碱,一般有下面三种方法:
1.加酸-碱提取法
首先将含有较丰富生物碱的植物用水清洗干净,沥干研碎,再用适量的稀盐酸或稀硫酸处理,使生物碱成为无机酸盐而溶于水中,然后往此溶液中加入适量的氢氧化钠使生物碱游离出来,最后用有机溶剂萃取游离的生物碱,蒸去有机溶剂便可得到较纯的生物碱。
2.加碱提取法
在某些情况下,可把研碎的植物直接用氢氧化钠处理,使原来与生物碱结合的有机酸与加入的氢氧化钠作用,生物碱就会游离出来,最后用溶剂萃取。
3.蒸馏法
有些生物碱(如烟碱)可随水蒸气挥发,则可用水蒸气蒸馏法提取。 13.2.4 个别化合物(Some Natural Bases)
*1.烟碱
烟碱又称尼古丁(Nicotine),是烟草所含的十二种生物碱中含量最多的一种(生烟叶含量为2-8%)。它在烟叶中以苹果酸盐或拧橡酸盐的形式存在。烟碱由吡啶环与四氢吡咯环所组成:
CH 3
N-甲基-2-(3-吡啶基)四氢吡咯
烟碱是无色油状液体,味辛辣,沸点247℃,呈左旋性。能溶于水、乙醇、乙醚等溶剂。能随水蒸气挥发而不分解。
强氧化剂(HNO 3)与烟碱作用,其分子中的四氢吡咯环被破坏,生成烟酸:
N
3
COOH
烟碱 烟酸
烟碱有剧毒,它能引起头痛、呕吐、吸入量达4O 毫克能致死。可用作农用杀虫剂。 2.麻黄碱
麻黄碱(麻黄素)存在于中草药麻黄中。在结构上它是一个非杂环生物碱,也是芳香族的醇胺,学名为1-苯基-2-甲氨基-1-丙醇。
C*
C*
H H CH 3
NH CH 3
分子中含有两个不同的手性碳原子,有两对对映异构体,其中左旋麻黄碱有生理作用。 麻黄碱是无色晶体,熔点38.1℃,易溶于水、乙醇,可溶于氯仿、乙醚、苯和甲苯中。麻黄碱可以兴奋交感神经,增高血压,扩张气管,用于治疗支气管哮喘症。
3.茶碱、可可碱和咖啡碱
茶碱、可可碱和咖啡碱分别存在于茶叶、可可豆和咖啡中,也可以用人工合成。
N
N
N N N N
N
N N N N
N O
O
CH 3
H CH 3
O O
CH 3
3
CH 3
O O
CH 3
3
H
茶碱 可可碱 咖啡碱
(1,3-二甲基黄嘌呤) (3,7-二甲基黄嘌呤) (1,3,7-三甲基黄嘌呤)
它们是无色针状结晶,有苦味,易溶于热水,难溶于冷水。茶碱熔点27O~272℃, 可可碱 熔点357℃,咖啡碱熔点235℃。
茶碱、可可碱和咖啡碱都是黄嘌呤的衍生物。黄嘌呤又称为2,6-二羟基嘌呤,存在于动物的血液、肝脏和尿中。它有酮式-烯醇式的互变异构体。
茶碱有利尿作用和松弛平滑肌作用。咖啡碱又称咖啡因,有兴奋中枢神经、止痛、利尿作用。可可碱能抑制胃小管再吸收和利尿作用。
4.金鸡纳碱(奎宁)
金鸡纳碱又称奎宁(quinine ),在金鸡纳树皮中含量达15%,分子中含有喹啉环,属喹啉族生物碱。分子结构如下:
N
CH 3O
HOCH
CH
CH 2
奎宁是无色针状晶体,无水物熔点172.8℃,味极苦,微溶于水,易溶于乙醇、乙醚等有机溶剂。奎宁可以用于治疗和预防各种疟疾并有退热作用。
5.吗啡(morphine)
吗啡是罂粟科植物鸦片中含量最多的一种生物碱。在鸦片中的含量达1O%。
吗啡属于异喹啉生物碱,它的基本结构可看作是与异喹啉稠合在一起的菲。分子式为 C 17H 19O 3 N·H 2O 。分子结构如下:
O
H O
H N CH 3
O
吗啡是白色结晶,熔点254℃,微溶于水,水溶液有苦味。它对中枢神经有麻痹作用,有显著的止咳、镇痛、抑制肠蠕动的作用,但连续使用成瘾。由于有毒,中毒后精神萎靡不振,瞳孔缩小,呼吸缓慢,逐渐呼吸困难而死亡,因此,使用时须十分慎重。
*6.秋水仙碱
秋水仙碱除了可有效地诱发染色体的加倍,在农业上用于多倍体育种外,还可以治疗风痛等疾病。特别是近年来发现它有一定的抗癌作用,能制止癌细胞的增长,对乳腺癌、皮肤癌等有很好的疗效。
OCH 3
CH 3O
CH 3O
CH 3O CH 3O
NHC O
秋水仙碱存在于植物秋水仙的球茎和种子中,我国云南的山慈菇中含量也较多。秋水仙碱是黄灰色针状结晶,熔点为155~157℃,能溶于水或稀乙醇溶液,易溶于氯仿,但不溶于无水乙醚和石油醚。秋水仙碱是环庚的三烯酮的衍生物,分子中有两个稠合的七碳环,氮在侧链上成酰胺状,因此呈中性。 阅读材料
鸦片吗啡海洛因
鸦片,学名阿片,在医药上有着重要的位置,是一种很好的麻醉镇痛药。阿片一词是由希腊文“浆汁”引申而来,确确实实它是从植物罂粟的切口流出的浆汁,经自然干燥而制得,色褐、味苦、异臭、可溶于水,主要成分是吗啡(占10%),其次是可待因与罂粟碱,具有成瘾性、耐受性、欣快性、等级性四大药理特点。所谓等级性是指越是高级神经中枢,作用就越强。
令人遗憾的是,世界上生产的阿片仅一小部分用在医疗上,绝大部分被非法买卖,为“隐君子”所用。阿片能使人慢性中毒,服用阿片半个月会出现瞳孔缩小,精神欣快,一旦停药会产生戒断综合症:流鼻涕、流眼泪、打哈欠、恶心呕吐、心烦意乱、软弱无力、精神萎靡,此时再服用阿片,戒断综合症立即消除。长此下去,成瘾者意志消沉,消瘦乏力,丧失生活及工作信心。为避免出现戒断综合症和获得欣快感,便会丧失理智地谋取阿片,即“强迫性求药行为”,导致严重的家庭与社会问题。
阿片的主要成分是吗啡,是镇痛的王牌药,又能提高胃肠平滑肌与括约肌的张力,减少蠕动,故可止泻固精,对此《本草纲目》曾有记载。吗啡一词来源于希腊文“梦神”,服用后会产生幻觉。阿片的另一成分是可待因,有中枢性镇咳作用及轻度镇痛作用。另外所含罂粟碱,具有松弛平滑肌作用和血管扩张作用,这一点与吗啡恰好相反。
阿片的近亲有印度大麻及其他人工合成品海洛因、杜冷丁、乙基吗啡。印度大麻曾作为麻醉药品使用过,但作为镇痛药已被否定,无明显成瘾性。海洛因即盐酸二乙基吗啡,白色粉末,味苦,易溶于水,进入机体后水解成吗啡产生类吗啡作用。它比吗啡镇痛作用大七倍,抑制呼吸中枢作用大四倍,它最大危险性是:只服小剂量,短时间就可成瘾,难以戒除,易复发。
治疗隐君子的药物与方法较多,用非那酮替代是其中一种,这是由于非那酮所产生的戒断综合症较阿片为轻,通过迅速减量至停用以达到戒除的目的。
习题
1、命名下列化合物或写出结构式:
N O
N
S N
N
Cl
3
COOH
CH 3
Cl
(1)
(2)
(3)
(4)
(5)2,5—二甲基喹啉 (6) 4—喹啉甲醛 (7) 糠醛 (8)1—甲
基—5—溴—2—吡咯甲酸
2、从电子效应说明为什么吡啶比苯难于发生亲电取代反应,而吡咯比苯易于发生亲电取代反应?
3、甲基喹啉氧化得到一种三元羧酸,该酸脱水时可得到两种酸酐的混合物,确定甲基在喹啉中的位置。
4、完成下列反应:
O
+(CH 3CO)2O
HNO 3
(1)
N H
+HO 3S N 2+Cl
(2)
N 25H
+Br 2
(3)
N
+Cl 2
3,o
C
(4)
N
+CH 3COCl
(5)
N
(6)
O
O
+O
O
(7)
5、写出下列反应中A 、B 、C 、D 的结构:
O
CHO I 2
A
B
C
D
NaOH SOCl 2
C 2H 5OH
6、按碱性由大到小的顺序排列下列化合物: (1) 苄胺 苯胺 吡咯 吡啶 氨 (2) 吡咯 吡啶 四氢吡咯
7、用化学方法除去下列化合物中的杂质:
(1)甲苯中的少量吡啶 (2)苯中的少量噻吩
第十一章杂环化合物和生物碱
第十一章 杂环化合物和生物碱 一、学习要求 1.掌握杂环化合物的分类和命名 2.掌握五元杂环、六元杂环和稠杂环的结构和性质 3.掌握生物碱的基本概念及分类 4.了解生物碱的一般性质、提取方法及重要的生物碱 二、本章要点 (一)杂环化合物的分类和命名 1.杂环化合物的概念 由碳原子和非碳原子所构成的环状有机化合物称为杂环化合物,环中的非碳原子称为杂原子,最常见的杂原子有氧、硫、氮等。 2.杂环化合物的分类 按环的数目不同,可分为单杂环和稠杂环两大类。单杂环按环的大小不同又可分为五元杂环和六元杂环。稠杂环通常由苯与单杂环或单杂环与单杂环稠合杂环化合物而成。 3.杂环化合物的命名 杂环化合物的命名比较复杂,目前我国常使用“音译法”,即按英文的读音,用同音汉字加上“口”字旁命名: O 1 2 3 45 5 43 2 1 S 5 432 1N 543 2 1 N S 543 2 1N N H 5432 1N N H 呋喃 噻吩 吡咯 噻唑 吡唑 咪唑 (furan ) (thiophene ) (pyrrole ) (thiazole ) (pyrazole ) (imidazole ) 6 54 32 1 O N N 1 2 3456 N N 1 2 3456 N N 1 2 3456 6 54 3 2 1 N 吡啶 哒嗪 嘧啶 吡嗪 吡喃(pyridine ) (pyridazine) (pyrimidine) (pyrazine) (pyran)
环上有取代基的杂环化合物的名称是以杂环为母体,并注明取代基的位置、数目和名称。杂原子的编号,除个别稠杂环外,一般从杂原子开始编号,环上有不同不同杂原子时,按O 、S 、NH 和N 的顺序编号;某些杂环可能有互变异构体,为区别各异构体,需用大写斜体“H ”及其位置编号标明一个或多个氢原子所在的位置。例如: 2,4-二羟基嘧啶 2-氨基-6-氧嘌呤 4H -吡喃 2H -吡喃 此外,还可以将杂环作为取代基,以官能团侧链为母体进行命名。例如: N ,N-二乙基-3- 4-嘧啶甲酸 3-吲哚乙酸 2-呋喃甲醛 吡啶甲酰胺 (二)含氮六元杂环 1.吡啶的结构 1 2345 6 7 8 9 N N N N H 2N O H N N OH OH 1 23 4 56 O 1 2 34 56 1 2 3 45O 6 1 2 1 CHO O CON(C 2H 5)2 N 2 34 56 COOH 6 5432 1 N N CH 2COOH N H 12 3 456 7 N .. 6 8 75 43 2 110 98 76 5321 6 58 7 654321 H N N N N N N 8 7 65 432 N 7 4 32 1H N 喹啉 异喹啉 吲哚 吖啶 嘌呤 ( quinoline) (isoquinoline) (indole) (acridine) (purine)
第十六章杂环化合物生物碱
第十六章 杂环化合物、生物碱 杂环化合物的定义:在环状有机化合物中,构成环的原子除了碳原子外还含有其他原子,这环状种化合物就叫做杂环化合物(heterocyclic compound )。除碳以外的其他原子叫做杂原子。常见的杂原子有:氮、氧、硫。 第一节 杂环化合物的分类和命名 一、 分类 按照环的大小和环的数目可分为: 杂环 单杂环 五元环 六元环 苯环与单杂环的稠合杂环(苯并杂环) 两个或两个以上单杂环的稠合杂环O S N H 稠杂环 N N N N N H N 二、 命名 1、音译法:根据外文译音,选用同音汉字,加“口”字旁表示杂环。 O S N H 吡咯呋喃噻吩吡啶N pyrrole furan thiophene pyridine N H 吲哚indole N N 咪啶pyrimidine 取代杂环的命名: ① 杂环的编号从杂原子起依次1,2,3 ……(或:α,β,γ……)。 ② 如环上不止一个杂原子时,则从O 、S 、N 的顺序依次编号。 ③ 有两个相同杂原子的,应从连有H 原子或取代基的开始编号。 ④ 编号时注意杂原子或取代基的位次之和最小。 ⑤ 稠杂环是特定的母体和固定的编号。 N S 5 1 2 4 3 5-乙基噻唑N N H 1 23454-甲基咪唑 CH 3 C 2H 5 N CH 31 23 4563-甲基吡啶 2、根据结构命名:
即根据相应于杂环的碳环来命名,把杂环看作是相应的碳环中的碳原子被杂原子置换而形成的。例如,吡啶可看作是苯环上一个碳原子被氮原子置换而成的,所以叫做氮杂苯。 O S N H N 茂 (环戊二烯)氮茂 氧茂 硫茂 N N 苯氮苯 1,3-二氮苯 第二节 一杂五元杂环化合物 含有一个杂原子的典型五元杂环是呋喃、噻吩、吡咯。 O S N H 一、 呋喃、噻吩、吡咯的结构 1、据现代物理方法证明: ① 呋喃、噻吩、吡咯都是一个平面的五元环结构,即成环的四个C 原子和一个杂原子都是以SP 2杂化轨道成键的。 ②环上每个碳原子的P 轨道有一个电子,杂原子P 轨道上有两个电子。 ③ P 轨道垂直于五元环的平面,互相侧面重叠而形成一个与苯环相似的闭合共轭体系。 ④ 五元环的六个π电子分布在包括环上五个原子在内的分子轨道。 2、分子结构符合休克尔(Huckel)规则(4n+2=6,n=1),π电子数为6。具有芳香性。但芳性比苯弱,环的稳定性差。 3、芳香性秩序: 苯 > 噻吩 > 吡咯 > 呋喃 呋喃的芳香性最弱,实际上它可以进行双烯加成反应,表现出共轭二烯烃的性质。 4、它们的键长数据如下[单位(ppm )]: O S N 140 145 135 172 143 137 138144 135 137 5、吡咯、呋喃、噻吩环上杂原子氮、氧、硫的未共用电子对参与环的共轭体系,使环上的电子云密 度增大。因此,它们都比苯活泼,比苯容易进行亲电取代反应,而且它们进行亲电取代反应的活泼性顺序是: 吡咯 > 呋喃 > 噻吩 > 苯 X +(CF 3CO)2O X COCF 3 +CF 3COOH 三氟乙酐酰化 二、 呋喃、噻吩、吡咯的性质 1、亲电取代反应——主要在杂原子的α位: 它是呋喃、吡咯、噻吩的典型反应。由于它们环上的电子云密度比苯大,比苯容易发生亲电取代反应。同时环稳定性比苯差,因此反应条件与苯不同,需要在较温和的条件下反应,以避免氧化、开环或聚合等副反应。
生物碱习题剖析
3 生物碱的碱性与哪些有关 (1)氮原子的杂化类型:随杂化度升高而增强;②诱导效应:氮原子所连接的基团如为供电基团则碱性增强,如为吸电基团则碱性减弱;③诱导一场效应:使生物碱的碱性降低;④共轭效应:若生物碱分子中氮原子孤对电子成P-兀共轭体系时,通常情况下,其碱性较弱;⑤空间效应:若生物碱的空间环境不利于氮原子接受质子,其碱性减弱;反之,则碱性增强;⑥分子内氢键形成:若生物碱分子结构中氮原子附近存在羟基、羰基等取代基团,碱性增强。 4.生物碱类化合物的鉴别方法①沉淀反应:大多数生物碱能和某些酸类、重金属盐类以及一些较大分子量的复盐反应,生成单盐、复盐或络盐沉淀。如与碘化铋钾试剂的反应; ②显色反应:用于生物碱的冠色试剂很多,它们往往因生物碱的结构不同而显示不同的颜色,Mandelin试剂(1%钒酸铵的浓硫酸溶液);③成盐反应:绝大多数生物碱可与酸形成盐类,但不同类型的生物碱与酸成盐的形式不同,主要有:季铵生物碱的成盐反应、含氮杂缩醛生物碱的成盐反应、具有烯胺结构生物碱的成盐反应、涉及氮原子跨环效应生物碱的成盐反应。 5.生物碱类化合物的提取一般从天然药物巾提取总生物碱通常采用溶剂法、离子交换法、沉淀法等提取分离方法。①对于脂溶性生物碱可采取酸水提取法、醇类溶剂提取法、亲脂性有机溶剂提取法;②对于水溶性生物碱可采取沉淀法、溶剂萃取法。 6.生物碱类化合物的分离对于生物碱的分离通常分为系统分离与特定分离。一般的方法是先对总碱进行初步分离,将性质相近的生物碱分成几个类别或部位。然后再按各成分的碱度、极性或功能团的差异分离生物碱单体。①总生物碱的初步分离:根据总生物碱中各成分理化性质的差异,可将其初步分离为强碱性的季铵碱、中等强度碱性的叔胺碱及其酚性碱、弱碱性生物碱及其酚性碱等几个部分;②生物碱单体的分离:利用生物碱碱性的差异、利用生物碱极性的差异或生物碱盐的溶解度差异、利用生物碱特殊官能团、利用色谱法进行分离。 7.生物碱类化合物的结构鉴定①色谱法:色谱法在生物碱鉴别中的应用主要体现在天然药物及天然药物制剂中有无生物碱存在的检识、指导生物碱的分离、检查生物碱的纯度及对已知生物碱的鉴定等多个方面,主要有:薄层色谱法、纸色谱法、高效液相色谱法、气相色谱法;②谱学法:目前,在生物碱结构鉴定工作中,最常用的分析方法有紫外光谱(U V)、红外光谱(IR)、质谱(M S)和核磁共振 (N M R)。 【习题】 一、名词解释 1.生物碱 2.两性生物碱 3.生物碱沉淀反应 4.诱导效应 5.共轭效府 6.空间效应 7.诱导一场效应 8.氢键效应 二、填空题 1.小檗碱呈黄色,而四氢小檗碱则无色,其原因在于。 2.弱碱性生物碱在植物体内是以状态存在。 3.在生物碱的色谱检识中常用的显色剂是,它与生物碱斑点作用常显色。 4.Mayer’s试剂的主要成分为;Dragendorff’s试剂的主要成分为。 5.总生物碱的提取方法大致有以下三类:、、。 6.麻黄碱和伪麻黄碱的分离可利用它们的——盐在水中的溶解度不同,在水中溶
杂环化合物及生物碱教材
第十一章杂环化合物及生物碱 杂环化学是有机化学的一个重要组成部分。所有的有机化合物,从结构上可以分为两大类,即链状化合物和环状化合物。在环状化合物中,所有的“环节”原子都是碳原子组成的,称为环状化合物。如果在“环节”原子中除了碳原子以外,还含有一个或者多个非碳原子时,则称为杂环化合物。杂环化学就是研究杂环化合物的化学。 杂环化合物中的非碳“环节”原子称为杂原子。在有机化学中,周期表中碳以外的其他元素,通常被看成是杂原子,并用以构成杂环化合物。实际上,到目前为止,有些元素——如零族和第Ⅱ族元素等,还尚未发现由它们组成的、稳定的杂环化合物。另外,金属元素的原子也能参与构成环状结构的分子,然而这种分子的键型结构和物理、化学性质都与一般的化合物不同,通常把它们称作金属有机化合物,而不作为杂环化合物来讨论。 在杂环化合物中,各种不同的“环节”原子的排列组合方式和键合类型是多种多样的,所以如此构成的杂环化合物的数目是十分的惊人的。据统计,在现今已知的有机化合物中,杂环化合物的数量,占总数的65%以上。因此,杂环化合物在有机化学的各领域研究中都占有极其重要的地位。 杂环化合物不仅种类繁多,而且在自然界中分布较为广泛。具有生物活性的天然杂环化合物对生物体的生长、发育、遗传和衰亡过程都起着关键性的作用。例如:在动、植物体内起着重要生理作用的血红素、叶绿素、核酸的碱基、中草药的有效成分——生物碱等都是含氮杂环化合物。一部分维生素、抗菌素、植物色素、许多人工合成的药物及合成染料分子结构也含有杂环。杂环化合物的应用范围极其广泛,涉及医药、农药、染料、生物膜材料、超导材料、分子器件、贮能材料等,尤其在生物界,杂环化合物几乎随处可见。 在此,就不对杂环化合物品种多样性、应用广泛性进行过多的陈述。以下将杂环化合物中具有代表的几种物质向读者进行简要的介绍。最常见的杂原子是氧、硫和氮。如: O O S S 呋喃四氢呋喃噻吩四氢噻吩
生物碱类药物的分析
生物碱类药物的分析 掌握盐酸麻黄碱、硫酸阿托品、硫酸奎宁、盐酸吗啡和硝酸士的宁的鉴别、杂质检查和含量测定方法。 一、概述 (一)定义:生物碱是一类存在于生物体内的含氮有机化合物。 (二)分类 1.芳烃胺类 硫酸苯丙胺,精神振奋药pKb=9.9 盐酸麻黄碱,肾上腺受体激动药pKb=9.6 2.异喹啉类 盐酸吗啡,镇痛药pKb1=8.0,pKb2=9.9 磷酸可待因,镇痛镇咳药;盐酸黄连素,抗菌药;度冷丁等 3.喹啉类 硫酸奎宁,抗疟药;异构体硫酸喹尼丁,抗心率失常药; pKb1=5.07,pKb2=9.7 4.托烷类 硫酸阿托品,抗胆碱药pKb=9.9 氢溴酸东莨菪碱,抗胆碱药pKb=7.6; 5.黄嘌呤类 咖啡因,pKb=14.15(碱性极弱); 茶碱,平滑肌松弛药,含活泼氢酸性; 6.吲哚类 硝酸士的宁,中枢神经兴奋药pKb1=6.0,pKb2=11.7(酰胺) 硫酸长春新碱,抗肿瘤药;利血平,抗高血压药;
7.其他类 硝酸毛果芸香碱,缩瞳药。 由上可知,生物碱类药物有如下特点。 (三)特点 1.数量多,绝大多数存在于植物体内;已发现3000多种,100多种有效,中成药中富含生物碱。 2.生理活性强,但大都有毒性 因此,质量控制和临床应用尤应慎重,许多为特殊管制药物,并已超出药物分析的范畴,体育运动中的兴奋剂问题,世界关注的毒品问题,许多是生物碱类成分。该类药物的质量应严格控制,以保证用药的安全和有效。 (四)结构特征和分析方法间的关系 1.碱性:N原子的存在,强弱从N上的取代基是供电子还是吸电子基团,空间位阻两方面考虑。 1)一般情况:季铵>仲铵>伯铵>叔铵>NH3>环酰铵 2)脂肪铵>脂环铵>芳铵 3)个别两性化合物如吗啡有酸性(酚羟基),茶碱只有酸性(活泼氢) 2.存在状态多数以盐的形式存在 1)植物中多与有机酸成盐如吗啡罂粟酸盐,鞣酸奎宁盐; 2)药用多为多为无机酸盐如盐酸、硫酸、磷酸和硝酸盐。 含量测定应考虑上述2个因素,碱性强弱选择滴定溶液和指示剂,成盐的情况在非水滴定时要考虑对滴定的干扰。 3.溶解性 1)共性:游离生物碱易溶于CHCl3等中等极性有机溶剂,难或不溶于水,溶于稀酸溶液;成盐易溶于水;(提问?) 2)个性:两性和酸性化合物易溶于稀碱溶液(吗啡和茶碱);麻黄碱和咖啡因能溶于水;咖啡因和利血平碱性极弱,不能与酸结合成稳定的盐。 溶解性可以用于提取分离和鉴别时的重要依据。
生物碱
第九章生物碱 一、填空 1.小檗碱呈黄色,而四氢小檗碱则无色,其原因在于(结构中有较长的共轭体系)。 2.弱碱性生物碱在植物体内主要是以(游离)状态存在。 3.在生物碱的色谱检识中常用的显色剂是(碘化铋钾),它与生物碱斑点作用常先 (橘红)色。 4.总生物碱的提取方法大致有(溶剂法)、(离子交换树脂)和(沉淀法)三类。 5.麻黄碱和伪麻黄碱的分离可利用它们的(草酸)盐在水中的溶解度不同, (草酸麻黄碱)在水中溶解度比较小,能先行结晶检出,(草酸伪麻黄碱)则留在母液中。。 6.生物碱沉淀反应可应用于:(预试中是否存在生物碱)、(在分离过程中可作为追踪生物碱的指标)、(分离提纯生物碱)等。 7.用硅胶柱层析进行生物碱的薄层色谱时,为克服硅胶的酸性,得到集中的斑点,有两种方法:(用高碱或缓冲液代替水来制硅胶板)、(用碱性溶剂作为展开剂)。 8.用pH 梯度萃取法分离生物碱,是将总生物碱溶于有机溶剂中,用不同pH 缓冲液进行萃 取,缓冲液pH 值(高)到(低),所得到的生物碱的碱度则由(强) 到(弱)。 二、判断题 1.所有生物碱都有不同程度的碱性。√ 2.含氮原子的杂环化合物都是生物碱。× 3.一般生物碱的旋光性都是左旋的。× 4.在所有生物碱中,季铵碱的碱性最强。× 5.生物碱与碘化铋钾多生成红棕色沉淀。√ 6.生物碱盐都易溶于水中。× 三、选择题(单选) 1.下列关于生物碱的论述,正确的是(A) A.含有氮原子 B. 显碱性 C.自然界的所有含氮成分 D.在植物体内以盐的状态存在 2.生物碱不具有的特点是(D) A.分子中含氮原子 B.氮原子多在环内 C. 具有碱性 D. 分子中多有苯环 3.小檗碱的结构类型是(B) A. 喹啉类 B.异喹啉类 C. 哌啶类 D.吲哚类 4. 下列生物碱碱性最强的是(D) A. 伯胺生物碱 B. 仲胺生物碱 C. 叔胺生物碱 D. 季胺生物碱 5. 下列生物碱碱性最弱的是(D) A. 伯胺生物碱 B. 仲胺生物碱 C. 叔胺生物碱 D. 酰胺生物碱 6.决定生物碱碱性最主要的因素是(A) A.氮原子的杂化方式 B. 诱导效应 C. 共轭效应 D. 分子内氢键 三、多选题题 1. 使生物碱碱性减弱的因素是(AE) A.吸电子诱导效应 B.供电子诱导效应 C.供电子共轭效应 D.立体效应 2. 使生物碱碱性减弱的吸电子基团是(BCD) A. 烷基 B.羰基 C.醚基 D.苯基
生物碱类化合物药理作用研究进展
收稿日期:2003-03-17; 修订日期:2003-09-18 作者简介:蒙其淼(1979-),男(汉族),广西横县人,在读研究生,主要从事药物分析工作. 生物碱类化合物药理作用研究进展 蒙其淼,梁 洁,吴桂凡,陆 晖 (广西中医学院,广西南宁 530001) 摘要:对生物碱类化合物的药理作用研究进展进行了概述和分析。生物碱类化合物具有心血管系统、中枢神经系统、抗炎、抗菌、抗病毒、保肝、抗癌等多方面的药理活性。 关键词:生物碱类化合物; 药理作用 中图分类号:R 285.5 文献标识码:B 文章编号:1008-0805(2003)11-0700-03 生物碱类化合物广泛存在于自然界植物中,有多种生物学活性。本文就其药理作用研究情况作一概述。1 心血管系统作用 苦参碱类生物碱是以苦参碱为代表的化学结构相似的一类生物碱,存在于豆科植物苦参、苦豆子、及广豆根中,主要包括苦参碱(matr ine ,M at )、氧化苦参碱(oxymatrine )、槐果碱(sopho-car pine )等。大量实验研究表明苦参碱类生物碱在强心和抗心率失常功能方面具有显著而肯定的作用,它们均能对抗乌头碱、哇巴因、氯仿-肾上腺素、氯化钡及冠脉结扎等诱发的动物实验性心率失常,且多为室性心率失常[1]。临床应用苦参治疗各种原因引起的心率失常,发现苦参对房性、室性心率失常均有作用[2]。苦参碱提高DET ,延长ERP 是其抗心率失常作用机制。槐果碱(sophocarpine )能对抗室性心率失常,可能是通过对心脏的直接作用及通过神经系统对心脏的间接作用。苦参碱、氧化苦参碱对心肌表现为正性肌力作用,能使离体家兔心房和豚鼠乳头肌标本、离体蛙心和蟾蜍心脏收缩力加强,振幅增加,并呈剂量依赖关系。用电激动左心房实验证明,苦参碱的正性肌力作用可被Ca 6通道阻滞剂维拉帕米显著抑制,推测其可能与激活钙通道有关。苦参总碱还能扩张冠状动脉,增加冠状动脉血流量,扩张离体兔的肾及耳血管,能延长小鼠在常压下的耐缺氧时间。用苦参碱50mg/kg 能显著降低大鼠实验性高脂血症的血清甘油三酯,升高HDL 水平,降低血黏度,使血液流变学各项指标有所改善,从而达到抑制动脉粥样硬化的形成[3]。 以具有心血管活性的异喹啉类生物碱为先导物,结合某些钾通道阻滞剂的结构特征,设计合成了28个3,4—二氢和1,2,3,4—四氢苄基/萘甲基异喹啉化合物及其有关季铵衍生物。药理实验表明,大多数化合物具有不同程度的降压和减慢心率活性。异喹啉母核氮原子电荷可能为影响作用于血管或心脏组织的重要因素之一[4]。从茜草科钩藤植物滇钩藤中分得的四氢鸭木碱具有舒张血管平滑肌的作用,其对兔胸主动脉平滑肌收缩的抑制百分率达53%以上[5]。枳实生物碱成分能迅速显著升高大鼠血压,给药前后比较,差异非常显著(P <0.01)[6]。 小檗碱主要来源于毛茛科植物黄连,其静脉注射或口服对麻醉(犬、猫、兔)或不麻醉大鼠均可引起血压下降。在一般剂量或小剂量时,它能兴奋心脏,增加冠状动脉血流量;大剂量则抑制心脏,即使再增加剂量,在离体蟾蜍或猫的心脏上亦无起搏现象。降 压机制可能是直接兴奋毒蕈碱样受体[7] 。从吴茱萸中分离得到的2-烃基取代的4(1H )-喹诺酮生物碱有一定的阻断钙离子通道并抑制高钾离子引起的钙离子富集作用,从而能扩张血管[8]。从中药川芎中得到的川芎嗪与阿魏酸反应合成阿魏酸川芎嗪盐,药理实验发现两者都具有较强的抗凝血功能和较强的抗血栓作用,能使APTT 、TT 和PT 延长,而阿魏酸川芎嗪盐作用强于川芎嗪[9]。 普洛托品(P rotopine,P ro)又名原阿片碱,是从夏天无、紫金龙等我国广泛分布的植物中提取的一种异喹啉类生物碱,具有对抗血小板聚集,影响血小板生物活性物质的释放,保护血小板内部超微结构的作用。P ro 对乌头碱、毒K 、中枢性心肌缺血再灌注、氯仿、苯-肾上腺等引起的心率失常有保护作用,负性频率作用和延长有效不应期是其抗心率失常作用的基础[10]。甲基连心碱(neferine ,Nef )是从睡莲科植物莲成熟种子的绿色胚芽中提取的一种双苄基异喹啉类生物碱,对心血管具有多种作用。Nef 能对抗乌头碱、氯仿-肾上腺素、电刺激丘脑下区诱发的心率失常作用。Nef 在较大剂量(6mg /kg )iv 后,对正常血压、醋酸去氧皮质酮盐型高压和肾性高压大鼠都有降压效应,其机制可能是通过直接扩张血管平滑肌而起作用。Nef 对离体大鼠心脏缺血—再灌注损伤有保护作用,能依剂量减少整体大鼠缺血再灌注后VF 发生率,缩VF 持续时间。Nef 对电解性氧自由基损伤离体大鼠心脏、冠脉流量减少、血管内皮细胞损伤也都具有保护作用。Nef 还具有抗血小板聚集和抗血栓的作用。对心肌收缩力,Nef 具有抑制作用,在一定剂量范围内可增加冠脉流量,为该药治疗心血管疾病提供了实验依据[11]。 附子中的双酯型二萜生物碱既是毒性成分,又是有效成分,如乌头碱具有扩张冠状血管和四肢血管的作用,在小剂量(未致心室纤颤)时,就已产生抗急性心肌缺血的作用,并有明显的常压耐缺氧作用[12]。贝母素丙4.2mg /kg 的剂量可导致猫的血压缓慢降低,并最终维持在较低水平。湖北贝母总碱对猫血压也有短时中等程度的降压作用,与阿托品作用相似。贝母生物碱FH 1与F H 2具有正性肌力、负性频率和舒张血管作用。在离体血管上,F H 1—F H 4均可明显对抗甲氧胺引起的血管收缩作用[13]。 汉防己甲素(tetr andine ,T ET )又称粉防已碱,是从防己科植物粉防己根中提取的双苄基异喹啉类生物碱。TET 有明显的降压作用,并能极显著降低高血压患者血内脂质过氧化物、血栓素水平,极显著升高SOD 、前列环素水平,降低T XB 2/6-Keto-PGF 1A 比值。在缺氧性肺动脉高压犬,TET 能明显降低升高的肺动脉压和肺血管阻力,并提高CO 和氧搬运能力而对系统循环和血气水平无明显影响。TET 有抗心绞痛作用,能显著降低心肌耗氧指数,是一个治疗心绞痛、预防心肌梗死和减轻心肌缺血—再 灌注损伤的有效药物[14] 。来自石蒜科植物的生物碱同样具有心血管系统作用。石蒜伦碱能抑制蟾蜍心脏。石蒜碱则先兴奋后抑制,对麻醉大鼠、猫、犬及兔均有降压作用,机制为直接扩张外周血管及抑制心脏。二氢石蒜碱可减弱肾上腺素的升压作用,因其能阻止儿茶酚胺的释放[15]。2 中枢神经系统作用 石蒜科植物生物碱加兰他敏及力克拉敏为可逆性胆碱酯酶抑制剂,小剂量对大脑皮层及延脑内胆碱酯酶活性有较强抑制作用,大剂量则抑制脑内胆碱酯酶活性。应用加兰他敏、二氢加兰他敏治疗小儿麻痹后遗、重症肌无力和外伤性截瘫等病症有效,且毒性较小。石蒜碱对小鼠及家兔有明显镇静作用,能延长巴比妥类药物的睡眠时间,还能加强延胡索乙素及吗啡的镇静作用。石蒜碱静脉注射或皮下注射,对人工致热家兔均有明显解热作用, · 700·时珍国医国药2003年第14卷第11期LISHIZHEN MEDICINE AND MATERIA MEDICA RESEARCH 2003VOL.14NO.11
天然药物化学(中药化学)第十章生物碱化合物章节练习及参考答案
二、选择题 1.生物碱碱性的表示方法多用( ) A.Kb B.pKb C.Ka D.pKa E.pH 3.碱性最强的生物碱类型为( ) A.酰胺生物碱 B.叔胺生物碱 C.仲胺生物碱 D.季铵生物碱 E.两性生物碱 9.可异构成季铵碱的是( ) A.黄连碱 B.甲基黄连碱 C.小檗胺 D.醛式小檗碱 E.醇式小檗碱 10.生物碱沉淀反应的条件是( ) A.酸性水溶液 B.碱性水溶液 C.中性水溶液 D.盐水溶液 E.醇溶液 11.碘化铋钾反应生成沉淀的颜色为( ) A.白色 B.黑色 C.棕色 D.橘红色 E.蓝色 12.不能与生物碱沉淀试剂产生沉淀的是( ) A.生物碱 B.多糖 C.多肽 D.蛋白质 E.鞣质 14.分离碱性不同的混合生物碱可用( ) A.简单萃取法 B.酸提取碱沉淀法 C.pH梯度萃取法 D.有机溶剂回流法 E.分馏法 16.可分离季铵碱的生物碱沉淀试剂是( ) A.碘化汞钾 B.碘化铋钾 C.硅钨酸 D.雷氏铵盐 E.碘-碘化钾 17.以硅胶为吸附剂进行薄层色谱分离生物碱时,常用的处理方法是( ) A.以碱水为展开剂 B.以酸水为展开剂 C.展开剂中加入少量氨水 D.展开剂中加入少量酸水 E.以CHCl3为展开剂 19.从苦参总碱中分离苦参碱和氧化苦参碱是利用二者( ) A.在水中溶解度不同 B.在乙醇中溶解度不同
C.在氯仿中溶解度不同 D.在苯中溶解度不同 E.在乙醚中溶解度不同 小檗碱 小檗胺 小檗碱 >小檗胺,为季铵碱,碱性强于为叔胺碱的小檗胺 樟柳碱 R = H 莨菪碱 R = OH 山莨菪碱 东莨菪碱 莨菪碱>山莨菪碱>东莨菪碱≈樟柳碱。东莨菪碱和樟柳碱由于6、7位氧环立体效应和诱导效应的影响,碱性较弱(p K a7.5);莨菪碱无立体效应障碍,碱性较强(p K a9.65);山莨菪碱分子中6位羟基的立体效应影响较东莨菪碱小,故其碱性介于莨菪碱和东莨菪碱之间。 士的宁 伪士的宁 士的宁>伪士的宁。伪士的宁氮原子邻位碳上虽有α-羟基,为氮杂缩醛结构,但由于氮原子处于桥头N 时具有刚性结构,不能发生质子化异构,相反由于OH 的吸电效应使碱性减小。 O N OH OMe OMe O C H 3H O N MeO CH 3H OCO N CH 3CH CH 2OH OCO N CH 3O CH CH 2OH OCO O N CH 3CH 2OH C OH R N O O H N N O O H N OH N N O N O C H 3O N CH 3
生物碱类药物的性质
生物碱类药物(重点在鉴别,n的位置,有哪些电效应) 苯烃胺类(盐酸麻黄碱和盐酸伪麻黄碱) 氮原子在侧链上,碱性较一般生物碱强,易与酸成盐。 托烷类(硫酸阿托品和氢溴酸山莨菪碱) 阿托品和山莨菪碱是由托烷衍生的醇(莨菪醇)和莨菪酸缩合而成,具有酯结构。分子结构中,氮原子位于五元酯环上,故碱性也较强,易与酸成盐。 喹啉类(硫酸奎宁和硫酸奎尼丁) 奎宁和奎尼丁为喹啉衍生物,其结构分为喹啉环和喹啉碱两个部分,各含一个氮原子,喹啉环含芳香族氮,碱性较弱;喹啉碱微脂环氮,碱性强。 异喹啉类(盐酸吗啡和磷酸可待因) 吗啡分子中含有酚羟基和叔胺基团,故属两性化合物,但碱性略强;可待因分子中无酚羟基,仅存在叔胺基团,碱性较吗啡强。 吲哚类(硝酸士的宁和利血平) 士的宁和利血平分子中含有两个碱性强弱不同的氮原子,n1处于脂肪族碳链上,碱性较n2强,故士的宁碱基与一分子硝酸成盐。 黄嘌呤类(咖啡因和茶碱) 咖啡因和茶碱分子结构中含有四和氮原子,但受邻位羰基吸电子的影响,碱性弱,不易与酸结合成盐,其游离碱即供药用。 鉴别试验:特征鉴别反应。 1.双缩脲反应系芳环侧链具有氨基醇结构的特征反应。 盐酸麻黄碱和伪麻黄碱在碱性溶液中与硫酸铜反应,cu2+与仲胺基形成紫堇色配位化合物,加入乙醚后,无水铜配位化合物及其有2 个结晶水的铜配位化合物进入醚层,呈紫红色,具有4个结晶水的铜配位化合物则溶于水层呈蓝色。 2.vitali反应系托烷生物碱的特征反应。
硫酸阿托品和氢溴酸山莨菪碱等托烷类药物均显莨菪酸结构反应,与发烟硝酸共热,即得黄色的三硝基(或二硝基)衍生物,冷后,加醇制氢氧化钾少许,即显深紫色。 3.绿奎宁反应系含氧喹啉(喹啉环上含氧)衍生物的特征反应硫酸奎宁和硫酸奎尼丁都显绿奎宁反应,在药物微酸性水溶液中,滴加微过量的溴水或氯水,再加入过量的氨水溶液,即显翠绿色。 4.marquis反应系吗啡生物碱的特征反应。 取得盐酸吗啡,加甲醛试液,即显紫堇色。灵敏度为0.05μg. 5.frohde反应系吗啡生物碱的特征反应。 盐酸吗啡加钼硫酸试液0.5ml,即显紫色,继变为蓝色,最后变为棕绿色。灵敏度为0.05μg. 6.官能团反应系吲哚生物碱的特征反应。 利血平结构中吲哚环上的β位氢原子较活泼,能与芳醛缩合显色。 与香草醛反应。利血平与香草醛试液反应,显玫瑰红色。 与对-二甲氨基苯甲醛反应。利血平加对-二氨基苯甲醛,冰醋酸与硫酸,显绿色,再加冰醋酸,转变为红色。 7.紫脲酸反应系黄嘌呤类生物碱的特征反应。 咖啡因和茶碱中加盐酸与氯酸钾,在水浴上蒸干,遇氨气即生成四甲基紫脲酸铵,显紫色,加氢氧化钠试液,紫色即消失。 8.还原反应系盐酸吗啡与磷酸可待因的区分反应。 吗啡具弱还原性。本品水溶液加稀铁氰化钾试液,吗啡被氧化生成伪吗啡,而铁氰化钾被还原为亚铁氰化钾,再与试液中的三氯化铁反应生成普鲁士蓝。 可待因无还原性,不能还原铁氰化钾,故此反应为吗啡与磷酸可待因的区分反应。 特殊杂质检查: 利用药物和杂质在物理性质上的差异。 硫酸奎宁中“氯仿-乙醇中不溶物”的检查盐酸吗啡中“其它生物碱”的检查旋光性的差异:用于硫酸阿托品中“莨菪碱”的检查对光选择性吸收的差异:利血平生产或储存
生物碱
第九章生物碱 第一节概述 生物碱是一类重要的天然含氮类化合物。 1.定义:生物碱是指一类来源于生物界(以植物为主)的含氮的有机物,多数生物碱分子具有较复杂的环状结构,且氮原子在环状结构内,大多呈碱性,一般具有生物活性。 含氮的有机化合物有很多,但低分子胺类(如甲胺、乙胺等)、非环甜菜因类、氨基酸、氨基糖、肽类(肽类生物碱除外)、蛋白质、核酸、核苷酸、卟啉类、维生素类等。 比较确切的表述:生物碱是含负氧化态氮原子、存在于生物体中的环状化合物。 负氧化态氮:包括胺(-3)、氮氧化物(-1)、酰胺(-3);排除含硝基(+3)、亚硝基(+1)的化合物。 环状结构:排除了小分子的胺类、非环的多胺和酰胺。(实际上有些非环的胺类或酰胺是属于生物碱范畴的,如麻黄碱) 2.分布: 低等植物(蕨类、菌类)、高等植物(单子叶植物、双子叶植物); 同科同属植物可能含有相同结构类型的生物碱; 在植物体内各个器官和组织都可能有分布,但对于一种植物来说,生物碱往往在植物的某种器官含量较高。 3.存在形式: (1)根据氮原子在分子中所处的状态,主要分为六类:①游离碱②盐类③酰胺类④N-氧化物⑤氮杂缩醛类⑥其它如亚胺、烯胺等。 在植物体内,除以酰胺形式存在的生物碱外,少数碱性极弱的生物碱以游离的形式存在,绝大多数以盐的形式存在;个别生物碱则以氮氧化物的形式存在,如氧化苦参碱。 第二节生物碱生物合成的基本原理 (一)环合反应 1.一级反环合应 (1)内酰胺形式:该反应主要限于肽类生物碱等的生物合成。 (2)希夫碱形式:含氨基(伯胺或仲胺)和羰基的化合物易加成-脱水形成希夫碱。 (3)曼尼希氨甲基化反应:醛、胺(一级胺或二级胺或氨)和负碳离子(含活泼氢的化合物)发生缩合反应,结果是活泼氢被氨甲基所取代,得到曼尼希碱。
生物碱
生物碱沉淀剂的种类很多,常用的有下面几种: (1)碘化汞钾试剂:在酸性溶液中与生物碱反应生成白色或淡黄色沉淀。 (2)碘化铋钾试剂:在酸性溶液中与生物碱反应生成桔红色沉淀。 (3)碘化钾碘试剂:在酸性溶液中与生物碱反应生成棕红色沉淀。 (4)硅钨酸试剂:在酸性溶液中与生物碱反应生成灰白色沉淀。 (5)磷钼酸试剂:很灵敏,在中性或酸性溶液中与生物碱反应生成鲜黄色或棕黄色沉淀。在试验时,通常选用三种以上不同的生物碱沉淀试剂进行试验,如均为正反应表示检液中可能有生物碱存在。如须确证,则要进一步精制后,再行检验,如再次均成正反应,即可肯定有生物碱存在。如第一次试验时就对三种沉淀剂呈负反应,即可肯定多无生物碱存在。 (6)有些生物碱能和某些试剂反应生成特殊的颜色,叫做显色反应,常用于鉴识某种生物碱。但显色反应受生物碱纯度的影响很大,生物碱愈纯,颜色愈明显。常用的显色剂有: ①矾酸铵一浓硫酸溶液(Mandelin试剂)为1%矾酸铵的浓硫酸溶液。如遇阿托品显红色,可待因显蓝色,士的宁显紫色到红色。 ②钼酸铵一浓硫酸溶液(Frohde试剂)为1%钼酸钠或钼酸铵的浓硫酸溶液,如遇乌头碱显黄棕色,小檗碱显棕绿色,阿托品不显色。 ③甲醛一浓硫酸试剂(Marquis试剂)为30%甲醛溶液0.2ml与10ml浓硫酸的混合溶液。如遇吗啡显橙色至紫色,可待因显红色至黄棕色。 ④浓硫酸如遇乌头碱显紫色、小檗碱显绿色,阿托品不显色。 ⑤浓硝酸如遇小檗碱显棕红色,秋水仙碱显蓝色,咖啡碱不显色。 生物碱的显色反应原理尚不太明了,一般认为是氧化反应、脱水反应、缩合反应或氧化、脱水与缩合的共同反应。(
乌头碱 生物碱(alkaloid)旧称植物碱,一般指植物中的含氮有机化合物(蛋白质、肽、氨基酸及维生素B1除外)。现在,人们从海洋生物、微生物、真菌及昆虫的代谢物中也发现了很多含氮化合物,有时也称之为生物碱。因此,广义上生物界所有含氮有机化合物都可称为生物碱。 生物碱是研究得最早的一类有生物活性的天然有机化合物。我国17世纪初的《白猿经》即记述了从乌头中提取出砂糖样毒物作箭毒用,用现代的经验分析推测它应该是乌头碱。此外,1806年德国科学家Serturner从鸦片中分离得到吗啡、1810年西班牙医生Gomes从金鸡纳树皮中分得结晶Cinchonino(奎宁与辛可宁的混合物)。1819年Weissner把这类植物中的碱性化合物统称为类碱(alkali-like)或生物碱,后者一直沿用至今。 生物碱大多具有生物活性,往往是很多药用植物,包括许多中草药的有效成分。例如,阿片中的镇痛成分吗啡、止咳成分可待因,麻黄的抗哮喘成分黄麻碱、颠茄的解痉成分阿托品、长春花的抗癌成分长春新碱等等。生物碱大多具有复杂的化学结构,能与酸结合成盐而溶于水,容易被体内吸收。目前已报道并搞清楚化学结构的生物碱已达4000多种,并以每年约上百个的速度递增。虽然大多数情况下,药用植物中含量最高的生物碱往往是主要的有效成分,但也有例外,如乌头碱是乌头的主要成分,但它的强心止痛成分却是含量极微的去甲乌头碱。 生物碱在植物中的分布较广,其中双子叶植物类的豆科(Leguminosae)、茄科(Solanace ae)、放己科(Manispermaceae)、罂粟科(Papaveraceae)和小蘖科(Berbereaceae)等科属含生物碱较多。生物碱在植物中的含量高低不一,如金鸡纳树皮中含生物碱高达3%以上,而长春花中的长春新碱含量仅为0.0001%,美登木中的美登素更是只含0.00002%,一般含量在0.1%以上就算比较高了。由于同一植物中的生物碱往往来自于同一个前体,一次它们的结构也往往类似,同科同属中的生物碱也大多属于同一结构类型。
有机化学 第十一章 杂环化合物和生物碱
第十一章杂环化合物和生物碱 杂环化合物和生物碱广泛存在于自然界中,在动植物体内起着重要的生理作用。本章介绍杂环化合物的分类、命名、结构特点、性质及重要的杂环化合物,生物碱的一般性质、提取方法和重要的生物碱。 第一节杂环化合物 环状有机化合物中,构成环的原子除碳原子外还含有其它原子,且这种环具有芳香结构,则这种环状化合物叫做杂环化合物。组成杂环的原子,除碳以外的都叫做杂原子。常见的杂原子有氧、硫、氮等。前面学习过的环醚、内酯、内酐和内酰胺等都含有杂原子,但它们容易开环,性质上又与开链化合物相似,所以不把它们放在杂环化合物中讨论。 杂环化合物种类繁多,在自然界中分布很广。具有生物活性的天然杂环化合物对生物体的生长、发育、遗传和衰亡过程都起着关键性的作用。例如:在动、植物体内起着重要生理作用的血红素、叶绿素、核酸的碱基、中草药的有效成分——生物碱等都是含氮杂环化合物。一部分维生素、抗菌素、植物色素、许多人工合成的药物及合成染料也含有杂环。 杂环化合物的应用范围极其广泛,涉及医药、农药、染料、生物膜材料、超导材料、分子器件、贮能材料等,尤其在生物界,杂环化合物几乎随处可见。
一、杂环化合物的分类和命名 为了研究方便,根据杂环母体中所含环的数目,将杂环化合物分为单杂环和稠杂环两大类。最常见的单杂环有五元环和六元环。稠杂环有芳环并杂环和杂环并杂环两种。另外,可根据单杂环中杂原子的数目不同分为含一个杂原子的单杂环、含两个杂原子的单杂环等。 杂环化合物的命名在我国有两种方法:一种是译音命名法;另一种是系统命名法。 译音法是根据IUPAC 推荐的通用名,按外文名称的译音来命名,并用带―口‖旁的同音汉字来表示环状化合物。例如: 呋喃 咪唑 吡啶 嘌呤 furan imidazole pyridine purine 杂环上有取代基时,以杂环为母体,将环编号以注明取代基的位次,编号一般从杂原子开始。含有两个或两个以上相同杂原子的单杂环编号时,把连有氢原子的杂原子编为1,并使其余杂原子的位次尽可能小;如果环上有多个不同杂原子时,按氧、硫、氮的顺序编号。例如: O N N N N N N H N
第十五章 杂环化合物、生物碱
第十五章 杂环化合物、生物碱 杂环化合物的定义:在环状有机化合物中,构成环的原子除了碳原子外还含有其他原子,这环状种化合物就叫做杂环化合物(heterocyclic compound )。除碳以外的其他原子叫做杂原子。常见的杂原子有:氮、氧、硫。 第一节 杂环化合物的分类和命名 一、 分类 按照环的大小和环的数目可分为: 杂环 单杂环 五元环 六元环 苯环与单杂环的稠合杂环(苯并杂环) 两个或两个以上单杂环的稠合杂环O S N H 稠杂环 N N N N N H N 二、 命名 1、音译法:根据外文译音,选用同音汉字,加“口”字旁表示杂环。 O S N H 吡咯呋喃噻吩吡啶N pyrrole furan thiophene pyridine N H 吲哚indole N N 咪啶pyrimidine 取代杂环的命名: ① 杂环的编号从杂原子起依次1,2,3 ……(或:α,β,γ……)。 ② 如环上不止一个杂原子时,则从O 、S 、N 的顺序依次编号。 ③ 有两个相同杂原子的,应从连有H 原子或取代基的开始编号。 ④ 编号时注意杂原子或取代基的位次之和最小。 ⑤ 稠杂环是特定的母体和固定的编号。 N S 5 1 2 4 3 5-乙基噻唑N N H 1 23454-甲基咪唑 CH 3 C 2H 5 N CH 31 23 4563-甲基吡啶 2、根据结构命名:
即根据相应于杂环的碳环来命名,把杂环看作是相应的碳环中的碳原子被杂原子置换而形成的。例如,吡啶可看作是苯环上一个碳原子被氮原子置换而成的,所以叫做氮杂苯。 O S N H N 茂 (环戊二烯)氮茂 氧茂 硫茂 N N 苯氮苯 1,3-二氮苯 第二节 一杂五元杂环化合物 含有一个杂原子的典型五元杂环是呋喃、噻吩、吡咯。 O S N H 一、 呋喃、噻吩、吡咯的结构 1、据现代物理方法证明: ① 呋喃、噻吩、吡咯都是一个平面的五元环结构,即成环的四个C 原子和一个杂原子都是以SP 2杂化轨道成键的。 ②环上每个碳原子的P 轨道有一个电子,杂原子P 轨道上有两个电子。 ③ P 轨道垂直于五元环的平面,互相侧面重叠而形成一个与苯环相似的闭合共轭体系。 ④ 五元环的六个π电子分布在包括环上五个原子在内的分子轨道。 2、分子结构符合休克尔(Huckel)规则(4n+2=6,n=1),π电子数为6。具有芳香性。但芳性比苯弱,环的稳定性差。 3、芳香性秩序: 苯 > 噻吩 > 吡咯 > 呋喃 呋喃的芳香性最弱,实际上它可以进行双烯加成反应,表现出共轭二烯烃的性质。 4、它们的键长数据如下[单位(ppm )]: O S N 140 145 135 172 143 137 138144 135 137 5、吡咯、呋喃、噻吩环上杂原子氮、氧、硫的未共用电子对参与环的共轭体系,使环上的电子云密 度增大。因此,它们都比苯活泼,比苯容易进行亲电取代反应,而且它们进行亲电取代反应的活泼性顺序是: 吡咯 > 呋喃 > 噻吩 > 苯 X +(CF 3CO)2O X COCF 3 +CF 3COOH 三氟乙酐酰化 二、 呋喃、噻吩、吡咯的性质 1、亲电取代反应——主要在杂原子的α位: 它是呋喃、吡咯、噻吩的典型反应。由于它们环上的电子云密度比苯大,比苯容易发生亲电取代反应。同时环稳定性比苯差,因此反应条件与苯不同,需要在较温和的条件下反应,以避免氧化、开环或聚合等副反应。
生物碱
生物碱类化合物-13 生物碱类化合物-13 13.苦参总生物碱具有什么活性() A.发汗平喘的作用 B.抗菌作用 C.镇痛的作用 D.镇静麻醉作用 E.消肿利尿,抗肿瘤的作用 答案:E 解析:苦参具有清热燥湿、杀虫、利尿等功效,总生物碱具有消肿利尿抗肿瘤等作用。 [1-5] A.发汗、平喘作用 B.抗菌作用 C.降血脂的作用 D.镇静麻醉的作用 E.消肿利尿、抗肿瘤的作用 1.东莨菪碱具有() 2.苦参碱具有() 3.小檗碱具有() 4.麻黄碱具有() 答案:D E B A 解析:东莨菪碱是洋金花主要有效成分之一,具有镇静、麻醉等作用。苦参碱是苦参主要有效成分之一,具有消肿利尿、抗肿瘤等作用。小檗碱是黄连主要有效成分之一,具有抗菌作用。麻黄碱是麻黄主要有效成分之一,具有发汗、平喘等作用。 [6-8] A.小檗碱 B.麻黄碱 C.伪麻黄碱 D.东莨菪碱
E.山莨菪碱 6.其共轭酸因分子内氢键稳定的是() 7.其草酸盐不溶于水的是() 8.其分子结构中具有氧环的是() 答案:C B D [9-11] A.氧化苦参碱 B.樟柳碱 C.莨菪碱 D.黄连碱 E.乌头碱 9.属季铵型生物碱的是() 10.属二萜双酯型生物碱的是() 11.属喹喏里西啶衍生物是() 答案:D E A [12-15] A.药根碱 B.次乌头碱 C.东莨菪碱 D.莨菪碱 E.甲基伪麻黄碱 12.水溶性的季铵碱是() 13.毒性极强的生物碱是() 14.6、7位具有含氧环结构的生物碱是() 15.经碱水加热可生成无酯键的醇胺型水解产物的生物碱是()答案:A B C B [16-17] A.羟基苦参碱 B.伪麻黄碱 C.巴马丁 D.表小檗碱 E.士的宁 16.可用水蒸气蒸馏法提取的生物碱是() 17.毒性极强的生物碱是()
杂环化合物和生物碱
13 杂环化合物和生物碱Heterocyclic Compounds and Natural Bases 杂环化合物是由碳原子和非碳原子共同组成环状骨架结构的一类化合物。这些非碳原子统称为杂原子,常见的杂原子为氮、氧、硫等。环状有机化合物中,构成环的原子除碳原子外还含有其它原子,且这种环具有芳香结构,则这种环状化合物叫做杂环化合物。组成杂环的原子,除碳以外的都叫做杂原子。前面学习过的环醚、内酯、内酐和内酰胺等都含有杂原子,但它们容易开环,性质上又与开链化合物相似,所以不把它们放在杂环化合物中讨论。本章将主要讨论的是环系比较稳定、具有一定程度芳香性的杂环化合物,即芳杂环化合物。 杂环化合物种类繁多,在自然界中分布很广。具有生物活性的天然杂环化合物对生物体的生长、发育、遗传和衰亡过程都起着关键性的作用。例如:在动、植物体内起着重要生理作用的血红素、叶绿素、核酸的碱基、中草药的有效成分——生物碱等都是含氮杂环化合物。一部分维生素、抗菌素、植物色素、许多人工合成的药物及合成染料也含有杂环。杂环化合物的应用范围极其广泛,涉及医药、农药、染料、生物膜材料、超导材料、分子器件、贮能材料等,尤其在生物界,杂环化合物随处可见。 13.1 杂环化合物Heterocyclic Compounds 分子中由碳原子和氧、硫、氮等其它原子形成的比较稳定的环状结构的化 合物称为杂环化合物。杂环中除碳原子以外的其它原子称为杂原子。最常见的杂原子有氧、硫、氮等。例如: S N H N N N O 呋喃噻吩吡咯吡啶嘧啶 furan thiophene pyrrole pyridine pyrimidine 前述章节中,我们遇到的内酯、交酯、内酰胺、内酐、环醚以及环状半缩醛等,虽然也有环状结构,但它们的环容易形成,也容易破裂,其性质与相应的脂肪族化合物相类似,因此不把它们列入杂环化合物之列,本章主要讨论环比较稳定且具有芳香性的杂环化合物。 杂环化合物可以含一个或多个相同的或不相同的杂原子,环的数目也可以是一个或多个。杂环化合物的种类繁多,数量庞大,其数量占已知有机物总数的三分之一左右。杂环化合物在自然界的分布极广,其中很多有重要的生理作用,如血红素、叶绿素、维生素、花色素、抗菌素、核酸、生物碱等都是含有杂环结构的化合物。杂环化合物也是合成许多染料、药物的原料。治疗癌症的一些有效药物也是杂环化合物的衍生物。因此,杂环化合物无论在理论研究或实际应用方面都很重要。 13.1.1杂环化合物的分类Classification of Heterocyclic Compounds 按照杂环的结构,杂环化合物大致可分为单杂环和稠杂环两大类。单杂环中最常见的为五员杂环和六员杂环;稠杂环中普遍存在的是苯环与单杂环稠合和杂环与杂环稠合。根据所含杂原子的种类和数目,单杂环和稠杂环又可分为多种。 常见杂环化合物的分类和名称见表13.1。 表13.1 常见杂环化合物的结构、分类和名称
