第十 十一单元 酸碱盐思维导图复习课
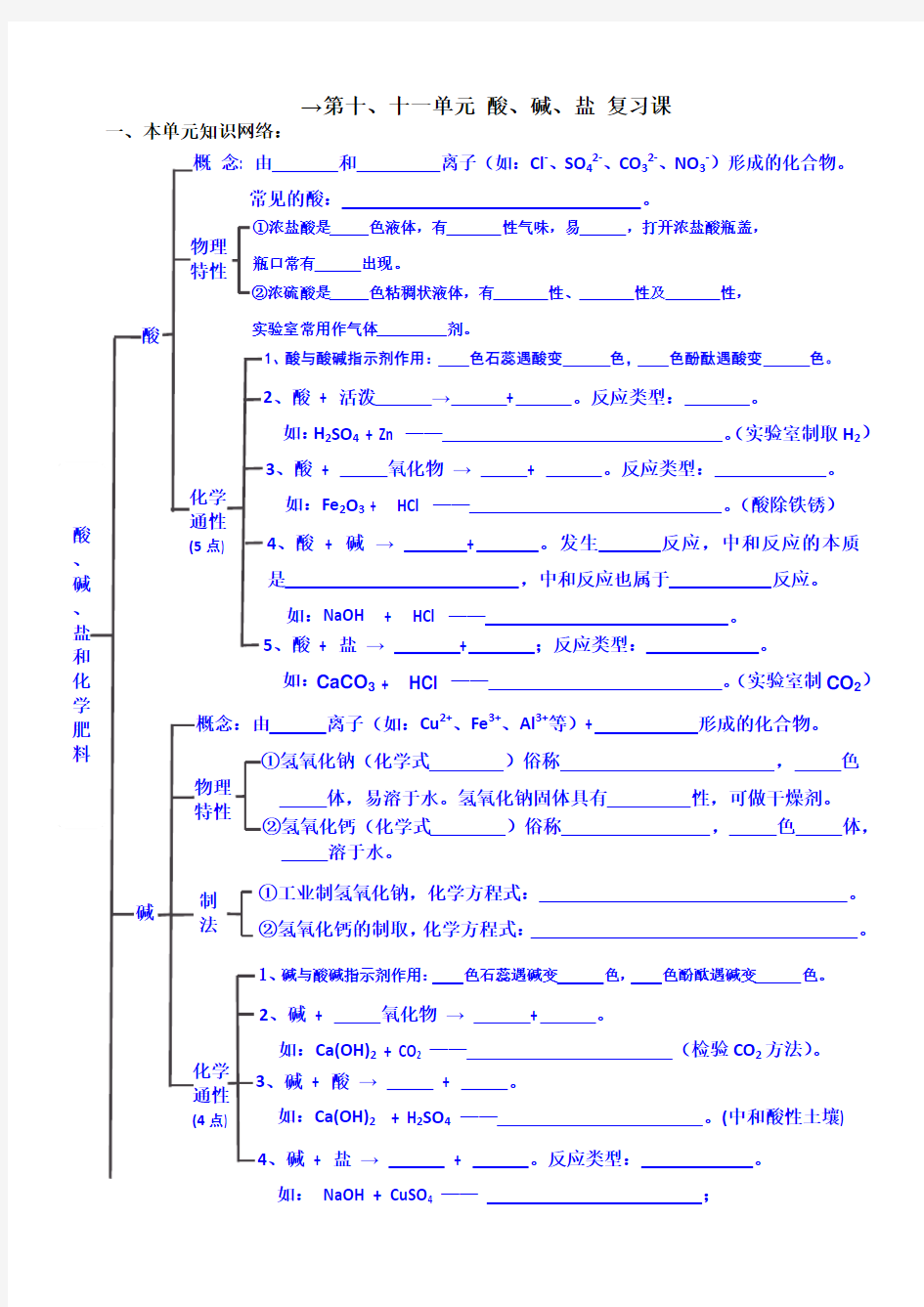

2、碱 + 氧化物 → + 。 如:Ca(OH)2 + CO 2 —— (检验CO 2方法)。
3、碱
+ 酸 → + 。 如:Ca(OH)2 + H 2SO 4 —— 。(中和酸性土壤)
概 念: 由 和 离子(如:Cl -、SO 42-、CO 32-、NO 3-)形成的化合物。 常见的酸: 。 4、碱 + 盐 → + 。反应类型: 。
如: NaOH + CuSO 4 —— ;
3、酸 + 氧化物 → + 。反应类型: 。 如:Fe 2O 3 + HCl —— 。(酸除铁锈) 5、酸 + 盐 → + ;反应类型: 。 如:CaCO 3 + HCl —— 。(实验室制CO 2) 物理 特性 ①氢氧化钠(化学式 )俗称 , 色 体,易溶于水。氢氧化钠固体具有 性,可做干燥剂。 概念:由 离子(如:Cu 2+、Fe 3+、Al 3+等)+ 形成的化合物。
4、酸 + 碱 → + 。发生 反应,中和反应的本质是 ,中和反应也属于 反应。 如:NaOH + HCl —— 。 →第十、十一单元 酸、碱、盐 复习课
一、本单元知识网络:
1、碱与酸碱指示剂作用: 色石蕊遇碱变 色, 色酚酞遇碱变 色。 化学 通性 (4点) 物理 特性 ①浓盐酸是 色液体,有 性气味,易 ,打开浓盐酸瓶盖, 瓶口常有 出现。 ②浓硫酸是 色粘稠状液体,有 性、 性及 性, 实验室常用作气体 剂。 1、酸与酸碱指示剂作用: 色石蕊遇酸变 色, 色酚酞遇酸变 色。 化学 通性 (5点)
2、酸 + 活泼 → + 。反应类型: 。 如:H 2SO 4 + Zn —— 。(实验室制取H 2) 制 法 ②氢氧化钙(化学式 )俗称 , 色 体, 溶于水。 ①工业制氢氧化钠,化学方程式: 。 ②氢氧化钙的制取,化学方程式: 。
①氮肥:含 元素,补 ,使作物叶子生长茂盛、翠绿,缺N 的作物叶子发黄。常见的氮肥:尿素:CO(NH 2)2 ②磷肥:含 元素,补 ,促使作物根系生长,果实饱满,增强作物 的能力,缺P 的作物生长矮小,叶子呈暗绿色。 ③钾肥:含 元素,补 ,使作物生长健壮,增强作物 能力,缺K 的作物叶子边缘有烧焦痕迹。常见钾肥:K 2CO 3 ④复合肥:含 中两种或两种以上的营养素。如:KNO 3。 化肥 常见 的盐 酸碱度: ①氯化钠:化学式 ,俗称 。用途: 。 ②碳酸钠:化学式 ,俗称 、 。用途: 。 ③碳酸氢钠:化学式 ,俗称 。用途: 。 ④碳酸钙:化学式 ,是 的主要成分。用途: 。 ⑤工业用盐亚硝酸钠(NaNO 2)有毒。 复分解 反应 ①概念:两种 相互 成分,生成另外两种 的反应。 ②一般形式:AB + CD → ; ③特点:成分交换,价(化合价)不变; ④条件:反应物溶于 或 ; 生成物要有 中的一种。 ⑤范围:酸与碱反应、酸与盐反应、碱与盐反应、盐与盐反应 酸与金属氧化物反应。(共五大类) PH 范围是 ,酸性PH 7,酸性越强,PH 值越 ;
碱性PH 7,碱性越强,PH 值越 ;中性PH 7。酸雨PH 小于 。 2、盐 + 酸 → + ;反应类型: 。 如:AgNO 3 + HCl —— 。 3、盐 + 碱 → + ;反应类型: 。 如:FeCl 3 + NaOH —— 。 4、盐 + 盐 → + ;反应类型: 。 如:CuSO 4 + BaCl 2 —— 。 1、盐 + 金属 → + ;反应类型: 。 如:CuSO 4 + Fe —— 。 概念:由 离子(如:Cu 2+、Fe 3+、Al 3+等)和 离子形成的化合物。 化学 通性 (4点)
盐 酸 、碱 、盐 和化学肥料
