影响化学平衡状态的因素-教案
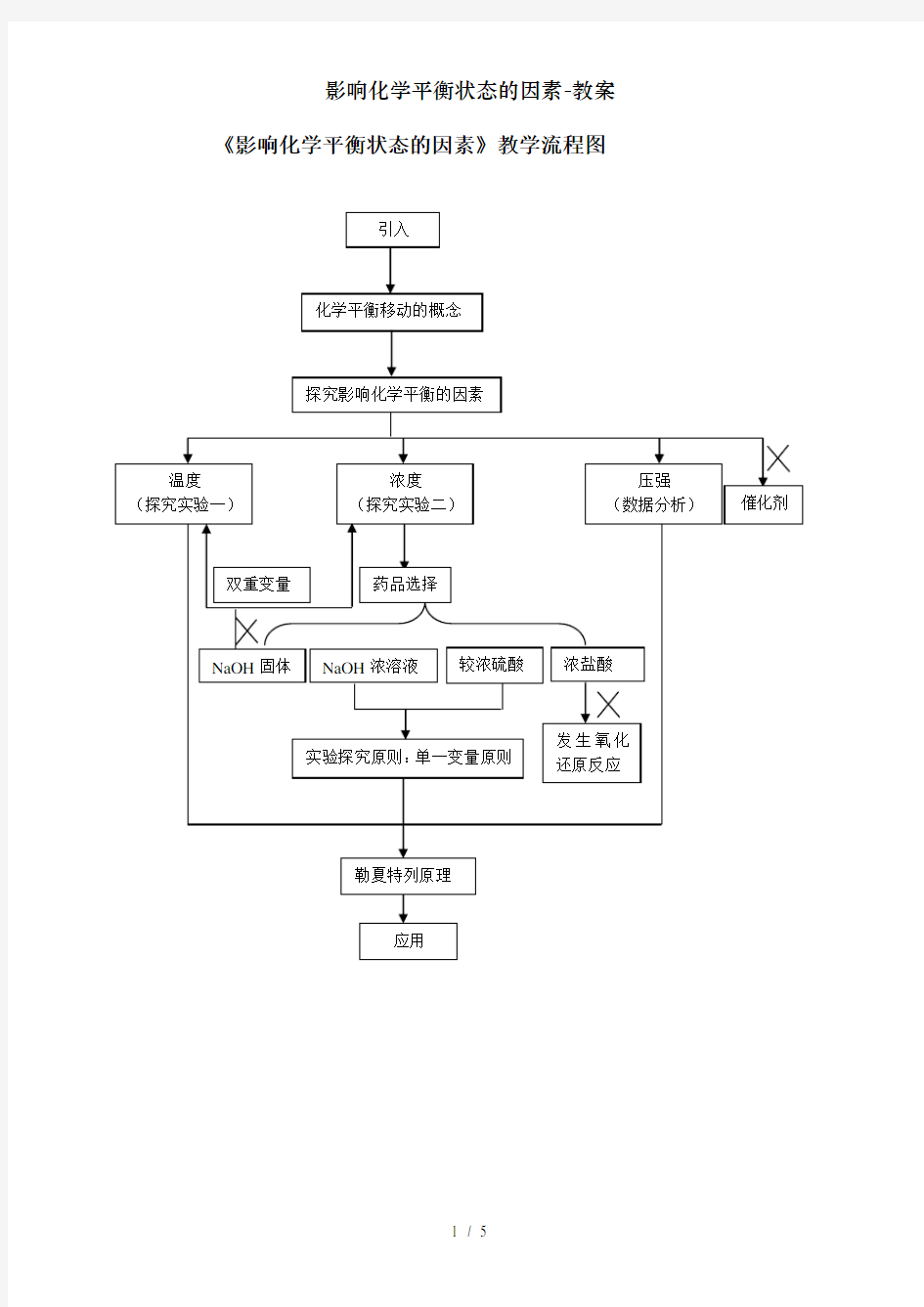

《影响化学平衡状态的因素》教学流程图
影响化学平衡状态的因素
嘉峪关市酒钢三中刘莉
教学目标
知识与技能
1、理解化学平衡移动的实质,了解浓度、压强、温度等外界条件对化学平衡移动的影响;
2、理解勒夏特列原理的涵义,并能简单运用。
过程与方法
1、通过温度、浓度实验,逐步探究平衡移动的原理,引导学生体验化学实验方法;
2、通过图表分析,提高学生数据分析及归纳能力;
3、通过对实验过程中认知冲突的解决,引导学生体会单一变量原则。
情感态度与价值观
1、通过科学史话,激发学生学习化学的兴趣;
2、在实验中培养学生尊重事实、严谨推理、缜密思考的科学态度。
教学重难点
教学重点:
浓度、压强、温度等条件对化学平衡移动的影响
教学难点:
勒夏特列原理的形成和理解
教学过程
【新课引入】
科学家勒夏特列、哈伯的重要贡献——化学平衡移动原理的发现及其应用
【新课推进】
一、化学平衡状态的改变:
v(正) >v(逆) 平衡向正反应方向移动
v(正) 二、影响化学平衡状态的因素 1、温度对化学平衡的影响 【探究实验一】 2NO2(g) N2O4(g) △H<0 NO2球浸泡在冰水、热水中,观察颜色的变化红棕色无 实验条件变化实验现象实验结论 放入热水中温度升高 放入冷水中温度降低 结论: 升高温度,化学平衡向吸热方向移动 降低温度,化学平衡向放热方向移动 2、浓度对化学平衡移动的影响 【实验探究二】探究浓度变化对化学平衡的影响 实验原理:已知在K2Cr2O7的溶液中存在如下平衡: Cr2O72- + H2O 2CrO42- + 2H+ 橙色黄色 现有药品: 0.1mol/L K2Cr2O7溶液、70%浓硫酸、浓盐酸、固体NaOH、NaOH浓溶液。 请根据上述原理及所给药品设计实验,并选择合适的药品,探究浓度对化学平衡状态的影响。 实验步骤:____________________________________________________ 所选试剂现象结论5mLK2Cr2O7溶液中滴加 8-10滴浓H2SO4 5mLK2Cr2O7溶液中滴加3-4滴NaOH浓溶液 分析上述实验现象及结论,在学生产生认知冲突的基础上引导学生体会单一变量原则。结论:增大反应物浓度(减少生成物浓度),平衡向正反应方向移动; 减少生成物浓度(增大生成物浓度),平衡向逆反应方向移动。 1、压强对化学平衡的影响 下表为500℃时,不同压强下N2(g)十 3H23(g)达到平衡时混合体系中NH3的体积分数: 试根据表中数据分析压强对化学平衡状态的影响。 结论:增大压强,平衡向气体分子数减小的方向移动; 减小压强,平衡向气体分子数增大的方向移动。 【思考】使用催化剂对化学平衡状态是否有影响? 催化剂能同等程度的增大正反应速率和逆反应速率,因此催化剂不能使化学平衡状态发生移动。 三、小结 如果改变影响平衡的条件之一(如温度、压强,以及参加反应的化学物质的浓度),平衡将向着能够减弱这种改变的方向移动。——勒夏特列原理 【科学史话】勒夏特列生平 【学以致用】工业合成氨条件选择 已知N2与H2反应合成NH3是一个可逆反应,其热化学方程式为: N2 (g)+3 H2 (g) 2 NH3 (g) △=-92.4kJ·mol-1 在工业生产中,可以通过以下途径来提高合成氨的产率。下列哪些措施可以用勒夏特列原理解释? 1、向反应器中注入过量N2; 2、采用适当的催化剂; 3、及时从合成塔中分离出NH3; 3、在高压下进行反应; 4、反应器温度为500℃。 【科学史话】哈伯生平 作业设置 1、书面作业:课本P32 3、6、7; 2、课后思考: 并与课本P27实验2-6进行对比,找出自己设计方案的优缺点。
