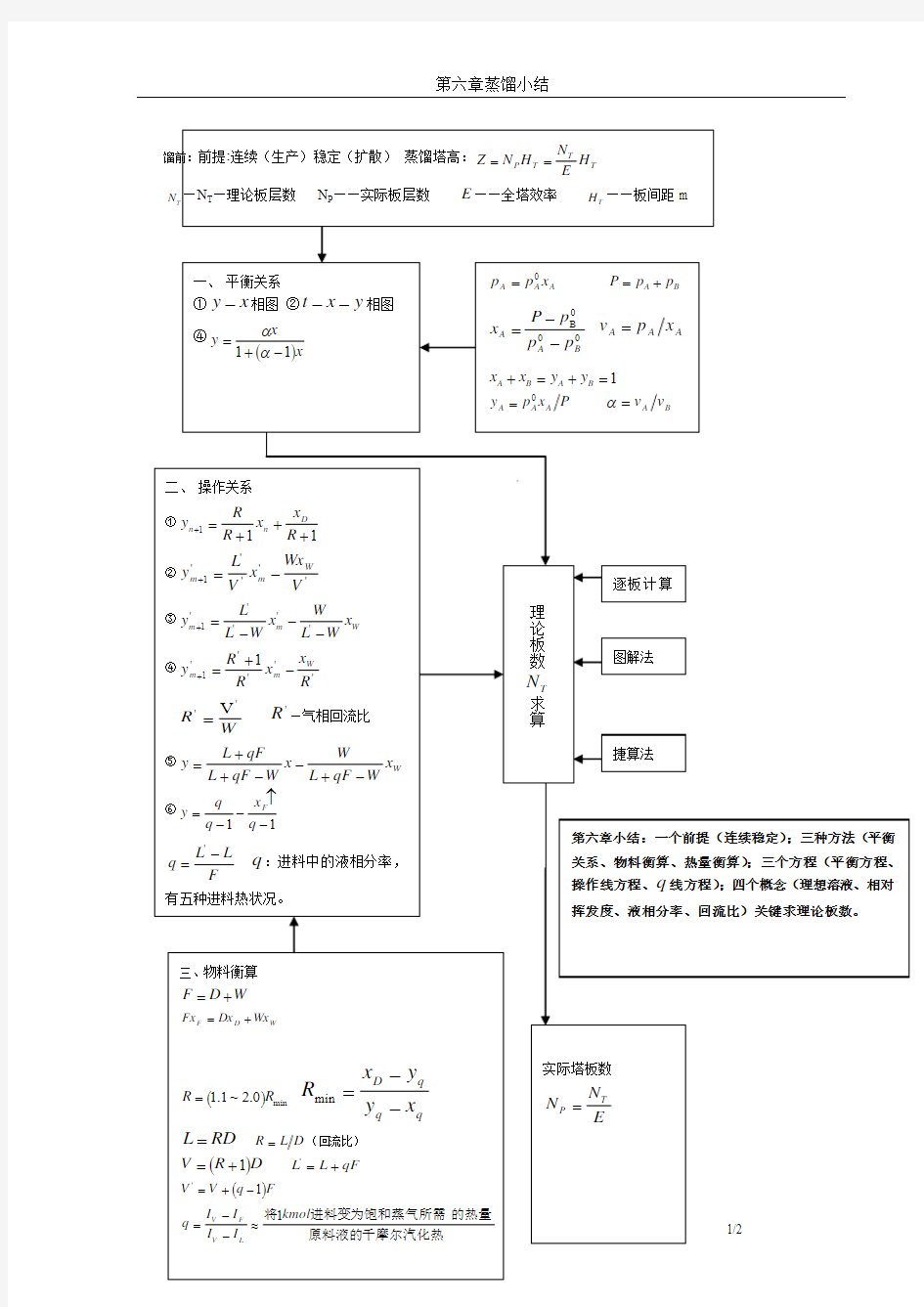
化工原理 第六章小结

2/2
南工大化工原理第六章习题解答
第六章习题 1)苯酚(C 6 H 5 OH)(A)和对甲酚(C 6 H 4 (CH 3 )OH)(B)的饱和蒸汽压数据为: 温度 ℃ 苯酚蒸汽压 kPa 对甲酚蒸汽压 kPa 温度 ℃ 苯酚蒸汽压 kPa 对甲酚蒸汽 压 kPa 113.7 10.0 7.70 117.8 11.99 9.06 114.6 10.4 7.94 118.6 12.43 9.39 115.4 10.8 8.2 119.4 12.85 9.70 116.3 11.19 8.5 120.0 13.26 10.0 117.0 11.58 8.76 试按总压P=75mmHg(绝压)计算该物系的“t—x—y”数据。此物系为理想物系。 t0C p A 0kPa p B 0kPa x A x B 113.7 10.0 7.70 1.0 1.0 114.6 10.4 7.94 0.837 0.871 115.4 10.8 8.2 0.692 0.748 116.3 11.19 8.5 0.558 0.624 117.0 11.58 8.76 0.440 0.509 117.8 11.99 9.06 0.321 0.385 118.6 12.43 9.39 0.201 0.249 119.4 12.85 9.70 0.0952 0.122 120.0 13.26 10.0 0.000 0.000 2)承第1题,利用各组数据,计算 ①在x=0至x=1围各点的相对挥发度α i ,取各α i 的算术平均值α,算出α对 α i 的最大相对误差。 ②以平均α作为常数代入平衡方程式算出各点的“y—x i ”关系,算出由此法得 出各组y i 值的最大相对误差。 t0C 113.7 114.6 115.4 116.3 117.0 117.8 118.6 119.4 120.0
化工原理知识点总结复习重点完美版
化工原理知识点总结复习重点完美版 标准化管理部编码-[99968T-6889628-J68568-1689N]
第一章、流体流动 一、 流体静力学 二、 流体动力学 三、 流体流动现象 四、 流动阻力、复杂管路、流量计 一、流体静力学: 压力的表征:静止流体中,在某一点单位面积上所受的压力,称为静压力,简称压力,俗称压强。 表压强(力)=绝对压强(力)-大气压强(力) 真空度=大气压强-绝对压 大气压力、绝对压力、表压力(或真空度)之间的关系 流体静力学方程式及应用: 压力形式 )(2112z z g p p -+=ρ 备注:1)在静止的、连续的同一液体内,处于同一 能量形式 g z p g z p 22 11 += +ρ ρ 水平面上各点压力都相等。 此方程式只适用于静止的连通着的同一种连续的流体。 应用: U 型压差计 gR p p )(021ρρ-=- 倾斜液柱压差计 微差压差计 二、流体动力学 流量 质量流量 m S kg/s m S =V S ρ 体积流量 V S m 3/s 质量流速 G kg/m 2s (平均)流速 u m/s G=u ρ 连续性方程及重要引论: 一实际流体的柏努利方程及应用(例题作业题) 以单位质量流体为基准:f e W p u g z W p u g z ∑+++=+++ρ ρ2222121121 21 J/kg 以单位重量流体为基准:f e h g p u g z H g p u g z ∑+++=+++ ρρ222212112121 J/N=m 输送机械的有效功率: e s e W m N = 输送机械的轴功率: η e N N = (运算效率进行简单数学变换) m S =GA=π/4d 2 G V S =uA=π/4d 2 u
化工原理第五章吸收题
六吸收 浓度换算 甲醇15%(质量)的水溶液, 其密度为970Kg/m3, 试计算该溶液中甲醇的: (1)摩尔分率; (2)摩尔比; (3)质量比; (4)质量浓度; (5)摩尔浓度。 分子扩散 估算1atm及293K下氯化氢气体(HCl)在(1)空气,(2)水(极稀盐酸)中的扩散系数。 一小管充以丙酮,液面距管口1.1cm,20℃空气以一定速度吹过管口,经5 小时后液面下降到离管口2.05cm,大气压为750[mmHg],丙酮的蒸汽压为180[mmHg] , 丙酮液密度为 7900[kg/m3],计算丙酮蒸汽在空气中的扩散系数。 浅盘内盛水。水深5mm,在1atm又298K下靠分子扩散逐渐蒸发到大气中。假定传质阻力相当于3mm厚的静止气层,气层外的水蒸压可忽略,求蒸发完所需的时间。 一填料塔在常压和295K下操作,用水除去含氨混合气体中的氨。在塔内某处,氨在气相中的组成y a=5%(摩尔百分率)。液相氨的平衡分压P=660Pa,物质通量N A = 10 - 4[kmol/m2·S],气相扩散系数D G=[cm2/s],求气膜的当量厚度。 相平衡与亨利定律 温度为10℃的常压空气与水接触,氧在空气中的体积百分率为21%,求达到平衡时氧在水中的最大浓度, (以[g/m3]、摩尔分率表示)及溶解度系数。以[g/m3·atm]及 [kmol/m3·Pa]表示。 当系统服从亨利定律时,对同一温度和液相浓度,如果总压增大一倍则与之平衡的气相浓度(或分压) (A)Y增大一倍; (B)P增大一倍;(C)Y减小一倍; (D)P减小一倍。 25℃及1atm下,含CO220%,空气80%(体积%)的气体1m3,与1m3的清水在容积2m3的密闭容器中接触进行传质,试问气液达到平衡后, (1)CO2在水中的最终浓度及剩余气体的总压为多少? (2)刚开始接触时的总传质推动力ΔP,Δx各为多少?气液达到平衡时的总传质推动力又为多少?
2017化工课程设计心得体会范文
2017化工课程设计心得体会范文 2017化工课程设计心得体会范文一 化工原理课程设计是综合运用化工原理及相关基础知识的实践性教学环节。设计过程中指导教师指引学生在设计过程中既要考虑理论上的可行性,还要考虑生产上的安全性和经济合理性。通过课程设计使我们初步掌握化工设计的基础知识、设计原则及方法。 本次化工原理课程设计历时两周,是上大学以来第一次独立的工业化设计。从老师以及学长那里了解到化工原理课程设计是培养我们化工设计能力的重要教学环节,通过课程设计使我们初步掌握化工设计的基础知识、设计原则及方法;学会各种手册的使用方法及物理性质、化学性质的查找方法和技巧;掌握各种结果的校核,能画出工艺流程、塔板结构等图形;在设计过程中不仅要考虑理论上的可行性,还要考虑生产上的安全性和经济合理性。由于第一次接触课程设计,起初心里充满了新鲜感和期待,因为自我认为在大学里学到的东西终于可以加以实践了。可是当老师把任务书发到手里是却是一头雾水,完全不知所措。可是在这短短的三周里,从开始的一无所知,到同学讨论,再进行整个流程的计算,再到对工业材料上的选取论证和后期的程序的编写以及流程图的绘制等过程的培养,我真切感受到了理论与实践相结合中的种种困难,也体会到了利用所学的有限的理论知识去解决实际中各种问题的不易。我的课程设计题目是苯――氯苯筛板式精馏塔设计图。在开始时,我们不知道如何下手,虽然有课程设计书作为参
考,但其书上的计算步骤与我们自己的计算步骤有少许差异,在这些差异面前,我们显得有些不知所措,通过查阅《化工原理》,《化工工艺设计手册》,《物理化学》,《化工原理课程设计》等书籍,以及在网上搜索到的理论和经验数据。我们慢慢地找到了符合自己的实验数据。并逐渐建立了自己的模版和计算过程。在这三周中给我印象最深的是我们这些“非泡点一族”在计算进料热状况参数q时,没有任何参考模板,完全靠自己捉摸思考。起初大家都是不知所措,待冷静下来,我们仔细结合上课老师讲的内容,一步一步的讨论演算,经大家一下午的不懈努力,终于把q算出来了。还有就是我们在设计换热器部分,在试差的过程中,我们大部分人都是经历了几乎一天多的时间才选出了合适的换热器型号,现在还清楚的记得我试差成功后那激动的心情,因为我尝到了自己在付出很多后那种成功的喜悦,因为这些都是我们的“血泪史”的见证哈。 在此感谢我们的杜治平老师.,老师严谨细致、一丝不苟的作风一直是我工作、学习中的榜样;老师循循善诱的教导和不拘一格的思路给予我无尽的启迪;这次课程设计的细节和每个数据,都离不开老师您的细心指导。而您开朗的个性和宽容的态度,帮助我能够很顺利的完成了这次课程设计。同时感谢同组的同学们,谢谢你们对我的帮助和支持,让我感受到同学的友谊。由于本人的设计能力有限,在设计过程中难免出现错误,恳请老师们多多指教,我十分乐意接受你们的批评与指正,本人将万分感谢。 2017化工课程设计心得体会范文二
化工原理下册--第六章吸收习题答案
6-1 已知在101.3 kPa(绝对压力下),100 g 水中含氨1 g 的溶液上方的平衡氨气分压为987 Pa 。试求: (1) 溶解度系数H (kmol ·m -3·Pa -1); (2) 亨利系数E(Pa); (3) 相平衡常数m ; (4) 总压提高到200 kPa(表压)时的H ,E ,m 值。 (假设:在上述范围内气液平衡关系服从亨利定律,氨水密度均为1000 3/m kg ) 解:(1)根据已知条件 Pa p NH 987*3= 3/5824.01000 /10117 /13m kmol c NH == 定义 333*NH NH NH H c p = () Pa m kmol p c H NH NH NH ??==-34/109.5333 (2)根据已知条件可知 0105.018 /10017/117 /13=+= NH x 根据定义式 333*NH NH NH x E p = 可得 Pa E NH 41042.93?= (3)根据已知条件可知
00974.0101325/987/* *33===p p y NH NH 于是得到 928.0333*==NH NH NH x y m (4)由于H 和E 仅是温度的函数,故3NH H 和3NH E 不变;而 p E px Ex px p x y m ====** ,与T 和p 相关,故309.0928.03 1' 3 =?=NH m 。 分析(1)注意一些近似处理并分析其误差。 (2)注意E ,H 和m 的影响因素,这是本题练习的主要内容之一。 6-2 在25℃下,CO 2分压为50 kPa 的混合气分别与下述溶液接触: (1) 含CO 2为0.01 mol/L 的水溶液; (2) 含CO 2为0.05 mol/L 的水溶液。 试求这两种情况下CO 2的传质方向与推动力。 解: 由亨利定律得到 * 2 250CO CO Ex kPa p == 根据《 化工原理》 教材中表 8-1 查出 ()kPa E CO 51066.1252?=℃ 所以可以得到 4 *1001.32 -?=CO x 又因为 ()()345 25/10347.318 1066.11000 22 2m kPa kmol EM H O H O H CO ??=??= ≈ -ρ℃ 所以得
化工原理答案-第五章--吸收
第五章 吸收 相组成的换算 【5-1】 空气和2的混合气体中,2的体积分数为20%,求其摩尔分数y 和摩尔比Y 各为多少? 解 因摩尔分数=体积分数,.02y =摩尔分数 摩尔比 ..020251102 y Y y = ==--. 【5-2】 20℃的l00g 水中溶解3, 3在溶液中的组成用摩尔分数x 、浓度c 及摩尔比X 表示时,各为多少? 解 摩尔分数//117 =0.010*******/18 x = + 浓度c 的计算20℃,溶液的密度用水的密度./39982s kg m ρ=代替。 溶液中3的量为 /3 11017n kmol -=? 溶液的体积 /.3 3101109982 V m -=? 溶液中 3的浓度//.333 11017==0.581/101109982 n c kmol m V --?=? 或 . 39982 00105058218 s s c x kmol m M ρ= = ?=../ 3 与水的摩尔比的计算 //117 0010610018 X = =. 或 ..00105001061100105 x X x = ==--. 【5-3】进入吸收器的混合气体中,3的体积分数为10%,吸收率为90%,求离开吸收器时3的组成,以摩尔比Y 和摩尔分数y 表示。 吸收率的定义为
12 2 11 1Y Y Y Y Y η-= ==-被吸收的溶质量原料气中溶质量 解 原料气中3的摩尔分数0.1y = 摩尔比 (11) 101 01111101 y Y y = ==-- 吸收器出口混合气中3的摩尔比为 () (2) 1 1109011100111Y Y η=-=-?=() 摩尔分数 (22) 200111 =0010981100111 Y y Y = =++ 气液相平衡 【5-4】 l00g 水中溶解lg 3 NH ,查得20℃时溶液上方3 NH 的平衡 分压为798。此稀溶液的气液相平衡关系服从亨利定律,试求亨利系数E(单位为kPa )、溶解度系数H[单位为/()3 kmol m kPa ?]和相平衡常数m 。 总压为100kPa 。 解 液相中3 NH 的摩尔分数/.//117 0010511710018 x = =+ 气相中3NH 的平衡分压 *.0798 P kPa = 亨利系数 *./.0798*******E p x ===/ 液相中3NH 的浓度 /./.333 11017 0581 101109982 n c kmol m V --?===?/ 溶解度系数 /*./../()3 058107980728H c p kmol m kPa ===? 液相中3NH 的摩尔分数 //117 0010511710018 x = =+./ 气相的平衡摩尔分数 **.0798100y p p ==// 相平衡常数 * (0798) 07610000105 y m x == =? 或 //.76100076m E p === 【5-5】空气中氧的体积分数为21%,试求总压为.101325kPa ,温度为10℃时,3 1m 水中最大可能溶解多少克氧?已知10℃时氧在水中的
化工原理实验报告
化工原理实验报告
————————————————————————————————作者:————————————————————————————————日期: ?
实验一 伯努利实验 一、实验目的 1、熟悉流体流动中各种能量和压头的概念及相互转化关系,加深对柏努利方程式的理解。 2、观察各项能量(或压头)随流速的变化规律。 二、实验原理 1、不可压缩流体在管内作稳定流动时,由于管路条件(如位置高低、管径大小等)的变化,会引起流动过程中三种机械能——位能、动能、静压能的相应改变及相互转换。对理想流体,在系统内任一截面处,虽然三种能量不一定相等,但能量之和是守恒的(机械能守恒定律)。 2、对于实际流体,由于存在内磨擦,流体在流动中总有一部分机械能随磨擦和碰撞转化为热能而损失。故而对于实际流体,任意两截面上机械能总和并不相等,两者的差值即为机械损失。 3、以上几种机械能均可用U 型压差计中的液位差来表示,分别称为位压头、动压头、静压头。当测压直管中的小孔(即测压孔)与水流方向垂直时,测压管内液柱高度(位压头)则为静压头与动压头之和。任意两截面间位压头、静压头、动压头总和的差值,则为损失压头。 4、柏努利方程式 ∑+++=+++f h p u gz We p u gz ρ ρ2222121122 式中: 1Z 、2Z ——各截面间距基准面的距离 (m) 1u 、2u ——各截面中心点处的平均速度(可通过流量与其截 面积求得) (m/s) 1P 、2p ——各截面中心点处的静压力(可由U型压差计的液位 差可知) (Pa ) 对于没有能量损失且无外加功的理想流体,上式可简化为 ρ ρ2 2 22121122p u gz p u gz + +=++ 测出通过管路的流量,即可计算出截面平均流速ν及动压g 22 ν,从而可得到各截面测管水头和总水头。 三、实验流程图
南工大化工原理第六章习题解答
第六章习题 1)苯酚(C6H5OH)(A)和对甲酚(C6H4(CH3)OH)(B)的饱和蒸汽压数据为: 温度 ℃苯酚蒸汽压 kPa 对甲酚蒸汽压 kPa 温度 ℃ 苯酚蒸汽压 kPa 对甲酚蒸汽 压 kPa 试按总压P=75mmHg(绝压)计算该物系的“t—x—y”数据。此物系为理想物系。 t0C p A0kPa p B0kPa x A x B 2)承第1题,利用各组数据,计算 ①在x=0至x=1范围内各点的相对挥发度αi,取各αi的算术平均值α,算出α对αi的最大相对误差。 ②以平均α作为常数代入平衡方程式算出各点的“y—x i”关系,算出由此法得出各组y i值的最大相对误差。 t0C
t0C x i0 y i0最大误差= 3)已知乙苯(A)与苯乙烯(B)的饱和蒸汽压与温度的关系可按下式算得: 式中p0的单位是mmHg,T的单位是K。 问:总压为60mmHg(绝压)时,A与B的沸点各为多少℃在上述总压和65℃时,该物系可视为理想物系。此物系的平衡汽、液相浓度各为多少摩尔分率
4)苯(A)和甲苯(B)混合液可作为理想溶液,其各纯组分的蒸汽压计算式为 式中p0的单位是mmHg,t的单位是℃。 试计算总压为850mmHg(绝压)下含苯25%(摩尔百分率)的该物系混合液的泡点。 5)试计算总压为760mmHg(绝压)下,含苯、甲苯(摩尔分率)的混合蒸汽的露点。若令该二元物系降温至露点以下3℃,求平衡的汽、液相摩尔之比。
6)有一苯(A)、甲苯(B)、空气(C)的混合气体,其中空气占2%,苯与甲苯浓度相等(均指摩尔百分数),气体压强为760mmHg(绝压)。若维持压强不变,令此三元物系降温至95℃,求所得平衡汽相的组成。A、B组分均服 从拉乌尔定律。已知95℃时,。 设X A 算得的X‘A 7)常压下将含苯(A)60%,甲苯(B)40%(均指摩尔百分数)的混合液闪蒸(即平衡蒸馏),得平衡汽、液相,汽相摩尔数占总摩尔数的分率——汽化率(1-q)为。物系相对挥发度α=,试求:闪蒸所得平衡汽、液相的浓度。
化工原理下复习小结
蒸 馏––––基本概念和基本原理 利用各组分挥发度不同将液体混合物部分汽化而使混合物得到分离的单元操作称为蒸馏。这种分离操作是通过液相和气相之间的质量传递过程来实现的。 对于均相物系,必须造成一个两相物系才能将均相混合物分离。蒸馏操作采用改变状态参数的办法(如加热和冷却)使混合物系内部产生出第二个物相(气相);吸收操作中则采用从外界引入另一相物质(吸收剂)的办法形成两相系统。 一、两组分溶液的气液平衡 1. 拉乌尔定律 理想溶液的气液平衡关系遵循拉乌尔定律: p A =p A 0x A p B =p B 0x B =p B 0(1-x A ) 根据道尔顿分压定律:p A =Py A 而P =p A +p B 则两组分理想物系的气液相平衡关系: B A A B P p x p p -= -———泡点方程 0A A A p x y P = ———露点方程 对于任一理想溶液,利用一定温度下纯组分饱和蒸汽压数据可求得平衡的气液相组成;反之,已知一相组成,可求得与之平衡的另一相组成和温度(试差法)。 2. 用相对挥发度表示气液平衡关系 溶液中各组分的挥发度v 可用它在蒸汽中的分压和与之平衡的液相中的摩尔分率来表示,即 B A B B =A A p p x x υυ= 溶液中易挥发组分的挥发度对难挥发组分的挥发度之比为相对挥发度。其表达式有: A A B A B A B B B A y x p p x x y x υαυ= == 对于理想溶液: 0 A B p p α= 气液平衡方程:1(1)x y x αα= +- α值的大小可用来判断蒸馏分离的难易程度。α愈大,挥发度差异愈大,分离愈易;α=1时不能用普通精馏方法分离。 3. 气液平衡相图 (1)温度—组成(t -x -y )图 该图由饱和蒸汽线(露点线)、饱和液体线(泡点线)组成,饱和液体线以下区域为液相区,饱和蒸汽线上方区域为过热蒸汽区,两曲线之间区域为气液共存区。 气液两相呈平衡状态时,气液两相温度相同,但气相组成大于液相组成;若气液两相组成相同,则气相露点温度大于液相泡点温度。 (2)x -y 图 x -y 图表示液相组成x 与之平衡的气相组成y 之间的关系曲线图,平衡线位于对角线的上方。平衡线偏
化工原理实验实验报告
篇一:化工原理实验报告吸收实验 姓名 专业月实验内容吸收实验指导教师 一、实验名称: 吸收实验 二、实验目的: 1.学习填料塔的操作; 2. 测定填料塔体积吸收系数kya. 三、实验原理: 对填料吸收塔的要求,既希望它的传质效率高,又希望它的压降低以省能耗。但两者往往是矛盾的,故面对一台吸收塔应摸索它的适宜操作条件。 (一)、空塔气速与填料层压降关系 气体通过填料层压降△p与填料特性及气、液流量大小等有关,常通过实验测定。 若以空塔气速uo[m/s]为横坐标,单位填料层压降?p[mmh20/m]为纵坐标,在z ?p~uo关系z双对数坐标纸上标绘如图2-2-7-1所示。当液体喷淋量l0=0时,可知 为一直线,其斜率约1.0—2,当喷淋量为l1时,?p~uo为一折线,若喷淋量越大,z ?p值较小时为恒持z折线位置越向左移动,图中l2>l1。每条折线分为三个区段, 液区,?p?p?p~uo关系曲线斜率与干塔的相同。值为中间时叫截液区,~uo曲zzz ?p值较大时叫液泛区,z线斜率大于2,持液区与截液区之间的转折点叫截点a。 姓名 专业月实验内容指导教师?p~uo曲线斜率大于10,截液区与液泛区之间的转折点叫泛点b。在液泛区塔已z 无法操作。塔的最适宜操作条件是在截点与泛点之间,此时塔效率最高。 图2-2-7-1 填料塔层的?p~uo关系图 z 图2-2-7-2 吸收塔物料衡算 (二)、吸收系数与吸收效率 本实验用水吸收空气与氨混合气体中的氨,氨易溶于水,故此操作属气膜控制。若气相中氨的浓度较小,则氨溶于水后的气液平衡关系可认为符合亨利定律,吸收姓名 专业月实验内容指导教师平均推动力可用对数平均浓度差法进行计算。其吸收速率方程可用下式表示: na?kya???h??ym(1)式中:na——被吸收的氨量[kmolnh3/h];?——塔的截面积[m2] h——填料层高度[m] ?ym——气相对数平均推动力 kya——气相体积吸收系数[kmolnh3/m3·h] 被吸收氨量的计算,对全塔进行物料衡算(见图2-2-7-2): na?v(y1?y2)?l(x1?x2) (2)式中:v——空气的流量[kmol空气/h] l——吸收剂(水)的流量[kmolh20/h] y1——塔底气相浓度[kmolnh3/kmol空气] y2——塔顶气相浓度[kmolnh3/kmol空气] x1,x2——分别为塔底、塔顶液相浓度[kmolnh3/kmolh20] 由式(1)和式(2)联解得: kya?v(y1?y2)(3) ??h??ym 为求得kya必须先求出y1、y2和?ym之值。 1、y1值的计算:
化工原理第六章吸收习题答案解析
6-1 已知在 kPa(绝对压力下),100 g 水中含氨1 g 的溶液上方的平衡氨气分压为987 Pa 。试求: (1) 溶解度系数H (kmol ·m -3·Pa -1); (2) 亨利系数E(Pa); (3) 相平衡常数m ; (4) 总压提高到200 kPa(表压)时的H ,E ,m 值。 (假设:在上述范围内气液平衡关系服从亨利定律,氨水密度均为 10003/m kg ) 解:(1)根据已知条件 Pa p NH 987*3= 3/5824.01000 /10117 /13m kmol c NH == 定义 333*NH NH NH H c p = () Pa m kmol p c H NH NH NH ??==-34/109.5333 (2)根据已知条件可知 0105.018 /10017/117 /13=+= NH x 根据定义式 333*NH NH NH x E p = 可得 Pa E NH 41042.93?= (3)根据已知条件可知 00974.0101325/987/* *33===p p y NH NH 于是得到 928.0333*==NH NH NH x y m (4)由于H 和E 仅是温度的函数,故3NH H 和3NH E 不变;而 p E px Ex px p x y m ====** ,与T 和p 相关,故309.0928.03 1' 3 =?=NH m 。 分析(1)注意一些近似处理并分析其误差。 (2)注意E ,H 和m 的影响因素,这是本题练习的主要内容之一。
6-2 在25℃下,CO 2分压为50 kPa 的混合气分别与下述溶液接触: (1) 含CO 2为 mol/L 的水溶液; (2) 含CO 2为 mol/L 的水溶液。 试求这两种情况下CO 2的传质方向与推动力。 解: 由亨利定律得到 * 2 250CO CO Ex kPa p == 根据《 化工原理》 教材中表 8-1 查出 ()kPa E CO 51066.1252?=℃ 所以可以得到 4 *1001.32 -?=CO x 又因为 ()()3 45 25/10347.318 1066.1100022 2m kPa kmol EM H O H O H CO ??=??= ≈ -ρ℃ 所以得 3 4*/0167.05010347.32 22m kmol p H c CO CO CO =??==- 于是:(1)为吸收过程,3/0067.0m kmol c =?。 (2)为解吸过程,3/0333.0m kmol c =?。 分析 (1)推动力的表示方法可以有很多种,比如,用压力差表示时: ① kPa H c p CO CO CO 9.2910347.301 .04 * 2 22 =?= = - 推动力 kPa p 1.20=?(吸收)
化工原理第五章吸收课后习题及答案
第五章 吸收 相组成的换算 【5-1】 空气和CO 2的混合气体中,CO 2的体积分数为20%,求其摩尔分数y 和摩尔比Y 各为多少? 解 因摩尔分数=体积分数,.02y =摩尔分数 摩尔比 ..02 0251102 y Y y = ==--. 【5-2】 20℃的l00g 水中溶解lgNH 3, NH 3在溶液中的组成用摩尔分数x 、浓度c 及摩尔比X 表示时,各为多少? 解 摩尔分数//117 =0.010*******/18 x = + 浓度c 的计算20℃,溶液的密度用水的密度./39982s kg m ρ=代替。 溶液中NH 3的量为 /3 11017n k m o l -=? 溶液的体积 /.33101109982 V m -=? 溶液中NH 3的浓度//.333 11017==0.581/101109982 n c kmol m V --?=? 或 . 39982 00105058218 s s c x kmol m M ρ= = ?=../ NH 3与水的摩尔比的计算 或 ..00105001061100105 x X x = ==--. 【5-3】进入吸收器的混合气体中,NH 3的体积分数为10%,吸收率为90%,求离开吸收器时NH 3的组成,以摩尔比Y 和摩尔分数y 表示。 吸收率的定义为 解 原料气中NH 3的摩尔分数0.1y = 摩尔比 (11101) 01111101 y Y y = ==-- 吸收器出口混合气中NH 3的摩尔比为 摩尔分数 (22200111) =0010981100111 Y y Y = =++ 气液相平衡 【5-4】 l00g 水中溶解lg 3 NH ,查得20℃时溶液上方3NH 的平衡分压为798Pa 。此稀溶液的气液相平衡关系服从亨利定律,试求亨利系数E(单位为kPa )、溶解度系数H[单位为/()3kmol m kPa ?]和相平衡常数m 。总压为100kPa 。 解 液相中3NH 的摩尔分数/.//117 0010511710018 x = =+ 气相中3NH 的平衡分压 *.0798 P k P a =
化工原理实验心得体会
化工原理实验心得体会 这个学期我们学习了《化工原理》这门课,在学习了部分理论知识后,我们进入了实验室,开始学习《化工原理实验》并分组进行了实验。和前几个学期类似,大家先要进行实验的预习,在了解和熟悉实验的要求和操作的基础上,然后在老师提问检查每一组各位组员对实验过程的预习程度后,对各位组员的预习情况进行点评,并指出其中的不足和缺漏。然后在指导老师的悉心讲解后,对实验有一个新的、更全面的认识后进行实验。通过动手实验,我更加深刻的理解了化工原理课上老师讲解的知识,增强了动手能力,对理论知识有了形象化的认识。 本学期我们共学习了五个实验,分别是: 实验一、离心泵的特性曲线实验; 实验二、流体流动阻力的测定; 实验三、空气—蒸汽对流传热系数的测定; 实验四、恒压过滤常数的测定; 实验五、填料塔的精馏实验, 通过对实验的学习并亲手操作,我掌握了许多知识。 这几个实验中我印象最深刻的是恒压过滤常数的测定,实验以生活中常见的碳酸钙的水浆液位测定原料。这个实验和空气—蒸汽对流传热系数的测定实验一起分组进行。老师讲解完实验原
理并强调了注意事项后,我们开始实验。我们小组先进行了恒压 过滤常数测定实验,首先我们对两个小组的成员进行了各项职责 的分配分别是:两位同学负责碳酸钙水浆液的搅拌和回收,由一 位同学负责数据的采集和记录的工作。每个三分钟记录床层温度 一次,取样一次,并由同组同学进行含水量的测定,由两位同学 负责装好板框,最后分别由其他两位同学负责压力阀的控制和滤 液进口阀、滤液出口阀的控制。这样一来整个实验的分工工作就 已经完成了。实验过程中,我们互相配合,进行的很顺利。但是 在第一次实验时由于我们的粗心大意,我们将四块滤板中的一块 方向装反了,使得我们第一次采集的数据无效了,因此指导老师 还对我们实验时的粗心大意进行了严厉的批评教育,这些批评教 育使我们牢记在这是一个教训,实验中细心认真完成每一步,我 们的动手能力才会在这个过程中得到提升。 在这一个学期短暂的实验学习过程中,使我们重新认识了在 大学学习生活中,在实验过程中一个实验者的认真预习和摈弃粗 心大意,认真、谨慎的进行好每一步的操作、合理的分工协同工 作对于一个实验的成败与否是至关重要的。或许在将来生活工作 中也一样,俗话说得好,所谓“细节决定成败”。一个做事粗心 大意,做事前从不做准备的人不管他将来从事什么样的工作都无 法取得好的成绩,因为在他的心理或许压根就没有重视过自己所 从事的事情或者是行业。俗话说“机遇永远是给有准备的人的”。 化工原理实验的任务主要是了解一些典型化工设备的原理和
化工原理各章节知识点总结
第一章流体流动 质点含有大量分子的流体微团,其尺寸远小于设备尺寸,但比起分子自由程 却要大得多。 连续性假定假定流体是由大量质点组成的、彼此间没有间隙、完全充满所占空间的连续介质。 拉格朗日法选定一个流体质点,对其跟踪观察,描述其运动参数(如位移、速度等)与时间的关系。 欧拉法在固定空间位置上观察流体质点的运动情况,如空间各点的速度、压强、密度等,即直接描述各有关运动参数在空间各点的分布情况和随时间的变化。定态流动流场中各点流体的速度u 、压强p不随时间而变化。 轨线与流线轨线是同一流体质点在不同时间的位置连线,是拉格朗日法考察的结果。流线是同一瞬间不同质点在速度方向上的连线,是欧拉法考察的结果。系统与控制体系统是采用拉格朗日法考察流体的。控制体是采用欧拉法考察流体的。 理想流体与实际流体的区别理想流体粘度为零,而实际流体粘度不为零。粘性的物理本质分子间的引力和分子的热运动。通常液体的粘度随温度增 加而减小,因为液体分子间距离较小,以分子间的引力为主。气体的粘度随温度上升而增大,因为气体分子间距离较大,以分子的热运动为主。 总势能流体的压强能与位能之和。 可压缩流体与不可压缩流体的区别流体的密度是否与压强有关。有关的称为可压缩流体,无关的称为不可压缩流体。 伯努利方程的物理意义流体流动中的位能、压强能、动能之和保持不变。平均流速流体的平均流速是以体积流量相同为原则的。 动能校正因子实际动能之平均值与平均速度之动能的比值。 均匀分布同一横截面上流体速度相同。 均匀流段各流线都是平行的直线并与截面垂直,在定态流动条件下该截面上
的流体没有加速度, 故沿该截面势能分布应服从静力学原理。 层流与湍流的本质区别是否存在流体速度u、压强p的脉动性,即是否存在流体质点的脉动性。 稳定性与定态性稳定性是指系统对外界扰动的反应。定态性是指有关运动参数随时间的变化情况。 边界层流动流体受固体壁面阻滞而造成速度梯度的区域。 边界层分离现象在逆压强梯度下,因外层流体的动量来不及传给边界层,而形成边界层脱体的现象。 雷诺数的物理意义雷诺数是惯性力与粘性力之比。 量纲分析实验研究方法的主要步骤: ①经初步实验列出影响过程的主要因素; ②无量纲化减少变量数并规划实验; ③通过实验数据回归确定参数及变量适用围,确定函数形式。 摩擦系数 层流区,λ与Re成反比,λ与相对粗糙度无关; 一般湍流区,λ随Re增加而递减,同时λ随相对粗糙度增大而增大; 充分湍流区,λ与Re无关,λ随相对粗糙度增大而增大。 完全湍流粗糙管当壁面凸出物低于层流层厚度,体现不出粗糙度过对阻力 损失的影响时,称为水力光滑管。Re很大,λ与Re无关的区域,称为完全湍流粗糙管。同一根实际管子在不同的Re下,既可以是水力光滑管,又可以是完全湍流粗糙管。 局部阻力当量长度把局部阻力损失看作相当于某个长度的直管,该长度即为局部阻力当量长度。 毕托管特点毕托管测量的是流速,通过换算才能获得流量。 驻点压强在驻点处,动能转化成压强(称为动压强),所以驻点压强是静压强与动压强之和。 孔板流量计的特点恒截面,变压差。结构简单,使用方便,阻力损失较大。转子流量计的特点恒流速,恒压差,变截面。 非牛顿流体的特性 塑性:只有当施加的剪应力大于屈服应力之后流体才开始流动。
化工原理实习心得
化工原理实习心得 化工原理实习是对化工原理知识的一个实践过程, 下面化工原理实习心得是想跟大家分享的,欢迎大家浏览。 第一篇:化工原理实习心得 在实习的过程中,自己学到了许多原先在课本上学 不到的东西,而且可以使自己更进一步接近社会,体会 到市场跳动的脉搏,如果说在象牙塔是看市场,还是比 较感性的话,那么当你身临企业,直接接触到企业的生 产与销售的话,就理性得多。因为,在市场的竞争受市 场竞争规则的约束,从采购、生产到销售都与市场有着 千丝万缕的联系,如何规避风险,如何开拓市场,如何 保证企业的生存发展,这一切的一切都是那么的现实。 于是理性的判断就显得重要了。在企业的实习过程中, 我发现了自己看问题的角度,思考问题的方式也逐渐开拓,这与实践密不可分,在实践过程中,我又一次感受 充实,感受成长。 通过安排到xxx车间进行实习,了解产品生产工艺 流程、职能部门的设置及其职能,了解企业的内部控制,在这一个多月的时间里,下到生产车间后,先了解整个 xxx生产的流程,从采购入库,到领料生产,到最后的
成品入罐,对整个车间的生产活动有了基本认识,这对 我们熟悉企业,进行实务操作打下良好基础。 其中,先前我们对xxx的生产几乎一无所知,但下 到车间之后,我们不仅了解了生产流程,还进一步了解 了xxx的生产工艺流程和用途,由于脂肪酸生产完后是直接用于公司后面的扬子石化生产,所以每个月的生产有一定的额度.而且由于季节和温度等条件的限制,机器开工的时间长度及强度也有相关的规定,另外,对一些流水 线的参观,也激发了我对如何通过新流水线的建设,对 降低生产成本的思考,于是,感受颇深的一点,要做一 名合格的会计人员,对基本、基础的作业环节是要了解的,否则,很容易让理论脱离实践. 在熟悉了车间的生产流程后,工作人员拿了以前的 交接班记录和中间产品申请单和报表等资料给我们看, 在翻看这些资料的过程中,有不懂或弄不清楚的资料, 积极向同事请教,在他们的耐心指导下,我们对车间的 整个产品检验的程序方法有了一定上的认识。 由于化工生产是不间断的,所以车间生产必须时刻有人,车间的工作人员采取四班两倒(一天白班12小时一天晚班休两天)和常白班制度.我们车间有四个人(主任,工 艺员,等)上长白班,其他人分成甲乙丙丁四个班四班两倒. 虽然我们没有正式分配,但我们都严格遵守车间的生
化工原理知识点总结
一、流体力学及其输送 1.单元操作:物理化学变化的单个操作过程,如过滤、蒸馏、萃取。 2.四个基本概念:物料衡算、能量衡算、平衡关系、过程速率。 3.牛顿粘性定律:F=±τA=±μAdu/dy ,(F :剪应力;A :面积;μ:粘度;du/dy :速度梯度)。 4.两种流动形态:层流和湍流。流动形态的判据雷诺数Re=duρ/μ;层流—2000—过渡—4000—湍流。当流体层流时,其平均速度是最大流速的1/2。 5.连续性方程:A1u1=A2u2;伯努力方程:gz+p/ρ+1/2u2=C 。 6.流体阻力=沿程阻力+局部阻力;范宁公式:沿程压降:Δpf=λlρu2/2d ,沿程阻力:Hf=Δpf/ρg=λl u2/2dg(λ:摩擦系数);层流时λ=64/Re ,湍流时λ=F(Re ,ε/d),(ε:管壁粗糙度);局部阻力hf=ξu2/2g ,(ξ:局部阻力系数,情况不同计算方法不同) 7.流量计:变压头流量计(测速管、孔板流量计、文丘里流量计);变截面流量计。孔板流量计的特点;结构简单,制造容易,安装方便,得到广泛的使用。其不足之处在于局部阻力较大,孔口边缘容易被流体腐蚀或磨损,因此要定期进行校正,同时流量较小时难以测定。 转子流量计的特点——恒压差、变截面。 8.离心泵主要参数:流量、压头、效率(容积效率?v :考虑流量泄漏所造成的能量损失;水力效率?H :考虑流动阻力所造成的能量损失;机械效率?m :考虑轴承、密封填料和轮盘的摩擦损失。)、轴功率;工作点(提供与所需水头一致);安装高度(气蚀现象,气蚀余量);泵的型号(泵口直径和扬程);气体输送机械:通风机、鼓风机、压缩机、真空泵。 9. 常温下水的密度1000kg/m3,标准状态下空气密度1.29 kg/m3 1atm =101325Pa=101.3kPa=0.1013MPa=10.33mH2O=760mmHg (1)被测流体的压力 > 大气压 表压 = 绝压-大气压 (2)被测流体的压力 < 大气压 真空度 = 大气压-绝压= -表压 10. 管路总阻力损失的计算 11. 离心泵的构件: 叶轮、泵壳(蜗壳形)和 轴封装置 离心泵的叶轮闭式效率最高,适用于输送洁净的液体。半闭式和开式效率较低,常用于输送浆料或悬浮液。 气缚现象:贮槽内的液体没有吸入泵内。汽蚀现象:泵的安装位置太高,叶轮中各处压强高于被输送液体的饱和蒸汽压。原因(①安装高度太高②被输送流体的温度太高,液体蒸汽压过高;③吸入管路阻力或压头损失太高)各种泵:耐腐蚀泵:输送酸、碱及浓氨水等腐蚀性液体 12. 往复泵的流量调节 (1)正位移泵 流量只与泵的几何尺寸和转速有关,与管路特性无关,压头与流量无关,受管路的承压能力所限制,这种特性称为正位移性,这种泵称为正位移泵。 往复泵是正位移泵之一。正位移泵不能采用出口阀门来调节流量,否则流量急剧上升,导致示损坏。 (2)往复泵的流量调节 第一,旁路调节,如图2-28所示,采用旁路阀调节主管流量,但泵的流量是不变的。 第二,改变曲柄转速和活塞行程。使用变速电机或变速装置改变曲柄转速,达到调 节流量,使用蒸汽机则更为方便。改变活塞行程则不方便。 13.流体输送机械分类 14.离心泵特性曲线: 222'2e 2e 2u d l l u d l l u d l h h h f f f ??? ? ??++=???? ??+=??? ??+=+=∑∑∑∑∑∑ζλλζλ
化工原理第五章吸收课后习题及答案.doc
第五章 吸收 相组成的换算 【5-1】 空气和 CO 2 的混合气体中, CO 2的体积分数为 20%,求其摩尔分数 y 和摩尔比 Y 各为多少? 解 因摩尔分数 =体积分数, y 0.2 摩尔分数 y 0 2 摩尔比 Y . 025. 1 y 1 0 2 . 【5-2】 20℃的 l00g 水中溶解 lgNH 3, NH 3 在溶液中的组成用摩尔分数 x 、浓度 c 及摩尔 比 X 表示时,各为多少? 解 摩尔分数 x 1 / 17 =0.0105 1 / 17 100/18 浓度 c 的计算 20℃,溶液的密度用水的密度 s 998 .2kg / m 3 代替。 3 n 1 10 3 / 17kmol 溶液中 NH 的量为 溶液的体积 V 101 10 3 / 998.2 m 3 溶液中 NH 3 的浓度 n 1 10 3 /17 3 c = =0.581 / m V 101 10 3 998 2 kmol /. s 998 2 3 或 c x . 0 0105 0 582 M s 18 . . kmol /m NH 3 与水的摩尔比的计算 1 /17 X 0.0106 100 / 18 x 0 0105 或 X . 0.0106 1 x 1 0 0105 . 【 5-3 】进入吸收器的混合气体中, NH 3 的体积分数为 10%,吸收率为 90%,求离开吸收器 时 NH 3 的组成,以摩尔比 Y 和摩尔分数 y 表示。 吸收率的定义为 被吸收的溶质量 Y 1 Y 2 1 Y 2 原料气中溶质量 1 1 Y Y 解 原料气中 NH 3 的摩尔分数 y 0.1 1 0 1 摩尔比 1 y . 0 111 1 1 0 1 Y 1 y . 吸收器出口混合气中 NH 3 的摩尔比为 Y 1 Y (1 09)0111 0 0111 2 ( ) 1 .. . 摩尔分数 Y 2 = 0 0111 0 01098 y 2 1 1 . Y 2 0 0111 . . 气液相平衡 【 5-4 】 l00g 水中溶解 lg NH 3 ,查得 20℃时溶液上方 NH 3 的平衡分压为 798Pa 。此稀
化工原理实验心得
实验心得 09生物工程一班钟鑫鑫20091466 经过这一学期的理论课学习和相关的实验操作,我认识到化工原理实验属于工程实验的范畴,它是用自然科学的基本原理和工程实验方法来解决化工及相关领域的工程实际问题。它与一般化学实验的不同之处在于它具有明显的工程特点,研究对象和研究方法也与物理化学等基础学科明显不同。工程实验以实际工程问题为研究对象,对于化学工程问题,由于被加工的物料千变万化,设备大小和形状相差悬殊,涉及的变量繁多,实验研究的工作量之大之难是可想而知的,因此,面对实际的工程问题我们采用处理实际问题的工程实验方法。一个化工过程往往由很多单元过程和设备组成为了进行完善的设计和有效的操作,我们必须掌握并正确判断有关设计或操作参数的可靠性,必须准确了解并把握设备的特性。化工过程的影响因素众多,有些重要工程因素的影响难以从理论上解释,还有些关键的设备特性和过程参数往往不能由理论计算而得,这些都必须通过实验加以研究解决。另外我们还学习操作了计算机仿真技术,模拟真实的化工过程,运用全数字化动态模型深入了解化工过程系统的操作原理。在加深对实验原理理解的基础上,可通过反复操作,握实验步骤为实际操作做好充分准备,同时培养了我们理论联系实际的能力提高了独立思考和独立工作的能力。 本学期我们学习了六个实验。例如:流体流动阻力的测定认识和掌握流体流动阻力实验的一般实验方法,来测定直管的摩擦阻力系数λ和突然扩大管和阀门的局部阻力系数ξ,还有层流管的摩擦阻力与雷诺数Re 的关系(λ=64/Re),同时验证湍流区内摩擦阻力系数λ为雷诺数Re 和相对粗糙度的函数λ=f(Re,ε/d)。离性泵性能实验通过实验了解离心泵的构造,并掌握其操作和调节方法,测定了离心泵在恒定转速下的特性曲线(He~Q,N 轴~Q,η~Q),并却确定泵的最佳工作范围,熟悉了孔板流量计的构造,测定其孔流系数与雷诺数的关系,还测定了管路特性曲线。(一)雷诺演示实验通过实验建立对层流和湍流两种流动类型的直观感性认识,观测雷诺数与流体流动类型的相互关系,观察层流中流体质点的速度分布(二)流体机械能转换演示实验通过实测静止和流动的流体中各项压头及其相互转换,验证流体静力学原理和伯努利方程,还通过实测流速的变化与之相应的压头损失的变化,确定两者之间的关系。通过这五个实验的学习,我学到最重要的一点就是:理论联系实际。它们将单元操作实验与实验技术的应用融为一体,实现了我们实验技术基本功的训练。三个验证试验也正是我们这学期化工原理理论课学习的重点内容,具体的实验操作让我们在理解理论的基础上加深了对化工操作的认识,这在工程理念上对我们以后从事科研或者工作都是一个很大的转折点。而且我发现我们学校的实验室设备相对其他工科高校来说是很齐全的,为我们提供了很好的实训环境,这在一定程度上大大提高了我们的操作能力竞争优势。实验前的预习和准备对实验操作来说是不可小觑的,如果能做到像老师那样对操作步骤和实验原理了然于心,那么实验操作时必然能达到游刃有余的地步,我也始终觉得实验预习是非常重要的环节,也是思考范围最不受局限的阶段,可以带着各种问题和验证性的假设进入实验室并在自己动手之后得到答案,进而思考操作意义,还能获得老师的经验指导,我相信这对每一个实验员来说都是值得令人欣喜的事。所以对于进实验室的我们来说,“有备而来”是至关重要的。实验中的数据处理也接近工程实验的范畴,我们采用了计算机处理,解决了实验数据量大繁杂及绘图技巧上的一系列问题。每次完成报告之前我都有尝试换一种方式,不看课本,就回想实验操作,根据每一步的操作来想实验原理,用自己的话陈述操作步骤,除了完成基本的报告要求,还会把实验创新方面的问题也提进来,可我总觉得有些使不上劲,不敢下笔,归结原因是自己理论知识还不够丰厚,这就提醒了我在以后的实验中需要做更多准备。另外一点就是培养了我们独立思考的能力和团队合作的精神,比如实验中相关参数的确定都是需要综合考虑设备及环境因素来
