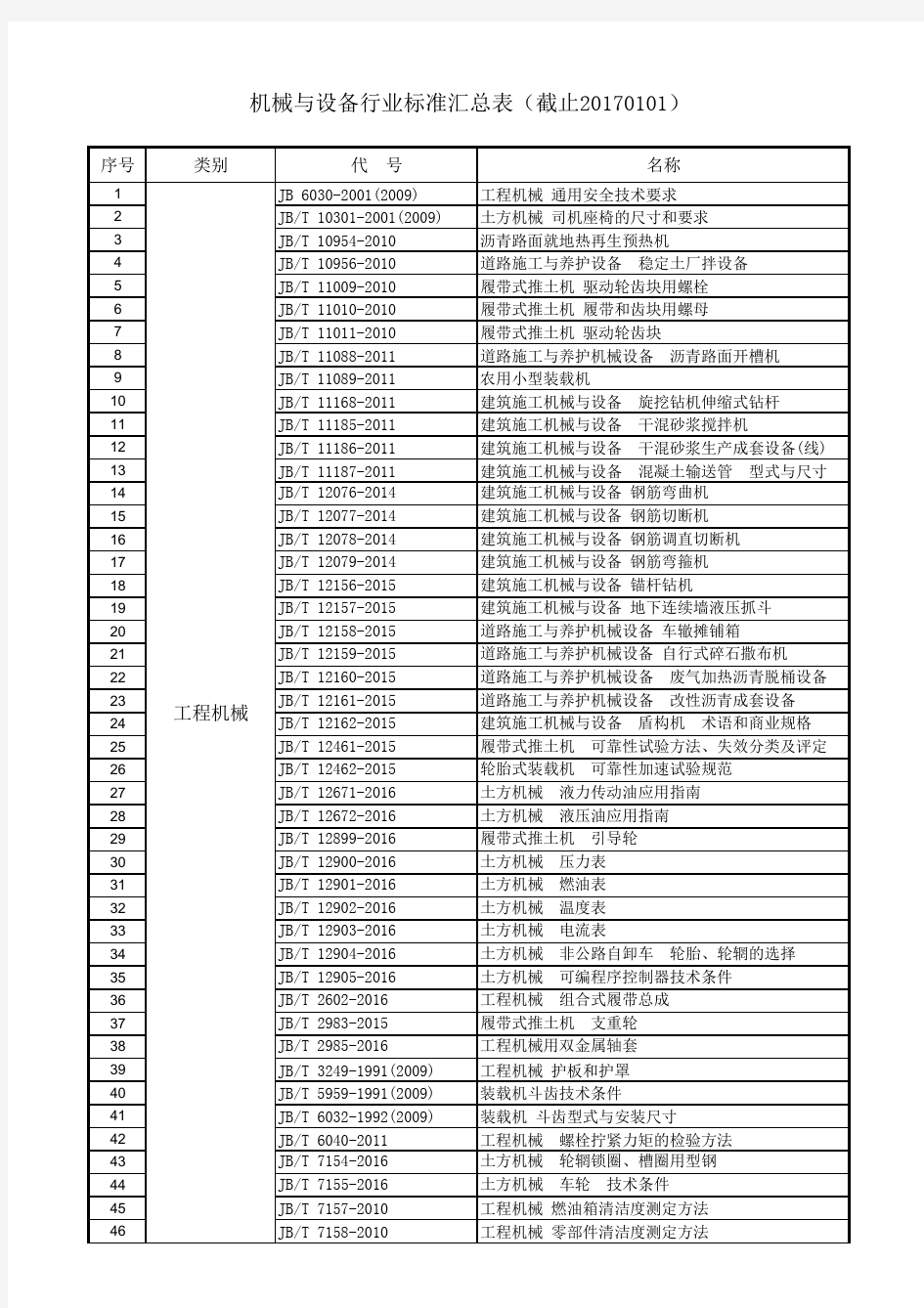
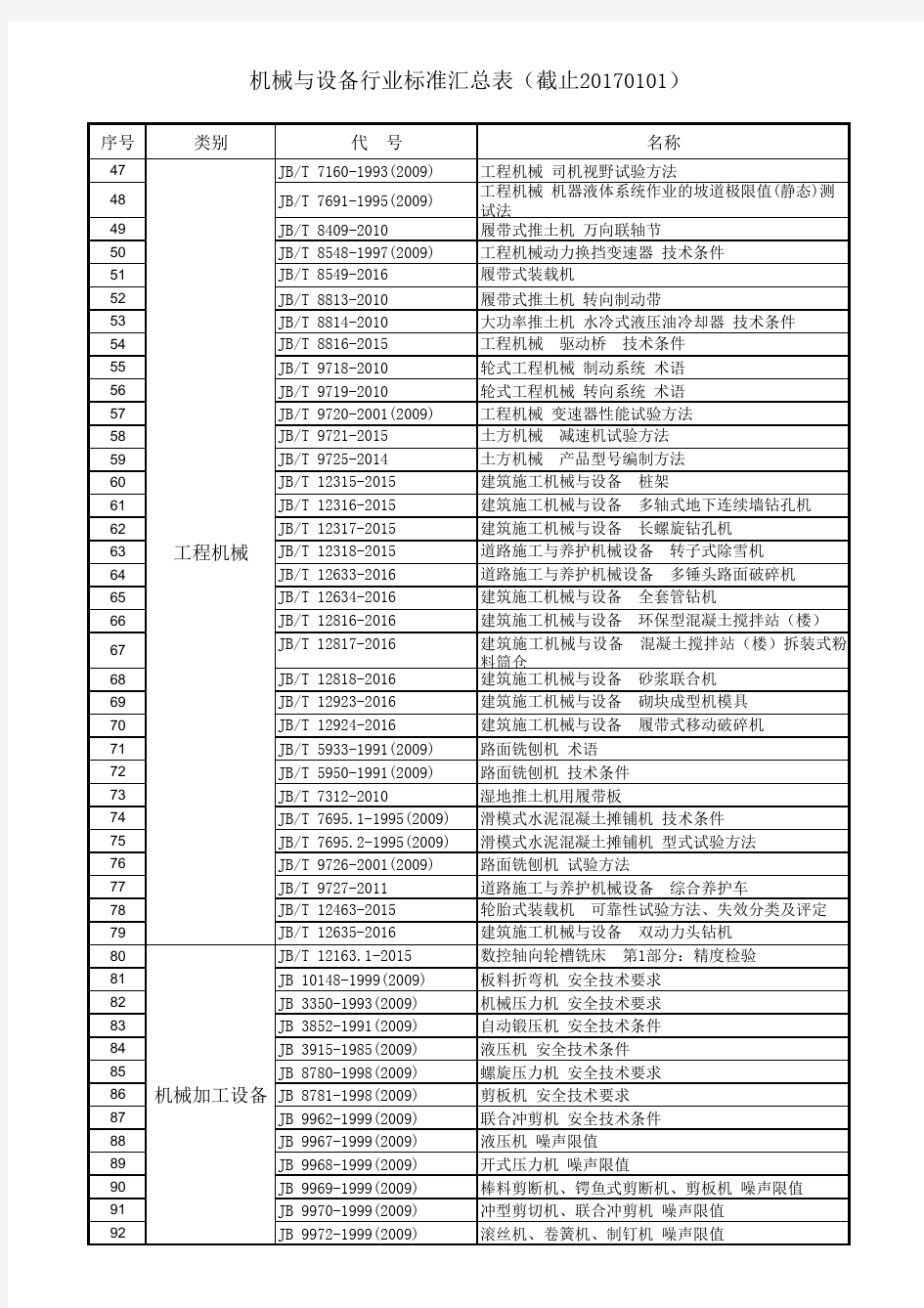
机械与设备行业标准汇总表(截止20170101)
制药设备发展现状
就目前来看,制药装备发展现状令人担忧。好药就需要好设备来制造。但是我国制药设备行业的发展现状却实在堪忧,低水平、无序竞争几乎成为行业标版。好比洗灌封联念头里安瓿割裂,导致玻屑满池的现象较凸起。有资料批注,1支安瓿折断时,被吸入的年夜于0.5微米以上的微粒可达两万粒以上,按现在的破损率盘算,若何扫除这些微粒并不是个小问题问题。 深入分析我国制药设备发展现状 况且,国内外都有报道,安瓿、西林瓶、输液瓶经超声波洗涤后,表皮松散易碎,受药液长期浸泡,轻易脱落微粒。而这些现象很难用肉眼搜检,因为眼睛所能看到的微粒至少在50微米以上,而人体微血管细的只有几微米,良多未被检测到的微粒会堵塞血管,造成血栓;再如用于固体口服制剂的破损、制粒、搅浑、压片、包衣等设置装备摆设良多还不是316钢,这些设置装备摆设的焊接粗糙,焊缝光洁度差,经由过程与物料的磨擦,磨屑就会混入药物中;至于带有传动装配的设置装备摆设,因为密封不严,造成机械磨损和润滑油渗漏而污染药物的现象也不为少数。 总之,因为设置装备摆设材质结构不妥,所造成的药品生产不对和污染,已到了不容轻忽的境界。若是与国外制药设置装备摆设对比,差距更为较着。
国外普遍操纵的在位清洗(cip)、在位灭菌(sip)、电抛光等手艺,我们的产品很少应用。 我国目前已有千余个专业制药机械厂,销售额达到10亿元。前些年由于药品生产企业的gmp认证使大量设备需要更新换代,为制药机械行业提供了发展的机遇。2002年和2003年是我国制药机械销售增长的“黄金”时期,到2004年,企业的数量由原先的300家发展到千余家。然而,随着药品生产企业gmp认证告一段落,千余家制药机械企业与全国5000余家药品生产企业形成了1000:5000的态势,供大于求,成为内需现状。各制药设备企业纷纷走出国门,寻求商机。 制药设备直接与药品、半成品和原辅料接触,是造成药品生产差错和污染的重要因素。国内外都有报道,安瓿、西林瓶、输液瓶经超声波洗涤后,表皮疏松易碎,受药液长期浸泡,容易脱落微粒。而这些现象很难用肉眼检查,因为眼睛所能看到的微粒至少在50微米以上,而人体微血管细的只有几微米,许多未被检测到的微粒会堵塞血管,造成血栓;再如用于固体口服制剂的粉碎、制粒、混合、压片、包衣等设备很多还不是316钢,这些设备的、焊接粗糙,焊缝光洁度差,通过与物料的磨擦,磨屑就会混入药物中;至于带有传动装置的设备,由于密封不严,造成机械磨损和润滑油渗漏而污染药物的现象也不为少数。 我国制药设备行业发展的三大瓶颈 1.低水平复制,同质化严重 由于制药设备技术含量不高,行业准入门槛较低,因此,在我国对制药企业进行gmp认证的时候,制药企业对设备需求大量上扬,使得中小设备企业一夜之间千军齐发。由于多数企业起步低,以仿制国外设备为主,在技术上不求甚高,导致同一产品复制现象严重,影响了整体的技术水平。 以干燥设备为例,国产的干燥设备绝大多数是供应国内市场,很少出口到国外,即使偶尔出口售价也不可观。虽然我国有众多的干燥设备厂,但这些厂主要集中在几个地域里。为什么会造成这种局面,重要的原因之一就是干燥设备便于仿制,几十家甚至近百家生产同一个机型。造成你能做我也能做,你不能做我也不能做。各家的说明书、宣传资料如出一辙,内容惊人地
机械制造行业三级标准化评分标准
机械制造企业安全质量标准化考核评级办法 一、为贯彻落实《国务院关于进一步加强安全生产工作的决定》(国发〔2004〕2号),指导全国机械制造企业开展安全质量标准化活动,切实加强基层和基础工作,促进企业建立自我约束、持续改进的安全生产长效机制,制定本考核评级办法。 二、本考核评级办法适用于各类机械制造企业。 三、机械制造企业安全质量标准化考核评级,应当按照《机械制造企业安全质量标准化考核评级标准》的要求,采用资料核对、抽查考核和现场查证的方法进行。其中: 基础管理考评部分,对人员抽查考核数量不少于现场(或在册)人数的10%; 设备设施安全考评部分,按设备设施及物品的拥有量(H)比例抽样: 1.H≤10,抽100%。 2.10<H≤100,抽10台。 3.100<H<500,抽10%。 4.500≤H≤1000,抽50台。 5.H>1000,抽5%。 四、机械制造企业安全质量标准化考核得分以1000分为满分。 被考核企业的得分计算方法: 各项目实得分之和×[1000÷(1000-各空项分之和)] 五、安全质量标准化机械制造企业分为三个等级: 一级:安全质量标准化考核得分不少于900分; 二级:安全质量标准化考核得分不少于800分;
三级:安全质量标准化考核得分不少于600分。 各空项分之和超过200分的,不得评为一级安全质量标准化机械制造企业。 六、考核评级的程序: 1.按照《机械制造企业安全质量标准化考核评级标准》的要求,企业成立由主要负责人任组长,各相关职能部门以及工会参加的小组进行自评。 2.企业自评后,形成自评报告,向承担安全质量标准化复评任务的机构(以下简称复评机构)提出复评申请(申请表格式见附件1)。 申请一级安全质量标准化机械制造企业的,应当向中国机械工业安全卫生协会(以下简称中机安协)提出复评申请。 3.复评机构收到企业的复评申请后,应按照《机械制造企业安全质量标准化考核评级标准》的要求进行复评,向企业和安全生产监督管理部门提交复评报告(复评报告格式见附件2)。符合相应等级安全质量标准化机械制造企业标准的,由安全生产监督管理部门核准;不符合的,由企业按照复评报告的要求进行整改。 4.安全质量标准化机械制造企业实行分级核准制。三级由复评机构报市(地)级安全生产监督管理部门核准;二级由复评机构报省级安全生产监督管理部门核准;一级由中机安协报省级安全生产监督管理部门审核同意后,由省级安全生产监督管理部门报国家局核准。 5.安全生产监督管理部门核准后,向企业颁发相应的证书和牌匾,并在有关媒体上予以公布。 七、各地的复评机构由省级安全生产监督管理部门研究确定,并报国家局备案。 八、安全质量标准化机械制造企业证书和牌匾有效期为3年。在3
【CN210229823U】一种高效的制药机械混合装置【专利】
(19)中华人民共和国国家知识产权局 (12)实用新型专利 (10)授权公告号 (45)授权公告日 (21)申请号 201920497134.7 (22)申请日 2019.04.13 (73)专利权人 福建神蜂制药机械设备有限公司 地址 350028 福建省福州市仓山区建新镇 洪山桥隧道口316号国道北侧1楼负一 层 (72)发明人 缪婧 (51)Int.Cl. B01F 13/10(2006.01) B01F 7/18(2006.01) B01F 11/00(2006.01) B01F 15/02(2006.01) B01F 15/00(2006.01) (54)实用新型名称 一种高效的制药机械混合装置 (57)摘要 本实用新型公开了一种高效的制药机械混 合装置,包括水平设置的底座,所述底座的上侧 侧壁固定连接有两个竖直设置的安装板,两个所 述安装板之间设有混药筒,所述混药筒上设有搅 拌装置,所述混药筒上设有带动装置,且带动装 置的两端均与安装板转动连接,所述混药筒的两 侧均设有竖直设置的推板,两个所述推板相背的 一侧侧壁均通过多个弹簧与安装板的侧壁连接, 两个所述推板相背的一侧侧壁均设有推动装置, 所述混药筒的下端固定连接有两个对称设置的 出药管。本实用新型多次混合药物,提高药物混 合效率。权利要求书1页 说明书3页 附图3页CN 210229823 U 2020.04.03 C N 210229823 U
权 利 要 求 书1/1页CN 210229823 U 1.一种高效的制药机械混合装置,包括水平设置的底座(1),其特征在于,所述底座(1)的上侧侧壁固定连接有两个竖直设置的安装板(2),两个所述安装板(2)之间设有混药筒(3),所述混药筒(3)上设有搅拌装置,所述混药筒(3)上设有带动装置,且带动装置的两端均与安装板(2)转动连接,所述混药筒(3)的两侧均设有竖直设置的推板(4),两个所述推板(4)相背的一侧侧壁均通过多个弹簧与安装板(2)的侧壁连接,两个所述推板(4)相背的一侧侧壁均设有推动装置,所述混药筒(3)的下端固定连接有两个对称设置的出药管(5),两个所述出药管(5)均与混药筒(3)内部连通,且两个出药管(5)上均设有节制阀(6)。 2.根据权利要求1所述的一种高效的制药机械混合装置,其特征在于,所述搅拌装置包括筒盖(7),所述筒盖(7)的上侧侧壁固定连接有驱动电机(8),所述驱动电机(8)的输出端贯穿筒盖(7)并固定连接有搅拌轴(9),且搅拌轴(9)上设有多个扇叶(10)。 3.根据权利要求1所述的一种高效的制药机械混合装置,其特征在于,两个所述推动装置均包括水平设置的推杆(11),两个所述安装板(2)上均设有安装腔(12),且两个推杆(11)相背的一端均依次贯穿安装腔(12)及安装板(2)的侧壁设置,两个所述安装腔(12)内均转动连接有第一转杆(13),两个所述第一转杆(13)的一端均依次贯穿安装腔(12)及安装板(2)的侧壁设置,且两个第一转杆(13)的另一端均固定连接有齿轮(14),两个所述推杆(11)的侧壁上均设有与齿轮(14)啮合设置的齿槽,两个所述安装板(2)的侧壁上均滑动连接有与推杆(11)匹配设置的第一滑动锁块(15)。 4.根据权利要求1所述的一种高效的制药机械混合装置,其特征在于,所述带动装置包括两个对称设置的弧形卡块(16),且两个弧形卡块(16)之间均通过多个锁钉连接,两个所述弧形卡块(16)相背的一端均固定连接有第二转杆(17),两个所述第二转杆(17)相背的一端均贯穿安装板(2)的侧壁设置。 5.根据权利要求2所述的一种高效的制药机械混合装置,其特征在于,所述筒盖(7)的两端均设有水平设置的插杆(18),且两个插杆(18)均依次贯穿筒盖(7)及混药筒(3)的侧壁设置,所述筒盖(7)的两侧侧壁均滑动连接有与插杆(18)匹配设置的第二滑动锁块(19)。 6.根据权利要求2所述的一种高效的制药机械混合装置,其特征在于,所述筒盖(7)上设有多个加药孔(20),且多个加药孔(20)均贯穿筒盖(7)设置。 2
项最新机械、制药装备行业标准名称及主要内容
附件: 100项机械、制药装备行业标准名称及主要内容 序 号 标准编号标准名称标准主要内容代替标准采标情况机械行业 JB/T 7743-2011 旋涡泵本标准规定了旋涡泵的型式、型号和基本参数、技术要求、 试验方法、检验规则、标志、使用说明书、包装、运输和贮存。 本标准适用于输送不含固体颗粒、运动粘度不大于 37.4mm2/s液体的机械密封泵和输送易燃、易爆、易挥发、有毒、 有腐蚀性以及贵重液体的磁力传动泵。被输送液体的温度:机械 密封泵为-20℃~120℃,磁力传动泵为-20℃~250℃。 JB/T 7743-1995 JB/T 8857-2011 离心式潜污泵本标准规定了离心式潜污泵的型式与基本参数、技术要求、 试验方法和检验规则等。 本标准适用于所输送液体中含有非磨蚀性固体颗粒、纤维、 污杂物(如城市生活污水、化学工业废水等)的泵。 JB/T 8857-2000 JB/T 11170-2011 凝结水和乏汽闭式回 收水泵装置 本标准规定了凝结水和乏汽闭式回收水泵装置的术语、分类与基本参数、性能要求、试验方法、试验规则,标志和供货要求等内容。 本标准适用于蒸汽供热系统中凝结水和乏汽回收使用的集水罐公称压力小于或等于PN16,介质最高温度不大于200℃的凝结水和乏汽闭式回收水泵装置。 JB/T 11171-2011 溴化锂吸收式空调机 内用屏蔽电泵 本标准规定了溴化锂吸收式空调机内用屏蔽电泵的型式与基本参数、技术要求、试验方法、检验规则、标志、包装、运输及贮存。
序 号 标准编号标准名称标准主要内容代替标准采标情况 本标准适用于设计压力为0.5MPa,输送介质温度范围为 0℃~150℃、不含固体颗粒的溴化锂溶液和冷剂水电泵。 JB/T 11172-2011 液环压缩机本标准规定了液环压缩机的术语定义、型式分类、技术要求、 试验方法、检验规则、保证期、标志、包装、运输和贮存。 本标准适用于输送或压缩不含固体颗粒气体的液环压缩 机。 JB/T 4296-2011 矿井轴流式通风机本标准规定了矿井轴流式通风机的技术要求,试验方法,检 验规则,标志﹑包装及运输,贮存及保养等。 本标准适用于矿井通风用的轴流式主通风机,可满足矿井通 风所需要流量和压力。环境介质温度为:-45~﹢50℃。 JB/T 4296-1999 JB/T 4362-2011 电站轴流式通风机本标准规定了电站轴流式通风机的技术要求,试验方法,检 验规则,标志﹑包装及运输,贮存及保养等。 本标准适用于火电站锅炉轴流式送风机﹑引风机及一次空 气风机,也适用于火电站轴流式脱硫﹑脱硝风机。送风机及一次 空气风机的工作介质温度,在正常情况下不得高于70℃;引风 机的工作介质温度不得高于250℃。 送风机及一次空气风机输送的介质为空气,引风机输送的介 质为烟气,烟气含尘量≤150mg/Nm3。 JB/T 4362-1999 JB/T 1460-2011 滚动轴承高碳铬不 锈钢轴承零件热处 理技术条件 本标准规定了采用符合GB/T 3086-2008规定的95Cr18 (原牌号为9Cr18)、102Cr18Mo(原牌号为9Cr18Mo)、 65Cr14Mo不锈钢制滚动轴承套圈和滚动体的退火、淬回火后的 技术要求、检验方法和规则等。 本标准适用于上述材料制造的轴承零件热处理质量检验。 JB/T 1460-2002 JB/T 7363-2011 滚动轴承低碳钢轴本标准规定了采用符合GB/T 699-1999规定的08、10、15、JB/T 7363-2002
浅谈制药厂与制药机械厂的现状与发展趋势
浅谈制药厂与制药机械厂的现状与发展趋势 我国改革开放以来,经济的稳步发展使中国综合国力迅速得到加强。在与世界接轨的同时,国内各行业都发生了可喜变化,期间医药行业及配套行业变化较为明显。自从20世纪80年代开始,我国引进国际通用的GMP药品质量管理理念以来,全国药厂企业内部反响很大。大家一致认为这是一套行之有效的科学管理理念,它从源头上开始监控,一直到成品出厂到用户手中,这一全过程、全系统、全方位、无死角的监控手段,使药品更安全、更可靠,做到万无一失。 20世纪80年代是中国文革后经济刚刚开始复苏的时期,根据当时国家制药行业的实际情况,国家医药管理总局协同卫生部等有关部委开始制定最初的适合国情的第一版GMP实施文件。从实施GMP质量管理标准到现在,已经走过了二十几个年头。其从最初的GMP试行版本到GMP修改版本,再到GMP正式实施版本,前后经历了上下多次修改、充实、提高,力求实用可操作性。经论证后国家有关部委发文,最后实施GMP质量管理标准的日期,硬性规定为:我国国内药厂必须在2004年6月30日以前完成并达标。这是一条时间鸿沟,一条需要花费大量财力、精力、时间才能翻越的鸿沟。为了在规定的期限内使自己的企业,能够从硬件(厂房、设备、设施),从软件(SMP、SOP、各种管理文件)达标完成取证工作,全国各地各药厂(当时初步估计8000余家药品制造厂)掀起了轰轰烈烈的GMP改造运动。在这股GMP改造热潮的推动下,各地医药设计院,为药厂配合的制药机械厂,其中也包括许多军工单位也都一起,投入到这场振兴中国医药工业的GMP认证潮流中去。 在落实GMP理念的同时,一方面国家医药管理总局、制药装备行业协会都相继举办各种类别的培训班、技术讲座、软件管理编制等培训班,这是根据当时形势培养GMP管理干部的有力措施;另一方面,国家医药管理总局、制药装备行业协会狠抓制药设备引进、仿制、消化工作,双管齐下出硕果。不久新的制药设备一个一个出现在全国药机会上,由于全国GMP改造来势凶猛,全国制药机械厂从一开始近百家企业发展到顶峰时期的960家之多。药机展览会展位从近千个展位发展到顶峰时期的5 051个展位,打造了医药、药机行业的兴旺局面。在这种大好形势下,我们冷静观察,发现在这股全国GMP改造的浪潮中,蕴藏了一种硬件、软件不到位的或到位不齐全的现象,致使全国药厂有近1/3被推出局外。我们应清楚看到,以前的GMP认证都是在静态中进行的,静态认证有许多不良因素不易被人发现被掩盖或没有暴露,但对药品生产来讲即留下隐患。为了紧跟国际步伐,加快与FDA理念的接轨,我国医药行业又要上一个新台阶,即cGMP管理规范。cGMP管理规范要比GMP管理规范严格许多,它更着眼于动态,着眼于细节。有许多在GMP规范中不易被暴露的问题,却在cGMP规范中完全暴露无疑。因为世界在进步,人民安全用药呼声越来越高。所以cGMP规范是紧跟国际步伐,符合人民意愿的产物。在新形势下,寻找一条适合我国医药、药机发展之路的门这是摆在我们面前并必须解决的重大课题。 1、我国医药行业与制药机械行业现状 1.1 我国医药行业现状 (1)新中国成立以来,我国医药行业发展很快,尤其是改革开放以来,药厂发展更为迅速,到目前为止已有药厂6 000多家,中国药厂已进入世界药品生产大国行列。由于我国新药研究与开发基础薄弱,再加上资金、人才短缺,自主创新能力弱,拿不出以自主知识产权为核心的技术药品。这就决定了我国药厂主要生产品种是以普药、仿制品药为主,高新药、生物制药少的局面。这些差距与世界的距离已相当明显,结果导致并延缓我国制药产业从大国向强国迈进的步伐。
2020年(安全生产)机械制造行业安全生产标准化达标标准
(安全生产)机械制造行业安全生产标准化达标标准
机械制造行业安全生产标准化达标标准(试行) 基础管理部分 1安全生产责任制 1.1企业主要负责人职责 1.1.1企业安全生产责任制完整; 1.1.2企业安全生产规章制度和作业指导书齐全; 1.1.3企业坚持安全生产投入规划和实施; 1.1.4企业坚持督促、检查安全生产工作且及时消除生产安全事故隐患; 1.1.5企业的生产安全事故应急救援预案完整、齐全,定期组织演练实施; 1.1.6企业发生生产安全事故能及时、准确向上级汇报; 1.1.7企业定期向职工大会、职工代表大会、股东会或股东大会方案安全生产情况,接受工会、从业人员、股东对安全生产工作的监督。 1.2建立各职能部门的安全职责且且定期进行检查考核。 1.3建立各级各类人员包括管理和从业人员的安全职责,定期对其职责进行检查考核。 2安全生产规章制度 2.1企业安全规章制度 2.1.1安全生产检查制度; 2.1.2安全生产教育培训制度; 2.1.3安全生产考核、奖惩制度; 2.1.4工伤事故管理制度; 2.1.5设备设施安全管理制度;
2.1.6现场安全管理制度; 2.1.7电气安全管理制度; 2.1.8劳动防护用品管理制度; 2.1.9安全投入保障制度; 2.1.10安全例会制度; 2.1.11消防安全管理制度; 2.2建立其他保障安全生产的规章制度。 3安全生产投入 3.1建立安全生产保障制度,按国家、省、市有关规定提取安全生产专项费用。 3.2建立安全生产专项费用台帐,做到专款专用。 3.3企业依法参加工伤社会保险,为从业人员交纳工伤保险费。 3.4为从业人员提供符合国家标准或行业标准的劳动防护用品。 4安全生产管理机构和人员 4.1安全生产管理机构和网络 4.1.1企业应建立安全生产委员会或领导小组,且积极开展工作; 4.1.2企业依法设置相应的安全生产管理机构人员,且且有管理职能; 4.1.3企业安全生产管理人员应当参加企业各种涉及安全生产的会议和有关决策决定; 4.1.4企业工会应履行监督职能。 4.2安全生产管理人员 4.2.1从业人员于50人以下的,应当配备专(兼)职安全生产管理人1名;4.2.2从业人员超过50人的,应配备不少于1名专职管理人员;
各种标准的代号
国家标准 GJB 国家军用标准 GBJ 工程建设国家标准GBn 国家内部标准 GB 国家标准 GWKB 国家污染物控制标准GWPB 国家污染物排放标准GHZB 国家环境质量标准JJG 国家计量检定规程 JJF 国家计量技术规范 行业标准 BB 包装行业标准 CB 船舶行业标准 CH 测绘行业标准 CECS 工程建设推荐性标准CJ 城建行业标准 CJJ 城建行业工程建设规程CY 新闻出版行业标准 DA 档案行业标准 DB 地震行业标准 DL 电力行业标准 DZ 地质行业标准 EJ 核工业行业标准 FZ 纺织行业标准 GA 公安行业标准 GY 广播电影电视行业标准HB 航空行业标准 HG 化工行业标准 HGJ 化工行业工程建设规程HY 海洋行业标准 HJ 环保行业标准 HS 海关行业标准 JB 机械行业标准 JC 建材行业标准 JG 建筑行业标准 JGJ 建筑行业工程建设规程JT 交通行业标准 JR 金融行业标准 JY 教育行业标准 LB 旅游行业标准 LD 劳动行业标准
LY 林业行业标准 GH 供销合作行业标准MH 民用航空行业标准MT 煤炭行业标准 MZ 民政行业标准 NY 农业行业标准 QB 轻工业行业标准QC 汽车行业标准 QJ 航天行业标准 QX 气象行业标准 SB 商业行业标准 SC 水产行业标准 SH 石油化工行业标准SJ 电子行业标准 SL 水利行业标准 SN 商品检验行业标准SY 石油行业标准 TB 铁道行业标准 TD 土地行业标准 WH 文化行业标准WM 外贸行业标准WB 物资行业标准WS 卫生行业标准 XB 稀土行业标准 YB 黑色冶金行业标准YC 烟草行业标准 YD 通信行业标准 YS 有色冶金行业标准YY 医药行业标准 YZ 邮政行业标准 ZY 中医药行业标准WB 物资行业标准WS 卫生行业标准 XB 稀土行业标准 YB 黑色冶金行业标准YC 烟草行业标准 YD 通信行业标准 YS 有色冶金行业标准YY 医药行业标准 YZ 邮政行业标准 ZY 中医药行业标准 国际标准
机械行业标准化创建过程
机械行业 标准化建设创建过程 为全面贯彻落实机械行业标准化建设,实施机械行业基础管理规范化、工作过程流程化、作业组织专业化,进一步提升该企业的管理水平和优质服务水平,我公司按照机械行业标准化要求,精心组织,明确责任分工,落实工作措施,制定了企业的标准化创建计划,现将该企业所创建工作的开展情况汇报如下: 一、**公司管理规范化、标准化的建设 (一)组织开展了该公司标准化建设评价标准 依据冶金等工贸企业安全生产标准化基本规范,我公司制定了适用于该企业的评价标准,包含安全生产目标、安全生产组织机械和职能、安全生产投入、法律法规与安全管理制度、教育培训、生产设备设施、作业安全、隐患排查和治理、重大危险源监控、职业健康、应急救援、事故报告、调查和处理、绩效评定和持续改进十三个大项的评价标准,充分对企业做好全面的标准化整改,努力使该公司成为现代化标准化企业。 (二)对现场作业标准化排查摸底,规范档案资料 我公司将努力使该企业达到标准化规范建设,更好的为企业安全生产服务,根据标准化建设要求,明确了总经理为第一负责人,生产经理、各车间主任、组长为成员创建小组,深入标准化现场,对不规范的操作及行为进行标准化建设,及时解决工作中遇到的困难和问题。
(三)按标准化建设要求明确分工管理 安全部、生产部、行政部召开专题讨论会,安全部和生产部分小组开展专题学习并组织专题培训,生产部和行政部完善标准化建设的制度管理、组织体系、考核标准和相关制度的制定及完善;针对标准化建设内容进行自查,最后进行自评,提交评估验收申请表。 二、安全标准化建设的方针和目标的制定 根据标准化的要求,我公司根据该企业的实际情况特制定了相应的安全生产的方针和目标;安全生产的方针为:安全生产,预防为主;全员参与,科学管理;关爱健康,持续发展。安全生产的目标为:追求最大限度的不发生事故、不损害人身健康;目标分解为:1、无重大火灾、爆炸、伤亡事故;2、每季度千人负伤率小于1%;3、隐患整改率大于或等于95%;按照方针和目标的要求,公司与各车间部门及员工签定安全目标责任书,各车间按照详细的安全工作规划,以保证安全方针的目标的效完成,并定期对目标的完成情况进行考核。三、安全生产管理制度的编制 我公司根据标准化建设的要求,对十三大项中的每一项需要的制度进行完善,通过安全部、生产部、行政部相互讨论对相应的制度根据实际情况进行编制,分别有《安全惩奖制度》《安全防护设备管理制度》《安全生产“五同时”管理制度》《安全生产检查制度》《厂内交通安全管理制度》《电气临时线审批制度》《防尘防毒设施管理制度》《防火安全管理制度》《劳动防护用品管理制度》《劳动合同管理制度》《女职工和未成年人特殊保护管理制度》《特种设备安全管理制度》
gbt制药机械(设备)清洗、灭菌验证导则
GBT 制药机械(设备)清洗、灭菌验证导则 欢迎各位朋友留言讨论。以下是全文内容,欢迎访问北京齐力佳网站获取本文和更多制药行业相关资讯及文档。 GB/T 36036-2018全文如下:制药机械(设备)清洗、灭菌验证导则1 范围本标准规定了制药机械( 设备)清洗与灭菌验 证的术语和定义、验证目的、验证原则、验证范围、验证程序、验证方案和验证文件。本标准适用于制药机械( 设备) 清洗与灭菌验证。2 规范性引用文件下列文件对于本文件 的应用是必不可少的。凡是注日期的引用文件,仅注日期的版本适用于本文件。凡是不注日期的引用文件,其最新版本(包括所有的修改单)适用于本文件。GB/T 36030-2018 制药机械(设备)在位清洗、灭菌通用技术要求药品生产质量管理规 范(2010年修订)(中华人民共和国卫生部)中华人民共和国药典(2015年版)(国家药典委员会) 3术语和定义 GB/T36030-2018界定的以及下列术讲和定义适应于本文件。 3.1 验证文件validation document验证总计划、验证计划、验证方案、验证报告和验证总结及验证过程中形成的其他相关文档或资料。[GB/T 28671-2012,定义3.8] 3.2 验证报告validation report对验证方案及已完成验证试验的结果、漏项及发生的偏差等进行回顾、审核并作出评估的文件。[GB/T 28671-2012,定义3.9] 3.3挑战性试验challenge test旨在确
定某一个工艺过程或一个系统的某一组件(如一个设备或一个设施)在设定的苛刻条件下能否达到预定质量要求的试验。[GB/T 28671-2012,定义3.10] 4 清洗与灭菌验证4.1验证目的4.1.1 验证制药机械(设备)清洗与灭菌符合《药品生产质量管理规范(2010年修订)》、GB/ T 36030-2018 和用户需求标准,达到规定的清洗与灭菌效果。4.1.2 验证制药机械(设备)清洗与灭菌系统结构符合药品生产工艺要求。4.1.3 验证制药机械(设备)清洗与灭菌规程,清洗、灭菌介质及运行参数正确有效。4.1.4 验证制药机械(设备)清洗与灭菌有效性、稳定性、重现性、可追溯性。4.2 验证原则4.2.1制药机械(设备)清洗与灭菌验证方案应根据《药品生产质量管理规范(2010年修订)》、GB/ T 36030-2018 和药品生产工艺要求制定。验证的每个阶段应有验证方案。4.2.2 验证方案应明确验证目的、参与实施验证部门、人员职责。验证内容应包括清洗和灭菌方法,风险分析,残留限度计算过程、试验方法、合格标准、偏差处理等。验证方案应经过质量管理部门审核、批准。4.2.3 验证应按预先确定和批准的方案实施,并有记录。4.2.4 验证工作完成后,应有验证报告、验证结果和评价、建议等结论,并经审核、批准:应有记录并存档。4.3 验证范围验证范围应根据《药品生产质量管理规范(2010年修订)》和制药工艺对制药机械(设备)清洗、灭菌要求确定。4.4 验证程序4.4.1验证程序应包括验证计划、清洗系统结构、制
制药机械市场研究报告
制药机械市场研究报告 制药机械是与药品直接接触的设备,在生产中对药品质量产生最直接的影响。回顾国内制药机械发展的历程,可早期追溯到 20 世纪 80 年代。当时国内只有三十余家制药装备生产商,其中辽阳药机、中南药机、重庆药机和宝鸡药机被称为四大家族,掌控着当时的药机市场。之后,制药机械行业得到了长足的发展。 一、我国制药机械行业透视 1 、我国制药机械市场增长迅速 制药(机械)装备行业从 1978 年始建至今,规模不断地发展壮大。目前,中国专产、兼产(以制药机械产品为主)的企业 600 余家,分布在全国 26 个省、自治区、直辖市。其中上海、江苏和浙江的制药机械厂家占了全国的一半以上,全行业年工业总产值超过 100 亿元,显示出近几年制药机械行业迅猛发展的趋势。 全行业产品共分八大类,有原料药机械与设备、制剂机械、药用粉碎机械、饮片机械、制药用水设备、药用包装机械、药物检测设备和其它制药机械设备。在这门类繁多的产品中,不仅有先进的单机设备,而且还有整套全自动生产机组。 3000 多个品种规格的药机产品,不仅为中国 4000 多家中、西制药厂、数千家保健品企业的基本建设、技术改造、设备更新,提供了大量的优质先进装备,而且还出口到美国、日本、韩国、俄罗斯、泰国、印度尼西亚、马来西亚、菲律宾、巴基斯坦、香港等数十个国家和地区。推动我国制药机械行业快速发展的原因有: 一是我国经济形势的持续高速发展,人民生活水平的不断提高,医药行业相应发展较快,由此推动了制药机械的需求增长,促进制药装备工业的繁荣。 二是国家对制药企业实行强制性 GMP 认证制度的推动,特别是 GMP 认证的截止期到来,是药机市场火爆的直接因素。制药装备是 GMP 硬件的重要部分,自从国家推出 GMP 强制认证制度以来,各地药厂纷纷加快了技术改造步伐,生产设备的大幅度更新为制药行业的上游产业——制药机械行业带来了重大利好,大量的生产线改造为制药机械企业带来了巨大的市场。 三是药机工业科技进步的推动。近几年来,我国药机工业狠抓科技进步,新产品日益增多,质量也有很大的飞跃,个别产品甚至达到了国际先进水平。 加入世贸组织后,随着中国市场开放程度的加大,新一轮关税水平的下调和非关税措施的逐步取消,又在一定程度上使我国制药机械行业受至进口产品更大的冲击。面对跨国公司雄厚的资金实力、现代化的技术、优质的产品、强有力的品牌、先进的营销和管理模式,国内企业不得不思考该如何更好地生存并努力扩大自己的市场。 医药行业的确是一个发展前景很好的行业,外国制药设备厂商都对中国医药生产和包装市场十分看好。上世纪 90 年代以来,许多国外厂商和代理商纷纷在中国设立分公司和办事机构,有的还同国内企业合资建立公司。这些厂商在中国的年销售额达几亿欧元,并且逐年增长。近几年来,意大利自动化机械制造商协会、英国药业加工与包装机械协会、美国包装机械制造协会、德国机械制造协会等国外行业包装机械协会都不断加大对中国市场的开发力度。 目前我国 4000 多家药厂可以分为四个层次: 一、以辉瑞、葛兰素史克为代表的世界 500 强企业在中国的独资合资企业,他们所用的绝大多数设备都是进口制药和包装设备; 二、国有大型股份有限公司为了进一步提高产品质量扩大生产能力,同外资企业竞争,近十年来他们纷纷引进国外成套生产线,同时也购买国内的优质产品;
机械工业产品企业标准制定管理办法
机械工业产品企业标准制定管理办法 (机电部机电科(1991)1698号C 1991年10月9日) 第一条根据《中华人民共和国标准化法》及其有关配套法规,为指导机械工业产品企业标准的制定与管理工作,结合行业特点,特制定本办法。 本办法适用于企业(包括事业单位,下同)民用产品企业标准的制定,军用产品企业标准的制定亦可参照执行。 第二条产品企业标准是指企业为保证产品的适用性,对产品必须达到的某些或全部要求所制定的标准。其主要内容包括:主题内容与适用范围、术语、产品分类、技术要求、试验(或测量)方法、检验(或质量评定)规则、标志、包装、运输、贮存等。 第三条根据标准化对象的特点和制定标准的目的,产品企业标准可分为以下四类:(一)没有相应产品国家标准、行业标准时,由企业制定作为组织生产和交货依据的产品企业标准。 (二)已有相应产品国家标准、行业标准时、为提高产品质量和技术进步,企业制定严于已有产品国家标准、行业标准的产品企业标准。 (三)对已有的产品国家标准、行业标准的技术内容加以补充制定的产品企业标准。 (四)为合理发展本企业产品的品种、规格,从已有的产品国家标准、行业标准中选用部分技术内容,由企业制定产品企业标准。 第四条新产品批量生产前,凡没有相应产品国家标准、行业标准的,必须制定产品企业标准,作为组织生产、经营活动的依据。单件生产或为特定用户提供的一次性生产的产品经用户同意,可按双方签订的合同或技术协议供货。 第五条为满足出口产品的需要,企业在与订货方签订合同时应明确供货技术要求、此种技术要求可以由双方协议规定或直接采用有关标准。 第六条产品企业标准由企业自行制定,亦可委托专业标准化机构或有关单位协助制定,由企业法定代表人或由企业法定代表人授权的企业主管领导批准、发布。产品企业标准由企业法定代表人授权的企业标准化职能部门统一管理。 第七条制定产品企业标准的企业应具备下列条件: (一)按本企业的生产规模、产品性质、技术复杂程度、专业化程度及其实际管理体制的需要,设置并配备相应的企业标准化职能部门和(或)称职的标准化专(兼)职技术人员,并保持相对稳定。 (二)产品企业标准的批准人应了解国家、部门与标准化工作有关的法律、法规、规章和政策,并具有有关的标准化知识。 第八条为确保产品企业标准的技术水平和文本编制质量,在制定产品企业标准时应遵循以下基本原则: (一)贯彻国家和行业的有关法律、法规、规章和政策;严格执行有关的强制性国家标准、行业标准以及行政主管部门规定贯彻执行的推荐性标准。
制药机械选材的要求
摘要:以GMP和制药工艺对制药机械的选材要求为切入点,重点对制药机械中常用奥氏体不锈钢选用原则进行了探讨,并结合实例阐述了其应用、选材与加工之间的关系。同时,简述了非金属材料的选用原则。 关键词:制药机械;选材;奥氏体不锈钢;原则;非金属材料;耐腐蚀;不溶性微粒 在当今,中国制药机械伴随着GMP在制药工业的实施,其已相当成熟,但制药企业的设备管理与采购人员对制药机械选材概念仍处于模糊状态,特别是对金属材料的选用更为扑朔迷离。认为选了316L材质便是符合了GMP,这个观念在中国乃至国外相关人士的世界观上有一定的沉淀,类似此类观点是否正确,回答很明确:非也。虽然,笔者撰写过此类文章,人们对此有所改观,但仍有部分业内人士仍沉溺于此,这是对GMP的一种曲解,其也与GMP内含所相悖的。因而,本文从GMP和制药工艺的内含出发,再议制药机械的选材原则。 1.GMP和制药工艺对制药机械选材的要求 1.1GMP对制药机械的选材要求 笔者查阅了GMP相关文件,现把涉及到制药机械选材做条款归纳如下: (1)GMP(98版)1第32条认为:“与药品直接接触的设备表面应光洁、平整、易清洗或消毒、耐腐蚀,不与药品发生化学变化或吸附药品。”第34条认为:“……储罐和输送管道所用材料应无毒、耐腐蚀。……注射用水储罐的通气口应安装不脱落纤维的疏水性除菌滤器。” (2)GMP(98版)附录2第一节3款第7条认为:“洁净室(区)内应使用无脱落物、易清洗、易消毒的卫生工具……。”第二节3款认为:“与药液接触的设备、容器具、管路、阀门、输送泵等应采用优质耐腐蚀材质,……。过滤器材不得吸附药液组份和释放异物。禁止使用含石棉的过滤器材。” 再看美国cGMP3中211.65条(a)款,其认为:“设备表面与组份、中间物料或药品接触时应不起反应,无吸着、吸附作用,以不致改变药品的安全性、鉴别特征、含量(或效价)、质量或纯度而使之超出法定或其它既定要求。” 可以说,查遍GMP相关文件均未见到制药机械选材的强制性条文,GMP对制药机械选材只作了定向的规定,而没有作具体的规定。虽然,在《药品生产验证指南》4这本国内权威性的专著中,对一些生产过程中设备和管道的选材作了若干陈述,如类似注射用水管路材质为316L,其是有的放矢,而不是一遇到制药机械与物料直接接触的材质便是316L这样叙述的,何况此书的前言中明确表示“是一本验证工作方面的指导性工具书,不具有法规性的验证规定4。”这说明:GMP对制药机械选材只作定向性的规定。 1.2制药工艺对制药机械的选材要求 人们在关注制药机械选材应“易清洗或消毒、耐腐蚀,不与药品发生化学变化或吸附药品”的同时,更不要遗忘另一个选材原则,这便是不溶性微粒的有效控制。 在药品中微粒大致有尘粒、金属或其它微粒,微粒的存在直接影响药品质量,危及人们的生命安全。大量临床资料表明,如药品被7-2μm的尘粒污染了,尤其是静脉注射用药,可以导致热原反应、肺动脉炎、微血栓或异物肉芽肿等,严重的会致人死命4。因此,我国药典1985年首次对输液不溶性微粒作出限定,规定每毫升中大于或等于10μm的粒子不得超过50个,大于或等于25μm的粒子不得超过5个4。 同时,文献4中也明确指出:无菌性及不溶性微粒的污染是无菌原料药区别于非无菌原料药的两大主要特征,也是生产工艺中与控制的最重要项目之一。不溶性微粒的污染的控制在无菌原料生产中最难控制的一项指标,每个无菌产品的不溶性微粒必须是在一定的范围内,
2012年最新国民经济行业分类标准
附件1: 国民经济行业分类 (GB/T 4754-2011) 1 范围 本标准规定了全社会经济活动的分类与代码。 本标准适用于在统计、计划、财政、税收、工商等国家宏观管理中,对经济活动的分类,并用于信息处理和信息交换。 2 术语和定义 下列术语和定义适用于本文件。 2.1 行业 industry 行业(或产业)是指从事相同性质的经济活动的所有单位的集合。 2.2 主要活动 principal activity 当一个单位对外从事两种以上的经济活动时,占其单位增加值份额最大的一种活动称为主要活动。如果无法用增加值确定单位的主要活动,可依据销售收入、营业收入或从业人员确定主要活动。 与主要活动相对应的是次要活动和辅助活动。次要活动是指一个单位对外从事的所有经济活动中,除主要活动以外的经济活动。辅助活动是指一个单位的全部活动中,不对外提供产品和劳务的活动。辅助活动是为保证本单位主要活动和次要活动正常运转而进行的一种内部活动。 2.3 单位 unit 本标准中的单位是指有效地开展各种经济活动的实体,是划分国民经济行业的载体。 2.4 产业活动单位 establishment 产业活动单位是法人单位的附属单位。产业活动单位应具备下列条件: ——在一个场所从事一种或主要从事一种经济活动; ——相对独立地组织生产、经营或业务活动; ——能够掌握收入和支出等资料。 2.5 法人单位 corporate unit 具备下列条件的单位为法人单位: ——依法成立,有自己的名称、组织机构和场所,能够独立承担民事责任; ——独立拥有和使用(或授权使用)资产,承担负债,有权与其他单位签定合同;
制药机械设备排名
制药装备板块,它由四个主要的技术和技术中心组成:生物制药,特种输液,中药和固体制剂。而在此过程中离心机的使用将给生产带来很大的方便。那么其使用有需要注意哪些维护措施呢?下面我们一起来看看。 1.通常每台设备到厂后均须空车运转3时左右,无异常情况即可工作。 2.检查其他部位有无松动及不正常情况。 3.严禁机器超速运转,以免影响机器使用寿命。 4.在离心机运转前可以采取先切断电源并先松开离心机刹车的方法,手试转动转鼓,看有无咬煞情况。 5.物料尽可能要放置均匀。
6.必须专人操作,容量不得超过额定量。 7.接通电源依顺时针方向开车启动(通常从静止状态到正常运转约需40-60秒左右)。 8.机器开动后,如果有异常情况应该停车检查,必要时需予以拆洗修理。 9.为了保证离心机的正常运转,其零部件请每隔6个月后加油保养一次。同时查看轴承处运转润滑情况以及有没有磨损现象;制动装置中的部件是否有磨损情况,严重的予以更换;轴承盖有无漏油情况。 10.滤布的目数应根据所分离物料的固相颗粒的大小而定,不然的话影响分离效果。另外滤布安装时可以将滤布密封圈嵌入转鼓密封槽内,以防物料跑入。 11.离心机工作时是高速运转,因此切不可用身体触及其转鼓,以防意外。 12.不能将非防腐型离心机与于高腐蚀性物料的分离;另外严格按照设备要求进行操作,非防爆型离心机不可以用于易燃、易爆场合。 13.机器使用完毕,可以作好清洁工作,保持机器整洁。
蚌埠精工制药机械有限公司是国内对分离机械集研发与制造一体的专业生产离心机的厂家。公司多年来一直致力于离心机的研究、生产,产品广泛适用于医药、化工、食品、味精、环保等行业领域。公司坚持将售前服务和售后服务做为一个整体,以崭新的姿态,宽阔的胸怀,良好的产品,与国内外朋友一起,共创辉煌。
常见制药机械中英文对照
常见制药机械中英文对照 Tablet Section片剂机械 ? Tablet Press Section压片机 ? Tablet Filling Section充填机械 ? Capsule Section胶囊机械 ? Ointment Section软膏机械 ? Liquid Section液体机械 ? Injection Section注射 机械 ? Tube filing软管充填机械 ? Preparation Machinery 制剂设备 ? Packing Machinery包装机械 ? Pulverizer粉碎机 ? Liquid Filling Machinery液体充填机 ? Filling and Sealing Machine填充和封口机 ? Drying Machinery干燥机 ? Mixer / Calibrator混合机 ? Coater包衣机 ? Granulator制粒机 ? Pharmaceutical Production Line医药生产线 ? Pharmaceutical Water Supply Equipment医药水处理设备 ? Syringe Assembling Machine注射机械 ? Labeling / Cartoning Machine 标签机/纸盒成型机 ? Laboratory & Quality Control Equipment实验室和质量控制设备 Tablet Section片剂机械 ? Rapid Mixer Granulator快速混合制粒机 ? Double Cone Blender / Mechanical Shifter双锥鼓式搅拌机/机械位移(传感)器 ? Spray Coating Machine喷雾包衣机 ? Rotary Tablet Press旋转式压片机 ? Tablet Counting Machine数片机 ? Tablet Polishing Machine片剂抛光机 ? Automatic Tablet Printing Machine自动药片印字机 ? Strip Packing Machine自动包装机 Capsule Section胶囊机械
2019年制药机械设备企业发展战略和经营计划
2019年制药机械设备企业发展战略和经营计划 2019年4月
目录 一、行业发展趋势 (3) 1、发展现状:整体规模快速增长行业竞争激烈 (3) 2、市场机遇:生物医药迅速发展为制药机械行业带来机遇 (3) 3、新版GMP推进为制药机械行业带来利好 (4) 二、公司发展战略 (4) 1、拓展新收入增长点 (4) 2、不断加强内部控制 (5) 三、公司经营计划 (5) 四、风险因素 (6) 1、技术更新风险 (6) 2、安全生产、产品质量风险 (6) 3、技术人员流失的风险 (7) 4、应收账款回收风险 (8)
一、行业发展趋势 1、发展现状:整体规模快速增长行业竞争激烈 从整体来看,我国制药机械设备行业随着医药市场需求的不断增长,规模正在不断壮大。据前瞻产业研究院《中国制药设备行业市场需求预测与投资战略规划分析报告》的分析,我国制药机械设备行业市场规模近年来一直保持20%以上的速度增长,目前我国制药机械设备行业企业已达800 余家,市场规模已经超过450 亿元,我国俨然已经发展成为制药机械设备生产大国。另外,在国家政策鼓励和支持下,我国各地都在促进制药机械设备行业转型升级,如今,制药机械设备产品技术也从简单仿制发展到合作开发和自主创新研发的阶段,我国制药机械设备行业研发能力有所提升。但是从目前来看,我国还并不是制药机械设备行业强国。 2、市场机遇:生物医药迅速发展为制药机械行业带来机遇 生物医药产业作为我国确定的七大战略新兴产业之一,具有巨大的发展机遇。根据国家发改委印发的《“十三五”生物产业发展规划》,2020 年,生物产业规模将达到8 万亿~10 万亿元。2018 年将是生物医药产业快速发展的关键之年,规模将日益扩大。我国不断加快发展生物医药产业,提升生物医药产业的整体发展水平,这也给制药机械设备行业带来无限商机。随着《生物医药产业发展“十三五”规划》的出台,未来生物医药产业将以产业化、市场化、规模化为重点,推动
