4超临界CO2状态观测及PVT关系测定实验
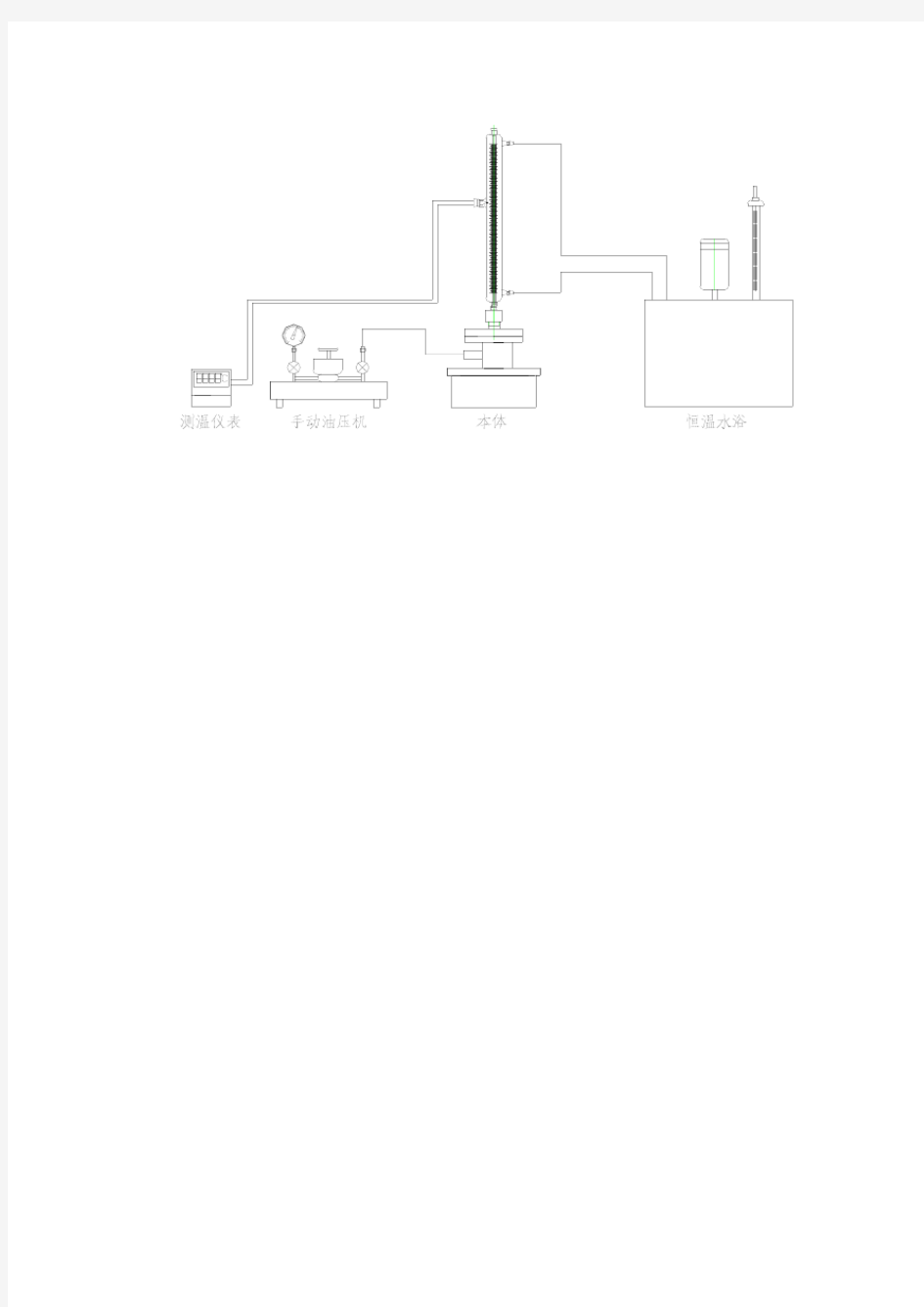
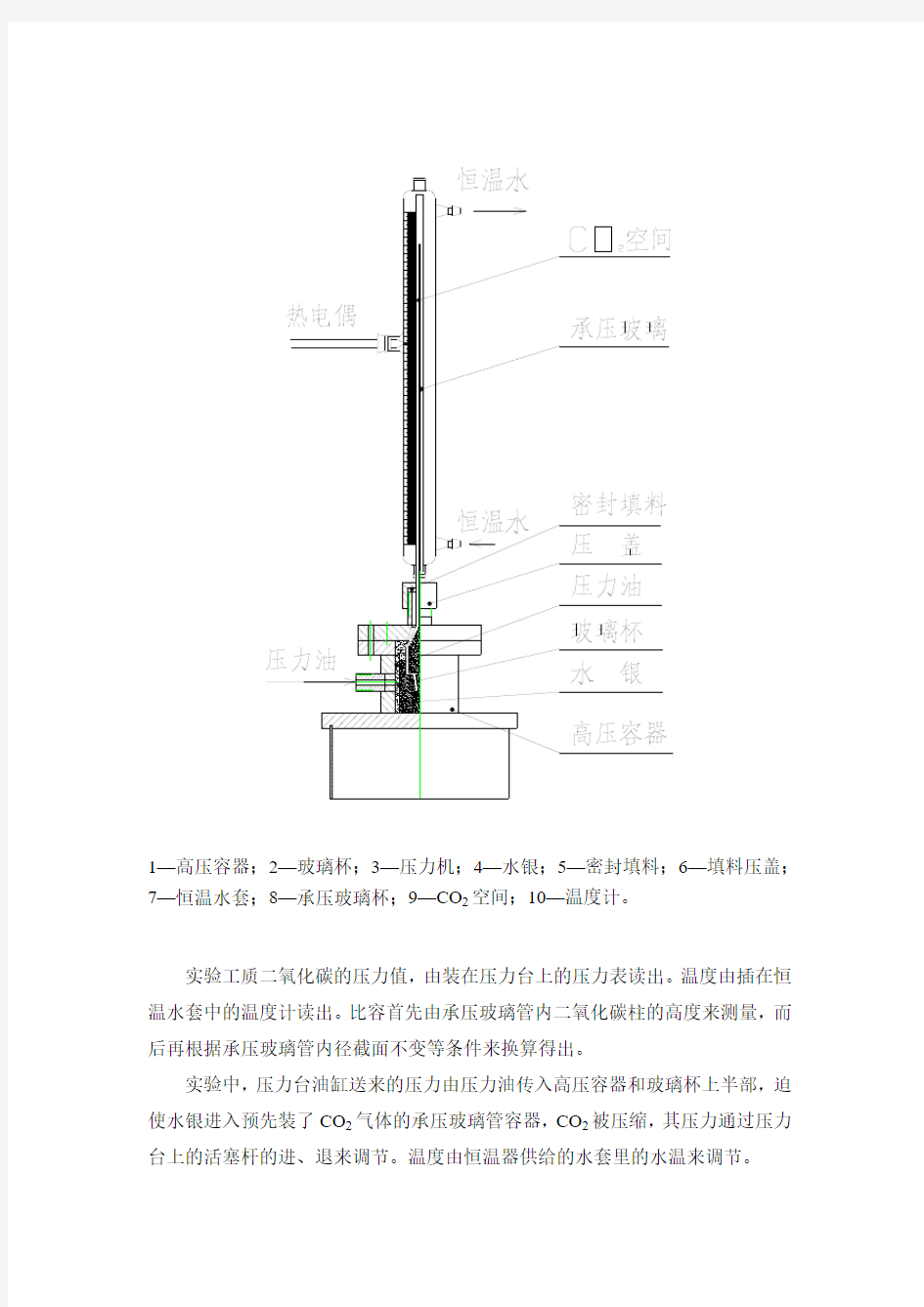
1—高压容器;2—玻璃杯;3—压力机;4—水银;5—密封填料;6—填料压盖;7—恒温水套;8—承压玻璃杯;9—CO2空间;10—温度计。
实验工质二氧化碳的压力值,由装在压力台上的压力表读出。温度由插在恒温水套中的温度计读出。比容首先由承压玻璃管内二氧化碳柱的高度来测量,而后再根据承压玻璃管内径截面不变等条件来换算得出。
实验中,压力台油缸送来的压力由压力油传入高压容器和玻璃杯上半部,迫使水银进入预先装了CO2气体的承压玻璃管容器,CO2被压缩,其压力通过压力台上的活塞杆的进、退来调节。温度由恒温器供给的水套里的水温来调节。
4、作好实验的原始记录: (1)设备数据记录:
仪器、仪表名称、型号、规格、量程、等。 (2)常规数据记录:
室温、大气压、实验环境情况等。
(3)测定承压玻璃管内CO 2质量不便测量,而玻璃管内径或截面积(A )又不易测准,因而实验中采用间接办法来确定CO 2的比容,认为CO 2的比容ν与其高度是一种线性关系。具体方法如下:
a )已知CO 2液体在20℃,9.8MPa 时的比容ν(20℃,9.8Mpa )=0.00117M 3·㎏。
b )实际测定实验台在20℃,9.8Mpa 时的CO 2液柱高度Δh 0(m )。(注意玻璃管水套上刻度的标记方法)
c )∵ν(20℃,9.8Mpa )=kg m m
A
h /00117.030=? ∴
)/(00117
.020m kg K h A m =?= 其中:K ——即为玻璃管内CO 2的质面比常数。 所以,任意温度、压力下CO 2的比容为:
K h
A m h ?=
?=
/ν (m 3/kg )
式中,Δh=h-h 0
h ——任意温度、压力下水银柱高度。 h 0——承压玻璃管内径顶端刻度。
5、测定低于临界温度t=20℃时的等温线。 (1)将恒温器调定在t=20℃,并保持恒温。
(2)压力从4.41Mpa 开始,当玻璃管内水银柱升起来后,应足够缓慢地摇进活塞螺杆,以保证等温条件。否则,将来不及平衡,使读数不准。
(3)按照适当的压力间隔取h 值,直至压力p=9.8MPa 。
(4)注意加压后CO 2的变化,特别是注意饱和压力和饱和温度之间的对应关系以及液化、汽化等现象。要将测得的实验数据及观察到的现象一并填入表1。
(5)测定t=25℃、27℃时其饱和温度和饱和压力的对应关系。
6、测定临界参数,并观察临界现象。
(1)按上述方法和步骤测出临界等温线,并在该曲线的拐点处找出临界压力p c和临界比容 c,并将数据填入表1。
(2)观察临界现象。
a)整体相变现象
由于在临界点时,汽化潜热等于零,饱和汽线和饱和液线合于一点,所以这时汽液的相互转变不是象临界温度以下时那样逐渐积累,需要一定的时间,表现为渐变过程,而这时当压力稍在变化时,汽、液是以突变的形式相互转化。
b)汽、液两相模糊不清的现象
处于临界点的CO2具有共同参数(p,v,t),因而不能区别此时CO2是气态还是液态。如果说它是气体,那么,这个气体是接近液态的气体;
如果说它是液体,那么,这个液体又是接近气态的液体。下面就来用实验证明这个结论。因为这时处于临界温度下,如果按等温线过程进行,使CO2压缩或膨胀,那么,管内是什么也看不到的。
现在,我们按绝热过程来进行。首先在压力等于7.64Mpa附近,突然降压CO2状态点由等温线沿绝热线降到液区,管内CO2出现明显的液面。这就是说,如果这时管内的CO2是气体的话,
那么,这种气体离液区很接近,可以说是接近液态的气体;当我们在膨胀之后,突然压缩CO2时,这个液面又立即消失了。这就告诉我们,这时CO2液体离气区也是非常接近的,可以说是接近气态的液体。
既然,此时的CO2既接近气态,又接近液态,所以能处于临界点附近。可以这样说:临界状态究竟如何,就是饱和汽、液分不清。这就是临界点附近,饱和汽、液模糊不清的现象。
7、测定高于临界温度t=50℃时的定温线。将数据填入原始记录表1。
二、实验记录
实验日期2019 年04 月20日气压101.3KPa 室温23℃气象情况晴(包括实验现象的观察,实验数据的记录)
实验原始数据记录表
三、撰写实验报告
1.数据处理(包括计算示例、数据图表)
以t=20℃时,p=4 MPa为例,已知此时△h=117mm 当p=9.8MPa时,△h=41.5 mm
故K=△h0/(0.00117)=13..5/0.117=11538.5 而V=△h/K=117/11538.5=0.01014
根据该计算方式列表计算并作图如下:
2.实验结果及讨论(包括误差分析)
通过对比实验作出的图形和标准曲线图分析误差及原因,根据标准曲线可得出V c=0.00216,而通过实验计算绘图所得到得到的V c实=0.0294,通过对比发现实验值和理论值基本接近,但仍然存在一定的误差。
总结造成误差的原因如下:1.读数误差较大,刻度线难以持平,读数时间既不能过快也不能过慢,过快容易导致读数错误,过慢则容易使平衡发生较大变化,使得读数不准确;2.实验过程中有温度变化的影响,实验的温度参数并不容易控制,常常因仪器本身的问题产生波动,难以精确控制;3.压力调控不精确,控制压力的操作不够熟练,导致实验读数过程中难以很好地保持稳压状态。
四、自评(包括实验收获)
通过本次二氧化碳临界状态观测及p-v-t关系测定实验,我了解CO2临界状态的观测方法,增加对临界状态概念的感性认识,同时我意识到,在实验时,细心和耐心一定要有,更应该去培养。而且实验前的预习对实验同样有很大的帮助的,一方面能够给我们节省大量的时间,另一方面能够让我们在实际操作的时候不至于手忙脚乱的,代替的是更加的得心应手。
在实验操作中操作顺序,操作时间也要严格的把握好,分毫都不能出差错。只有这样才能真正增加我们对课堂所讲的工质热力状态、凝结、汽化、饱和状态等基本概念的理解,熟练地掌握CO2的p-v-t关系的测定方法,学会用实验测定实际气体状态变化规律的方法和技巧。此外我还学会了学会活塞式压力计,恒温器等热工仪器的正确使用方法。
最后,由于我们需要操作的东西很多,而且很繁琐,这就给我们创造了些许的麻烦,在其中我深刻的体会到实验是一门操作性很强的科目,只有自己亲自动手操作了才能真正的掌握其中的要点。
五、指导老师批审意见
实验报告评分表
碱度的测定(全套步骤)
一.天平的使用 实验室电子天平:梅特勒-托利多AL204/01 1. 工作原理 电磁力平衡的原理 2. 基本操作 使用环境:首先,放置天平的工作台应稳定牢固,远离震动源;周围没有高强电磁场;没有排放有毒有腐蚀性气体的污染源;尽可能远离门、窗、散热器以及空调装置的出风口。其次,天平室温度和湿度应保持恒定,温度控制在20℃~28℃、湿度在40%RH-70%RH之间。 调整:开机前,首先检查天平是否处于水平状态,即天平水平仪中水平泡是否处于中心位置,如果天平未处于水平,则调节天平底脚两个水平旋钮加以校正。如果在称重过程中不可避免的要移动天平,则每次移动后,都要重新调整水平。 开机预热:连接电源,让秤盘空载,按“On/Off”按钮。天平开启并进行自检,自检通过显示0.0000g,进入预热。为保证获得精确的称量结果,必须至少在校准前60 分钟开机,以达到工作温度。但在一般情况下,天平开机后,让其保持在待机状态下,预热20 分钟,即可称量。 校准:在开机状态下,将天平称盘上的被称量物清除,按“->0/T<-”(清零/ 去皮)键,待显示器稳定显示。接着按住“Cal”键不放,直到显示“Cal 200.0000g”字样,放入标值200g 的校准砝码在秤盘中心位置,天平自动进行校准,当“Cal 0.0000g”闪烁时,移去砝码,随后显示屏上短时间出现“CAL donE”信息,紧接着又出现“0.0000g”时,天平校准结束。天平进入称量工作状态,等待称量。 称量:打开玻璃防风罩密封门,将待测物轻轻放在秤盘中心,关上密封门,待示值稳定后,记录下待测物的质量,再将被测物轻轻取出,关紧密封门;当称量过程中需要去皮,按去皮按钮(O/T),此时示值为“0.0000g”。 关机:称量完毕,确定天平秤盘上清洁无物后,按住“On/Off”按钮直至关机(屏幕上无显示)。如还需要继续使用,可以不关闭天平。 3.注意事项 应使用自带的电源适配器,并按说明书选择适当的电压(~220V 或110V)。 当称量易挥发和具有腐蚀性的物品时,要将物品盛放在密闭的容器内,以免称量不准和腐蚀天平。在称重过程,一定要避免用尖锐的物品接触天平的操作键盘。尽量避免裸指直接接触按键,否则日久天长,手指上的汗渍会侵蚀坏按键保护层。 4.维护和保养方法 经常对电子天平进行自校或定期外校,使其处于最佳工作状态。 当称量易挥发和具有腐蚀性的物品时,要将物品盛放在密闭的容器内,以免腐蚀和损坏电子天平。一般情况下,不要将过热或过冷的物体放在天平内称量,宜当物体的温度与天平室的温度达到一致后,方可进行称量。 在称重时,电子天平严禁超载,称量较重物品时,称量时间应尽可能短。 在对秤盘和外壳擦拭时,可以用一块柔软、没有绒毛的织物来轻轻擦拭,严禁使用具有强溶性的清洁剂清洗。对称量时撒落在称量室的物品要及时清理干净。如果电子分析天平长时间搁置不用,应定期对其进行通电检查,确保电子元器件的干燥。
二氧化碳含量的测定方法
实验:水中亚硝酸盐的测定 学号: 姓名: 班级: 【实验方法】 偶合分光光度法 【实验原理】 在PH 以下,水中亚硝酸盐与对氨基苯磺酰胺重氮化,再与盐酸N-(1-萘)-乙二胺产生偶合反应,生成紫红色的偶氮染料,比色定量。 【实验试剂】 1、对氨基苯磺酰胺溶液(10g/L):称取5g对氨基苯磺酰胺(H2NC6H4SO3NH2),溶于350 mL盐 酸溶液中。用纯水稀释至500 mL。 2、盐酸N-(1-萘)-乙二胺溶液(1.0g/L):又名NEDD溶液,称取0.2g盐酸N-(1-萘基)- 乙二胺(C10H7NH2CHCH2·NH2·2HCl),溶于200 mL纯水中。储存于冰箱中。可稳定数周,如试剂颜色变深,应弃去重配。 3、亚硝酸盐氮标准使用溶液【ρ(NO2-N)=μg/mL】 【实验仪器】 1、分光光度计 2、50 mL具塞比色管: 30支 3、5 mL刻度吸管:10支 4、1mL比色皿:1个 【分析步骤】 1、取50mL水样置于比色管中。 2、取50mL比色管7支,分别加入亚硝酸盐氮标准液0mL、、、、、、,用纯水稀释至50mL。 3、向水样及标准色列管中分别加入1 mL对氨基苯磺酰胺溶液,摇匀后放置2min~8min。加 入 mL盐酸N-(1-萘基)-乙二胺溶液,立即混匀。 4、于540nm波长,用1cm比色皿,以纯水作参比,在10min至2h内,测定吸光度。
5、绘制标准曲线,从曲线上查出水样中亚硝酸盐氮的含量。 【数据分析】 ρ(NO2-N)=m/V 注:ρ(NO2-N)——水样中亚硝酸盐氮的质量浓度,单位为mg/L m——从标准曲线上查得样品管中亚硝酸盐氮的质量,单位为微克(μg)V——水样体积,单位为毫升(mL)
吸收(二氧化碳-水)实验讲义
填料吸收塔实验 【实验目的】 ⒈ 了解填料吸收塔的结构和流体力学性能。 ⒉ 学习填料吸收塔传质能力和传质效率的测定方法。 【实验内容】 1.测定填料层压强降与操作气速的关系,确定填料塔在某液体喷淋量下的液泛气速。 2.采用水吸收二氧化碳,空气解吸水中二氧化碳,测定填料塔的液侧传质膜系数和总传质系数。 【实验原理】 1.气体通过填料层的压强降 压强降是塔设计中的重要参数,气体通过填料层压强降的大小决定了塔的动力消耗。压强降与气液流量有关,不同喷淋量下的填料层的压强降ΔP 与气速u 的关系如图6-1-1所示: 图6-1-1 填料层的ΔP ~u 关系 当无液体喷淋即喷淋量L 0=0时,干填料的ΔP ~u 的关系是直线,如图中的直线0。当有一定的喷淋量时,ΔP ~u 的关系变成折线,并存在两个转折点,下转折点称为“载点”,上转折点称为“泛点”。这两个转折点将ΔP ~u 关系分为三个区段:恒持液量区、载液区与液泛区。 2.传质性能 吸收系数是决定吸收过程速率高低的重要参数,而实验测定是获取吸收系数的根本途径。对于相同的物系及一定的设备(填料类型与尺寸),吸收系数将随着操作条件及气液接触状况的不同而变化。 (1) 膜系数和总传质系数 根据双膜模型的基本假设,气相侧和液相侧的吸收质A 的传质速率方程可分别表达为 气膜 )(Ai A g A p p A k G -= (6-1-7) 液膜 )(A Ai l A C C A k G -= (6-1-8)
式中:A G —A 组分的传质速率,1 -?s kmoI ; A —两相接触面积,m 2; A P —气侧A 组分的平均分压,Pa ; Ai P —相界面上A 组分的平均分压,Pa ; A C —液侧A 组分的平均浓度,3-?m kmol Ai C —相界面上A 组分的浓度3-?m kmol k g —以分压表达推动力的气侧传质膜系数,112---???Pa s m kmol ; k l —以物质的量浓度表达推动力的液侧传质膜系数,1-?s m 。 P 2 ,F L P A P A +dP C A +dC A P 1=P A 1 C A1,F L 图6-1-2双膜模型的浓度分布图 图6-1-3 填料塔的物料衡算图 以气相分压或以液相浓度表示传质过程推动力的相际传质速率方程又可分别表达为 )(*-=A A G A p p A K G (6-1-9) )(A A L A C C A K G -=* (6-1-10) 式中:* A p —液相中A 组分的实际浓度所要求的气相平衡分压,Pa ; * A C —气相中A 组分的实际分压所要求的液相平衡浓度,3 -?m kmol ; K G —以气相分压表示推动力的总传质系数或简称为气相传质总系数, 112---???Pa s m kmol ;
金属腐蚀与防护考试试卷(附实验)及答案
金属腐蚀与防护试卷1 一、解释概念:(共8分,每个2分) 钝性,碱脆、SCC、缝隙腐蚀 二、填空题:(共30分,每空1分) 1.称为好氧腐蚀,中性溶液中阴极反应为,好氧腐蚀主要为控制,其过电位与电流密度的关系为。 2.在水的电位-pH图上,线?表示关系,线?表示关系,线?下方是的稳定存在区,线?上方是的稳定存在区,线?与线?之间是的稳定存在区。 3.热力系统中发生游离CO2腐蚀较严重的部位是,其腐蚀特征是,防止游离CO2腐蚀的措施是,运行中将给水的pH值控制在范围为宜。 4.凝汽器铜管在冷却水中的脱锌腐蚀有和形式。淡水作冷却水时易发生脱锌,海水作冷却水时易发生脱锌。 5.过电位越大,金属的腐蚀速度越,活化极化控制的腐蚀体系,当极化电位偏离E corr足够远时,电极电位与极化电密呈关系,活化极化控制下决定金属腐蚀速度的主要因素为、。 ) 6.为了防止热力设备发生氧腐蚀,向给水中加入,使水中氧含量达到以下,其含量应控制在,与氧的反应式为,加药点常在。 7.在腐蚀极化图上,若P c>>P a,极极化曲线比极极化曲线陡,这时E corr值偏向电位值,是控制。 三、问答题:(共24分,每小题4分) 1.说明协调磷酸盐处理原理。 2.自然界中最常见的阴极去极化剂及其反应是什么 3.锅炉发生苛性脆化的条件是什么 4.凝汽器铜管内用硫酸亚铁造膜的原理是什么 5.说明热力设备氧腐蚀的机理。 6.说明腐蚀电池的电化学历程,并说明其四个组成部分。 /
四、计算:(共24分, 每小题8分) 1.在中性溶液中,Fe +2=106-mol/L ,温度为25℃,此条件下碳钢是否发生析氢腐蚀并求出碳钢在此条件下不发生析氢腐蚀的最小pH 值。(E 0Fe 2+/Fe = - ) 2.写出V -与i corr 的关系式及V t 与i corr 的关系式,并说明式中各项的物理意义。 3.已知铜在含氧酸中和无氧酸中的电极反应及其标准电极电位: Cu = Cu 2+ + 2e E 0Cu 2+/Cu = + H 2 = 2H + + 2e E 02H +/H = 2H 2O = O 2 + 4H + + 4e E 0O 2/H 2O = + 问铜在含氧酸和无氧酸中是否发生腐蚀 五、分析:(共14分,每小题7分) 1.试用腐蚀极化图分析铁在浓HNO 3中的腐蚀速度为何比在稀HNO 3中的腐蚀速度低 { 2. 炉水协调磷酸盐-pH 控制图如图1,如何根据此图实施炉水水质控制,试分析之。 (25 15 20 pH o C) 9.809.609.409.209.008.80 2 3 4 5 6 7 8 9 10 R =2.8R =2.6 R =2.4R =2.3R =2.2R =2.1
二氧化碳填料吸收与解吸实验.
二氧化碳填料吸收与解吸实验装置说明书 天津大学化工基础实验中心 2013.06
一、实验目的 1.了解填料吸收塔的结构、性能和特点,练习并掌握填料塔操作方法;通过实验测定数据的处理分析,加深对填料塔流体力学性能基本理论的理解,加深对填料塔传质性能理论的理解。 2.掌握填料吸收塔传质能力和传质效率的测定方法,练习对实验数据的处理分析。 二、实验内容 1. 测定填料层压强降与操作气速的关系,确定在一定液体喷淋量下的液泛气速。 2. 固定液相流量和入塔混合气二氧化碳的浓度,在液泛速度下,取两个相差较大的气相流量,分别测量塔的传质能力(传质单元数和回收率)和传质效率(传质单元高度和体积吸收总系数)。 3. 进行纯水吸收二氧化碳、空气解吸水中二氧化碳的操作练习,同时测定填料塔液侧传质膜系数和总传质系数。 三、实验原理: 气体通过填料层的压强降:压强降是塔设计中的重要参数,气体通过填料层压强降的大小决定了塔的动力消耗。压强降与气、液流量均有关,不同液体喷淋量下填料层的压强降P ?与气速u 的关系如图一所示: 图一 填料层的P ?~u 关系 当液体喷淋量00=L 时,干填料的P ?~u 的关系是直线,如图中的直线0。当有
一定的喷淋量时,P ?~u 的关系变成折线,并存在两个转折点,下转折点称为“载点”,上转折点称为“泛点”。这两个转折点将P ?~u 关系分为三个区段:既恒持液量区、载液区及液泛区。 传质性能:吸收系数是决定吸收过程速率高低的重要参数,实验测定可获取吸收系数。对于相同的物系及一定的设备(填料类型与尺寸),吸收系数随着操作条件及气液接触状况的不同而变化。 1.二氧化碳吸收-解吸实验 根据双膜模型的基本假设,气侧和液侧的吸收质A 的传质速率方程可分别表达为气膜 )(Ai A g A p p A k G -= (1) 液膜 )(A Ai l A C C A k G -= (2) 式中:A G —A 组分的传质速率,1-?s kmoI ; A —两相接触面积,m 2; A P —气侧A 组分的平均分压,Pa ; Ai P —相界面上A 组分的平均分压,Pa ; A C —液侧A 组分的平均浓度,3-?m kmol Ai C —相界面上A 组分的浓度3-?m kmol g k —以分压表达推动力的气侧传质膜系数,112---???Pa s m kmol ; l k —以物质的量浓度表达推动力的液侧传质膜系数,1-?s m 。 以气相分压或以液相浓度表示传质过程推动力的相际传质速率方程又可分别表达为: )(*-=A A G A p p A K G (3) )(A A L A C C A K G -=* (4) 式中:*A p —液相中A 组分的实际浓度所要求的气相平衡分压,Pa ; * A C —气相中A 组分的实际分压所要求的液相平衡浓度,3-?m kmol ; G K —以气相分压表示推动力的总传质系数或简称为气相传质总系数, 112---???Pa s m kmol ;
实验二氧化碳分子量的测定
实验二氧化碳分子量的 测定 TTA standardization office【TTA 5AB- TTAK 08- TTA 2C】
实验二氧化碳相对分子量的测定 实验目的 1、学习气体相对密度法测定分子量的原理、加深理解理想气体状态方程式和阿佛加德罗定律。 2、掌握二氧化碳分子量的测定和计算方法 3、进一步练习使用启普气体发生器和电子天平称量的操作。 实验原理 1、阿佛加得罗定律:同温、同压、同体积的气体含有相同的分子数,即摩尔数相同。根据阿佛加德罗定 律,只要在同温、同压下,比较同体积的两种气体(设其中之一的分子量为巳知)的质量,即可测定气态 物质的分子量。 本实验是把同体积的二氧化碳气体与空气(其平均分子量为相比,此时有: m空气/ M空气 = m CO2 / M CO2, 即 M CO2= m CO2·M空气/ m空气其中, M空气= 2、理想气体状态方程 PV=n R T 3、制备二氧化碳 反应方程式: CaCO3+2HCl=CaCl2+CO2+H2O 因为大理石中含有硫,所以在气体发生过程中有硫化氢、酸雾、水汽产生。此时可通过硫酸铜溶液,碳酸氢钠溶液以及无水氯化钙除去硫化氢,酸雾和水汽。 实验内容 1、二氧化碳的制取、收集和净化 2、第一次称量 取一个洁净而干燥的锥形瓶,选一个合适的瓶塞塞入瓶口,并在塞子上做一记号,以固定塞子塞入瓶口的位置,在电子天平上称量质量m A:m A=m空气+m锥形瓶+m瓶塞 3、收集二氧化碳 在启普发生器中产生二氧化碳气体,经过净化、干燥后导入锥形瓶中。由于二氧化碳气体略重于空气,所以必须把导管伸入瓶底。收集满气体后,轻轻取出导气管,用塞子塞住瓶口(应与原来塞入瓶 口的位置相同)。 4、第二次称量: 在电子天平上称量二氧化碳、锥形瓶、瓶塞总质量m1: m1=m co2+m锥形瓶+m瓶塞 5、平行称量重复3、4步操作,得m2 m2=m co2+m锥形瓶+m瓶塞 6、将4、5的称量值即m1、m2求平均值m B。 m B= m co2平均+m锥形瓶+m瓶塞 7、在锥形瓶内装满水,塞好瓶塞,注意橡皮塞进入的高度与记号相齐。 8、第四次称量 在台秤上称取水+锥形瓶+瓶塞的质量为 m c: m c=m水+m锥形瓶+m瓶塞 数据处理 根据阿佛加得罗定律: m空气/ M空气 = m CO2 / M CO2, 即 M CO2=m CO2·M空气/ m空气 其中, M空气= 即 M CO2= .m CO2/ m空气 (1) 那么, m空气=?
水中总有机碳TOC的测定
水中总有机碳(TOC)的测定 一、实验目的: 通过本实验,了解本仪器的工作原理,熟悉各操作步骤。 二、方法原理: 总有机碳TOC(Total Organic Carbon),是以构成有机物成分之一的碳的数量表示有机污染物质的量。它是把水中所含有机物质里面的碳转化成二氧化碳后加以测定而求得的。 TOC-10B自动测定仪采用分别测出总碳量和无机碳量,并从两者的差值求得TOC的方法。测定原理如下: 用空气泵将空气引入吸气管,吸气管置于TC电炉内。900℃的高温足以把空气中含碳的物质变成CO2,由吸气管而来的空气经由空气过滤器除尘,由CO2吸收器除CO2制成载气。 载气被通入TC和IC两个通道,它们由各自的流量控制阀控制在给定的流速下,空气按给定的流速进入燃烧管(不是T C燃烧管就是IC反应管,这要根据所需要的途径来选择)。一定量的样品由微量注射器通过注射口注入,使其燃烧或分解。分解或燃烧后的气体直接通过T C一IC选择部分到除水器以除去剩余水气。经这样处理的气体引入红外分析部分去测量CO2浓度。 (1)总碳量(TC )的测定: 用微量注射器将样品注入燃烧管中,在900℃的高温及C O304催化剂的作用下样品中所有含碳物质(T C)燃烧和氧化成CO2,被载气带到红外线分析部分检测,样品所含C的浓度正比于记录议出出现的峰高。 (2) 无机碳(IC)的测量: 用微量注射器将样品注入IC反应管中,在160℃的温度及磷酸催 化剂的作用下样品中所含无机碳(IC)分解产生CO2,被载气带到红外分析部分检测,样品所含C的浓度正比于记录议出出现的峰高。 (3)TOC (总有机碳)的测量: 从T C(总碳)减去IC(无机碳)得到TOC (总有机碳),或者将样 品预处理除去IC,然后在TC通道中进行测量,这样就能直接测量TOC。 (4)红外线分析原理: 由一种原子组成的那些分子如N2、O2、和H2不吸收红外线,由两种原子组成的分子,如CO2和CH3吸收红外线,所吸收的红外线的波长与组成分子的原子种类、结合状态有关。在TOC-10B中,载气中的N2和O2不吸收红外线。但是CO2吸收4.3μm的红外线。所吸收的光量正比于气体的浓度。根据朗勃-比尔定律,气体的浓度可由吸收的光量来测定。红外线分析部分原理如下: 为了测量起见,采用非色散系统代替色散光谱,两股间断平行光由检测器测量,并 对之进行选择,被测气体引入测定池光路中的样品池,在另一光路上的参比池封有不吸
二氧化碳吸收与解吸实验
二氧化碳吸收与解吸实验 一、实验目的 1.了解填料吸收塔的结构、性能和特点,练习并掌握填料塔操作方法;通过实验测定数据的处理分析,加深对填料塔流体力学性能基本理论的理解,加深对填料塔传质性能理论的理解。 2.掌握填料吸收塔传质能力和传质效率的测定方法,练习实验数据的处理分析。 二、实验内容 1. 测定填料层压强降与操作气速的关系,确定在一定液体喷淋量下的液泛气速。 2. 固定液相流量和入塔混合气二氧化碳的浓度,在液泛速度下,取两个相差较大的气相流量,分别测量塔的传质能力(传质单元数和回收率)和传质效率(传质单元高度和体积吸收总系数)。 3. 进行纯水吸收二氧化碳、空气解吸水中二氧化碳的操作练习,同时测定填料塔液侧传质膜系数和总传质系数。 三、实验原理: 气体通过填料层的压强降:压强降是塔设计中的重要参数,气体通过填料层压强降的大小决定了塔的动力消耗。压强降与气、液流量均有关,不同液体喷淋量下填料层的压强降P ?与气速u 的关系如图一所示: 1 2 3 L 3L 2L 1 L 0 = >>0 图一 填料层的P ?~u 关系 当液体喷淋量00=L 时,干填料的P ?~u 的关系是直线,如图中的直线0。 ΔP , k P a
当有一定的喷淋量时,P ?~u 的关系变成折线,并存在两个转折点,下转折点称为“载点”,上转折点称为“泛点”。这两个转折点将P ?~u 关系分为三个区段:既恒持液量区、载液区及液泛区。 传质性能:吸收系数是决定吸收过程速率高低的重要参数,实验测定可获取吸收系数。对于相同的物系及一定的设备(填料类型与尺寸),吸收系数随着操作条件及气液接触状况的不同而变化。 1.二氧化碳吸收-解吸实验 根据双膜模型的基本假设,气侧和液侧的吸收质A 的传质速率方程可分别表达为 气膜 )(Ai A g A p p A k G -= (1) 液膜 )(A Ai l A C C A k G -= (2) 式中:A G —A 组分的传质速率,1-?s kmoI ; A —两相接触面积,m 2 ; A P —气侧A 组分的平均分压,Pa ; Ai P —相界面上A 组分的平均分压,Pa ; A C —液侧A 组分的平均浓度,3-?m kmol Ai C —相界面上A 组分的浓度3-?m kmol g k —以分压表达推动力的气侧传质膜系数,112---???Pa s m kmol ; l k —以物质的量浓度表达推动力的液侧传质膜系数,1-?s m 。 以气相分压或以液相浓度表示传质过程推动力的相际传质速率方程又可分别表达为: )(*-=A A G A p p A K G (3) )(A A L A C C A K G -=* (4) 式中:*A p —液相中A 组分的实际浓度所要求的气相平衡分压,Pa ; * A C —气相中A 组分的实际分压所要求的液相平衡浓度,3-?m kmol ; G K —以气相分压表示推动力的总传质系数或简称为气相传质总系数,112---???Pa s m kmol ;
ASTM D513-02 水中溶解二氧化碳总量和容量的测量方法(中文版)
水中溶解二氧化碳溶解量和总量的测量方法 1适用范围 1.1 本标准用于指导测定如二氧化碳(CO2)、碳酸、碳酸氢根离子、碳酸根离子在水中的总量和溶量: 测量范围章节范围 方法A(气体感应电极) 2-800 毫克/升8-15 方法B(CO2发生库仑滴定) 5-800毫克/升16-24 1.2 本标准也可用于对样品微粒中的碳酸盐进行二氧化碳含量测定 1.3方法A适用于各种天然水和盐水 1.4方法B适用于天然水、盐水以及在16.4节中所描述的各种工业水 1.5使用者有责任确保采用这些水体测试方法对未测试母体水样所得到的结果的有效性。 1.6几种标准测量方法1988年被废止,其历史信息见附录X1。 1.7该标准不支持所有安全考虑的表述,如果有的话,应该与它的使用联系起来。本标准的使用者有责任建立一套适当的安全和健康实施程序并可以在使用前预先做一些相应、局部的调整。 2参考文献 2.1 ASTM标准: D1066 蒸汽取样的实施标准 D1129 与水相关的专用术语 D1192 密闭管蒸汽取样与水取样设备指南 D1193 试剂用水规格说明 D1293 水PH的测定方法 D2777可行的测试标准D19对水的测量的精确度和偏差的判断实施标准 D3370 密闭管水取样的实施标准 D5847 采用标准方法进行水质分析,书面质量控制规格实施标准 E200 化学分析中试剂溶液的配制、贮存的标准化及实施标准 3 专用术语 3.1 注释参照专用术语D1129,对这些测量方法中所用的术语进行定义
4 用途及重要性 4.1 二氧化碳是动植物呼吸最主要的产物,有机物质和部分矿物质分解也产生二氧化碳,大气中二氧化碳的平均含量约为0.04体积%,除去在异常的有机物质和矿物质分解区的地方外,地表水二氧化碳的含量通常都低于10毫克/升,但是地下水,尤其是深层地下水二氧化碳的含量有可能达到几百毫克/升。 4.2当水中溶解有二氧化碳时,它会对水处理系统产生很强的腐蚀作用,尤其在蒸汽冷凝系统这特别是一项麻烦,水处理系统中部分CO2的溢出,将破坏碳酸盐的溶解平衡,从而导致局部表面产生方解石覆盖物。热水器就是一个很好的例子写照,由于存在有微弱的侵蚀和覆盖平衡,水处理系统中一定要重视控制好CO2及其相类似的气体含量。城市供应中蒸汽冷凝的最后阶段进行水软化和胺中和时,采用再碳酸化也就是这一目的。 5 试剂的纯度 5.1在所有测试中使用标准化学试剂。除非有别的说明,所有的试剂都应遵守美国化学委员会 分析试剂委员会的规范,这些规范可以从中得到5别的等级的试剂可使用,但首先必须弄清楚试 剂必须具有足够的纯度才允许使用,从而不会降低测试精度。 5.2除非有别的说明,参考的水应当被认为是平均试剂水,遵守D1193规程,类型Ⅰ。另外在其它的测定方法中需要的去CO2水,可以参考规程E200中的第8.2章。 6注意事项 6.1注意――二氧化碳气体在样品运输和贮存过程中很容易从溶液中逃溢,由于碳酸钙微弱的分解,导致溶液中温度和压力发生改变,所以样品中CO2浓度增加是可能的。 7 取样 7.1 根据规程D1066、D1192和规程D3370上说明进行取样。 7.2 如果过滤样品微粒中含有碳酸盐,那么仅测量CO2溶量。当从试验瓶中取出部分含有微粒的 样品时,试剂瓶应该先摇晃或者让微粒均匀分布来保证所取的样品有代表性。取样后,样品中的微粒形态随温度、pH等变化而改变。这些微粒再样品测试时必须包括在内。样品过滤均质化过程中需小心防止CO2损失.如果不是要求除掉潜在的干扰微粒,样品不要过滤。 7.3用一种坚固的、抗化学作用的玻璃瓶子来取样。 7.4 将取样瓶完全灌满,使其在瓶盖下不留任何空间,将样品在低于取样温度下存放,直至检测。 测试方法A—气体感应电极法
空气中二氧化碳含量的测定实验
空气中二氧化碳含量的测定实验教案 化学一班申伟静郝冬丽冬冬徐亚辉 一,教学目标 知识目标: 1、了解测定二氧化碳含量的简单方法; 2、掌握二氧化碳的基本性质和生活中的应用; 3、通过老师讲解理解二氧化碳在整个环境中作用。 技能目标: 1、通过观看教师的演示实验提高对实验的观察、比较能力。 2、学习掌握如何使用针筒和使用玻璃仪器要注意事项; 3、感悟用分类、对比的学习方法来学习化学的重要作用。 情感目标: 1、通过实验探究来激发学生学习的积极性和主动性, 2、实验初步养成严谨的科学态度。 3、通过对课程的学习可以让同学认识到环境保护重要性。 二,教材分析 本节主要围绕探究测定空气中二氧化碳含量的实验,学习定量测定混合气体中某种气体含量的方法,认识空气中二氧化碳组成及表示方法,增进对二氧化碳的理解。增加学生爱护环境的意识。 三,学情分析 已知 1、学生通过前面的学习,已了解和初步掌握了关于二氧化碳的基本性质。 2、学生通过对实验前的预习掌握了空气中二氧化碳含量测定的基本原理和操作方法。 3、学生在学习中,知道了二氧化碳在我们生活中的作用和在生活中应用。 4、学生在生活中知道保护环境重要意义。 未知 1、学生在实际操作中会出现不规操作,对实验的结果造成影响。还可能损坏仪器。 2、学生在生活中虽然知道环保知识,但付诸实践上仍然不知如何做。 3、学生缺少实验中观察实验现象变化能力。在实验过程中都需要一直观察严谨的态度。 四,重点难点 重点:空气中二氧化碳含量测定的实验步骤 难点:实验的原理
五,教学过程
六,板书设计 一、教学目标 1、让同学们通过实验学会测量空气中二氧化碳的含量 2、通过教学讲解实验操作知道测量二氧化碳含量的原理二,实验原理 向滴有酚酞的氨水入CO2: CO2 + 2NH3H2O === (NH4)2CO3 CO2 + (NH4)2CO3 + H2O === 2NH4HCO3 pH==8 溶液红色无色 计算公式 N1x ==0.033%N2 三,实验步骤: 1, ,2,装药品:10ml带有酚酞的稀氨水溶液(已配好)3,抽气 4,排气,重复操作,记录次数N,记录在下表 N1是实验室抽气的次数 N2是空旷地点抽气的次数
二氧化碳吸收与解吸实验汇总情况
实用标准 二氧化碳吸收与解吸实验 一、实验目的 1.了解填料吸收塔的结构、性能和特点,练习并掌握填料塔操作方法;通过实验测定数据的处理分析,加深对填料塔流体力学性能基本理论的理解,加深对填料塔传质性能理论的理解。 2.掌握填料吸收塔传质能力和传质效率的测定方法,练习实验数据的处理分析。 二、实验内容 1. 测定填料层压强降与操作气速的关系,确定在一定液体喷淋量下的液泛气速。 2. 固定液相流量和入塔混合气二氧化碳的浓度,在液泛速度下,取两个相差较大的气相流量,分别测量塔的传质能力(传质单元数和回收率)和传质效率(传质单元高度和体积吸收总系数)。 3. 进行纯水吸收二氧化碳、空气解吸水中二氧化碳的操作练习,同时测定填料塔液侧传质膜系数和总传质系数。 三、实验原理: 气体通过填料层的压强降:压强降是塔设计中的重要参数,气体通过填料层压强降的大小决定了塔的动力消耗。压强降与气、液流量均有关,不同液体喷淋量下填料层的压强降P ?与气速u 的关系如图一所示: 图一 填料层的P ?~ u 关系 当液体喷淋量00=L 时,干填料的P ?~u 的关系是直线,如图中的直线0。
当有一定的喷淋量时,P ?~u 的关系变成折线,并存在两个转折点,下转折点称为“载点”,上转折点称为“泛点”。这两个转折点将P ?~u 关系分为三个区段:既恒持液量区、载液区及液泛区。 传质性能:吸收系数是决定吸收过程速率高低的重要参数,实验测定可获取吸收系数。对于相同的物系及一定的设备(填料类型与尺寸),吸收系数随着操作条件及气液接触状况的不同而变化。 1.二氧化碳吸收-解吸实验 根据双膜模型的基本假设,气侧和液侧的吸收质A 的传质速率方程可分别表达为 气膜 )(Ai A g A p p A k G -= (1) 液膜 )(A Ai l A C C A k G -= (2) 式中:A G —A 组分的传质速率,1-?s kmoI ; A —两相接触面积,m 2 ; A P —气侧A 组分的平均分压,Pa ; Ai P —相界面上A 组分的平均分压,Pa ; A C —液侧A 组分的平均浓度,3-?m kmol Ai C —相界面上A 组分的浓度3-?m kmol g k —以分压表达推动力的气侧传质膜系数,112---???Pa s m kmol ; l k —以物质的量浓度表达推动力的液侧传质膜系数,1-?s m 。 以气相分压或以液相浓度表示传质过程推动力的相际传质速率方程又可分别表达为: )(*-=A A G A p p A K G (3) )(A A L A C C A K G -=* (4) 式中:*A p —液相中A 组分的实际浓度所要求的气相平衡分压,Pa ; * A C —气相中A 组分的实际分压所要求的液相平衡浓度,3-?m kmol ; G K —以气相分压表示推动力的总传质系数或简称为气相传质总系数,112---???Pa s m kmol ;
瓦斯等级鉴定及二氧化碳检测报告
XXXXXXXX项目 瓦斯等级鉴定及二氧化碳 检测报告 XXX单位 二〇一四年一月二十五日
XXX隧道 瓦斯等级鉴定及二氧化碳检测报告检测人员: 报告编写: 报告审查: XXX单位 二〇一四年一月二十五日
声明 1、本报告未加盖本中心公章无效。 2、报告内容不得自行涂改、增删,否则因此引起的一切后果与本中心无关。 3、未经本中心书面批准,不得复制测试报告。 4、送样委托检验,本中心不对样品来源负责,报告结果仅对所鉴定样品有效。 5、对试验报告若有异议,请在报告发出之日起十五日内向本中心提出。
《XXX隧道瓦斯等级鉴定及 二氧化碳检测报告》内审意见 2014年1月25日,XXX单位组织有关专业技术人员对《XXX隧道瓦斯等级鉴定及二氧化碳检测报告》进行了内部审查,经认真审查,形成初步审查意见如下: (1)本检测报告依据较充分,使用规范恰当,工作方法合理。 (2)隧道区地质条件分析较为详尽,对隧道区瓦斯等气体的形成原因以及涌出形式的分析基本符合实际。 (3)瓦斯(二氧化碳)涌出量的测定方法与计算公式正确,计算参数与计算结果基本准确。 (4)在瓦斯涌出量分析基础上,对隧道瓦斯等级的认定符合规定,由此提出的瓦斯等气体防治方案的建议基本可行。 同意上报相关部门审查后实施。 审查负责人: XXX单位 二0一四年一月二十二日
目录 1 概况 (1) 1.1 项目概况 (1) 1.2 目的及任务 (1) 1.3 执行的技术规范、规定及标准 (2) 1.4 以往地质资料 (3) 1.5 鉴定工作情况 (3) 1.5.1工作组织情况 (3) 1.5.2完成工作量 (3) 2 隧道区地质条件简述 (5) 2.1 自然地理 (5) 2.1.1 地形地貌 (5) 2.1.2 气象及水文 (5) 2.2 地层岩性 (6) 2.3 地质构造及地震 (7) 2.4 水文地质 (8) 3 隧道瓦斯地质分析 (10) 3.1 瓦斯成因分析 (10) 3.2 瓦斯涌出形式分析 (10) 4 瓦斯(二氧化碳)测定与计算 (12) 4.1 测定方法 (12)
二氧化碳结合力
. 二氧化碳结合力是在特定温度和压力下测定溶解至血浆或血清中二氧化碳的量,也就是指在隔绝空气的条件下,将病人血浆用正常人的肺泡气(pCO2均为5.32kpa)平衡过,所测得血浆内CO2的含量,减去已知的溶于血浆中的CO2部分所得的值,反映体内的碱贮备量,主要用来了解血中碳酸氢钠的含量,判断有无酸碱平衡失调及其程度,测定肾脏调节酸碱平衡的功能。 二氧化碳结合力正常值:成人22~29mmol/L;儿童18~27mmol/L. 二氧化碳结合力临床意义:(1)增高示代谢性碱中毒(如由急性胃炎、幽门梗阻、妊娠呕吐、肾上腺皮质功能亢进、低钾、服用碱性药物过多、服用地塞米松类药物过多等引起)、或代偿后的呼吸性酸中毒(如由慢性支气管炎、阻塞性肺气肿、肺心病、支气管哮喘持续状态、支气管扩张、广泛性肺纤维化、肺实变、吗啡中毒等引起)。常见于幽门梗阻、剧烈呕吐、胃酸损失过多;或服过量碱性药物后所致之代谢性碱中毒,以及肺源性心脏病等呼吸中枢抑制疾患所致代偿性呼吸性酸中毒。 (2)减低示碱储备不足,为代谢性酸中毒,亦可为代偿性呼吸性碱中毒。只有代谢性酸中毒,或呼吸性碱中毒才显示降低。 二氧化碳结合力降低,最常见于感染性休克,流行性出血热等病,降低越多,示病情越重且预后不良。出血热休克期、少尿期,糖尿病昏迷时降低均较显著。降低还常见于严重腹泻、肾功能衰竭、肠道瘘管等病引起的代谢性酸中毒,及各种病因引起的呼吸中枢兴奋,各种呼吸道疾患等呼吸性碱中毒。 此外服过量酸性药物(如水杨酸钠等),亦可致二氧化碳结合力降低。代谢性酸中毒的轻重,根据二氧化碳结合力降低程度分为 轻度酸中毒22.45~17.96mmol/L 中度酸中毒17.96~13.47mmol/L 重度酸中毒<13.47mmol/L; 预后极严重<6.74mmol/L。 .
二氧化碳吸收与实验
二氧化碳吸收实验装置 说明书 天津大学化工基础实验中心 2015.04
一、实验目的 1.了解填料吸收塔的结构、性能和特点,练习并掌握填料塔操作方法;通过实验测定数据的处理分析,加深对填料塔流体力学性能基本理论的理解,加深对填料塔传质性能理论的理解。 2.掌握填料吸收塔传质能力和传质效率的测定方法,练习对实验数据的处理分析。 二、实验内容 1. 测定填料层压强降与操作气速的关系,确定在一定液体喷淋量下的液泛气速。 2. 固定液相流量和入塔混合气二氧化碳的浓度,在液泛速度下,取两个相差较大的气相流量,分别测量塔的传质能力(传质单元数和回收率)和传质效率(传质单元高度和体积吸收总系数)。 3. 进行纯水吸收二氧化碳、空气,解吸水中二氧化碳的操作练习。 三、实验原理: 气体通过填料层的压强降: 压强降是塔设计中的重要参数,气体通过填料层压强降的大小决定了塔的动力消耗。压强降与气、液流量均有关,不同液体喷淋量下填料层的压强降P ?与气速u 的关系如图一所示: 图-1 填料层的P ?~u 关系 当液体喷淋量00=L 时,干填料的P ?~u 的关系是直线,如图中的直线0。当有
一定的喷淋量时,P ?~u 的关系变成折线,并存在两个转折点,下转折点称为“载点”,上转折点称为“泛点”。这两个转折点将P ?~u 关系分为三个区段:既恒持液量区、载液区及液泛区。 传质性能: 吸收系数是决定吸收过程速率高低的重要参数,实验测定可获取吸收系数。对于相同的物系及一定的设备(填料类型与尺寸),吸收系数随着操作条件及气液接触状况的不同而变化。 1.二氧化碳吸收-解吸实验 根据双膜模型的基本假设,气侧和液侧的吸收质A 的传质速率方程可分别表达为气膜 )(Ai A g A p p A k G -= (1) 液膜 )(A Ai l A C C A k G -= (2) 式中:A G —A 组分的传质速率,1-?s kmoI ; A —两相接触面积,m 2 ; A P —气侧A 组分的平均分压,Pa ; Ai P —相界面上A 组分的平均分压,Pa ; A C —液侧A 组分的平均浓度,3-?m kmol Ai C —相界面上A 组分的浓度3-?m kmol g k —以分压表达推动力的气侧传质膜系数,112---???Pa s m kmol ; l k —以物质的量浓度表达推动力的液侧传质膜系数,1-?s m 。 以气相分压或以液相浓度表示传质过程推动力的相际传质速率方程又可分别表达为: )(*-=A A G A p p A K G (3) )(A A L A C C A K G -=* (4) 式中:*A p —液相中A 组分的实际浓度所要求的气相平衡分压,Pa ; * A C —气相中A 组分的实际分压所要求的液相平衡浓度,3-?m kmol ; G K —以气相分压表示推动力的总传质系数或简称为气相传质总系数,
空气中二氧化碳含量的测定实验
空气中二氧化碳含量的测定实验 空气中二氧化碳含量的测定实验教案 化学一班申伟静郝冬丽张冬冬徐亚辉一,教学目标 知识目标: 1、了解测定二氧化碳含量的简单方法; 2、掌握二氧化碳的基本性质和生活中的应用; 3、通过老师讲解理解二氧化碳在整个环境中作用。 技能目标: 1、通过观看教师的演示实验提高对实验的观察、比较能力。 2、学习掌握如何使用针筒和使用玻璃仪器要注意事项; 3、感悟用分类、对比的学习方法来学习化学的重要作用。 情感目标: 1、通过实验探究来激发学生学习的积极性和主动性, 2、实验初步养成严谨求实的科学态度。 3、通过对课程的学习可以让同学认识到环境保护重要性。 二,教材分析 本节主要围绕探究测定空气中二氧化碳含量的实验,学习定量测定混合气体中某种气体含量的方法,认识空气中二氧化碳组成及表示方法,增进对二氧化碳的理解。增加学生爱护环境的意识。 三,学情分析 已知 1、学生通过前面的学习,已了解和初步掌握了关于二氧化碳的基本性质。 2、学生通过对实验前的预习掌握了空气中二氧化碳含量测定的基本原理和操作方
法。 3、学生在学习中,知道了二氧化碳在我们生活中的作用和在生活中应用。 4、学生在生活中知道保护环境重要意义。 未知 1、学生在实际操作中会出现不规范操作,对实验的结果造成影响。还可能损坏仪器。 2、学生在生活中虽然知道环保知识,但付诸实践上仍然不知如何做。 3、学生缺少实验中观察实验现象变化能力。在实验过程中都需要一直观察严谨的态度。四,重点难点 重点:空气中二氧化碳含量测定的实验步骤 难点:实验的原理 五,教学过程 实验教学过程 实验环 节教师活动预想学生活动设计意图 【导入新课】:前一段时间日本的核辐射 引起了一场轩然大波,中国的一些城市也 依次检测到碘-131微量辐射。核安全检测空局利用的是手势核素检测仪检测到的微量创设情境,激发兴趣, 元素。同学们,设想一下如果让我们来测引入新课。 碘-131这种微量元素含量大家怎么测呢,让学生通过自主、合 气这个问题放在实验室来进行试验是不是与作学习,了解探究实 以往的实验不一样了呢,这个实验我们提验步骤、方法和原理, 出的是一个问题。那是因为今天我们的实齐声回答:是培养学生阅读和解决中验即将进入一个新的转折点——探究式实问题的能力。 验
2017RQ-1压力容器检验员承压设备损伤模式识别学习资料、答案
一、单选题【本题型共44道题】 1.如果已经发现了碱腐蚀,还应注意下列哪些可能伴随的损伤?() A.蒸汽阻滞 B.球化 C.蠕变 D.敏化 正确答案:[A] 2.下列哪种金属合金元素对耐高温硫化物腐蚀(无氢气环境)能力的影响最明显?() A.镍 B.铬 C.碳 D.钛 正确答案:[B] 3.通过什么方法可以判定是否发生石墨化损伤?() A.抗拉强度测试 B.硬度测定 C.涡流检测 D.金相检验 正确答案:[D] 4.承压设备会因渗氮而发生材质劣化,()材料耐渗氮能力强,不易受到影响。 A.低合金钢 B.400系列不锈钢 C.球墨铸铁 D.镍基合金 正确答案:[D] 5.下列哪个关于球化的表述是错误的?() A.目视检测一般不能发现球化 B.碳钢中片状碳化物形成球状碳化物 C.材料因球化而强度降低的同时延展性也会降低 D.可通过金相分析判断是否发生球化 正确答案:[C] 6.下列哪项不是耐火材料退化伴随的其他损伤?() A.高温氧化腐蚀 B.高温硫化物腐蚀 C.烟气露点腐蚀 D.钛氢化 正确答案:[D]
7.检查燃灰腐蚀的最有效的方法为()。 A.目视检测 B.超声波测厚 C.金相分析 D.沉积物分析技术 正确答案:[A] 8.硫酸浓度低于70%(质量比)时,碳钢的腐蚀速率()。 A.随浓度增高而增大 B.随浓度增高而减小 C.随浓度降低而减小 D.与浓度无关 正确答案:[B] 9.下列哪种已知合金可以耐受所有条件下的金属粉化影响?() A.低合金钢 B.奥氏体不锈钢 C.碳钢 D.目前没有 正确答案:[D] 10.与高温氢腐蚀损伤相关或相伴的其他损伤为()。 A.脱碳 B.渗碳 C.脱硫 D.脱氧 正确答案:[A] 11.下列哪种材料最不耐酸性水腐蚀(碱式酸性水)?() A.双相不锈钢 B.碳钢 C.300系列不锈钢 D.铝合金 正确答案:[B] 12.下列不属于易发生振动疲劳损伤的设备或装置是()。 A.泵、压缩机的管道 B.高压降压力调节阀 C.旋转和往复设备周围的旁通细管及回流细管 D.搅拌反应器 正确答案:[D] 13.运行期间可采用什么方法来检测冷壁设备的高温部位、判断耐火材料的损伤程度?()
二氧化碳吸收实验
填料吸收塔实验装置 说明书 天津大学化工基础实验中心 2014.10
一、实验目的: 1.了解填料吸收塔的结构、性能和特点,练习并掌握填料塔操作方法;通过实验测定数据的处理分析,加深对填料塔流体力学性能基本理论的理解,加深对填料塔传质性能理论的理解。 2.掌握填料吸收塔传质能力和传质效率的测定方法,练习实验数据的处理分析。 二、实验内容: 1.测定填料层压强降与操作气速的关系,确定在一定液体喷淋量下的液泛气速。 2.固定液相流量和入塔混合气二氧化碳的浓度,在液泛速度以下,取两个相差较大的气相流量,分别测量塔的传质能力(传质单元数和回收率)和传质效率(传质单元高度和体积吸收总系数)。 3.进行纯水吸收混合气体中的二氧化碳、用空气解吸水中二氧化碳的操作练习,同时测定填料塔液侧传质膜系数和总传质系数。 三、实验原理: 气体通过填料层的压强降:压强降是塔设计中的重要参数,气体通过填料层压强降的大小决定了塔的动力消耗。压强降与气、液流量均有关,不同液体喷淋量下填料层的压强降P ?与气速u 的关系如图1所示: 图1 填料层的P ?~u 关系 当液体喷淋量00=L 时,干填料的P ?~u 的关系是直线,如图中的直线 0。当有一定的喷淋量时,P ?~u 的关系变成折线,并存在两个转折点,下转折点称为“载点”,上转折点称为“泛点”。这两个转折点将P ?~u 关系分为三个区段:既恒持液量区、载液区及液泛区。
传质性能:吸收系数是决定吸收过程速率高低的重要参数,实验测定可获取吸收系数。对于相同的物系及一定的设备(填料类型与尺寸),吸收系数随着操作条件及气液接触状况的不同而变化。 二氧化碳吸收实验 根据双膜模型的基本假设,气侧和液侧的吸收质A 的传质速率方程可分别表达为 气膜 )(Ai A g A p p A k G -= (1) 液膜 )(A Ai l A C C A k G -= (2) 式中:A G —A 组分的传质速率,1-?s kmoI ; A —两相接触面积,m 2 ; A P —气侧A 组分的平均分压,Pa ; Ai P —相界面上A 组分的平均分压,Pa ; A C —液侧A 组分的平均浓度,3-?m kmol Ai C —相界面上A 组分的浓度3-?m kmol g k —以分压表达推动力的气侧传质膜系数,112---???Pa s m kmol ; l k —以物质的量浓度表达推动力的液侧传质膜系数,1-?s m 。 以气相分压或以液相浓度表示传质过程推动力的相际传质速率方程又可分别表达为: )(*-=A A G A p p A K G (3) )(A A L A C C A K G -=* (4) 式中:*A p —液相中A 组分的实际浓度所要求的气相平衡分压,Pa ; * A C —气相中A 组分的实际分压所要求的液相平衡浓度,3-?m kmol ; G K —以气相分压表示推动力的总传质系数或简称为气相传质总系数,112---???Pa s m kmol ; L K -以气相分压表示推动力的总传质系数,或简称为液相传质总系数,1-?s m 。
