个性化基因检测EGFR KRAS BRAF

EGFR基因突变检测试剂盒(PCR-荧光探针法)
EGFR突变的发生率在亚洲人群达到50%,《NCCN非小细胞肺癌诊断治疗指南》指出,活化的EGFR突变是重要生物学指标。认为EGFR基因突变检测是患者EGFR TKI治疗疗效最好的预测因子。
本试剂盒以石蜡包埋病理切片组织中提取的DNA为检测样本,对体细胞突变的检测,从而辅助非小细胞肺癌(NSCLC)的临床诊断及指导临床用药。
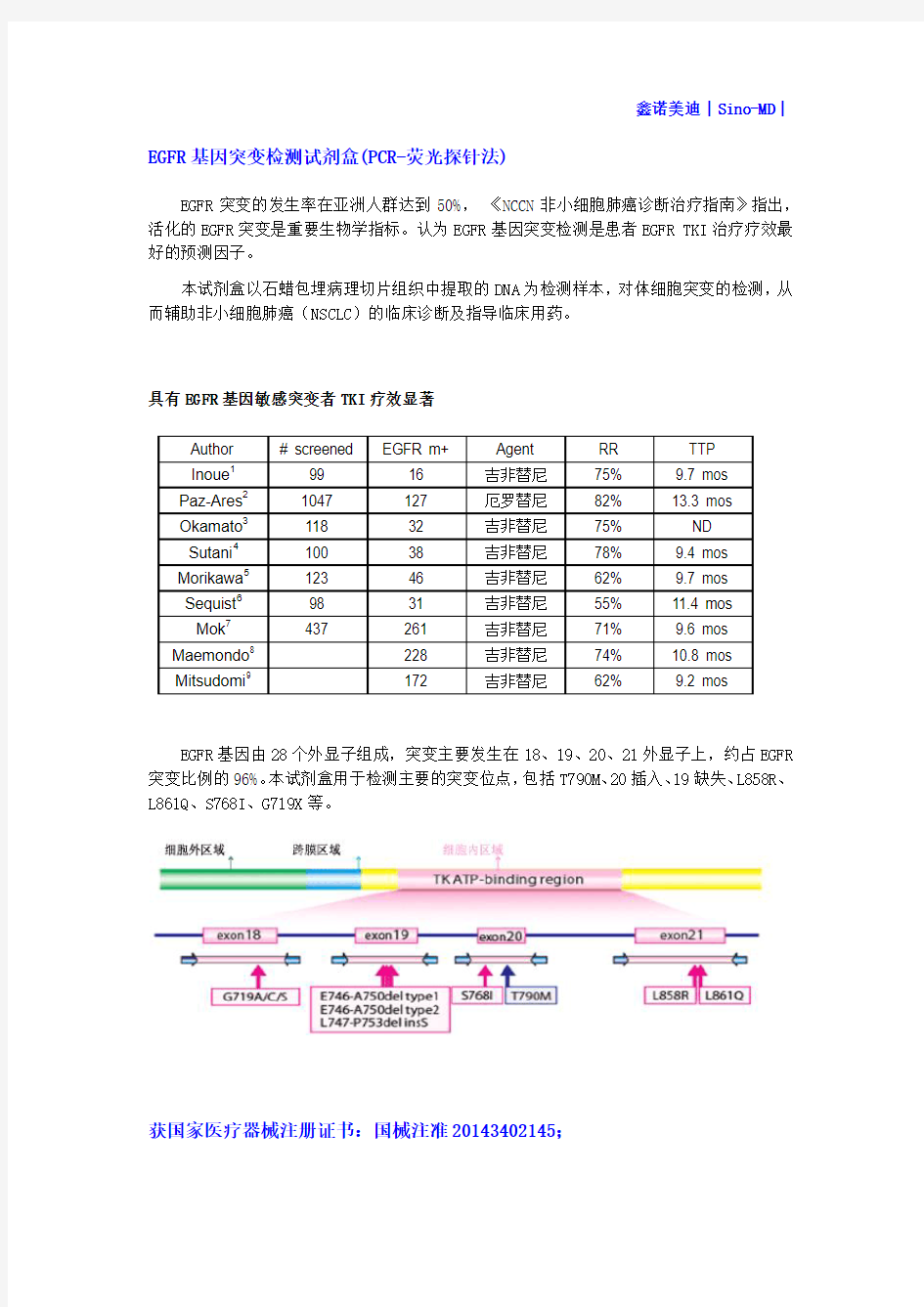
具有EGFR基因敏感突变者TKI疗效显著
EGFR基因由28个外显子组成,突变主要发生在18、19、20、21外显子上,约占EGFR 突变比例的96%。本试剂盒用于检测主要的突变位点,包括T790M、20插入、19缺失、L858R、L861Q、S768I、G719X等。
获国家医疗器械注册证书:国械注准20143402145;
K-ras 基因突变检测试剂盒(PCR-荧光探针法)
KRAS蛋白处于EGFR信号通路的下游。在生
理情况下,EGFR信号通路活化后,KRAS蛋白短
暂激活,其后迅速失活,KRAS激活/失活效应是
受控的。
而KRAS基因突变时,可以导致EGFR信号
通路持续激活,加速肿瘤细胞增殖。
KRAS基因突变96%发生在第2号外显子的
12、13号密码子。
20%非小细胞肺癌、30-35%大肠癌患者中存
在KRAS基因突变。
结直肠癌《肿瘤学临床实践指南—2013年第3版》指出,肿瘤KRAS 基因的第12 号和13 号密码子突变后对EGFR 抑制剂(如西妥昔单抗、帕尼单抗)治疗均不敏感。
因此专家组强烈推荐:
(1)所有转移性结直肠癌患者(原发灶或转移灶组织均可)均应进行KRAS 基因型检测。(2)强调凡涉及西妥昔单抗或帕尼单抗治疗时均应仅限于KRAS 基因野生型。
本产品用于定性检测石蜡包埋大肠癌病理组织切片DNA中K-ras基因突变情况,其中包括K-ras基因第2外显子12、13位密码子7种体细胞突变。
获国家医疗器械注册证书:国械注准20143402142;
B-raf基因V600E突变检测试剂盒(PCR-荧光探针法)
突变。89%的BRAF突变集中在BRAF蛋白的P-环/活
化片段。而V600E是最常见的(90%),与临床联系
最为密切的BRAF突变类型。
部分没有K-ras基因突变的患者也会对EGFR
靶向药物产生耐药性,研究证明这主要是由于
K-ras下游的B-raf基因V600E突变造成的。
B-raf基因突变在多种恶性肿瘤细胞中都有报道,除了结直肠癌外,B-raf在恶性黑色素瘤、肺癌、甲状腺癌、卵巢癌等均存在不同比例的突变。检测B-raf基因突变可用于指导
EGFR-TKI的靶向用药。
结直肠癌《肿瘤学临床实践指南—2013年第3版》建议对KRAS 野生型的患者进行检测BRAF 分型。
获国家医疗器械注册证书:国食药监械(准)字2013第3402096号;
基因突变的检测方法
基因突变的检测方法 基因突变的研已成为当今生命科学研究的热点之一,检测方法也随之迅速发展。人类细胞癌基因的突变类型已如上所述,对于基因突变的检测,1985以前,利用Southern印迹法,可以筛选出基因的缺失、插入和移码重组等突变形式。对于用该法法不能检测的突变,只能应用复杂费时的DNA序列测定分析法。多聚酶链反应(polymerase chain reaction,PCR)技术是突变研究中的最重大进展,使基因突变检测技术有了长足的发展,目前几乎所有的基因突变检测的分子诊断技术都是建立于PCR的基础之上,并且由PCR衍生出的新方法不断出现,目前已达二十余种,自动化程度也愈来愈高,分析时间大大缩短,分析结果的准确性也有很大很提高。其中包括单链构象多态性(single-strand comformational polymorphism,SSCP)和异源双链分析法(heteroduplex analysis,HA)。下面分别介绍几种PCR衍生技术及经典突变检测方法,可根据检测目的和实验室条件选择时参考。 PCR-SSCP法 PCR-SSCP法是在非这性聚丙烯酰胺凝胶上,短的单链DNA和RNA分子依其大街基序列不同而形成不同构象,一个碱基的改变将影响其构象而导致其在凝胶上的移动速度改变。其基本原理为单链DNA在中性条件下会形成二级结构,这种二级结构依赖于其碱基组成,即使一个碱基的不同,也会形成不同的二级结构而出刺同的迁移率。由于该法简单快速,因而被广泛用于未知基因突变的检测。用PCR-SSCP法检测小于200bp的PCR产物时,突变检出率可达70%-95%,片段大于400bp时,检出率仅为50%左右,该法可能会存在1%的假阳性率。应用PCR-SSCP法应注意电泳的最佳条件,一般突变类型对检测的灵敏度无大的影响,同时该法不能测定突变的准确位点,还需通过序列分析来确定。Sarkar等认为对于大于200bp的片段,用其RNA分子来做SSCP会提高其录敏度。应用PCR-SSCP检测点突变已见报道于人类大部分的肿瘤组织或细胞,如乳腺癌、食管癌、肺癌、胃癌、肝癌、胰腺癌等。检测的基因包括多种癌基因及抑癌基因,也是检测抑癌基因p53突变最常用的方法,仅检测第5-8外显子即可发现85%以上的p53基因突变。由于该法简便快速,特别适合大样本基因突变研究的筛选工作。 异源双链分析法(HA) HA法直接在变性凝胶上分离杂交的突变型一野生型DNA双链。由于突变和野生型DNA形成的异源杂合双链DNA在其错配处会形成一突起,在非变性凝胶中电泳时,会产生与相应的同源双DNA不同的迁移率。该法与SSCP相似,所不同的是SSCP分离的是单链DNA,HA法分离的是双链DNA,也只适合于小片段的分析。但HA对一些不能用SSCP 检出的突变有互补作用,两者结合使用,可使突变检出率提高到近100%。
(3)理解基因突变的检测方法
第十章基因突变 一、教学目的与要求: (1)了解基因突变的类型和性质、特征 (2)掌握基因突变分子机理和诱变因素的作用方式 (3)理解基因突变的检测方法 (4) 掌握基因突变的修复途径 二、教学重点、难点、疑点: 1.突变的概念、类型和性质 2.诱发突变的分子基础 3.诱发突变与人类癌症 4.生物体基因突变的修复机制 5.果蝇基因突变的检出 6.植物基因突变的检出 7.人类基因突变的检出 [解决方法] (1)通过出示基因结构变化的示意图,加深学生对基因突变内涵的理解。 (2)课堂教学中不断提出问题,让学生通过概念的运用达到巩固概念和知识迁移的目的。 2.教学难点及解决办法 基因突变的原因。 [解决办法] 对人类镰刀型细胞贫血症病因结合图解进行分析,使学生真正明白基因突变的原因——DNA复制过程也可能发生差错,基因中个别碱基的变化,就会造成性状改变。 3.教学疑点及解决办法 为什么说基因突变是变异的主要来源? [解决办法]讲明基因突变与基因重组的区别,联系实际举例。 三、教学方法设计: 四、教具或教学手段:多媒体课件 五、教学过程与板书设计:
第一节基因突变的概念和特征 一、基因突变的概念及类别 1、基因突变:指在染色体上一定位点基因内部的化学变化引起的突变基因突变:指染色体上一定位点基因内部的化学变化引起的突变 2、类别 隐性突变:A a 显性突变:a A 自发突变—外界环境条件的自然作用或生物体内的生理生化变化而产生的突变 诱发突变—在专门诱变因素影响引起的突变,为“诱发突变” 形态突变型—可见突变:指造成外形改变的突变型 至死突变型—能造成个体死亡或生命力明显下降的突变型 条件突变型—在一定条件下有致死效应 3.一般特征 ①突变的频率:指生物体在每一世代中发生突变的机率,或者在一定时 间内突变可能发生的次数。 高等植物 10-5— 10-8 细菌和噬菌体 10-4—10-10范围大、突变频率比动植物高 例如:氨基酸过程中三种疾病是由三种基因突变导致酶发生变化引起的,有一定的突变频率 苯丙氨酸羟化酶缺乏导致苯丙酮尿症;尿黑尿酸氧化酶缺乏会产生尿黑酸尿症;酪氨酸酶缺乏导致白化病 苯丙氨酸羟化酶 苯丙酮酸苯丙氨酸酪氨酸 积累尿黑尿酸氧化酶 酪氨酸酶 苯丙酮尿症尿黑酸黑色素
基因突变的检测方法(完整资料).doc
此文档下载后即可编辑 基因突变的检测方法 基因突变的检测方法 基因突变的研已成为当今生命科学研究的热点之一,检测方法也随之迅速发展。人类细胞癌基因的突变类型已如上所述,对于基因突变的检测,1985以前,利用Southern印迹法,可以筛选出基因的缺失、插入和移码重组等突变形式。对于用该法法不能检测的突变,只能应用复杂费时的DNA序列测定分析法。多聚酶链反应(polymerase chain reaction,PCR)技术是突变研究中的最重大进展,使基因突变检测技术有了长足的发展,目前几乎所有的基因突变检测的分子诊断技术都是建立于PCR的基础之上,并且 由PCR衍生出的新方法不断出现,目前已达二十余种,自动化 程度也愈来愈高,分析时间大大缩短,分析结果的准确性也有很大很提高。其中包括单链构象多态性(single-strand comformational polymorphism,SSCP)和异源双链分析法(heteroduplex analysis,HA)。下面分别介绍几种PCR衍生技术及经典突变检测方法,可根据 检测目的和实验室条件选择时参考。 PCR-SSCP法PCR-SSCP法是在非这性聚丙烯酰胺凝胶上,短的单链DNA和RNA分子依其大街基序列不同而形成不同构象, 一个碱基的改变将影响其构象而导致其在凝胶上的移动速度改变。其基本原理为单链DNA在中性条件下会形成二级结构,这种二级结构依赖于其碱基组成,即使一个碱基的不同,也会形成不同的二级结构而出刺同的迁移率。由于该法简单快速,因而被广泛用于未知基因突变的检测。用PCR-SSCP法检测小于200bp 的PCR产物时,突变检出率可达70%-95%,片段大于400bp时,检出率仅为50%左右,该法可能会存在1%的假阳性率。应用PCR-SSCP法应注意电泳的最佳条件,一般突变类型对检测的灵敏度无大的影响,同时该法不能测定突变的准确位点,还需通过
基因突变检测多少钱检测方法是什么
基因突变检测多少钱检测方法是什么 一代测序法(Sanger法): 科学家Sanger,于1977年建立,他本人也因此而获得了诺贝尔奖。该技术至今已用 三十多年,现在已相当成熟完善。人类基因组计划的测序工作就是使用该项技术完成的, 现在***的仪器是美国ABI公司的***3730型全自动遗传分析仪,是经过国际和国家认证的仪器,可重复性达到100%,是亲子鉴定和法医鉴定的专用仪器。该方法是目前基因检测的国际金标准。缺点是通量小,适合少量样本,可进行个性化位点检测,成本极高,比芯片 或高通量检测高100倍。 Taqman法: 准确性好,适合于大量样本、少量位点,价格贵,缺点是不能读出序列,不太直观。 质谱法: 准确性较好,缺点只能读出质量数据,不能读出序列,对于缺失和插入突变无法读出,但这种突变更加可怕,适合于大量样本、多位点(最多能检测25个位点),所以可能会 出现少量假阳性和假阴性。 二代基因检测芯片法: 适合于超多位点,大量样品检测和科研参考,每个样本做几百个位点和做几千个位点 的检测成本,相差无几,最大优点是成本低廉,一个位点的价格只相当于一代测序价格的1%,缺点是出来的大量数据,可信度不高。 我们都知道“是药三分毒”,癌症患者的过度治疗会造成患者的器脏损伤,甚至化疗 整个过程费钱费力却“不讨好”,所以进行在进行治疗之前先进行基因测序检测,会让靶 向药物治疗事倍功半。 肺癌的靶向药基因检测,现在很多公司都可以做,医院基本上也是外送公司做,看你 检测几个几个基因,一般不会超过7200,一般检测就是EGFR,融合基因ALK,ROS1,C-MET,中源协和基因检测。 一般的,基因检测是通过血液、其他体液、或细胞对DNA进行检测的技术。 基因检测可以诊断疾病,也可以用于疾病风险的预测。疾病诊断是用基因检测技术检 测引起遗传性疾病的突变基因。目前应用最广泛的基因检测是新生儿遗传性疾病的检测、 遗传疾病的诊断和某些常见病的辅助诊断。目前有1000多种遗传性疾病可以通过基因检 测技术做出诊断。
基因突变的鉴定
基因突变的鉴定 (2010-07-05 17:37:50) 转载▼ 标签: 杂谈 一.植物形态突变的鉴定 经人工诱发或自然发生的变异是否属于真实的基因突变,是显性突变还是隐性突变,突变频率的高低等,都应进行鉴定。 1.真实遗传变异的鉴定 变异有可遗传的变异,有不可遗传的变异。基因本身发生化学性质的变化而引起的变异是可以遗传的,因环境条件而导致的表现型变异是不遗传的。所以,在诱变处理材料的后代中一旦发现与原始亲本不同的变异体,首先要鉴定它是否真实遗传。例如,在农作物诱变育种过程中,某种高杆植物经理化因素处理后,在其后代中发现个别矮杆植株,这种变异究竟是基因突变引起的呢?还是由环境条件引起的呢?二者如何鉴别呢? 把变异体与原来的亲本种植在土壤条件和栽培条件均匀一致的环境下,若变异体与原始亲本的表现大体相似,即原来的变异消失了,说明它不是遗传的变异;反之,若变异体与原始亲本不同,仍然表现为矮杆,说明它是基因突变的结果。 2.如何鉴别显性突变和隐性突变 利用杂交试验的方法,可以区分显性突变还是隐性突变。以上例而言,让矮杆突变体植株与原始亲本杂交,若F1表现高杆,F2中既有高杆,也有矮杆植株,说明矮杆突变是隐性突变。若是显性突变情况又如何呢?F1表现为矮杆,F2中矮杆:高杆为3:1。 3.利用花粉直感现象估算配子的突变率 为了测定玉米子粒非甜籽变为甜粒(Su→su)的基因突变频率,以甜粒玉米纯合体作母本,用经诱变处理过的非甜粒纯合体的花粉授粉。 susu×SuSu 在正常情况下,非甜(Su)对甜(su)为显性,授粉后的果穗应该完全是非甜粒种子,假如在果穗上发现甜粒种子,就可以认为是Su花粉经诱发处理以后发生了Su→su突变,并可计算出突变频率。
P53基因突变检测方法
2、试剂和耗材) GIAGEN,德国QIAamp?DNA Blood Mini Kit ()Platiinim?Taq DNA Polymerase High Fidelity (Invitrogen, 11304-102 Nuclease-Free Water (Promega,P 1195) d NTP Mix (Promega,P 151B) PCR引物:北京博迈德科技有限公司合成 DL10000 DNA Marker(TAKARA,大连宝生物)DNA分子定量标准:技术Bioer 产物回收纯化试剂盒(BioSpiii Gel Extraction kit,日本PCR有限公司)公司) Axygen, 200-1000 ul 吸头(美国110.5?10 u、2?20 u k 20-200 □、管EP、 仪.器3 ;Taimon1600R凝胶成像系统分析仪(上海天龙公司)Eppendorf 5417R 高速冷冻离心机(Eppendorf公司,德国)公司,美国)Allegra 6R离心机(Beckman-Coulter应涡旋混合器(北京北德科学仪器厂)MVS-1公司,德国) 1000 u 150 口1、200 ul、(Eppendorf^ 口1 移液器、10 U 1、NEWAIR 公司,美国)1【级生物安全柜NU425-400E (拓速冷冻离心机(BECKMAN COULTER 公司,美国)X-15R 公司德国)仪(Eppendorf Eppendorf Masteicycter PCR 公司,美国)(Bio-Rad电泳仪:Universal 024BR电热恒温水浴器(北京来亨科贸有限责任公司)240全自动凝胶成像系统(中国)凝胶成像分析系统:Tocan 测序仪:GenomeLab CEQ/GeXP (BECKMAN COULTER 公司,美国)20 u k 200 ul和1000 ul加样器(吉尔森公司,法国)旋涡震荡器(Scientific Industries公司,美国) 二、实验方法 1、样品采集,送检和保存 乙二胺四乙酸(EDTA) -3K抗凝管采集HIV和HEV合并感染者外周静脉血,于24h内测定CD4+T淋巴细胞计?数,抗凝血经常规离心分离全血中间层,分装后-80°C冻存用于P53基因变异的测定。 2、血浆样本DNA的提取 取200 P1全血中间层于1.5ml无菌EP管中,加入20 口1蛋白酶K;再加入200 ul AL缓冲液,涡旋振荡15秒,56°C孵育10分钟;瞬时离心EP管,加入200 u 1 无
肿瘤基因突变检测
肿瘤基因突变检测 癌症是一类难以预防的疾病,中晚期癌症治愈的可能性又很小,而早期癌症的治愈率可达65%以上,有些肿瘤可达90%以上,因此,战胜癌症的关键是早期发现癌症。由于癌症早期常无特殊症状,甚至毫无症状,故癌症的早期发现、早期诊断主要是通过定期健康体检和人群筛查完成。目前筛查癌症的方法主要是通过化验血肿瘤指标及B超、CT、MRI、PET-CT 等检查,但这些方法的敏感性和特异性均不高,发现有异常时往往已是中晚期。 17种常见高发肿瘤,包括乳腺癌(breast cancer)、结肠癌(colorectalcancer)、子宫癌(endometrial cancer)、脑胶质瘤(glioma)、白血病(leukemia)、肺癌(lungcancer)、淋巴癌(lymphoma)、成神经管细胞瘤(medulloblastoma)、黑色素癌(melanoma)、间皮瘤(mesothelioma) 、多性骨髓瘤(multiple myeloma) 、卵巢癌(ovarian cancer)、胰腺癌(pancreatic cancer) 、真性红细胞增多(polycythemia vera) 、前列腺癌(prostatecancer) 、肾细胞癌(renal cell cancer)和恶性内瘤(sarcoma),其发病机制涉及与多种肿瘤发生共同相关的肿瘤易感基因群介导的分子改变,参与了肿瘤发生的早期分子事件。系统寻找和探讨它们在肿瘤发生发展过程中的遗传学变异,对阐明肿瘤早期发生机制及寻找肿瘤早期预警、早期诊断和早期治疗的分子靶标都具有重要的现实意义。利用高通量分子测序技术平台,可同时开展多个肿瘤基因突变检测项目,如EGFR、K-RAS 、N-RAS、B-RAF、PI3K 、p53、p16、BRCA1、
基因突变的检测方法
基因突变的检测方法
基因突变的检测方法 基因突变的研已成为当今生命科学研究的热点之一,检测方法也随之迅速发展。人类细胞癌基因的突变类型已如上所述,对于基因突变的检测,1985以前,利用Southern印迹法,可以筛选出基因的缺失、插入和移码重组等突变形式。对于用该法法不能检测的突变,只能应用复杂费时的DNA序列测定分析法。多聚酶链反应(polymerase chain reaction,PCR)技术是突变研究中的最重大进展,使基因突变检测技术有了长足的发展,目前几乎所有的基因突变检测的分子诊断技术都是建立于PCR的基础之上,并且由PCR衍生出的新方法不断出现,目前已达二十余种,自动化程度也愈来愈高,分析时间大大缩短,分析结果的准确性也有很大很提高。其中包括单链构象多态性(single-strand comformational polymorphism,SSCP)和异源双链分析法(heteroduplex analysis,HA)。下面分别介绍几种PCR衍生技术及经典突变检测方法,可根据检测目的和实验室条件选择时参考。 PCR-SSCP法 PCR-SSCP法是在非这性聚丙烯酰胺凝胶上,短的单链DNA和RNA分子依其大街基序列不同而形成不同构象,一个碱基的改变将影响其构象而导致其在凝胶上的移动速度改变。其基本原理为单链DNA在中性条件下会形成二级结构,这种二级结构依赖于其碱基组成,即使一个碱基的不同,也会形成不同的二级结构而出刺同的迁移率。由于该法简单快速,因而被广泛用于未知基因突变的检测。用PCR-SSCP法检测小于200bp的PCR产物时,突变检出率可达70%-95%,片段大于400bp时,检出率仅为50%左右,该法可能会存在1%的假阳性率。应用PCR-SSCP法应注意电泳的最佳条件,一般突变类型对检测的灵敏度无大的影响,同时该法不能测定突变的准确位点,还需通过序列分析来确定。Sarkar等认为对于大于200bp的片段,用其RNA分子来做SSCP会提高其录敏度。应用PCR-SSCP检测点突变已见报道于人类大部分的肿瘤组织或细胞,如乳腺癌、食管癌、肺癌、胃癌、肝癌、胰腺癌等。检测的基因包括多种癌基因及抑癌基因,也是检测抑癌基因p53突变最常用的方法,仅检测第5-8外显子即可发现85%以上的p53基因突变。由于该法简便快速,特别适合大样本基因突变研究的筛选工作。 异源双链分析法(HA) HA法直接在变性凝胶上分离杂交的突变型一野生型DNA双链。由于突变和野生型DNA形成的异源杂合双链DNA在其错配处会形成一突起,在非变性凝胶中电泳时,会产生与相应的同源双DNA不同的迁移率。该法与SSCP相似,所不同的是SSCP分离的是单链DNA,HA法分离的是双链DNA,也只适合于小片段的分析。但HA对一些不能用SSCP 检出的突变有互补作用,两者结合使用,可使突变检出率提高到近100%。 突变体富集PCR法(mutant-enriched PCR)本法的基本原理是利用ras基因家族某个密码子部位存在已知的限制性内切酶位点,如K-ras基因第12密码子的BstNI位点,第13密古巴子有BgⅠⅡ位点。用链续二次的巢式PCR来扩增包括K-ras第12、13密码子的DNA片段,在两次扩增反应之间用相应的内切酶消化扩增的DNA片段,野生型因被酶切而不能进入第二次PCR扩增,而突变型则能完整进入第二次PCR扩增并得到产物的富集。 变性梯度凝胶电泳法(denaturing gradinent electrophoresis,DGGE) DGGE法分析PCR 产物,如果突变发生在最先解链的DNA区域,检出率可达100%,检测片段可达1kb,最适围为100bp-500bp。基本原理基于当双链DNA在变性梯度凝胶中进行到与DNA变性湿度一致的凝胶位置时,DNA发生部分解链,电泳适移率下降,当解链的DNA链中有一个碱基改变时,会在不同的时间发生解链,因影响电泳速度变化的程
KRAS基因突变的检测及其临床意义
KRAS基因突变的检测及其临床意义 RAS基因家族由KRAS、HRAS 和NRAS组成,基因家族各成员间同源性可达85%。RAS 基因编码p21蛋白,分子量为21KD,位于细胞膜的内表面,具有GTP酶活性,参于传导细胞增殖信号的调控系统。其激活状态为GTP结合状态,失活状态为GDP结合状态,其转变为活性致癌基因的主要部位是第12、13 和61 密码子的突变,其中以第12 密码子点突变最常见。 RAS基因是人体肿瘤中常见的致癌基因,该基因的体细胞突变常见于多种恶性肿瘤,在肺癌患者中的突变率为15%-30%,在结直肠癌患者中为20%-50%。作为EGFR信号通路下游最重要的的效应因子,KRAS在肿瘤信号转导中发挥重要作用。对KRAS基因突变的检测,可以为肿瘤患者的个体化治疗提供更确切的依据。 西妥昔单抗和帕尼单抗都是特异性针对人类EGFR胞外区的单克隆抗体。美国FDA批准该药单药用于治疗难治性结肠癌,及在放疗基础上治疗进展性头颈部癌。已知EGFR信号途径下游的基因突变则会使患者对西妥昔单抗和帕尼单抗治疗产生耐药性。2009年7月15日,美国FDA批准了对帕尼单抗和西妥昔单抗的说明书的修改,在西妥昔单抗和帕尼单抗说明书的“适应证和用法”部分明确指出,KRAS基因第12或13密码子突变的患者接受治疗无生存获益;不推荐这两种表皮生长因子受体(EGFR)抗体用于KRAS基因突变的转移性结直肠癌(mCRC)患者治疗。根据这一提示,临床医生可以将KRAS基因突变的患者排除在接受抗EGFR单抗治疗之外,重新安排其接受其他药物替代治疗,避免对不能获益的患者进行不必要的治疗。 此外,研究表明,K-ras基因突变状态与非小细胞肺癌对吉非替尼、厄罗替尼等靶向治疗药物的原发性耐药有关,直肠癌患者中K-ras的突变对西妥昔单抗等药物的耐药性有关。美国国家癌症综合网络(NCCN) 2011年版临床治疗指南指出:K-ras基因突变是EGFR酪氨酸激酶抑制剂疗效的预测指标,肿瘤患者在接受EGFR靶向药物治疗前必须进行K-ras基因突变检测,以帮助决定患者是否接受EGFR酪氨酸激酶抑制剂类药物(易瑞沙/特罗凯/埃克替尼等)治疗。携带K-ras永久激活性突变的患者本检验所不建议使用EGFR酪氨酸激酶抑制剂类药物(易瑞沙/特罗凯/埃克替尼等),建议使用靶向的Ras抑制剂药物治疗。 作为RAS/FTI(法尼基转移酶抑制剂)的安卓健通过抑制Ras 的活性,进而影响其下游讯息传递因子,包括抑制PI3K 的表现量与降低Akt 的磷酸化程度;以及活化AMPK促使TSC1/TSC2 结合更紧密,进而大大的降低mTORC1 的活性,开启癌细胞的自噬作用机制;安卓健同时会活化MEK1/ ERK1/2 的路径,促进癌细胞的自噬作用机制;另外,安卓健会使线粒体不稳定,降低Bcl-2、Bcl-XL 与MCl-1 的蛋白质量,使癌细胞程序性凋亡。由于安卓健能同时诱导癌细胞启动自噬作用与程序性凋亡的机制,而实验室的细胞毒性测试亦指出安卓健对多数的癌细胞(脑癌、淋巴癌、血癌、肺腺癌、乳癌、肝癌、胰脏癌、胃癌、直肠癌、前列腺癌与膀胱癌等) 都有药用效果。 上海佳辰投资发展有限公司联合上海张江转化医学研发中心研发K-ras基因突变检测,详细如下: 检测内容:K-ras基因突变 检测方法:ARMS法 主要材料:ABI荧光定量试剂盒 主要设备:ABI 7500荧光定量PCR仪 检测项目和样本类型:
基因突变的检测方法
基因突变的检测方法 基因突变的检测方法 基因突变的研已成为当今生命科学研究的热点之一,检测方法也随之迅速发展。人类细胞癌基因的突变类型已如上所述,对于基因突变的检测,1985以前,利用Southern印迹法,可以筛选出基因的缺失、插入和移码重组等突变形式。对于用该法法不能检测的突变,只能应用复杂费时的DNA序列测定分析法。多聚酶链反应(polymerase chain reaction,PCR)技术是突变研究中的最重大进展,使基因突变检测技术有了长足的发展,目前几乎所有的基因突变检测的分子诊断技术都是建立于PCR的基础之上,并且由PCR衍生出的新方法不断出现,目前已达二十余种,自动化程度也愈来愈高,分析时间大大缩短,分析结果的准确性也有很大很提高。其中包括单链构象多态性(single-strand comformational polymorphism,SSCP)和异源双链分析法(heteroduplex analysis,HA)。下面分别介绍几种PCR衍生技术及经典突变检测方法,可根据检测目的和实验室条件选择时参考。 PCR-SSCP法 PCR-SSCP法是在非这性聚丙烯酰胺凝胶上,短的单链DNA和RNA分子依其大街基序列不同而形成不同构象,一个碱基的改变将影响其构象而导致其在凝胶上的移动速度改变。其基本原理为单链DNA在中性条件下会形成二级结构,这种二级结构依赖于其碱基组成,即使一个碱基的不同,也会形成不同的二级结构而出刺同的迁移率。由于该法简单快速,因而被广泛用于未知基因突变的检测。用PCR-SSCP法检测小于200bp的PCR产物时,突变检出率可达70%-95%,片段大于400bp时,检出率仅为50%左右,该法可能会存在1%的假阳性率。应用PCR-SSCP法应注意电泳的最佳条件,一般突变类型对检测的灵敏度无大的影响,同时该法不能测定突变的准确位点,还需通过序列分析来确定。Sarkar等认为对于大于200bp的片段,用其RNA分子来做SSCP会提高其录敏度。应用PCR-SSCP检测点突变已见报道于人类大部分的肿瘤组织或细胞,如乳腺癌、食管癌、肺癌、胃癌、肝癌、胰腺癌等。检测的基因包括多种癌基因及抑癌基因,也是检测抑癌基因p53突变最常用的方法,仅检测第5-8外显子即可发现85%以上的p53基因突变。由于该法简便快速,特别适合大样本基因突变研究的筛选工作。 异源双链分析法(HA) HA法直接在变性凝胶上分离杂交的突变型一野生型DNA双链。由于突变和野生型DNA形成的异源杂合双链DNA在其错配处会形成一突起,在非变性凝胶中电泳时,会产生与相应的同源双DNA不同的迁移率。该法与SSCP相似,所不同的是SSCP分离的是单链DNA,HA法分离的是双链DNA,也只适合于小片段的分析。但HA对一些不能用SSCP 检出的突变有互补作用,两者结合使用,可使突变检出率提高到近100%。 突变体富集PCR法(mutant-enriched PCR)本法的基本原理是利用ras基因家族某个密码子部位存在已知的限制性内切酶位点,如K-ras基因第12密码子的BstNI位点,第13密古巴子有BgⅠⅡ位点。用链续二次的巢式PCR来扩增包括K-ras第12、13密码子的DNA片段,在两次扩增反应之间用相应的内切酶消化扩增的DNA片段,野生型因被酶切而不能进入第二次PCR扩增,而突变型则能完整进入第二次PCR扩增并得到产物的富集。 变性梯度凝胶电泳法(denaturing gradinent electrophoresis,DGGE) DGGE法分析PCR 产物,如果突变发生在最先解链的DNA区域,检出率可达100%,检测片段可达1kb,最适
preMiD基因突变检测技术原理和应用
preMiD?基因突变检测技术原理和临床应用简介: 原癌基因和抑癌基因的驱动突变(driver mutation)是肿瘤特有的标记。以PreGen-Plus?筛查大肠癌4基因突变的粪便筛查被FDA批准为标志,更多突变检测肿瘤的新技术和产品处于临床开发阶段。自主创新的preMid?技术可一次检测38个基因198突变点,覆盖包括胰腺癌、肺癌、乳腺癌和胃癌等14种肿瘤,国际上第一次实现多突变的血浆检测。临床验证preMid?技术可实现癌症(超)早期,疑似患者的辅助诊断和术后复发的实时监控,总体准确率可达80%。 正文: 原理: 1. 突变——肿瘤特异标志。 癌症是基因突变累积的结果。“所有癌症的发生,都源自脱氧核糖核酸(DNA)序列的异常。”国际癌症基因组联合计划参与单位之一、英国剑桥大学桑格研究所首席科学家斯特拉顿教授指出。 癌变的形成要经过8--10年甚至更长,而这漫长的时间其实就是一个多基因突变并累积的过程(图1)。肿瘤相关基因可分为原癌基因和抑癌基因,其中起主要作用的突变属于驱动型突变(driver mutation)。当抑癌基因突变失去抑制癌症作用,或原癌基因突变激活,就会诱发癌症。正常细胞在向癌细胞转化的过程中,发生多种不同原癌基因和抑癌基因突变。 图1 肿瘤是基因突变的结果 相比临床检测中常规使用的肿瘤蛋白血清标志物,突变无疑是更特异的肿瘤标记。 2009年12月,桑格研究所在《自然》杂志上刊文宣布,他们率先在世界上破译肺癌、
皮肤癌和乳腺癌等5种肿瘤全部基因密码,绘制出相应的肿瘤基因突变图谱(表1)。 表1 5种癌症基因突变相关数据 Nature.2010.8;466(7308):869-873. 2.循环DNA是检测突变的重要来源 肿瘤起源DNA存在于血液循环DNA中。循环DNA存在于血清或血浆、滑膜液和脑脊液等体液中的非细胞里面存在的片段,亦称细胞游离DNA(cell-free DNA,cfDNA)。 早在1947年Mandel和Metais就发现循环核酸;30年后Leon等研究表明肿瘤患者外肿瘤患者cfDNA水平大大高于正常人1989年Stroun等发现血液游离DNA具有肿瘤细胞DNA的一些特征;5年后研究者在肿瘤患者的血浆和血清中检测到癌基因突变,与原发肿瘤一致。 图2 肿瘤cfDNA来源示意图 肿瘤细胞cfDNA如何进入血液,目前认为:1) 循环肿瘤细胞或微转移灶的裂解;2) 肿瘤细胞的凋亡;3) 肿瘤细胞坏死;4) 肿瘤细胞自发性释放。 cfDNA突变检测具有特异、实时且无创等突出特点,无疑是肿瘤早期筛查、辅助诊断、预后判断及跟踪复发等有效靶标。
基因变异的研究方法与进展
基因变异广义上说就是指基因结构变化从而产生了可遗传的变异。也就是说DNA水平上的突变造成的基因改变。而这一突变过程可能有很多原因,有自发性的,比如DNA配对过程中的装配错误,也有外源性的诱导因素,如物理,化学,生物因素等造成染色体结构改变或者基因结构的直接变化。 突变的形式多种多样,常见的有:点突变,即一个或多个核苷酸发生了改变;框内突变指的是3个或是的倍数的碱基缺失或插入导致的突变,使基因丢失或增加1个或几个氨基酸;除此之外,还存在着DNA大片段的缺失,通常是指几百个bp至几十个kb的碱基缺失或复制。 这其中,最常见的莫过于点突变,他是指一个或者几个核苷酸的缺失或改变,通常会形成三种类型,第一种是同义突变,即碱基替换后,虽然密码子发生改变,但编码氨基酸没有改变(遗传密码的兼并性),亦称静止突变,第二种是错义突变,指的是碱基替换,密码子发生改变后,编码氨基酸亦发生改变,编码另一个氨基酸,第三种是无义突变,即碱基替换后,使编码氨基酸的密码子变成一个终止密码子。 基于上述的变化,常见的基因变异研究方法有如下几种 一、筛选性方法 有人将这类方法分为2类,根据电泳性质不同及其他包括化学修饰法等 1 RNase 法 该法是一种最早提出的检测DNA突变的方法口。其原理是RNase可以识别RNA:DNA或RNA:RNA杂交链中错误配对的碱基并将其切断。经聚丙烯酰胺凝胶电泳将正常链及被切断的含有突变点的链区分开来。杂交方法是将同位素或其它方法标记的正常野生型RNA 片段与相对应的待测DNA 片段混合,90"C
左右变性并在室温下复性形成杂交分子。当待测DNA 片段中存在碱基突变时,在该位点上二条链不能正常配对,便成为RNase的识别和切割位点 2 DGGE、CDGE、TGGE、TSGE法 梯度变性凝胶电泳(DGGE)原理是当双链DNA在梯度变性的聚丙烯酰胺凝胶中行进到与DNA变性温度(熔点温度)一致的凝胶变性浓度位臵时,DNA 发生解旋变性此时电泳速度迅速降低。而当解旋的DNA链中有一个碱基突变时,将会影响其电泳速度变化的程度,从而将正常与突变的DNA区别开。 CDGE(constant denatural gel electrophoresis)法通过预实验或理论计算预先精确确定待测DNA片段的熔点温度后采用单一变性浓度凝胶电泳,简化了DGGE 法的操作 类似于CDGE法,TSGE (temperature sweep gel electropnoresis)法则取消了温度梯度而代之以单一温度 这类方法的优点是:(1)检出率高,~100 (2)可用于分析突变——正常DNA 混合样品;(3)可以回收分离出的DNA 片段;(4)可以直接测定未经扩增的DNA 。这类方法的缺点也很多,如(1)分析片段较小,<500 bp;(2)需要制备昂贵的GC clamp(3)需要事先经过复杂的计算机处理计算熔点温度或预试验确定变性条件; (4)位于高度富含GC的片段中的突变可能漏检。鉴于以上不利因素,DGGE等一类方法有逐渐被SSCP(单链构象多态性)法取代的倾向。尽管如此,这类方法一经建立,应用十分方便,适于大规模样品分析 3 SSCP法 单链构象多态性(single strand conlotraation polymorphism,)是在非变性聚丙烯酰胺凝胶上,短的单链DNA或RNA分子依其碱基序列不同而形成不同构象,
P53基因突变检测方法
2、试剂和耗材 QIAamp?DNA Blood Mini Kit(GIAGEN,德国) Platinum?Taq DNA Polymerase High Fidelity(Invitrogen,11304-102) Nuclease-Free Water(Promega,P1195) d NTP Mix(Promega,P151B) PCR引物:北京博迈德科技有限公司合成 DNA分子定量标准:DL10000 DNA Marker(TAKARA,大连宝生物) PCR产物回收纯化试剂盒(BioSpin GelExtraction kit,日本Bioer技术有限公司) 0.5~10 μl、2~20 μl、20~200 μl、200~1000 μl吸头(美国Axygen,公司) EP管 3、仪器 Tannon1600R凝胶成像系统分析仪(上海天龙公司); Eppendorf 5417R高速冷冻离心机(Eppendorf公司,德国) Allegra 6R离心机(Beckman-Coulter公司,美国) MVS-1型涡旋混合器(北京北德科学仪器厂) 移液器2 μl、10 μl、50 μl、200 μl、1000μl(Eppendorf公司,德国)Ⅱ级生物安全柜NU425-400E(NEWAIR公司,美国) X-15R高速冷冻离心机(BECKMAN COULTER公司,美国) Eppendorf Mastercycter PCR仪(Eppendorf 公司德国) 电泳仪:Universal 024BR(Bio-Rad公司,美国) 电热恒温水浴器(北京来亨科贸有限责任公司) 凝胶成像分析系统:Tocan240全自动凝胶成像系统(中国) 测序仪:GenomeLab CEQ/GeXP(BECKMAN COULTER公司,美国)20μl、200μl和1000μl加样器(吉尔森公司,法国) 旋涡震荡器(Scientific Industries公司,美国) 二、实验方法 1、样品采集,送检和保存
1_肿瘤相关突变基因检测试剂(高通量测序法)性能评价通用注册技术审查指导原则
附件1 肿瘤相关突变基因检测试剂(高通量测序法)性能评价通用注册技术审查指导原则 本指导原则旨在指导注册申请人对肿瘤相关基因检测试剂分析性能评价注册申报资料的准备及撰写,同时也为技术审评部门对注册申报资料的技术审评提供参考。 本指导原则是针对肿瘤相关基因检测试剂分析性能评价的一般要求,申请人应依据产品的具体特性确定其中内容是否适用,若不适用,需具体阐述理由及相应的科学依据,并依据产品的具体特性对注册申报资料的内容进行充实和细化。 本指导原则是对申请人和审查人员的指导性文件,但不包括注册审批所涉及的行政事项,亦不作为法规强制执行,如果有能够满足相关法规要求的其他方法,也可以采用,但需要详细阐明理由,并对其科学合理性进行验证,提供详细的研究资料和验证资料,相关人员应在遵循相关法规的前提下使用本指导原则。 本指导原则是在现行法规和标准体系以及当前认知水平下制定的,随着法规和标准的不断完善,以及科学技术的不断发展,本指导原则相关内容也将适时进行调整。 一、适用范围 本指导原则所述肿瘤相关基因检测试剂分析性能评价主要是指基于高通量测序(high-throughput sequencing)即下一代测 —1 —
序(next generation sequencing,NGS),又称为大规模平行测序(massively parallel sequencing,MPS),体外检测人体组织肿瘤细胞中的肿瘤相关基因变异。用于检测体细胞突变的NGS正在广泛用于肿瘤诊疗相关的分子检测,包括对特定基因的DNA/RNA进行测序,以寻找与肿瘤临床诊疗相关的基因变异。肿瘤基因突变类型包括点突变、插入、缺失、基因重排、拷贝数异常等广义的基因突变。 基于NGS测序原理的体外诊断(In Vitro Diagnosis,IVD)检测可能包括以下步骤:样本收集、处理和保存、核酸提取及处理、文库制备、测序和碱基识别、序列比对、变异识别和过滤、变异注释和解读以及检测报告的生成。同时,某些产品还可能会包括软件部分,但上述相关步骤并不一定被全部包括,应根据产品的具体设计流程来进行判断。对于每个检测步骤,申请人需要结合产品设计和临床意义来建立特定的可接受的质量评价指标和合格判断标准。此外,为满足产品特定预期用途,申请人需通过科学和适当的检测性能研究来确定适用的试剂、消耗品、仪器和软件。基于上述考虑因素,NGS检测产品的设计和工作流程中的任何差异均可能导致结果的不同,因此申请人需要清楚地描述相关检测性能指标。 分析性能评价的初衷在于提出产品性能有效性、安全性相关问题的假设,然后通过研究进行确认。NGS在测序通量及发现未知基因变异方面具有优势,但是在NGS技术应用需求及使用中存在包括相关临床样本收集处理、NGS检测内容、测序流程、—2 —
PCR技术用于基因突变的检测
PCR技术用于基因突变的检测 PCR 技术用于基因突变的检测 基因结构的异常可引起多种疾病的发生,它包括点突变、插入、缺失、重排、易位、基因扩增、基因结构多态性异常等形式。许多人类遗传性疾病源于基因的突变,基因突变分析是指对单个或低拷贝基因序列等位基因改变的鉴别,对诊断和理解遗传病有非常重要的价值。 聚合酶链反应 (PCR)是一种高特异和高灵敏性的基因分析手段, PCR 操作简便, 可以在几个小时内使 DNA 段的拷贝数扩增百万倍, 使对微量 DNA 的分析鉴定成为可能,伴随着分子生物学各领域的飞速发展, PCR 及其衍生技术以其快速准确在基因突变的检测中得到了广泛的应用。 虽然特异基因序列区段的直接测序是基因突变分析最可信和最精确的手段 , 但该方法繁琐、耗时、费力。 PCR 的应用则提供了一系列比直接测序更方便、快捷的方法。 PCR 在此领域也引起了巨大的革新。 基于 PCR 技术的常用基因突变检测方法有: 1、 PCR/ASO(allele specific oligonucleotide,ASO,等位基因特异性寡核苷酸 ) PCR/ASO探针诊断点突变,系在扩增 DNA 段后,直接与相应的寡核苷酸探针杂交,来明确诊断是否有突变以及突变是纯合子还是杂合子。 2、 PCR-SSCP(single strand conformation polymorphism, SSCP) PCR-SSCP 系 1989年由 Orita 首先报道的,它是一种基于单链 DNA 构象差别来检测点突变的方法。该方法操作简单、灵敏且特异性高,是目前检测点突变最简捷的方法。 3、 PCR-RFLP (restriction fragment length polymorphism , RFLP , 限制性片段长度多态性分析 )RFLP 分析与 PCR 反应相结合, 先用 PCR 来扩增待检的片段,再进行 RFLP 来检测那些发生在酶切位点的突变简化了 RFLP 的分析过程,并使该项技术得到了广泛的应用。 4、 DNA 序列测定法 (direct sequencing, DS)
人类Kras基因突变检测试剂盒说明书
人类Kras基因突变检测试剂盒说明书
人类K-ras基因突变检测试剂盒(PCR-熔解曲线法)说明书【产品名称】 通用名:人类K-ras基因突变检测试剂盒(PCR-熔解曲线法) 英文名:Diagnostic kit for Mutations of Human K- ras Gene (PCR-Melting Curve Analysis) 【包装规格】20测试/盒 【预期用途】 K-ras基因位于12号染色体短臂上,是重要的癌基因之一,编码一种21kD 的kras蛋白,参与细胞内的信号传递,主要包括PI3K/PTEN/AKT 和RAF/MEK/ERK信号转导途径,这些转导途径是当前肿瘤靶向药物研究的热点,靶向药物经过抑制这些途径发生药理作用。K-ras基因第12和13密码子发生突变,将导致kras蛋白变异并处于持续激活状态,使药物失效。。据中国《肿瘤学临床实践指南》,在一项包含101例肺腺癌亚型细支气管肺泡癌患者的回顾性研究中,所有患者均接受厄洛替尼单药一线治疗。K-ras突变者无一例缓解(0/18),而无K-ras突变者则有20例缓解(20/62,32%),差别有统计学意义(P <0.01)。因此,指南建议,非小细胞肺癌和结直肠癌患者
使用靶向药物前应进行K-ras基因突变状态的检测。 本试剂盒以人非小细胞肺癌、结直肠癌肿瘤组织切片提取的基因组DNA为检测样本,用于检测肿瘤组织K-ras基因第12,13密码子的12种体细胞突变(表1),提供突变状态的定性结果。为临床肿瘤靶向药物的个体化用药提供辅助诊断依据,本品适用于进入个体化靶向治疗疗程前的患者使用。 【检验原理】 本试剂盒基于实时PCR平台,结合了特异引物、荧光探针和熔解曲线技术,定性检测DNA样品中K-ras基因12,13密码子是否存在突变。用一对K-ras基因特异引物,该引物可扩增12种突变型和野生型的K-ras目标序列,利用标记了FAM荧光基团和淬灭基团的双标记探针一方面抑制野生型基因的扩增,提高突变基因的检测灵敏度,另一方面在扩增后用熔解曲线法实现对扩增产
(完整word版)基因突变及其他变异测试题 - 答案
基因突变、染色体变异、基因重组专项训练 一、选择题 1.生物在紫外线、电离辐射等影响下将可能发生突变。这种突变易发生在() A.细胞减数分裂的第一次分裂时 B.细胞减数分裂的第二次分裂时 C.细胞有丝分裂的间期 D.细胞有丝分裂的分裂期 [答案] C [解析]DNA分子中发生碱基对的替换、增添和缺失,而引起的基因结构的改变叫基因突变,发生于DNA 复制过程中,在细胞周期的间期完成DNA复制。 2.将普通小麦的子房壁细胞进行离体培养,得到的植株是() A.单倍体B.二倍体C.三倍体D.六倍体 [答案] D [解析]子房壁是体细胞,进行离体培养,得到的植株细胞中的染色体组与普通小麦的子房壁细胞相同,即该植株是六倍体。 3.三体综合征、并指、苯丙酮尿症依次属() ①单基因病中的显性遗传病②单基因病中的隐性遗传病③常染色体病④性染色体病 A.②①③B.④①②C.③①②D.③②① [答案] C 4.DNA分子经过诱变,某位点上的一个正常碱基(设为P)变成了尿嘧啶。该DNA连续复制两次,得到的4个子代DNA分子相应位点上的碱基对分别为U—A、A—T、G—C、C—G,推测“P”可能是() A.胸腺嘧淀B.腺嘌呤C.胸腺嘧啶或腺嘌呤D.胞嘧啶 [答案] D [解析]据半保留复制的特点,DNA分子经过两次复制后,突变锭形成的两个DNA分子中含有U—A,A—T 碱基对,而另一条正常,正常链形成的两个DNA分子中含有G—C、C—G碱基对,因此被替换的可能是G,也可能是C。 5.已知某小麦的基因型是AaBbCc,三对基因分别位于三对同源染色体上,利用其花药进行离体培养,获得N株小麦,其中基因型为aabbcc的个体约占() A.N/4 B.N/8 C.N/6 D.0 [答案] D [解析]基因型是AaBbCc的小麦,三对基因分别位于三对同源染色体上,通过减数分裂产生23种配子,利用其花药进行离体培养,获得N株单倍体小麦,基因型不可能为aabbcc。 6.当牛的卵原细胞进行DNA复制时,细胞中不可能发生() A.DNA的解旋B.蛋白质的合成C.基因突变D.基因重组 [答案] D [解析]卵原细胞进行DNA复制时属于细胞分裂间期,若DNA复制发生差错,会产生基因突变,细胞中同时要合成有关蛋白质;基因重组是指在生物体进行有性生殖的过程中,控制不同性状的基因重新组合,发生在减数分裂期。 7.将一粒花药培育成幼苗,对它的茎尖用秋水仙素处理,长大后该植株能正常开花结果。该植株下列细胞中哪一细胞与其他三种细胞染色体数目不相同() A.根细胞B.种皮细胞C.子房壁细胞D.果实细胞 [答案] A [解析]将一粒花粉培育成单倍体幼苗,对它的茎尖用秋水仙素处理,长大后该植株地上部分细胞中染色体加倍了,但根细胞染色体数未改变。 8.基因型为AaBb(位于非同源染色体上)的小麦,将其花粉培养成幼苗,用秋仙素处理后的成体自交后代的表现型及其比例为() A.1种,全部B.2种,3∶1 C.4种,1∶1∶1∶1 D.4种,9∶3∶3∶1 [答案] C [解析]基因型为AaBb(位于非同源染色体上)的小麦,将其花粉培养成幼苗,用秋水仙素处理后的成体为纯合体,共四种:AABB、AAbb、aaBB、aabb,纯合体自交后代不发生性状分离,仍为纯合体,表现型及其比例为1∶1∶1∶1。 9.下列基因组合中,不可能是由二倍体产生的配子是() A.Dd B.YR C.Ab D.BCd [答案] A
