锂离子电池理论知识考试大纲1

四新知识大纲(电池)
锂离子电池
基本要求
1.具有电化学的基础知识。
2.掌握锂离子电池的基本概念。
3.了解锂离子电池的工作原理和基本组成。
4.了解锂离子电池的生产工艺流程。
5.具有计算机的基础知识及英语知识,能使用充放电仪器测试电池的电性能。
6.具有安全生产知识。
考试内容
一.基础知识
1.锂离子电池的工作原理以及正负极活性物质的化学组成,并能写出反应方程式。
2.锂离子电池的组成、各工序对环境的要求以及主要技术性能参数。
3.电池容量的计算方法,能根据有效物质的用量计算出电池的理论容量。
4.电路的简单知识及锂离子电池的测试方法。
二.锂离子电池的种类和生产流程
1.种类:液态锂离子电池和固态锂离子电池。
2.生产流程:
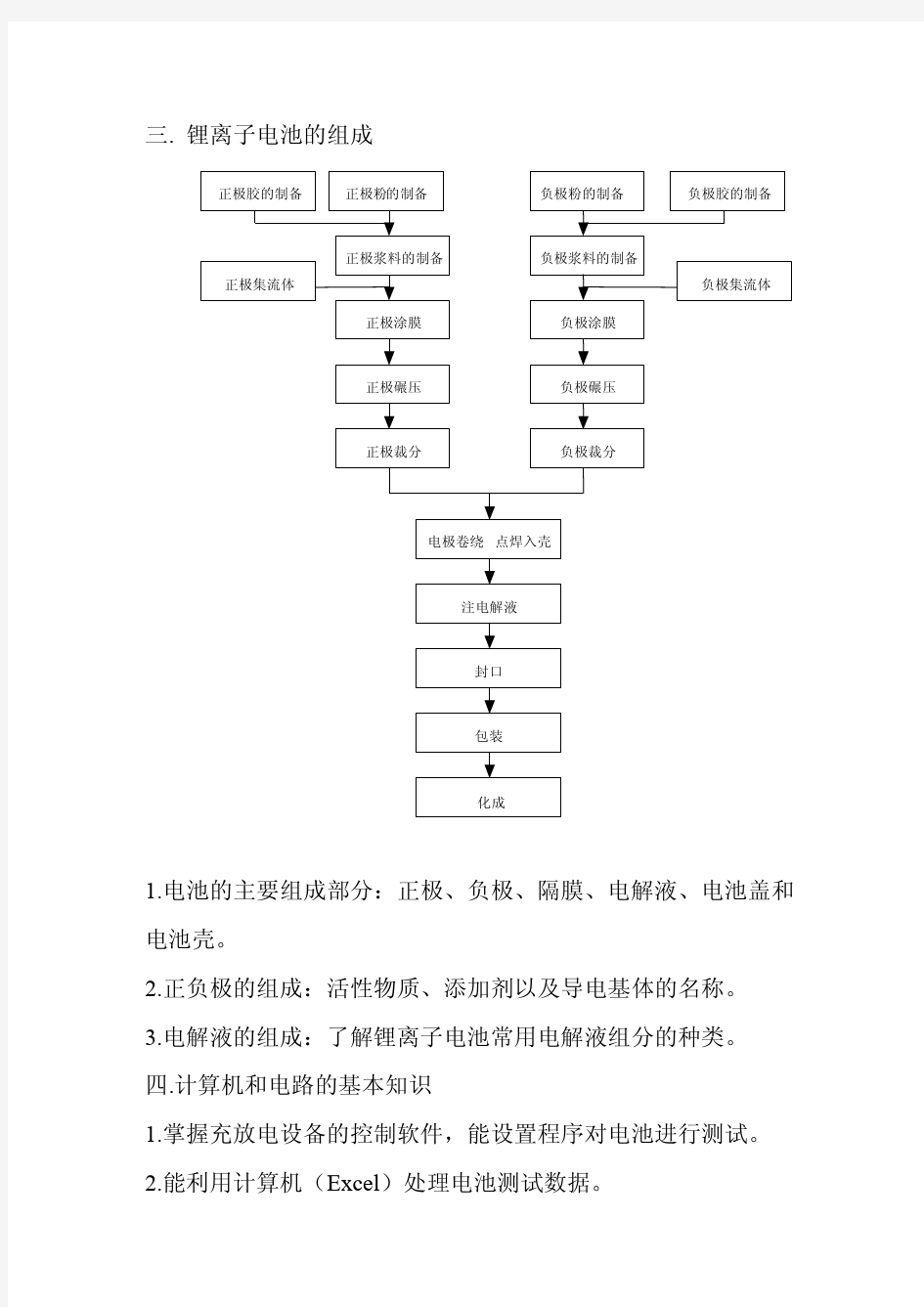
三.锂离子电池的组成
1.电池的主要组成部分:正极、负极、隔膜、电解液、电池盖和电池壳。
2.正负极的组成:活性物质、添加剂以及导电基体的名称。
3.电解液的组成:了解锂离子电池常用电解液组分的种类。
四.计算机和电路的基本知识
1.掌握充放电设备的控制软件,能设置程序对电池进行测试。
2.能利用计算机(Excel)处理电池测试数据。
3.了解电路的基础知识:能进行组合电池以及保护线路板间的连接。安全性能测试时能进行数据采集。
五.了解聚合物锂离子电池的结构组成以及生产流程
1.聚合物锂离子电池的结构
2.聚合物锂离子电池生产工艺流程
六.锂离子电池的正确使用方法
1.防止电池过充、过放,锂离子蓄电池在过充、过放状态下电池材料的结构就会发生变化,
造成电池的不安全,因此在使用过程中一定要控制电池的状态,即电池的电压在4.2V ~2.75V
之间。
方型锂离子聚合物电池结构图
聚合物锂离子电池制造工艺流程
2.使用锂离子蓄电池专用的充电器。
3.注意电池的使用环境,远离高温高湿环境,不要接近火源,防止剧烈振动和撞击,电池有漏液现象
应立即停止使用并妥善处理电池。
燃料电池
基本要求
1.了解燃料电池基础知识。
2.了解质子交换膜燃料电池基础知识。
3.了解质子交换膜燃料电池基本组成。
4.了解质子交换膜燃料电池电堆的结构与性能。
5.了解质子交换膜燃料电池电源系统的组成。
考试内容
一、燃料电池基础知识
1.燃料电池原理与概念
2.燃料电池的特点及应用
3.燃料电池的分类
二、质子交换膜燃料电池基础知识
1.工作原理与概念
2.特点与应用
三、质子交换膜燃料电池基本组成
1.质子交换膜燃料电池单体的组成
2.电催化剂
3.质子交换膜
4.膜电极组件
5.双极板
四、质子交换膜燃料电池电堆的结构与性能
1.质子交换膜燃料电池电堆的结构
2.质子交换膜燃料电池电堆的性能
五、质子交换膜燃料电池电源系统的组成
1.系统组成
2.氢源技术
砷化镓太阳电池
基本要求
1.具有砷化镓太阳电池的基础知识。
2.了解砷化镓太阳电池的基本结构及各结构层的作用。
3.了解砷化镓太阳电池制备的工艺方法。
考试内容
一、基础知识
1.太阳电池的光电转换原理。
2.与硅太阳电池相比砷化镓太阳电池的三个优点
(光电转换效率高、温度系数低和抗辐照能力强)。
3.砷化镓太阳电池的四个性能参数(短路电流、开路电压、
太阳电池的光电转换效率和填充因子)。
二、砷化镓太阳电池的基本结构及各结构层的作用下电极、单晶衬底、缓冲层、背反射层、基区、发射区、窗口层、接触层、上电极和减反射膜。
三、砷化镓太阳电池制备的工艺方法
1.单晶衬底制备工艺方法:
砷化镓单晶:直拉单晶制备工艺,水平法单晶制备工艺
锗单晶:直拉单晶制备工艺(或称CZ法),悬浮区熔法单晶制备工艺(或称FZ法)
2.半导体薄层的制备工艺方法
砷化镓太阳电池的结构中的缓冲层、背反射层、基区、发射区、窗口层、接触层等统称半导体薄层。
(1)液相外延法(LPE);
(2)金属有机化学沉积(MOCVD)或称金属有机化学汽相外延(MOVPE);
(3)LPE和MOCVD技术各自的原理和特点。
3.器件工艺技术
器件工艺技术是指由外延片制作成电池的全部半导体工艺技术,以完成下电极、上电极和减反射膜的制备。主要包括:
(1)真空蒸镀:主要用于蒸镀下电极、上电极和减反射膜工序。
(2)光刻:主要用于制备上电极掩模。
(3)腐蚀:主要用于蒸镀下电极、上电极和减反射膜工序前的
表面制备。
(4)烧结:主要用于下电极、上电极的加固。
(5)划片:划成所要求的尺寸。
四、参考书
1、《太阳电池及其应用》赵富鑫魏彦章国防工业出版社
1985年2月第1版
2、《太阳电池工作原理、工艺和系统的应用》马丁·格林箸,
李秀文等译电子工业出版社1987年8月第1版
3、《卫星电源技术》(导弹与航天丛书卫星工程系列)马世俊主编
宇航出版社2001年12月第1版第1次印刷
4、《电子工业生产技术手册》半导体与集成电路卷第6分册
《半导体材料》责任编辑王晓光国防工业出版社1989年3月第一版
5、《电子工业生产技术手册》半导体与集成电路卷第8分册
《化合物半导体器件》责任编辑王晓光国防工业出版社1992年5月第一版
6、《物理电源》(电子技术培训教材),电子元器件专业技术培
训教材编写组,责任编辑:吴金生,电子工业出版社1985
年4月第1版
超级电化学电容器
基本要求
1.明白超级电容器的概念
2.了解超级电容器的分类
3.了解超级电容器的发展史
4.了解超级电容器的组成
5.了解超级电容器的工作原理
6.了解超级电容器的性能指标
7.了解超级电容器的主要电极材料及其制备
8.了解超级电容器的现状及发展趋势
考试内容
一、超级电容器的概念
超级电容器是介于充电电池与传统电容器之间的一种新型能源器件。它兼有常规电容器功率密度大、充电电池功率密度高的优点,可快速充放电,而且寿命长、工作温限宽、电压记忆性好、免维护,是一种新型、高效、实用的能量储存装置。
二、超级电容器的分类
目前人们研究的超级电容器按电极材料的不同大致可分为活性炭、金属氧化物、导电高分子聚合物三类超级电容器。按工作原理的不同可分为双电层电容器和电化学电容器。按电解质的不同又可分为液体电解质和固体电解质两种,其中液体电解质包括水溶液电解质和有机电液电解质两种。
三、超级电容器的发展史
早在1879年德国亥姆霍金(Helmboltz)就提出了双电层的理
论。液体电解质双电层电容器1956年才出现,20世纪60年代开始了广泛的研究、试制工作,70年代已有商品化产品出现,固体双电层电容器于1965年出现,但至今尚未达到完全商品化。目前的研究主要倾向于液体电解质双电层电容器的研究、而电极材料方面主要研究的有活性炭、活性炭纤维、碳气凝胶、纳米碳管等。
日本NFC公司1991年研制出了1000F/5.5V、储能约6kJ的活性炭双电层电容器。他们将活性炭粉和酚醛树脂粉按7:3混合,球磨至1500m2,在10MPa、150℃下热压10min成型,然后在900℃、保持下焙烧2h制成电极方块、切成适当大小的薄片作为电极使N
2
用,电解液用30%的硫酸;该电容器单元工作电压0.9V、6个单元组成一个5.5v电容器。
Takeuchi等将石油焦和沥青在700—850℃煅烧获得石墨层状结构的碳,再用KOH在800℃下处理,然后制成了25—30F/cm3的电极。
Tan Ming X用聚氯乙烯膜在惰性气氛中加热制备微孔碳膜(平均密度0.7-1.08g/cm2)。其比容量达到120—315F/g,并申请了美国专利。
活化处理过的活性炭纤维电极和水溶Kim等用在900℃下CO
2
液电解液制成了比容量165F/g,循环寿命达30000次以上的双电层电容器。Hirahara Satoshi等采用在有机电解液中添加锂离子使碳电极活化,得到工作电压>3V,并具有更高的能量密度和更长的使用寿命的双电层电容器。
Osaka Tetsuya等用比表面积2500m2/g的活性炭制成的电极和聚氟乙烯-聚六氟丙烯凝胶电解液(PVDE-HEP/PC/EC/TEABF4=23/3l/35/11)制成了比容量123F/g、循环寿命>104/次的双电层电容器。
Bispo Fonseca采用有机铵盐为电解液,两种电极制作方法:(1)在镍箔上喷涂电极材料的悬浮液;(2)将电极材料压覆在镍集流体上。用第二种方法制成600F/2.5V超级电容器单元,并进一步组合成100F/12V超级电容器,经测试用第二种方法制成电极性能更好。比较镍网、泡沫镍两种集流体,泡沫镍集流体更好,其等效串联电阻取决于泡沫镍的等级。
Diederich L.等用其合成的纳米碳膜(1g/cm3)制成电极,其单极容量为75F/g,以聚碳酸酯有机电解液制成能量密度和功率密度分别为76wh/kg和706kw/kg的超级电容器电极。
古可隆等采用现代仪器和化学分析方法比较深入地研究了双电层电容器用多孔碳质材料(活性炭)的孔隙容积、孔半径分布、比表面积、含氧基团、吸附性能对静电容量、等效串联电阻等电性能的影响,并在此基础上确定和优化了制备技术路线,为双电层电容器的电极板材料国产化提供了理论依据和可行的技术路线。
Gouerec P.等用比表面积400—500m2/g的多孔热聚合丙烯晴气凝胶薄膜制成双电层电容器电极,在5mol/L KOH水溶液中比容量达到130F/g,能量密度和功率密度分别为4.4Wh/kg和
1400W/kg。
Morimoto等研究了双电层电容器用有机电解液的性能,他们采用活性炭作阴极、掺杂锂的石墨作阳极,制成有机电解液的电容器,其工作电压>4.0V、能量密度4wh/kg、功率密度600W/kg。
另外,Bonnefoi L.等研究了大电极(32cm2)的制造技术,并制成了2V/250F的超级电容器单元[100cm3],功率达到120-130W;他们还研制了一种低成本碳/碳超级电容器,单元工作电压
2.0V,功率密度1.1kw/kg,单电极的体积比容25F/cm3。Nakagawa Hiroyuki等研制了一种用高密度话性炭纤维(HD-ACF)电极的高
容量双电层电容器。Salitra Gregory等对双电层电容器的话性炭电极离子和孔径的关系进行了研究。Sakata Yusaku等用金属离子交换树脂碳化制备双电层电容器的碳电极。日本昭和电工株式会社武内正隆发明了一种由聚合物和电解质盐构成的膜,其强度和可加工性很好,而且离子导电率高,适合制作薄电极、电池和双电层电容器。还有人研究了多孔硅电极制成的超级电容器。
四、超级电容器的组成
超级电容器主要由极化电极、集电极、电解质、隔离膜、端板、引线和封装材料几部分组成。电极的制造技术、电解质的组成和隔离膜质量对超级电容器的性能有决定性的影响,电解质的分解电压决定超级电容器的工作电压,所以以水溶液为电解液的电容器工作电压只有lV左右,而有机电解液的可达3V左右。五、超级电容器的工作原理
1.双电层超级电容器的工作原理
当金属插入电解液中时,金属表面上的净电荷将从溶液中吸引部分不规则分配的带异种电荷的离子,使它们在电极—溶液界面的溶液一侧离电极一定距离排成一排,形成一个电荷数量与电极表面剩余电荷数量相等而符号相反的界面层。这个界面由两个电荷层组成,一层在电极上,另一层在溶液中,因此称为双电层。由于界面上存在一个位垒,两层电荷都不能越过边界彼此中和,按照电容器原理将形成一个平板电容器。如图1所示。
图1双电层超级电容器工作原理图
2.电化学电容器的工作原理
电极表面或体相中的二维或准二维空间上,电活性物质进行欠电位沉积,发生高度可逆的化学吸脱附或氧化还原反应,产生与电极充电电位有关的电容,或者是发生n型/p型元素掺杂/去掺杂反应,从而产生与电极电荷有关的所谓“法拉第准(假)电容。如图2所示。按照使用的材料不同,这类超级电容器又可以分为“贵金属氧化物超级电容器”以及“导电聚合物超级电容器”两类。前者的代表为氧化钌超级电容器,后者的代表为聚苯胺超级电容器。
图2电化学超级电容器工作原理图
六、超级电容器的性能指标
1.比容量
比容量是指单位重量或单位体积的电容器所给出的容量,称之为重量比容量或体积比容量。
2.比能量
比能量是指单位重量或单位体积的电容器所给出的能量,也叫重量比能量或体积比能量,也称能量密度,常用Wh/kg或Wh/L 表示。
3.比功率
单位重量或单位体积的超级电容器所给出的功率。表征超级电容器所承受电流的大小。超级电容器的比功率是电池的数量级倍数。
4.循环寿命
超级电容器经历一次充电和放电,称为一次循环或叫一个周期。与充电电池相比,超级电容器的循环寿命很长,可达10万次以上。
超级电容器和蓄电池的性能比较见表1。
表1超级电容器和蓄电池性能比较条件蓄电池超级电容器电化学位变化
由活性物质的热力学性质决定随活性物质的变化而变化充放电电极电位变化如果不发生非热力学过程或物相变化,
电极电位随充电状态而发生变化
电极电位保持不变
电量储存方式
非电容性电容性恒电位变化时
得不到恒流曲线可得恒流曲线呈线性变化恒流放电时电位变化
基本不变呈线形变化比能量
20-200Wh/kg 0.2-20Wh/kg 比功率
<500W/kg 102-104W/kg 充放电次数<104>105七、超级电容器的主要电极材料
1.碳电极
碳是最早被用于制作超级电容器的电极材料。从1954年Beck 发表相关专利以来,已有40多年的发展史。目前常用的碳素材料有:碳纳米管、玻璃碳、粉末、纤维、凝胶、薄膜、高密度石墨和热解聚合物基体得到的泡沫。这些材料共同的特点是具有高的比表面积。
2.金属氧化物电极
目前对金属氧化物电极电化学电容器的研究,主要是一些过渡金属氧化物。例如,α-MnO2·nH20、α-V 2O 5·n H 20、α-RuO 2·nH 20、H 3Pmo·nH 20、IrO 2、、NiOx、WO 3、PbO 2J、C0304、SrRuO 3等。其中以硫酸为电解液的α-RuO 2·nH 20电化学电容器
和以氢氧化钾为电解液的NiOx 电化学电容器研究最多。
3.导电聚合物电极
常见的导电聚合物材料有:聚吡咯、聚噻吩、聚苯胺、聚乙炔、聚亚胺酯以及它们衍生物的聚合物,然后在这些聚合物材料
中掺杂n型或p型元素,制成电极。
导电聚合物电极电容器可分为3种类型:(1)对称结构——电容器中两电极为相同的可p型掺杂的导电聚合物(如聚噻吩);(2)不对称结构——两电极为不同的可进行p型掺杂的聚合物材料(如聚吡咯和聚噻吩);(3)导电聚合物可以进行p型和n型掺杂,充电时电容器的一个电极是n型掺杂状态而另一个电极是P型掺杂状态,放电后都是去掺杂状态,这种导电聚合物电极电容器可提高电容电压到3V,而两电极的聚合物分别为n型掺杂和P型掺杂时,电容器在无放电时能充分利用溶液中的阴阳离子,结果它具有很类似蓄电池的放电特征,因此被认为是最有发展前景的电化学电容器。
超级电容电极材料有待进一步研究,为即将兴起的混合电动车(HEV)和电动车(EV)以及其它能源管理系统的需要做准备。目前,国外已经开展了不少研究工作,国内也有科研人员开展这方面的工作,并取得了一定进展,但在导电聚合物材料方面的研究还比较薄弱,有理由相信不久在我国也会有较大的发展。
八、超级电容器的现状及发展趋势
超级电容器可应用于许多领域,如电动车辆、激光微波武器、移动通讯装置、便携式仪器设备、数据记忆存储系统、应急后备电源以及作为燃料电池的启动电源等,特别是在电动汽车上的应用具有非常明显的优势。最近,电动车实用化的过程中,发现车辆在启动、爬坡和加速时急需供应大电流脉冲电能,在刹车时,
需大电流储存电能,这些是蓄电池难以做到的。超级电容器的使用可以大大延长蓄电池的循环使用寿命,提高电动车的实用性,于是人们对超级电容器更加感兴趣。
目前,国外特别是美国和日本的研究重点主要在于如何提高超级电容器的储能密度以满足电动车等应用,其研究内容涉及到新材料的研发、制作工艺、方法改进等。例如,日本设立新电容器研究会,美国设立有SupercapaciterSymposium,并对全密封电容器制定了发展目标,近期目标(1998年—2003年)为:比功率为500w/kg,比能量为2.5W·h/kg;远期目标(2003年)为:比功率为1500w/kg,比能量为15W·h/kg。每年定期召开讨论会,且都设有相关的开发机构,如像美国能源部和美国三大汽车巨头建立有USABC(US Advanced Battery Consortium),日本有New Sun Shine开发机构,欧盟有Saft公司。其技术现状如表2所示。
国内对超级电容器的研究则刚刚起步,目前只有1—2家企业可以工业化生产活性碳类超级电容器。大庆华随电子有田公司是首家实现超级电容器产业化的公司,其产品有5.5v、3.5v、11v 等系列;北京金正平科技有田公司和石家庄开发区高达科技开发有田公司共同研究开发成功大功率超级电容器产品,并已开始批量生产,其技术水平已与俄罗斯相近。但从整体来看,我国在超级电容器领域仍明显落后于世界先进水平。
虽然超级电容器在应用中越来越显示出其强大的生命力,但
是也要看到,目前的超级电容器在电能储存方面与电池相比还有一定的差距,因此怎样提高单位体积内的储能密度是目前超级电容器领域的一个研究重点与难点。应该说制作工艺与技术的改进是提高超级电容器的储存电能能力的一个行之有效的方法。但从长远来看,寻找新的电极活性材料才是根本之所在,但同时这也是难点之所在。超级电容器越来越轻、供电能力越来越强的目标的实现可能需要借助于一些高新技术的开发与应用,比如象纳米技术。只有这样,超级电容器的前景才会越来越光明。
表2国外超级电容器技术现状
《传感器与检测技术》习题答案
第1章传感器与检测技术基础思考题答案 l.检测系统由哪几部分组成?说明各部分的作用。 答:一个完整的检测系统或检测装置通常是由传感器、测量电路和显示记录装置等几部分组成,分别完成信息获取、转换、显示和处理等功能。当然其中还包括电源和传输通道等不可缺少的部分。下图给出了检测系统的组成框图。 检测系统的组成框图 传感器是把被测量转换成电学量的装置,显然,传感器是检测系统与被测对象直接发生联系的部件,是检测系统最重要的环节,检测系统获取信息的质量往往是由传感器的性能确定的,因为检测系统的其它环节无法添加新的检测信息并且不易消除传感器所引入的误差。 测量电路的作用是将传感器的输出信号转换成易于测量的电压或电流信号.通常传感器输出信号是微弱的,就需要由测量电路加以放大,以满足显示记录装置的要求。根据需要测量电路还能进行阻抗匹配、微分、积分、线性化补偿等信号处理工作. 显示记录装置是检测人员和检测系统联系的主要环节,主要作用是使人们了解被测量的大小或变化的过程。 2。传感器的型号有几部分组成,各部分有何意义? 依次为主称(传感器)被测量—转换原理—序号 主称——传感器,代号C; 被测量——用一个或两个汉语拼音的第一个大写字母标记。见附录表2; 转换原理—-用一个或两个汉语拼音的第一个大写字母标记。见附录表3; 序号-—用一个阿拉伯数字标记,厂家自定,用来表征产品设计特性、性能参数、产品系列等。若产品性能参数不变,仅在局部有改动或变动时,其序号可在原序号后面顺序地加注大写字母A、B、C等,(其中I、Q不用)。 例:应变式位移传感器: C WY-YB—20;光纤压力传感器:C Y—GQ—2. 3。测量稳压电源输出电压随负载变化的情况时,应当采用何种测量方法? 如何进行? 答:测定稳压电源输出电压随负载电阻变化的情况时,最好采用微差式测量.此时输出电压认可表示为U0,U0=U+△U,其中△U是负载电阻变化所引起的输出电压变化量,相对U来讲为一小量。如果采用偏差法测量,仪表必须有较大量程以满足U0的要求,因此对△U,这个小量造成的U0的变化就很难测准.测量原理如下图所示: 图中使用了高灵敏度电压表-—毫伏表和电位差计,R r和E分别表示稳压电源的内阻和电动势,凡表示稳压电源的负载,E1、R1和R w表示电位差计的参数.在测量前调整R1使电位
锂离子电池基本知识
一.电池常规知识 目录 1.什么是电池? 2.一次电池和二次电池有什么区别? 3、充电电池是怎样实现它的能量转换? 4、什么是Li-ion电池? 5、Li-ion电池的工作原理? 6、Li-ion电池的主要结构。 7、Li-ion电池的优缺点。 8、Li-ion电池安全特性是如何实现的? 9、什么是充电限制电压?额定容量?额定电压?终止电压? 10、Li-ion铝壳和钢壳电池比较它的区别有哪些? 11、目前常见的各种可充电电池之间有什么区别? 1、什么是电池? 电池是一种能源。当它正负极连接在用电器上时,因为正负极之间存在电势之差,电流从正极流向负极,储存在电池中的化学能直接转化成电能释放出来,一只电池必然由两种不同电化学活性的物质组成正负两极,正负极活性物质之间的电动势差形成电池的电压,根据其电化学系统的不同,各种类型的电池
电压各有不同。 2、一次电池和充电电池有什么区别? ?电池内部的电化学设计决定了该类型的电池是否可充。根据它 们的电化学成分和电极的结构可知,可充电电池的内部结构之 间所发生的反应是可逆的。 ?理论上,这种可逆性是不会受循环次数的影响,既然充放电会 在电极的体积和结构上引起可逆的变化,那么可充电电池的内 部设计就支持这种变化。而一次电池在给定的电池环境中两个 电极之间的电化学反应是不可逆的,因此,不可以将一次电池 拿来充电,这种做法很危险也很不经济。如果需要反复使用, 应选择真正的循环次数在1000次左右的充电电池,这种电池又 称为二次电池。 ?另一明显的区别就是它们具有较高的比能量和负载能力,以及 自放电率。一次电池能量密度远比一次电池高。然而他们的负 载能力相对要小。 ?二次电池具有相对较高的负载能力,可充电电池Li-ion,随着 近几年的发展,具有高能量容量。 ?不管何种一次电池的电化学系统属于哪种,所有的一次电池的 自放电率都很小。 3、充电电池是怎样实现它的能量转换? ?每种电池都具有电化学转换的能力,即将储存的化学能直接转 换成电能。就二次电池而言(另一术语也称可充电便携式电池),
自动检测技术题库
第一章检测技术的基础知识 一、填空题 1.检测技术是一门以研究自动检测系统中的信息提取、信息转换以及信息处理的理论和技术为主要内容的应用技术学科。 2.一个完整的检测系统或检测装置通常由传感器、测量电路和输出单元及显示装置等部分组成。 3.传感器一般由敏感元件、转换元件和转换电路三部分组成,其中敏感元件是必不可少的。 4.在选用仪表时,最好能使其工作在不小于满刻度值2/3 的区域。 5.准确度表征系统误差的大小程度,精密度表征随机误差的大小程度,而精确度则指准确度和精密度的综合结果。6.仪表准确度等级是由系统误差中的基本误差决定的,而精密度是由随机误差和系统误差中的附加误差决定的。 7、若已知某直流电压的大致范围,选择测量仪表时,应尽可能选用那些其量程大于被测电压而又小于被测电压1.5倍的电压表。(因为U≥2/3Umax) 二、选择题 1.在一个完整的检测系统中,完成信息采集和信息转换主要依靠 A 。 A.传感器 B. 测量电路 C. 输出单元 2.构成一个传感受器必不可少的部分是 B 。 A.转换元件B.敏感元件C.转换电路D.嵌入式微处理器 3.有四台量程均为0-600℃的测量仪表。今要测一约为500℃的温度,要求相对误差≤2.5%,选用精度为 D 的最为合理。 A.5.0级B.2.5级C.2.0级D.1.5级 4.有四台量程不同,但精度等级均为1.0级的测温仪表。今欲测250℃的温度,选用量程为 C 的最为合理。A.0~1000℃B.300~500℃C.0~300℃D.0~500℃ 5.某采购员分别在三家商店购买100kg大米、10kg苹果、1kg巧克力,发现缺少约0.5kg,但该采购员对卖巧克 力的商店意见最大,在这个例子中,产生此心理作用的主要因素是B。 A.绝对误差B.示值相对误差C.满度相对误差D.精度等级 6.在选购线性仪器时,必须在同一系列的仪表中选择适当的量程。这时必须考虑到应尽量使选购的仪表量程为 欲测量的C左右为宜。 A.3倍B.10倍C.1.5倍D.0.75倍 7.用万用表交流电压档(频率上限为5kHz)测量100kHz、10V左右的高频电压,发现示值不到2V,该误差属 于 B 。用该表主流电压档测量5号电池电压,发现每次示值均为1.8V,该误差属于 A 。 A.系统误差B.粗大误差C.随机误差D.动态误差 8.重要场合使用的元器件或仪表,购入后需进行高、低温循环老化试验,其目的是为了D。 A.提高精度B.加速其衰老C.测试其各项性能指标D.提高可靠性能 9.电工实验中,采用平衡电桥测量电阻的阻值,是属于 B 测量,而用水银温度计测量水温的微小变化,是属于C 测量。 A.偏位式B.零位式C.微差式 三、计算题 1.有一温度计,它的测量范围为0~200℃,精度为0.5级,求: 1)该仪表可能出现的最大绝对误差。 2)当示值分别为20℃、100℃时的示值相对误差。 2.已知待测拉力约为70N左右。现有两只仪表,一只为0.5级,测量范围为0~500N;另一只为1.0级,测量范围 为0~100N。问选用哪一只测力仪表较好?为什么? 3.有一台测量压力的仪表,测量范围为(0~10)Mpa,压力与仪表输出电压之间的关系为U0=a0+a1p+a2p2,式中a0=1V, a1=0.6V/ Mpa,a2=-0.02V/Mpa2 求: 1)该仪表的输出特性方程; 2)该仪表的灵敏度表达式;
锂离子电池基础知识
电池基础知识培训资料 一、锂离子电池工作原理与性能简介: 1、电池的定义:电池是一种能量转化与储存的装置,它通过反应将化学能或物理能转化为电能,电池 即是一种化学电源,它由两种不同成分的电化学活性电极分别组成正负极,两电极浸泡在能提供媒体传 导作用的电解质中,当连接在某一外部载体上时,通过转换其内部的化学能来提供能源。 2、锂离子电池的工作原理:即充放电原理。Li-ion的正极材料是氧化钴锂,负极是碳。当对电池进行充电时,电池的正极上有锂离子生成,生成的锂离子经过电解液运动到负极。而作为负极的碳呈层状结构,它有很多微孔,达到负极的锂离子就嵌入到碳层的微孔中,嵌入的锂离子越多,充电容量越高。同样, 当对电池进行放电时(即我们使用电池的过程),嵌在负极碳层中的锂离子脱出,又运动回正极。回正 极的锂离子越多,放电容量越高。我们通常所说的电池容量指的就是放电容量。在Li-ion的充放电过程中,锂离子处于从正极→负极→正极的运动状态。Li-ion就象一把摇椅,摇椅的两端为电池的两极,而锂离子就象运动员一样在摇椅两端来回奔跑。所以,Li-ion又叫摇椅式电池。 通俗来说电池在放电过程中,负极发生氧化反应,向外提供电子;在正极上进行还原反应,从外电路接收电子,电子从负极流到正极,而电流方向正好与电子流动方向相反,故电流经外电路从正 极流向负极。电解质是离子导体,离子在电池内部的正负极之间定向移动而导电,阳离子流向正极,阴 离子流向负极。整个电池形成了一个由外电路的电子体系和电解质的离子体系构成的完整放电体系,从 而产生电能。 正极反应:LiCoO2==== Li1-x CoO2 + xLi+ + xe 负极反应:6C + xLi+ + xe- === Li x C6 电池总反应:LiCoO2 + 6C ==== Li1-xCoO2 + LixC6
锂电池基础知识讲解
锂电池基础知识讲解 理想的锂离子电池,除了锂离子在正负极之间嵌入和脱出外,不发生其他副反应,不出现锂离子的不可逆消耗。实际的锂离子电池,每时每刻都有副反应存在,也有不可逆的消耗,如电解液分解,活性物质溶解,金属锂沉积等,只不过程度不同而己。实际电池系统,每次循环中,任何能够产生或消耗锂离子或电子的副反应,都可能导致电池容量平衡的改变。一旦电池的容量平衡发生改变,这种改变就是不可逆的,并且可以通过多次循环进行累积,对电池性能产生严重影响。 ⑴正极材料的溶解 尖晶石LiMn2O4中Mn的溶解是引起LiMn2O4可逆容量衰减的主要原因,对于Mn的溶解机理,一般有两种解释:氧化还原机制和离子交换机制。氧化还原机制是指放电末期Mn3+的浓度高,在LiMn2O4表面的Mn+会发生歧化反应: 2Mn3+(固)Mn4+(固)+Mn2+(液) 歧化反应生成的二价锰离子溶于电解液。离子交换机制是指Li+和H+在尖晶石表面进行交换,最终形成没有电化学活性的HMn2O4。 Xia等的研究表明,锰的溶解所引起的容量损失占整个电池容量损失的比例随着温度的升高而明显增大(由常温下的23%增大到55℃时的34%)[14]。 ⑵正极材料的相变化[15] 锂离子电池中的相变有两类:一是锂离子正常脱嵌时电极材料发生的相变;二是过充电或过放电时电极材料发生的相变。 对于第一类相变,一般认为锂离子的正常脱嵌反应总是伴随着宿主结构摩尔体积的变化,同时在材料内部产生应力,从而引起宿主晶格发生变化,这些变化减少了颗粒间以及颗粒与电极间的电化学接触。 第二类相变是Jahn-Teller效应。Jahn-Teller效应是指由于锂离子的反复嵌入与脱嵌引起结构的膨胀与收缩,导致氧八面体偏离球对称性并成为变形的八面体构型。由于Jahn-Teller效应所导致的尖晶石结构不可逆转变,也是LiMn2O4容量衰减的主要原因之一。在深度放电时,Mn的平均化合价低于3.5V,尖晶石的结构由立方晶相向四方晶相转变。四方晶相对称性低且无序性强,使锂离子的脱嵌可逆程度降低,表现为正极材料可逆容量的衰减。 ⑶电解液的还原[15] 锂离子电池中常用的电解液主要包括由各种有机碳酸酯(如PC、EC、DMC、DEC 等)的混合物组成的溶剂以及由锂盐(如LiPF6 、LiClO4 、LiAsF6 等)组成的电解质。在充电的条件下,电解液对含碳电极具有不稳定性,故会发生还原反应。电解液还原消耗了电解质及其溶剂,对电池容量及循环寿命产生不良影响,由此产生的气体会增加电池的内部压力,对系统的安全造成威胁。 ⑷过充电造成的量损失[15] 负极锂的沉积:过充电时,发生锂离子在负极活性物质表面上的沉积。锂离子的沉积一方面造成可逆锂离子数目减少,另一方面沉积的锂金属极易与电解液中的溶剂或盐的分子发生反应,生成Li2CO3、LiF或其他物质,这些物质可以堵塞电极孔,最终导致容量损失和寿命下降。 电解液氧化:锂离子电池常用的电解液在过充电时容易分解形成不可溶的Li2CO3等产物,阻塞极孔并产生气体,这也会造成容量的损失,并产生安全隐患。 正极氧缺陷:高电压区正极LiMn2O4中有损失氧的趋势,这造成氧缺陷从而导致容量损失。 ⑸自放电 锂离子电池的自放电所导致的容量损失大部分是可逆的,只有一小部分是不可逆的。造成不可逆自放电的原因主要有:锂离子的损失(形成不可溶的Li2CO3等物质);电解液氧化产物堵塞电极微孔,造成内阻增大。
锂离子电池电芯知识培训
关于Li-ion电池的安全认证 ?国际国内关于锂离子电池的安全认证机构及其标准: ?GB(国家标准); ?UL(Underwriter Laboratory)美国安全认证机构; ?CE(COMMUNATE EUROPIEA欧共体的缩写)。表示该商品符合安全、卫生、环保和消费者保护等一系列欧洲指令的要求。证实该产品已通过了相应的合格评定程序或制造商的合格声明,是该产品被允许进入欧盟市场销售的“通行证”; ?企业内部的认证标准,一旦通过各个企业的内部标准,表明具有向该企业供货的能力,并基本达成供货意向。如:MOTOROLA、SAMSUNG。 UL安全认证的测试项目 ?UL(Underwriter Laboratory)在认证过程中所要进行的项目及其测试目标值有: ?电性能方面包括: ?短路测试。不爆炸,不起火,外部温度不超过150℃ ?过充测试。不爆炸,不起火。 ?过放测试。不爆炸,不起火。 ?机械性能方面包括: ?挤压测试。不爆炸,不起火。 ?重物冲击测试。不爆炸,不起火。 ?高频振荡测试。不爆炸,不起火;不漏气或漏液。 ?振动测试。不爆炸,不起火;不漏气或漏液。 ?环境适应性能包括: ?热冲击测试。不爆炸,不起火。 ?温度循环测试。不爆炸,不起火。不漏气或漏液 ?低压测试。不爆炸,不起火。不漏气或漏液 GB要求的安全性能测试项目 ?GB(国标标准)所规定进行的安全性能测试项目: ?电性能方面包括: ?短路测试。不爆炸,不起火,外部温度不超过150℃
?过充测试。不爆炸,不起火。 ?机械性能方面包括: ?重物冲击测试。不爆炸,不起火。允许变形。 ?振动测试。无明显损伤、漏液、冒烟、或爆炸,电池电压不低于N*3.6V ?碰撞测试。无明显损伤、漏液、冒烟、或爆炸,电池电压不低于N*3.6V ?环境适应性能包括: ?热冲击测试。不爆炸,不起火。 ?恒定湿热性能。不爆炸,不起火;不漏气或漏液。 电池基本知识 1、什么是电池? ?电池是一种能源。当它正负极连接在用电器上时,因为正负极之间存在电势之差,电流从正极流向负极,储存在电池中的化学能直接转化成电能释放出来,一只电池必然由两种不同电化学活性的物质组成正负两极,正负极活性物质之间的电动势差形成电池的电压,根据其电化学系统的不同,各种类型的电池电压各有不同。 2、一次电池和充电电池有什么区别? ?电池内部的电化学设计决定了该类型的电池是否可充。根据它们的电化学成分和电极的结构可知,可充电电池的内部结构之间所发生的反应是可逆的。 ?理论上,这种可逆性是不会受循环次数的影响,既然充放电会在电极的体积和结构上引起可逆的变化,那么可充电电池的内部设计就支持这种变化。而一次电池在给定的电池环境中两个电极之间的电化学反应是不可逆的,因此,不可以将一次电池拿来充电,这种做法很危险也很不经济。如果需要反复使用,应选择真正的循环次数在1000次左右的充电电池,这种电池又称为二次电池。 ?另一明显的区别就是二次电池具有较高的比能量和负载能力,但自放电率较大。一次电池能量密度远比二次电池高。然而他们的负载能力相对要小。 3、充电电池是怎样实现它的能量转换? ?每种电池都具有电化学转换的能力,即将储存的化学能直接转换成电能。就二次电池而言(另一术语也称可充电便携式电池),在放电过程中,是将化学能转换成电能;而在充电过程中,又将电能重新转换成化学能。这样的过程根据电化学系统不同,一般可充放电500次以上。
锂电池基本知识
锂电池基本知识 Li-ion电池有哪些优点?哪些缺点? Li-ion具有以下优点: 1)单体电池的工作电压高达2.75-4.2V(标称电压3.6V或者3.7V) 2)比能量大,循环寿命长,一般均可达到500次以上,甚至1000次. 4)安全性能好,无公害,无记忆效应. 作为Li-ion前身的锂电池,因金属锂易形成枝晶发生短路,缩减了其应用领域:Li-ion中不含镉、铅、汞等对环境有污染的元素:部分工艺(如烧结式)的Ni-Cd 电池存在的一大弊病为“记忆效应”,严重束缚电池的使用,但Li-ion根本不存在这方面的问题。 5)自放电小 室温下充满电的Li-ion储存1个月后的自放电率为10%左右, 2、什么充电限制电压?额定容量?额定电压?终止电压? A、充电限制电压 按生产厂家规定,电池由恒流充电转入恒压充电时的电压值。一般单节电池充电限制电压4.2V,多节就是N*4.2(n=1,2,3,4......) B、额定容量 生产厂家标明的电池容量,指电池在环境温度为20℃±5℃条件下,以5h率放电至终止电压时所应提供的电量,用C5表示,单位为Ah(安培小时)或mAh(毫安小时)。 C、标称电压 用以表示电池电压的近似值。 D、终止电压
规定放电终止时电池的负载电压,其值为n*2.75V(锂离子单体电池的串联只数用“n”表示)。 10、为什么恒压充电电流为逐渐减少? 因为恒流过程终止时,电池内部的电化学极化然后保持在整个恒流中相同的水平,恒压过程,再恒定电场作用下,内部Li+的浓差极化在逐渐消除,离子的迁移数和速度表现为电流逐渐减少。 11、什么是电池的容量? 电池的容量有额定容量和实际容量之分。电池的额定量是指设计与制造电池时规定或保证电池在一定的放电条件下,应该放出最低限度的电量。Li-ion规定电池在常温、恒流(1C)恒压(4.2V)控制的充电条件下充电3h,电池的实际容量是指电池在一定的放电条件下所放出的实际电量,主要受放电倍率和温度的影响(故严格来讲,电池容量应指明充放电条件)。容量常见单位有:mAh、Ah=1000mAh) 12、什么是电池内阻? 是指电池在工作时,电流流过电池内部所受到的阻力。有欧姆内阻与极化内阻两部分组成。电池内阻大,会导致电池放电工作电压降低,放电时间缩短。内阻大小主要受电池的材料、制造工艺、电池结构等因素的影响。是衡量电池性能的一个重要参数。注:一般以充电态内阻为标准。测量电池的内阻需用专用内阻仪测量,而不能用万用表欧姆档测量。 13、什么是开路电压? 是指电池在非工作状态下即电路无电流流过时,电池正负极之间的电势差。一般情况下,Li-ion充满电后开路电压为4.1-4.2V左右,放电后开压为3.0V左
《现代检测技术基础复习题》
现代检测技术基础试题 一、阐述仪器线性度的概念,说明有哪些直线拟合方法。阐述回程差、灵敏度和分辨力的概念。 二、仪表的精确度等级是怎样规定的?写出计算公式。某测温仪表的测温范围为0---600℃,准确度等级为2.5级;另一测温仪表的测温范围为0---1200℃,准确度等级为1.5级。现欲测量温度为500℃的设备温度,问选哪种测温仪表会更好?计算说明为什么? 三、(1)假设你开发一台称重仪,在实验室完成了传感器、放大电路和单片机系统的设计制作,但是没有条件施加标准砝码或标准力对传感器和你的系统进行实际标定,你只有一块可用来测量电压和电流的表(或万用表), 在这种条件下你应该首先对仪器的那些指标进行测定?从误差的角度出发,你对你使用的表有何要求? (2)设传感器误差为0.1%;测量放大电路误差为0.03%;系统采用的A/D转换器为10位,试分析仪器最后能达到的最好精度等级是多少? (3)用干电池分压的办法模拟传感器输出信号对电路进行测试,试在整个量程范围内确定其测试点。若每一个测试点测试了十次,说明你对这些数据的处理方法并写出数据处理公式。 三、画图并说明光电池的下列特性: (1)开路电压、短路电流与光照度的关系; (2)输出电流与负载电阻及光照度的关系。 四、画图并说明光电二极管与放大器的电流放大连接法、电压放大连接法和阻抗变换连接法。说明各连接法适用于哪些测量情况。 五、(1)怎样测试光敏电阻的好坏?(2)比较光敏电阻、光电池、光电二极管的异同点。(3)说明选择光电检测器时应注意哪些问题。 六、写出朗伯-比尔定律的数学表达式,说明各符号的含义。 七、用于测量输送皮带上粉粒物料的近红外水分仪为何要采用三个波长进行测
锂电池基本学习知识讲解
锂电池基本知识讲解 电池基本知识 1.电池 电池是将化学反应产生的能量直接转化为电能的一种电化学装置。 2.原电池 原电池是指经过放电后,不能用一般的充电方法使其复原而继续使用的电池,也叫一次电池。 3.蓄电池 指可以通过充电方法使两极活性物质复原而可以再次放电的电池,也叫二次电池。 4.干电池 干电池是指电解液不流动的电池,通常是指锌、锰干电池。 5.电解池 电解池是一种将电能转化为化学能的电化学装置,电池充电时相当于电解池。 6.电子导体 是指依靠物质内部的自由电子在外加电场作用下做定向运动而导电的导体,也叫第一类导体。各种金属通常为第一类。
7.离子导体 是依靠物质内部的可移动离子在外加电场作用在做定向移动而导电的导体,也叫第二类导体。各种电解液通常为第二类导体。如氢氧化钾水溶液。 8.电解质 一定条件下具有离子导电性的物质称为电解质。 9.电极 是指由两类导体即电子导体和离子导体串联组成的导电体系,也叫半电池,通常为了方便把构成电极的金属导体部分称为电极。 10.正/负极 在一个电化学装置中,电极电位较高的电极称为正极;电极电位较低的电极为负极。 11.电池充电 借助于外直流电源,将电能输入电池迫使其内部发生电化学反应的过程叫电池充电。 12.电池放电 电池内部发生电化学反应产生电能并向外电路输出电能的过程叫电池放电。 13.活性物质 是指在电池中将化学能转变为电能的过程中参加电极反应的物质。
14.为什么电池放电时不需要外接电源而电池充电时需要外接电源? 电池放电时的电化学反应是一种自发的过程,电池向外电路供电是可以自发进行的过程,而充电时的电池相当于电解池,电解池中消耗电能的化学反应是一种不可以自发进行的过程,所以要借助于外接电源强迫化学反应逆方向进行。 15.电池电动势 电池正极平衡电极电位与负极平衡电极电位之差称为电池电动势,又叫理论电压。 16.开路电压 电池开路时,正负极之间的电位差叫开路电压,开路电压在数值上等于正负极稳定电极电位之差,是一个实测值。 17.标称电压 一般被认为是电池工作在标准条件下可具有的电压值。18.放电电压 电池放电时正负极间的电位差叫放电电压,也叫工作电压或负载电压或端电压。 19.充电终止电压 电池充电所允许的最高电压叫充电终止电压。 20.放电终止电压 电池放电时,电压下降到不宜再继续放电的最低工作电压
锂离子电池基本知识
锂离子二次电池简介 概述: 锂离子二次电池是指Li+嵌入化合物为正、负极的二次电池,正极采用锂化合 物LiCoO 2、LiMn 2 O 4 ,负极采用锂—碳层间化合物Li x C 6 ,电解质为溶解有锂盐LiPF 6 、 LiAsF 6 等的有机溶液。在充、放电过程中,Li+在两个电极之间往返嵌入和脱嵌,被形象地称为“摇椅电池”(Rocking Chair Batteries,缩写为RCB)。锂离子二次电池由于工作电压高(3.6V)、无记忆效应、无污染、自放电小、循环寿命长,在移动电话、摄相机、笔记本电脑、便携式电器上得到大量应用。 一、工作原理 1、化学反应方程式 锂离子电池正极主要成分为LiCoO 2 ,负极主要为C,充电时 正极反应:LiCoO 2 Li ( 1-x) CoO 2 + xLi+ + xe- 负极反应:C + xLi+ + xe- CLi x 电池总反应:LiCoO 2 + C Li ( 1-x) CoO 2 + CLix 放电时发生上述反应的逆反应。 2、化学反应原理图 二、命名 根据IEC61960标准二次锂电池的标识如下: 1. 电池标识组成3个字母后跟5个数字(圆柱形)或6个(方形数字); 2. 第一个字母表示电池的负极材料:I表示有内臵电池的锂离子,L表示锂金属电 极或锂合金电极; 3. 第二个字母表示电池的正极材料:C基于钴的电极,N基于镍的电极,M基于锰 的电极V基于钒的电极; 4. 第三个字母表示电池的形状:R表示圆柱形电池,P表示方形电池;
5. 数字:圆柱形电池5个数字分别表示电池的直径和高度,直径的单位为毫米,高度 的单位为十分之一毫米,直径或高度任一尺寸大于或等100mm时两个尺寸之间应加 一条斜线。方型电池6个数字分别表示电池的厚度、宽度和高度,单位均为毫米, 三个尺寸任一个大于或等于100mm时尺寸之间应加斜线,三个尺寸中若有任一小于 1mm,则在此尺寸前加字母t,此尺寸单位为十分之一毫米。 例如: ICR18650:表示一个圆柱形二次锂离子电池正极材料为钴其直径约为18mm高约为 65mm。 ICR20/1050 ICP083448:表示一个方形二次锂离子电池正极材料为钴,其厚度约为8mm,宽度约 为34mm,高约为48mm。 ICP08/34/150:表示一个方形二次锂离子电池正极材料为钴其厚度约为8mm,宽度约 为34mm,高约为150mm。 ICPt73448:表示一个方形二次锂离子电池正极材料为钴其厚度约为0.7mm,宽度约 为34mm,高约为48mm。 三、组成结构 1、正极 正极材料一般由钴酸锂、导电石墨、碳黑、粘接剂、溶剂等组成。 2、负极 负极材料一般由碳黑、粘接剂、溶剂等组成。 3、隔膜纸 隔膜纸由PP、PE复合膜组成,厚度一般为25微米,国内有些厂家也有用16 微米的,著名的生产厂家有日本UBE。 4、电解液 电解液为溶解有锂盐LiPF 6、LiAsF 6 等的有机溶液,常用的有机溶液有EC(碳 酸乙烯酯)、DEC(二乙基碳酸)、DMC(二甲基碳酸)等。 5、绝缘垫片 6、外壳 有钢壳和铝壳。 四、制造工艺
锂离子电池基本知识
锂离子电池基本知识
锂离子电池基本知识 1、什么是Li-ion电池? Li-ion是锂电池发展而来。所以在介绍Li-ion之前,先介绍锂电池。举例来讲,以前照相机里用的扣式电池就属于锂电池。锂电池的正极材料是锂金属,负极是碳。当对电池进行充电时,电池的正极上有锂离子生成,生成的锂离子经过电解液运动到负极。而作为负极的碳呈层状结构,它有很多微孔,达到负极的锂离子就嵌入到碳层的微孔中,嵌入的锂离子越多,充电容量越高。同样,当对电池进行放电时(即我们使用电池的过程),嵌在负极碳层中的锂离子脱出,又运动回正极。回正极的锂离子越多,放电容量越高。我们通常所说的电池容量指的就是放电容量。在Li-ion的充放电过程中,锂离子处于从正极→负极→正极的运动状态。Li-ion就像一把摇椅,摇椅的两端为电池的两极,而锂离子就象运动员一样在摇椅来回奔跑。所以Li-ion又叫摇椅式电池。 2、Li-ion电池有哪几部分组成? (1)电池上下盖(2)正极——活性物质为氧化锂钴(3)隔膜——一种特殊的复合膜 (4)负极——活性物质为碳(5)有机电解液(6)电池壳(分为钢壳和铝壳两种) 3、Li-ion电池有哪些优点?哪些缺点? Li-ion具有以下优点: 1)单体电池的工作电压高达3.6-3.8V: 2)比能量大,目前能达到的实际比能量为100-115Wh/kg和240-253Wh/L(2倍于Nl-Cd,1.5倍于Ni-MH),未来随着技术发展,比能量可高达150Wh/kg和400 Wh/L 3)循环寿命长,一般均可达到500次以上,甚至1000次.对于小电流放电的电器,电池的使用期限将倍增电器的竞争力. 4)安全性能好,无公害,无记忆效应.作为Li-ion前身的锂电池,因金属锂易形成枝晶发生短路,缩减了其应用领域:Li-ion中不含镉、铅、汞等对环境有污染的元素:部分工艺(如烧结式)的Ni-Cd 电池存在的一大弊病为“记忆效应”,严重束缚电池的使用,但Li-ion根本不存在这方面的问题。5)自放电小 室温下充满电的Li-ion储存1个月后的自放电率为10%左右,大大低于Ni-Cd的25-30%,Ni、MH的30-35%。Li-ion也存在着一定的缺点,如: 1)电池成本较高。主要表现在LiCoO2的价格高(Co的资源较小),电解质体系提纯困难。2)不能大电流放电。由于有机电解质体系等原因,电池内阻相对其他类电池大。故要求较小的放电电流密度,一般放电电流在0.5C以下,只适合于中小电流的电器使用。 3)需要保护线路控制。 A、过充保护:电池过充将破坏正极结构而影响性能和寿命;同时过充电使电解液分解,内部压力过高而导致漏液等问题;故必须在4.1V-4.2V的恒压下充电; B、过放保护:过放会导致活性物质的恢复困难,故也需要有保护线路控制。 4、什么是锂离子制造过程? 1)配料 用专门的溶液和粘接剂分别与粉末状的正负极活性物质混合,经高速搅拌均匀后,制成浆状的正负极物质。 2)涂漠 将制成的浆料均匀地涂覆在金属箔的表面,烘干,分别制成正负极极片。 3)装配 按正极片——隔膜——负极片——隔膜自上而下的顺序放好,经卷绕制成电池极芯,在经注入电解
锂电池基础知识
(一)锂电池的构成 锂电池主要由两大块构成,电芯和保护板PCM(动力电池一般称为电池管理系统BMS),电芯相当于锂电池的心脏,管理系统相当于锂电池的大脑。 电芯主要由正极材料、负极材料、电解液、隔膜和外壳构成,而保护板主要由保护芯片(或管理芯片)、MOS管、电阻、电容和PCB板等构成。 锂电池的产业链结构如下图: 电芯的构成如下面两图所示: 锂电池的PACK的构成如下图所示: (二)锂电池优缺点 锂电池的优点很多,电压平台高,能量密度大(重量轻、体积小),使用寿命长,环保。 锂电池的缺点就是,价格相对高,温度范围相对窄,有一定的安全隐患(需加保护系统)。
(三)锂电池分类 锂电池可以分成两个大类:一次性不可充电电池和二次充电电池(又称为蓄电池)。 不可充电电池如锂二氧化锰电池、锂-亚硫酰胺电池。 二次充电电池又可以分为下面根据不同的情况分类。 1.按外型分:方形锂电池(如普通手机电池)和圆柱形锂电池(如电动工具的18650);2.按外包材料分:铝壳锂电池,钢壳锂电池,软包电池; 3.按正极材料分:钴酸锂(LiCoO2)、锰酸锂(LiMn2O4)、三元锂(LiNi x Co y Mn z O2)、磷酸铁锂(LiFePO4);
4.按电解液状态分:锂离子电池(LIB)和聚合物电池(PLB); 5.按用途分:普通电池和动力电池。 6.按性能特性分:高容量电池、高倍率电池、高温电池、低温电池等。 (四)常用术语解释 1. 容量(Capacity) 指一定的放电条件下可以从电池锂获得的电量。 我们在高中学物理是知道,电量的公式为Q=I*t,单位为库伦,电池的容量单位规定为Ah (安时)或mAh(毫安时)。意思是1AH的电池在充满电的情况下用1A的电流放电可以放1个小时。 以前的NOKIA的老手机的电池(像BL-5C)一般是500mAh,现在的智能手机电池800~1900mAh,电动自行车一般都是10~20Ah,电动汽车一般都是20~200Ah等。 2. 充放电倍率(Charge-Rate/Discharge-Rate) 表示以多大的电流充电、放电,一般以电池的标称容量的倍数为计算,一般称为几C。
测试与检测技术基础习题
测试与检测技术基础习题 例3-1 以阻值R=120?,灵敏度S=2的电阻应变片与R=120?的固定电阻组成电桥,供桥电压为3V ,并假设负载为无穷大,当应变片的应变值为2με和2000με时,分别求出单臂、双臂电桥的输出电压,并比较两种情况下的电桥灵敏度。(με:微应变,即10-6) 例3-2 有一钢板,原长l=1m ,钢板弹性模量使用BP 3灵敏度E=2*1011Pa ,使用BP-3箔式应变片R=120?,灵敏度系数S=2,测出的拉伸应变值为300με。求:钢板伸长量Δl ,应力σ,ΔR/R 以及ΔR 。如果要测出1με应变值则相应的ΔR/R 是多少? 测试与检测技术基础习题 例3-3 一电容测微仪,其传感器的圆形极板的半径r=4mm ,工作初始间隙d =0.3mm ,空气介质,0试求解: 1)通过测量得到电容变化量为ΔC=±3*10-3pF ,则传感器与工件之间由初始间隙变化的距离Δd=? 2)如果测量电路的放大倍数K =100V/pF ,读数仪表的灵1p 敏度S 2=5格/mV ,则此时仪表指示值变化多少格? 测试与检测技术基础习题 例3-4 为防止电容传感器击穿,在两极之间加入厚 度为a的云母片(见图3-82),其相对介电常数为εr ,空气介电常数ε0,求传感器的总电容量C=?(圆形极板直径D,两云母片间距离δ0)。 a A D 电缆则此时的电压灵敏度S =?电荷灵敏度有无变化?(g u 为重力加速度) 图2 例3-5题图
测试与检测技术基础习题 例3-6 压电加速度计与电荷放大器联接的等效电路如图3所示。图中C为传感器固有电容、电缆电容和放大器输入电容之和。已知传感器的电荷灵敏度 S q=100pC/g,反馈电容C f=0.01μF。试求:当被测加速度为a=0.5g时,电荷放大器输出电压是多少? C f C q E 图3 例3-6题图测试与检测技术基础习题 例3-7 极距变化型电容传感器采用比例运放电路如图4所示。图中:C0为输入阻抗电容;u i为激励电压; u o为输出电压;C x为反馈电容;也即变极距型电容传感器的电容,且C x=ε0εr A/δ;δ为传感器变化极距 。试求: 1)输出电压u o与变化极距δ之间的关系。 2)电容传感器的输出灵敏度S=du i/dδ=? 图4 例3-7题图 测试与检测技术基础习题 例3-8 磁电式绝对振动速度传感器的弹簧刚度 K=3200N/m,测得其固有频率f=20Hz,欲将f减为 00 10Hz,则弹簧刚度应为多少?能否将此类结构传感器的固有频率降至1Hz或更低? 例3-9 参量式传感器与发电式传感器有何主要不同。测试与检测技术基础习题 例3-10 有一霍尔元件,其灵敏度S H=1.2mV/mA x kGs ,把它放在一个梯度为5kGs/mm的磁场中,如果额定控制电流时20mA,设霍尔元件在平衡点附近做±0.01mm摆动,问输出电压可达到多少毫伏? 例3-11 设计利用霍尔元件测量转速的装置,并说明其工作原理。 例3-12 用电涡流传感器实时监测轧制铝板厚度δ的装置,试画出装置框图,简要说明其工作原理。
关于锂电池的基本知识
首先进行一些基础的解释,解释一下锂电池的这些指标,看到现在有很多很多的新手甚至是老鸟总被这些指标弄得一头雾水的在此作为一个知识性的普及吧!应该对大家有用说的不对的欢迎指正。 1.电压:通常有3.6V锂离子电池,3.7V锂聚合物电池他们在%电压方面的%充电和使用基本上可以归为一类,标准放电平台都是3.0V~4.2V 也就是安全电压。当然这个使用上的一类只是电压上的!电流方面锂离子电池远远不如锂聚合物电池。稍候阐述。 2.容量:通常有mAh Ah等。这是一个复合型单位,mA,A代表的是电流 1000MA=1A (A:安培amper)H当然就是时间(H:Hour,小时)这些都是英文的简写。例如一块电池如果是1000mAh的那么就代表该电池在1小时放完自身所有电量的情况下(从4.2V~2.0V)(V:volt 伏特)能够达到1000mA的平均电流。或者简单一些可以理解为能够以1000mA的电流放电持续1小时。1000MAH可以换算为1Ah,这里大家存在一个误区,可能简单的认为我们以2000mAh的电流放这块电池那么这块电池的放电时间就可以坚持半小时。这样说不能说是错误的但至少是不严谨的。因为随着电流的增加电池的内阻不变的情况下,产生的热量在不断的增加,并且电池的内阻越是大电流的情况下体现的越明显,因为外部电路的电阻随着放电电流的增加必然减少而电池内阻不变的情况下必然导致效率降低发热增高,所以刚才提到的举例的那块电池在2000MAH下放电时间必然少于半小时并且电流越大
这点体现的越明显,也就是说这块电池在10A的情况下放电时间将远远少于6分钟! 还有另一种容量单位,在模型中不常用,就是瓦时(WH)瓦特/每小时简单的说就是用电压乘以电流得到的。仍然是上边举例的电池1000ma放电1小时那么它的电量就是3.7Vx1000mah=3700mWh(毫瓦/小时)=3.7WH代表这块电池能够以3.7瓦的功率放电1小时。换一个例子大家就可以理解了,例如我的450级直升机的电池是3S1P 2200MAH 20C 11.1V的那么我的这个电池就是 大概是120W左右这样用电池的24.4Wh除以120W约等于0.2小时=12分钟了。希望这么说大家可以理解。 3.电流:关于电流锂聚和锂离子电池的区别就明显了。锂聚合物电池的放电能力通常在同等容量的锂离子电池的数倍至数十倍。放电电流的概念通常就存在于这里~1C作为一个标准单位电流表示的是放电倍率,代表的是电池在1小时放电平台( 4.2~3.0V)放完时候能够达到的平均电流,看到这里可能很容易和上边的容量单位的解释联系起来,没错,1000mah的电池容量在1C的情况下放电电流就是1000MA 也正是因为这个,很多时候大家都会在这里产生误解。c本身是倍率的意思,目前电池标注的C 都是按照电池最大的放电电流除以1C标准电流得出来的,例如一块1000mah的电池最大能够提供10A的电流那么就用10A/1A=10C 但是个人认为只有在十分之一小时的时间能够放完所有电量
锂电池配料基础知识
锂电池配料基础知识 一、电极的组成: 1、正极组成: a、钴酸锂:正极活性物质,锂离子源,为电池提高锂源。 b、导电剂:提高正极片的导电性,补偿正极活性物质的电子导电性。 提高正极片的电解液的吸液量,增加反应界面,减少极化。 c、 PVDF粘合剂:将钴酸锂、导电剂和铝箔或铝网粘合在一起。 d、正极引线:由铝箔或铝带制成。 2、负极组成: a、石墨:负极活性物质,构成负极反应的主要物质;主要分为天然石墨和人造 石墨两大类。 b、导电剂:提高负极片的导电性,补偿负极活性物质的电子导电性。 提高反应深度及利用率。 防止枝晶的产生。 利用导电材料的吸液能力,提高反应界面,减少极化。 (可根据石墨粒度分布选择加或不加)。 c、添加剂:降低不可逆反应,提高粘附力,提高浆料黏度,防止浆料沉淀。 d、水性粘合剂:将石墨、导电剂、添加剂和铜箔或铜网粘合在一起。 e、负极引线:由铜箔或镍带制成。 二、配料目的: 配料过程实际上是将浆料中的各种组成按标准比例混合在一起,调制成浆料,以利于均匀涂布,保证极片的一致性。配料大致包括五个过程,即:原料的预处理、掺和、浸湿、分散和絮凝。 三、配料原理: (一)、正极配料原理 1、原料的理化性能。 (1)钴酸锂:非极性物质,不规则形状,粒径D50一般为6-8 μm,含水量≤0.2%,通常为碱性,PH值为10-11左右。 锰酸锂:非极性物质,不规则形状,粒径D50一般为5-7 μm,含水量≤0.2%,通常为弱碱性,PH值为8左右。 (2)导电剂:非极性物质,葡萄链状物,含水量3-6%,吸油值~300,粒径一般为 2-5 μm;主要有普通碳黑、超导碳黑、石墨乳等,在大批量应用时一般选择超导碳黑和石墨乳复配;通常为中性。 (3) PVDF粘合剂:非极性物质,链状物,分子量从300,000到3,000,000不等;吸水后分子量下降,粘性变差。 (4) NMP:弱极性液体,用来溶解/溶胀PVDF,同时用来稀释浆料。 2、原料的预处理 (1)钴酸锂:脱水。一般用120 oC常压烘烤2小时左右。 (2)导电剂:脱水。一般用200 oC常压烘烤2小时左右。 (3)粘合剂:脱水。一般用120-140 oC常压烘烤2小时左右,烘烤温度视分子量的大小决定。 (4) NMP:脱水。使用干燥分子筛脱水或采用特殊取料设施,直接使用。
测试与检测技术基础-传感器大作业-传感器的应用与发展综述
传感器的应用与发展综述 班级,姓名A 学号分工 班级姓名B学号分工 班级姓名C学号分工 一、引言 一个测试系统的第一个环节是信号的传感,传感即将被测的量或被观察的量通过一个被测量传感器或敏感元件转换成一个电的、液压的、气动的或其他形式的物理输出量,被测的或被观察的量与被转换的输出量之间根据可利用的物理定律应该具有一种明确的关系。用来完成这种转换的装置称为传感器或敏感元件。其中敏感元件是指直接感受被测物理量并对其进行转换的单元,而传感器则是敏感元件及其相关辅助元件和电路组成的整个装置,其中敏感元件是传感器的核心部件。本文通过对部分常用传感器的原理、性能、应用等方面的探究,做出对传感器发展趋势的展望。 二、不同传感器的工作原理 (一)电感式传感器 电感式传感器由振荡器、开关电路及放大输出电路三大部分组成。振荡器产生一个交变磁场,当金属目标接近这一磁场,并达到感应距离时,在金属目标内产生涡流,从而导致振荡衰减,以至停振。振荡器振荡及停振的变化被后级放大电路处理并转换成开关信号,触发驱动控制器件,从而达到非接触式之检测目的。电感式传感器的工作原理是电磁感应。它是把被测量(如位移等)转换为电感量变化的一种装置。按照转换方式的不同,可分为自感式(包括可变磁阻式与涡流式)和互感式(差动变压器式)两种。电感式传感器主要用于位移测量和可以转换成位移变化的机械量(如力、张力、压力、压差、加速度、振动、应变、流量、厚度、液位、比重、转矩等)的测量。电感式传感器组成如下图1所示。 图1 (二)磁电式传感器 磁电式传感器是基于电磁感应原理,通过磁电相互作用将被 测量(如振动、位移、转速等)转换成感应电动势的传感器,它也被 称为感应式传感器、电动式传感器。根据电磁感应定律,N匝线 圈中的感应电动势。感应电动势的大小由磁通的变化率决定。磁 通量协的变化可以通过很多办法来实现:如磁铁与线圈之间作相 对运动;磁路中磁阻变化;恒定磁场中线圈面积变化等。因此可以制 造出不同类型的磁电式传感器。磁电式传感器是一种机一电能量 变换型传感器,不需要供电电源,电路简单,性能稳定,输出信 号强,输出阻抗小,具有一定的频率响应范围,适合于振动、转 速、扭矩等测量。但这种传感器的尺寸和重量都较大。 一种装在柴油机上的磁电式传感器原理如右图所示,它主要
锂电池隔膜基础知识
.电池隔离膜 1.功用:(1)阻隔电池正负极2)让离子电流(ionic current )通过,但阻力要尽可能地小。因此,吸收电解液之后所表现出来的离子导电度便与(1)隔离膜孔隙度(porosity )、(2)孔洞弯曲度(tortuosity )、(3)电解液导电度、(4)隔离膜厚度、及(5)电解液对隔离膜的润湿程度等因素有关系 隔离膜的引入而对离子传导所额外产生之电阻,应该是隔离膜吸收电解液之后的电阻减去与隔离膜相同面积和厚度之纯电解液的电阻,亦即R (隔离膜) = R (隔离膜 +电解液) – R (电解液) 电阻R 的定义为:A σ1R ?=( 是离子传导途径的长度,A 是离子传导的有效面积,σ是离子导电度(比电阻ρ的倒数))多孔薄膜的孔洞弯曲度d s T =s 是离子经由隔离膜所必须行经之长度,d 则是隔离膜的厚度。多孔薄膜的孔隙度P 之定义为孔洞的体积和隔离膜外观几何体积的比值Ad A P s s =(其中A s 代表隔离膜负责离子传导的有效面积)所以得T P A A s ?= ??? ? ??-?=1 R 2P T R 電解液隔離膜 吸收了电解液之后的隔离膜,其电阻是原先没有隔离膜存在时的 (T 2/P) 倍。当孔洞弯曲度T 愈大,薄膜孔隙度P 愈小时,隔离膜的电阻就愈大 2. 隔离膜之材质与制备 隔离膜具多孔性的结构,孔径范围约在0.1 μm 或100 nm ,表面积非常大,受到电解液侵蚀的机率也当然跟着提高,材料的选择重要。材质有塑料类、玻璃类、和纤维素(cellulose )类等,以塑料类为最大宗,最常见的有聚氯乙烯(polyvinyl chloride ;PVC )、聚醯胺(polyamide )、聚乙烯(polyethylene ;PE )、及聚丙烯(polypropylene ;PP )。塑料类隔离膜之所以应用地最广,除了是因为它比较易于控制厚度之外,也跟1960年代开始日益成熟的高分子科学及加工技术有密不可分的关系.目前, 商业化的锂离子电池都是采用聚烯烃类(polyolefin )的多孔高分子薄膜(如表1.1)作为隔离膜,有的是PP ,有的是PE ,也有用PP/PE/PP 三层合一的。聚烯烃类的隔离膜不仅成本较低廉,而且有优良的机械强度和化学稳定度。关于高分子隔离膜的生产方法则可分为干式和湿式两种,其中干式制程中虽不使用溶剂,具有不污染电池的优点,但实际上现在却是以湿式法较为普遍。此外,两种制程最后均采取至少一个方向的拉伸(orientation )动作,以便提升孔隙度与薄膜强度[]。若以多孔性聚乙烯隔离膜为例,其湿式法的制造程序(如)就是先将超高分子量的PE (23%)、二氧化硅(silica ;60%)、矿油(mineral oil ;12%)、和其它如抗氧化剂的加工助剂(processing aids ;2%)混合在一起,待均匀之后进行挤出程序(extrusion ),所得的膜再压延(calendaring )到所要的厚度,通常是25 μm 左右。此时,膜的内部还含有很多矿油,所以呈现亮黑色。接着,再利用三氯乙烯(trichloroethylene )当作萃取液将矿油从PE 膜里萃取(extract )出来,以便留下孔洞结构[]。最后,成品中仍旧有绝大部份的SiO 2和少量的矿油(9-15%),前者的功用是在巩固孔洞以避免崩塌,而后者则有助于成品保持柔软性。
