2015 12 31细胞培养基本技术 讲座

幻灯片1
细胞培养基本技术
幻灯片2
细胞培养基本概念
细胞培养(动物)是指从体内组织取出细胞在体外模拟体内环境下,使其生长繁殖,并维持其结构和功能的一种培养技术。
细胞培养的培养物可以是单个细胞,也可以是细胞群。
幻灯片3
细胞培养目的与用途
1、科学研究:药物研究开发与基础研究
2、应用于生物制药
幻灯片4
1、科学研究:药物研究开发与基础研究
药物研究与开发
(1) 新药筛选:如化学合成药物药效研究、中药有效成分筛选与鉴定等。
(2) 疫苗研究与开发:如病毒性疫苗的研究与开发(肝炎病毒疫苗、艾滋病疫苗等)、肿瘤疫苗(多肽疫苗)等。(预防性,治疗性)
(3) 基因工程药物研究与开发:如抗毒素,干扰素等各类细胞生长因子的研究与开发等。
幻灯片5
药物研究与开发
(4) 细胞工程药物研究与开发:生物活性多肽研究与开发,人参皂甙、紫杉醇等生物活性成分研究与开发。
(5) 单克隆抗体制备:包括诊断用单克隆抗体,治疗用单克隆抗体。
幻灯片6
基础研究
(1)药物作用机理(活性肽、蛋白类、雪莲等)
(2)基因功能 (比如抗冻蛋白表达、防冻)
(3)疾病发生机理 (比如HPV HeLa细胞,病毒感染)
幻灯片7
2、应用于生物制药
●疫苗生产(组装病毒颗粒、表达):如病毒性疫苗(肝炎病毒疫苗、艾滋病疫苗等)、肿
瘤疫苗(多肽疫苗)等。
●基因工程药物生产:如在临床医学中具有治疗价值的一些细胞生长因子如干扰素、粒细
胞生长因子、胸腺肽等。
●诊断用和治疗药用单克隆抗体生产。
●细胞工程药物生产:生物细胞内的一些生物活性多肽,生物活性物质等。
幻灯片8
原代培养
取自体内新鲜组织并置于体外条件下生长的细胞在传代之前称为原代培养。
传代:
细胞在培养器皿中生长一定时间后,被分开接种到新的培养器皿中。
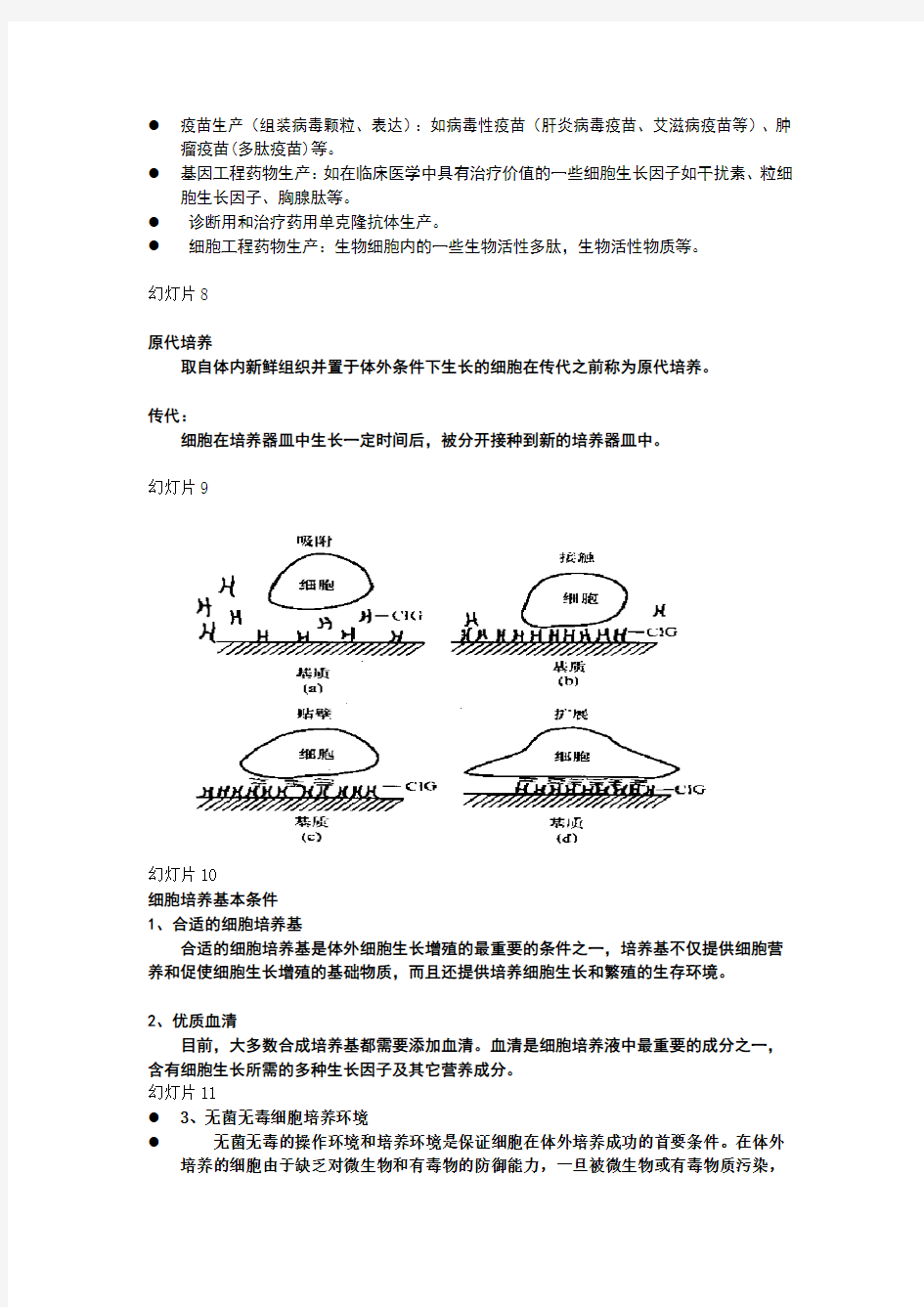
幻灯片9
幻灯片10
细胞培养基本条件
1、合适的细胞培养基
合适的细胞培养基是体外细胞生长增殖的最重要的条件之一,培养基不仅提供细胞营养和促使细胞生长增殖的基础物质,而且还提供培养细胞生长和繁殖的生存环境。
2、优质血清
目前,大多数合成培养基都需要添加血清。血清是细胞培养液中最重要的成分之一,含有细胞生长所需的多种生长因子及其它营养成分。
幻灯片11
●3、无菌无毒细胞培养环境
●无菌无毒的操作环境和培养环境是保证细胞在体外培养成功的首要条件。在体外
培养的细胞由于缺乏对微生物和有毒物的防御能力,一旦被微生物或有毒物质污染,
或者自身代谢物质积累,可导致细胞中毒死亡。因此,在体外培养细胞时,必须保持细胞生存环境无菌无毒,及时清除细胞代谢产物。
●4、恒定的细胞生长温度
●维持细胞旺盛生长(人体),恒定适宜的温度37 ℃。
●5、合适的气体环境
●气体是哺乳动物细胞培养生存必需条件之一,所需气体主要有氧气和二氧化碳。
● 95%空气加5%CO2(细胞代谢产物,也是细胞生长繁殖所需成分); pH: 7.2-7.4
( NaHCO3 )
●
幻灯片12
常用设施及设备
(1)超净工作台(或生物安全柜),
二氧化碳培养箱
(2)无菌操作间:
一般由更衣间、缓冲间和操作间三部分组成。操作间放置净化工作台及二氧化碳培养箱、离心机、倒置显微镜等。缓冲间可放置电冰箱、冷藏器及消毒好的无菌物品等。
幻灯片13
(3)缓冲准备间:离心机、水浴锅、普通天平及日常分析处理物
(4)洗刷消毒间:烤箱、消毒锅、蒸馏水处理器及酸缸等。
幻灯片14
●实验用品:
●超净工作台,压力蒸汽消毒器,电热干燥箱,滤器,酸缸
●CO2培养箱
●倒置显微镜
●酶标仪、微孔板震荡器
●液氮罐
●自动双重纯水蒸馏器,纯水仪
●耗材:培养瓶,吸管,电动吸引器,培养板,冻存管
幻灯片15
●压力蒸汽消毒器:湿热消毒,用途广
●电热干燥箱:干热消毒(160 ℃,2小时)。主要用于玻璃
●器皿消毒
●滤器:过滤除菌:大多数培养用液,如人工合成培养基、血
●清、酶液等均采用滤过法除菌
●超净工作台:为细胞操作提供无菌环境
●紫外灯:紫外线消毒。主要用于培养室空气、操作台、塑料
●培养皿和培养板等表面消毒
●
幻灯片16
超净台
●
●超净工作台的工作原理
是利用鼓风机驱动空气穿过高效滤器除去空气中的尘埃颗粒,使空气得到净化。净化空气徐徐通过工作台面,使工作台内构成无菌环境。
幻灯片17
滤器
幻灯片18
幻灯片19
CO2培养箱
●CO2培养箱设定的条件为37 ℃,5%
CO2 。
●使用CO2培养箱培养细胞时应注意的问题:
●①用螺旋口瓶培养细胞时,需将瓶盖微松,以保证通气。
●②保持培养箱内空气干净。定期消毒
●(90 ℃,14 h)。
●③箱内灭菌蒸馏水3000毫升蒸馏水槽中以保持箱内湿度,避免培养液蒸发。
幻灯片20
幻灯片21 自动双重纯水蒸馏器纯水仪
幻灯片22 酶标仪微孔板震荡器
幻灯片23 培养板
幻灯片24
培养瓶
幻灯片25
细胞培养用液的配制
水:新鲜配置的三蒸水或去离子水
平衡盐溶液:无Ca2+、Mg2+的缓冲液
PBS:NaCl 8.0 g
KCl 0.2 g
Na2HPO4.H2O 1.56 g
KH2PO4 0.20
加水至1000 ml
幻灯片26
●消化液:
●胰蛋白酶作用于与赖氨酸或精氨酸相连接的肽键,除去细胞间粘蛋白及糖蛋白,影响
细胞骨架,从而使细胞分离。
●
●胰蛋白酶液浓度越高,作用越强,但超过一定限度会损伤细胞。
●胰蛋白酶是一种黄白色粉末,用无Ca2+、Mg2+的PBS缓冲液配制,常用的胰蛋白酶液
浓度是0.25%。用滤器过滤除菌。
●胰蛋白酶液消化时间:2-10分钟。
●用含血清培养液终止其对细胞的消化作用。
幻灯片27
培养基
●培养基(培养液)是维持体外细胞生存和生长的溶液,分天然培养基和合成培养基。
●天然培养基:
●天然培养基有血清、血浆和组织提取液(如鸡胚和牛胚浸液)。
●优点:营养成分丰富,培养效果好
●缺点:来源受限。
●成分复杂,影响对某些实验产物的提取和实验结果的分析。
●易发生支原体污染
幻灯片28
合成培养基
●合成培养基是根据细胞生存所需物质的种类和数量,用人工方法模拟合成的。目前已
设计出许多种培养基,如TC199、MEM、RPMI-1640、 DMEM等。
●合成培养基主要成分是氨基酸、维生素、碳水化合物、无机盐和其它一些辅助物质。
●优点:标准化生产,组分和含量相对固定。
●成本低
●缺点:缺少某些成分,不能完全满足体外细胞生长需要。
幻灯片29
●人工合成培养基只能维持细胞生存,要想使细胞生长和繁殖,还需补充一定量的天然
培养基(如血清)。
●支持细胞生长一般需加10%血清。
●
●
幻灯片30
●血清质量好坏是实验成败的关键。
●常用血清有胎牛血清、新生牛血清、小牛血清、兔血清、马血清等,其中以胎牛血清
质量最好。
●优质血清的标准:透明,淡黄色,无沉淀物,无细菌、支原体、病毒污染。
●血清的灭活(消除补体活性):56 ℃,30min
●血清的消毒:过滤除菌
幻灯片31
●抗生素的使用:
●在培养液配制后,培养液内常加适量抗生素,以抑制可能存在的细菌的生长。
●通常是青霉素和链霉素联合使用。培养基内青霉素、链霉素最终使用浓度为每毫升100
单位。
●庆大霉素:每毫升100单位——方便、广谱、稳定
幻灯片32
完全培养基的组成
●基础培养基 80%—95%
●血清 5%—20%
●碳酸氢钠 2.0 g/L
●青、链霉素各100单位/毫升
幻灯片33
培养基的配制
RPMI-1640培养粉 1袋
碳酸氢钠 2.0 g
青、链霉素各100单位/毫升
加三蒸水至 1000ml, 过滤除菌。
调节pH值至7.2
加血清(终浓度 10%)
幻灯片34
细胞传代方法
●根据细胞生长的特点,传代方法有3种。
● 1悬浮生长细胞传代
●离心法传代:离心(1000转/分)去上清,沉淀物加新培养液后再混匀传代。
●直接传代法:悬浮细胞沉淀在瓶壁时,将上清培养液去除l/2一2/3,然后
用吸管直接吹打形成细胞悬液再传代。
● 2 半悬浮生长细胞传代(HeLa细胞)
●此类细胞部分呈现贴壁生长现象,但贴壁不牢,可用直接吹打法使细胞从瓶
壁脱落下来,进行传代。
● 3 贴壁生长细胞传代
●采用酶消化法传代。常用的消化液有0.25%的胰蛋白酶液。
幻灯片35
贴壁生长细胞传代方法:
● 1 吸光培养瓶中的培养液
● 2 加入1-2 ml 0.25%的胰蛋白酶液(以消化液能覆盖整个瓶底为准)
●静置2-10 min(显微镜下动态监测)。
● 3 加入培养液。
● 4 用吸管吸取瓶内培养液,反复吹打瓶壁细胞,形成细胞悬液。
● 5 吸取1/10—1/40细胞悬液,接种于新的培养瓶内。
● 6 加适量新鲜培养液于接种了细胞悬液的新培养瓶内。
●7 将后者放入培养箱中培养。
幻灯片36
细胞计数
●血细胞计数器:手工计数细胞
●Coulter计数仪:人工计数
幻灯片37
幻灯片38
细胞培养无菌操作基本技术
无菌操作技术分为三个部分:
1.工作环境及表面的处理(紫外);
2.细胞培养所用玻璃及塑料制品的处理;
3.培养液与培养细胞的处理。
工作环境的处理
使用层流超净工作台是最经济有效的手段。超净工作台正常工作时,向下的气流可阻挡外界空气污染物进入超净台。
幻灯片39
(1)实验前,无菌室及无菌操作台用紫外灯照射20-30分钟灭菌,用70% 酒精擦拭无菌操作台面,并开启无菌操作台风机运转10分钟后,才可开始实验操作。每次操作只处理一株细胞,以免造成细胞交叉污染。
实验结束后,将实验物品带出工作台。如需要继续进行下一个实验,则用70% 酒精擦拭无菌操作台面,再让无菌操作台风机运转10分钟后,才可进行下一个实验操作。
幻灯片40
(2)无菌操作工作区域应保持清洁与宽敞,必要物品,如试管架、移液器或吸管头等可以暂时放置,其它实验用品用完后应及时移出,以利气体流通。实验用品要用70%酒精擦拭后才能带入无菌操作台内。实验操作应在操作台中央无菌区域内进行,勿在边缘非无菌区域操作。
(3)小心取出无菌实验用品,避免造成污染。切勿碰触吸管与吸头头部或容器瓶口,不要在打开的容器正上方操作实验。容器打开后,用手夾住瓶盖并握住瓶身,倾斜约45°角取用,尽量勿将瓶盖盖口朝上放在台面上。
幻灯片41
(4)工作人员应注意自身的安全,必须穿戴实验衣与手套后才进行实验。对于来自人源性或病毒感染的细胞株应特别小心,并选择适当等级的无菌操作台(至少两级)。小心有毒性
试剂,例如DMSO及TPA等,并避免尖锐物品伤人等。
(5)定期检查下列项目:CO2钢瓶内的CO2压力;CO2培养箱内的CO2浓度、温度、及水盘是否有污染;无菌操作台内气流压力是否正常,定期更换紫外灯管及HEPA过滤器滤膜,预滤网﹙300小时/预滤网,3000小时/HEPA)。
幻灯片42
细胞培养所用玻璃及塑料制品的清洗与消毒
清洗在组织细胞培养中,体外细胞对任何有害物质都非常敏感。若有微生物产品附带杂物,上次细胞残留物及非营养成分的化学物质,均能影响培养细胞的生长。因此对新使用玻璃器皿和重新使用的培养器皿都要严格彻底的清洗,且要根据器皿的组成材料不同,选择不同的清洗方法。
玻璃器皿的清洗组织细胞培养中,使用量最大的是玻璃器皿,故工作量最大的是玻璃器皿的清洗。一般玻璃器皿的清洗包括浸泡、刷洗、浸酸和冲洗四个步骤。清洗后的玻璃器皿不仅要求干净透明无油迹,而且不能残留任何物质。
幻灯片43
消毒细胞培养的最大危险是发生培养物的细菌,真菌和病毒等微生物的污染。污染主要是由于操作者的疏忽而引起,常见的原因有操作间或周围空间的不洁,培养器皿和培养液消毒不合格或不彻底。由于有关培养的每个环节的失误均能导致培养失败,故细胞培养的每个环节都应严格遵守操作常规,防止发生污染。
幻灯片44
消毒方法分为三类:物理灭菌法(紫外线、湿热、干烤、过滤等),化学灭菌法(各种化学消毒剂)和抗生素。
化学消毒法:最常见的是70%酒精及1‰的新洁而灭,前者主要用于操作者的皮肤,操作台表面及无菌室内的壁面处理。后者则主要用器械的浸泡及皮肤和操作室壁面的擦试消毒。化学消毒法操作简单、方便有效。
抗生素消毒:主要用于培养用液灭菌或预防培养物污染.
幻灯片45
常用玻璃器皿清洗
●浸泡(自来水)、刷洗(洗衣粉)、 50℃烘干、酸泡(24小时)、流水冲洗6-10遍、蒸
溜水浸泡和冲洗3-5次、50℃烘干,包扎后湿热灭菌,烘干。
幻灯片46
清洁液的配制
幻灯片47
细胞冻存和复苏
●细胞低温冷冻贮存是细胞室的常规工作。细胞冻存与细胞传代保存相比可以减少人力、
经费,减少污染,减少细胞生物学特性变化。
幻灯片48
冻存和复苏的原则:慢冻快融
●当细胞冷到零度以下,可以产生以下变化:细胞器脱水,细胞中可溶性物质浓度升高,
并在细胞内形成冰晶。
●如果缓慢冷冻,可使细胞逐步脱水,细胞内不致产生大的冰晶;相反结晶就大,大结
晶会造成细胞膜、细胞器的损伤和破裂。
●复苏过程应快融,目的是防止小冰晶形成大冰晶,即冰晶的重结晶。
幻灯片49
低温保护剂的应用
●在细胞冻存时加入低温保护剂,能大大提高冻存效果。
●常用的低温保护剂是DMSO,它是一种渗透性保护剂,可迅速透入细胞,提高胞膜对水
的通透性,降低冰点,延缓冻结过程,能使细胞内水分在冻结前透出细胞外,在胞外形成冰晶,减少胞内冰晶,从而减少冰晶对细胞的损伤。
幻灯片50
冷冻保存要点:
冷冻过程要缓慢。需要冷冻保存的细胞先在4℃冰箱中放置 30-60分钟;然后转入-20℃,放置30分钟;然后再转入-50℃放置2小时,最后放入液氮中长期保存。
有条件的地方,可用程控降温仪,按每分钟-1 到 -3℃速度降温,一直到-80℃以下,然后直接放入液氮中长期保存。
幻灯片51
细胞冻存方法
●1预先配制冻存液:含20%血清培养基
● 10% DMSO
● 2 取对数生长期细胞,经胰酶消化后,加入适量冻存液, 用吸管吹打制成细胞悬液(1
×106 ~ 5 ×106细胞/ml)
● 3 加入0.5 ~ 1ml细胞于冻存管中,密封后标记冷冻细胞名称和冷冻日期。
●DMSO液用培养液配好,避光保存。避免因临时配制产热而伤害细胞。
幻灯片52
细胞复苏方法
●(l)从液氮中取出冷冻管,迅速投入37~38 ℃水浴中,使其融化(1分钟左右)。
●(2)5分钟内用培养液稀释至原体积的10倍以上。
●(3)低速离心10分钟。
●(4)去上清,加新鲜培养液培养刚复苏的细胞。
幻灯片53
●要防止培养细胞污染需要注意以下几点:
1. 污染源大多来自换液和消化时的操作不正规,如果你在处理细胞的操作过程
中污染,即便你加入双抗也很难除去。所以你必须掌握好细胞处理过程或培养基配制过程中的无菌操作。
2. 霉菌污染占大多数,除了操作有关外,另一主要来源是培养箱。必须做到1-2周清
洗、消毒培养箱一次。铜的培养箱隔板比不锈钢好。
3.一次在操作台操作不要超过2小时,不要用一个吸管在不同培养瓶间操作。换液建
议用1ml移液枪,枪头盒在操作台最多放1周。
幻灯片54
本实验室内的细胞室管理:
●预约制度:每天提前在预约记录本上登记,写下作实验的时间,目的(冻存、复苏、
传代、药物处理)等,尽量估算好时间,以便别人好安排实验。若在登记时间晚30分钟还没有前来做实验,其他人可以先做。通过登记判断是否有人在做实验,以防突然开紫外灯,对在里面做实验的人造成伤害。
●用液氮罐需登记:记录液氮量,以便及时补充。
●卫生维护:每次做完实验及时清理。每周1次,彻底清洁包括超净工作台,培养箱,
工作台和地面。用强力碘,蒸馏水,酒精和次氯酸钠( 0.1-0.5% ),以及新洁尔灭溶
液( 0.1%)。
幻灯片55
●冷冻干燥机
●荧光倒置显微镜
●低速冷冻大容量离心机技术
