物质的量专题复习(基础梳理+典例精析)
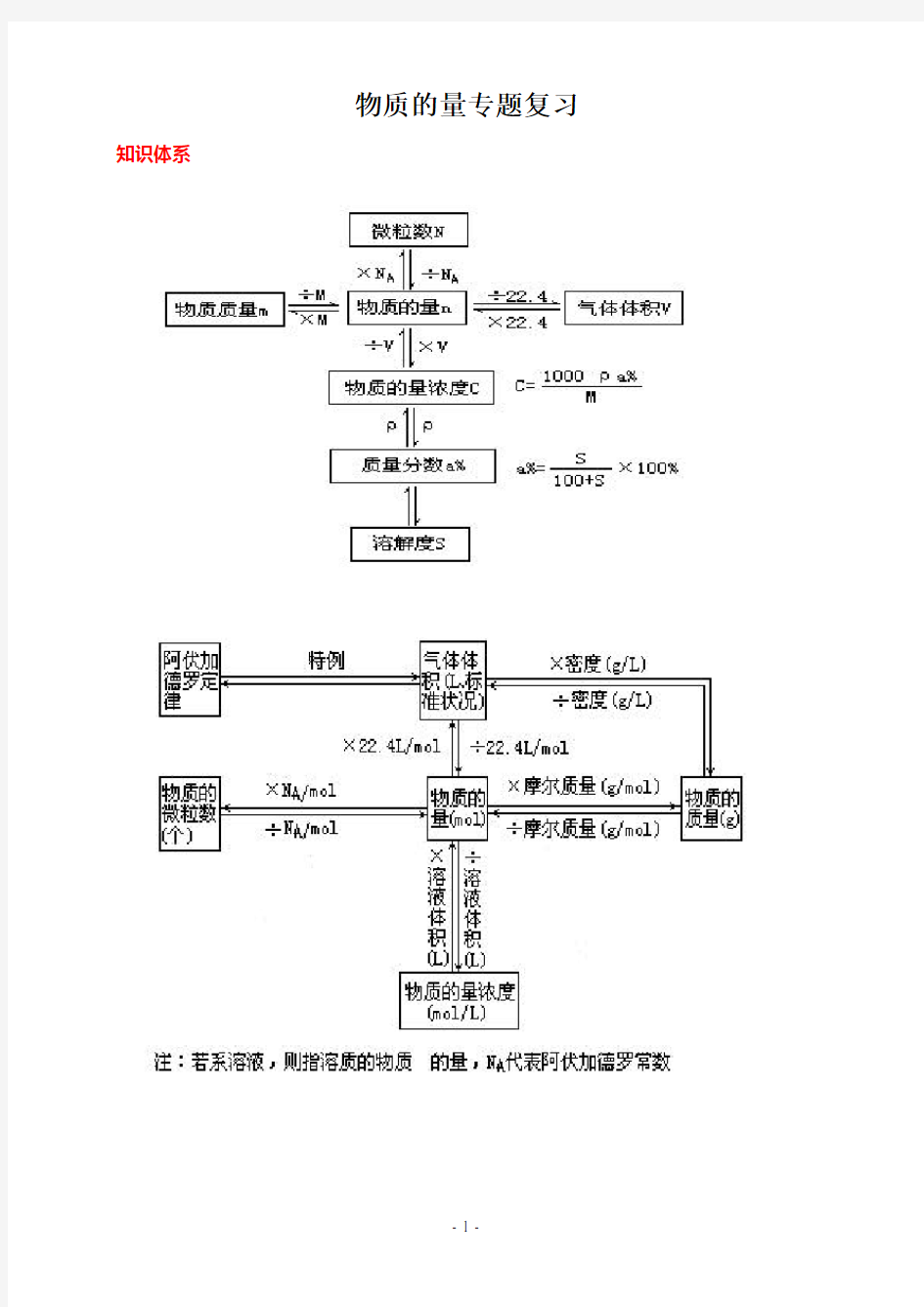

物质的量专题复习知识体系
基础梳理 一、 物质的量、阿伏加德罗常数、摩尔质量
1.物质的量
(1)物质的量是七个基本物理量之一,其意义是表示含有一定量数目的粒子的集体。符号为:n ,单位为:摩尔(mol )。
(2)物质的量的基准(N A ):以0.012kg 12C 所含的碳原子数即阿伏加德罗常数作为物质的量的
基准。阿伏加德罗常数可以表示为N A ,其近似值为6.02×1023 mol -1
2.摩尔质量(M )
1摩尔物质的质量,就是该物质的摩尔质量,单位是g/mol 。1mol 任何物质均含有阿伏加德罗常数个粒子,但由于不同粒子的质量不同,因此,1 mol 不同物质的质量也不同;12C 的相对原子质
量为12,而12 g 12C 所含的碳原子为阿伏加德罗常数,即1 mol 12C 的质量为12g 。同理可推出1 mol
其他物质的质量。
3.关系式:n =A N N
;n =M m
典例精析
【例1】下列关于物质的量的叙述中,错误的是( )
A.1 mol 任何物质都含有6.02×1023个分子
B.0.012 kg 12C 中含有约6.02×1023个碳原子
C.1 mol 水中含有2 mol 氢和1 mol 氧
D.1 mol Ne 含有6.02×1024个电子
解析:因为有些物质是由分子组成(例如水、硫酸等),有些物质是由离子组成(例如NaCl 、Ca(OH)2等),还有些物质是由原子直接构成的(例如金刚石等),所以A 的叙述是错误的。碳是由原子构成的,根据规定,0.012 kg 12C 中所含的碳原子数即为阿伏加德罗常数,其近似值为6.02×1023 mol -1,所以B 的叙述是对的。根据规定,“使用摩尔表示物质的量时,应该用化学式指明粒子的种类,而不使用该粒子的中文名称............
”。C 中表示水的组成时,却用名称表示,所以也是不正确的。氖原子核外有10个电子,则1 mol Ne 也应含有10×6.02×1023个电子,所以D 的叙述是正确的。
【例2】(2010福建卷)N A 表示阿伏伽德罗常数,下列判断正确的是( )
A .在18g 18O 2中含有N A 个氧原子
B .标准状况下,22.4L 空气含有N A 个单质分子
C .1 molCl 2参加反应转移电子数一定为2N A
D .含N A 个Na +的Na 2O 溶解于1L 水中,Na +的物质的量浓度为1mol/L
解析:本题考察阿弗加德罗常数的计算和判断
A 18182g O 正好是0.5mol ,一个氧分子正好含有两个氧原子,所以氧原子的物质的量为1mol ,
即为1A N
B 空气是混合物
C 在氯气与水的反应中,1molCl 2 就只转移1A N 的电子
D 所得溶液中含A N 个Na +,可得氢氧化钠的物质的量为1mol ,但这时候溶液不是1L ,所以物
质的量浓度不是1mol/L.
基础梳理 二、气体摩尔体积
1.定义:单位物质的量的气体所占的体积,叫做气体摩尔体积。
2.表示符号:Vm
3.单位:L/mol (或L ·mol -1)
4.标准状况下,气体摩尔体积约为22.4L/mol
5.数学表达式:气体的摩尔体积=气体的物质的量气体所占的体积
, 即n V V m =
6. 气体摩尔体积的一个特例就是标准状况下的气体摩尔体积(V0)。在标准状况下,1mol 任何气体的体积都约等于22.4 L 。在理解标准状况下的气体摩尔体积时,不能简单地认为“22.4 L 就是气体摩尔体积”,因为这个22.4 L 是有特定条件的。这些条件就是: ①标准状况,即0℃和101.325 kPa ,气体的物质的量为1 mol ,只有符合这些条件的气体的体积才约是22.4 L 。因此,22.4 L 是1 mol 任何气体在标准状况下的体积。 ②这里所说的标准状况指的是气体本身所处的状况,而不指其他外界条件的状况。例如,“1 mol H 2O(g)在标准状况下的体积为22.4 L ”是不正确的,因为在标准状况下,我们是无法得到气态水的。
③1mol 任何气体的体积若为22.4 L ,它所处的状况不一定就是标准状况。根据温度、压强对气体分子间平均距离的影响规律知,温度升高一倍或压强降低一半,分子间距将增大一倍;温度降低一半或压强增大一倍,分子间距将减小一半。由此可知,1 mol 任何气体在0℃ 、101 kPa 条件下的体积与273℃ 、202kPa 条件下的体积应相等,都约为22.4L 。
典例精析
【例】判断下列说法是否正确?并说明理由
1. 常温常压下,11.2L 氧气所含的原子数为N A
2. 在25℃,压强为1.01×105
Pa 时,11.2L 氮气所含的原子数目为N A
3.标准状况下的22.4L 辛烷完全燃烧,生成CO 2分子数为8N A
4.标准状况下,11.2L 四氯化碳所含分子数为0.5N A
5.标准状况下,1L 水所含分子数为(1/22.4)N A
6.标准状况下,11.2L SO 3中含1.5N A 个氧原子
解析:1、标准状况下,11.2L 氧气为0.5mol ,其所含原子数为N A 。而常温常压(25℃,1.01×105 Pa )
下,11.2L 氧气物质的量小于0.5mol ,其所含原子数必小于N A ,故叙述错误。
2、本题叙述错误,分析方法同上。
3、4、5题中的辛烷、四氯化碳、水在标准状况下均为液体,第6题中SO 3在标准状况下为固体。
故都不正确。
基础梳理三、阿伏加德罗定律及其推论
1.阿伏加德罗定律:
在同温同压下,同体积的气体含有相同的分子数。即:T1=T2;P1=P2 ;V1=V2 n1 = n2 2.阿伏加德罗定律的推论:
(1)三正比:
同温同压下,气体的体积比等于它们的物质的量之比.V1/V2=n1/n2
同温同体积下,气体的压强比等于它们的物质的量之比.p1/p2=n1/n2
同温同压下,气体的密度比等于它们的相对分子质量之比.M1/M2=ρ1/ρ2
(2)二反比:
同温同压下,相同质量的任何气体的体积与它们的相对分子质量成反
比.V1/V2=M2/M1同温同体积时,相同质量的任何气体的压强与它们的摩尔质量的
反比.p1/p2=M2/M1。
(3)一连比:
同温同压下,同体积的任何气体的质量比等于它们的相对分子质量之比,也等
于它们的密度之比。m1/m2=M1/M2=ρ1/ρ2
(注:以上用到的符号:ρ为密度,p为压强,n为物质的量,M为摩尔质量,m为质量,V为体积,T为温度;上述定律及其推论仅适用于气体,不适用于固体或液体。) 阿佛加德罗常数考点命题陷阱归类分析
阿佛加德罗常数(用N A表示)涉及的知识面广,灵活性强,是高考的热点之一,主要以选择题的形式(选择正确的或错误的)进行考查。分析近几年的高考试题,此类题型常以选择题形式出现,容易引起错误的有以下几点:
1、温度和压强:22.4L/mol是在标准状况(0 ℃,1.01×105Pa)下的气体摩尔体积。命题者有意在题目中设置非标准状况下的气体体积,让考生与22.4L/mol进行转换,从而误入陷阱。
2、物质状态:22.4L/mol使用的对象是气体(包括混合气体)。命题者常把一些容易忽视的液态或固态物质作为气体来命题,让考生落入陷阱。如SO3:常温下是固态;水:常温下是液态。戊烷,辛烷常温下是液态等。
3、物质变化:一些物质间的变化具有一定的隐蔽性,有时需要借助方程式分析才能挖掘出隐含的变化情况。考生若不注意挖掘隐含变化往往会误入陷阱。如NO2:存在与N2O4的平衡。
4、单质组成:气体单质的组成除常见的双原子分子外,还有单原子分子(如稀有气体Ne:单原子分子)、三原子分子(如O3)、四原子分子(如P4)等。考生如不注意这点,极容易误入陷阱。
5、粒子数目:粒子种类一般有分子、原子、离子、质子、中子、电子等。1mol微粒的数目即为阿佛加德罗常数,由此可计算分子、原子、离子、质子、中子、电子等微粒的数目。命题者往往通过N A与粒子数目的转换,巧设陷阱。。
典例精析
【例1】(2010上海卷,7)N A 表示阿伏加德罗常数,下列叙述正确的是 ( )
A .等物质的量的N 2和CO 所含分子数均为N A
B .1.7g H 2O 2中含有的电子数为0.9 N A
C .1mol Na 2O 2 固体中含离子总数为4 N A
D .标准状况下,2.24L 戊烷所含分子数为0.1 N A
解析:此题考查了阿伏伽德罗常数知识。阿伏伽德罗常数是指1mol 任何微粒中含有的微粒数,等物质的量不一定是1mol ,A 错;H 2O 2的相对分子质量为:34,故其1.7g 的物质的量为0.05mol ,
其每个分子中含有的电子为18个,则其1.7g 中含有的电子的物质的量为0.9mol ,数目为0.9N A ,B 对;Na 2O 2固体中,含有的是Na +和O 22-两种离子,1mol 固体中含有3mol 离子,故其中的离子总数为:
4 N A ,C 错;戊烷在标准状况下为液态,故其2.24L 不是0.1mol ,D 错。
易错警示:进行阿伏伽德罗常数的正误判断的主要考查点有:①判断一定量的物质所含的某种粒子数目的多少;②物质的组成;③通过阿伏加德罗常数进行一些量之间的换算等,在解题时要抓住其中的易错点,准确解答。
【例2】(2010江苏卷,5)设N A 为阿伏加德罗常数的值,下列叙述正确的是
A .常温下,1L0.1mol/L 的43NH NO 溶液中氮原子数为0.2N A
B .1mol 羟基中电子数为10N A
C .在反应中,每生成3mol 2I 转移的电子数为6N A
D .常温常压下,22.4L 乙烯中C H —键数为4N A
【解析】本题主要考查的是以阿伏伽德罗常数为载体考查如下知识点①考查22.4L/mol 的正确使用;②考查在氧化还原反应中得失电子数的计算等内容。A 项,无论4N H +水解与否,根据元素
守恒;B 项,1mol 羟基中有9A N 个电子;C 项,在该反应中,每生成3mol 2I ,转移5A N 个电子;
D 项,常温常压下,气体摩尔体积V m 不为22.4L/mol 。综上分析得知,本题选A 项。
【例3】(2010广东理综卷,8)设 N A 为阿伏加德罗常数的数值,下列说法正确的是( )
A.16g CH 4中含有4N A 个C-H 键
B.1mol ·L —1NaCl 溶液含有N A 个Na +
C.1mol Cu 和足量稀硝酸反应产生 N A 个NO 分子
D.常温常压下,22.4L CO 2中含有 N A 个CO 2分子
解析:每个4C H 中含有4个C-H 键,故16g 4C H (1mol )中含有4A n 个C-H 键
,A 正确;
没有告诉溶液的体积,无法知道N aC l 的物质的量,故B 错;
根据关系式,1mol Cu~2mol NO ,故C 错;
常温常压下,22.4L 2C O 不是1mol 。
答案:A
基础梳理
四、 混合气体的平均摩尔质量
1.已知混合物质的总质量m(混)和总物质的量n(混):M (混)=混)
混()(n m
2.已知混合物各成分的摩尔质量和在混合体系内的物质的量分数或体积分数。
M(混)=M 1×n 1%+M 2×n 2%+……=M 1×V 1%+M 2×V 2%+……
3.已知标准状况下混合气体的密度:M (混)=22.4ρ(混)
4.已知同温同压下与单一气体A 的相对密度:)
混A M M ()(=)()(A ρρ混 典例精析
【例】(山东)已知NH 4HCO 3
NH 3+H 2O+CO 2↑,则150℃时NH 4HCO 3分解产生的混合气体A 的密度是相同条件下H 2密度的 倍。 A.26.3 B.13.2 C.19.8
D.无法计算 [解析]假设NH 4HCO 3为1 mol ,则其质量为79 g ,完全分解产生的气体为3 mol ,故有:M 混合气体=79g/3mol =26.3g/mol ;又由“相同条件下,气体的密度比等于其摩尔质量比”,故混合气体A 的密度是相同条件下H 2密度的26.3/2 = 13.2倍。
[答案]B
基础梳理
五、 物质的量浓度
1.定义:以1L 溶液里所含溶质B 的物质的量来表示溶液的浓度叫做物质的量浓度.符号为:c B ;单位为: mol ﹒L -1
2.表达式:c B =V n (n 为溶质B 的物质的量,单位为mol ;V 为溶液的体积,单位为L)
3.难点提示
①理解物质的量浓度的物理意义和相关的量。
物质的量浓度是表示溶液组成的物理量,衡量标准是单位体积溶液里所含溶质的物质的量的多少。这里的溶质可以是单质、化合物,也可以是离子或其他的特定组合,单位是mol ;体积指溶液的体积而不是溶剂的体积,单位是L ;因此,物质的量浓度的单位是mol ·L -1。
②明确溶液中溶质的化学成分。
求物质的量浓度时,对一些特殊情况下溶液的溶质要掌握清楚,如NH 3溶于水得NH 3·H 2O ,但我们习惯上认为氨水的溶质为NH 3;SO 3溶于水后所得溶液的溶质为H 2SO 4;Na 、Na 2O 、Na 2O 2溶于水后所得溶液的溶质为NaOH ;CuSO 4·5H 2O 溶于水后所得溶液溶质
为CuSO 4
③熟悉表示溶液组成的其他物理量。
表示溶液组成的物理量除物质的量浓度外,还有溶质的质量分数、质量物质的量浓度等。它们之间有区别也有一定的联系,如物质的量浓度(c )与溶质的质量分数(ω)的关系为c=ρg ·mL -1×1000mL ·L -1×ω/Mg ·mol -1。
4、溶液的稀释或混合
溶液加水稀释前后溶质的物质的量不变。
溶质的物质的量=物质的量浓度(mol /L)×溶液体积数(L)
通常溶液稀释的表达式为:
c 1V 1=c 2V 2(c —物质的量浓度,V —溶液体积)
对于两种浓度不同的溶液相混合,体积会改变,计算体积应先求出溶液的质量,通过密度换算成溶液的体积。只有当两种溶液浓度很稀时,或浓度接近时,体积变化可忽略不计,近似用
V 混=V 1+V 2计算。
5、物质的量浓度与溶质的质量分数换算
若用c 表示物质的量浓度,ρ表示溶液密度,a %表示溶质质量分数,M 表示溶质的摩尔质量,则有下列换算式:
)/(%
1000)(1)
/()
/(1000)/(3
3L mol M a L mol g M cm g cm L mol c ?=?=ρρ; %1001000%?=ρcM
a
典例精析
【例】(2010四川理综卷,12)标准状况下VL 氨气溶解在1L 水中(水的密度近似为1g/ml ),所得溶液的密度为p g/ml,质量分数为ω,物质浓度为c mol/L ,则下列关系中不正确...
的是 A.()()1722400/22.422.4p V V =++ B. ()17/1000W c ρ=
C. ()17/1722400W V V =+
D.C=1000V ρ/(17V+22400)
解析:本题考查基本概念。考生只要对基本概念熟悉,严格按照基本概念来做,弄清质量分数与物质的量浓度及密度等之间的转化关系即可。
基础梳理
六、一定物质的量浓度溶液的配制
1.仪器:天平(量筒或滴定管、移液管)、烧杯、玻璃棒、容量瓶、胶头滴管,(药匙) 容量瓶的使用要注意以下事项:
①容量瓶为细颈磨口梨形平底瓶,带有与磨口吻合的玻璃塞(长脖子、大肚子、平底子、 带盖子)
②容量瓶上标有刻度线、体积和使用温度(一般为20℃)
③规格有1000mL、500mL、250mL、100mL、50mL等多种,每一规格容量瓶只能配制瓶上既定容积的溶液,如50mL容量瓶只能配制50.00mL溶液
④容量瓶不可以用来长期存放溶液,不能加热,更不能用来做反应容器。
⑤容量瓶使用之前一定要检查瓶塞是否漏水
2.物质的量浓度溶液的配制步骤:
以配制250ml 1mol/L的氢氧化钠溶液为例
①计算——配制250mL 1mol/L的氢氧化钠溶液需要氢氧化钠的质量为计算所需溶质的量为:250×10-3L×1mol/L×40g/mol=10.0g
②称量——用小烧杯或称量瓶盛装NaOH固体,用托盘天平称量,(液体用量筒或滴定管、移液管移取)。因NaOH固体易潮解,且有腐蚀性,必须用带盖的称量瓶或小烧杯快速称量,称量过程中时间越长,吸水越多,误差越大,若直接在纸上称NaOH,则有损失且易腐蚀托盘。
③溶解或稀释——在烧杯中加适量的蒸馏水(加水不要过量),用玻璃棒搅拌使之溶解。
④冷却——将溶解所得溶液冷却至室温
⑤转移——把烧杯内液体用玻璃棒引流转入250mL容量瓶
⑥洗涤——洗涤烧杯和玻璃棒2~3次,将洗涤液一并移入容量瓶,振荡摇匀
⑦定容——向容量瓶中注入蒸馏水至距离刻度线1~2 cm处改用胶头滴管滴蒸馏水至溶液凹液面与刻度线正好相切。
⑧摇匀——盖好瓶塞,用食指顶住瓶塞,用另一只手托住瓶底,手心空出,反复上下颠倒,摇匀
⑨装瓶——将配好的溶液装入干净的试剂瓶中,贴上标签,注明名称(NaOH)、浓度
(1mol/L)。
3. 在配制物质的量浓度的溶液时,按操作顺序来讲,需注意以下几点:
1).计算所用溶质的多少时,以下问题要弄清楚:
①溶质为固体时,分两种情况:溶质是无水固体时,直接用c B=n(mol)/V(L)=[m(g)/ M(g·mol–1)]/V(L)公式算m;溶质是含结晶水的固体时,则还需将无水固体的质量转化为结晶水合物的质量。
②溶质为浓溶液时,也分两种情况:如果给定的是浓溶液的物质的量浓度,则根据公式c(浓)×V(浓)=c(稀)×V(稀)来求V(稀);如果给定的是浓溶液的密度(ρ)和溶质的质量分数(ω),则根据c=[ρg·mL-1×V’(mL)×ω/Mg·mol-1]/V(mL)来求V’(mL)。
③所配溶液的体积与容量瓶的量程不符时:算溶质时则取与实际体积最接近的量程数据做溶液的体积来求溶质的多少,不能用实际量。如:实验室需配制480mL1moL·L-1的NaOH溶液,需取固体NaOH的质量应为20.0g,而不是19.2g;因为容量瓶只能配制其规定量程体积的溶液,要配制符合要求的溶液时,选取的容量瓶只能是500 mL量程的容量瓶。故只能先配制500 mL溶液,然后再取出480mL。
2)称、量溶质时,一要注意所测数据的有效性(即精度)。二要选择恰当的量器,称
量易潮解的物质如NaOH时,应用带盖的称量瓶(或小烧杯)快速称量;量取液体时,量器的量程与实际体积数据相差不能过大,否则易产生较大误差。
3)容量瓶使用前要用蒸馏水洗涤2~3次;溶解或稀释溶质后要冷却溶液至室温;定容、摇匀时,不能用手掌贴住瓶体,以免引起体积的变化;摇匀后,如果液面降到刻度线下,不能向容量瓶中再加蒸馏水了,因为瓶塞、瓶口是磨口的,有少量溶液残留。
4)定容时如果液面超过了刻度线或摇匀时洒出少量溶液,均须重新配制。
4.误差分析:
A.误差分析原理:c=n/V;
①V不变时,操作使n偏大,则c偏高;反之,偏低。
②.n不变时,操作使V偏大,则c偏低;反之,偏高。
B.实验过程中的误操作对实验结果的影响:
(1)使所配溶液的物质的量浓度偏高的主要原因:
①天平的砝码沾有其他物质或已锈蚀。使所称溶质质量偏高,物质的量浓度偏大
②调整天平零点时,没调平,指针向左偏转(同①)。
③用量筒量取液体时仰视读数(使所取液体体积偏大)。
④把量筒中残留的液体用蒸馏水洗出倒入烧杯中(使所量液体体积偏大)。
⑤把高于20℃的液体转移进容量瓶中(所量液体体积小于容量瓶所标液体体积)
⑥定容时,俯视容量瓶刻度线(使液体体积偏小)。
(2)使所配溶液的物质的量浓度偏低的主要原因:
①称量时,物码倒置,并动用游码(使所称溶质的质量偏低,物质的量偏小)。
②调整天平零点时,没调平,指针向右偏转(同①)。
③用量筒量取液体时俯视读数(使所取液体体积偏小)。
④没洗涤烧杯和玻璃棒或洗涤液没移入容量瓶中(使溶质的物质的量减少)。
⑤定容时,仰视容量瓶刻度线(使溶液体积偏大)。
⑥定容加水时,不慎超过了刻度线,又将超出部分吸出(使溶质物质的量减少)(3)对实验结果无影响的操作
①使用蒸馏水洗涤后未干燥的小烧杯溶解溶质。
②配溶液用的容量瓶用蒸馏水洗涤后未经干燥。
典例精析
【例】(高考题改编)甲乙两位同学分别用不同的方法配制100mL 3.6mol/L的稀硫酸。
(1)若采用18mol/L的浓硫酸配制溶液,需要用到浓硫酸的体积为。(2)甲学生:量取浓硫酸,小心地倒入盛有少量水的烧杯中,搅拌均匀,待冷却至室温后转移到100 mL 容量瓶中,用少量的水将烧杯等仪器洗涤2~3次,每次洗涤液也转移到容量瓶中,然后小心地向容量瓶加入水至刻度线定容,塞好瓶塞,反复上下颠倒摇匀。
①将溶液转移到容量瓶中的正确操作是。
②洗涤操作中,将洗涤烧杯后的洗液也注入容量瓶,其目的是__ _______。
③定容的正确操作是。
④用胶头滴管往容量瓶中加水时,不小心液面超过了刻度,处理的方法是________(填序号)。
A.吸出多余液体,使凹液面与刻度线相切
B.小心加热容量瓶,经蒸发后,使凹液面与刻度线相切
C.经计算加入一定量的浓盐酸
D.重新配制
(3)乙学生:用100 mL 量筒量取浓硫酸,并向其中小心地加入少量水,搅拌均匀,待冷却至室温后,再加入水至100 mL 刻度线,再搅拌均匀。你认为此法是否正确?若不正确,指出其中错误之处。
[答案](1)20.0mL (2)①将玻璃棒插入容量瓶刻度线以下,使溶液沿玻璃棒慢慢地注入容量瓶中;②使溶质完全转移到容量瓶中;③ 加水至离刻度线1~2cm时,改用胶头滴管滴加水至凹液面与刻度线相切;④ D;
(3)不能用量筒配制溶液,不能将水加入到浓硫酸中。
知识讲解_物质的量(基础)
物质的量 编稿:房鑫审稿:曹玉婷 【学习目标】 1.了解物质的量的单位——摩尔。 2.掌握物质的量、物质的质量、微粒数目、标准状况下气体体积之间的关系。 【要点梳理】 要点一、物质的量及其单位(摩尔) 【高清课堂:物质的量】 化学实验中,取用的药品无论是单质还是化合物,都是可以用器具称量的。而物质间发生的化学反应是原子、离子或分子之间按一定的数目关系进行的,对此,不仅我们用肉眼直接看不到,也难以称量。国际科学家建议用“物质的量”将一定数目的原子、离子或分子等微观粒子与可称量物质联系起来,所以物质的量是联系宏观物质与微观粒子的一种物理量。1、物质的量的定义及单位: 物质的量通常是表示物质所含微观粒子数目多少的物理量,符号通常为n。单位:“摩尔”简称“摩”,符号mol。 要点诠释: “物质的量”四个字是一个整体,不可分割或插入其他字。它不具有字面含义,不能望文生义。将其理解为“物质的质量”或“物质的数量”,这些都是错误的。 2、物质的量的对象: 物质的量的计量对象是构成物质的微观粒子(如分子、原子、离子、电子、质子、中子等)或某些微观粒子的特定组合(如NaCl可看成Na+、Cl—的微粒组合,每摩尔NaCl晶体含1 mol Na+和1 mol Cl-。)等。因此在使用物质的量这一物理量时必须指明微粒的种类。例如:如1 mol H表示1摩尔氢原子,1 mol H2表示1摩尔氢分子,1 mol H+表示1摩尔氢离子。不能笼统地称1 mol氢,应该说1 mol氢原子(或分子或离子)。 物质的量不可用于计量宏观物质。如“1 mol铁钉”、“1 mol牛”等说法都是错误的。 3、国际单位制中的基本物理量: 物质的量表示含有一定数目粒子的集合体。物质的量(符号为n),是国际单位制中的七个基本物理量之一,其单位为摩尔(符号为mol)。它与国际单位制中的其他六个基本物理量呈并列关系。“物质的量”与“摩尔”的关系,就像“长度”与“米”、“质量”与“千克”、“时间”与“秒”的关系一样,是基本物理量与其单位名称的关系。 要点二、阿伏加德罗常数
2020年高考化学一轮必刷好题专题2:物质的量浓度含答案
2020年高考化学一轮必刷好题专题02:物质的量浓度 1.(2019天津)下列实验操作或装置能达到目的的是() A B C D NO气体证明乙炔可使溴水褪色 混合浓硫酸和乙醇配制一定浓度的溶液收集2 【答案】B 【解析】A、乙醇的密度小于浓硫酸,混合时应将浓硫酸沿烧杯壁倒入乙醇中,边倒边搅拌,若顺序相反则容易引起液体飞溅,故A不能达到目的;B、容量瓶上的刻度与凹液面的最低处相切,胶头滴管垂直位于容量瓶的正上方,故B能达到目的;C、二氧化氮的密度大于空气,集气瓶中的导气管应长进短出,故C不能达到目的;D、乙炔中的H2S等杂质也能使溴水褪色,应先通过一个盛碱液的洗气瓶将杂质除去,故D不能达到目的。 2.(2019北京)化学小组用如下方法测定经处理后的废水中苯酚的含量(废水中不含干扰测定的物质)。Ⅰ.用已准确称量的KBrO3固体配制一定体积的a mol·L?1 KBrO3标准溶液; Ⅱ.取v1 mL上述溶液,加入过量KBr,加H2SO4酸化,溶液颜色呈棕黄色; Ⅲ.向Ⅱ所得溶液中加入v2 mL废水; Ⅳ.向Ⅲ中加入过量KI; Ⅴ.用b mol·L?1 Na2S2O3标准溶液滴定Ⅳ中溶液至浅黄色时,滴加2滴淀粉溶液,继续滴定至终点,共消耗Na2S2O3溶液v2 mL。 已知:I2+2Na2S2O3=2NaI+ Na2S4O6 Na2S2O3和Na2S4O6溶液颜色均为无色 (1)Ⅰ中配制溶液用到的玻璃仪器有烧杯、玻璃棒、胶头滴管和____________。 【答案】(1). 容量瓶、量筒 【解析】(1)准确称量KBrO3固体配置溶液所需的玻璃仪器有烧杯、量筒、玻璃棒、胶头滴管,一定规格的容量瓶,因而该空填容量瓶、量筒; 3.(2018课标Ⅱ)下列实验过程可以达到实验目的的是
高中化学物质的量浓度及有关计算
物质的量浓度及有关计算 教学目标 知识技能:理解有关物质的量浓度的涵义,掌握有关计算的基本题型。 能力培养:有关物质的量浓度的计算思维能力。 科学思想:在溶液计算中,贯彻守恒的思想。 科学方法:演绎推理法,比较分析法。 重点、难点有关物质的量浓度计算的6种基本类型是重点;电荷守恒、建立参比的基本解题方法是难点。 教学过程设计 教师活动 【引入】今天我们复习物质的量浓度。 【提问】物质的量浓度的定义是什么?请写出它的计算公式。 学生活动 回答:1L溶液中含有溶质的物质的量。 板书:c=n(mol)/V(L) 【再问】溶液的组成还常用什么来表示? 回答:也常用溶质的质量分数来表示。 溶质的质量分数表示单位质量溶液中所含溶质的质量。 板书:a%=m(溶质)/m(溶液)×100%
【提问】根据物质的量浓度的计算公式c=n/V,我们能够联想起哪些有关的计算思想?请同学们讨论后回答。 思考,讨论,回答: (1)在公式计算中,已知任何两个量,可以求得第三个量。 (2)还可以根据物质的量联系溶质的质量、气体溶质在标准状况下的体积及微粒数目等。 (3)当溶质的量一定时,浓度和体积成反比;当体积一定时,浓度和溶质的物质的量成正比。 (4)根据n=cV,当取出一定浓度的溶液时,溶液的浓度不变,但溶质的物质的量和所取溶液的体积成正比。 【评价】同学们说的都很正确,不过,有一个问题,为什么当取出一定浓度的溶液时,溶液的浓度不变? 回答:溶液是均匀稳定的体系。 【板书】类型1 代入公式的计算 【投影】填空: 思考,完成练习。
【强调】体积必须以升(L)为单位进行计算。如果题目给的体积为mL,则必须进行换算。 【提问】为什么醋酸的[H+]小于其酸的浓度? 回答:醋酸为弱酸,[H+]=ca, 因此,[H+]小于酸的浓度。 【板书】类型2 溶液物质的量浓度和溶质质量分数的换算 【提问】在进行换算时,根据那个不变的量来推导计算公式?请写出计算公式? 回答:溶液中溶质的量是不变的,分别用物质的量浓度和溶质的质量分数计算,于是得到如下方程: m=cVM=1000Vρa % 【强调】在此公式中,物质的量浓度(c)、溶质的质量分数(a%)、溶质的摩尔质量(M)和溶液密度(ρ),已知任何三个量,可计算第四个量。 【投影】练习:63%硝酸溶液的物质的量浓度为14 mol· L-1,溶液的密度为______。 思考,完成练习。 答案:1.4 g·mL-1 【板书】类型3 稀释问题 【提问】溶液在加水稀释过程中,不变的量和变化的量是什么?计算的依据是什么?
物质的量的相关基础计算
以物质的量为中心的计算 【知识网络】 一、网络构建 1. 基本概念和重要定律 ?????????????????????????????? ?????????????????????????????????--------式及进行计算的依据此定律是书写化学方程相同各种原子的种类及个数或反应前后的质量总和总和等于反应后生成物参加反应的各物质质量 质量守恒定律气体摩尔体积特例同体积同压同温使用条件气体使用范围注意含有相同数目的分子相同体积的任何气体都在相同的温度和压强下阿伏加德罗定律律定要重或常用的单位为其符号为的物质的量浓度叫做溶质组成的物理量的物质的量来表示溶液溶质以单位体积溶液里所含物质的量浓度分子质量相等原子质量或相对在数值上与该粒子相对摩尔质量以克为单位时或单位为其符号为量具有的质量叫做摩尔质单位物质的量的物质所摩尔质量单位为其符号为积的体积叫做气体摩尔体单位物质的量气体所占气体摩尔体积这个近似值通常使用新测定数据为 最其符号为阿伏加德罗常数任何粒子的粒子数叫做阿伏加德罗常数合中子以及它们的特定组质子电子离子原子这里的粒子指分子原子数相同中所含的碳任何粒子的粒子数与符号为简称摩其单位是摩尔 物质的量的符号为有一定数目粒子的集体物质的量实际上表示含物质的量念概关有律定其及量计用常).(::)3(;,,:)2(;:)1(.,:),(,,:)5(,.,,:)4(,.,:)3(1002.6,100221367.6,,1:)2(,,,,,.012.01.,,,.:)1(311113112312312m m ol L m ol B c B B m ol kg m ol g M m ol m m ol L V m ol m ol N m ol C kg m ol m ol n m A 二.关于阿伏加德罗常数的理解与综合应用 阿伏加德罗常数问题主要有: (1)一定质量的物质中所含原子数、电子数,其中考查较多的是H 2O 、N 2、O 2、H 2、NH 3、P 4 等。 (2)一定体积的物质中所含原子数、分子数,考的物质有Cl 2、NH 3、CH 4、O 2、N 2、CCl 4等 (3)一定量的物质在化学反应中的电子转移数目,曾考过的有Na 、Mg 、Cu 等。 三.物质的量在化学计算中的典型应用 c 、ω%、ρ之间的计算关系 (1)计算关系:M c %1000ρω= (2)使用范围:同一种溶液的质量分数与物质的量浓度之间的换算 (3)推断方法:①根据物质的量浓度的定义表达式 ②溶质的物质的量用M V M m n ρ?== 计算 ③注意溶液体积的单位 四.有关气体定律的计算 (1)气体摩尔体积的计算
物质的量知识点小结
物质的量知识点小结(一) 有关概念: 1、物质的量(n) ①物质的量是国际单位制中七个基本物理量之一。 ②用物质的量可以衡量组成该物质的基本单元(即微观粒子群)的数目的多少,它的单位是摩尔,即一个微观粒子群为1摩尔。 ③摩尔是物质的量的单位。摩尔是国际单位制中七个基本单位之一,它的符号是mol。 ④“物质的量”是以摩尔为单位来计量物质所含结构微粒数的物理量。 ⑤摩尔的量度对象是构成物质的基本微粒(如分子、原子、离子、质子、中子、电子等)或它们的特定组合。如1molCaCl2可以说含1molCa2+,2molCl-或3mol阴阳离子,或含54mol质子,54mol电子。摩尔不能量度宏观物质,如果说“1mol氢”就违反了使用准则,因为氢是元素名称,不是微粒名称,也不是微粒的符号或化学式。 ⑥使用摩尔时必须指明物质微粒的名称或符号或化学式或符号的特定组合。 2.阿伏加德罗常数(N A): ①定义值(标准):以0.012kg(即12克)碳-12原子的数目为标准;1摩任何物质的指定微粒所含的指定微粒数目都是阿伏加德罗常数个。 ②近似值(测定值):经过科学测定,阿伏加德罗常数的近似值一般取6.02×1023,单位是mol-1,用符号N A表示。 3.摩尔质量(M): ①定义:1mol某微粒的质量 ②定义公式:, ③摩尔质量的单位:克/摩。 ④数值:某物质的摩尔质量在数值上等于该物质的原子量、分子量或化学式式量。⑤注意:摩尔质量 有单位,是克/摩,而原子量、分子量或化学式的式量无单位。 物质的量练习题(一) 一、选择题(每小题1~2个正确答案) 1、下列关于摩尔质量的说法正确的是 A、氯气的摩尔质量是71克 B、氯化氢的摩尔质量为36.5 g/moL C、1摩氢气的质量为2克 D、O2的摩尔质量为16g/moL。 2、对于相同质量的二氧化硫和三氧化硫来说,下列关系正确的是 A、含氧原子的个数比为2∶3 B、含硫元素的质量比是5∶4 C、含氧元素的质量比为5∶6 D、含硫原子的个数比为1∶1 3、1克氯气含有n个Cl2分子,则阿佛加德罗常数可表示为 A、71n B、(1/71)n C、35.5n D、(1/35.5).n 4、将a g氯化钾溶于1.8L水中,恰使K+离子数与水分子数之比为1∶100,则a值为 A.0.745 B.0.39 C.39 D.74.5 5、在一定体积的容器中加入1.5mol氙气(Xe)和7.5mol氟气,于400℃和2633kPa压强下加热数 小时,然后迅速冷却至25℃,容器内除得到一种无色晶体外,还余下4.5mol氟气,则所得无色
高考化学专题:物质的量浓度计算
高考化学专题:物质的量浓度计算 1. 下图是某同学用500 mL 容量瓶配制0.10 mol·L - 1 NaOH 溶液的过程: 该同学的错误步骤有 ( ) A .1处 B .2处 C .3处 D .4处 2. 若20 g 密度为ρ g·cm - 3的Ca(NO 3)2溶液中含有2 g Ca(NO 3)2,则溶液中NO - 3的物质的量浓度为 ( ) A.ρ400 mol·L - 1 B.20ρ mol·L -1 C. 50ρ41 mol·L - 1 D. 25ρ41 mol·L - 1 3. 只给出下列甲和乙中对应的量,不能求出物质的量的是 ( ) A B C D 甲 物质的粒子数 标准状况下的气体摩尔体积 固体的体积 溶液中溶质的物质的量浓度 乙 阿伏加德罗常数 标准状况下的气体体积 固体的密度 溶液的体积 好使反应后的溶液呈中性,则下列叙述错误的是 ( ) A .溶液中c (Na + )=2c (SO 2- 4) B.a 2 mol >沉淀的物质的量>0 C .沉淀的物质的量=a 2 mol D .原浓硫酸中H 2SO 4的物质的量>a 2 mol 5. 3 g 镁铝合金与100 mL 稀硫酸恰好完全反应,将反应后的溶液加热蒸干,得到无水硫酸盐17.4 g ,则 原硫酸的物质的量浓度为 ( ) A .1 mol·L - 1 B .1.5 mol·L - 1 C . 2 mol·L -1 D .2.5 mol·L - 1
6.等质量的CuO和MgO粉末分别溶于相同体积的硝酸中完全溶解,得到的Cu(NO3)2和Mg(NO3)2溶液的浓度分别为a mol·L-1和b mol·L-1,则a与b的关系为() A.a=b B.a=2b C.2a=b D.a=5b 7.300 mL Al2(SO4)3溶液中,含Al3+为1.62 g,在该溶液中加入0.1 mol·L-1 Ba(OH)2溶液300 mL,反应后溶液中SO2-4的物质的量浓度为() A.0.4 mol·L-1B.0.3 mol·L-1 C.0.2 mol·L-1D.0.1 mol·L-1 8.在标准状况下,将a L NH3完全溶于水得到V mL氨水,溶液的密度为ρ g·cm-3,溶质的质量分数为w,溶质的物质的量浓度为c mol·L-1。下列叙述中正确的是() ①w= 35a 22.4Vρ×100%②c= 1 000a 22.4V③若上述溶液中再加入V mL水后,所得溶液的质量分数大于 0.5w④若上述溶液中再加入0.5V mL同浓度稀盐酸,充分反应后溶液中离子浓度大小关系为 c(NH+4)>c(Cl-)>c(OH-)>c(H+) A.①④B.②③C.①③D.②④ 9.右图是NaCl、MgSO4的溶解度曲线。下列说法正确的是() A.只有在t1℃时,NaCl和MgSO4的溶解度才相等 B.t1~t2℃,MgSO4的溶解度随温度升高而减小 C.在t2℃时,MgSO4饱和溶液的溶质质量分数最大 D.把MgSO4饱和溶液的温度从t3℃降至t2℃时,有晶体析 出 10.36.5 g HCl溶解在1 L水中(水的密度近似为1 g·mL-1),所得溶液的密度为ρ g·mL-1,质量分数为W,物质的量浓度为c mol·L-1,N A表示阿伏加德罗常数,则下列叙述中正确的是 () A.所得溶液的物质的量浓度:c=1 mol·L-1 B.所得溶液中含有N A个HCl分子 C.36.5 g HCl气体占有的体积为22.4 L D.所得溶液的质量分数:W=36.5 c/(1 000ρ) 11.试回答下列问题。 (1)已知24 g A和40 g B恰好完全反应生成0.4 mol C和32 g D,则C的摩尔质量为________。 (2)把1 mol Na和1 mol Mg分别投入到等量且过量的盐酸中,分别得到溶液a和b,则溶液a和b的 质量关系为m a________m b。 (3)如图为实验室某浓盐酸试剂瓶的标签上的有关数据,试根据标签上的有关数据回答下列问题: 盐酸 分子式:HCl 相对分子质量:36.5
高中化学 物质的量浓度计算练习题
物质的量浓度计算 一、选择题(每小题有一个或两个正确选项符合题意) 1、标准状况下,a L HCl气体溶于1000g水中,得到的盐酸的密度为bg·cm—3,则该盐酸的物质的量浓度为 A、a / 22.4摩·升—1 B、ab / 22.4摩·升—1 C、ab / (22400 + 36.5a )摩·升—1 D、1000ab / (22400 + 36.5a )摩·升—1 2、 100毫升0.3摩·升—1的硫酸钠溶液和50毫升0.2摩·升—1的硫酸铝溶液混合后,溶液中硫酸根的物质的量浓度为 A、0.20摩·升—1 B、0.25摩·升—1 C、0.40摩·升—1 D、0.50摩·升—1 3、密度为d g·cm—3的溶液V毫升,含有式量为M的溶质mg,其物质的量浓度为c摩·升—1,质量分数为W%,下列表示式不正确的是 A、c = 1000m / VM B、m=dV W/100 C、d= cM/10W D、W%= (cM/1000d)% 4、 VmLAl2(SO4)3溶液中含有a g Al3+,取出V/4 mL溶液,加水稀释到4V mL,则稀释后溶液中SO42—的物质的量浓度为 A、125 a / 9V摩·升—1 B、125 a / 18V摩·升—1 C、125 a / 36V摩·升—1 D、125 a / 54V摩·升—1 5、 0.5L 1摩·升—1FeCl3溶液与0.2 L 1摩·升—1的KC1溶液中,Cl—的浓度比为 A、15:2 B、1:1 C、3:1 D、1:3 6、有一未知浓度的硫酸溶液25mL,在加入0.5摩·升—1的Ba (NO3)2溶液25mL后,改加NaOH 溶液,结果用去1.0摩·升—1NaOH溶液50mL恰好完全反应,则硫酸的物质的量浓度为 A、0.5摩·升—1 B、1.0摩·升—1 C、1.5摩·升—1 D、2.0摩·升—1 7、实验室里需用480mL0.1摩·升—1的硫酸铜溶液,现选取容量瓶进行配制,以下操作正确的是 A、称取7.68g无水硫酸铜,加入500毫升水 B、称取12.0g胆矾配成500毫升溶液 C、称取8.0g无水硫酸铜,加入500毫升水 D、称取12.5g胆矾配成500毫升溶液 8、已知25%的氨水的密度为0.91 g·cm—3,5%氨水的密度为0.98 g·cm—3,若将上述两溶液等体积混合,所得氨水的溶液的质量分数为 A、等于15% B、大于15% C、小于15% D、无法确定 二、填空题 9、某温度下,22%的硝酸钠溶液150毫升,加100克水稀释后浓度为14%,原溶液的物质的量浓度为
高一化学物质的量基础练习题及答案
物质的量热身题 一、[判断正误] 1、摩尔是七个物理量之一() 2、摩尔是物质的质量单位() 3、摩尔是物质的数量单位() 4、1摩尔小麦含有6.02 ×1023个麦粒() 5、3mol氢() 6、4.5molNH3( ) 7.摩尔是国际科学界建议采用的一种物理量( ) 8.摩尔是物质的量的单位,简称摩,符号为mol( ) 9.我们把含有约6.02×1023个粒子的任何粒子的集体计量为1摩尔( ) 10.1mol氧含6.02×1023个O2( ) 二、计算 1、某物质中含有6.02×1022个Na+,则Na+物质的量为多少? 2、2.5molO2多少个O原子? 3、已知1mol Al 所含Al原子的个数为阿佛伽德罗常数,那么0.5mol Al 所含Al原子的个数为,2mol Al 所含Al原子的个数为。 4、9.03×1023个H2O的物质的量为.所含H的物质的量为.所含氧原子的物质的量为. 三、填空 1、1.5molH2SO4的物质的量为_____,所含H+的物质的量为____________. 硫酸根离子的物质的量为__________,所含硫酸分子的数目为_________. 2、1mol CO和______mol CO2所含氧原子数相等? 3、0.5molH2O中有________mol原子. 物质的量练习题一 一、选择题(每小题1~2个正确答案) 1、下列关于摩尔质量的说法正确的是() A、氯气的摩尔质量是71克 B、氯化氢的摩尔质量为36.5 g/moL C、1摩氢气的质量为2克 D、O2的摩尔质量为16g/moL。 2、对于相同质量的二氧化硫和三氧化硫来说,下列关系正确的是()
物质的量知识点总结
物质的量知识点复习 1、摩尔 物质的量是国际规定的七个基本物理量之一,用来表示含一定数目粒子的集体,符号是n,单位是mol。 摩尔是计量原子、分子、或离子等微观粒子的物质的量的单位。 阿伏伽德罗常数是任何粒子的粒子数,符号是N A,常用×1023这个近似值。 2、摩尔质量 1mol任何粒子或物质的质量以克为单位时,在数值上都与相对原子质量或相对分子质量相等。 摩尔质量是指单位物质的量的物质所具有的质量,符号是M,常用单位是g·mol-1 3、- 4、 5、使用摩尔这个概念时应注意的事项 (1)摩尔是物质的量单位,每摩尔物质含有阿伏伽德罗常数个粒子,摩尔简称摩,符号mol。 (2)摩尔的量度对象是构成物质的基本粒子,这里的“粒子”是指“基本单元”,这个基本单元可以是分子、原子、离子、电子、质子、中子等单一粒子,也可以是这些粒子的特定组合。如 1molCaCl2可以说含1molCa2+,2molCl-或3mol阴、阳离子,或 含54mole-等。 (3)摩尔概念只适用微观不适用于宏观。
(4) 使用摩尔表示物质的量时,应该用化学式指明粒子种类,而不 是使用该粒子的中文名称。 6、 气体摩尔体积 当分子数目相同时,气体体积大小主要决定于气体分子间的距离。要比较一定质量的气体体积,必须在相同温度和压强下进行。 ; 气体摩尔体积:单位物质的量气体所占的体积,符号为Vm,单位是L/mol 或m 3/mol 。 标准状况下气体的摩尔体积:标准状况下,即温度为0℃,压强为101Kpa 时,1mol 任何气体所占的体积都约是。 5阿伏伽德罗定律及推论: 根据气体状态方程PV =nRT =RT M m 可以得到以下定律和推论: (1) 同温同压下,相同体积的任何气体都含有相同数目的分子。(阿 伏伽德罗定律) (2)同温同压下的不同气体,其体积之比等于物质的量之比,等于所含粒子数目之比。2 12121N N n n V V == (3) 同温同压下的不同气体,其密度之比等于相对分子质量之比,等于相对密度。2121ρρ=M M =D 12 (4)同温同压下同质量的不同气体,其密度之比等于物质的量的比。2121 ρρ= n n @ (5)同温同压下同质量的不同气体,其体积之比等于相对分子质量
物质的量浓度计算训练题(新)
物质的量浓度的计算训练题 一、选择题 1. 下列溶液中氯离子的浓度与150mL0.5 mol/L氯化铝溶液中的氯离子的浓度相等的是: A.150mL1mol/L氯化镁溶液 B.450mL1.5 mol/L氯酸钾溶液 C.50mL1.5 mol/L氯化钾溶液 D.50mL0.5 mol/L氯化铁溶液 2.用胆矾配制0.1mol/L的硫酸铜溶液,应该 A.取29.9g胆矾溶于1L水中 B.取16g胆矾溶于水后稀释到1L C.将胆矾加热除去结晶水,再取无水硫酸铜16g溶于1L水中 D.取25g胆矾溶于水配成1L溶液 3. 设N A为阿伏加德罗常数,下列关于0.2mol/L的B a(N O3)2溶液不正确的说法是 A.2L溶液中有阴、阳离子总数为0.8N AB.500mL溶液中NO3―离子浓度为0.2mol/L C.500mL溶液中含Ba2+离子浓度为0.2mol/L D.500mL溶液中含NO3―离子总数为0.2N A 4. 下列关于物质的量浓度表述正确的是 A.0.3mol/L的Na2SO4溶液中含有的Na+和SO42―的总物质的量为0.9mol。 B.当1L水吸收22.4L氨气时所得氨水的浓度不是1mol/L,只有当22.4L氨气溶于水制得1L氨水时,其浓度才是1mol/L。 C.在K2SO4和NaCl的中性混合水溶液中,如果Na+和SO42―的物质的量浓度相等,则K+和Cl-的物质的量浓度一定相等。 D.10℃时,0.35mol/L的KCl饱和溶液100mL,蒸发掉5g水,冷却到10℃时,其体积小于100mL,它的物质的量浓度仍为0.35mol/L。 5. 一种NaOH溶液的浓度为a mol/L, 密度为ρg/cm3,则这种溶液的质量分数是: A.1000a/40ρ B.40ρ/1000a C.1000ρ/40a D.40a/1000ρ 6. 在NaCl、MgCl2和MgSO4三种盐配成的混合溶液中,若Na+离子为0.1mol,Mg2+离子为0.25mol,Cl- 离子为0.2mol,则SO42―离子物质的量为 A.0.5mol B.0.15mol C.0.2mol D.0.25mol 7.200mL 0.5mol/L的H2SO4溶液与24.4g BaCl2·xH2O刚好完全反应,则x的值是A.4 B.3 C.2 D.1 8.溶质质量分数为14%的KOH溶液,加热蒸发掉100g水后,得到溶质质量分数为28%的KOH溶液80mL,所得溶液的物质的量浓度为 A.6.25mol/L B.12.5mol/L C.3mol/L D.2mol/L 9.含重金属离子R n+,物质的量浓度为0.8mol/L,这种溶液20mL正好使20mL浓度为0.4mol/L的CO32―完全沉淀,n值为 A.4 B.3 C.2 D.1
物质的量-基础知识
四组名词 一、物质的量与摩尔: 1、物质的量 我们知道,物质都是由分子、原子、离子等微观粒子组成的。这些微粒非常小,质量很轻,难于称量。但是物质之间的反应,既是按照一定的微粒个数进行,又是以可称量的物质来进行反应的。这就需要一个物理量把微粒的多少与可称量的物质的质量联系起来,这个物理量就是“物质的量”,为了帮助同学尽快理解掌握这一概念,分析如下几点: (1)物质的量是国际单位制中七个基本物理量之一。 七个基本物理量的名称、单位(SI单位)及单位符号 量。如同长度、质量等物理量一样,“物质的量”这四个字不得简化,也不得增添任何字,不能多一个字,也不能少一个字,更不能把它当作表示物质数量或质量多少的量。它是表示微观粒子集体的一个物理量。它有量纲,有明确的物理含义,是一个科学专有名词。 2、摩尔 (1)摩尔的概念 摩尔是物质的量的单位。同其它物理量都有度量各自的单位一样,“物质的量”也有计量单位。正如米是长度的单位一样,摩尔是物质的量的单位。 摩尔可简称为“摩”,其符号是“mol”。 使用摩尔做物质的量的单位时,要注意: A、摩尔只使用于微观粒子,不适用于宏观物质。 B、应用符号表明微观粒子的种类或其特定组合(如分子、原子、离子、电子、质子、中子及其他有化学意义的特定组合),强调“用符号”而非“用汉字”,这和以前的有所不同。 (2)摩尔的确定 按规定,科学上应用0.012kg(即12g)碳 12(指原子核内含6个质子和6个中子的一种碳原子,12C)所含碳原子数目就是1摩尔。也就是说,摩尔这个单位是以0.012kg12C所含通常表示为12C或 6 的原子个数为标准,来衡量其它物质中所含微粒数目的多少。 二、阿佛加德罗常数与6.02×1023 mol-1 0.012kg12C中所含有的碳原子数就是阿佛加德罗常数,常用N A表示,N A是一个准确数字。 阿佛加德罗常数是一个非常庞大的数值,现在已经由实验测得相当精确的数值,在使用时常取其近似值为6.02×1023。例如2mol H2约含2×6.02×1023个H2分子。12.04×1023个O2分子约是2mol。 阿佛加德罗常数的单位是mol-1或/mol。 每摩尔物质含阿佛加德罗常数个微粒。 物质的量是以阿佛加德罗常数为计数单位,表示物质的基本微粒数目多少的物理量。 (4)使用摩尔时的注意事项 ①摩尔只能用于微观粒子,如分子、原子、离子、中子、质子、电子等;而不能用于宏观物质,如不能说1mol苹果、1mol小米等。 ②使用摩尔时,必须指明量度的微观粒子的名称或化学式。通常将微粒的名称或化学式或微粒符号
高考化学专题训练物质的量浓度的计算(含解析)
2019高考化学专题训练-物质的量浓度的计算(含解析) 一、单选题 1.同温同压下,两个等体积的干燥圆底烧瓶中分别充满:①NH3 ,②NO2 ,进行喷泉实验.经充分反应后,瓶内溶液的物质的量浓度为() A. ①> ② B. ①< ② C. ①=② D. 不能确定 2.将标准状况下的 a L氨气溶于1000g水中,得到氨水的密度为 b g?cm﹣3 ,则该氨水的物质的量浓度为() A. mol?L﹣ 1 B. mol?L﹣1 C. mol?L﹣ 1 D. mol?L﹣1 3.在80 g密度为d g/cm3的硫酸铁溶液中,含有 2.8 g Fe3+离子,则此溶液 中SO42-的物质的量浓度为(单位为mol·L-1)() A. B.
C. D. 4.用等体积的0.2mol/L的BaCl2 溶液,可使相同体积的Na2SO4、KAl(SO4)2、Fe2(SO4)3三种溶液中的SO42ˉ完全沉淀,则三种硫酸盐的物质的量浓度之比为() A. 6∶3∶1 B. 6∶3∶2 C. 9∶3∶1 D. 12∶3∶2 5.用98%的浓硫酸(密度为1.84 g·cm-3)配制80 mL 1 mol·L-1的稀硫酸。现给出下列仪器(配制过程中可能用到):①100 mL量筒②10 mL量筒③50 mL 烧杯④托盘天平⑤100 mL容量瓶⑥胶头滴管⑦玻璃棒⑧80 mL容量瓶按使用仪器的先后顺序排列正确的是() A. ④③⑦⑧⑥ B. ② ⑤⑦⑥ C. ①③⑧⑥⑦ D. ②⑥③⑦⑤⑥ 6.将8g铁片放入100mLCuSO4溶液中,Cu2+全部被置换后,取出附有铜的铁片洗涤、干燥、称重,其质量变为8.2g,则原溶液中CuSO4的物质的量浓度是()A. 0.125 mol?L-1 B. 0.25 mol?L-1 C. 0.175 mol?L-1 D. 0.5 mol?L-1 7.实验室欲配制 1.00mol/L的NaCl溶液80mL。下列说法正确的是() A. 选用100mL容量瓶,并用蒸馏水洗净后烘干 B. 用托盘天平称取5.9g NaCl固体倒入容量瓶中溶解 C. 定容时俯视刻度线会导致所配溶液浓度偏高 D. 摇匀、静置后发现凹液面低于刻度线1~2mm,用胶头滴管加水至与刻度线相平即可 8.有一在空气里暴露过的KOH固体样品,经分析其含水7.65%,含K2CO34.32%,其余是KOH。若将ag样品放入bmL1mol/L的盐酸中,使其充分作用后,残酸用25.25mLcmol/L的KOH溶液恰好中和完全。蒸发所得溶液,得到固体质量的表达 式中(单位g)() A. 只含有a B. 只含有 b C. 必含有 b D. 一定有a、b和c 9.现有等体积,等物质的量浓度的NaCl、MgCl2、AlCl3三种溶液,用物质的量
《物质的量浓度》练习题附答案
《物质的量浓度》 一、选择题(共10小题,每小题3分,共30分。只有1个正确答案) 1.在容量瓶上无需有标记的是 ( ) A .标线 B .温度 C .浓度 D .容量 2.某实验需要0.2 mol NaOH 固体,用托盘天平称取固体时,天平读数(游码及砝码)将( ) A .等于8.0g B .等于8.00g C .大于8.0g D .等于0.2g 3.0.5L 1mol/L 的FeCl 3溶液与0.2L 1 mol/L 的KCl 溶液中,Cl - 浓度比为 ( ) A .15∶2 B .1∶1 C .3∶1 D .1∶3 4.相对分子质量为M 的某物质在室温下的溶解度为S g ,此时测得饱和溶液的密度为 ρg ·cm - 3,则该饱和溶液的物质的量浓度是 ( ) A . 110-?L mol S M ρ B . 1)100(1000-?+L mol S M S ρ C . 110-?L mol M S ρ D . 11000) 100(-?+L mol S S M ρ 5.将标准状况下的a L HCl (气)溶于1000g 水中,得到的盐酸密度为b g/cm 3,则该盐酸的 物质的量浓度是 ( ) A . L mol a /4 .22 B . L mol ab /22400 C .L mol a ab /5.3622400+ D .L mol a ab /5.36224001000+ 6.NA 为阿伏加德罗常数,下列关于0.2mol/L K2SO4溶液的正确说法是 ( ) A .500mL 溶液中所含K +、SO 42- 总数为0.3N A B .500mL 溶液中含有0.1N A 个K +离子 C .1L 溶液中K +离子浓度是0.2mol/L D .2L 溶液中SO 42- 离子浓度是0.4mol/L 7.已知某KOH 样品中含水7.62%,含K 2CO 3 2.23%,含KOH 90%。现将1.00g 样品加入 46.00mL 1.00mol/L 的盐酸中,过量的酸用1.070mol/L KOH 溶液中和。蒸发溶液,蒸发到 无水时,可得的固体的质量为 ( ) A .3.00g B .3.43g C .4.50g D .无法计算
物质的量知识点讲解讲解学习
五、物质的量知识点复习 一、有关概念: 1、物质的量(n) ①物质的量是国际单位制中七个基本物理量之一。 ②用物质的量可以衡量组成该物质的基本单元(即微观粒子群)的数目的多少,它的单位是摩尔,即一个微观粒子群为1摩尔。 ③摩尔是物质的量的单位。摩尔是国际单位制中七个基本单位之一,它的符号是mol。 ④ “物质的量”是以摩尔为单位来计量物质所含结构微粒数的物理量。 ⑤摩尔的量度对象是构成物质的基本微粒(如分子、原子、离子、质子、中子、电子等)或它们的特定组合。如1molCaCl2可以说含1molCa2+,2molCl-或3mol阴阳离子,或含54mol质子,54mol电子。摩尔不能量度宏观物质,如果说“1mol氢”就违反了使用准则,因为氢是元素名称,不是微粒名称,也不是微粒的符号或化学式。 ⑥使用摩尔时必须指明物质微粒的名称或符号或化学式或符号的特定组合。2.阿伏加德罗常数(N A):①定义值(标准):以0.012kg(即12克)碳-12原子的数目为标准;1摩任何物质的指定微粒所含的指定微粒数目都是阿伏加德罗常数个。 ②近似值(测定值):经过科学测定,阿伏加德罗常数的近似值一般取6.02×1023,单位是mol-1,用符号N A表示。 3.摩尔质量(M): ①定义:1mol某微粒的质量 ②定义公式:, ③摩尔质量的单位:克/摩。 ④数值:某物质的摩尔质量在数值上等于该物质的原子量、分子量或化学式式量。⑤注意:摩尔质量有单位,是克/摩,而原子量、分子量或化学式的式量无单位。 4.气体摩尔体积(V m) ①定义:在标准状况下(0℃,101kPa时),1摩尔气体所占的体积叫做气体摩尔体积。 ②定义公式为: ③数值:气体的摩尔体积约为22.4升/摩(L/mol)。 ④注意:对于气体摩尔体积,在使用时一定注意如下几个方面:一个条件(标准状况,符号SPT),一个对象(只限于气体,不管是纯净气体还是混合气体都可),两个数据(“1摩”、“约22.4升”)。如“1mol 氧气为22.4升”、“标准状况下1摩水的体积约为22.4升”、“标准状况下NO2的体积约为22.4升”都是不正确的。 ⑤理解:我们可以认为22.4升/摩是特定温度和压强(0℃,101kPa)下的气体摩尔体积。当温度和压强发生变化时,气体摩尔体积的数值一般也会发生相应的变化,如273℃,101kPa时,气体的摩尔体积为44.8升/摩。 5.阿伏加德罗定律 ①决定物质体积的三因素:物质的体积由物质的微粒数、微粒本身体积、微粒间的距离三者决定。气体体积主要取决于分子数的多少和分子间的距离;同温同压下气体分子间距离基本相等,故有阿伏加德罗定律:在相同的温度和压强下,相同体积的任何气体都含有相同数目的分子。反之也成立。 ②阿伏加德罗定律:在相同的温度和压强下,相同体积的任何气体都含有相同数目的分子。 ③阿伏加德罗定律及推论适用的前提和对象:可适用于同温、同压的任何气体。 6.阿伏加德罗定律的有关推论: (其中V、n 、p、ρ、M分别代表气体的体积、物质的量、压强、密度和摩尔质量。) ①同温同压下:; ②同温同体积:。 7.标准状况下气体密度的计算 根据初中所学知识,密度=质量÷体积,下面我们取标准状况下1mol某气体,则该气体的质量在数值上等于摩尔质量,体积在数值上等于摩尔体积,所以可得如下计算公式: 标况下气体的密度(g·L-1)=气体的摩尔质量(g·mol-1)÷标况下气体的摩尔体积(L·mol-1)。 8.物质的量浓度 浓度是指一定温度、压强下,一定量溶液中所含溶质的量的多少。常见的浓度有溶液中溶质的质量分数,溶液中溶质的体积分数,以及物质的量浓度。 ①定义:物质的量浓度是以单位体积(1升)溶液里所含溶质B的物质的量来表示溶液组成的物理量。 ②定义公式为: ③单位:常用mol/L
2020高考化学一轮复习专题1-2-物质的量浓度(练习)
1.2物质的量浓度 1.下列目的能达到的是() A.将58.5g NaCl溶于1L水中可得1mol/L的NaCl溶液 B.将标准状况下22.4L HCl溶于1L水中可得1mol/L盐酸 C.将25.0g胆矾溶于水后配成100mL溶液所得溶液浓度为1mol/L D.将78g Na2O2溶于水,配成1L溶液可得到浓度为1mol/L溶液 【答案】C 【解析】A项把溶剂的体积误当作溶液的体积;B项不知溶液的体积;D项发生反应:2Na2O2+2H2O===4NaOH+O2↑,得到溶液的浓度为2mol/L。 2.下列关于容量瓶的说法不正确的是() A.容量瓶上一般标有规格、温度和刻度线 B.容量瓶在使用前要检查是否漏水 C.可将固体或浓溶液直接在容量瓶中溶解或稀释 D.容量瓶不能长时间盛放所配制的溶液,应及时分装在试剂瓶中 【答案】C 【解析】容量瓶是配制一定物质的量浓度溶液的精确仪器,固体或浓溶液溶解或稀释时会产生热效应,使溶液发生热胀冷缩,导致结果不准确,故不可将固体或浓溶液直接在容量瓶中溶解或稀释,C不正确。3.下列溶液中,跟100mL0.5mol/L NaCl溶液中所含的Cl-物质的量浓度相同的是() A.100mL0.5mol/L MgCl2溶液 B.200mL0.25mol/L AlCl3溶液 C.50mL1mol/L NaCl溶液 D.25mL0.5mol/L HCl溶液 【答案】D 【解析】物质的量浓度与溶液的体积无关,100mL0.5mol/L NaCl溶液中c(Cl-)=0.5mol/L,而A、B、C、D项中,c(Cl-)分别为1mol/L、0.75mol/L、1mol/L、0.5mol/L,D项正确。 4.下列有关溶液配制的说法正确的是() A.在50mL量筒中配制0.1000mol/L碳酸钠溶液 B.仅用烧杯、量筒、玻璃棒就可配制100mL0.1000mol/L K2Cr2O7溶液 C.用100mL容量瓶、烧杯、玻璃棒、量筒、胶头滴管和pH=1的盐酸配制100mL pH=2的盐酸D.配制溶液时,若加水超过容量瓶刻度,应用胶头滴管将多余液体吸出 【答案】C 【解析】配制一定物质的量浓度的溶液,应在容量瓶中进行,选项A、B错误;配制溶液定容时,若加水超过容量瓶刻度,即使用胶头滴管将液体吸出,也会造成配制结果偏低。 5.取100mL0.3mol·L-1和300mL0.25mol·L-1的硫酸注入500mL容量瓶中,加水稀释至刻度线,该混合溶液中H+的物质的量浓度是() A.0.21mol·L-1B.0.42mol·L-1 C.0.56mol·L-1D.0.26mol·L-1 【答案】B
常见物质的量浓度的计算题型
常见物质的量浓度的计算题型 一、公式归纳与解题巧法 n=N/N A =m/M=V/V m =cV, ,n 1/n 2=N 1/N 2=V 1/V 2(同T,P)=m 1/m 2(M 同)=c 1/c 2 (同溶液中,V 同), PV=nRT,PM=ρRT,ρ1/ρ2=M 1/M 2=D ;M =m 总/n 总=ρ标=MD=M 1a%+M 2b%+M 3c%+… c=1000ρω/M 或c=ρω/M(SI 制),ω=S/(100+S), 稀释公式c 1V 1=c 2V 2 ,平均值法与十字交叉法, 差量法,同大同小规律与大小小大规律,溶液中的电荷守恒、元素守恒等。 二、物质的量浓度的几种常见计算 (1).溶液中离子浓度的计算(化合物电离离子) 例1.求L 的Fe 2(SO 4)3溶液中c(Fe 3+)、c(SO 42-) 例2. V mL Al 2(SO 4)3溶液中含Al 3+ a g ,取4 V mL 溶液稀释到4V mL ,稀释后溶液中SO 42-的物质的量浓度是( ) A .L /mol V 9a 100 B. L /mol V 18a 125 C.L /mol V 36a 125 D. L /mol V 54a 100 。 例3.跟500 mL mol/L Na 2SO 4溶液所含Na +的物质的量浓度相同的溶液是( ) mL 1 mol/L NaNO 3溶液 B. 500 mL mol/L NaCl 溶液 C .1000 mL mol/L NaCl 溶液 D. 250 mL 2 mol/L NaNO 3溶液 例4.下列溶液中的c (Cl -)与50 mL 1 mol/L AlCl 3溶液中的c (Cl -)相等的是( ) A .150 mL 1 mol/L NaCl 溶液 B. 75 mL 2 mol/L NH 4Cl 溶液 C .150 mL 3 mol/L BaCl 2溶液 mL 1 mol/L AlCl 3溶液 例5.下列溶液中,Cl -的物质的量浓度最小的是( ) A .100 mL mol/L NaCl 溶液 B. 500 mL mol/L AlCl 3溶液 C .250 mL 2 mol/L MgCl 2溶液 mL 5 mol/L KClO 3溶液 例6.将7.45g 氯化钾和11.1g 氯化钙组成的混合物溶于水配成200mL 溶液,此溶液中Cl -的物质的量浓度是( ) A . mol/L B. mol/L mol/L D. 3 mol/L 例7.物质的量浓度相同的NaCl 、MgCl 2、AlCl 3三种溶液,当它们的体积比为3∶2∶1时, 三种溶液中Cl -的物质的量浓度之比为( ) ) A .1∶1∶1 ∶2∶3 C. 3∶2∶1 D. 6∶3∶2 (2).溶液混合的计算(体积可以直接相加的四种情况——浓度很稀、相近、注明忽略V 变化或要求粗略计算;其他溶液混合总体积都减小.①ω1、ω2同溶质溶液等体积混合求ω混——同大同小规律②c 1、c 2同溶质溶液等质量混合求c 混——大小小大规律) 例8.将200 mL mol/L KCl 溶液与100 mL mol/L KCl 溶液混合,所得溶液的物质的量浓度为(设混合后溶液体积变化忽略不计) ( ) A . mol/L B. mol/L mol/L D. mol/L 例9.将标况下448LNH 3溶于1L 水中,得到密度为cm 3的氨水,则该氨水的物质的量浓度 为 。 例10.将标况下VL 相对分子质量为M 的某气体B 溶于1L 水中,得到密度为 g/cm 3的B 溶 液,则该溶液的c B = 。 例11.将10%KCl 与70%KCl 溶液混合后得到30%KCl 溶液,则两溶液混合的质量比为 。 例12.将30%的HCl 加水稀释至20%,所加水的质量与浓盐酸的质量比为 。 例13. 将10mol/LKOH 与3mol/LKOH 溶液混合后得到5mol/LKOH 溶液,则两溶液混合的体积比约为 。 例14.将L 的KNO 3加水稀释至L ,则浓KNO 3与所加水的体积比约为 。 例15.将30%的KOH 与70%的KOH 溶液等体积混合,所得混合溶液中溶质的质量分数( ) \ A.大于50% B. 小于50% C. 等于50% D. 无法确定
