第5章 己二酸

第5章己二酸、戊二酸、丁二酸在甲醇己二酸二甲
脂混合溶剂中溶解度及关联
根据前面混合二元酸甲酯化反应工艺与反应动力学研究发现,酯化剂甲醇是要求过量才能保证DBA酯化高产率。酯化剂甲醇在DBA甲酯化反应体系中既是酯化剂也是反应体系溶剂,DBA甲酯化过程涉及到DBA在甲醇中溶解反应耦合过程,随着反应发生己二酸二甲酯不断生成,DBA在甲醇与己二酸二甲酯混合溶剂中溶解反应耦合过程逐渐占用主导作用,因此研究DBA在甲醇与己二酸二甲酯混合溶剂中固液相平衡有利于分析DBA溶解平衡对反应的影响,为DBA大规模生产提供可靠的基础工程热力学数据。
5.1混合二元酸在甲醇与己二元酸二甲酯混合溶剂中溶解度
5.1.1混合二元酸在甲醇与己元酸二甲酯溶解度测定实验可靠性的验证
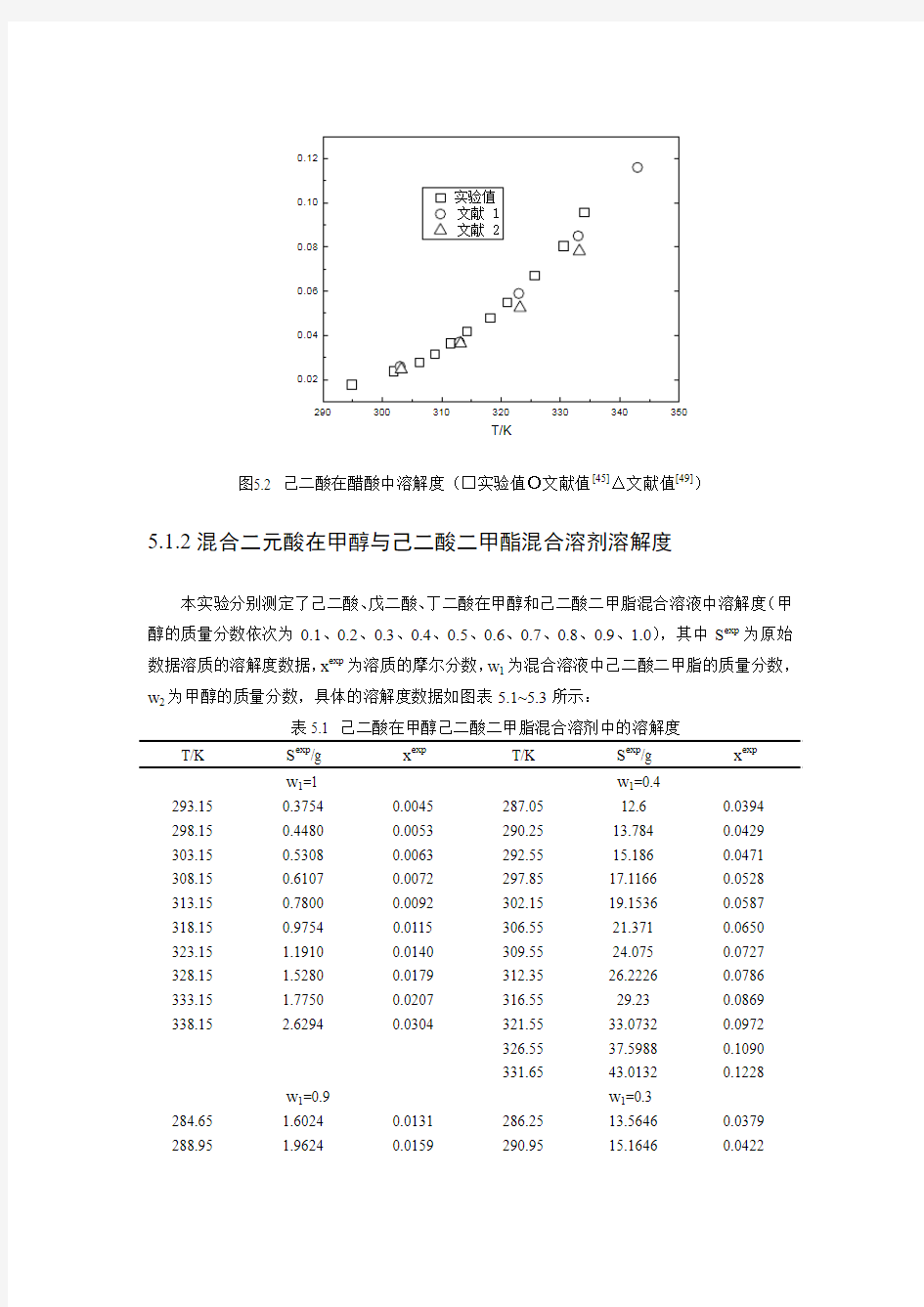
混合二元酸在甲醇与混合二元酸二甲酯溶解度测定实验采用激光动态法,为了检验该装置的准确性,本实验做了己二酸在甲醇和醋酸中的溶解度,将测得的部分值与文献[45,49,62]进行比较,结果如图5.1~5.2,测量值与文献值基本吻合。说明这套激光装置用来测定这三种二元酸在己二酸二甲脂和甲醇混合溶剂中的溶解度是可信的。
x
T/K
图5.1 己二酸在甲醇中的溶解度(□实验值△文献值[62])
X
T/K
图5.2 己二酸在醋酸中溶解度(□实验值○文献值[45]△文献值[49])
5.1.2混合二元酸在甲醇与己二酸二甲酯混合溶剂溶解度
本实验分别测定了己二酸、戊二酸、丁二酸在甲醇和己二酸二甲脂混合溶液中溶解度(甲醇的质量分数依次为0.1、0.2、0.3、0.4、0.5、0.6、0.7、0.8、0.9、1.0),其中S exp为原始数据溶质的溶解度数据,x exp为溶质的摩尔分数,w1为混合溶液中己二酸二甲脂的质量分数,w2为甲醇的质量分数,具体的溶解度数据如图表5.1~5.3所示:
表5.1 己二酸在甲醇己二酸二甲脂混合溶剂中的溶解度T/K S exp/g x exp T/K S exp/g x exp
w1=1 w1=0.4 293.15 0.3754 0.0045 287.05 12.6 0.0394 298.15 0.4480 0.0053 290.25 13.784 0.0429 303.15 0.5308 0.0063 292.55 15.186 0.0471 308.15 0.6107 0.0072 297.85 17.1166 0.0528 313.15 0.7800 0.0092 302.15 19.1536 0.0587 318.15 0.9754 0.0115 306.55 21.371 0.0650 323.15 1.1910 0.0140 309.55 24.075 0.0727 328.15 1.5280 0.0179 312.35 26.2226 0.0786 333.15 1.7750 0.0207 316.55 29.23 0.0869 338.15 2.6294 0.0304 321.55 33.0732 0.0972
326.55 37.5988 0.1090
331.65 43.0132 0.1228
w1=0.9 w1=0.3
284.65 1.6024 0.0131 286.25 13.5646 0.0379 288.95 1.9624 0.0159 290.95 15.1646 0.0422
294.75 2.373 0.0192 293.55 16.2908 0.0452 299.75 2.7594 0.0223 297.55 18.302 0.0505 303.95 3.1618 0.0254 300.65 20.8262 0.0570 307.35 3.6802 0.0295 304.65 23.0756 0.0628 311.75 4.1942 0.0335 308.95 26.0736 0.0704 315.45 4.736 0.0376 311.65 28.0506 0.0753 319.75 5.3432 0.0423 315.65 31.353 0.0834 323.85 5.9786 0.0470 320.25 35.785 0.0941 327.45 6.581 0.0515 324.45 40.7172 0.1057 330.85 7.2196 0.0563 328.95 45.9172 0.1176 w1=0.8 w1=0.2
283.95 4.4 0.0270 285.25 13.8 0.0349 288.45 4.9528 0.0303 290.95 16 0.0402 293.25 5.587 0.0341 293.75 18 0.0450 298.75 6.4932 0.0394 297.65 20.3456 0.0506 302.75 7.3146 0.0442 301.45 22.3544 0.0553 308.05 8.4076 0.0504 304.55 24.886 0.0612 311.35 9.3114 0.0555 308.45 27.8884 0.0681 316.35 10.3958 0.0616 312.35 30.8378 0.0748 320.95 11.6254 0.0684 316.45 34.4424 0.0828 325.15 13.2318 0.0771 320.65 38.8932 0.0925 328.85 14.436 0.0836 324.65 44.3688 0.1041 331.75 15.5502 0.0894 328.55 50.0624 0.1160 w1=0.7 w1=0.1
291.45 8.0194 0.0394 285.15 14 0.0323 296.15 8.7602 0.0429 289.15 16 0.0368 299.35 9.4904 0.0463 292.65 18 0.0412 302.45 10.439 0.0507 297.35 21 0.0477 305.35 11.4172 0.0552 300.65 23.4126 0.0529 309.05 12.5822 0.0605 304.45 26.1556 0.0588 312.25 13.8844 0.0663 308.85 29.9748 0.0668 315.45 15.3416 0.0727 311.15 32.574 0.0722 318.75 16.944 0.0797 315.35 36.8792 0.0809 323.05 19.142 0.0892 320.15 42.603 0.0923 326.45 20.8258 0.0962 324.65 48.611 0.1040 330.05 22.615 0.1037 327.65 54.6112 0.1153 w1=0.6 w1=0
289.65 10 0.0412 284.85 14 0.0298 294.25 11.2 0.0459 288.95 16 0.0339 297.55 12.21 0.0498 291.45 18 0.0380 300.85 13.2472 0.0538 296.45 20.999 0.0440 304.85 14.9492 0.0603 299.45 23.4098 0.0488 308.65 16.666 0.0668 302.95 26.0174 0.0540 312.55 18.392 0.0732 306.95 29.6358 0.0610
315.85 19.9936 0.0791 309.55 32.66 0.0668 319.05 21.859 0.0858 313.55 37.0676 0.0752 322.95 24.4664 0.0951 318.65 43.2644 0.0866 328.65 27.4558 0.1055 323.85 49.8798 0.0986 331.55 29.4888 0.1124 327.15
57.2142
0.1115
w 1=0.5 287.85 10.9814 0.0391 290.75 12.029 0.0427 294.55 13.4636 0.0475 298.35 15.0426 0.0528 302.35 16.8736 0.0588 306.25 18.929 0.0655 311.15 21.4544 0.0736 314.35 23.5396 0.0802 317.75 25.5964 0.0866 321.95 28.6232 0.0958 326.55 32.4864 0.1074 332.15 37.4672
0.1219
S /g (100g )
-1
T/K
图5.3 己二酸在甲醇己二酸二甲脂混合溶剂中的溶解度(w 2甲醇质量分数)
表5.2 戊二酸在甲醇己二酸二甲脂混合溶剂中的溶解度
T/K
S exp /g
x exp (mole fraction)
T/K
S exp /g
x exp (mole fraction)
w1=1 w1=0.4
294.85 4.348616 0.0542 289.15 78 0.2193 297.15 5.584235 0.0686 294.45 86 0.2364 300.85 7.069294 0.0853 298.15 94 0.2529 304.55 8.569319 0.1015 303.55 106 0.2762 306.35 9.748666 0.1139 307.45 118 0.2982 309.05 11.26805 0.1294 310.95 130 0.3188 310.75 12.78823 0.1443 315.65 146.64 0.3455 312.95 14.79012 0.1632 319.15 162.64 0.3693 315.25 17.2452 0.1853 322.35 181.48 0.3952 w1=0.9 w1=0.3
291.95 20.0156 0.1546 289.95 88 0.2203 293.65 22.166 0.1684 296.35 99.72 0.2426 296.55 25.366 0.1881 300.65 109.48 0.2601 299.85 28.2676 0.2052 304.35 118.92 0.2764 302.75 31.4088 0.2229 307.65 129.12 0.2931 308.05 35.1888 0.2432 310.65 139.8 0.3099 312.55 39.5888 0.2656 314.15 153 0.3295 316.45 44.8432 0.2906 317.75 169.6 0.3526 320.85 53.3232 0.3275 321.15 187.84 0.3763 w1=0.8 w1=0.2
289.25 32.984 0.1873 290.65 96 0.2177 292.75 37.146 0.2060 295.75 108 0.2384 296.35 41.2452 0.2237 299.85 120 0.2580 301.35 45.6504 0.2418 305.85 138.88 0.2870 303.95 49.8048 0.2581 310.65 154.08 0.3087 307.35 54.77716 0.2768 315.15 172.12 0.3328 312.05 60.96996 0.2987 318.15 185.32 0.3494 314.75 65.63676 0.3144 321.35 206.44 0.3743 316.35 71.56956 0.3333 322.55 219 0.3883 w1=0.7 w1=0.1
289.45 46.824 0.2094 292.45 110 0.2251 293.85 51.8956 0.2269 295.85 118.5 0.2383 297.75 56.0524 0.2407 299.35 129.3 0.2545 301.15 60.2924 0.2543 302.95 141.7 0.2723 304.45 65.3848 0.2700 306.55 156.7 0.2927 308.35 72.1848 0.2899 310.35 172.9 0.3135 312.75 80.1848 0.3120 313.95 191.05 0.3353 317.25 89.5732 0.3363 317.15 212.3 0.3592 321.35 101.6532 0.3651 320.55 238.3 0.3862 w1=0.6 w1=0
290.15 60 0.2219 293.55 118 0.2225 296.65 66.8 0.2410 295.25 122 0.2283 301.55 73.6 0.2591 297.25 128 0.2369
304.65 81.6 0.2794 299.55 136 0.2480 308.45 91.04 0.3020 302.95 148 0.2641 312.35 101.32 0.3250 308.05 168 0.2895 316.35 113.76 0.3509 312.35 188 0.3132 319.65 126.16 0.3748 317.55 218 0.3459 323.75 144.48 0.4071
321.55 248 0.3756 w 1=0.5
293.05 74.16 0.2330 298.35 80.84 0.2488 301.35 84.764 0.2578 303.25 88.794 0.2667 306.25 95.914 0.2821 309.95 105.514 0.3018 313.45 116.594 0.3233 316.75 128.994 0.3458 320.55 146.274
0.3747
S /g (100g )
-1
T/K
图5.4 戊二酸在甲醇己二酸二甲脂混合溶剂中的溶解度
表5.3丁二酸在甲醇己二酸二甲脂混合溶剂中的溶解度
T/K
S exp /g x exp (mole fraction) T/K
S exp /g x exp (mole fraction) w 1=1 w 1=0.4 293.15 0.334113
0.0049
288.75
12
0.0461
298.15 0.409671 0.0060 293.45 13.2436 0.0506 303.15 0.482315 0.0071 297.65 14.2906 0.0544 308.15 0.616781 0.0090 301.45 15.3454 0.0582 313.15 0.675533 0.0099 304.35 16.3504 0.0618 318.15 0.746532 0.0109 307.35 17.371 0.0654 323.15 0.87153 0.0127 310.15 18.6924 0.0700 328.15 0.996839 0.0145 313.55 20.3924 0.0759 333.15 1.223796 0.0177 319.95 23.358 0.0860 338.15 1.703534 0.0245 325.95 26.3938 0.0961
332.35 30.1078 0.1082 w1=0.9 w1=0.3
289.05 2 0.0200 287.35 12.42 0.0427 296.65 2.4726 0.0246 291.65 13.7702 0.0471 303.35 2.7994 0.0278 295.95 15.1626 0.0517 309.15 3.05 0.0302 299.65 16.442 0.0558 313.75 3.3036 0.0327 303.05 17.6658 0.0597 317.75 3.719 0.0366 306.75 19.0462 0.0640 324.55 4.5722 0.0446 309.85 20.6684 0.0691 335.15 5.7322 0.0553 314.05 22.643 0.0752
318.75 25.8154 0.0849
323.05 29.3666 0.0954
326.45 33.1626 0.1065 w1=0.8 w1=0.2
289.45 4.4 0.0332 286.85 12.92 0.0402 296.35 5.11 0.0384 291.05 14.4124 0.0446 301.45 5.6252 0.0421 295.05 16.008 0.0493 306.55 6.2834 0.0468 298.85 17.7656 0.0545 308.65 6.6794 0.0496 302.45 19.4064 0.0592 312.85 7.3102 0.0540 306.15 21.1594 0.0642 318.95 8.4556 0.0620 309.85 23.043 0.0695 326.35 9.9602 0.0722 314.35 25.123 0.0753 331.85 11.6244 0.0833 318.65 27.843 0.0828
323.55 30.697 0.0905
328.25 34.299 0.1001 w1=0.7 w1=0.1
290.95 7.1 0.0430 286.15 12.92 0.0368 297.15 7.8812 0.0475 290.35 14.6062 0.0414 302.45 8.6374 0.0518 294.15 16.2406 0.0458 307.45 9.6886 0.0578 297.45 17.8818 0.0502 311.85 10.5004 0.0623 301.15 19.8712 0.0554 315.65 11.4858 0.0678 305.35 22.1312 0.0614 319.45 12.8566 0.0752 309.35 24.4512 0.0674 325.95 14.4418 0.0837 313.75 26.7912 0.0733 331.65 16.2868 0.0934 317.55 29.3712 0.0798
322.35 32.3586 0.0873 328.45
37.1094 0.0988 w 1=0.6 w 1=0 289.35 8.4 0.0427 285.75 14 0.0366 294.55 9.24 0.0468 290.95 16.026 0.0417 299.15 9.94 0.0502 295.85 17.8548 0.0462 303.15 11.23 0.0563 298.15 19.787 0.0510 306.15 11.9538 0.0598 302.55 22.2064 0.0568 309.65 13.0676 0.0650 307.85 24.8964 0.0633 314.05 14.2998 0.0707 311.35 27.1644 0.0686 320.25 16.2998 0.0797 314.35 29.721 0.0746 325.45 18.1988 0.0882 319.85 33.4262 0.0832 330.65
20.5988
0.0987
324.45 36.6426 0.0904 327.75
39.6466
0.0971
w 1=0.5 290.95 11 0.0480 295.05 11.868 0.0516 298.15 12.7984 0.0554 301.35 13.7676 0.0594 304.55 14.7016 0.0631 308.35 15.9414 0.0681 312.25 17.5672 0.0745 318.45 19.8948 0.0836 323.95 22.1952 0.0923 331.15 25.256
0.1037
S /g (100g )
-1
T/K
图5.5 丁二酸在甲醇己二酸二甲脂中的溶解度
结合图5.3~5.5和表5.1~5.3可以观察出:
(1)从图5.3~5.5可以看出,在同一种溶剂配比中己二酸、戊二酸、丁二酸的溶解度随温度的升高而增加;
(2)从图5.2、图5.3可以看出己二酸和丁二酸在己二酸二甲脂中的溶解度非常小,随温度升高其增加的幅度很缓慢;混合溶剂中甲醇的质量分数越高,三种溶质的溶解度随温度增长的斜率越大,说明甲醇是敏感因素,Hu, Yong-Hong 认为是由于二元羧酸分子与甲醇分子以非共价键的形式络合,降低了溶剂中分子化学势[48],因而在甲醇中表现出更易溶。
(3将图5.3、图5.5与图5.4比较可以得出与同一种溶剂中,戊二酸的溶解性强于己二酸和丁二酸,290K 时戊二酸的溶解度约为己二酸和丁二酸的十倍,随着温度的升高,当温度为320K 时戊二酸的溶解度为丁二酸的6倍。这可能是由于戊二酸的分子结构决定的,其含有奇数个碳原子,戊二酸分子更容易发生弯曲、叠成,没有偶数碳原子二元羧酸稳定,导致熔点和摩尔融化焓都比另外两种酸小,见表5-5,也表现出更易容[58,64]。
5.2混合二元酸在混合溶剂中溶解度模型关联
实验得到的固液平衡数据毕竟有限,固液平衡模型研究是十分必要的,目前对于固—液相平衡模型的研究成型的方法主要有活度系数法、状态方程法、经验方程法、拓扑法和人工神经网络法。本节采用了经验方程阿尔伯特方程、半经验方程λh 方程和涉及到活度系数的理论方程NRTL 方程分别对己二酸—甲醇—己二酸二甲脂、戊二酸—甲醇—己二酸二甲脂、丁二酸—甲醇—己二酸二甲脂三个体系的溶解度数据进行了关联。
5.2.1混合二元酸在混合溶剂中溶解度模型关联计算基础
当固液两相达到平衡时,可以认为是溶质从固相进入液相和液相进入固相速率相等,即溶质在固液两相中的逸度相等,根剧热力学理论可以得到固液平衡一般关系式:
11ln 1ln tp i p tr tr
P i i tr H C T T C x R T T R T R T γ???????=--+-- ?
???
?? (5.1) 上式:i γ—组分i 在液相里的活度系数; i x —组分i 在液相里的摩尔分数; t p i H ?—组分i 的相变焓; R —气体常数; T —相平衡温度;
tr T —组分i 的三相点温度;
P C ?—组分i 在固相和液相的恒压热容差。 prausnitz 对式(1.4)作出两个假设:
1.物质的三相点难以测得但是其和熔点相差很小,因而实际中可以用熔点代替三相点,以熔化温度下的融化焓代替相变焓;
2.由于P C ?值比较小,可以忽略右边的第二项和第三项。这样将其化简可得:
11ln fus i i fus H x R T T γ??
?=-- ? ??
? (5.2) 其中fus H ?和fus T
分别为溶质的摩尔融化焓和熔点
由固液平衡方程(5.2)可知只要知道了溶质的活度系数,就可以知道固液平衡关系,关于活度系数的求法本文采用的是NRTL 方程,对于固液平衡关联中所要用到的本体系中所涉及的三种溶质己二酸、戊二酸、丁二酸、的熔点和摩尔融化焓[65]如表5.5所示: 表5.5己二酸、戊二酸、丁二酸熔点和摩尔融化焓
溶质 fus T (K)
fus H ?(KJ/mol )
己二酸 426.15 34.9 戊二酸 369.15 20.9 丁二酸 458.15
32.9
5.2.2 NRTL 模型
本节采用的NRTL 方程形式如下:
3
3
31133
31
111ln ji j ji k kj kj j j ji
k ij j ki k kj k k kj k k k x G x G x G i G x G x x G ττγτ======??
?
?=+- ? ??
?
∑∑∑∑∑∑ (5.3)
ij ij ij G =exp(-)ητ /i j i j i j a b T τ=+ i j j i ηη= i j j i ττ≠ 0ii τ= (5.4)
a ij 、
b ij 和ηij 为待回归参数,Renon 根据化学理论,将溶液分为七类,并将ηij 的值定在0.2~0.47,对于大部分系统的ηij =0.3,对于某些体系ηij 的取值对数据的拟合影响显著,可以NRTL 方程按三参数方程处理,本体系参考[49]ηij 取0.3处理。
这样NRTL 方程就简化为两参数方程,那么本体系中所需要待定的二元相互作用参数如表5.6所示:
表5.6 体系所涉及二元相互作用参数
i j aij aji bij bji ηij DMA
CH 3OH
a 12
a 21
b 12
b 21
DMA AA a 13 a 31 b 13 b 31 0.3
DMA GA a 14 a 41 b 14 b 41 DMA SA a 15 a 51 b 15 b 51 CH 3OH AA a 23 a 32 b 23 b 32 CH 3OH GA a 24 a 42 b 24 b 42 CH 3OH SA a 25 a 52 b 25 b 52
由上表可知一共有28个参数需要回归,文献中也没有相关模型参数的报道,因为本实验是分别测定的三种溶质在甲醇和己二酸二甲脂混合溶剂中的溶解度,本应该对每种溶质的溶解度数据单独处理,但是这样会出现溶剂之间的相互作用参数出现不唯一性,实际应用中三种溶质是同时存在的,所以从整体性考虑,有将所有参数一起回归的必要性,虽然[51]提到溶质与溶质之间会对相互的溶解度产生影响,但是通过实验证明这种影响是可以忽略的。初值的给定很大程度上会影响拟合的好坏,本节数据处理采用的方法是先对单一溶质逐个处理得到各自相互作用参数,最后将各自得到的相互作用参数作为初值放到一个大程序中去拟合,这样就保证了参数的唯一性。具体的计算方法及过程如下:
对于5.2节得到的溶解度数据,主要是采用MA TLAB 数学软件,采用Nelder-Mead 单纯形法(直接搜索法)函数fminsearch (F )对待回归模型参数进行优化,F 为目标函数,其定义为实验室和计算值相对偏差的平方,具体表达式如下:
2
1exp *100exp n
x i xcali F x i ??
??-=?? ?
????
∑ (5.4) 相对偏差及相对平均偏差定义为:
exp exp *100%i cali i i x x RD x ??
-= ? ???
(5.5) 1
()i ARD abs RD n
=
∑ (5.6) x cal 为通过式(5.1)模拟出来的计算值,所需活度系数由NRTL 模型(5.2)算出,n 为实验点个数。
整个计算回归过程可用计算流程框图来表示,见图5.5:
输出回归参数
图5.5 NRTL 方程计算流程
NRTL 方程具有预测功能,可以进行外推计算,得出回归的模型参数后就可以用于该体系中三种溶质的溶度的预测。
5.2.3 Apelblat 模型
Apelblat 方程形式比较简单,其中a 、b 、c 为三个待回归参数,T 为热力学温度,x 为溶质的摩尔分数。
? ?b lnx a clnT T
=++
(5.7) 此模型认为溶质的溶解度仅仅是温度的函数,理论基础相对活度系数法薄弱,适于内插数据点,而不具备外推的功能,但由于它具有针适应性强的特点,阿尔伯特方程能够很好的描述大部分的固液平衡方程。因为其不涉及活度系数,拟合模型较为简单,采用MA TLAB 中工具箱非线性最小二乘法函数lsqnonlin()进行拟合,得到相应的模型参数,可用于数据的内插。
5.2.4 λh 模型
()111+12i i m x ln h x T T λλ-????
=- ???
????
(5.8) 此方程理论基础较阿尔伯特方程强,该方程认为溶质的溶解度不仅与相平衡温度有关还
与溶质的熔点有关,其中参数λ和h具有一定的物理意义,但是通常也当作经验方程处理,计算过程和Apelblat方程类似,x i为溶质的摩尔分数,λ和h为模型待回归参数,T为相平衡热力学温度,T m为溶质的熔点,见表5.4。
5.3 混合二元酸在混合溶剂中溶解度模型关联结果分析
5.3.1己二酸
先将己二酸在不同温度不同配比的甲醇己二酸二甲脂溶剂中的溶解度数据分别采用5.3中三种模型通过MA TLAB软件进行拟合,获得计算值并得到相应的回归参数,关联结果见表5.6:
Apelblat方程λh方程NRTL方程
T/K x exp
x cal RD% x cal RD% x cal RD%
1
293.15 0.0045 0.0048 6.7 0.0023 -48.8 0.0040 9.4 298.15 0.0053 0.0054 1.9 0.0031 -41.5 0.0051 4.8 303.15 0.0063 0.0062 -1.6 0.0043 -31.7 0.0063 -0.2 308.15 0.0072 0.0074 2.8 0.0059 -18.0 0.0078 -7.8 313.15 0.0092 0.0089 -3.3 0.0079 -14.1 0.0096 -4.3 318.15 0.0115 0.011 -4.4 0.0106 -7.8 0.0118 -2.6 323.15 0.0140 0.0137 -2.1 0.0141 0.7 0.0144 -2.9 328.15 0.0179 0.0175 -2.2 0.0185 3.3 0.0176 1.9 333.15 0.0207 0.0226 9.2 0.024 15.9 0.0212 -2.4 338.15 0.0304 0.0296 -2.6 0.031 1.9 0.0260 14.4
w1=0.9
284.65 0.0131 0.0131 0.0 0.007 -46.6 0.0139 -6.4 288.95 0.0159 0.0155 -2.5 0.0089 -44.0 0.0161 -0.7 294.75 0.0192 0.0191 -0.5 0.0123 -35.9 0.0195 -1.5 299.75 0.0223 0.0228 2.2 0.016 -28.2 0.0230 -3.1 303.95 0.0254 0.0262 3.2 0.0198 -22.5 0.0263 -3.2 307.35 0.0295 0.0292 -1.0 0.0235 -20.4 0.0292 1.0 311.75 0.0335 0.0334 -0.3 0.029 -13.4 0.0335 -0.1 315.45 0.0376 0.0373 -0.8 0.0346 -7.9 0.0375 0.3 319.75 0.0423 0.0421 -0.5 0.0421 -0.4 0.0427 -1.1 323.85 0.0470 0.047 0.0 0.0505 7.4 0.0483 -2.7 327.45 0.0515 0.0517 0.4 0.059 14.5 0.0537 -4.2 330.85 0.0563 0.0563 0.0 0.0681 20.9 0.0593 -5.4
w1=0.8
283.95 0.0270 0.0268 -0.7 0.0247 -8.5 0.0251 7.1 288.45 0.0303 0.0303 0.0 0.0286 -5.6 0.0285 5.9 293.25 0.0341 0.0344 0.9 0.0333 -2.3 0.0327 4.1 298.75 0.0394 0.0397 0.8 0.0394 0.0 0.0380 3.6 302.75 0.0442 0.044 -0.5 0.0444 0.5 0.0423 4.3 308.05 0.0504 0.0504 0.0 0.0518 2.7 0.0487 3.4 311.35 0.0555 0.0547 -1.4 0.0569 2.5 0.0531 4.4 316.35 0.0616 0.0619 0.5 0.0654 6.1 0.0607 1.6 320.95 0.0684 0.0692 1.2 0.0741 8.3 0.0684 0.0 325.15 0.0771 0.0766 -0.7 0.0829 7.5 0.0761 1.4 328.85 0.0836 0.0836 0.0 0.0914 9.3 0.0837 -0.2 331.75 0.0894 0.0895 0.1 0.0986 10.2 0.0901 -0.7
w1=0.7
291.45 0.0394 0.0378 -4.1 0.038 -3.5 0.0396 -0.5 296.15 0.0429 0.0432 0.7 0.0435 1.4 0.0448 -4.5 299.35 0.0463 0.0471 1.7 0.0476 2.8 0.0486 -5.0 302.45 0.0507 0.0513 1.2 0.0519 2.3 0.0524 -3.4 305.35 0.0552 0.0555 0.5 0.0561 1.6 0.0562 -1.8 309.05 0.0605 0.0612 1.2 0.062 2.4 0.0615 -1.8 312.25 0.0663 0.0666 0.5 0.0674 1.6 0.0664 -0.2 315.45 0.0727 0.0724 -0.4 0.0732 0.7 0.0716 1.5 318.75 0.0797 0.0789 -1.0 0.0797 0.0 0.0775 2.9 323.05 0.0892 0.088 -1.4 0.0888 -0.5 0.0858 3.7 326.45 0.0962 0.0959 -0.3 0.0966 0.4 0.0932 3.1 330.05 0.1037 0.1048 1.1 0.1054 1.6 0.1019 1.7
w1=0.6
289.65 0.0412 0.0403 -2.2 0.0409 -0.7 0.0417 -1.1 294.25 0.0459 0.0458 -0.2 0.0462 0.7 0.0467 -1.8 297.55 0.0498 0.0501 0.6 0.0503 1.0 0.0507 -1.7 300.85 0.0538 0.0547 1.7 0.0547 1.7 0.0550 -2.2 304.85 0.0603 0.0606 0.5 0.0605 0.3 0.0605 -0.2 308.65 0.0668 0.0667 -0.2 0.0664 -0.6 0.0662 0.9 312.55 0.0732 0.0734 0.3 0.073 -0.3 0.0729 0.5 315.85 0.0791 0.0794 0.4 0.079 -0.1 0.0790 0.2 319.05 0.0858 0.0855 -0.4 0.0851 -0.8 0.0852 0.8 322.95 0.0951 0.0935 -1.7 0.0932 -2.0 0.0933 1.9 328.65 0.1055 0.106 0.5 0.1062 0.7 0.1076 -2.0 331.55 0.1124 0.1128 0.4 0.1134 0.9 0.1154 -2.6
w1=0.5
287.85 0.0391 0.0393 0.5 0.0395 1.0 0.0411 -5.2 290.75 0.0427 0.0427 0.0 0.0429 0.5 0.0441 -3.5 294.55 0.0475 0.0475 0.0 0.0476 0.2 0.0485 -2.0 298.35 0.0528 0.0528 0.0 0.0528 0.0 0.0532 -0.9 302.35 0.0588 0.0587 -0.2 0.0587 -0.2 0.0587 0.1
306.25 0.0655 0.0651 -0.6 0.065 -0.8 0.0646 1.4 311.15 0.0736 0.0738 0.3 0.0736 0.0 0.0730 0.8 314.35 0.0802 0.0799 -0.4 0.0798 -0.5 0.0789 1.6 317.75 0.0866 0.0869 0.4 0.0867 0.1 0.0859 0.8 321.95 0.0958 0.0962 0.4 0.096 0.2 0.0951 0.8 326.55 0.1074 0.1072 -0.2 0.1072 -0.2 0.1062 1.1 332.15 0.1219 0.1218 -0.1 0.1222 0.3 0.1216 0.2
w1=0.4
287.05 0.0394 0.0393 -0.3 0.0394 0.0 0.0394 0.0 290.25 0.0429 0.043 0.2 0.0431 0.5 0.0429 0.1 292.55 0.0471 0.0459 -2.6 0.046 -2.3 0.0453 3.9 297.85 0.0528 0.0531 0.6 0.0532 0.8 0.0523 0.8 302.15 0.0587 0.0596 1.5 0.0596 1.5 0.0586 0.1 306.55 0.0650 0.0669 2.9 0.0668 2.8 0.0659 -1.3 309.55 0.0727 0.0722 -0.7 0.0722 -0.7 0.0706 2.8 312.35 0.0786 0.0775 -1.4 0.0774 -1.5 0.0757 3.7 316.55 0.0869 0.0861 -0.9 0.0859 -1.2 0.0843 2.9 321.55 0.0972 0.0971 -0.1 0.097 -0.2 0.0959 1.4 326.55 0.1090 0.1093 0.3 0.1093 0.3 0.1087 0.3 331.65 0.1228 0.1229 0.1 0.1231 0.2 0.1232 -0.3
w1=0.3
286.25 0.0379 0.0372 -1.9 0.0368 -2.9 0.0370 2.3 290.95 0.0422 0.0426 1.0 0.0424 0.5 0.0425 -0.7 293.55 0.0452 0.0459 1.6 0.0457 1.1 0.0457 -1.3 297.55 0.0505 0.0513 1.6 0.0513 1.6 0.0511 -1.3 300.65 0.0570 0.056 -1.8 0.0561 -1.6 0.0552 3.1 304.65 0.0628 0.0625 -0.5 0.0626 -0.3 0.0618 1.6 308.95 0.0704 0.0701 -0.4 0.0704 0.0 0.0694 1.4 311.65 0.0753 0.0754 0.1 0.0757 0.5 0.0746 0.9 315.65 0.0834 0.0838 0.5 0.084 0.7 0.0830 0.6 320.25 0.0941 0.0944 0.3 0.0945 0.4 0.0935 0.7 324.45 0.1057 0.1051 -0.6 0.1051 -0.6 0.1038 1.8 328.95 0.1176 0.1178 0.2 0.1174 -0.2 0.1164 1.0
w1=0.2
285.25 0.0349 0.0351 0.6 0.0337 -3.4 0.0341 2.2 290.95 0.0402 0.0413 2.7 0.0406 1.0 0.0408 -1.4 293.75 0.0450 0.0447 -0.7 0.0443 -1.6 0.0441 2.0 297.65 0.0506 0.0499 -1.4 0.0501 -1.0 0.0495 2.2 301.45 0.0553 0.0555 0.4 0.0562 1.6 0.0555 -0.4 304.55 0.0612 0.0604 -1.3 0.0616 0.7 0.0605 1.1 308.45 0.0681 0.0673 -1.2 0.069 1.3 0.0676 0.7 312.35 0.0748 0.0748 0.0 0.0771 3.1 0.0756 -1.2 316.45 0.0828 0.0836 1.0 0.0864 4.4 0.0848 -2.5 320.65 0.0925 0.0936 1.2 0.0969 4.8 0.0950 -2.7
324.65 0.1041 0.1041 0.0 0.1078 3.6 0.1052 -1.0 328.55 0.1160 0.1153 -0.6 0.1193 2.8 0.1161 -0.1
w1=0.1
285.15 0.0323 0.0326 0.9 0.0302 -6.5 0.0321 0.8 289.15 0.0368 0.0369 0.3 0.0352 -4.4 0.0366 0.6 292.65 0.0412 0.0412 0.0 0.0401 -2.7 0.0410 0.6 297.35 0.0477 0.0475 -0.4 0.0475 -0.4 0.0475 0.5 300.65 0.0529 0.0525 -0.8 0.0533 0.8 0.0526 0.6 304.45 0.0588 0.0588 0.0 0.0607 3.2 0.0591 -0.6 308.85 0.0668 0.067 0.3 0.0703 5.2 0.0674 -0.9 311.15 0.0722 0.0716 -0.8 0.0757 4.9 0.0719 0.3 315.35 0.0809 0.0809 0.0 0.0865 6.9 0.0812 -0.3 320.15 0.0923 0.0927 0.4 0.1003 8.7 0.0928 -0.6 324.65 0.1040 0.1052 1.2 0.1148 10.4 0.1050 -1.0 327.65 0.1153 0.1143 -0.9 0.1252 8.6 0.1130 2.0
w1=0
284.85 0.0298 0.03 0.7 0.0274 -8.1 0.0297 0.3 288.95 0.0339 0.0344 1.5 0.032 -5.6 0.0344 -1.6 291.45 0.0380 0.0374 -1.6 0.0352 -7.4 0.0374 1.5 296.45 0.0440 0.0441 0.2 0.0422 -4.1 0.0445 -1.0 299.45 0.0488 0.0485 -0.6 0.0469 -3.9 0.0490 -0.4 302.95 0.0540 0.0542 0.4 0.053 -1.9 0.0550 -2.0 306.95 0.0610 0.0613 0.5 0.0607 -0.5 0.0624 -2.3 309.55 0.0668 0.0663 -0.8 0.0661 -1.1 0.0675 -1.0 313.55 0.0752 0.0747 -0.7 0.0753 0.1 0.0762 -1.3 318.65 0.0866 0.0867 0.1 0.0884 2.1 0.0885 -2.2 323.85 0.0986 0.1005 1.9 0.1035 5.0 0.1029 -4.4 327.15 0.1115 0.1102 -1.2 0.1141 2.3 0.1118 -0.3
表5.7 己二酸apelblat 方程回归参数
System a b c ARD%
w1=1 -657 26952 98 3.67
w1=0.9 77.9 -6244.1 -10.7 0.95
w1=0.8 -48.5 53.3 7.9 0.56
w1=0.7 -46.1 -169.9 7.6 1.16
w1=0.6 13.9 -2770.5 -1.3 0.74
w1=0.5 -8.7 -1084 2.1 0.25
w1=0.4 -13.4 -1582.1 2,.8 0.96
w1=0.3 -44.9 -241.1 7.5 0.85
w1=0.2 -70.6 892.5 11.3 0.91
w1=0.1 -55.6 50.0 9.2 0.50
w1=0 -22.3 -1560.1 4.3 0.84
表5.8 己二酸λh 方程回归参数
w1=1 1.1 5450.7 18.41
w1=0.9 1.7 2818.7 21.83
w1=0.8 0.5 5104 5.32
w1=0.7 0.5 4965.9 1.59
w1=0.6 0.4 5301.1 0.81
w1=0.5 0.5 4651.8 0.32
w1=0.4 0.5 4545.5 1.0
w1=0.3 0.6 4136.1 0.86
w1=0.2 0.7 3622.3 2.43
w1=0.1 1.5 2343.2 5.21
w1=0 1.09 2907 3.49
表5.9 己二酸NRTL 方程回归参数
i j a ij a ji b ij b jiηij=ηji ARD
% DBA CH3OH -6.38 0.79 626.91 2604.7
DBA AA -0.013 2.05 326.5 -612.6
0.3 2.0
CH3OH AA 0.82 1.17 305.8 -677.7
由表5.7~5.9可知NRTL方程和apelblat方程均能很好的关联己二酸在甲醇和己二酸二甲脂中的溶解度,平均相对误差分别为2%和1.04%,但是λh的平均相对误差为5.5%,特别是己二酸二甲脂含量较低时,相对误差最高可达21.83%,相比较而言NRTL方程和apelblat 方程更适合关联己二酸的溶解度。
5.3.2 戊二酸
将测得的戊二酸在甲醇己二酸二甲脂混合溶剂中的溶解度数据分别采用三种模型通过matlab软件进行拟合,并得到相应的回归参数,关联结果见表5.10,
表5.10 三种模型关联戊二酸溶解度的比较
Apelblat方程λh方程NRTL方程
T/K x exp
x cal RD% x cal RD% x cal RD%
w1=1
294.85 0.0542 0.0577 6.39 0.0569 4.83 0.0518 4.5 297.15 0.0686 0.0663 -3.36 0.0657 -4.15 0.0703 -2.5 300.85 0.0853 0.0825 -3.25 0.0825 -3.26 0.0874 -2.5 304.55 0.1015 0.1022 0.63 0.1026 1.08 0.1026 -1.0 306.35 0.1139 0.1132 -0.65 0.1138 -0.12 0.1154 -1.3
309.05 0.1294 0.1316 1.77 0.1323 2.25 0.1300 -0.5 310.75 0.1443 0.1446 0.22 0.1451 0.55 0.1450 -0.5 312.95 0.1632 0.1631 -0.08 0.1630 -0.09 0.1632 0.0 315.25 0.1853 0.1846 -0.37 0.1836 -0.92 0.1840 0.7
w1=0.9
291.95 0.1546 0.1546 4.50 0.1643 6.28 0.1618 -4.7 293.65 0.1684 0.1615 0.72 0.1714 1.79 0.1737 -3.2 296.55 0.1881 0.1696 -2.28 0.1841 -2.13 0.1904 -1.2 299.85 0.2052 0.1838 -2.20 0.1995 -2.77 0.2060 -0.4 302.75 0.2229 0.2007 -3.06 0.2140 -4.02 0.2212 0.8 308.05 0.2432 0.2161 0.95 0.2426 -0.24 0.2440 -0.3 312.55 0.2656 0.2455 2.31 0.2695 1.49 0.2669 -0.5 316.45 0.2906 0.2717 1.56 0.2949 1.49 0.2906 0.0 320.85 0.3275 0.2951 -1.63 0.3260 -0.45 0.3228 1.4
w1=0.8
289.25 0.1873 0.1900 1.47 0.1903 1.63 0.1884 -0.6 292.75 0.2060 0.2045 -0.74 0.2047 -0.68 0.2032 1.4 296.35 0.2237 0.2204 -1.49 0.2203 -1.50 0.2185 2.3 301.35 0.2418 0.2441 0.93 0.2438 0.84 0.2384 1.4 303.95 0.2581 0.2572 -0.36 0.2569 -0.47 0.2521 2.4 307.35 0.2768 0.2753 -0.54 0.2750 -0.64 0.2694 2.7 312.05 0.2987 0.3020 1.11 0.3019 1.07 0.2935 1.7 314.75 0.3144 0.3183 1.26 0.3185 1.30 0.3092 1.7 316.35 0.3333 0.3284 -1.49 0.3287 -1.39 0.3216 3.5
w1=0.7
289.45 0.2094 0.2101 0.35 0.2091 -0.13 0.2050 2.1 293.85 0.2269 0.2257 -0.52 0.2255 -0.63 0.2203 2.9 297.75 0.2407 0.2409 0.05 0.2411 0.16 0.2349 2.4 301.15 0.2543 0.2551 0.31 0.2556 0.50 0.2493 2.0 304.45 0.2700 0.2699 -0.03 0.2705 0.19 0.2649 1.9 308.35 0.2899 0.2888 -0.39 0.2894 -0.20 0.2849 1.7 312.75 0.3120 0.3120 0.00 0.3123 0.09 0.3087 1.1 317.25 0.3363 0.3381 0.54 0.3379 0.48 0.3354 0.3 321.35 0.3651 0.3641 -0.28 0.3633 -0.49 0.3632 0.5
w1=0.6
290.15 0.2219 0.2191 -1.26 0.2134 -3.83 0.2148 3.2 296.65 0.2410 0.2429 0.79 0.2421 0.48 0.2360 2.0 301.55 0.2591 0.2641 1.93 0.2659 2.63 0.2563 1.1 304.65 0.2794 0.2792 -0.07 0.2821 0.95 0.2730 2.3 308.45 0.3020 0.2997 -0.76 0.3030 0.35 0.2936 2.8 312.35 0.3250 0.3231 -0.58 0.3261 0.33 0.3157 2.9 316.35 0.3509 0.3500 -0.26 0.3514 0.13 0.3402 3.1 319.65 0.3748 0.3746 -0.06 0.3736 -0.32 0.3621 3.4 323.75 0.4071 0.4085 0.35 0.4032 -0.95 0.3915 3.8
w1=0.5
293.05 0.2330 0.2322 -0.36 0.2251 -3.40 0.2272 2.5 298.35 0.2488 0.2485 -0.11 0.2477 -0.44 0.2459 1.2 301.35 0.2578 0.2598 0.77 0.2614 1.43 0.2578 0.0 303.25 0.2667 0.2677 0.35 0.2705 1.41 0.2670 -0.1 306.25 0.2821 0.2815 -0.20 0.2855 1.19 0.2826 -0.2 309.95 0.3018 0.3011 -0.23 0.3050 1.06 0.3029 -0.4 313.45 0.3233 0.3224 -0.25 0.3248 0.47 0.3238 -0.2 316.75 0.3458 0.3454 -0.12 0.3446 -0.32 0.3450 0.2 320.55 0.3747 0.3755 0.22 0.3691 -1.51 0.3711 1.0
w1=0.4
289.15 0.2193 0.2185 -0.36 0.2151 -1.90 0.2171 1.0 294.45 0.2364 0.2377 0.51 0.2370 0.24 0.2334 1.3 298.15 0.2529 0.2527 -0.07 0.2535 0.23 0.2485 1.7 303.55 0.2762 0.2773 0.40 0.2794 1.14 0.2732 1.1 307.45 0.2982 0.2973 -0.28 0.2997 0.50 0.2941 1.4 310.95 0.3188 0.3170 -0.56 0.3191 0.07 0.3141 1.5 315.65 0.3455 0.3464 0.23 0.3471 0.44 0.3422 1.0 319.15 0.3693 0.3705 0.32 0.3695 0.06 0.3653 1.1 322.35 0.3952 0.3945 -0.17 0.3914 -0.96 0.3880 1.8
w1=0.3
289.95 0.2203 0.2202 -0.07 0.2170 -1.53 0.2202 0.0 296.35 0.2426 0.2427 0.05 0.2425 -0.03 0.2414 0.5 300.65 0.2601 0.2601 0.00 0.2613 0.43 0.2597 0.2 304.35 0.2764 0.2768 0.16 0.2786 0.79 0.2775 -0.4 307.65 0.2931 0.2931 0.00 0.2950 0.63 0.2951 -0.7 310.65 0.3099 0.3092 -0.21 0.3108 0.29 0.3124 -0.8 314.15 0.3295 0.3296 0.04 0.3303 0.25 0.3334 -1.2 317.75 0.3526 0.3526 0.00 0.3518 -0.23 0.3567 -1.2 321.15 0.3763 0.3764 0.03 0.3735 -0.73 0.3801 -1.0
w1=0.2
290.65 0.2177 0.2194 0.80 0.2180 0.15 0.2214 -1.7 295.75 0.2384 0.2387 0.13 0.2385 0.06 0.2393 -0.4 299.85 0.2580 0.2558 -0.86 0.2564 -0.64 0.2576 0.2 305.85 0.2870 0.2838 -1.11 0.2849 -0.73 0.2876 -0.2 310.65 0.3087 0.3090 0.09 0.3100 0.41 0.3135 -1.6 315.15 0.3328 0.3350 0.66 0.3356 0.83 0.3407 -2.4 318.15 0.3494 0.3539 1.27 0.3539 1.28 0.3599 -3.0 321.35 0.3743 0.3753 0.26 0.3746 0.07 0.3828 -2.3 322.55 0.3883 0.3837 -1.17 0.3827 -1.43 0.3924 -1.1
w1=0.1
292.45 0.2251 0.2251 0.00 0.2224 -1.18 0.2281 -1.3 295.85 0.2383 0.2389 0.24 0.2380 -0.14 0.2403 -0.8 299.35 0.2545 0.2545 -0.02 0.2550 0.18 0.2556 -0.4
302.95 0.2723 0.2720 -0.10 0.2735 0.46 0.2732 -0.3 306.55 0.2927 0.2913 -0.48 0.2933 0.20 0.2929 -0.1 310.35 0.3135 0.3136 0.05 0.3154 0.63 0.3146 -0.4 313.95 0.3353 0.3369 0.46 0.3378 0.74 0.3367 -0.4 317.15 0.3592 0.3595 0.06 0.3589 -0.09 0.3579 0.4 320.55 0.3862 0.3855 -0.18 0.3827 -0.92 0.3815 1.2
w1=0
293.55 0.2225 0.2223 -0.08 0.2212 -0.60 0.2295 -3.1 295.25 0.2283 0.2291 0.33 0.2284 0.04 0.2353 -3.0 297.25 0.2369 0.2374 0.20 0.2372 0.14 0.2435 -2.8 299.55 0.248 0.2474 -0.26 0.2477 -0.12 0.2542 -2.5 302.95 0.2641 0.2632 -0.36 0.2641 -0.02 0.2709 -2.6 308.05 0.2895 0.2893 -0.07 0.2905 0.34 0.2987 -3.2 312.35 0.3132 0.3138 0.19 0.3147 0.49 0.3245 -3.6 317.55 0.3459 0.3467 0.26 0.3467 0.23 0.3586 -3.7 321.55 0.3756 0.3749 -0.19 0.3735 -0.56 0.3870 -3.0
表5.11 戊二酸apelblat 方程回归参数
System a b c ARD% w1=1 3.7 -4779.9 1.7 1.86 w1=0.9 117.75 -7329.8 -16.6 2.13 w1=0.8 -36.5 9.88 6.1 1.04 w1=0.7 -106.3 3400.2 16.4 0.27 w1=0.6 -190.9 7160.2 29.1 0.67 w1=0.5 -322.7 13247.5 48.6 0.29 w1=0.4 -150.3 5353.9 22.9 0.32 w1=0.3 -162.15 5939.8 24.7 0.06 w1=0.2 -112.7 3676.5 17.4 0.70 w1=0.1 -152.7 5367.7 23.4 0.18
1
w1=1 3.30 1749.8 1.92
w1=0.9 0.61 3185.7 2.30
w1=0.8 0.46 3094.9 1.06
w1=0.7 0.26 3472.6 0.32
w1=0.6 0.46 2873.2 1.11
w1=0.5 0.34 3177.8 1.23
w1=0.4 0.38 3012.9 0.61
w1=0.3 0.298 3254,2 0.55
w1=0.2 0.314 3225.7 0.62
w1=0.1 0.504 2784.6 0.50
w1=0 0.392 3113.9 0.28
己二酸的制备
己二酸的制备 1.在反应过程中,有环己烯存在时,温度计的读数会维持在72~80℃之间,而 不会随加热的程度而升高,为什么? 2.反应进行的过程中,必须确保回流冷凝管一直处于通水状态,为什么? 3.描述在反应过程中反应体系和催化剂的变化状况。催化剂能否再利用? 4.由过氧化氢氧化环己烯制备1,2-环氧环己烷是否可行,为什么? 5、加料时,量过环己醇的量筒能否直接用来量取50%硝酸? 答:量过环己醇的量筒不可直接用来量取50%的硝酸。因为50%硝酸与残留的环己醇会剧烈反应,同时放出大量的热,这样一来,量取50%硝酸的量不准,而且容易发生意外事故。 6、量过环己醇的量筒为何要加少量温水洗涤?且要将此洗液倒入加料用的滴液漏斗中? 答:实验所用的环己醇的凝固点是21—24℃,因此在室温时是粘稠状的液体,极易残留在量筒里,所以要用温水洗涤量筒,并将其倒入滴液漏斗中,以免造成损失。另外,环己醇中加少量的水还可以防止滴液漏斗加料时堵塞漏斗的小孔,便于环己醇放尽。7、用环己醇氧化制备己二酸时,为什么要在回流冷凝管的上端接气体吸收装置?吸收此尾 气是用水还是用碱液好? 答:由于环己醇被氧化成己二酸的同时会生成一氧化氮,一氧化氮遇到氧后就转变成有毒的二氧化氮。故应接上气体吸收装置,除去此尾气避免造成污染和中毒。由于酸性 在水中溶解度不大,因此用碱液吸收更好。 的NO 2 8、为什么有些实验在加入最后一个物料之前,都要先加热前面的物料(如己二酸制备实验中 就得先预热到50—60℃)? 答:不论是吸热反应还是放热反应都需要活化能。对活化能较高的一些反应(室温时仍达不到其活化能的),都需通过外部加热供给能量,使其达到所需要的活化能。 9、制备己二酸实验的操作关键是什么?说明其原因? 答:控制环己醇的滴加速度是制备己二酸实验的关键。因为此反应是一个强放热的反应,所以必须等先加入反应瓶中的少量环己醇作用完全后才能继续滴加。若滴加太快,反应过于剧烈,无法控制,会使反应液冲出烧瓶造成事故。滴加太慢,反应进行的缓慢,需要的时间太长。所以操作时应控制滴加环己醇的速度,维持反应液处于微沸状态。10、制备己二酸时,你如何控制反应温度? 答:在未加入最后一个物料环己醇之前,先预热反应瓶中的稀硝酸接近沸腾。在振摇下,慢慢滴加5—6滴环己醇,反应发生同时放出热量。这时应控制滴加环己醇的速度,维持反应液呈微沸状态,直至滴加完所有的环己醇。若反应液出现暴沸时,应及时用冷水浴冷却至微沸状态。注意不能冷却太久,否则,又得重新加热,才能继续发生反应。 11、用硝酸法制备己二酸时,为什么要用50%的硝酸而不用71%的浓硝酸? 答:若用71%的浓硝酸氧化环己醇,反应太剧烈,不易控制。同时浓硝酸与空气接触,产生大量有刺激性的酸雾,影响操作,故采用50%的硝酸为好。 12、反应完毕后,为什么要趁热倒出反应液、抽滤后得到的滤饼为何要用冰水洗涤? 答:反应刚结束的时候,反应液容易倒出,若任其冷却至室温的话,己二酸就结晶析出,不容易倒出造成产品的损失。 己二酸在冰水中的溶解度比室温时在水中的溶解度要小得多。为了洗涤己二酸晶体,又减少损失,所以实验中用冰水洗涤滤饼。
己二酸制备
实验报告 尼龙66前体的制备 一、实验目的 1、学习由环己醇氧化制备环几酮和由环几酮氧化制备己二酸的基本原理。 2、掌握由环己醇氧化制备环己酮和由环己酮氧化制备己二酸的实验操作。 3、进一步了解盐析效应及萃取在分离有机化合物中的应用。 4、综合训练并掌握控温、减压抽滤、蒸馏、重结晶等操作技能。 二、实验原理 实验室制备脂肪和脂环醛、酮最常用的方法是将伯醇和仲醇用铬酸氧化。铬酸是重铬酸盐与40-50%硫酸的混合液。制备相对分子量低的醛,可以将铬酸滴加到热的酸性醇溶液中,以防止反应混合物中有过量的氧化剂存在,同时将较低沸点的醛不断蒸出,可以达到中等产率。尽管如此,仍有部分醛被进一步氧化成羧酸,并生成少量的酯。用此法制备酮,酮对氧化剂比较稳定,不易进一步被氧化。铬酸氧化醇是放热反应,必须严格控制反应温度以免反应过于剧烈。 本实验反应方程式为: 羧酸常用烯烃、醇、醛、酮等经硝酸、重铬酸钾的硫酸溶液或高锰酸钾等氧化来制备。本实验以环己酮为原料,在碱性条件下以高锰酸钾为氧化剂来制备己二酸,反应方程式: C 6H 10 O+MnO 4 -+2OH-→HOOC(CH 2 ) 4 COOH+MnO 2 +H 2 O 三、实验试剂和仪器装置: 1、仪器: 圆底烧瓶(250ml,100ml),烧杯(250ml,100ml) ,量筒(100ml ,10ml),,直型冷凝管,尾接管,蒸馏头,温度计,电热套,抽滤瓶,布氏漏斗,真空泵,蒸发皿,表面皿,分液漏斗,玻璃棒,石棉网,铁架台,酒精灯。 2、主要试剂: 浓H 2SO 4 ,Na 2 Cr 2 O 7 ,H 2 C 2 O 4 ,NaCl,无水MgSO 4 ,KMnO 4 ,NaOH10%,Na 2 SO 3
己二酸的制备
己二酸的制备 一、实验目的 1.掌握用环己醇氧化制备己二酸的基本原理和方法。 2.掌握电动搅拌器的安装及使用方法 3.巩固浓缩、过滤、重结晶等基本操作。 二、实验原理 制备羧酸最常用的方法是烯、醇、醛等的氧化法。常用的氧化剂有硝酸、重铬酸钾(钠)的硫酸溶液、高锰酸钾、过氧化氢及过氧乙酸等。本实验采用环己醇在高锰酸钾的酸性条件发生氧化反应,然后酸化得到已二酸。 三、实验仪器及药品 仪器:三口烧瓶(250ml)烧杯(1000ml)、温度计(0-150℃)、电动搅拌器、球形冷凝管、抽滤瓶、布氏漏斗、循环水多用真空泵、滴管、滤纸等。 药品:环己醇、高锰酸钾、NaOH;亚硫酸氢钠、浓盐酸、活性炭等。 四、实验步骤 1. 在250mL三口烧瓶上安装电动搅拌器。 在安装电动搅拌装置时应做到: ①.搅拌器的轴与搅拌棒在同一直线上。 ②.先用手试验搅拌棒转动是否灵活,再以低转速开动搅拌器,试验运转情况。 ③.搅拌棒下端位于液面以下,以离烧杯底部3~5mm为宜。 ④.温度计应与搅拌棒平行且伸入液面以下。 2. 往三口烧瓶中加入1.0gNaOH和50mL水。搅拌下加入6.0g高锰酸钾。搅拌加热至35℃使之溶解,然后停止加热; 3. 用滴管慢慢加入3mL的环己醇,控制滴加速度,维持温度在45℃左右。 4. 滴加完毕后若温度下降至43℃以下。,可在50℃的水浴中继续加热,直到高锰酸钾溶液颜色褪去。在沸水浴中将混合物加热5分钟,使氧化反应完全,可观察到有大量二氧化锰的沉淀凝结。 5. 用玻璃棒蘸一滴反应物到滤纸上做点滴实验。如有高锰酸盐存在,则在棕色二氧化锰点的周围出现紫色的环,可加入少量固体亚硫酸氢钠直到点滴试验呈阴性为止。 6. 趁热抽滤混合物,用少量热水洗涤滤渣3次。 7. 将洗涤液与滤液合并置于烧杯中,加少量活性炭脱色,趁热抽滤。
己二酸的制备
己二酸的制备 [目标] 学习用硝酸氧化环己醇制备已二酸的原理和方法,掌握尾气吸收、过滤、等操作技术。 [重点] 已二酸的原理和方法,尾气吸收操作技术。 [难点] 控制好氧化反应速度,防止有毒的二氧化氮气体外逸。 【实验目的】 通过本次实验,要求大家掌握己二酸的制备原理和方法,掌握尾气吸收、过滤等操 作技术。 【实验原理】 OH O 3 HOC(CH 2)4COH O O 3++ 7H 2O 32 2 硝酸和高锰酸钾都是强氧化剂,由于其氧化的选择性较差,故硝酸主要用于羧酸的制备,高锰酸钾氧化的应用范围较硝酸广些,它们都可以将环己醇直接氧化为己二酸。 本实验以50%硝酸为氧化剂,并以(偏)钒酸铵为催化剂,氧化环己醇至环己酮,后者再通过烯醇式被氧化开环而生成己二酸。在反应过程中产生的一氧化氮极易被空气中的氧气氧化成二氧化氮气体,用碱液吸收。 【实验装置图】 图1 己二酸制备装置图 【实验步骤】反应瓶中加入6 mL 50%的硝酸[1]和少许钒酸铵[2],水浴加热至50 C 后移去水浴[3], 缓慢滴加5~6滴环己醇[4],摇动至反应开始,即有红棕色二氧化氮气体放出,维持反应
温度50~60 ?C ,将剩余的环己醇滴加完毕,总量为2 mL [5]。加完后继续振荡,并用80~90 ?C 水浴加热10 min 。无红棕色气体逸出,反应即结束。将反应液倒入50 mL 烧杯中[6],冷却,结晶,抽滤,3 mL 水洗,2 mL 石油醚分两次洗[7],干燥,称重。 纯己二酸为白色晶体,mp.153 ?C 。 【实验流程图】 50-60 o C , 产生 2 mL 石油醚洗涤 【注释】 [1] 浓硝酸和环己醇切不可用同一个量筒取用,以防两者相遇剧烈反应发生爆炸。建议两位学生合 用两个量筒。 [2] 钒酸铵不可多加,否则产品发黄。不加钒酸铵也可以。 [3] 实验中要同时监测水浴温度和反应液的温度。 [4] 为防止反应过快,环己醇要慢加,并注意控温,防止太多有毒的二氧化氮气体产生,来不及被 碱液吸收而外逸到空气中。另外,环己醇的熔点为25.15 ?C ,通常为粘稠的液体。为了减少转移的损失,可用少量水冲洗量筒,并入滴液漏斗中,这样既降低了环己醇的凝固点,也可避免漏斗堵塞。 [5] 此反应为强放热反应,切不可大量加入,以免反应过于剧烈,引起爆炸。 [6] 反应结束后,装置中还有残留的二氧化氮气体,拆卸装置请至通风橱内。 [7] 利于样品快干。 [作业] P.120 第1,2题
已二酸的制备的实验报告
已二酸的制备的实验报告 一、实验目的 1、学习环己醇氧化制备己二酸的原理和方法; 2、掌握浓缩、过滤及重结晶等操作技能 二、实验原理 三、实验药品及其物理常数 环己醇:2g2.1ml(0.02mol);高锰酸钾6g(0.038mol); 0.3N氢氧化钠溶液50ml;亚硫酸氢钠;浓盐酸 四、主要仪器和材料 水浴锅三口烧瓶(100 mL、19#×3)恒压滴液漏斗空心塞(14#)球形冷凝管(19#)螺帽接头(19#,2只)温度计(100℃)布氏漏斗吸滤瓶烧杯冰滤纸水泵等. 氧化剂可用浓硝酸、碱性高锰酸钾或酸性高锰酸钾。本实验采用碱性高锰酸钾作氧化剂 五、操作步骤 (1)向250ml烧杯内加入50ml 0.3N氢氧化钠溶液,置于磁力搅拌上;(2)边搅拌边将6g高锰酸钾溶解到氢氧化钠溶液中; (3)用滴管滴加2.1ml环己醇到上述溶液中,维持反应物温度为43~47℃。(4)当醇滴加完毕且反应混合物温度降低至43℃左右时,沸水浴将混合物加热,使二氧化锰凝聚。 (5)在一张平整的滤纸上点一小滴混合物以试验反应是否完成,如果观察到试液的紫色存在,那么可以用少量固体亚硫酸氢钠来除掉过量的高锰酸钾。 (6)趁热抽滤,滤渣二氧化锰用少量热水洗涤3次(每次2 mL),每次尽量挤压掉滤渣中的水分;
(7)合并滤液和洗涤液,用4ml浓盐酸酸化至pH2.0;(8)小心地加热蒸发使溶液的体积减少到10ml左右,冷却,分离析出的己二酸。(9)抽滤、洗涤、烘干、称重、计算产率。 (10)测量产品的熔点和红外光谱,并与标准光谱比较。 六、操作要点及注意事项 1.KMnO4要研细,以利于KMnO4充分反应。 2.滴加:本实验为强烈放热反应,所以滴加环己醇的速度不宜过快(1-2滴/秒),否则,因反应强烈放热,使温度急剧升高而引起爆炸。 3.严格控制反应温度,稳定在43~47℃之间。 4.反应终点的判断: (1)反应温度降至43℃以下。 (2)用玻璃棒蘸一滴混合物点在平铺的滤纸上,若无紫色存在表明已没有KMnO4。5.用热水洗涤MnO2滤饼时,每次加水量约5~10 ml,不可太多。6.用浓盐酸酸化时,要慢慢滴加,酸化至pH=1~3。 7.浓缩蒸发时,加热不要过猛,以防液体外溅。浓缩至10ml左右后停止加热,让其自然冷却、结晶。 8.环己醇常温下为粘稠液体,可加入适量水搅拌,便于用滴管滴加; 9.此反应是放热反应,反应开始后会使混合物超过45℃,假如在室温下反应开始5min后,混合物温度还不能上升至45℃,则可小心温热至40℃,使反应开始;10.要不断振摇或搅拌,否则极易爆沸冲出容器;11.最好是将滤饼移于烧杯中,经搅拌后再抽滤; 12.为了提高收得率,最好用冰水冷却溶液以降低己二酸在水中的溶解度。 七、实验结果 1、产品性状:; 2、理论产量:2.08g;
己二酸的制备(详细参考)
苏州大学材料与化学化工学部课程教案 [实验名称] 己二酸的制备 [教学目标] 知识与技能: 学习用硝酸氧化环己醇制备已二酸的原理和方法,掌握尾气吸收、 过滤、等操作技术。 [教学重点] 已二酸的原理和方法,尾气吸收操作技术。 [教学难点] 控制好氧化反应速度,防止有毒的二氧化氮气体外逸。 [教学过程] 【实验目的】 通过本次实验,要求大家掌握己二酸的制备原理和方法,掌握尾气吸收、 过滤等操作技术。 【实验原理】 OH O 3 2)4O O 3++ 7H 2O 32 2 硝酸和高锰酸钾都是强氧化剂,由于其氧化的选择性较差,故硝酸主要用于羧酸的制备,高锰酸钾氧化的应用范围较硝酸广些,它们都可以将环己醇直接氧化为己二酸。 本实验以50%硝酸为氧化剂,并以(偏)钒酸铵为催化剂,氧化环己醇至环己酮,后者再通过烯醇式被氧化开环而生成己二酸。在反应过程中产生的一氧化氮极易被空气中的氧气氧化成二氧化氮气体,用碱液吸收。 【实验装置图】 图1 己二酸制备装置图
【实验步骤】反应瓶中加入6 mL 50%的硝酸[1]和少许钒酸铵[2],水浴加热至50 ?C 后移去 水浴[3],缓慢滴加5~6滴环己醇[4],摇动至反应开始,即有红棕色二氧化氮气体放出,维持反应温度50~60 ?C ,将剩余的环己醇滴加完毕,总量为2 mL [5]。加完后继续振荡,并用80~90 ?C 水浴加热10 min 。无红棕色气体逸出,反应即结束。将反应液倒入50 mL 烧杯中[6],冷却,结晶,抽滤,3 mL 水洗,2 mL 石油醚分两次洗[7],干燥,称重。 纯己二酸为白色晶体,mp.153 ?C 。 【实验流程图】 50-60 o C , 产生 2 mL 石油醚洗涤 【注释】 [1] 浓硝酸和环己醇切不可用同一个量筒取用,以防两者相遇剧烈反应发生爆炸。建议两位 学生合用两个量筒。 [2] 钒酸铵不可多加,否则产品发黄。不加钒酸铵也可以。 [3] 实验中要同时监测水浴温度和反应液的温度。 [4] 为防止反应过快,环己醇要慢加,并注意控温,防止太多有毒的二氧化氮气体产生,来 不及被碱液吸收而外逸到空气中。另外,环己醇的熔点为25.15 ?C ,通常为粘稠的液体。为了减少转移的损失,可用少量水冲洗量筒,并入滴液漏斗中,这样既降低了环己醇的凝固点,也可避免漏斗堵塞。 [5] 此反应为强放热反应,切不可大量加入,以免反应过于剧烈,引起爆炸。 [6] 反应结束后,装置中还有残留的二氧化氮气体,拆卸装置请至通风橱内。 [7] 利于样品快干。 [作业] P.120 第1,2题
己二酸的合成
己二酸的合成方案 1. 名称:己二酸、肥酸 2. 分子式:HOOC(CH2)4COOH 3. 分子量:146.14 4. CAS RN:42331-63-5 5. 外观:白色固体粉末, 能升华。 6. MP/BP:153℃/33 7.5℃ 7. 分子结构: 8. 主要物化性质 1)钨酸钠:白色具有光泽的片状结晶或结晶粉末,溶于水呈微碱性(PH8.5-9),不溶于乙醇,微溶于氨。在空中风化。加热到100℃失去结晶水而成无水物。与强酸(氢氟酸除外)反应生成不溶于水的黄色钨酸, 与磷酸或磷酸盐反应生成磷钨杂多酸络合物, 与酒石酸、柠檬酸、草酸等有机酸反应生成相应有机酸络合物。2)硫酸氢钾:白色片状或粒状结晶。易吸湿。在乙醇中分解。高温时失去水分并易成为焦硫酸盐。溶于1.8份冷水、0.85份沸水。相对密度2.24。熔点197℃。低毒,半数致死量(大鼠,经口)2340mg/kg。有腐蚀性。 3)环己酮:有机化合物,为羰基碳原子包括在六元环内的饱和环酮。无色透明液体,带有泥土气息,含有痕迹量的酚时,则带有薄荷味。不纯物为浅黄色,随着存放时间生成杂质而显色,呈水白色到灰黄色,具有强烈的刺鼻臭味。与空气混合爆炸极与开链饱和酮相同。环己酮有致癌作用,在工业上主要用作有机合成原料和溶剂,例如它可溶解硝酸纤维素、涂料、油漆等。 4)过氧化氢:化学式为H2O2,其水溶液俗称双氧水,外观为无色透明液体,是一种强氧化剂,适用于伤口消毒及环境、食品消毒。 9.合成路线 10. 实验部分 (1)反应方程式
投料量 实验操作: 1、加料、搅拌,在三口烧瓶中依次加入0.5g钨酸钠,0.4g硫酸氢钾,10ml环己酮,最后加40ml30%过氧化氢溶液。装好仪器,于室温下搅拌20min,以使物料混合均匀。 2、加热边搅拌边慢慢加热至90~95℃,在此温度下搅拌反应4h. 3、酸化反应完毕,趁热将反应物倒入250ml烧杯中,加酸,酸化至pH为1~2,冷却,若固体析出不多,可将溶液加热浓缩至30ml左右,待固体析出完全。 4、过滤将上述溶液抽滤,用少量冰水洗涤,再抽干。 5、烘干、称量、计算产率,将上述滤饼移在表面皿上进行烘干。然后将干燥的产物进行称量,在计算产率。
己二酸的制备
实验九:己二酸的制备 [实验目的] 学习用环己醇制备己二酸的原理和方法;掌握浓缩、过滤、重结晶等操作技能。 [实验原理] 己二酸是合成尼龙-66的主要原料之一,它可以用硝酸或高锰酸钾氧化环己醇制得。 OH HNO 3HOOCCH 2CH 2CH 2CH 2COOH [药品仪器] 药品:50%HNO 3,NH 4VO 3,环己醇,NaOH 吸收液。 仪器:球形冷凝管、温度计、分液漏斗、100ml 三颈烧瓶、布氏漏斗、抽滤瓶等。 [实验步骤] 在装有回流冷凝管、温度计、和分液漏斗的100ml 三颈烧瓶中,放置18ml(0.18mol) 50%HNO 3,及少许偏钒酸铵(约0.03g ),并在冷凝管上接一气体吸收装置,用稀NaOH 吸收反应过程中产生的二氧化氮气体。三颈烧瓶用水浴预热到50o C 左右,移去水浴,先滴入5~6滴环己醇,同时加以摇动,至反应开始放出二氧化氮气体,然后慢慢加入其余部分的环己醇,总量为6ml (约0.06mol ),调节滴加速度,使瓶内温度维持在50~60o C 之间(滴加时应不时摇动)。温度过高时,用冷水浴冷却,温度过低时,则用热水浴加热,滴加完毕约需15min 。加完后继续摇荡,并用80~90o C 的热水浴加热10min ,至几乎无棕红色气体放出为止。然后将此热溶液倒入100ml 的烧杯中,冷却后析出己二酸,抽滤,用15ml 冷水洗涤两次,干燥,粗产物约6克。 粗制的己二酸可以在水中重结晶。纯己二酸为白色棱状晶体,产量约5.1g ,mp 为153o C 。 [实验注意事项] 1. 环己醇和硝酸切不可用同一量筒量取。 2. 偏钒酸铵不可多加,否则产品发黄。
己二酸的合成
己二酸总结报告 中文名称:己二酸 英文名称:Adipic acid 中文别名:己二酸(电容器级);肥酸 英文别名:Hexanedioic acid; 1,4-Butanedicarboxylic acid~Hexanedioic acid; hexanedioate CAS号:124-04-9 分子式:C6H10O4 分子量:146.1264 SMILES:OC(=O)CCCCC(=O)O[1] 毒性: 草酸有毒。对皮肤、粘膜有刺激及腐蚀作用,极易经表皮、粘膜吸收引起中毒。空气中最高容许浓度为1m g/m3。 用途: 有机合成中间体,主要用于合成纤维(尼龙-66,大约占己二酸 总量的70%)其它的(30%) 在制备聚氨酯:PA-46,PA-66,PA-610,合成树脂,合成革,聚酯泡沫塑料,塑料增塑剂,润滑剂,食品添加剂,粘合剂,杀虫剂,染料,香料,医药等领域得以广泛应用。 危害: 草酸在人体内不容易被氧化分解掉,经代谢作用后形成的产物,属于酸性物质,可导致人体内酸碱度失去平衡,吃得过多还会中毒。 而且草酸在人体内如果遇上钙和锌便生成草酸钙和草酸锌,不易吸收而排出体外,影响钙与锌的吸收。 儿童生长发育需要大量的钙和锌。如果体内缺乏钙和锌,不仅可导致骨骼、牙齿发育不良,而且还会影响智力发育。
过量摄入草酸还会造成结石。 实验方法 1.环己烷一步氧化法: 此法优点是工艺流程短,可省去硝酸装置和一套氧化装置;但为防止深度氧化和腐蚀,必须在低温下长时间反应,并且这种条件易引起爆炸,生产能力和产率不高,产品分离亦较复杂 2.以过氧化氢为氧化剂生产己二酸: 工艺优点是产率高,对环境无污染;缺点是反应时间长,催化剂回收困难,工艺有待进一步完善。现阶段的研究主要集中在相转化剂和配位体 3.KMO4氧化环已醇制备已二酸: 工艺优点是产率高,对环境无污染,易控制,适合在实验室进行 二、实验原理 己二酸是合成尼龙-66的主要原料之一,它可以用硝酸或高锰酸钾氧化环己醇制得。 三、药品仪器 抽滤装置、100℃温度计、环己醇2.1mL 、高锰酸钾6g、氢氧化钠50mL0.3mol/L 、亚硫酸氢钠、浓盐酸、试纸。
己二酸的制备思考题完整版
己二酸的制备思考题集团标准化办公室:[VV986T-J682P28-JP266L8-68PNN]
己二酸的制备 1.在反应过程中,有环己烯存在时,温度计的读数会维持在72~80℃之间, 而不会随加热的程度而升高,为什么? 2.反应进行的过程中,必须确保回流冷凝管一直处于通水状态,为什么? 3.描述在反应过程中反应体系和催化剂的变化状况。催化剂能否再利用 4.由过氧化氢氧化环己烯制备1,2-环氧环己烷是否可行,为什么? 5、加料时,量过环己醇的量筒能否直接用来量取50%硝酸? 答:量过环己醇的量筒不可直接用来量取50%的硝酸。因为50%硝酸与残留的环己醇会剧烈反应,同时放出大量的热,这样一来,量取50%硝酸的量不准,而且容易发生意外事故。 6、量过环己醇的量筒为何要加少量温水洗涤且要将此洗液倒入加料用的滴液漏斗中 答:实验所用的环己醇的凝固点是21—24℃,因此在室温时是粘稠状的液体,极易残留在量筒里,所以要用温水洗涤量筒,并将其倒入滴液漏斗中,以免造成损失。另外,环己醇中加少量的水还可以防止滴液漏斗加料时堵塞漏斗的小孔,便于环己醇放尽。 7、用环己醇氧化制备己二酸时,为什么要在回流冷凝管的上端接气体吸收装置吸收此尾气 是用水还是用碱液好 答:由于环己醇被氧化成己二酸的同时会生成一氧化氮,一氧化氮遇到氧后就转变成有毒的二氧化氮。故应接上气体吸收装置,除去此尾气避免造成污染和中毒。由于 在水中溶解度不大,因此用碱液吸收更好。 酸性的NO 2 8、为什么有些实验在加入最后一个物料之前,都要先加热前面的物料(如己二酸制备实验 中就得先预热到50—60℃) 答:不论是吸热反应还是放热反应都需要活化能。对活化能较高的一些反应(室温时仍达不到其活化能的),都需通过外部加热供给能量,使其达到所需要的活化能。 9、制备己二酸实验的操作关键是什么说明其原因 答:控制环己醇的滴加速度是制备己二酸实验的关键。因为此反应是一个强放热的反应,所以必须等先加入反应瓶中的少量环己醇作用完全后才能继续滴加。若滴加太快,反应过于剧烈,无法控制,会使反应液冲出烧瓶造成事故。滴加太慢,反应进行的缓慢,需要的时间太长。所以操作时应控制滴加环己醇的速度,维持反应液处于微沸状态。 10、制备己二酸时,你如何控制反应温度? 答:在未加入最后一个物料环己醇之前,先预热反应瓶中的稀硝酸接近沸腾。在振摇下,慢慢滴加5—6滴环己醇,反应发生同时放出热量。这时应控制滴加环己醇的速度,维持反应液呈微沸状态,直至滴加完所有的环己醇。若反应液出现暴沸时,应及时用冷水浴冷却至微沸状态。注意不能冷却太久,否则,又得重新加热,才能继续发生反应。 11、用硝酸法制备己二酸时,为什么要用50%的硝酸而不用71%的浓硝酸?
己二酸合成.
用分子氧一步法催化氧化环己烷制备己二酸 表面催化研究中心,化学系,雷丁大学,校区,雷丁,英国RG66广告 2006年6月1日收到,2006年6月29日受理 用锰-钴转变的合金和羟基临苯二甲酰亚胺作催化剂,在温度353K用分子氧一步氧化环己烷制备己二酸,得到生成氧化物大于95%的选择性,以己二酸为主的转化产率为78%。74%的部分氧化被记录下来。 关键词:己二酸,一步氧化,催化剂,环己烷氧化,羟基临苯二甲酰亚胺,自由基,选择性1.前言 值得注意的研究努力已被付出去研究有效地方法,为了环己烷未活化的C-H键的氧化,因为考虑到工业和合成方面基板的重要性。 已经用不同的氧化剂探讨烷烃类的催化氧化,在温和条件下用分子氧的反应是可行的,归因于他的廉价的有效性和只有产物水为无污染的副产物。 然而,环己烷的氧化在所有主要工业生产过程中表现出很低的效率。 目前,工业氧化环己烷制备己二酸经历了两步过程。第一步包括了环己烷氧化成环己酮和环己醇(KA油),在约温度423K和1-2MPa压力条件下,用可溶性钴催化剂或无催化剂,在液相中,所有环己烷转化率低于4%。 在这样低的转化下朝向环己醇和环己酮的选择性可以优化到70%-85%,没有太多产物的过氧化。第二步历程包括了KA油的氧化制成己二酸,通过硝酸作为温和氧化剂的使用。 这一步产生的副产物包括一氧化二氮(N2O),它显示的全球变暖效率比二氧化碳高300倍。提高这两步反应选择性的研究还在继续。例如,向氧化混合物中加入硼酸被证明是有效的,它允许约环己烷的10%转化朝向KA油有90%的选择性。 Murahashi等人指出环己烷在铁粉上的氧化,观察到11%的转化率,生成KA油95%的选择性。 然而,寻求一步法从环己烷生产己二酸且没有NOx生成,从绿色化学角度是迫切的事情。Tomas和他的同事做了些很有意思的工作,在气相(无溶剂)中用分子筛催化剂在活性部位隔离直接氧化环己烷制备己二酸。 在类似的研究中,Moden 等人已经声明了为了环己烷氧化反应的MnAPO-5催化剂的选择性性质。 从反应机械论方面考虑环己烷制备己二酸的关键难题,它可能需要催化体系去激活分子的C-H键,可能通过烷基自由基的一代,一个C-C键的明确断裂造成开环,在终端形成酸官能度更进一步的氧化之前。 然而,产物和反应中间体含C-H和C-C键,将在高度转化中同样易受相同催化体系的进攻。已经有一些尝试,在有自由基引发剂热力过程下首先聚集烷基自由基。 但是,这自动氧化过程需要严格的反应条件,反应需在高温下进行。 在这样的条件下,C-H键和C-C键的均裂分裂都对于合成己二酸将有很低选择性。 至今为止,还没有满意的一般方法,去在温和条件下环己烷碳氢键的均裂分歧去选择的生成碳自由基。 为了实现它,一种在温和条件下让碳自由基增长的新方法是被需要的。这样一种方法对于有机合成可能变成一种不可或缺的工具。 目前,学者们发现PINO自由基,产生于羟基邻苯二甲酰亚胺,在温和条件下,从不同烃类包括烷烃类,醇类,酯类,缩醛类,还有醛类等的碳氢键摘取一个氢原子,形成相应的碳自由基,有很高的选择性和高催化效率。 羟基邻苯二甲酰亚胺已被命名为“碳自由基生成催化剂”(这在此后为CRPC)。这NHPI能
己二酸制备
实验报告 尼龙66前体的制备
一、实验目的 1、学习由环己醇氧化制备环几酮和由环几酮氧化制备己二酸的基本原理。 2、掌握由环己醇氧化制备环己酮和由环己酮氧化制备己二酸的实验操作。 3、进一步了解盐析效应及萃取在分离有机化合物中的应用。 4、综合训练并掌握控温、减压抽滤、蒸馏、重结晶等操作技能。 二、实验原理 实验室制备脂肪和脂环醛、酮最常用的方法是将伯醇和仲醇用铬酸氧化。铬酸是重铬酸盐与40-50%硫酸的混合液。制备相对分子量低的醛,可以将铬酸滴加到热的酸性醇溶液中,以防止反应混合物中有过量的氧化剂存在,同时将较低沸点的醛不断蒸出,可以达到中等产率。尽管如此,仍有部分醛被进一步氧化成羧酸,并生成少量的酯。用此法制备酮,酮对氧化剂比较稳定,不易进一步被氧化。铬酸氧化醇是放热反应,必须严格控制反应温度以免反应过于剧烈。 本实验反应方程式为: 羧酸常用烯烃、醇、醛、酮等经硝酸、重铬酸钾的硫酸溶液或高锰酸钾等氧化来制备。本实验以环己酮为原料,在碱性条件下以高锰酸钾为氧化剂来制备己二酸,反应方程式: C6H10O+MnO4-+2OH-→HOOC(CH2)4COOH+MnO2+H2O 三、实验试剂和仪器装置: 1、仪器: 圆底烧瓶(250ml,100ml),烧杯(250ml,100ml) ,量筒(100ml ,10ml),,直型冷凝管,尾接管,蒸馏头,温度计,电热套,抽滤瓶,布氏漏斗,真空泵,蒸发皿,表面皿,分液漏斗,玻璃棒,石棉网,铁架台,酒精灯。 2、主要试剂: 浓H2SO4,Na2Cr2O7,H2C2O4,NaCl,无水MgSO4,KMnO4,NaOH10%,Na2SO3 3、主要实验装置:
己二酸生产工艺详解(图)
3.1.2 工艺流程及排污节点 本项目以精苯为原料,通过选择加氢生成环己烯,环己烯水合生成环己醇,环己醇经硝酸氧化生成己二酸。其中氢气以甲醇合成驰放气为原料,采用变压吸附技术生产;硝酸以液氨为原料,采用双加压法生产。主体工艺流程框图见图3.1-1,生产工艺污染源排放节点一览表见表31-14。 图3.1-1 己二酸生产主体工艺流程框图 3.1.2.1 制氢装置工艺流程及排污节点 本装置采用8-2-4PSA工艺流程,即:装置的8个吸附塔中有2个吸附塔始终处于进料吸附的状态。其吸附和再生工艺过程由吸附、连续四次均压降压、顺放、逆放、冲洗、连续四次均压升压和产品气升压等步骤组成。 制氢装置产生的污染物为安全阀排放气(G1)、生产不正常排放气(G2)、解析气(G3)、废气中主要污染物CH4、CO、H2,送火炬进行焚烧处理。 3.1.2.2 硝酸装置工艺流程及排污节点 项目采用氨氧化法生产硝酸,其生产过程包括氨-空混合气制备、氨的氧化和热能回收、一氧化氮氧化及吸收等工序,硝酸装置生产及排污工艺流程图见图3.1-2.。
图3.1-2 硝酸装置生产及排污工艺流程图 3.1.2.3 环己醇装置工艺流程及排污节点 项目采用环己烯法制环己醇,其生产过程包括苯加氢、萃取精馏、水合、环己烷精制、加氢催化剂再生、水合催化剂再生等工序,环己醇装置生产及排污工艺流程图见图3.1-3。
图3.1-3 环己醇装置排污节点图 3.1.2.4 己二酸装置工艺流程及排污节点 己二酸是以铜和钒作催化剂,用硝酸氧化环己醇反应生成,然后经过结晶、增浓、离心得到粗己二酸。粗己二酸经溶解、活性炭脱色再经过结晶、增浓、离心、干燥后得到精己二酸产品。后续系统包括:氧化氮气体回收、硝酸浓缩、催化剂及己二酸回收。己二酸装置生产及排污工艺流程图见图3.1-4。溶剂
己二酸的制备
己二酸的制备文档编制序号:[KKIDT-LLE0828-LLETD298-POI08]
己二酸的制备 一、实验目的 1.学习环己醇氧化制备已二酸的原理和了解由醇氧化制备羧酸的常用方法。 2.熟悉电动搅拌,抽滤等实验技术。 3.熟练掌握熔点的测定技术。 二、实验原理 己二酸(ADA),又称肥酸。常温下为白色晶体, 熔点152 ℃,沸点℃。 主要用途:有机合成中间体,主要用于合成纤维 (尼龙-66,大约占己二酸总量的70%)其 它的 (30%) 在制备聚氨酯:PA-46,PA-66,PA-610,合成树脂,合成革,聚酯泡沫塑料, 塑料增塑剂,润滑剂,食品添加剂,粘合剂,杀虫剂,染料,香料,医药等领域得以广泛应用。 产量情况 1902年首次合成。目前世界产量大约 Mt/a,并以% 年增长率增长。 其中世界上最大的5 家企业是: Dupont Mt/a)、Rhodia (417 kt/a)、Solutia (385 kt/a)、BASF (240 kt/a) 和旭化成 (112 kt/a)。 2002年我国年生产能力12万t/a (巴陵石化,辽阳石化,太原化学,上海燎原化工,神马集团),市场消费量约为万t/a。预计2010年全球ADA生产能力有望达到 Mt/a。 制备羧酸最常用的方法是烯、醇、醛等的氧化法。常用的氧化剂有硝酸、重铬酸钾(钠)
的硫酸溶液、高锰酸钾、过氧化氢及过氧乙酸等。但其中用硝酸为氧化剂反应非常剧烈,伴有大量二氧化氮毒气放出,既危险又污染环境。因而本实验采用环己醇在高锰酸钾的碱性条件发生氧化反应,然后酸化得到已二酸。 反应式 环己醇 环己酮 己二酸 OH MnO 338H 2+KMnO 4+HO 2C (CH 2)4CO 2H ++8KOH 8三、仪 器和药品 抽滤装置、100℃温度计、环己醇、高锰酸钾、氢氧化钠、亚硫酸氢钠、浓盐酸、试纸。 四、实验步骤 1.安装反应装置,在烧杯中加入6g 高锰酸钾和L 氢氧化钠溶液,搅拌加热至35℃使之溶解,然后停止加热; 2.在继续搅拌下用滴管滴加环己醇,控制滴加速度,维持反应温度43~47℃,滴加完毕后若温度下降,可在50℃的水浴中继续加热,直到高锰酸钾溶液颜色褪去。在沸水浴中将混合物加热几分钟使二氧化锰凝聚; 3. 待反应结束后,在一张平整的滤纸上点一小滴混合物以试验反应是否完成,如果观察到试液的紫色存在,可加入固体亚硫酸氢钠来除去过量的高锰酸钾。趁热抽滤,滤渣二氧化锰用少量热水洗涤3次,每次尽量挤压掉滤渣中的水分; 4.滤液用小火加热蒸发使溶液浓缩至原来体积的一半,冷却后再用浓盐酸酸化至pH 值为2~4止。冷却析出结晶,抽滤后得粗产品 ; 5.将粗产物用水进行重结晶提纯。然后在烘箱中烘干。 五 注意事项
实验8 己二酸的合成(高锰酸钾法)
实验8 己二酸的合成(高锰酸钾法) 4学时 每组带瓶开水 一、实验目的 1.学习用环己醇氧化制备己二酸的原理和方法。(应知) 2.掌握电动搅拌器的使用方法及浓缩、过滤等基本操作。(应会) 二、实验原理 OH MnO 3 38H 2+KMnO 4+ HO 2C (CH 2)4CO 2H ++8KOH 8 四、电动搅拌装置安装要点 1.搅拌器的轴与搅拌棒在同一直线上。 2.先用手试验搅拌棒转动是否灵活,再以低转速开动搅拌器,试验运转情况。 3.搅拌棒下端位于液面以下,以离烧杯底部3~5 mm 为宜。 4.温度计应与搅拌棒平行且伸入液面以下。 五、仪器和试剂 仪 器:搅拌回流加热装置1套,抽滤装置1套,玻棒,500mL 烧杯1个,滴管1个。 试 剂:环己醇2g(2.1mL,约0.02mol),高锰酸钾6.3g(0.038mol),10%氢氧化钠溶液5mL ,浓盐酸 4mL,固体亚硫酸氢钠,广泛pH 试纸,滤纸 六、实验步骤 在装有搅拌装置、温度计和回流冷凝管的100mL 三颈(或四颈瓶)瓶中加入5mL10%氢氧化钠溶液(或0.5gNaOH 固体)和50mL 水,搅拌使其溶解,然后加入6.3g 高锰酸钾。小心预热溶液到40o C ,高锰酸钾溶解后,从冷凝管上口【也可四颈烧瓶的一个口滴管加入,漏气关系不大】用滴管缓慢滴加2.1mL 环己醇[1] ,【滴1滴休息3秒左右】反应随即开始(放热)。控制滴速,使反应温度维持在45o C 左右[2] 。滴完,反应温度开始下降时,水浴保温45o C 左右【55度左右的水浴】,继续搅拌保温20min 后,在沸水浴上加热5min ,促使反应完全并使MnO 2沉淀凝聚 [3] 。 用玻璃棒蘸一滴反应混合物点到滤纸上做点滴实验。如有高锰酸盐存在,则在棕色二氧化锰点的周围出现紫色的环,可加入少量【0.1g 左右】固体亚硫酸氢钠直到点滴试验呈阴性为止。 趁热抽滤混合物,用少量热水【溶剂尽量少,否则后面蒸发时间很长】洗涤滤渣MnO 23次,将洗涤液与滤液合并置于烧杯中。若溶液带黄色,加入少许活性炭,煮沸过滤【锥形瓶内做,防止溶剂挥发,活性炭可以稍微多点】,可得无色滤液。加热浓缩使溶液体积减少至10mL 左右,冷却后,
己二酸的制备
实验二己二酸的制备 一、实验目的 1、练习并熟练掌握液体的搅拌、浓缩、过滤、重结晶等基本操作; 2、了解KMnO4氧化环己醇制备己二酸的原理和方法。 二、实验原理 叔醇一般不易被氧化,仲醇氧化得到酮,酮遇到强氧化剂KMnO4、HNO3等时可以被氧化,碳链断裂生成多种碳原子数较少的羧酸混合物。环己酮是环状结构,控制好反应温度,氧化断裂后得到单一产物——己二酸。 环己酮是对称酮,在碱作用下只能得到一种烯醇负离子,氧化生成单一化合物,若为不对称酮,就会产生两种烯醇负离子,每一种烯醇负离子氧化得到的产物不同,合成意义不大。 三、实验药品及物理常数 四、主要仪器名称、规格 烧杯300ml 150ml 温度计 滴管玻璃棒 抽滤装置1套
五、主要试剂、用量 环己醇 2.1ml(2g 约0.02mol)KMnO4 8.5g(约0.053mol) 10%NaOH溶液5ml浓HCl 4ml 活性炭NaHSO4 (备用) 六、实验步骤、现象记录 八、产率计算: m理论=nM=2.0÷100.16×146.14=2.92g 产率w=m实际÷m理论×100%=1.35÷2.92=46.23% 九、思考题 1、在实验过程中为什么必须控制反应温度和环己醇的滴加速度? 答案:因为该反应为放热反应,控制好反应温度和环己醇的滴加速度,其目的均在于反应能在一个较为理想的条件下进行,若反应温度太高,产物中可能会有其他副产物生成(碳键断裂,形成羧酸)温度太低,又阻碍了反应的进行。 2.为什么有些实验在加入最后一个反应物前要预热,而开始滴加时却又不能滴加的太快?反应开始反而可以适当的加快加料速度,原因何在? 答案:预热是为了提供一个适宜的反应条件; 反应开始时速度较慢,若滴加速度过快,会使环己醇积聚,反应进行过程中又释放出大量的热量,不利于得到单一产物;反应开始后,反应速度较快,可以适当的加快滴加的速度,此时环己醇能及时的反应。
己二酸的制备实验报告
实验八己二酸的制备 一、实验目的 1、学习环己醇氧化制备己二酸的原理和方法; 2、掌握浓缩、过滤及重结晶等操作技能 二、实验原理 三、实验药品及其物理常数 化 合物名称 分子 量 性 状 比重 (d ) 熔点 (℃) 沸点 (℃) 折光 率 (n) 溶解度 水 乙 醇 乙醚 环 己醇100.16 液体 或晶 体 0.962425.2161 1.4613.520 可 溶 可溶 高 锰酸钾158.04 斜方 晶体 2.703 240 分解 -- 830 32.75 难 溶 不溶 己 二酸146.14 单斜 晶棱 柱体 1.360151-3265-100 易 溶 0.615
环己醇:2g 2.1ml(0.02mol);高锰酸钾6g(0.038mol); 0.3N氢氧化钠溶液 50ml;亚硫酸氢钠;浓盐酸 四、主要仪器和材料 水浴锅三口烧瓶(100 mL、19#×3) 恒压滴液漏斗空心塞(14#) 球形冷凝管(19#) 螺帽接头(19#,2只) 温度计(100℃) 布氏漏斗吸滤瓶烧杯冰滤纸水泵等. 氧化剂可用浓硝酸、碱性高锰酸钾或酸性高锰酸钾。本实验采用碱性高锰酸钾作氧化剂 五、实验装置 六、操作步骤 (1)向250ml烧杯内加入50ml 0.3N氢氧化钠溶液,置于磁力搅拌上; (2)边搅拌边将6g 高锰酸钾溶解到氢氧化钠溶液中; (3)用滴管滴加2.1ml 环己醇到上述溶液中,维持反应物温度为43~47 ℃。 (4)当醇滴加完毕且反应混合物温度降低至43 ℃左右时,沸水浴将混合物加热,使二氧化锰凝聚。
(5)在一张平整的滤纸上点一小滴混合物以试验反应是否完成,如果观察到试液的紫色存在,那么可以用少量固体亚硫酸氢钠来除掉过量的高锰酸钾。 (6)趁热抽滤,滤渣二氧化锰用少量热水洗涤3次(每次2 mL),每次尽量挤压掉滤渣中的水分; (7)合并滤液和洗涤液,用4ml浓盐酸酸化至pH2.0; (8)小心地加热蒸发使溶液的体积减少到10ml左右,冷却,分离析出的己二酸。 (9)抽滤、洗涤、烘干、称重、计算产率。 (10)测量产品的熔点和红外光谱,并与标准光谱比较。【操作要点及注意事项】 1.KMnO4要研细,以利于KMnO4充分反应。 2. 滴加:本实验为强烈放热反应,所以滴加环己醇的速度不宜过快(1-2滴/秒),否则,因反应强烈放热,使温度急剧升高而引起爆炸。 3.严格控制反应温度,稳定在43~47℃之间。 4.反应终点的判断: (1)反应温度降至43℃以下。 (2)用玻璃棒蘸一滴混合物点在平铺的滤纸上,若无紫色存在表明已没有KMnO4。 5.用热水洗涤MnO2滤饼时,每次加水量约5~10 ml,不可太多。 6.用浓盐酸酸化时,要慢慢滴加,酸化至pH=1~3。 7.浓缩蒸发时,加热不要过猛,以防液体外溅。浓缩至10 ml 左右后停止加热,让其自然冷却、结晶。 8. 环己醇常温下为粘稠液体,可加入适量水搅拌,便于用滴管滴加; 9. 此反应是放热反应,反应开始后会使混合物超过45℃,假如在室温下反应开始5min后,混合物温度还不能上升至45℃,则可小心温热至40℃,使反应开始; 10. 要不断振摇或搅拌,否则极易爆沸冲出容器; 11. 最好是将滤饼移于烧杯中,经搅拌后再抽滤;
