低温高活性甲醇水蒸气重整制氢催化剂的研究

低温高活性甲醇水蒸气重整
制氢催化剂的研究
李永红,任杰,孙予罕
(中科院山西煤炭化学研究所煤转化国家重点实验室,太原 030001)
摘要:研究了Cu/La 2O 3/Zr O 2基催化剂在甲醇水蒸气重整制氢反应中的反应活性、选择性及其还原行为,并考察了反应条件(温度、水醇比、液体空速)对活性和选择性的影响。结果表明:Cu/La 2O 3/Zr O 2基催化剂在甲醇水蒸气重整制氢反应过程中显示出较好的反应活性和高的选择性。在常压、反应温度190~240 、液体空速为1 0~3 0h -1和水醇摩比为1~3 0的反应条件下,甲醇转化率随着反应温度的升高而增大,重整产物中CO 含量有所增加;提高水醇比有利于提高甲醇转化率,同时可降低重整产物中CO 含量;甲醇转化率随着液体空速的增加有所降低,而重整产物中CO 含量也有所降低。在Cu/L a 2O 3/ZrO 2基催化剂上,甲醇重整反应和水-汽变换反应有可能同时进行。
关键词:氢气;甲醇水蒸气重整;催化剂
中图分类号:T Q 426 文献标识码:A 文章编号:1001-9219(2001)01-05-03
收稿日期:2000-11-27;基金来源:山西省自然科学基金项目 (20001019);作者简介:李永红,女,1965年生,助理研究员。
0 前言
甲醇水蒸气重整制氢是近年来发展较快的制氢方法,该方法与传统电解法、烃类蒸汽转化法相比,具有操作方便、原料易得、工艺流程短、反应条件温和、副产物少等优点[1],而且装置规模大小均宜,并可做成可移动的装置来满足不同用户对氢源的要求。因此,这一制氢方法受到许多研究者的广泛重视[2,3]。目前,对甲醇水蒸气重整制氢反应研究较多的有合成甲醇用Cu/ZnO/Al 2O 3催化剂和在此基础上的改性[5,6]
,以及在Cu/Al 2O 3催化剂上添加各种助剂等[4],它们的反应温度大多在260~300 ,并且抗烧结能力较差。中国科学院山西煤化所近年来在甲醇水蒸气重整制氢催化剂上进行了大量研究工作,采用共沉淀法制备的Cu/La 2O 3/ZrO 2基催化剂,在甲醇水蒸气重整制氢反应过程中显示出良好的低温活性和高的选择性。本试验考察了Cu/La 2O 3/ZrO 2系列催化剂的催化活性及其还原行为,并研究了反应条件(温度、水醇比、液体空速)对Cu/La 2O 3/ZrO 2基催化剂活性和选择性的影响。
1 实验部分
1 1 催化剂的制备
[7]
将催化剂各组分的盐溶液混合,用碳酸钠溶液为沉淀剂,采用并流共沉淀法,在恒温、搅拌和一定pH 值下进行沉淀,经老化、洗涤、烘干和焙烧后,完成催化剂的制备。使用时将催化剂研磨至20~40目。
1 2 催化剂的活性评价及测试
催化剂活性评价采用常压连续流动式固定床反应器,内径为8mm 。先对催化剂进行预还原处理,还原条件为:氢气流量50m l/min,程序升温至350 ,在该温度下还原活化催化剂2h 后,临氢降温至180 ,切换成甲醇和水混合液进行反应。反应后气体经冰水浴冷却后,用GC -920气相色谱仪的热导检测器通过六通阀进行在线分析,液体样品用氢火焰检测器进行分析。
1 3 程序升温还原(TPR)
催化剂的TPR 试验是在不锈钢微反装置上进行,催化剂装填量为0 1g(40~60目),用氢含量为5%的氢氩混合气以40ml/m in 的流速通过催化剂,待系统稳定后,以10 /min 的升温速率从333K 升至723K,其间氢消耗信号用热导检测器检测。
2 结果与讨论
2 1 催化剂组成对其还原行为的影响
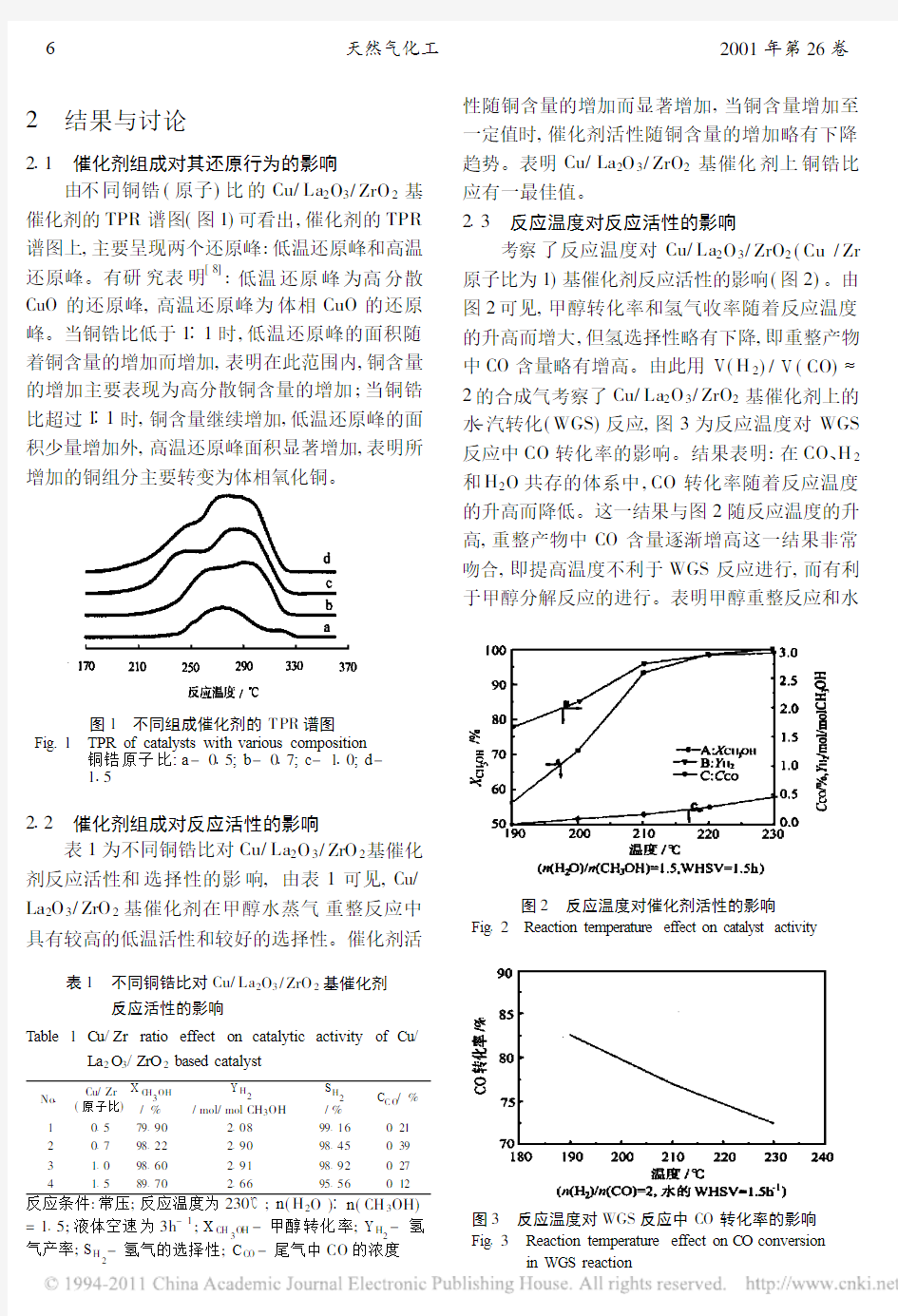
由不同铜锆(原子)比的Cu/La 2O 3/ZrO 2基催化剂的TPR 谱图(图1)可看出,催化剂的TPR 谱图上,主要呈现两个还原峰:低温还原峰和高温还原峰。有研究表明[8]
:低温还原峰为高分散CuO 的还原峰,高温还原峰为体相CuO 的还原峰。当铜锆比低于1 1时,低温还原峰的面积随着铜含量的增加而增加,表明在此范围内,铜含量的增加主要表现为高分散铜含量的增加;当铜锆比超过1 1时,铜含量继续增加,低温还原峰的面积少量增加外,高温还原峰面积显著增加,表明所
增加的铜组分主要转变为体相氧化铜。
图1 不同组成催化剂的T PR 谱图
Fig.1 TPR of catalysts with various composition
铜锆原子比:a -0 5;b -0 7;c -1 0;d -1 5
2 2 催化剂组成对反应活性的影响
表1为不同铜锆比对Cu/La 2O 3/ZrO 2基催化剂反应活性和选择性的影响,由表1可见,Cu/La 2O 3/ZrO 2基催化剂在甲醇水蒸气重整反应中具有较高的低温活性和较好的选择性。催化剂活
表1 不同铜锆比对Cu/L a 2O 3/ZrO 2基催化剂
反应活性的影响
Table 1C u/Zr ratio effect on catalytic activity of Cu/
La 2O 3/ZrO 2based catalyst
No Cu/Zr (原子比)X C H 3OH /%Y H
2
/mol/mol CH 3OH
S H
2
/%C C O /%10 579 902 0899 160 2120 798 222 90
98 450 3931 098 602 9198 920 274
1 5
89 70
2 66
95 56
0 12
反应条件:常压;反应温度为230 ;n (H 2O ) n (CH 3OH)
=1 5;液体空速为3h -1;X CH 3O H -甲醇转化率;Y H 2-氢气产率;S H 2
-氢气的选择性;C CO -尾气中CO 的浓度
性随铜含量的增加而显著增加,当铜含量增加至一定值时,催化剂活性随铜含量的增加略有下降趋势。表明Cu/La 2O 3/ZrO 2基催化剂上铜锆比应有一最佳值。
2 3 反应温度对反应活性的影响
考察了反应温度对Cu/La 2O 3/ZrO 2(Cu /Zr 原子比为1)基催化剂反应活性的影响(图2)。由图2可见,甲醇转化率和氢气收率随着反应温度的升高而增大,但氢选择性略有下降,即重整产物中CO 含量略有增高。由此用V (H 2)/V (CO) 2的合成气考察了Cu/La 2O 3/ZrO 2基催化剂上的水-汽转化(WGS)反应,图3为反应温度对WGS 反应中CO 转化率的影响。结果表明:在CO 、H 2和H 2O 共存的体系中,CO 转化率随着反应温度的升高而降低。这一结果与图2随反应温度的升高,重整产物中CO 含量逐渐增高这一结果非常吻合,即提高温度不利于WGS 反应进行,而有利
于甲醇分解反应的进行。表明甲醇重整反应和水
图2 反应温度对催化剂活性的影响
Fig 2 Reaction tem perature effect on catalyst
activity
图3 反应温度对WGS 反应中CO 转化率的影响Fig 3 Reaction temperature effect on C O conversion
in WGS reaction
气变换反应在Cu/La 2O 3/ZrO 2基催化剂上有可能同时进行,其竞争反应和作用机理还有待进一步研究。
2 4 水醇比对反应活性的影响
图4是水醇比对Cu/La 2O 3/ZrO 2(Cu /Zr 原子比为1)基催化剂反应活性的影响。在同样反应温度和液体空速的条件下,甲醇转化率和氢气收率随水醇比增大而增加,表明提高水醇比有利于提高甲醇转化率,同时可降低重整产物中的CO
含量。
图4 水醇比对催化剂反应活性的影响
Fig 4 H 2O/C H 3OH ratio effect on catalyst
activity
图5 液体空速对催化剂反应活性的影响Fig 5 Liquid space v elocity effect on catalyst activ ity
2 5 液体空速对反应活性的影响
图5是液体空速对Cu/La 2O 3/ZrO 2(Cu/Zr 原子比为1)基催化剂反应活性的影响。在同样反应温度和水醇比条件下,甲醇转化率和氢气收率随液体空速增大有所下降,但重整产物中CO 含量有所降低。表明在Cu/La 2O 3/ZrO 2基催化剂
上,甲醇吸附重整为一控制步骤,而水气变换反应速度可能较快,在此也进一步表明在该体系催化剂上甲醇重整反应和水气变换反应可能同时发生。
3 结论
(1)Cu/La 2O 3/ZrO 2基催化剂对甲醇水蒸气重整反应具有良好的低温活性和高的选择性。提高铜含量有利于提高催化剂活性,但在甲醇水蒸气重整反应过程中,铜锆比应有一最佳值。(2)当Cu/Zr 原子比为1的Cu/La 2O 3/ZrO 2
基催化剂,在常压、反应温度190~240 、液体空速为1 0~3 0h -1和水醇摩比为1~3 0的反应条件下,甲醇转化率和氢气收率随着反应温度的升高而增大,但重整产物中C O 含量略有增高;提高水醇比有利于提高甲醇转化率,同时可降低重整产物中CO 含量;甲醇转化率随着液体空速的增加有所降低,同时重整产物中C O 含量也有所降低。
(3)在Cu/La 2O 3/ZrO 2基催化剂上,甲醇重整反应和水气变换反应有可能同时进行。
参考文献
[1] 钱新荣 甲醇制氢技术的经济特性[J] 石油化工,
1988,17(5):317-321.
[2] 郝树仁,李言浩,程玉春,等 甲醇蒸汽转化制氢技
术[J] 精细化工,1988,15(5):52-54
[3] I dem R O,Bakhshi N N,Productio n of hydr ogen from
methanol 2 Ex perimental studies [J ] Ind.Eng.
Chem.Res.,1994,33:2047-2055
[4] Hor at io A garas and Craciela Cerr ella,Copper catalysts
for t he steam refor ming of methanol[J] Appl Catal ,1988,45:53-60
[5] B A Peppley,J C Amphlett,L M K earns,et al ,
M ethano-l steam r eforming on Cu/ZnO/Al 2O 3[J] A ppl Catal A,1999,179:21-49
[6] 陈兵,董新法,林维明 甲醇水蒸气重整反应制氢
的研究[J] 天然气化工,2000,25(2):1-3 [7] 中科院山西煤化所 一种甲醇水蒸气重整制氢催
化剂及其应用方法[P] 中国专利:00121571 X [8] 吴贵升 Cu/Zr 基合成醇催化剂各组元协同效应及
其助剂效应的研究[D] 太原:中科院山西煤化所,2000
Production of hydrogen from the low-temperature methano-l steam reforming
L I Yong-hong,REN J ie,S UN Y u-han
(State Key Laboratory of Coal Conversion,Institute of Coal Chemistry,Chinese Academy of Sciences,Taiyuan030001,China)
A series of Cu/La2O3/ZrO2catalysts were studied for production of hydrogen from methano-l steam re-form ing,w hile the reactive conditions(reaction temperature,feed ratio etc )have also been tested The re-sults show that Cu/La2O3/ZrO2catalysts have high low-temperature activity and good selectivity The reac-tion conditions were investigated using Cu/La2O3/ZrO2(Cu Zr=1)catalyst over a temperature190~ 230 ,methano-l w ater space velocities(WHSV)1 0~3 0h-1and w ater:methanol molar ratio1 0~3 0 It showed that methanol conversion and CO concentration in the overall products increased w ith reaction temperature;Methanol conversion and CO concentration decreased w ith methano-l w ater WHSV increase; CO concentration decreased,methanol conversion increased w ith the w ater:m ethanol ratio going up The experimental results also indicated that methanol reforming and w ater g as shift(WGS)reactions maybe take place simultaneously
Key words:hydrogen;met hano-l steam reforming;catalyst
(上接第4页)
Study on the Ag-SAPO-34automobile exhaust catalyst under lean-burn condition
WA N G L e-f u1,L i X ue-hui1,T A N Yu-x in2,X U Shou-chong1
(1 Department of Chemical Engineering,South China University of T echno logy,Guangzhou510640,China;2 Guangzhou City Committee of Communications,China)
T he effects of preparation technique and reaction conditions of Ag-SAPO-34catalyst on the catalyst ac-tivity are studied The Ag-SAPO-34catalyst w hich is active at low temperature has been prepared,on w hich the highest conversion of NO reduction to N2is74 1%at the ox ygen concentration of3 6Vol % and the temperature of340 The most suitable pH value of the ion ex changed Ag NO3solution and ion ex-changed temperature are7 0and40 respectively,and the calcined temperature is600 T he catalytic activity rises w ith the concentration of C3H6and decreases w ith GH SV
Key words:lean-bur n condition;automobile ex haust;A g-SA PO-34catalyst;activity
甲醇水蒸汽重整制氢催化剂甲醇还原方案
甲醇水蒸汽重整制氢催化剂甲醇还原方案 甲醇水蒸汽重整制氢催化剂的还原活化原则上应用H2还原剂,可以得到高的催化活性,在对转化率要求不太严格的情况下可以采用甲醇作为还原剂,但可能造成约10%活性损失。 催化剂的装填采用阶梯式装填方式可得到较好的温度分布。可以用相应颗粒大小的石英砂作为补充以形成催化剂的梯度分布,由入口到出口阶梯式增加催化剂的用量。 催化剂的还原温度和使用温度对催化剂的活性及寿命影响很大,严禁出现超温现象。当温度>320℃易形成积碳,铜烧结,催化剂的活性显著降低甚至失活。 现根据适当的资料就甲醇作为还原剂,提供如下方案以供参考。 1,催化剂的升温 1.1升温介质 通常情况下应用氮气作为升温介质,当氮气不便时也可应用空气作为升温介质。但还原阶 段的升温应用还原剂的气态组分作为升温用介质。 1.2升温的空速 考虑到小反应器,由于放热量有限,拟采用相对较小的空速,一般为2.0~4.0h-1。还原初期,当反应放热较大时,宜采用较低的空速,以方便温度的控制。 1.3升温中注意事项 MW-612型催化剂在升温过程中,于50~130℃之间可能发生温升较慢的现象,这是因为催 化剂在脱除制备过程中加入的物理水有关。 1.4催化剂的还原 MW-612型催化剂的H2还原的特点是速度快,当利用甲醇还原时,受甲醇分子结构的影响,需采用较高的甲醇分压以利于甲醇的渗透和与催化剂表面的接触,所以适当的提高系统压力对催化剂还原时有益和必须的。还原实践证明,进口温度为180℃,催化剂可在较低甲醇浓度下完成还原反应。 1.4.1还原剂 甲醇水,甲醇:水=1:0.2~1,甲醇中不含氯、硫和油,水用去离子水。 1.4.2甲醇与水的比,刚开始时,利用较小的液空速,较高的甲醇含量,以利于氧化铜的还原和水分的排除,随着还原反应的进行,逐渐提高水的比例。甲醇、水的比例可根据流量泵的流量来调整,计量应准确,应根据反应床层的温度变化随时调整,防止催化剂床层飞温,造成催化剂活性的降低。 1.4.3还原温度
甲醇重整制氢装置项目可研报告备案用(专业版)
甲醇重整制氢装置项目可研报告 (备案用/专业版) 普慧投资研究中心
甲醇重整制氢装置项目可研报告 (备案用/专业版) 项目负责人:齐宪臣注册咨询工程师 参加人员:郑西芳注册咨询工程师 胡冰月注册咨询工程师 王子奇高级经济师 杜翔宇高级工程师 项目审核人:张子宏注册咨询工程师 普慧投资研究中心
目录 甲醇重整制氢装置项目可研报告常见问题解答 .... 错误!未定义书签。 1、甲醇重整制氢装置项目应该在经信委还是发改委立项? (1) 2、编制甲醇重整制氢装置项目可研报告企业需提供的资料清单 (1) 一、总论 (2) (一)项目背景 (2) 1、项目名称 (2) 2、建设单位概况 (2) 3、可研报告编制依据 (2) 4、项目提出的理由与过程 (3) (二)项目概况 (3) 1、拟建项目 (3) 2、建设规模与目标 (3) 3、主要建设条件 (3) 4、项目投入总资金及效益情况 (4) 5、主要技术经济指标 (4) (三)主要问题说明 (6) 1、项目资金来源问题 (6) 2、项目技术设备问题 (6) 3、项目供电供水保障问题 (6) 二、市场预测 (7) (一)甲醇重整制氢装置市场分析 (7) 1、国际市场 (7) 2、国内市场 (7) (二)主要竞争企业分析(略) (8) (三)目标市场分析 (9) 1、目标市场调查 (9) 2、价格现状与预测 (10) (四)营销策略 (10)
1、销售队伍建设 (10) 2、销售网络建设 (10) 3、销售策略 (10) 三、建设规模与产品方案 (12) (一)建设规模 (12) (二)产品方案 (12) 四、场址选择 (13) (一)场址所在位置现状 (13) 1、地点与地理位置 (13) 2、场址土地权属类别及占地面积 (13) 3、土地利用现状 (14) (二)场址建设条件 (14) 1、地理环境位置 (14) 2、地形、地貌 (14) 3、气候、水文 (14) 4、交通运输条件 (14) 5、公用设施社会依托条件 (14) 6、环境保护条件 (15) 7、法律支持条件 (15) 8、征地、拆迁、移民安置条件 (15) 9、施工条件 (15) 五、技术方案、设备方案和工程方案 (16) (一)技术方案 (16) 1、生产方法 (16) 2、工艺流程 (17) (二)主要设备方案 (18) 1、设备选配原则 (18) 2、设备选型表 (19) (三)工程方案 (20) 1、土建工程设计方案 (20)
甲醇制氢操作规程
400Nm3/h甲醇制氢 操作规程
目录 目录 .................................................................................................................................................. I 操作规程. (1) 一岗位管辖及任务 (1) 1.1岗位管辖范围 (1) 1.2岗位任务: (1) 二、工艺说明及流程示意图: (1) 2.1工艺说明 (1) 2.2流程示意图 (4) 三岗位工艺指标: (5) 3.1温度指标: (5) 3.2流量指标: (5) 3.3压力指标:MPa (5) 3.4液位: (6) 3.5分析指标 (6) 四:装置启动初次开车及停车后的再启动 (6) 4.1管道的试漏、保压 (6) 4.2催化剂的装填 (6) 4.3设备、仪表的调校 (9) 4.6投料启动 (10) 4.7停车后再启动 (10) 4.8催化剂的卸出 (12) 五正常停车步骤和紧急停车: (12) 5.1正常停车 (12) 5.2紧急停车 (13) 5.3临时停车 (14)
六常见故障及处理方法: (14) 6.1外界供给条件失常 (14) 6.2操作失调 (15) 6.3 PLC故障 (16) 5.4操作注意事项 (16) 七巡回检查制度: (17) 八岗位责任制: (17) 九设备维护保养制度: (18) 十设备润滑管理制度: (18) 十一安全注意事项: (19)
操作规程 一岗位管辖及任务 1.1岗位管辖范围 界区内所有管道、设备、阀门、电气及仪表等均属于岗位管辖范围。 1.2岗位任务: 利用甲醇和水的重整反应制氢,重整气组成为氢气约75%,二氧化碳约25%,还有微量的甲烷,二乙醚的等杂质,之后在通过变压吸附分离提氢,改变变压吸附(PSA)操作条件可生产不同纯度的氢气,氢气纯度最好可达99.999%以上。 二、工艺说明及流程示意图: 2.1工艺说明 2.1.1重整工段 甲醇进入界区后直接进入混配罐中,通过液位控制甲醇进料量,无离子水进入界区后直接进入混配罐中,通过控制液位控制无离子水进料量,两台混配罐一台陪料,一台使用。混配罐内甲醇、水混合液体能维持一个班八小时的工作用量。混配罐中的混合液经计量泵输送到换热器中。本工艺现场配备三台计量泵,其中一台输送混合液体,一台给水洗塔输送无离子水,另一台备用,三台泵型号、结构完全相同,开二备一。甲醇、水混合液体进入换热器与由反应器出来的重整气进行换热,换热后混合液温度由室温升至140℃,并呈现部分气化的气液胶着状态,然后接着进入气化过热器,被过热器下部管壳内高温导热油加热气化,气化后的甲醇、水混合蒸气通过气化过热器上部列管被管壳中的高温导热油进一步加热到240~300℃范围内,然后进入反应器中。进入反应器的甲醇、水混合蒸气由上而下通过催化剂床层,在催化剂的作用下发生甲醇、水蒸气重整反应,生成产物为二氧化碳和氢气—重整气。由反应器出来的重整气进入换热器中与原料甲醇、水液体进行换热,完成热量交换后,重整气的温度由240~300℃降为160℃左右,然后进入水冷却器进一步冷却至室温,经冷却
甲醇催化制氢技术
甲醇催化制氢技术 一、氢气的主要用途 能源与环境是未来人类社会可持续发展涉及的最主要问题。目前, 全球绝大多数能量需求来源于化石燃料, 这最终必将导致化石燃料的枯竭, 而其使用也导致严重的环境污染,因此,可持续发展、无污染的非化石能源的开发利用是未来能源发展的必然趋势。 氢气的应用领域很广,其中用量最大的是作为一种重要的石油化工原料,用于生产合成氨、甲醇以及石油炼制过程的加氢反应。此外,在电子工业、冶金工业、食品加工、浮法玻璃、精细化工合成、航空航天工业等领域也有应用。 在石油炼制过程中,石油产品的加氢裂化和加氢精制过程需要应用大量的氢气作为一种反应原料;另外,氢气在电子工业、冶金工业、浮法玻璃等行业中主要作为还原气体;在电子工业中用作燃料;在航天领域主要应用的是液氢,作为火箭推进的主要燃料。 除以上常规用途之外,目前越来越多的科研机构在着力于研究氢能的开发和利用。以氢为能源的燃料电池已成为世界范围内的重点攻关课题。从20世纪80年代后期开始,由于汽车尾气污染日益加剧,世界各国争相研究开发“零排放”的燃料电池电动车(FCEV),其中洁静、对环境友好的质子膜燃料电池(PEMFC)汽车被公认为是取代传统内燃机汽车的最佳选择。目前商业可行的PEMFC汽车一般使用随车携带的甲醇重整器供应燃料氢气。由于燃料电池技术新的发展,氢气作为燃料电池的燃料,展现了极其广泛的潜在市场。 工业上大量生产氢气的方法主要包括: 1)用水蒸汽通过灼热的焦炭, 生成的水煤气经过分离得到氢气, 以及煤直接汽化生成煤气经过分离得到氢气; 2)天然气催化分解以及天然气与水蒸汽重整后生成的物质经分离也可以得到氢, 3)甲醇催化重整制氢, 4)电解水制氢, 5)重油的部分氧化制氢,其他还有氨分解制氢等途径。 目前,国内外甲醇催化制氢的技术方法主要包括甲醇水蒸汽重整、甲醇部分氧化,以及甲醇分解三种制氢技术。工业化生产过程中主要使用甲醇水蒸汽重整制氢技术。甲醇水蒸汽重整制氢工艺以其投资小、生产成本较低、技术先进、产品氢气易分离、原料甲醇便于运输等优点得到较多生产型企业的青睐,已经在全国各行各业得到广泛应用。 二、甲醇催化制氢工艺介绍 在甲醇催化制氢工艺中,具有应用前景的技术主要是甲醇水蒸汽重整制氢、甲醇部分氧化制氢,以及甲醇分解制氢。以下简单介绍一下三种甲醇催化制氢工艺过程。 1)甲醇水蒸汽重整制氢(methanol steam reforming)
甲醇裂解制氢技术
2014-10-29IG IG IG_CHINA全球最大气体交流平台,提供最新最综合的新闻和商务资讯,欢迎大家进来交流! 新朋友:点击上方蓝字:[中国气体] +关注 老朋友:点击右上角“…”按钮将本文分享到朋友圈 8<---------------------------------------- 为减少化工生产中的能耗和降低成本,以替代被称为“电老虎”的“电解水制氢”的工艺,利用先进的甲醇蒸气重整──变压吸附技术制取纯氢和富含CO2的混合气体, 经过进一步的后处理, 可同时得到氢气和二氧化碳气。 甲醇与水蒸气在一定的温度、压力条件下通过催化剂, 在催化剂的作用下, 发生甲醇裂解反应和一氧化碳的变换反应,生成氢和二氧化碳, 这是一个多组份、多反应的气固催化反应系统。反应方程如下: CH3OH→CO+2H2 (1) H2O+CO→CO2+H2 (2) CH3OH+H2O→CO2+3H2 (3) 重整反应生成的H2和CO2, 再经过变压吸附法(PSA)将H2和CO2分离,得到高纯氢气。 2 制取途径 工业上利用甲醇制氢有二种途径:甲醇分解、甲醇部分氧化和甲醇蒸汽重整。 甲醇蒸汽重整制氢由于氢收率高(由反应式可以看出其产物的氢气组成可接近75%),能量利用合理,过程控制简单,便于工业操作而更多地被采用。 3 工艺流程 甲醇蒸汽重整是吸热反应,可以认为是甲醇分解和一氧化碳变换反应的综合结果。我公司蓝博净化科技的甲醇蒸汽重整制氢工艺,经历了多次技术改进,已相当成熟。该过程的典型工艺流程见图1。 甲醇蒸汽重整反应通常在250-300℃,1-5MPa,H20与CH30H摩尔比为1.0-5.0的条件下进行,重整产物气经过变压吸附等净化过程,可得不同规格的氢气产品。 甲醇蒸汽重整过程既可以使用等温反应系统,也可以使用绝热反应系统。等温反应系统采用管式反应器,管壳中充满热载体进行换热,保持恒温反应。在绝热反应系统中,蒸汽与甲醇混合物经过一系列绝热催化剂床层,床层之间配备换热器1。 反应产物净化系统可根据产品质量等级要求选择,变压吸附及膜分离技术是非常实用的气体净化技术。变压吸附净化可获得纯度高于99.99%的氢气产品,依据所使用的不同吸附剂及工艺条件,氢回收率在70%-87%之间变化。溶剂洗涤、CO催化转化、甲烷化等过程均可用于净化氢气。
