溶质分配与成分过冷
合金凝固界面前沿的成分过冷

距离x’逐渐降低。 液相线温度TL(x’)逐渐 上升(图c)
当界面前沿液相的实际
温度梯度G1实际等于或大于 界面处液相线的斜率时,
界面前沿不 出现过冷;
当温度梯度G2实际小于 液相线斜率时,即满足条件
实际温度在前沿某处与 TL(x’)相交,并在液相 前沿某一区域温度低于液相 线温度,则出现过冷。 这种由于溶质成分富集 引起的过冷称为“成分过冷”
对ΔT(x‘)求导,求最大过冷度
求导
最大过冷度对应的x’为
代入式ΔT,得
上式是只有扩散 情况下的成分过冷的最大过 冷度,出现过冷的区域宽度ΔX
成分过冷的最大过冷度ΔTmax及成分过冷的区 域宽度ΔX,是成分过冷程度的两个重要指标, 它们对凝固方式有影响
单相固溶体的凝固情况: 完全互溶的单相固溶体; 部分互溶的端际固溶体; 具有共晶及包晶反应合金的先期固溶体。
时,出现成分过冷
于是有 上式为出现成分过冷判据
两边除以dx’,得 满足上式时,出现成分过冷
由液相中部分混合(有对流作用)的溶质再 分配表达式
整理后可得
上式为液相部分混合情况下出现成分过冷的 判别式,是成分过冷通式。 如,液相只有有限扩散时,
代入上式,得
是上式的一个特解
1)液相中温度梯度GL小,有助于成分过冷; 2)晶体生长速度快(R大),易形成成分过冷
合金结晶长大的形态主要与传热及传质有关
先讨论“热过冷”及其对纯金属凝固的影响
纯金属的液相在正温度 梯度的区域内
晶体生长的固液界面通常 为平直形态,而且是等温面。 其温度低于平衡熔点温度Tm。 这种过冷正好提供凝固所需要的动力学驱动 力,称为动力学过冷ΔTk
材料成形技术基础 知识点总结

材料成形技术基础知识点总结滑移系:晶体中一个滑移面及该面上的一个华滑移方向的组合。
纤维组织:金属经冷加工变形后,晶粒形状发生改变,其变化趋势大致与金属的宏观变形一致,若变形程度很大,则晶粒呈现一片纤维状的条纹。
拉深:当凸模下降与坯料接触,坯料首先弯曲,于凸模圆角接触的材料发生胀形形变,凸模继续下降,法兰部分坯料在切向压应力,径向拉应力的作用下沿凹模圆角向直壁流动,形成筒部,进行拉深变形。
自发形核:在单一的液相中,通过自身的结构起伏形成新相核心的过程。
非自发形核:在不均匀的液体中,依靠外来杂质和容器壁面提供衬底而进行形核的过程。
焊接热循环:在焊接热源的作用下,焊件上的某一点温度随时间变化的过程。
焊接残余应力:由于焊接过程中的不均匀加热等因素而导致的焊接结构中存在残余应力。
温度场:加热和冷却过程中某一瞬间温度分布。
材料成型过程中的三种流:材料流,能量流,信息流。
液态金属在凝固和冷却到室温时发生:液态,凝固,固态三种收缩。
减小及消除焊接残余应力的措施有:热处理,温差拉伸,拉力载荷,爆炸冲击,振动法等。
液态金属结构:液态金属有许多近程有序的原子集团组成,原子集团内部原子规则排列,其结构与原固体相似;有大的能量起伏,激烈的热运动和大量的空穴;所有原子集团和空穴时聚时散,时小时大,始终处于瞬息万变的状态。
形核剂应具备哪些条件:失配度小,粗糙度大,分散性好,高温稳定性好。
加工硬化:金属经冷塑性变形后,随着变形程度的增加,金属的强度硬度增加,而塑性韧性降低,这种现象叫。
其成因与位错的交互作用有关,随着塑性变形的进行,位错密度不断增加,位错反应和相互交割加剧,结果产生固定割阶,位错缠结等障碍,以致形成胞装亚结构,使位错难以越过这些障碍而被限制在一定范围内运动,这样,要使金属继续变形就需要不断增加外力才能克服位错间强大的交互作用力。
滑移变形时通常把滑移因子u为0.5或接近0.5的取向称为软取向,把u为0或接近0 的取向称为硬取向。
过冷温度对金属凝固的影响
过冷度对金属凝固的影响金属材料作为支撑国民生活富裕及安全的基础结构材料而大量使用。
随着材料使用方法的多样化,对材料特性的要求也日益严格。
因此,利用现代科学技术开发出高质量和高性能的钢铁材料将具有重大的现实意义。
金属的凝固过程对金属的机械性能特点有重大影响,它决定着该零件组织,包括各种相的形态,大小和分布,直接影响到该零件后面的加工处理工艺,间接地影响了工件的加工性能和使用性能。
而对于铸件和焊接件来说,结晶过程基本上就决定了它的使用性能和使用寿命,而对尚需进一步加工的铸锭来说,结晶过程既直接影响了它的轧制和锻压工艺性能,又不同程度地影响着其制品的使用性能。
因此,研究和控制金属的结晶过程,已成为了提高金属力学性能和工艺性能的重要手段。
而金属的结晶过程总是伴随着过冷,可以说研究金属的结晶过程就是相当于研究结晶过程对过冷的控制。
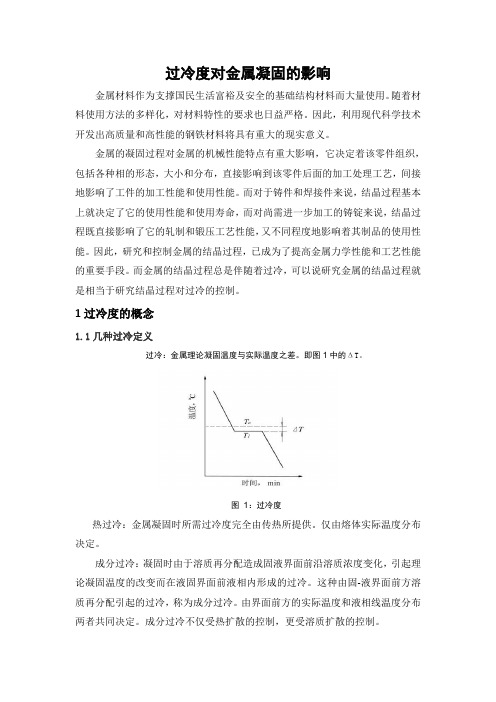
1过冷度的概念1.1几种过冷定义过冷:金属理论凝固温度与实际温度之差。
即图1中的ΔT。
图1:过冷度热过冷:金属凝固时所需过冷度完全由传热所提供。
仅由熔体实际温度分布决定。
成分过冷:凝固时由于溶质再分配造成固液界面前沿溶质浓度变化,引起理论凝固温度的改变而在液固界面前液相内形成的过冷。
这种由固-液界面前方溶质再分配引起的过冷,称为成分过冷。
由界面前方的实际温度和液相线温度分布两者共同决定。
成分过冷不仅受热扩散的控制,更受溶质扩散的控制。
1.2过冷现象实验表明纯金属的实际凝固温度Tn总比其熔点Tm低,这种现象叫做过冷。
金属实际结晶温度Tn与理论结晶温度Tm之差,称为过冷度,用△T表示。
其大小取决于:1)液态金属的本性,金属不同,△T也不同;2)纯度越高,△T越大;3)冷却速度越快,△T越大。
但无论多慢也不能在Tm结晶。
2金属结晶的必要条件2.1过冷是结晶的必要条件由热力学规律可知,在等温等压条件下,物质系统总是自发地从自由能较高的状态向自由能较低的状态转变。
如果液相的自由能比固相的自由能低,那么金属将自发地从固相转变为液相,即金属发生熔化。
成分过冷(end)

任何凸起必将伸入过热熔体中而被熔化,凸起消失,界面 以平界面生长。
23
(a) 无成分过泠的平界面生长 (a)粗糙界面)(b)光滑界面
(b)
24
界面前方成分过冷很小
当
mC0 (1 k0 ) GL R DL k0
33
典型的非小面-非小面共晶组织(纵截面)
34
当
时,
a相成杆状,否则是片状。
非小面-非小面片状共晶组织(横截面) 非小面-非小面杆状共晶组织(横截面)
35
非小面-小面柱状共晶组织
36
非小面-小面等轴共晶组织——共晶团
37
共晶组织的生长机理
• 领先相析出后,后析出相依附于其上析出,形成具有两相 共同生长界面的双相核心,然后以相互“搭桥”的方式进 行生长; • 溶质元素在界面前沿两相间横向扩散,互相不断为相邻相 提供生长所需组元而使两相彼此共生生长。
与此同时,在固/液界面前沿,真实的温度分布 可能是这样两种情况,即: • 温度分布相对比较平坦(温度梯度GL小),与液 相线的温度分布曲线有交点; • 另外一种情况,温度分布相对比较陡峭(温度梯 度GL大),与液相线的温度分布曲线没有交点。
15
第一种情况下在固液界面前沿存在一个区域, 该区域内真实温度低于液相线温度,即发生了过 冷,这种在温度更高的熔体中,由于成分分布的 变化造成的过冷叫“成分过冷”
该公式就是Scheil公式
6
(2)固相无扩散,液相只有扩散而无对流时的溶质再分配
7
(2)固相无扩散,液相只有扩散而无对流时的溶质再分配
当液相中溶质边界层达到稳定后,其浓度从固液界面 (x=0)开始的分布为:
6.3凝固过程溶质再分配全解

第三节 “成分过冷”对合金单相固溶体
结晶形态的影响
第四节 共晶合金的凝固
1
第一节 单相合金的凝固 ----溶质再分配
教学内容:
平衡凝固时的溶质再分配;近平衡凝固时的溶质再 分配;非平衡凝固时的溶质再分配
教学要求 : 1. 了解平衡凝固时的溶质再分配规律 2. 理解近平衡凝固时的溶质再分配规律
8
• 随着固相分数(fS)增加,凝固界 面上固、液相中的溶质含量均增 加,因此已经凝固固相的平均成 分比平衡的要低。 • 当温度达到平衡的固相线时,势
必仍保留一定的液相(杠杆原
理),甚至达到共晶温度TE时仍有 液相存在。这些保留下来的液相 在共晶温度下将在凝固末端形成 部分共晶组织。
9
三、液相只有有限扩散时的溶质再分配
四、液相中部分混合(有对流作用)
6
一、平衡凝固条件下的溶质再分配
开始( T=T )时: CS = K C = C 0 0 L L 0 0C0 : C 的平衡成分,即固、液相中成分均能及时充分 扩散均匀 。 凝固终了时,固相成分均匀地为 C = C S C S fS C f LC S 1 (1 0 K 0 ) f S C sC0 ( f S f L ) C1 SL L CL
K C
平衡凝固是指液、固相溶质成分完全达到平衡状态图对应温度 凝固过程 固、液相质量分数 ( T = T* )中,固 fs 、fL -与固液相成分匀时的溶质再分配
该情况下溶质在固相中没有扩散,而在液相中充分混合均匀。 起始凝固时与平衡凝固时相同: 接着凝固时由于固相中无扩散,
60% 30% 20%
56%
21
溶质再分配与成分过冷

8.5 单相合金的结晶—溶质再分配与成分过冷Crystallization of single phase alloy--Solute redistribution and constitutional undercooling溶质再分配固液两相成分不同除纯金属外,单相合金的结晶是在固液两相区间内完成溶质再分配类似于凝固潜热的释放随着凝固过程的进行,由于固液两相成分差,越来越多的溶质原子被排出,释放到前方液相中与凝固潜热释放不同,液相中溶质扩散不可能很快均匀除间隙固溶体外,溶质原子在固相中扩散系数比液相低4个数量级液相中溶质扩散系数比热扩散系数也要低4个数量级溶质再分配具体分配形式与决定传质过程的动力学因素密切相关,决定着界面处,乃至固液两相内部成分变化溶质再分配影响到宏观及微观成分及偏析现象、晶体的生长形态、组织分布,一定程度上决定了材料各种性能同温度分布一样,溶质再分配也是合金结晶一大特点,二者共同控制晶体生长行为相图基本知识对于单相合金,将液相线和固相线近似看成直线当合金成分为C 0时液相线及液相线斜率m l 固相线及固相线斜率m s00*C m T T l l +=液相线温度00*C m T T s s +=固相线温度当合金成分为T 时()l l m T T C /0−=液相成分()ss m T T C /0−=固相成分平衡溶质分配系数平衡溶质分配系数s l ls m m c c k ==**0液固相直线:k 0为常数固相和液相内部的成分始终相等结晶初期,T = T L 时:C S *=C 0k 0,C L *=C 0结晶末期,T = T S 时:C S *=C 0,C L *=C 0/k 0平衡条件下溶质再分配-杠杆定律合金原始成分为C 0,固液两相在某一瞬间平衡成分为C S *与C l *,相应质量分数为f S *和f l *,则有:****c f c f c l l s s =+平衡结晶中溶质再分配;)1(10*00*k f k c c s s −−=)1(0*00*k f k c c l l−+=平衡条件下溶质再分配-杠杆定律A-B相图一部分液相线温度附近(凝固初期)固相线温度附近(凝固末期)液固相线区间内(中间阶段)近平衡/非平衡条件下溶质再分配一般条件下:溶质原子在液态金属中扩散系数为5×10-9m 2/s数量级溶质原子在固相中的扩散系数为5×10-12m 2/s数量级平衡凝固是指液、固相溶质成分完全达到平衡相图对应的平衡成分,即固、液相中成分均能及时充分扩散均匀平衡结晶极难实现,实际结晶过程都是近/非平衡结晶几种情况下溶质分配系数平衡凝固:平衡分配系数(界面与固液相内部均平衡)近平衡凝固:有效分配系数(仅界面处相平衡)非平衡凝固:非平衡分配系数(均不满足相平衡)近平衡凝固条件下溶质再分配-Scheil 公式凝固时,固相原子来不及扩散,液相中如存在足够对流和搅拌,任一温度下都能保证液相溶质原子的均匀分布,其成分沿着液相线变化除间隙固溶体外,溶质原子在固相中扩散系数比液相低四个数量级近平衡凝固条件下溶质再分配-Scheil 公式以水平圆棒自左向右单向结晶为例。
成份过冷的名词解释

成份过冷的名词解释在科学领域中,有一种现象被称为成份过冷。
成份过冷是指当物质的成分超过其平衡浓度,而仍然保持在液体状态下的现象。
这种现象通常在溶液、合金或玻璃中发生,虽然其具体机理还存在争议,但成份过冷已成为许多领域的研究热点。
1. 成份过冷的现象成份过冷是指当溶液中溶质的浓度超过其平衡浓度时,溶质仍然保持在溶液中的液体状态。
这种现象的发生可能是由于溶质分子之间的相互作用力的影响,以及溶剂分子结构的变化而导致。
例如,当饮用水中溶解的盐超过饱和度时,即超过了水能够容纳的最大盐量,溶解过程会变得不稳定。
在这种情况下,溶质颗粒会发生不规则的聚集,形成云雾状的物质。
这种云雾状的物质具有液体的性质,但其成分又超过了平衡浓度,因此被称为成份过冷。
2. 成份过冷的机制成份过冷的具体机制还存在许多争议。
一种观点认为,成份过冷发生时,溶质分子之间的相互作用力会增强,使得分子更难逸出溶液而形成固体。
这种观点解释了为什么成份过冷的物质具有液体的性质,而非固体。
另一种观点则认为,成份过冷是由于溶剂分子结构的变化导致的。
溶剂分子在过冷的状态下,其结构可能发生改变,导致成分超过平衡浓度的物质仍能保持液体状态。
这种观点强调了溶剂分子的动力学行为对成份过冷的影响。
无论是哪种观点,成份过冷的机制都需要进一步的研究和实验证实。
目前,科学家们正在利用先进的实验和计算方法,以及对成份过冷物质的结构和性质的深入了解,来揭示这个现象的奥秘。
3. 成份过冷的应用成份过冷现象在实际应用中具有一定的价值。
例如,在材料科学中,研究成份过冷现象可以帮助人们设计新型合金材料,以改善其力学性能和稳定性。
利用成份过冷的特性,可以制备出具有良好性能的金属玻璃材料,这在传统金属材料中是很难实现的。
在药物制剂领域,成份过冷现象也有着重要的应用。
药物的溶解度常常与其生物利用度相关,过冷状态下的药物溶液可以提高溶解度,从而增加其吸收速率和生物利用度。
这为药物的研究和开发提供了新的思路和方法。
成分过冷

一、名词解释1、成分过冷:凝固时由于溶质再分配造成固液界面前沿溶质浓度变化,引起理论凝固温度的改变而在液固界面前液相内形成的过冷。
这种由固-液界面前方溶质再分配引起的过冷;2、粗糙界面:原子散乱随机分布在界面上,形成一个坑坑洼洼、凹凸不平的界面层,其微观上是粗糙的;3、均质形核:形核前液相金属或合金中无外来固相质点而从液相自身发生形核的过程;4、能量起伏:有一些原子的能量大于或大大超过原子的平均能量,而有的原子的能量则小于平均能量,这种能量的不均匀性称为能量起伏;5、加热斑点:热源把热能传给工件是通过一定的作用面积进行的,对于焊接圆弧来说,这个面积称为加热斑点;6、流动应力:对应于变形过程某一瞬时进行塑性流动所需的真实应力叫做该瞬时的屈服应力,也叫做流动应力;7、边界摩擦:在被压平的峰顶与工、模具表面之间,或者保留了很薄的一层润滑膜,或者这层膜被挤掉出现了黏膜,这种摩擦状态;8、应变增量:变形过程中某一微小阶段的应变;9、加工硬化:由于塑性变形使金属内部组织发生变化,金属的强度,硬度增加,塑性韧性降低的现象;二、填空1、世界液态金属内部存在能量起伏、浓度起伏和相起伏;2、焊接过程有以下一些特点:热源的局部集中性和焊接热过程的瞬时性和热源的运动性;3、衡量界面张力大小的标志是润湿角的大小,润湿角越小,说明界面能越小;4、影响滞粘性的因素有:温度、化学成分和非金属夹杂物;5、当液态金属中出现晶核时,体系自由能的变化由两部分组成:一部分是液态和固态体积,它是相变的驱动力,另一方面是由于出现了固-液界面,使体系增加了界面自由能差Gv能,它是相变的阻力;6、成形件中的裂纹按材料中裂纹的形成机理分为热裂纹、冷裂纹和应力腐蚀裂纹;三、简答题1、变形温度、变形速度对塑性有何影响?塑性来讲,变形温度越高,加工硬化的同时材料的回复机制(动态回复或动态再结晶)启动,材料的塑性越好;与此相反,变形速度越高,加工硬化的越厉害,材料表现出较差的塑性;2、减小或消除残余应力的措施:减小:(1)设计措施:减少焊缝数量;避免焊缝过于集中,采用拘束度小的结构形式(2)工艺措施:采用合理的装配焊接顺序和方向,缩小焊接区域结构整体之间的温差,降低焊缝拘束度,加热其他部位,使焊缝膨胀自由度加大,减小压缩塑性变形;消除:自然时效:将存在残余应力的铸件放在露天环境中数月至半年以上,让应力自然消失的过程为自然时效人工时效:将铸件缓慢加热到塑性转变温度Tk以上,相变温度Tcr以下(对于铸铁,加热温度为650~700℃),较长时间保温,然后缓慢冷却以消除残余应力的热处理方法为人工时效共振时效:利用激振器的激振作用使铸件发生共振,从而消除铸件残余应力的方法为共振法3、简述晶体宏观长大方式和微观长大方式:宏观:(1)表面细晶粒区的形成:当金属浇入温度较低的铸型时,与铸型接触的一层金属液受到强烈激冷,产生很大的过冷而大量生核,这些晶核迅速长大并互相连接在一起,形成无方向性的表面细晶粒区。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
单相合金的凝固特点
• 除纯金属外,单相合金的凝固过程一般是 在一个固、液两相共存的温度区间内完成 的。
• 在平衡凝固过程中,这一温度区间是从平 衡相图中液相线温度开始,至固相线温度 结束。随温度的下降,固相成分沿固相线 变化,液相成分沿液相线变化。可见,凝 固过程中必有传质过程发生,固-液界面两 侧都将不断地发生溶质再分配的现象,其 原因在于各组元在不同相中化学势不同。
(3)最终瞬态
当液/固相界面离凝固器终端的距离小于DL/R 时,界面处及其前沿液相溶质浓度要比C0/k0高得 多,终端的固相浓度也不再是C0,而是大大高于 C0,这时上式也就不再适用。这个最后的阶段称 最终瞬态。
如界面的浓度达到共 晶成分,在共晶温度下 就会结晶出共晶体。
液相中只有有限扩散时的溶质再分配
T2处:固相无扩散,成分不均匀。 凝固过程中固-液界面上的成分为(Scheil
公式):
CS* k0C0 (1 fS )k0 1
CL*
C0
f k0 1 L
实际合金近平衡凝固的例子:Al-2%Cu及Al-5%Cu合金。
这两个合金在近平衡凝固后都应是单相α,但
在非平衡凝固后除了出现偏析外,还出现共晶组 织。很明显,5%Cu合金比2%Cu合金含有较多的共 晶。
的容器中,从左端开始冷却凝固,界面始终以宏 观的平面形态向右推进。
凝固方向
固
液
C
CL C0
k0C0
k0 CS* / CL* 1
平衡凝固条件下的溶质再分配
固、液两相在温度T*时的平衡成分为 CS*与CL* ,
相应的体积分数为
f
S*和f
* L
,则由平衡条件下的杠
杆定律,得
C
* S
f
* S
C
7.1.4 近平衡凝固时溶质再分配
假设: ①界面始终处于局部平衡状态,即界面 两侧的浓度符合相应界面温度下相图所给出的平 衡浓度。 ②没有过冷,也不考虑长大时的动力学过冷。 ③界面的推移由其前沿的溶质输运所控制。 ④由于溶质在液体内的扩散系数(约为10-5cm2/s)
比固体内的(约为10-8cm2/s)大几个数量级,故 忽略固相内扩散。 ⑤相图中的液、固相线均近似为直线。即平衡分配 系数不随温度变化。
有色金属及合金的 熔炼与铸锭
• 第七讲 铸锭凝固过程的质量传输
大纲
➢凝固过程的溶质平衡 ➢传质过程的控制方程 ➢凝固过程中的溶质再分配 ➢固-液界面前沿熔体过冷
7.1 凝固过程的溶质平衡
• 保守体系凝固过程的溶质守恒方程
ws sdVs wLLdVL wc0LV0
•总的质量守恒方程
DL
d 2CL (x) dx2
R
dCL (x) dx
0
此方程的通解为:
C
L ( x)
A
R
Be DL
x
根据边界条件:CL(x=0)=C0/k0;CL(x=∞)=C0
得: , A C0
B
C0 k0
C0
凝固稳定态阶段富集
层溶质分布规律(指数
衰减曲线):
CL (x)
C0 (1
1 k0 k0
近平衡凝固为接近实际生产条件下的凝固, 也称正常凝固。
三种近平衡凝固
1.固相无扩散、液相均匀混合
2.固相无扩散、液相只有有限扩散 3.液相中部分混合
非平衡凝固:是指绝对的非平衡凝固,如快速 凝固、激光重熔及合金雾化冷却等近代先进的材 料成形技术中液态合金的凝固。此时已不遵循热 力学规律,即使在固-液界面紧邻处也达不到平 衡凝固条件。
如图(b)所示。
不同类型的平衡相图 (a)mL 0, k0 1 (b) mL 0, k0 1
假定相图中的液相线和固相线均为直线(其斜
率分别为mL、mS),则
k0
C
* S
C
* L
(T0 T * ) / mS (T0 T * ) / mL
mL mS
(4-2)
即k0值为与温度及浓度无关的常数。
三种凝固条件下固—液界面附近的溶质分配情况
a)平衡凝固 b)近平衡凝固 c)非平衡凝固
7.1.2 基本知识——溶质平衡分配系数
平衡溶质分配系数k0的定义:当凝固进行到某
一温度T *时,平衡固相溶质成分CS*与液相溶质
成分CL*之比,即
k0
C
* S
C
* L
(4-1)
对于不同的相图(或相图的不同部分),k0值 可以小于1,如图(a)所示; k0也可以大于1,
* L
f
L*
C0
因为 ,故得 f
* S
f
* L
1
CS*
1
C0k0
f
* S
(1
k0 )
CL*
1
C0
f
* S
(1
k0
)
此即平衡凝固中的溶质再分配规律。
T1处(开始凝固时): 固相成分k0C0 液相成分接近C0
T2处(凝固终了时): 固相成分C0 液相成分接近C0/k0
平衡条件下溶质再分配-杠杆定律
Al-2%Cu合金
Al-5%Cu合金
应用:区域熔炼 区域熔炼法,又称区域提纯。是一种提纯金属、 半导体、有机化合物的方法。
区域熔炼技术 K0<1时,左端纯化,右端富集溶质组元 K0>1时,右端纯化,溶质富集于左端
区域熔炼已广泛用于提纯许多半导体材料、 金属、有机及无机化合物等。
区域熔炼技术的原理
DL
d
2CL (x) dx2
R
dCL (x) dx
dCL (x) dt
(2)稳定态
界面的不断推进,堆积的溶质越多,浓度梯 度越大,扩散越快。当界面温度达到T2时,界 面推进所排出的溶质量等于液相中溶质扩散走 的量,此时,固相成分保持C0,在界面一侧的 液相浓度为C0/k0,前沿的浓度场不再随时间改 变,即dCL(x)/dt=0,凝固便进入稳定态:
初始条件:fS
0
时,C
* s
k0C0
,得积分常数
C
k0C0
,
因此
CS* k0C0 (1 fS )k0 1
CL*
C0
f k0 1 L
上式被称为Scheil公式,或非平衡杠杆定律。 此公式描述了固相无扩散、液相均匀混合下的溶 质再分配规律,有着广泛的用途。
T1处:固相成分k0C0,液相成分大于C0,成分均 匀。(k0<1)
区域熔炼技术的原理
• 此法可生产纯度达99.999%的材料,且一次达 不到要求,可以重复操作。此法设备与操作 简单,且可自动化。
2、固相无扩散、液相只有有限扩散时的溶质再分配
如果没有搅拌和对流,液相内只能靠扩散进行 成分均匀化。
以一个二元系讨论:合金 成分为C0。设R为固-液界面的 生长速度;x是以界面为原点 沿界面法线方向伸向熔体的动 坐标;CL(x)为液相中沿x方向 的浓度分布; dCL(x) 为界面处液相中浓度梯度。
dx x0
起始瞬态
稳定态
最终瞬态
固相无扩散,液相有限扩散下的溶质再分配
(1)起始瞬态
液态金属温度到达T1时,结晶出成分为k0C0的 固相,多余溶质排向液相,由于扩散(无对流) 不足以使溶质完全排向远方,界面前沿出现溶质 富集。
界面前沿的浓度场变化包括两项:扩散引起的:
DLd2CL(x)/dx2;界面推进所排出的溶质量:溶质随 距离的变化为dC/dx,由于界面推进造成单位时 间沿溶 的质 浓的 度变 场化 的量微为分R方(程dC为L(x:)/dx),这时,界面前
当温度达到平衡的固相线时, 势必仍保留一定的液相(杠杆原
理),甚至达到共晶温度TE时仍
有液相存在。这些保留下来的液 相在共晶温度下将在凝固末端形 成部分共晶组织。
Scheil公式推导 在任一温度为T*时,因溶质量 守恒,形成微量固相所排出的溶质原子量应等于
液相内溶质原子量的变化:
(C
* L
CS* )dfSRLeabharlann e DLx)
此即Tiller公式。
从界面到成分为C0处是溶质原子富集层。 当 x DL 时,
R
[CL(x)-C0]降到:
C0
(
1 k0
1) 1 e
特征距离
DL / R 称为溶质富
x DL R
集层的“特征距离”。
在稳定生长阶段,界面两侧以不变的成分CS*=C0 与CL*=C0/k0向前推进,一直到最终瞬态为止。稳 定生长的结果,可以获得成分为C0的单相均匀固 溶体。
0
R
此方程的通解为:
C L(x)
A
Be DL
x
边界条件是:CL(x=0)=C*L;CL(x=δ)=C0
得:
Rx
CL (x) C0 CL* C0
1
1
e
DL R
1 e DL
上式中CL(x)为边界层内任意一点x的液相成分。
如果液相容量不是很大,则在扩散层外的液体
成分逐渐提高,以平均值 C表示。则上式写成:
平衡溶质分配系数k0的物理意义: • 对于 k0 1,k0越小,固相线、液相线张开程度 越大,开始凝固时与凝固终了时的固相成分差别 越大,最终凝固组织的成分偏析越严重。 • 对于 k0>1 的情况, k0越大,则偏析越严重。
7.1.3平衡凝固时的溶质再分配
K0<1合金 条件:初始成分为C0的合金,将其置于长度为 L
