无机化学课件16-d区元素(一)
无机分析12第十六章d区元素

Fe2+
浅绿色
Co2+
酒红色
Ni2+
绿色
Cu2+
蓝色
Zn2+
无色
上页 下页 目录 返回
许多二价过渡元素金属离子 M 2+ (aq)的 颜色与d-d 跃迁或 f-f 跃迁有关。这种 跃迁发生在金属离子本身,通常强度都 很弱,不能解释无机颜料的颜色。副篇 介绍了荷移跃迁和价层间跃迁。
第一过渡系金属水合离子的颜色
●熔点、沸点高
同周期元素单质的熔 点,从左到右一般是先逐渐
升高,然后又缓慢下降。在
同一族中,第二过渡系元素 的单质的熔点、沸点大多高 于第一过渡系,而第三过渡 系的熔点、沸点又高于第二 过渡系(第 3 族除外),熔点 最高的单质是钨。 熔点最高的单质: 钨(W) 3683±20℃
上页 下页 目录 返回
(4)
金属元素的电极电势
φθ的单位为V
元素
Ca -2.87 Sc Ti V Cr Mn Fe Co Ni Cu 0.34 Zn -0.76
φθ(M2+/M)
Φθ (M3+/M2+)
- -1.63 -1.18
-0.91 -1.18 -0.44 -0.28 -0.23
-
-
-0.37 -0.256 -0.41 +1.51
d 电子组态 M2+(aq)
d1 d2 Sc2+ Ti2+
d3 d4 V2+ Cr2+
d5 d6 d7 Mn2+ Fe2+ Co2+
d8 d9 d10 Ni2+ Cu2+ Zn2+
稳 定 性 增 大
原子结构和元素周期律—元素周期表(无机化学课件)

课程小结
本节重点
一、周期表的结构 周期(横行)结构: 三长、三短、一不全。 族(纵行)结构: 七主、七副、零和Ⅷ族。
二、原子结构与元素在周期表中位置的关系 a.周期序数=电子层数 b.主族序数=最外层电子数
无机化学
˝
元素周期表
案例导入
插入二维动画(待制作)
元素周期表是怎么来的?
目录
CONTENTS
01 元素周期表
02 元素周期表的结构及特点
01
元素周期表
一、元素周期表
定义:把电子层数相同的各元素, 按原子序数递增的顺序从左到右排 成横行;把不同行中外层电子数相 同的元素,按电子层递增的顺序由 上而下排成纵列,就可以得到一张 表格,叫元素周期表。 元素周期表是元素周期律的具体表 现形式。
02
元素周期表的结构及特点
二、元素周期表的结构及特点
二、元素周期表的结构及特点
1 周期(横行)具有相同电子层数的元素按照原子序数递增的顺 序排列的一个横行。
短周期 长周期
不完全周期
1
1
2K 2
234
5
6
7
8
9
10
L K
8 2
3 11 12
M 18
13 14 15 16 17 18 L 8
k
2
4 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36
二、元素周期表的结构及特点
族的分类 包含元素
表示 个数
主族
副族
长、短周期元素 ⅠA,ⅡA等
长周期元素 ⅠB,ⅡB等
7
7
零族
Ⅷ族
稀有气体元素 8、9、10纵行
大学化学无机化学课件

大学化学无机化学课件一、无机化学简介无机化学是研究无机物质及其性质、结构和变化规律的科学。
它是化学的一个重要分支领域,对于理解和应用化学知识都具有重要意义。
本课程主要介绍无机化学的基本概念、化学键、离子化合物、配位化合物、无机酸碱等内容,并涉及到无机化学在实际应用中的一些案例。
二、无机化学基本概念1. 原子和元素在无机化学中,原子是构成化学物质的基本单位。
元素是指由具有相同原子序数的原子组成的物质,不同的元素具有不同的性质和特征。
2. 化学键化学键是原子之间通过共用电子或转移电子而形成的连接。
常见的化学键包括共价键、离子键和金属键。
三、无机化合物的分类1. 离子化合物离子化合物是由带正电荷的阳离子和带负电荷的阴离子通过离子键结合而成的化合物。
离子化合物具有良好的溶解性,在水中可以形成电解质溶液。
2. 配位化合物配位化合物是由一个或多个配位体与一个中心金属离子形成的化合物。
配位体通过与金属离子之间的配位作用形成配位键。
配位化合物具有丰富的颜色和独特的物理性质。
四、无机酸碱1. 酸碱理论酸碱理论主要有三种:奥斯特酸碱理论、布朗酸碱理论和劳里亚-布来斯酸碱理论。
其中,奥斯特酸碱理论认为酸是能够释放H+离子的物质,碱是能够释放OH-离子的物质。
2. 酸碱反应酸碱反应是指酸和碱在一定条件下发生反应生成盐和水的化学反应。
常见的酸碱反应包括中和反应、水解反应等。
五、无机化学在实际应用中的案例1. 无机化学在药物研发中的应用无机化合物在药物研发中起到了重要作用,如抗癌药物顺铂和含铁的血红素。
通过研究无机化合物的性质和结构,可以设计出更有效的药物。
2. 无机化学在环境保护中的应用无机化学在环境保护领域中也扮演着重要角色。
例如,利用氧化剂高锰酸钾可以对水中的有机物进行氧化分解,净化水质。
利用催化剂沸石可以催化废气中的有害物质转化为无害的物质,减少大气污染。
六、总结无机化学是化学的重要分支,研究无机物质及其性质、结构和变化规律。
无机化学大连理工第十六章-d区元素(一)-习题解

第十六章 d区元素(一) 习题解1.完成并配平下列反应方程式。
(1)2TiO2+ + Zn + 4H+→2Ti3+ + Zn2+ + 2H2O(2)2Ti3+ + 3CO32- + 3H2O →2Ti(OH)3(s) + 3CO2(g)(3)TiO2 + H2SO4(浓) →TiOSO4 + H2O(4)TiCl4 + 3H2O →H2TiO3(s) + 4HCl(5)TiCl4 + 2Mg →2MgCl2 + Ti(s)2.完成并配平下列反应方程式。
(1)V2O5 + 2Cl- + 6H+→2VO2+ + Cl2(g) + 3H2O(2)2NH4VO3→V2O5 + 2NH3(g) + H2O (加热)(3)2VO2+ + SO32- + 2H+→ 2VO2+ + SO42- + H2O(4)5VO2+ + MnO4- + H2O →5VO2+ + Mn2+ + 2H+3.已知下列电对的标准电极电势:VO2+ + 2H++ e-→VO2+ + H2O φθ = 0.9994VVO2+ + 2H++ e-→V3+ + H2O φθ = 0.337VV3+ + e-→V2+φθ = -0.255VV2+ + 2e-→V φθ = -1.2V在酸性溶液中分别用1mol·L-1Fe2+,1mol·L-1Sn2+和Zn还原1mol·L-1的VO2+时,最终得到的产物各是什么(不必计算)?解:查附表六可知:Fe3+ + e-→Fe2+φθ(Fe3+/ Fe2+) = 0.769VSn4+ + 2e-→Sn2+φθ(Sn4+/ Sn2+) = 0.1539VZn2+ + 2e-→Zn φθ(Zn2+/ Zn) = -0.7621V当用1mol·L-1 Fe2+还原1mol·L-1的VO2+时,只能得到VO2+离子;当用1mol·L-1 Sn2+Z 在酸性溶液中还原1mol·L-1的VO2+时,首先被还原为VO2+离子,可继续被被还原为V3+离子。
《d区元素》PPT课件

精选PPT
11
• ②第一过渡系列的低氧化态化合物具有还 原性
TiCl2 +TiOCl2 +H2
4CrCl2 +4HCl +O2 == 2CrCl3 +2H2O 2V2VO2 (aq)
Cr3/ Cr2 = 0.41V
VO2 / V2 = 0.05V
2CrCl2 +2HCl== 2CrCl3 +H2
==TiO2·XH2O + 4C4H9OH
精选PPT
22
• 钛的检验: • 以H2SO4—HCl溶解式样生成TiO2+ • TiO2+ +H2O2 ==[TiO(H2O2)]2+ • 3TiO2+ +Al +6H+ ==3Ti3+ +Al3+ +3H2O • Ti3+ +Fe3+ +H2O ==TiO2+ +Fe2+ +2H+ • 以FeCl3滴定,NH4SCN(aq)作指示剂
第十六章 d区元素(过渡)元素
IIIB —VIII 25个元素 (n-1)d 1-9ns1-2
Sc Ti V Cr Mn Fe Co Ni
Y Zr Nb Mo Tc Ru Rh Pd
La Hf Ta W Re Os
Ir Pt
Ac
精选PPT
1
§16—1过渡金属元素的通性
• 第一过渡系列 3d1-84s2 例外Cr : 3d54s1
精选PPT
16
• 三、钼的冶炼
• 辉钼矿 MoS2
• 灼烧 MoS2+2O2 == 2MoO3 +4SO2
大学无机化学d区元素介绍
3.物理性质
(1) 熔点、沸点高
熔点最高的单质:钨(W)
(2) 硬度大 (3) 密度大
熔点: 3410℃ 沸点: 5900℃
硬度最大的金属:铬(Cr)
以金刚石为10,铬为9
密度最大的单质:锇(Os)
(4) 导电性,导热性,延展性好
22.7gcm-3
4.离子呈现多种颜色
物质显色的原因是由于可见光作用到物质上以后物质
12.2.3(2)钒的化学性质
•价电子层结构3d34s2,主要氧化态+5,也能形成氧化态为 +4,+3,+2的化合物。化学性质相当复杂。
VO2+ 1.0 VO2+ 0.36 V3+
-0.25
-0.25
V2+ -1.2 V
17
12.2.3(3)钒的氧化物(V2O5)
•酸碱性: VO碱O2+ 2C +2Cl2 = TiCl4 +2CO 四氯化钛是无色液体,有剌鼻的气味,极易水解, 在潮湿的空气中由于水解而发烟——利用此反应可 制造烟幕:
•TiCl4高温氧化制备优质钛白——氩气氛保护下得Ti: TiCl4(l) +Mg = Ti +2MgCl2
16
12.2.3(1) 钒
•钒在地壳中的含量比锌、铜、铅等普通元素还要多,但分 布很分散,属稀有元素。 •钒被广泛用于制造特种钢和催化剂。
在钛的化合物中,以+4氧 化态的化合物最稳定。二 氧化钛在自然界中有三种 晶型:金红石、锐钛矿和 板钛矿。其中最重要的是 金红石,天然金红石中因 含少量杂质而呈红色或橙 色。
金红石的结构
13
12.2.1(3) 化学性质
•室温下金属钛较稳定,但受热时,钛可与许多非金属,如: 氧、氮、碳、卤素等反应。 •钛在室温下不能与水或稀酸反应,但可溶于浓盐酸或热的 稀盐中形成三价钛离子:
湖南理工学院无机化学习题库第16章d 区元素(一)

第16章 d 区元素(一)一是非题1.按照酸碱质子理论,[Fe(H2O)5(OH)]2+的共轭酸是[Fe(H2O)6]3+, 其共轭碱是[Fe(H2O)4(OH)2]+。
()2. 由Fe3+能氧化I-,而[Fe(CN)6]3-不能氧化 I-,可知[Fe(CN)6]3-的稳定常熟小于[Fe(CN)6]4-的稳定常数。
()3. 某溶液中共存有NO− , Cr O 2− , K + , Fe3+ , Cl −I 和I-,并无任何反应。
()GAGGAGAGGAFFFFAFAF4. 在[Ti(H2O)6]3+配离子中,Ti3+的d轨道在H2O的影响下发生能级分裂,d 电子可吸收可见光中的绿色光而发生d-d 跃迁,散射出紫红色光。
()5. 在 M n+ +ne ====M 电极反应中,加入M n+的沉淀剂,可使标准电极电势Eθ的代数值增大,同类型的难溶盐的K sp值越小,其Eθ的代数值越大。
()二选择题1. 下列过渡元素中能呈现最高氧化数的化合物是()⑴ Fe⑵ CoGAGGAGAGGAFFFFAFAF⑶ Ni⑷ Mn2. Fe3O4与盐酸作用的产物为()⑴ FeCl3+H2O ⑵ FeCl2+H2O⑶ FeCl3+FeCl2+H2O ⑷ FeCl3+Cl2GAGGAGAGGAFFFFAFAF3. Co3O4与盐酸作用的产物为()⑴ CoCl2+H2O ⑵ CoCl3+CoCl2+H2O ⑶CoCl2+Cl2+H2O ⑷ CoCl3+ H2O4. 欲除去 FeCI3中含有的少量杂质 FeCI2,应加入的物质是()⑴通 CI2⑵KMnO4⑶HNO3⑷ K2C r2O75. 下列哪个溶液中,当加入 NaOH 溶液后,仅有颜色发生变化而无沉淀生成的是()⑴ FeSO4⑵KMnO4⑶GAGGAGAGGAFFFFAFAFNiSO4⑷ K2 Cr2O76. 欲制备Fe2+的标准溶液,应选择的最合适的试剂是()⑴ FeCI2溶于水⑵硫酸亚铁铵溶于水⑶ FeCI3溶液中加铁屑⑷铁屑溶于稀酸7. 用来检验 Fe2+离子的试剂为()GAGGAGAGGAFFFFAFAF⑴ NH4SCN ⑵ K3[Fe(CN)6]⑶ K4[Fe(CN)6]⑷ H2S8. 用来检验 Fe3+离子的试剂为()⑴ KI ⑵NH4SCN ⑶ NaOH⑷ NH3·H2O9. [Co(CN)6]4-与[Co(NH3)6]2+的还原性相比较()⑴ [Co(NH3)6]2+还原性强⑵ [Co(CN)6]4-还原性强GAGGAGAGGAFFFFAFAF⑶两者都强⑷两者都不强10 CoCl3·4NH3用H2SO4溶液处理再结晶, SO 可取代化合物中的 Cl-,但NH3的含量不变,用过量AgNO3处理该化合物溶液,每摩尔可得到1mol的AgCl沉淀这种化合物应该是()⑴ [Co(NH3)4]Cl3⑵ [Co(NH3)4Cl]Cl2⑶ [Co(NH3)4Cl2]Cl⑷ [Co(NH3)4Cl3]GAGGAGAGGAFFFFAFAF11. 由 Cr2O3出发制备铬酸盐应选用的试剂是()⑴浓 HNO3⑵ KOH(s) +KCIO3(s) ⑶CI2⑷H2O212. 下列哪一种元素的氧化数为+ IV 的氧化物,通常是不稳定的()⑴ Ti ( IV ) ⑵V( IV ) ⑶Cr( IV ) ⑷ Mn ( IV ) 13. 镧系收缩的后果之一,是使下列哪些元素的性质相似()GAGGAGAGGAFFFFAFAF⑴ Sc 和 La ⑵Cr 和Mo ⑶ Fe、Co 和Ni ⑷ Nb 和 Ta14. 下列各组元素中最难分离的是()⑴ Li 和 Na ⑵ K 和Ca ⑶ Cu 和Zn ⑷ Zr 和 Hf15. 在酸性介质中,欲使 Mn2+氧化为 MnO4,采用的氧化剂应为()⑴ H2O2⑵王水⑶ K2C r2O7+ H2SO4⑷ NaBiO3GAGGAGAGGAFFFFAFAF16 . 向 FeCl3溶液中加入氨水生成的产物之一是()⑴Fe(NH)⑵Fe(OH)Cl2⑶Fe(OH)2Cl ⑷ Fe(OH)317. 下列物质不能在溶液中大量共存的是()⑴ Fe(CN)和OH-⑵Fe(CN)和I-⑶ Fe(CN)和I-⑷Fe3+和Br18. 下列新制出的沉淀在空气中放置,颜色不发生变化的是()GAGGAGAGGAFFFFAFAF⑴ Mg (OH)2⑵Fe(OH)2⑶Co(OH)2⑷ Ni(OH)219. 下列化合物中与浓盐酸作用没有氯气放出的是()⑴ Pb2O3⑵Fe2O3⑶ C o2O3⑷ Ni2O320. 酸性条件下 H2O2与 Fe2+作用的主要产物是()GAGGAGAGGAFFFFAFAF⑴ Fe, O2 和 H+⑵ Fe3+和H2O ⑶ Fe 和H2O ⑷ Fe3+和O2三填空题1. 在地壳中储量居前十位的元素中属于过渡金属的有2. 向 FeCl3溶液中加入KSCN溶液后,溶液变为色,再加入过量的NH4F溶液后,溶液又变为色,最后滴加NaOH溶液时,又有生成。
无机化学课件——第十九章 d区元素

OH
H
(亮绿色)
Cr(OH)
4
H2O Cr2O3 (绿)
19.2.3. 水溶液中离子及其反应
1.Cr(Ⅲ)的盐
Cr(2 SO
4)3,KCr(SO
)
42
12H
2O,
CrCl3
•水解
[Cr(H 2O)6 ]3
[Cr(OH)(H 2O)5 ]2 H
K 104
2Cr3 3S2 6H2O Cr(OH)3(s) 3H2S(g) 2Cr3 3CO32- 3H2O 2Cr(OH)3(s) 3CO2 (g)
2
O
-0.91 Cr
-0.74
EB / V
CrO
2 4
-0.12
Cr(OH)
4
-1.1
Cr(OH) 2
-1.4
Cr
-1.3
•性质 ① 灰白色, 熔点沸点高,硬度大。
② 活泼金属,表面已形成一层氧化膜,活 泼性下降。 ③ 无膜金属与酸的反应
2Cr 2H 2SO4 (浓) Cr(2 SO4)3 3SO2 H2O 在冷、浓硝酸中钝化。
•Cr(Ⅲ)的配合物的多种颜色
[Cr(H2O)6 ]Cl3紫色,[Cr(H2O)5Cl]Cl2 H2O蓝绿色 [Cr(H2O)4Cl2 ]Cl 2H2O绿色
2.Cr2O72-与CrO42-间的转化
•pH值的影响
2CrO
2 4
2H
(黄)
2HCrO
4
Cr2O
2 7
H
2
O
(橙)
pH<2:Cr2O72-为主 pH>6:CrO42-为主
•还原性
酸性条件:E (Cr2O72 / Cr3 ) 1.33V
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
4
Cr2O72 H2O (橙)
pH<2:Cr2O72-为主,pH>6:CrO42-为主。 编辑ppt
(4) Cr(Ⅵ) 的难溶盐
铬酸盐比相应的重铬酸盐溶解度小。 K sp (Ag2CrO4) 1.1×1012 K sp (Ag2Cr2O7 )2.0×107
(3) Cr(Ⅵ) 含氧酸及其离子在溶液中的转化
•H2Cr2O7, H2CrO4均为强酸,仅存在于稀溶液
HC2rO7 H Cr2O72 Ka2 0.85
H2CrO4 H HCrO4 Ka1 9.55
HCrO4 H CrO24 •pH的影响
Ka2 3.2×107
2CrO
2 4
2H
(黄)
2HCrO
2. d区元素原子的价电子层构型
(n-1)d1-10ns1-2 (Pd为5s0)
编辑ppt
3. d区元素的3原. 同六子族周半元期径素(除从Ⅲ上B往)外下由原于子镧半系径收增缩大使,其但同五、
Cs 250 Rb
过族 性渡元质元素相素原似的子。半原径子十半分接径近,导致其元素
原子半径/pm
K 200
编辑ppt
16.1.3 d区元素的化学性质
元素
M2/M
EV
可溶该 金属的
酸 元素
E M2/M V 可溶该 金属的 酸
Sc ---
各种酸
Fe -0.409 稀 HCl H2SO4
等
Ti
-1.63
热 HCl HF Co
-0.282 缓慢溶解 在 HCl 等
酸中
V -1.2 (估算值) HNO3, HF 浓 H2SO4 Ni
同多酸和杂多酸及其盐
编辑ppt
16.3.1 铬、钼、钨的单质
铬分族(VIB):Cr, Mo, W, Sg 价层电子构型:(n-1)d 4-5ns1-2
灰白色金属,熔沸点高,硬度大。 表面易形成氧化膜。
室温时纯铬溶于稀HCl,H2SO4,在浓 HNO3中钝化。高温下与活泼的非金属及 C,B,N反应。
期 族族族族族
族族
4(第一 过渡系)
Sc
Ti
V
Cr
Mn
Fe Co Ni
铁系
Cu
Zn
5(第二
Ru Rh Pd
过渡系) Y Zr Nb Mo Tc 轻铂组 Ag Cd
6 (第三 La过渡系) Lu
Hf
Ta
W
Re
Os Ir Pt
重铂组
Au
Hg
7(第四 Ac过渡系) Lr
Rf
Db
Sg
Bh Hs Mt Uun Uuu Uub
150
2. 同一周期元素从左到右原子半径缓慢
Ba Sr
减小,到铜族元素又稍增第大一。过渡系
第二过渡系
Ca
1. 过渡元素原子半径第一三般过比渡系
Y
较小。
Lu
Zr
Hg
Sc Hf Ti
Ta
Nb
W Re Os
Ir
Au
Cd
Pd
Ag
V
Mo Tc Ru Rh Pt Cr Mn Fe Co Ni Cu
Zn
100
ⅠA ⅡA ⅢB ⅣB ⅤB ⅥB ⅦB Ⅷ Ⅷ Ⅷ ⅠB ⅡB
-0.236
稀 HCl H2SO4 等
Cr -0.90
稀 HCl H2SO4
Cu +0.339
HNO3,浓 热 H2SO4
Mn
-1.18
稀 HCl H2SO4
等 Zn
-0.762
稀 HCl H2SO4
等
编辑ppt
1. 第一过渡系的单质比第二过渡系的单质 活泼; 例:第一过渡系除Cu外均能与稀酸作用, 第二、三过渡系仅能溶于王水、 氢氟酸,而Ru,Rh,Os,Ir不溶于王水。
-0.74
EB
/
V
CrO
2 4
-0.12
Cr(OH)
4
-1.1
Cr(OH) 2
-1.4
Cr
-1.3
酸Cr性O24溶 无液氧中化,性Cr2O
2 7
有强氧化性碱性溶液中,
酸性溶液中, Cr3+稳定
碱性溶液中, [Cr(OH)4]-有还原性
无论酸性或碱性溶液,Cr(Ⅱ)均不稳定
编辑ppt
1.铬(Ⅵ)的化合物
族 编辑ppt
4.d区元素的第一电离能
总趋势:同周期 左右由小大,幅度不大。 同副族 不规律。
编辑ppt
16.1.2 d区元素的物理性质
•熔点、沸点高 熔点最高的单质:钨(W)
•硬度大
硬度最大的金属:铬(Cr)
•密度大
密度最大的单质:锇(Os)
•导电性,导热性,延展性好。
编辑ppt
熔 点 变 化 示 意 图
第十六章 d区元素(一)
§16.1 d区元素概述 §16.2 钛 钒 §16.3 铬 钼 钨 多酸型配合物 §16.4 锰 §16.5 铁 钴 镍 *§16.6 铂系元素简介 *§16.7 金属有机化合物
编辑ppt
族 ⅢB ⅣB ⅤB ⅥB ⅦB Ⅷ ⅠBⅡB
周
钪 钛钒铬 锰 分 分分分 分
铜锌 分分
编辑ppt
16.3.2 铬的化合物
水溶液中铬的各种离子
Cr2+(aq)
颜色 存在的pH
Cr2O
27
橙红
CrO
24
黄
Cr3+(aq) 紫
<2 >6 酸性
Cr(OH)-4 亮绿 Cr2+(aq) 蓝 编辑ppt
强碱 酸性
Cr3+(aq)
• 铬元素的电势图
EA
/V
Cr
2
O
2 7
1.33
Cr 3 -0.41 Cr 2 -0.91 Cr
E Zn2/Zn 0.762V E Cd2/Cd 0.402V E Hg2/Hg 0.852V
总趋势:从上到下活泼性降低。
编辑ppt
16.1.4 d区元素的氧化态
多种氧化态。例如:Mn的氧化态呈连续状, Mn(CO)5Cl(+1),Mn(CO)5,NaMn(CO)5(-1)。 注:红色为常见的氧化态。
2. 与活泼非金属(卤素和氧)直接形成化合物。 3. 与氢形成金属型氢化物:
如:VH18,TaH0.76,LaNiH5.7 。 4. 与硼、碳、氮形成间充型化合物。
编辑ppt
E (Ni2+/Ni) =-0.2363V E (Pd2+/Pd) = +0.92V E (Pt2+/Pt) = +1.2V(估计值)
编辑ppt
§16.1 d区元素概述
16.1.1 d区元素的原子半径和 电离能
16.1.2 d区元素的物理性质 16.1.3 d区元素的化学性质 16.1.4 d区元素的氧化态 16.1.5 d区元素离子的颜色
编辑ppt
16.1.1 d区元素的原子半径和电离能
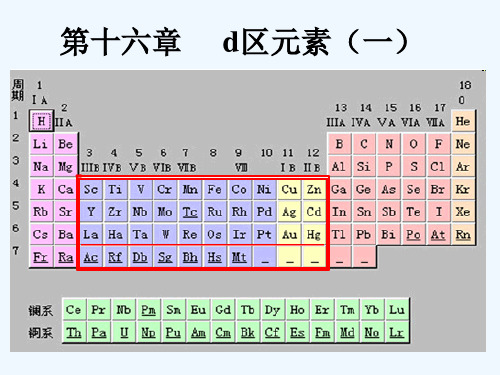
1.d区元素在周期表中的位置
编辑ppt
编辑ppt
16.1.5 d区元素离子的颜色
Mn (Ⅱ) Fe(Ⅱ) Co(Ⅱ) Ni(Ⅱ) Fe(Ⅲ)
水合离子呈现多种颜色。
编辑铬 钼 钨 多酸型配合物
16.3.1 铬、钼、钨的单质 16.3.2 铬的化合物 *16.3.3 钼、钨的化合物 *16.3.4 多酸型配合物
