黄冈中学2018自主招生化学模拟考试题D卷和答案解析
湖北省黄冈中学2018届高三化学5月第三次模拟考试试题201806260353

黄冈中学2018年高三5月第三次模拟考试理科综合化学试题2.可能用到的相对原子质量:H-1 O-16 Na-23 S-32 Fe-56 Cu-647.化学与人类的生产、生活密切相关。
下列说法正确的是()A.某糕点只含面粉、油脂、蛋白质,不含糖,是糖尿病人的最佳食品B.用作荧光灯内壁保护层的氧化铝纳米材料属于胶体C.聚酯纤维属于新型无机非金属材料,可制作宇航服D.高温结构陶瓷耐高温、耐氧化,是喷气发动机的理想材料8.下列实验操作不能达到实验目的的是()实验目的实验操作A 除去蛋白质溶液中混有的(NH4)2SO4 将混合物装入半透膜袋内,并放入流动的蒸馏水中B 除去Mg粉中混有的Al粉加入足量NaOH溶液,过滤、洗涤、干燥C 制备溴苯将苯、溴水、溴化铁混合置于一洁净的试管中D 确定Na2SO3是否变质向Na2SO3溶液中滴加适量的盐酸与BaCl2溶液9.下列关于有机物(a) 、(b) 、(c) 的说法不正确的是()A.三种物质都能发生加成反应B.b物质与甲苯均能使酸性高锰酸钾溶液褪色C.a 与b互为同系物,b与c互为同分异构体D.a、b、c的一氯代物的个数相同,c的二氯代物有7种10.某小组同学利用下图装置测定某过氧化钠样品是否变质,Q为弹性良好的气球不与药品反应,取定量的样品放入其中,按图示安装好仪器,打开分液漏斗的活塞,将稀硫酸滴入气球Q中。
下列说法中不正确的是()A.准确读取量筒I读数后,先关闭K3后打开K2,再打开K1,准确读取量筒II读数B.导管a的作用是平衡分液漏斗上下的压强,使分液漏斗内液体顺利滴下- 1 -C.由相同状况下I、II中测量的气体体积可推知过氧化钠样品是否变质D.b中的固体试剂可以是碱石灰,也可以是无水氯化钙11.A、B、C、D是原子序数依次增大的短周期主族元素,A、B、C的单质(用a、b、c表示)与化合物x、y、z有如图所示的转化关系,D与B同主族,下列说法正确的是()A.x、y、z均是离子化合物B.氢化物的沸点:C>B>DC.B和C元素组成的化合物的水溶液一定呈碱性D.简单离子半径:D>C>B12.装置(I)是一种可充电电池,装置(Ⅱ)为惰性电极的电解池。
2018届黄冈中学自主招生化学模拟试题2

2018届黄冈中学自主招生化学模拟试题2时间:40分钟分值:50分可能用到的相对原子质量:H :1,C :12,N :14,O :16,S :32,K :39,Ca :40,Fe :56 一、单项选择题(每小题2分,共8小题,共16分)1.以下是我们熟悉的几种气体,其中可用右图所示装置干燥并收集的是(省略了铁架台等仪器) :( ) ①H 2 ②O 2 ③CO 2 ④SO 2 ⑤CH 4 A .①② B .③④ C .①⑤ D .①②⑤3.某种溶液里含有K +、Cu 2+、SO 42一、Al 3+和Cl 一,则该溶液中的溶质至少有( ) A .2种 B .3种 C .4种 D .5种2.某同学用含有杂质碳酸钠的烧碱样品与盐酸发生中和反应,那么与等质量等溶质质量分数的盐酸溶液恰好中和时,所用烧碱样品质量比用纯氢氧化钠的质量( ) A .偏高 B .偏低 C .不变 D .无法比较3.有A 、B 两种混合粉末,质量分别为m 1,m 2。
A 由CaCO 3和KHCO 3组成,B 由MgCO 3和NaHCO 3组成。
将A 、B 分别与足量稀盐酸反应,生成二氧化碳气体的质量均为wg 。
下列说法正确的是( ) (已知:KHCO 3+HCl=KCl+CO 2↑+H 2O NaHCO 3+HCl=NaCl + CO 2↑+ H 2O ) A .100m 1 = 84m 2 B .m 1 = m 2C .混合物B 中MgCO 3和NaHCO 3质量比可为任意比D .混合物A 中CaCO 3和KHCO 3质量比一定为1∶1 4.取一定量氧化铁与氧化铜的混合物,向其中加入50克、14.6%的稀盐酸,恰好完全反应生成盐和水,则原混合物中氧元素的质量是( ) A.6.4克B.3.2克 C .1.6克 D .0.8克5.已知所含元素化合价发生变化的反应是氧化还原反应,其中被还原的元素化合价降低,被氧化的元素化合价升高.海洋中有丰富的资源,如图所示利用海水可获得许多化工产品。
湖北省黄冈中学化学自主招生试卷
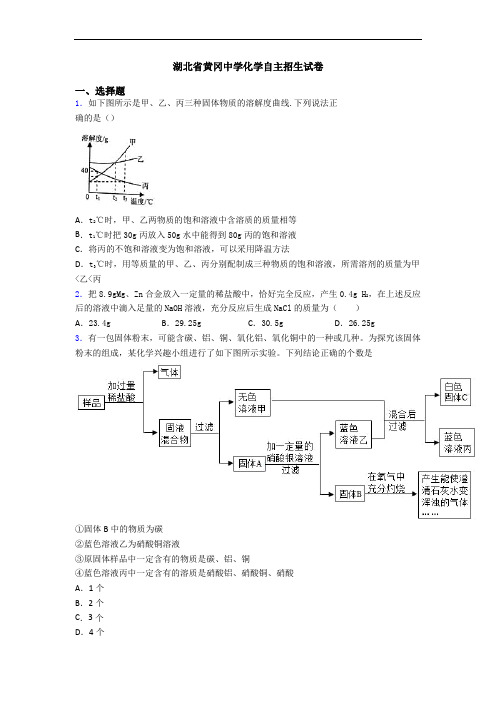
湖北省黄冈中学化学自主招生试卷一、选择题1.如下图所示是甲、乙、丙三种固体物质的溶解度曲线.下列说法正确的是()A.t2℃时,甲、乙两物质的饱和溶液中含溶质的质量相等B.t1℃时把30g丙放入50g水中能得到80g丙的饱和溶液C.将丙的不饱和溶液变为饱和溶液,可以采用降温方法D.t3℃时,用等质量的甲、乙、丙分别配制成三种物质的饱和溶液,所需溶剂的质量为甲<乙<丙2.把8.9gMg、Zn合金放入一定量的稀盐酸中,恰好完全反应,产生0.4g H2,在上述反应后的溶液中滴入足量的NaOH溶液,充分反应后生成NaCl的质量为()A.23.4g B.29.25g C.30.5g D.26.25g3.有一包固体粉末,可能含碳、铝、铜、氧化铝、氧化铜中的一种或几种。
为探究该固体粉末的组成,某化学兴趣小组进行了如下图所示实验。
下列结论正确的个数是①固体B中的物质为碳②蓝色溶液乙为硝酸铜溶液③原固体样品中一定含有的物质是碳、铝、铜④蓝色溶液丙中一定含有的溶质是硝酸铝、硝酸铜、硝酸A.1个B.2个C.3个D.4个4.如图所示,其中甲、乙、丙、丁、戊分别是铁、盐酸、氢氧化钙、二氧化碳、碳酸钠中的一种.图中相连的两圆表示相应物质能发生反应,已知乙是铁.下列说法错误的是A.五种物质中,只有铁是单质B.丙是盐酸C.戊是氢氧化钙D.甲与丁反应属于复分解反应5.除去下列各组物质括号内的杂质,所选用的试剂及操作方法均正确的是A.Fe2O3(Fe)——用盐酸浸泡,然后过滤、洗涤、烘干B.CO(CO2)——先通入足量的浓NaOH溶液,后通过浓硫酸C.CaO(CaCO3)——加水溶解,过滤、烘干D.NaCl(Na2CO3)——加入过量CaCl2溶液,过滤、蒸发、结晶6.用数形结合的方法表示某些化学知识直观、简明、易记.下列用数轴表示正确的是()A.不同物质的着火点:B.硫及其化合物与化合价的关系:C.50g19.6%的稀硫酸与足量的金属反应产生氢气的质量:D.物质形成溶液的pH:7.甲、乙两种固体物质(不含结晶水)的溶解度曲线如图所示。
广东省惠州市黄冈中学2018-2019学年高一化学模拟试卷含解析

广东省惠州市黄冈中学2018-2019学年高一化学模拟试卷含解析一、单选题(本大题共15个小题,每小题4分。
在每小题给出的四个选项中,只有一项符合题目要求,共60分。
)1. 在碱性溶液中能大量共存且溶液为无色透明的离子组是()A.K+、MnO4-、Na+、Cl-B.K+、Na+、NO3-、CO32-C.Na+、H+、NO3-、SO42-D.Fe3+、Na+、Cl-、SO42-参考答案:B略2. 氧化还原反应的实质是电子的转移,下列关于氧化还原反应的叙述正确的是()A.在氧化还原反应中,有一种元素被氧化,肯定有另一种元素被还原B.11.2 L Cl2通入足量的NaOH溶液中,转移的电子数为0.5N AC.难失电子的原子,得电子的能力一定强D.元素由化合态变成游离态时,它可能被氧化,也可能被还原参考答案:D【考点】氧化还原反应.【分析】A.在氧化还原反应中,被氧化或被还原是元素可能是同一种元素;B.温度和压强未知导致气体摩尔体积未知;C.难失电子的原子得电子的能力不一定强;D.元素由化合态转化为游离态,得电子被还原,失电子被氧化.【解答】解:A.在氧化还原反应中,被氧化或被还原是元素可能是同一种元素,如Cl2+2NaOH=NaCl+NaClO+H2O,故A错误;B.温度和压强未知导致气体摩尔体积未知,则无法计算气体的物质的量和转移电子数,故B错误;C.难失电子的原子得电子的能力不一定强,如稀有气体原子,故C错误;D.元素由化合态转化为游离态,如果得电子发生还原反应而被还原,如果失电子发生氧化反应而被氧化,故D正确;故选D.3. 根据所给的信息和标志,判断下列说法错误的是 ( )碳酸氢钠药片该药是抗酸药,服用时喝看到有该标志的丢弃物,贴有该标志的物参考答案:BA. 麻黄碱具有平喘功能,常常用于治疗气喘咳嗽,A正确;B.醋酸能够与碳酸氢钠反应,降低药效,B错误;C.图示标志为放射性标志,对人体伤害较大,看到有该标志的丢弃物,应远离并报警,C正确;D.该标志为可回收物标志,D正确;答案选B。
湖北黄冈中学自主招生考试化学模拟试题

2018年预录模拟考试化学试题(五)相对原子质量H:1 C:12 N:14 O:16 Mg:24 S:32 Cu:64 Cl:35.5 Ag:108 Ba:137 一、选择题(本题包括9个小题,每小题有1个或2个选项符合题意,共18分。
) 1.下列各组内的物质充分反应后过滤 , 所得溶液的质量与反应前溶液的质量相比,一定减少的是 A. 铜加入到硝酸银溶液中 B. 铝加入到稀硫酸中C.二氧化碳通入到石灰水中D. 碳酸钠固体加入到稀盐酸中 2.根据下表物质的命名规律,可将K 2CS 3应命名为名称 硫代硫酸钠 多硫化钙 过氧化钡 超氧化钾化学式Na 2S 2O 3 CaS x BaO 2 KO 2 A .三硫代碳酸钾 B .多硫碳酸钾 C .过硫碳酸钾 D .超硫碳酸钾3.工业品盐酸中因含有Fe 3+而带黄色,若某工业品盐酸中的H +和Cl -的个数比为91:94,则该盐酸中Fe 3+和Cl -的个数比为A .1:1B .1:3C .91:94D .1:944、如右图所示的甲、乙两个装置中,胶头滴管中吸入某种液体,平底烧瓶中充入(或放入)另一种物质,挤压胶头滴管加入液体,一段时间后两装置中的气球都明显胀大(忽略液体体 积对气球体积的影响)。
则滴管和烧瓶中所用试剂可能是5.某溶液中存在Mg 2+、Ag +、Ba 2+三种金属离子,现用NaOH 、Na 2CO 3、NaCl 三种溶液使它们分别沉淀并分离出来,要求每次只加一种溶液滤出一种沉淀,所加溶液顺序正确的是A 、Na 2CO 3 NaCl NaOHB 、NaOH NaCl Na 2CO 3C 、NaCl NaOH Na 2CO 3D 、NaCl Na 2CO 3 NaOH 6.根据“绿色化学”的思想,某化学家设计了下列化学反应步骤:该方案的主要目的是为了制备A .HBrB .CaOC .H 2 D. Hg7.新型纳米材料MFe 2O x 中M 表示+2价的金属元素,在反应中化合价不发生变化。
湖北省黄冈中学高三化学5月第三次模拟考试试题

黄冈中学2018年高三5月第三次模拟考试理科综合化学试题2.可能用到的相对原子质量:H-1 O-16 Na-23 S-32 Fe-56 Cu-64 7.化学与人类的生产、生活密切相关。
下列说法正确的是()A.某糕点只含面粉、油脂、蛋白质,不含糖,是糖尿病人的最佳食品B.用作荧光灯内壁保护层的氧化铝纳米材料属于胶体C.聚酯纤维属于新型无机非金属材料,可制作宇航服D.高温结构陶瓷耐高温、耐氧化,是喷气发动机的理想材料8.下列实验操作不能达到实验目的的是( )9.下列关于有机物 (a)、(b) 、(c) 的说法不正确的是()A.三种物质都能发生加成反应B.b物质与甲苯均能使酸性高锰酸钾溶液褪色C.a 与b互为同系物,b与c互为同分异构体D.a、b、c的一氯代物的个数相同,c的二氯代物有7种10.某小组同学利用下图装置测定某过氧化钠样品是否变质,Q为弹性良好的气球不与药品反应,取定量的样品放入其中,按图示安装好仪器,打开分液漏斗的活塞,将稀硫酸滴入气球Q中。
下列说法中不正确的是()A.准确读取量筒I读数后,先关闭K3后打开K2,再打开K1,准确读取量筒II读数B .导管a 的作用是平衡分液漏斗上下的压强,使分液漏斗内液体顺利滴下C .由相同状况下I 、II 中测量的气体体积可推知过氧化钠样品是否变质D .b 中的固体试剂可以是碱石灰,也可以是无水氯化钙11.A 、B 、C 、D 是原子序数依次增大的短周期主族元素,A 、B 、C 的单质(用a 、b 、c 表示)与化合物x 、y 、z 有如图所示的转化关系,D 与B 同主族,下列说法正确的是()A .x 、y 、z 均是离子化合物B .氢化物的沸点:C>B>DC .B 和C 元素组成的化合物的水溶液一定呈碱性D .简单离子半径:D>C>B12.装置(I)是一种可充电电池,装置(Ⅱ)为惰性电极的电解池。
下列说法正确的是()A .闭合开关K 时,电极B 为负极,且电极反应式为:2Brˉ-2eˉ=Br 2B .装置(I)充电时,总反应为:Na 2S 4+2NaBr=2Na 2S 2+Br 2C .该装置电路中有0.1moleˉ通过时,电极X 上析出3.2gCuD .一段时间后装置(Ⅱ)中X 电极周围溶液的pH 减小13.25℃时,向Na 2CO 3溶液中滴入盐酸,混合溶液的pH 与离子浓度变化的关系如图所示。
广东省潮州市黄冈中学2018-2019学年高三化学模拟试题含解析

广东省潮州市黄冈中学2018-2019学年高三化学模拟试题含解析一、单选题(本大题共15个小题,每小题4分。
在每小题给出的四个选项中,只有一项符合题目要求,共60分。
)1. 下列现象或事实不能用同一原理解释的是()A.浓硝酸和氯水用棕色试剂瓶保存 B.硫化钠和亚硫酸钠固体长期暴露在空气中变质C.Cl2和SO2都能使品红溶液褪色 D.SO2和Na2SO3溶液都能使溴水褪色参考答案:C略2. 咖喱是一种烹饪辅料,若白衬衣被咖喱汁玷污后,用普通肥皂洗涤该污渍时会发现,黄色污渍变成红色,经水清洗后红色又变成黄色。
据此现象,你认为咖喱汁与下列何种试剂有相似的化学性质()A.品红溶液 B.石蕊溶液 C.次氯酸钠 D.无水硫酸铜参考答案:B略3. 催化加氢可生成3-甲基己烷的是A.B.C.D.参考答案:C4. 下表是元素周期表的一部分,有关说法正确的是A.e的氢化物比d的氢化物稳定B.a、b、e三种元素的原子半径:e>b>aC.六种元素中,c元素单质的化学性质最活泼D.c、e、f的最高价氧化物对应的水化物的酸性依次增强参考答案:D略5. 下列物质的分类结果全部正确的是A.NO2—酸性氧化物 Na2O2—碱性氧化物Al2O3—两性氧化物 B.汽油—混合物胆矾—纯净物HD—单质C.纯碱—碱硫化氢—酸小苏打—酸式盐D.液氯—非电解质硫酸钡—强电解质醋酸—弱电解质参考答案:B6. 用N A表示阿伏加德罗常数的值,下列叙述正确的是A.含有N A个氮原子的氮气在标准状况下的体积约为11.2LB.25℃,1.01×105Pa,64gSO2中含有的原子数小于3N AC.在常温常压下,11.2L Cl2含有的分子数为0.5N AD.标准状况下,11.2LH2O含有的分子数为0.5N A参考答案:A解析:A、0.5mol氮气含N A个氮原子,故标况下氮气体积约为0.5Vm=11.2L,故A正确;B、64gSO2中含有的原子数等于3N A,故B错误;C、强调标况下,故C错误;D、标况下水是液体,故D错误;7. 下列离子方程式中正确的是A.在漂白粉的溶液中通入一定量的二氧化硫气体B.在偏铝酸钠溶液中通入过量的二氧化碳气体C.纯碱溶液与胆矾溶液混合生成正盐、酸式盐、碱式盐D.在氯化铝溶液中滴入过量的氨水参考答案:C8. 在甲、乙两烧杯溶液中,分别含有大量的Cu2+、K+、H+、Cl-、CO32-、OH-6种离子中的3种,已知甲烧杯的溶液呈蓝色,则乙烧杯的溶液中大量存在的离子是()A.Cu2+、H+、Cl- B.CO32-、OH-、Cl-C.K+、H+、Cl- D.K+、OH-、CO32-参考答案:D略9.参考答案:答案:D10. 常温下,0.1mol/L醋酸溶液的pH=3。
2018年湖北省黄冈市中考化学一模试卷(解析版)
2018年湖北省黄冈市中考化学一模试卷一、选择题(每题1分,共8分)1.(1分)下列生活中的变化过程只发生物理变化的是()A.从铝土矿中提取金属铝B.秸秆、杂草、粪便等在沼气池中发酵制得甲烷C.二氧化碳气体经降温、加压制得干冰D.排放到空气中的二氧化硫形成酸雨2.(1分)下列图示的实验操作中,错误的是()A .稀释浓硫酸B .测定溶液的pHC .加入粉末状固体D .蒸发食盐水3.(1分)归纳是学习化学的基本方法。
下面是小明整理的部分化学知识,完全正确的一组是()A.A B.B C.C D.D4.(1分)关于C、CO、CO2三种物质,有下列说法:①三种物质都含有碳元素,都具有还原性②CO、CO2都是没有颜色、没有气味的气体③CO2可用于光合作用,CO可用于人工降雨④CO2能产生温室效应,CO易于血液中的血红蛋白结合引起中毒⑤CO2可用来灭火,CO可用作燃料上述说法中正确的是()A.①②③B.②③④C.②④⑤D.①③⑤5.(1分)如图是甲、乙、丙三种物质的溶解度曲线,下列说法正确的是()A.t1℃时,将等质量的甲、丙不饱和溶液分别用添加溶质的方法形成饱和溶液,所加的溶质质量相等B.t2℃时,将30g甲物质加入到50g水中不断搅拌,形成的溶液中溶质的质量分数是37.5%C.t2℃时,将甲、乙、丙三种物质的饱和溶液降温到t1℃,析出晶体最多的是甲D.要配制相同质量分数的甲、丙两种物质的饱和溶液,应该将温度控制在t1℃6.(1分)工业上用甲、乙制备化学肥料丙,同时有丁生成。
根据下列微观示意图得出的结论中,正确的是()①甲的化学式为NH3②乙、丙、丁都是氧化物③丙中氮、氢元素质量比为7:1 ④参加反应的甲、乙质量比为17:44。
A.①B.①③C.①④D.②④7.(1分)下列设计的实验方案中(括号中为方法或试剂),你认为可行的是()A.验证铁、铜、银的金属活动性顺序(硫酸亚铁溶液、硝酸铜溶液、银丝)B.鉴别NaCl溶液、Na2SO4溶液和(NH4)2SO4[分别滴加Ba(OH)2溶液]C.除去CO中的少量H2O和CO2(先通过浓硫酸,再通过氢氧化钠溶液)D.分离氧化钙中混有的碳酸钙粉末(加水溶解,过滤)8.(1分)含硫煤燃烧会产生SO2造成大气污染,某工厂设计了如下工艺流程,防治污染的同时可以得到化工产品,下列叙述不正确的是()A.该流程中可得到化工产品H2SO4B.该流程中化合价发生改变的元素为Fe和SC.流程中涉及到的反应之一为:Fe(SO4)3+SO2+2H2O=2FeSO4+2H2SO4D.该工艺流程中Fe2(SO4)3溶液可以循环使用二、填空简答题(4小题,共20分)9.(4分)化学是一门以实验为基础的科学,下面是初中化学中几个重要的对比实验(1)在甲实验中,观察到烧杯溶液变红,由此可验证分子的性质;(2)图乙装置是电解水的实验,实验中用来检验a中收集到的气体,实验说明水是由氢元素和氧元素组成的,得出该结论的化学方程式是。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
黄冈中学2017年自主招生(理科实验班)预录考试化学模拟试题(D卷)可能用到的相对原子质量 H=1 O=16 S=32 C=12 Cu=64 Mg=24 Al=27 Ca=40 Ba=137 Fe=56一、选择题。
(每小题只有1个答案,共18分)1、下列实验操作能达到目的的是 ( )A. 向滴有酚酞的Na2CO3溶液中加入BaCl2溶液,溶液褪色,则证明BaCl2有酸性B. 准确称取2.80gCa(OH)2,加入97.2g水中配制100g 2.8%的Ca(OH)2溶液C. 在实验室,可无需查阅资料用50%的硝酸来配制50g20%的硝酸溶液D. 通过灼热的镁粉除去CO2中的O22、实验室制备氯气:MnO2+4HCl(浓)MnCl2+ Cl2↑+2 H2O反应会因盐酸浓度下降而停止。
为测定反应残余液中盐酸的浓度,探究小组同学设计了4组实验方案(每次均量取20 g反应残余液进行实验),其中正确的是()A.与足量AgNO3溶液反应,过滤、洗涤、干燥,称量生成的沉淀质量为a gB.稀释10倍后取20 mL用已知浓度的NaOH溶液滴定,消耗NaOH的体积为b gC.与足量NaHCO3固体反应,逸出气体用足量碱石灰吸收,增重c gD.加入d1g CaCO3(过量)充分反应后,过滤、洗涤、干燥,称量剩余固体质量为d2 g (已知:相同条件下 MnCO3的溶解度远远小于CaCO3)3、甲、乙两烧杯内盛有等质量、等质量分数的盐酸.将镁逐渐加入甲烧杯,铁逐渐加入乙烧杯,测量加入的金属质量m和相应的烧杯内物质质量变化量△m,画出△M﹣m曲线oac和obc的示意图,如图所示.根据图中信息,下列说法错误的是()A.m1:m2=3:7 B.m1﹣△M1<m2﹣△M2C.曲线oac表示的是甲烧杯中△M与m的变化关系D.当乙烧杯内加入铁的质量为m1时,溶液中溶质不止一种4、小明向盛有盐酸和MgCl2溶液的烧杯中加入一定量的NaOH溶液,为判断反应后溶液的成分,他分别取少量反应后的溶液a于试管中,用下表中的试剂进行实5、列表和作图是常用的数据处理方法.结合所绘图表判断下列说法正确的是()氢氧化钠、碳酸钠分别在水、酒精中的溶解度A .图象与表格均能反映温度对固体物质溶解度的影响,其中表格的优点是变化规律更直观B .由表格数据可知,物质的溶解度只受温度影响C .40℃时,将50g NaOH 分别投入到100g 水和酒精中都能得到饱和溶液D .40℃时,将CO 2通入饱和的NaOH 酒精溶液中有沉淀生成 6、下列有关实验现象和解释或结论都正确的是 ( )A.黑色粉末:FeO 、Fe 、CuO 、C 只用一种试剂即可鉴别B.无色溶液:KOH 、H 2SO 4、CuCl 2、NaNO 3 只用一种试剂即可鉴别C.无色溶液:Na 2CO 3、AgNO 3、BaCl 2、HCl 不用其他试剂就可以鉴别D.无色溶液:Ba(OH)2、Na 2CO 3、BaCl 2、HNO 3 不用其他试剂就无法鉴别8、某溶液可能含有盐酸、硫酸、硫酸镁、碳酸钠、硝酸钠、氯化铜中的一种或几种,为了探究其组成,向一定质量的该溶液中逐滴加入氢氧化钡溶液,钡溶液的质量之间的关系如图所示。
下列相关说法正确的是 ( ) A .加入氢氧化钡溶液至过量,可能发生了三个化学反应 B .该溶液一定含有盐酸,应该含有氯化铜或硫酸镁中的 一种或两种,可能含有硝酸钠C .反应过程生成的沉淀是氢氧化铜,依据沉淀质量9.8克 可以求出到达b 点时所消耗氢氧化钡溶液中溶质的质量是17.1gD .到达a 点时溶液中溶质是BaCl 2 、CuCl 2,可能有NaNO 3 9、右下图中相连的两个圆圈里的物质在一定条件下可以发生化学反应.下列四组选项中, 不A.A B.B C.C D.D10、已知t℃时,盐M(不含结晶水,式量═126)的溶解度为S g.在一定量的M的水溶液中加入ag M后,恰好为t℃时的饱和溶液.若用M•7H2O代替M,欲使原溶液在t℃时恰好饱和,则需加入M•7H2O的质量(g)为()A.2a B.(2+)a C.D.(2+)a11、现有含杂质的硝酸钠溶液,为确定其组成,某同学设计了如下实验:下列判断正确的是()A.无色溶液B的溶质是硝酸钙B.原溶液中的杂质可能由氯化钙、硝酸钙和氯化钠三种物质组成C.原溶液中的杂质只有氯化钙D.该实验中涉及的基本反应类型不止一种12、已知硝酸是一种强氧化性酸,能把SO32-氧化成为SO42-,则下列实验方案能够确定某未知试液中存在SO42-的是( )A. 取少量试液,滴加BaCl2溶液,生成白色沉淀,再加入足量稀盐酸,沉淀不溶解B. 取少量试液,加入足量稀硫酸,没有明显现象,再滴加BaCl2溶液,生成白色沉淀C. 取少量试液,加入足量稀盐酸,没有明显现象,再滴加BaCl2溶液,生成白色沉淀D. 取少量试液,加入足量稀硝酸,没有明显现象,再滴加Ba(NO3)2溶液,生成白色淀二、填空及简答题。
(3个小题,共19分)13.水是生命之源,与生活生产关系密切.保护水环境、珍爱水资源,是每个公民应尽的责任和义务.(1)为了防止水的污染,下列做法有利于保护水资源的是______(填编号).①抑制水中所有动、植物的生长;②不任意排放工业废水;③大量使用化肥农药;④生活污水经过净化处理后再排放.(2)天然水中含有许多杂质,自来水生产过程中,常用过滤的方法除去水中悬浮的杂质,同时还必须进行消毒.ClO2是一种新型的自来水消毒剂,工业上用Cl2与NaClO2制取ClO2,另外得到一种常见的盐.写出化学方程式:。
(3)在化学实验和科学研究中,水也是一种常用的试剂.水分子在特定条件下容易得到一个H+,形成水合氢离子(H3O+).下列对上述过程的描述不合理的是______A.氧元素发生了改变 B.微粒的组成发生了改变C.微粒的化学性质发生了改变 D.与水分子比水合离子的电子数发生了改变(4)医药上可用石膏来固定骨折部位.石膏有熟石膏(2CaSO4•H2O)和生石膏(CaSO4•2H2O)两种,骨折固定时发生反应的化学方程式.(5)要检验硬水需要用到肥皂水。
肥皂的主要成分为硬脂酸钠(C17H35COONa),它是一种有机酸的钠盐,在肥皂水中滴入盐酸会发生复分解反应出现白色沉淀,这沉淀物是(写化学式);若在肥皂水中加入硬水(含Ca2+、Mg2+)也会出现白色沉淀,此沉淀主要是(写名称)。
14、(8分)(1)金属钴(相对原子质量59)和铁一样,也有+2和+3价,可以组成三种氧化物。
在空气中煅烧草酸亚钴(CoC2O4)生成钴的一种氧化物和CO2气体。
取一定草酸亚钴充分煅烧后,测得固体质量为4.82g,生成CO2的质量为5.28g。
试写出空气中煅烧草酸亚钴的化学方程式:。
(2分)(2) CO与 PdCl2溶液反应产生黑色金属钯粉末,反应中有水参加,利用此反应可用氯化钯检测CO对大气的污染情况,此反应的化学方程式为(3) Ag3PO4、Ag2HPO4均为黄色沉淀.某同学向Na3PO4溶液中逐滴滴加硝酸银溶液至恰好完全反应,生成黄色沉淀,①若黄色沉淀是Ag3PO4,写出反应的化学方程式③试设计一个简单的实验方案,来证明所生成的黄色沉淀是Ag3PO4还是Ag2HPO4 :过滤,取反应后的溶液15、在A、B、C、D四种元素原子的核电荷数均小于18,且依次增大。
A、C可按原子个数比为1:1或2:1形成X、Y两种常见化合物,常温下为液态, B、C可按原子个数比为1:1或1:2形成M、N两种常见化合物,常温下为气态, D、C 可按原子个数比为1:2或1:3形成Q、R两种化合物,Y能分别与Q、R发生化合反应得到两种产物的水溶液常温时pH都小于7。
(1) 写出有关物质的化学式,X为,M为。
(2) X也能与Q发生化合反应,其化学方程式为。
(3)Y与 R发生化合反应的化学方程式为。
(3)当两微粒的原子个数相等、核外电子数之和也相等时,可互称为等电子体。
如:SO2与O3、CN-与N2互为等电子体,写出与N2O互为等电子体的一种微粒的化学式。
三、实验探究题16、(10分)现有一瓶含NaCl杂质的Na2CO3样品,某同学设计了一种测定其纯度的方法,装置如下图,其中A容器中盛有样品10.0 g,分液漏斗内盛有稀硫酸,B容器内为碱石灰固体。
(1)该同学重复操作了三次,每次操作均正确,且装置不漏气,可是结果数据出现了较大偏差(容器内反应均完全,装置内空气的影响忽略不计),请你分析可能的原因(最少写出两条) ,。
(2)通过仔细分析,该同学重新设计了一套实验装置如下图,请回答有关问题:(可供选择的试剂还有..Zn片、浓硫酸、NaOH溶液、CaCO3固体、蒸馏水、碱石灰)①该套装置未画完整,请在你认为需要补充装置的虚框内画出合适的简图,并注明试剂。
(多画适当扣分)②A装置的广口瓶中应加入的试剂是;该装置的作用是。
③如果实验后测得E装置质量增重3.52 g,则该Na2CO3试样的纯度为__________。
(3)测定该Na2CO3试样纯度的方法有多种,请你利用不同的反应原理.......再设计一套方案。
要求写出实验操作流程和试样中Na2CO3纯度的表达式。
(试剂任选)操作流程按下列图示表述:①操作流程为:②实验时称量样品的质量为a克,所测物质的质量为b克,该试样中Na2CO3纯度的表达式为:。
参考答案化学模拟试题(D卷)可能用到的相对原子质量 H=1 O=16 S=32 C=12 Cu=64 Mg=24 Al=27 Ca=40 Ba=137 Fe=56 一、选择题。
(每小题只有1个答案共18分)CBBBDD DDCCBC二、填空及简答题。
(4个小题,共19分)13.(1)②④(2) Cl2+ 2NaClO2═2NaCl+ 2ClO2(3) A D (4)[2CaSO4•H2O]+ 3H2O==== 2 [CaSO4•2H2O](5) C17H35COOH 硬脂酸钙14、 (1) 3CoC2O4+2O2Co3O4+6CO2(3)① Na3PO4 + 3AgNO3═ Ag3PO4↓+3NaNO3② Na3PO4 + 2AgNO3 + H20 == Ag2HPO4↓+ 2NaNO3 + NaOH③过滤,测滤液的pH值15.(1) H2O2 CO (2) H2O2+SO2=H2SO4(3) H2O + SO3=H2SO4 (4) CO2三、实验及计算(2题,共13分)16、(1)①A中产生的CO2气体未全部进入B;②CO2中混有的少量水蒸气进入B;③ B吸收了空气中的水蒸气、CO2。
(2)①② Zn片和蒸馏水;利用A中生成的H2将C中的CO2全部排入E中被碱石灰吸收;③ 84.8%(3)①或②53b/50a 或 106(b-a)/11a17、(1)1、2; ( 2)40; (3)10.6%.。
