有机化学-第12章 习题解答
有机化学各大名校考研真题第十二,十三章

12-1试为下述反应建议合理的,可能的分布反应机理:O CH 3OCH3OHCH3ONaCH3OO解:钠醇攻击羰基,打开碳氧双键,形成烷氧负离子,同时OCH3加到碳原子上,电子发生转移后,环断裂,同时另一个环上的酮异构为烯醇式结构,再成环即得到产物。
机理过程为:OOOCH3OO OCH3CH3COOCH3O CCH3O OOCH3 CH3O OCH3OCH3HO OOCH3OCH3O12-2反应机理推断 1)CHO+CH 3NO 2NaOHC HCHNO 2(2)C OR 'CH 2R+HCHO +HN(CH 3)2HCOR 'H C RCH 2N(CH 3)2解(1)硝基甲烷在碱性条件下失去一个质子形成碳负离子,碳负离子为亲核试剂,攻击羰基使电子转移形成氧负离子,得到一个质子后氧负离子变为羟基,脱去一分子水形成双键,得到所求产物,反应机理如下:OHCH 3NO 2OHCH 2NO 2+CH 2NO2C OHCH 2NO2C OH HCH 2NO 2H 2OCH CHNO 2(2)甲醛与仲胺发生加成反应,羟基在酸性条件下脱去形成双键和氮原子,酮异构为烯醇结构,电子转移后发生亲核加成得到产物,过程为:H 2CO+HN(CH 3)2H 2COHN(CH 3)2HH 2CN +(CH 3)2COR 'CH 2RHCCHROHR'H 2CN(CH 3)2COHR 'H C CH 2N(CH 3)2RCR 'H C OHRCH 2N(CH 3)2-H +12-3对下列反应提出合理解释。
OO+OEtONaOO解; 该题涉及两个反应,分别为碳负离子与羰基加成以及碳负离子与αβ不饱和烯烃的迈克尔加成反应,均为碳负离子机理。
机理为:OOEtO -OOOOOEtO -OOO OHO O-H 2OOOO12-4用合理分步的反应机理解释下列反应事实:OOOHOHHOO解:环状缩酮中的一个O 结合H 开环生成羟基,另一个收H 2O 攻击,碳氧双键断裂。
陈宏博主编有机化学题解
CH3 + H3O Br NH2
Br NHCCH3 O
(6)
HNO3 浓H2SO4 NO2 Fe HCl NH2 NO2 Fe HCl NH2 H2SO4 180~1900C SO3H NaNO2,HCl 0~50C NH2 CH3OH
N(CH3)2 _ N+ 2Cl
加 NaOH 水 溶 液 , 过 滤 , 在 滤 液 中 加 HCl, 得
2
CH3CH2CH2CH2NH2
CH3CH2CH2CH2NHCH3 加Na CO ,分液,在水相中加入HCl,得
2 3
COOH
,有机相中加NaOH,
分液在水相中通入CO2,得
H3 C
OH
O2N
,在有机相中,加HCl溶液,分液,在水相中加NaOH,
(5)
CH3
OH
(6)
CH3
OH CH3 N N
(7)
CH3
N N
N(CH3)2
(8)
12-9 完成下列合成。 (1)乙烯 丙腈和丁二腈 已二胺 正戊胺和正丙胺 (2)1-溴丁烷 (4)甲笨 2-氨基丁烷
CH3O CH2CH2NH2
(3)1,3-丁二烯 (5)正丁醇
CH2=CH2 + HBr 答: (1)A:
Br
+
N2Cl C2H5OH NO2
Br
Fe HCl NO2
Br NH2
NaNO2 , HCl 0~5℃
CuCl2
Br Cl
(4)
HNO3 浓H2SO4
NO2 Fe HCl
NH2 NH2 H2SO4 180~1900C Br Br2 H2O SO3H
有机化学课后习题答案12第十二章醛和酮核磁共振谱(第5轮)答案

R1 CO
R2
Nu- R1 OC
slow R2 Nu
A+
fast
R1 OA C
R2 Nu
影响亲核加成反应的因素: A. 亲核试剂的浓度和强度 B. 羰基的极性大小,羰基碳上的正电荷越多反应活性越大 C. 羰基所连基团的空间体积的大小,空间体积大,体阻大,反应活性小。
132
综合影响的结果,其活性顺序为:
O R CH C
羰基的亲核加成反应及还原反应
α—H的反应
H
H (R')
2.醛、酮的化学性质
(1)亲核加成反应(π键断裂):
醛的氧化反应
HCN OH-
R
OH
C
CN
H2O H+
R
OH 与氢氰酸的反应,醛、脂肪族甲基酮及少于
C COOH 8个碳的脂环酮能发生该反应。生成2-羟 基酸,多用于增加1个碳原子的合成。
三.例题解析 【例题 1】用系统命名法命名下列化合物
133
1. HO CH2CH2CHO 2.
CH2COCH3
C6H5
CH3
3.
4.
CH3CHCHO
3–羟基丙醛
1–苯基–2–丙酮
2–苯基丙醛
【例题 2】写出下列化合物的结构式
1. 2-丁烯醛
2. 环己基甲醛 3. 3-(间羟基苯基)丙醛
O 4–甲基环己酮
8.
CHCHO
CH3
2-环己基丙醛
9.
O CH3
CH3 C CHCH2CHO
3-甲基-4-氧代戊醛
10. CH3CHCH2COCH2CH3
134
一.用系统命名法命名下列化合物
CHO
有机化学(曾昭琼高教四版)课后习题答案12第四版-第十二章-羧酸-习题解答
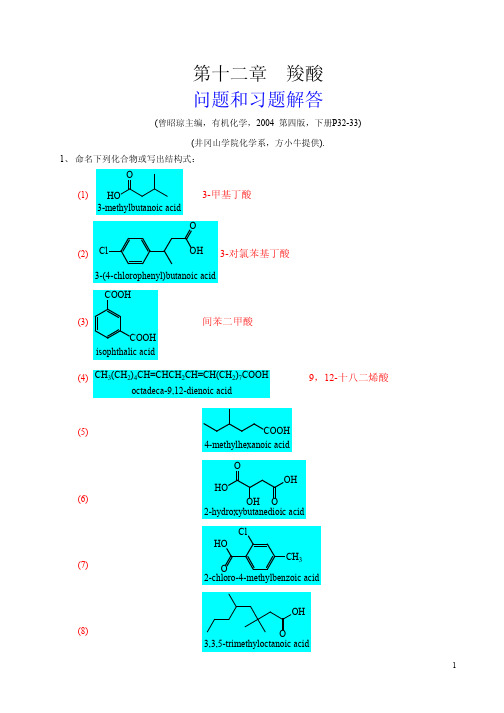
第十二章羧酸问题和习题解答(曾昭琼主编,有机化学,2004 第四版,下册P32-33)(井冈山学院化学系,方小牛提供).1、命名下列化合物或写出结构式:(1)3-甲基丁酸(2)3-对氯苯基丁酸(3) 间苯二甲酸(4) CH3(CH2)4CH=CHCH2CH=CH(CH2)7COOHoctadeca-9,12-dienoic acid9,12-十八二烯酸(5)(6)(7)(8)2、试以反应式表示乙酸与下列试剂的反应:(1) 乙醇(2) 三氯化磷(4) 氨3、区别下列各组化合物:(1)甲酸、乙酸和乙醛;(2)乙醇、乙醚和乙酸;(3)乙酸、草酸、丙二酸;(4)丙二酸、丁二酸、己二酸解:4、指出下列反应的主要产物:(1)(2)5、完成下列转变:(1) CH2=CH2→CH3CH2COOH(2) 正丙醇→2-甲基丙酸(3) 丙酸→乳酸(4) 丙酸→丙酐(5) 溴苯→苯甲酸乙酯6、化合物甲、乙、丙的分子式都是C3H6O2,甲与碳酸钠作用放出二氧化碳,乙和丙不能,但在氢氧化钠溶液中加热后可水解,在乙的水解液蒸馏出的液体有碘仿反应,试推测甲、乙、丙的结构。
解:由题意推知:甲与碳酸钠作用放出二氧化碳说明甲为丙酸CH3CH2COOH;乙的水解液蒸馏出的液体有碘仿反应,说明乙的水解产物中有乙醇,即乙为甲酸乙酯HCOOC2H5;则丙为乙酸甲酯(水解后的产物乙酸和甲醇都不能发生碘仿反应)CH3COOCH3。
7、指出下列反应中的酸和碱。
(1) 二甲醚和无水三氯化铝; (2) 氨和三氟化硼; (3) 乙炔钠和水解:按Lewis酸碱理论:凡可接受电子对的分子、离子或基团称为酸,凡可给予电子对的分子、离子或基团成为碱。
所以这三组物质中,无水三氯化铝,三氟化硼和水是Lewis酸,而二甲醚,氨和乙炔钠为Lewis碱。
8、 (1) 按照酸性降低的次序排列下列化合物:①乙炔、氨、水;②乙醇、乙酸、环戊二烯、乙炔(2) 按照碱性降低的次序排列下列离子CH3-CH3O-HC≡C-CH3O-(CH3)3CO-(CH3)2CHO-解:(1) 酸性从大到小:水> 乙炔> 氨;乙酸> 环戊二烯> 乙醇> 乙炔(2) 碱性从大到小:甲基负离子> 乙炔负离子> 甲氧基负离子叔丁氧基负离子> 异丙氧基负离子> 甲氧基负离子KJK9、分子式为C6H12O的化合物(A),氧化后得(B)C6H10O4。
有机化学课后习题答案(张凤秀主编)

第1章 习题答案1. 1. 指出下列化合物中每个碳原子的杂化轨道类型:(1)均为sp 3 杂化。
(2)(3)(4)(5)(6)2. 指出下列分子或离子哪些是路易斯酸?哪些是路易斯碱?(1)路易斯碱; (2)路易斯酸; (3)路易斯碱; (4)路易斯碱; (5)路易斯碱; (6)路易斯酸; (7)路易斯碱; (8)路易斯酸; (9)路易斯酸; (10)路易斯酸; (11)路易斯碱; (12)路易斯酸3. 指出下列化合物中官能团的名称及所属化合物的类别:(1)卤素,卤代烃; (2)醚键,醚; (3)羟基,醇; (4)醛基,醛 (5)双键,烯烃; (6)氨基,胺; (7)羧基,羧酸; (8)酯基,酯 (9)酐键,酸酐; (10)酰胺基,酰胺 (11)三键,炔 (12)羟基,酚 4. 下列化合物哪些易溶于水?哪些易溶于有机溶剂? 易溶于水的有(1)、(3)、(4)、(5)、(6);易溶于有机溶剂的有:(1)、(2)、(3)、(4)、(5)。
5求该化合物的实验式和分子式。
该化合物的实验式为:CH 2O ,分子式为C 2H 4O 2、第2章 饱和烃习题答案1.用系统命名法命名下列化合物:(1)2-甲基戊烷 (2)2,2,4-三甲基-3-乙基戊烷 (3)2,2-二甲基己烷 (4)2-甲基-5-乙基庚烷 (5)反-1-氯-2-溴环丁烷 (6)反-1,2-二甲基环戊烷 (7)9-甲基-2-乙基二环[3.3.1]壬烷 (8)3,5-二甲基螺[3.4]辛烷 2.写出下列化合物的结构式:CH 3CHCH 2CH 2CH 33CH 3CH 2CHCHCH 2CH 2CH 3CH 32H 5(1)(2)CH CH 3CH 3C CH CH 32H 5CH 3CH 3(3)(4)(5)HCH 3HC(CH 3)3(6)sp 2CH 2C 3O 232杂化3杂化sp 杂化杂化33杂化32杂化sp 332CH 2CH 3C CH (CH 2)3CH 33CH 3CH CH 2CH 3CH 3CH 3C CH CH 3CH 3(CH 2)4CH 33)2(7)(8)(9)(10)2H 53.写出分子式为C 6H 14 烷烃的各种异构体,并正确命名。
2022年高考化学大一轮复习练习:第12章 有机化学基础(选修5)-第3讲 Word版含答案

课时规范训练[单独成册]1.下列关于有机物的叙述正确的是()A.乙醇可以被氧化为乙酸,二者均能发生酯化反应B.人体内的蛋白质不断分解,最终生成水和二氧化碳排出体外C.我国居民传统膳食以糖类为主,淀粉、脂肪都是糖类物质D.由CH2===CH—COOCH3合成的聚合物为CH2CHCOOCH 3答案:A2.某有机物的结构如图,该有机物不行能具有的性质是()①可以燃烧氧化②能使酸性KMnO4溶液褪色③能跟NaOH溶液反应④能发生一个分子内或n个分子间酯化反应⑤能发生加聚反应⑥它有手性碳原子⑦能被催化氧化成醛⑧该有机物的碳原子存在sp2、sp3杂化A.①④B.④⑥C.⑤⑦D.只有⑥答案:D3.某同学用2 mL 1 mol/L的CuSO4溶液与4 mL 0.5 mol/L的NaOH溶液混合,然后加入0.5 mL 4%的HCHO溶液,加热至沸腾,未见红色沉淀,试验失败的主要缘由()A.甲醛量太少B.硫酸铜量少C.NaOH量少D.加热时间短解析:选C。
醛基和新制的氢氧化铜悬浊液反应必需在碱性条件下才能进行的,所以依据题意可知,氢氧化钠不足,试验不能成功,答案选C。
4.人们已进入网络时代。
常观看显示屏,会使人感到眼睛疲惫,甚至会对眼睛产生肯定的损害。
人眼中的视色素里含有视黄醛(见图a),作为辅基的蛋白质,而与视黄醛相像结构的维生素A(见图b)常作为保健药物。
从结构上看,维生素A与视黄醛的关系是()A.同分异构体B.同系物C.维生素A是视黄醛的还原产物D.维生素A是视黄醛的氧化产物解析:选C。
从结构上看,a催化加氢得到b,即维生素A是视黄醛的还原产物。
5.有机物A、B均为合成某种抗支气管哮喘药物的中间体,A在肯定条件下可转化为B(如图所示),下列说法正确的是()A.分子A中全部碳原子均位于同一平面B .用FeCl 3溶液可检验物质B 中是否混有AC .物质B 既能发生银镜反应,又能发生水解反应D .1 mol B 最多可与5 mol H 2发生加成反应解析:选B 。
有机化学课后习题参考答案
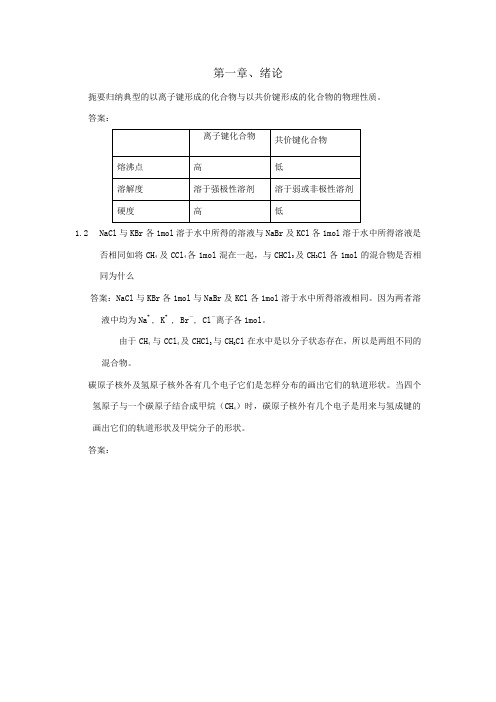
第一章、绪论扼要归纳典型的以离子键形成的化合物与以共价键形成的化合物的物理性质。
答案:1.2NaCl与KBr各1mol溶于水中所得的溶液与NaBr及KCl各1mol溶于水中所得溶液是否相同如将CH4 及CCl4各1mol混在一起,与CHCl3及CH3Cl各1mol的混合物是否相同为什么答案:NaCl与KBr各1mol与NaBr及KCl各1mol溶于水中所得溶液相同。
因为两者溶液中均为Na+ , K+ , Br-, Cl-离子各1mol。
由于CH4 与CCl4及CHCl3与CH3Cl在水中是以分子状态存在,所以是两组不同的混合物。
碳原子核外及氢原子核外各有几个电子它们是怎样分布的画出它们的轨道形状。
当四个氢原子与一个碳原子结合成甲烷(CH4)时,碳原子核外有几个电子是用来与氢成键的画出它们的轨道形状及甲烷分子的形状。
答案:C+624H CCH 4中C 中有4个电子与氢成键为SP 3杂化轨道,正四面体结构CH 4SP 3杂化2p y2p z2p x2sH写出下列化合物的Lewis 电子式。
a. C 2H 4b. CH 3Clc. NH 3d. H 2Se. HNO 3f. HCHOg. H 3PO 4h. C 2H 6i. C 2H 2 j. H 2SO 4答案:a.C C H H H HCC HH HH 或 b.H C H c.H N H Hd.H S H e.H O NOf.OC H Hg.O P O O H H Hh.H C C HHH H HO P O O H HH或i.H C C Hj.O S O HH OH H或下列各化合物哪个有偶极矩画出其方向。
a. I 2b. CH 2Cl 2c. HBrd. CHCl 3e. CH 3OHf. CH 3OCH 3 答案:b.ClClc.HBrd.He.H 3COHH 3COCH 3f.1.6 根据S 与O 的电负性差别,H 2O 与H 2S 相比,哪个有较强的偶极-偶极作用力或氢键答案:电负性 O > S , H 2O 与H 2S 相比,H 2O 有较强的偶极作用及氢键。
有机化学第二版高占先课后习题第12章答案
H N
O NH2 H N
NH2
OHH N
H2/Pd
12-12 根据下列反应,试确定A的构造式。
(1)CH3I过量 A(C8H15N) (2湿)Ag2O, △ 答案 A N H
(1)CH3I过量 (2湿)Ag2O, △
12-13 (1)利用RX和NH3合成伯胺的过程有什么副反应? (2)如何避免或减少这些副反应? (3)在这一合成中哪一种卤代烷不合适? (1)可发生二烷基化、三烷基化反应,生成R2NH和R3N; (2)使NH3大量过量,以增加 RX和NH3的碰撞机会生成RNH2; (3)叔卤代烃将发生消除反应,芳卤ArX也不易发生该反应。
CH3 (4)
2HNO3 2 H2SO4
CH3 NO2
Cl2 hv
CH2Cl NO2
(1) NaCN
CH2COOH NO2
Fe/HCl
CH2COOH NH2
(2) H3O,△
NO2
NO2
NO2
NH2
(5)
2HNO3 2 H2SO 4
NO2
((NH4)2S
NO2
NO2
NaNO 2-HCl 0~5¡ æ
pH=8~10
NH2 NaNO2-HCl
0~5℃
N N OH
(3)
参考(1)合成
OH COCH3 CH2CH3
HNO3 H2SO4
CH2CH3
Sn/HCl
CH2CH3
CH3COCl AlCl3
Zn-Hg HCl
CH2CH3
NaNO2-HCl 0~5℃ pH=8~10
OH H3CH2C
NO2
HO
NH2
NaNO2 / HCl
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第12章 杂环化合物
1.解:
(1) α-呋喃甲醛 (2) N -甲基-2-乙基吡咯 (3) 2-噻吩磺酸 (4) 3-吡啶甲酸 (5) 2-氨基嘧啶 (6) N -甲基-2-羟基咪唑 (7) 3-硝基-5-羟基吲哚 (8) 8-羟基-5-喹啉磺酸 (9) 4-乙基吡啶-N -氧化物 (10) 咪唑并[4,5-d]噁唑 (11) 咪唑并[2,1-b]噻唑 (12) 6-巯基嘌呤
N
N NH 2
CH 3N
S O 2N
(13)
N
N H 2N
(14)
(15)(16)
H
S
(20)
(19)
H
(18)
(17)N
Br
N H 3C
CH 3
Br N SO 3
N
2.解:
O
NO 2
(1)
(2)
(3)
(4)
H
N
SO 3H
S
Br
H
N COCH 3
(5)
(6)
(7)
(8)
NH 2
N
N
COOH
N
Cl OCH 3
N CH 3
H
(9)(11)
(10)
N
N C 2H 5
NH 2
3
3
3N N N
H 3C
CH 3
H
3.解:
(2)、(5)和(7)有芳香性。
4.解:
(1) 4-甲基吡啶 > 吡啶 > 吡咯 (2) 四氢吡咯 > 氨 > 苯胺 > 吡咯 5.解:
(1) 吡啶的未共用电子对在sp 2杂化轨道上,s 成分多,受到核的束缚强,不易给出电子,所以碱性弱。
六氢吡啶是仲胺,未共用电子对在sp 3杂化轨道上,s 成分少,离原子核远,受核束缚力小,易给出电子,因而碱性强。
(2) 吡啶氮原子上处于sp 2杂化轨道的未共用电子对不参与形成大π键,能结合氢质子而显碱性。
吡咯氮上的孤对电子参与了环的共轭体系,使氮上的电子云密度降低,因而难以与质子结合,碱性极弱,不能与酸形成稳定的盐。
相反,由于这种共轭作用,吡咯的N-H 键极
性增加,显示出弱酸性。
6.解:
(1) 加水,与水混溶不分层的是吡啶,不混溶分层的是苯。
(2) 加浓硫酸,不分层的是噻吩,分层的是苯。
(3) 加高锰酸钾溶液,紫红色褪去的是3-甲基吡啶,不褪色的是吡啶。
7.解:
(1) 噻吩可以在室温下与浓硫酸发生磺化反应生成噻吩磺酸而溶于浓硫酸,而苯则不易,因此可以用少许浓硫酸洗涤含少量噻吩的苯来除去噻吩。
(2) 吡啶有弱碱性,易溶于稀盐酸而甲苯不溶。
因此,可用稀盐酸水溶液洗涤来除去甲苯中的少量吡啶。
(3) 六氢吡啶为仲胺,易与苯磺酰氯发生磺酰化反应形成磺酰胺,磺酰胺沸点很高,可通过蒸馏与吡啶分离。
因此,可以通过先加入适量苯磺酰氯然后再蒸馏的方法除去吡啶中的少量六氢吡啶。
8.解:
S COCH3。
