铁、铝化学方程式(全)
初中化学方程式大全

初中化学方程式大全初中化学方程式大全化合反应1.镁在空气中燃烧:2Mg + O2 → 2MgO2.铁在氧气中燃烧:3Fe + 2O2 → Fe3O43.铝在空气中燃烧:4Al + 3O2 → 2Al2O34.氢气在空气中燃烧:2H2 + O2 → 2H2O5.红磷在空气中燃烧:4P + 5O2 → 2P2O56.硫粉在空气中燃烧:S + O2 → SO27.碳在氧气中充分燃烧:C + O2 → CO28.碳在氧气中不充分燃烧:2C + O2 → 2CO9.二氧化碳通过灼热碳层:C + CO2 → 2CO10.一氧化碳在氧气中燃烧:2CO + O2 → 2CO2分解反应11.二氧化碳和水反应(二氧化碳通入紫色石蕊试液):CO2 + H2O → H2CO3 → H2O + CO2↑12.生石灰溶于水:CaO + H2O → Ca(OH)213.无水硫酸铜作干燥剂:CuSO4 + 5H2O → CuSO4·5H2O14.钠在氯气中燃烧:2Na + Cl2 → 2NaCl置换反应15.铁和硫酸铜溶液反应:Fe + CuSO4 → FeSO4 + Cu16.锌和稀硫酸反应(实验室制氢气):Zn + H2SO4 → ZnSO4 + H2↑17.镁和稀盐酸反应:Mg + 2HCl → MgCl2 + H2↑18.氢气还原氧化铜:H2 + CuO → Cu + H2O19.木炭还原氧化铜:C + 2CuO → 2Cu + CO2↑20.水蒸气通过灼热碳层:H2O + C → CO + H2↑21.焦炭还原氧化铁:3C + 2Fe2O3 → 4Fe + 3CO2↑其他22.氢氧化钠溶液与硫酸铜溶液反应:2NaOH + CuSO4 → Cu(OH)2↓ + Na2SO423.甲烷在空气中燃烧:CH4 + 2O2 → CO2 + 2H2O24.酒精在空气中燃烧:C2H5OH + 3O2 → 2CO2 + 3H2O25.一氧化碳还原氧化铜:CO + CuO → Cu + CO226.一氧化碳还原氧化铁:3CO + Fe2O3 → 2Fe + 3CO232.通过澄清石灰水可以检验二氧化碳,反应式为:Ca(OH)2+CO2==CaCO3↓+H2O。
铁、铝化学方程式(全)

铁、铝化学方程式一、铁1.与O 2反应:3Fe+2O 2−−→−点燃Fe 3O 4 2.与Cl 2反应:2Fe+3Cl 2−−→−点燃2FeCl 3 3.与Br 2反应:2Fe+3Br 2−−→−点燃2FeBr 3 4.与I 2反应:Fe+I 2−−→−点燃FeI 2 5.与S 反应:Fe+S −→−∆FeS +Q 6.加热下与浓H 2SO 4反应:2Fe+6H 2SO 4(浓)−→−∆2Fe 2(SO 4)3+3SO 2↑+6H 2O 7.加热下与稀HNO 3反应:Fe+4HNO 3−→−∆Fe(NO 3)3+NO ↑+2H 2O 8.高温下与水蒸气反应:3Fe+4H 2O(g)−−→−高温Fe 3O 4+4H 2↑ 二、铁的氢氧化物(一)Fe(OH)28.被氧气氧化:4Fe(OH)2+O 2+2H 2O →4Fe(OH)39.制取:FeSO 4+2NaOH →Na 2SO 4+Fe(OH)2↓(二)Fe(OH)310.受热分解:2Fe(OH)3−→−∆Fe 2O 3+3H 2O 11.制取:Fe 3++OH —→Fe(OH)3↓三、铁盐和亚铁盐(一)Fe 2+12.和Cl 2反应:Fe 2++ Cl 2→2Fe 3++2Cl —13.和H 2O 2反应:2H ++2Fe 2++H 2O 2→2Fe 3++2H 2O(二)Fe 3+14.和Fe 反应:2Fe 3++Fe →3Fe 2+15.和Cu 反应:Fe 3++Cu →Cu 2++Fe 2+16.和I —反应:2Fe 3++2I —→2Fe 2++I 217.和SCN—反应:Fe3++3SCN— Fe(SCN)318.与Cl 2反应:2Al+3Cl 2−−→−点燃2AlCl 3 19.与S 反应:2Al+3S −→−∆Al 2S 3 20.与O 2反应:4Al+3O 2→2Al 2O 3(常温下生成氧化膜)4Al+3O 2−−→−点燃2Al 2O 3(纯氧中剧烈燃烧) 21.毛刷实验:2Al+3Hg(NO 3)2→2Al(NO)3+3Hg ,4Al+3O 2→2Al 2O 322.与水反应:2Al+6H 2O →2Al(OH)3+3H 2↑23.与浓HNO 3反应:Al+6HNO 3(浓)−→−∆Al(NO 3)3+3NO 2↑+3H 2O 24.与NaOH 反应:2Al+2NaOH+2H 2O →2NaAlO 2+3H 2↑25.铝热反应:2Al+Fe 2O 3−−→−高温Al 2O 3+2Fe 五、氧化铝26.与HCl 反应:Al 2O 3+6HCl →2AlCl 3+3H 2O27.与NaOH 反应:Al 2O 3+2NaOH →2NaAlO 2+H 2O(以上相应的离子方程式对应系数相同)六、氢氧化铝28.酸、碱式电离:H 2O+ AlO 2—+H +↔Al(OH)3↔Al 3++3OH —29.与HCl 反应:Al(OH)3+3HCl →AlCl 3+3H 2O30.与NaOH 反应:Al(OH)3+NaOH →NaAlO 2+2H 2O(以上相应的离子方程式对应系数相同) 31.受热分解:2Al(OH)3−→−∆Al 2O 3+3H 2O 32.制备方法:(1)Al 3+与碱(NH 3·H 2O )反应:AlCl 3+3NH 3·H 2O →Al(OH)3↓+3NH 4Cl(2)AlO 2—与酸(CO 2+H 2O )反应:(CO 2少量)2NaAlO 2+CO 2+3H 2O →Na 2CO 3+2Al(OH)3↓(CO 2过量)NaAlO 2+CO 2+2H 2O →NaHCO 3+Al(OH)3↓(3)双水解反应(Al 3++AlO 2—):AlCl 3+3NaAlO 2+6H 2O →4Al(OH)3↓+3NaCl33.明矾净水原理:Al3++3H2O↔Al(OH)3(胶体)+3H+34.AlCl3与NaOH反应:(1)向AlCl3中加NaOH:AlCl3+3NaOH→Al(OH)3↓+3NaCl(少量)Al(OH)3+NaOH→NaAlO2+2H2O(过量)总反应:AlCl3+4NaOH→NaAlO2+2H2O+3NaCl(2)向NaOH中加AlCl3:AlCl3+4NaOH→NaAlO2+2H2O+3NaCl(少量)AlCl3+3NaAlO2+6H2O→4Al(OH)3↓+3NaCl(过量)八、偏铝酸盐35.偏铝酸盐的水解:AlO2—+2H2O→Al(OH)3 +OH—36.与HCl反应:(1)向NaAlO2加HCl:NaAlO2+HCl+H2O→Al(OH)3↓+NaCl(少量)Al(OH)3+3HCl→AlCl3+3H2O(过量)总反应:NaAlO2+4HCl→AlCl3+2H2O+NaCl(2)向HCl加NaAlO2:NaAlO2+4HCl→AlCl3+2H2O+NaCl(少量)AlCl3+3NaAlO2+6H2O→Al(OH)3↓+3NaCl(过量)37.总结:Al3+↔碱强酸Al(OH)3↔强碱酸AlO2—如有侵权请联系告知删除,感谢你们的配合!。
初中常见的化学方程式(全)(1)

初中常见的化学方程式汇总一、化合反应: A+B →AB1. 镁在空气中燃烧: 2Mg + O 2 点燃====== 2MgO(白) (现象:2. 铁在氧气中燃烧: 3Fe + 2O 2 点燃====== Fe 3O 4(黑)3. 铝在空气中燃烧: 4Al + 3O 2 点燃====== 2Al 2O 3(白)4. 氢气中空气中燃烧: 2H 2 + O 2 点燃====== 2H 2O5. 红磷在空气中燃烧: 4P + 5O 2 点燃====== 2P 2O 5(白)6. 硫粉在空气中燃烧: S + O 2 点燃====== SO 27. 碳在氧气中充分燃烧: C + O 2 点燃====== CO 28. 碳在氧气中不充分燃烧: 2C + O 2 点燃====== 2CO9. 铜在空气中受热: 2Cu (紫红) + O 2 加热====== 2CuO(黑色)10. 一氧化碳在氧气中燃烧:2CO + O 2 点燃====== 2CO 211. 二氧化碳溶解于水: CO 2 + H 2O === H 2CO 312. 二氧化硫溶于水: SO 2 + H 2O ==== H 2SO 3(亚硫酸)13. 三氧化硫溶于水: SO 3 + H 2O ==== H 2SO 4(硫酸)14. 生石灰溶于水: CaO + H 2O ==== Ca(OH)215. 氧化钠溶于水: Na 2O + H 2O ==== 2NaOH16. 无水硫酸铜作干燥剂: CuSO 4 (白)+ 5H 2O ==== CuSO 4·5H 2O(蓝)17. 二氧化碳通过炽热的炭层:CO 2 + C 高温====== 2CO 二.几个分解反应:AB →A+B18. 水在直流电的作用下分解: 2H 2O 通电====== 2H 2↑+ O 2 ↑19. 双氧水分解: 2H 2O 2 2MnO ====== 2H 2O+ O 2 ↑20. 加热氯酸钾(有二氧化锰):2KClO 3 (白)2O M n 加热====== 2KCl(白) + 3O 2 ↑ 21. 加热高锰酸钾: 2KMnO 4 (紫黑)加热====== K 2MnO 4 + MnO 2 (黑)+ O 2↑22. 碳酸不稳定而分解: H 2CO 3 加热====== H 2O + CO 2↑23. CaCO 3 高温====== CaO + CO 2↑24. Cu(OH)2 加热====== CuO + H 2O25. 2Fe(OH)3 加热====== Fe 2O 3 + 3H 2O26. 硫酸铜晶体受热分解: CuSO 4·5H 2O 加热====== CuSO 4 + 5H 2O 三.置换反应:A+BC →AC+B(还原剂C 、H 2与金属氧化物的反应)27. 氢气还原氧化铜:H2 + CuO加热======Cu + H2O28. 氢气还原氧化铁:3H2+ Fe2O3(红)加热======2Fe(粉末、黑) + 3 H2O29. 木炭还原氧化铜:C+ 2CuO高温======2Cu + CO2↑30. 焦炭还原氧化铁:3C+ 2Fe2O3高温======4Fe + 3CO2↑31.高温32. 244233. 锌和稀盐酸反应:Zn + 2HCl === ZnCl2 + H2↑34. 铁和稀硫酸反应:Fe + H2SO4 === FeSO4(浅绿色) + H2↑(FeSO4--硫酸亚铁)35. 铁和稀盐酸反应:Fe + 2HCl === FeCl2(浅绿色) + H2↑(FeCl2--氯化亚铁)36. 镁和稀盐酸反应:Mg + 2HCl === MgCl2 + H2↑37. 镁和稀硫酸反应:Mg + H2SO4 === MgSO4 + H2↑38. 铝和稀硫酸反应:2Al + 3H2SO4 === Al2(SO4)3 + 3H2↑39. 铝和稀盐酸反应:2Al + 6HCl === 2AlCl()40. 铁和硫酸铜溶液反应:Fe + CuSO4(蓝441. 锌和硫酸铜溶液反应:Zn + CuSO4 ===== ZnSO4 + Cu42. 铜和硝酸汞溶液反应:Cu + Hg(NO3)2 === Cu(NO3)2 + Hg43. 铜和硝酸银溶液反应:Cu +2 AgNO3 ==== Cu(NO3)2 +2 Ag→(44. 233245. 氧化铁和稀硫酸反应:Fe2O3 + 3H2SO4 === Fe2(SO4)3(黄色) + 3H2O46. 氧化铜和稀盐酸反应:CuO + 2HCl ====== CuCl2 + H2O47. 氧化铜和稀硫酸反应:CuO + H2SO4 ===== CuSO4 + H2O48. 氧化镁和稀硫酸反应:MgO + H2SO4 ===== MgSO4 + H2O49.()50. 251. 盐酸和氢氧化钾反应:HCl + KOH ===== KCl +H2O52. 盐酸和氢氧化铜反应:2HCl + Cu(OH)2 ==== CuCl2 + 2H2O53. 盐酸和氢氧化钙反应:2HCl + Ca(OH)2 ==== CaCl2 + 2H2O54. 盐酸和氢氧化铁反应:3HCl + Fe(OH)3 ==== FeCl3 (黄色)+ 3H2O55. 氢氧化铝药物治疗胃酸过多:3HCl + Al(OH)3 ==== AlCl3 + 3H2O56. 硫酸和烧碱反应:H2SO4 + 2NaOH ==== Na2SO4 + 2H2O57. 硫酸和氢氧化钾反应:H2SO4 + 2KOH ===== K2SO4 + 2H2O58. 硫酸和氢氧化铜反应:H2SO4 + Cu(OH)2 ===== CuSO4 + 2H2O59. 硫酸和氢氧化铁反应:3H2SO4 + 2Fe(OH)3==== Fe2(SO4)3 + 6H2O60.()61. 322262. 碳酸钠与稀盐酸反应:2HCl +Na2CO3=== 2NaCl + H2O + CO2↑63. 碳酸镁与稀盐酸反应:2HCl +MgCO3=== MgCl2 + H2O + CO2↑64. 盐酸和硝酸银溶液反应:HCl + AgNO3 === HNO3+AgCl↓ (白色、不溶于稀硝酸)65. 硫酸和碳酸钠反应:H2SO4 +Na2CO3 === Na2SO4 + H2O + CO2↑66. 硫酸和氯化钡溶液反应:H2SO4 + BaCl2 == 2HCl+BaSO4↓ (白色、不溶于稀硝酸) (碱+盐()67. 424268. 氢氧化钠与氯化铁:3NaOH + FeCl3 ==== 3NaCl +Fe(OH)3↓(红褐色沉淀)69. 氢氧化钠与氯化镁:2NaOH + MgCl2 ==== Mg(OH)2↓(白) + 2NaCl70. 氢氧化钠与氯化铜:2NaOH + CuCl2 ==== Cu(OH)2↓(蓝)+ 2NaCl71. 氢氧化钙与碳酸钠:Ca(OH)2 + Na2CO3 === CaCO3↓(白)+ 2NaOH72. 氢氧化钠与氯化铵:NaOH + NH4Cl 微热NaCl + NH3↑ +H2O73. 氢氧化钙与氯化铵:Ca(OH)2 + 2NH4微热CaCl 2+ 2NH3↑ + 2H2O74. 氢氧化钾与硫酸铵:2KOH + (NH4)2SO微热K2SO4 + 2NH3↑ + 2H2O(()75. 3376. 硫酸钠和氯化钡:Na2SO4 + BaCl2 ==== BaSO4↓ + 2NaCl76. 碳酸钠和氯化钙:Na2CO3 + CaCl2 ==== CaCO3↓+ 2NaCl五.其它反应:77. 甲烷在空气中燃烧:CH4 + 2O2点燃======CO2 + 2H2O78. 酒精(乙醇)在空气中燃烧:C2H5OH + 3O2点燃======2CO2 + 3H2O79. 甲醇在空气中燃烧:2CH3OH + 3O2点燃======2CO2 + 4H2O80. 一氧化碳还原氧化铜:CO+ CuO加热======Cu + CO281. 一氧化碳还原氧化铁:3CO+ Fe2O3高温======2Fe + 3CO282. 一氧化碳还原四氧化三铁:4CO+ Fe3O4高温======3Fe + 4CO283. 3CO+ WO 加热2()83. 223 + H2O84. 苛性钠吸收二氧化硫气体:2NaOH + SO2 ===== Na2SO3 + H2O85. 苛性钠吸收三氧化硫气体:2NaOH + SO3 ===== Na2SO4 + H2O86. 熟石灰放在空气中变质:Ca(OH)2 + CO2 ==== CaCO3↓+ H2O87. 消石灰吸收二氧化硫:Ca(OH)2 + SO2 ==== CaSO3 + H2O。
初中常见化学式及化学方程式大全
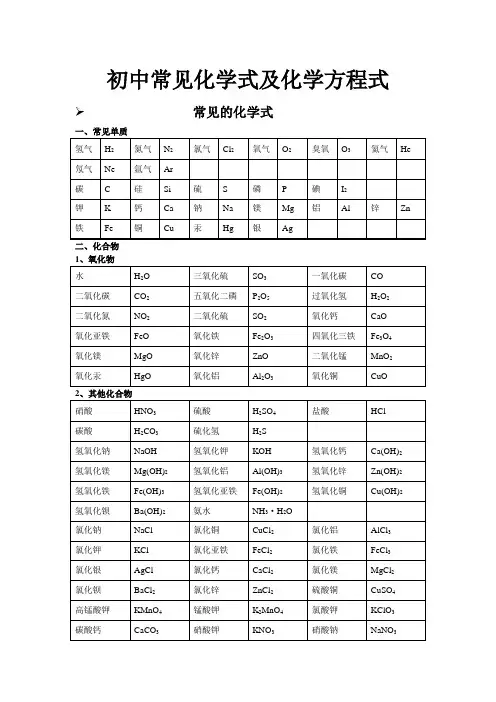
初中常见化学式及化学方程式 常见的化学式一、常见单质二、化合物初中化学方程式全(已配平).一、化合反应1、镁在空气中燃烧:2Mg+ O2点燃 2MgO2、铁在氧气中燃烧:3Fe +2O2点燃 Fe3O43、铝在空气中燃烧:4Al+ 3O2点燃 2Al2O34、氢气在空气中燃烧:2H2 +O2点燃 2H2O5、红磷在空气中燃烧:4P +5O2点燃 2P2O56、硫粉在空气中燃烧: S+ O2点燃 SO27、碳在氧气中充分燃烧:C +O2 点燃 CO28、碳在氧气中不充分燃烧:2C +O2点燃 2CO9、二氧化碳通过灼热碳层: C +CO2高温 2CO10、一氧化碳在氧气中燃烧:2CO +O2 点燃 2CO211、二氧化碳和水反应(二氧化碳通入紫色石蕊试液):CO2+H2O === H2CO312、生石灰溶于水:CaO+ H2O === Ca(OH)213、无水硫酸铜作干燥剂:CuSO4 +5H2O ==== CuSO4·5H2O14、钠在氯气中燃烧:2Na+ Cl点燃 2NaCl二、分解反应15、实验室用双氧水制氧气:2H2O2 MnO2 2H2O +O2↑16、加热高锰酸钾:2KMnO4 加热 K2MnO4 + MnO2 +O2↑17、水在直流电的作用下分解:2H2O 通电 2H2↑+O2↑18、碳酸化学物理学报不稳定而分解:H2CO3 === H2O +CO2↑19、高温煅烧石灰石(二氧化碳工业制法):CaCO3高温 CaO+ CO2↑三、置换反应20、铁和硫酸铜溶液反应:Fe+ CuSO4 == FeSO4 +Cu21、锌和稀硫酸反应(实验室制氢气):Zn+ H2SO4 == ZnSO4+H2↑22、镁和稀盐酸反应:Mg +2HCl === MgCl2 +H2↑23、氢气还原氧化铜:H2 +CuO 加热 Cu +H2O24、木炭还原氧化铜:C+ 2CuO 高温 2Cu +CO2↑25、甲烷在空气中燃烧:CH4 +2O2 点燃 CO2+2H2O26、水蒸气通过灼热碳层:H2O +C 高温 H2 +CO27、焦炭还原氧化铁:3C +2Fe2O3高温 4Fe +3CO2↑其他28、氢氧化钠溶液与硫酸铜溶液反应:2NaOH+ CuSO4 == Cu(OH)2↓+ Na2SO429、甲烷在空气中燃烧:CH4 +2O2点燃 CO2 +2H2O30、酒精在空气中燃烧:C2H5OH+ 3O2点燃 2CO2 +3H2O31、一氧化碳还原氧化铜:CO +CuO 加热 Cu+ CO232、一氧化碳还原氧化铁:3CO+ Fe2O3高温 2Fe+ 3CO233、二氧化碳通过澄清石灰水(检验二氧化碳):Ca(OH)2+ CO2 ==== CaCO3 ↓+ H2O34、氢氧化钠和二氧化碳反应(除去二氧化碳):2NaOH+ CO2 ==== Na2CO3 +H2O35、石灰石(或小学音乐教案大理石)与稀盐酸反应(二氧化碳的实验室制法):CaCO3 +2HCl === CaCl2 +H2O +CO2↑36、碳酸钠与浓盐酸反应(泡沫灭火器的原理): Na2CO3+ 2HCl === 2NaCl +H2O +CO2↑一.物质与氧气的反应:(1)单质与氧气的反应:1. 镁在空气中燃烧:2Mg+ O2点燃 2MgO2. 铁在氧气中燃烧:3Fe+ 2O2点燃 Fe3O43. 铜在空气中受热:2Cu+ O2加热 2CuO4. 铝在空气中燃烧:4Al +3O2 点燃 2Al2O35. 氢气中空气中燃烧:2H2 +O2点燃 2H2O6. 红磷在空气中燃烧:4P+ 5O2点燃 2P2O57. 硫粉在空气中燃烧: S +O2 点燃 SO28. 碳在氧气中充分燃烧:C+ O2点燃 CO29. 碳在氧气中不充分燃烧:2C+ O2点燃 2CO(2)化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO+ O2点燃 2CO211. 甲烷在空气中燃烧:CH4 +2O2点燃 CO2 2H2O12. 酒精在空气中燃烧:C2H5OH +3O2点燃 2CO2+3H2O二.几个分解反应:13. 水在直流电的作用下分新概念英语第一册解:2H2O 通电 2H2↑+ O2↑14. 加热碱式碳酸铜:Cu2(OH)2CO3加热 2CuO +H2O +CO2↑15. 加热氯酸钾(有少量的二氧化锰):2KClO3 ==== 2KCl+ 3O2↑16. 加热高锰酸钾:2KMnO4 加热 K2MnO4 +MnO2 +O2↑17. 碳酸不稳定而分解:H2CO3 === H2O +CO2↑18. 高温煅烧石灰石:CaCO3 高温 CaO +CO2↑三.几个氧化还原反应:19. 氢气还原氧化铜:H2+ CuO 加热 Cu+ H2O20. 木炭还原氧化铜:C+ 2CuO 高温 2Cu +CO2↑2 初三化学方程式大合集21. 焦炭还原氧化铁:3C+ 2Fe2O3 高温 4Fe+ 3CO2↑22. 焦炭还原四氧化三铁:2C +Fe3O4高温 3Fe+ 2CO2↑23. 一氧化碳还原氧化铜:CO +CuO 加热 Cu+ CO224. 一氧化碳还原氧化铁:3CO+ Fe2O3高温 2Fe +3CO225. 一氧化碳还原四氧化三铁:4CO +Fe3O4高温 3Fe+ 4CO2四.单质、氧化物、酸、碱、盐的相互关系(1)金属单质+酸 -------- 盐+氢气(置换反应)26. 锌和稀硫酸Zn+ H2SO4 = ZnSO4+ H2↑27. 铁和稀硫酸Fe +H2SO4 = FeSO4+ H2↑28. 镁和稀硫酸Mg +H2SO4 = MgSO4 +H2↑29. 铝和稀硫酸2Al+ 3H2SO4 = Al2(SO4)3 +3H2↑30. 锌和稀盐酸Zn +2HCl === ZnCl2+ H2↑31. 铁和稀盐酸Fe+ 2HCl === FeCl2+ H2↑32. 镁和语文教案格式稀盐酸Mg 2HCl === MgCl2+ H2↑33. 铝和稀盐酸2Al+ 6HCl == 2AlCl3 +3H2↑(2)金属单质+盐(溶液) ------- 另一种金属+另一种盐34. 铁和硫酸铜溶液反应:Fe+ CuSO4 === FeSO4+ Cu35. 锌和硫酸铜溶液反应:Zn+ CuSO4 === ZnSO4+ Cu36. 铜和硝酸汞溶液反应:Cu +Hg(NO3)2 === Cu(NO3)2 +Hg (3)碱性氧化物+酸 -------- 盐+水37. 氧化铁和稀盐酸反应:Fe2O3+ 6HCl === 2FeCl3+ 3H2O38. 氧化铁和稀硫酸反应:Fe2O3 +3H2SO4 === Fe2(SO4)3+ 3H2O39. 氧化铜和稀盐酸反应:CuO +2HCl ==== CuCl2 +H2O40. 氧化铜和稀硫酸反应:CuO +H2SO4 ==== CuSO4+ H2O41. 氧化镁和稀硫酸反应:MgO+ H2SO4 ==== MgSO4+ H2O42. 氧化钙和稀盐酸反应:CaO +2HCl ==== CaCl2 +H2O (4)酸性氧化物+碱 -------- 盐+水43.苛性钠暴露在空气中变质:2NaOH +CO2 ==== Na2CO3+H2O 44.苛性钠吸收二氧化硫气体:2NaOH +SO2 ==== Na2SO3 +H2O 45.苛性钠吸收三氧化硫气体:2NaOH+ SO3 ==== Na2SO4+ H2O46.消石灰放在空气中变质:Ca(OH)2+ CO2 ==== CaCO3 ↓+ H2O 47. 消石灰吸收二氧化硫:Ca(OH)2 +SO2 ==== CaSO3↓+H2O(5)酸+碱 -------- 盐+水48.盐酸和烧碱起反应:HCl+ NaOH ==== NaCl+ H2O49. 盐酸和氢氧化钾反应:HCl+ KOH ==== KCl+H2O50.盐酸和氢氧化初中家长会课件铜反应:2HCl+ Cu(OH)2==== CuCl2 +2H2O51. 盐酸和氢氧化钙反应:2HCl+ Ca(OH)2 ==== CaCl2 +2H2O52. 盐酸和氢氧化铁反应:3HCl+ Fe(OH)3 ==== FeCl3 +3H2O53.氢氧化铝药物治疗胃酸过多:3HCl +Al(OH)3 ==== AlCl3 +3H2O54.硫酸和烧碱反应:H2SO4 +2NaOH ==== Na2SO4 +2H2O55.硫酸和氢氧化钾反应:H2SO4 +2KOH ==== K2SO4 +2H2O56.硫酸和氢氧化铜反应:H2SO4 +Cu(OH)2 ==== CuSO4 +2H2O57. 硫酸和氢氧化铁反应:3H2SO4 +2Fe(OH)3==== Fe2(SO4)3+ 6H2O58. 硝酸和烧碱反应:HNO3+ NaOH ==== NaNO3 +H2O(6)酸+盐 -------- 另一种酸+另一种盐59.大理石与稀盐酸反应:CaCO3 +2HCl === CaCl2 H2O +CO2↑ 60.碳酸钠与稀盐酸反应: Na2CO3 +2HCl === 2NaCl +H2O+ CO2↑ 61.碳酸镁与稀盐酸反应: MgCO3 +2HCl === MgCl2 +H2O+CO2↑ 62.盐酸和硝酸银溶液反应:HCl+ AgNO3=== AgCl↓+ HNO363.硫酸和碳酸钠反应:Na2CO3 +H2SO4 === Na2SO4 +H2O +CO2↑64.硫酸和氯化钡溶液反应:H2S O4 +BaCl2 ==== BaSO4↓+ 2HCl(7)碱+盐 -------- 另一种碱+另一种盐65.氢氧化钠与硫酸铜:2NaOH CuSO4 ==== Cu(OH)2↓ Na2SO466.氢氧化钠与氯化铁:3NaOH FeCl3 ==== Fe(OH)3↓ 3NaCl 67.氢氧化钠与氯化镁:2NaOH MgCl2 ==== Mg(OH)2↓ 2NaCl68. 氢氧化钠与氯化铜:2NaOH CuCl2 ==== Cu(OH)2↓ 2NaCl69. 氢氧化钙与碳酸钠:Ca(OH)2 Na2CO3 === CaCO3↓ 2NaOH(8)盐+盐 ----- 两种新盐70.氯化钠溶液新概念英语第二册和硝酸银溶液:NaCl +AgNO3 ==== AgCl↓+ NaNO371.硫酸钠和氯化钡:Na2SO4+ BaCl2 ==== BaSO4↓+ 2NaCl五.其它反应:72.二氧化碳溶解于水:CO2+ H2O === H2CO373.生石灰溶于水:CaO+ H2O === Ca(OH)274.氧化钠溶于水:Na2O +H2O ==== 2NaOH75.三氧化硫溶于水:SO3 +H2O ==== H2SO476.硫酸铜晶体受热分解:CuSO4·5H2O 加热 CuSO4 5H2O77.无水硫酸铜作干燥剂:CuSO4+ 5H2O ==== CuSO4·5H2化学方程式反应现象应用2Mg+ O2点燃或Δ2MgO 剧烈燃烧.耀眼白光.生成白色固体.放热.产生大量白烟白色信号弹2Hg +O点燃或Δ2HgO 银白液体、生成红色固体拉瓦锡实验2Cu+ O点燃或Δ2CuO 红色金属变为黑色固体4Al+ 3O点燃或Δ2Al2O3银白金属变为白色固体3Fe+ 2O点燃Fe3O4 剧烈燃烧、火星四射、生成黑色固体、放热 4Fe +3O2高温2Fe2O3C+ O2点燃CO2剧烈燃烧、白光、放热、使石灰水变浑浊S +O2点燃SO2剧大学英语四级烈燃烧、放热、刺激味气体、空气中淡蓝色火焰.氧气中蓝紫色火焰2H2 O2点燃2H2O 淡蓝火焰、放热、生成使无水CuSO4变蓝的液体(水)高能燃料4P +5O2 点燃2P2O5剧烈燃烧、大量白烟、放热、生成白色固体证明空气中氧气含量CH4+2O点燃2H2O+ CO2蓝色火焰、放热、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)甲烷和天然气的燃烧2C2H2+ 5O2点燃2H2O +4CO2 蓝色火焰、放热、黑烟、生成使石灰水变浑浊气体和使无水CuSO4变蓝的液体(水)氧炔焰、焊接切割金属2KClO3MnO2、Δ2KCl +3O2↑ 生成使带火星的木条复燃的气体实验室制备氧气2KMnO4Δ K2MnO4 MnO2 +O2↑ 紫色变为黑色、生成使带火星木条复燃的气体实验室制备氧论文气2HgOΔ2Hg+ O2↑ 红色变为银白、生成使带火星木条复燃的气体拉瓦锡实验2H2O通电2H2↑+ O2↑ 水通电分解为氢气和氧气电解水Cu2(OH)2CO3Δ2CuO +H2O+ CO2↑ 绿色变黑色、试管壁有液体、使石灰水变浑浊气体铜绿加热NH4HCO3ΔNH3↑+ H2O+ CO2↑ 白色固体消失、管壁有液体、使石灰水变浑浊气体碳酸氢铵长期暴露空气中会消失Zn+ H2SO4=ZnSO4 +H2↑ 有大量气泡产生、锌粒逐渐溶解实验室制备氢气Fe +H2SO4=FeSO4 +H2↑ 有大量气泡产生、金属颗粒逐渐溶解Mg +H2SO4 =MgSO4 +H2↑ 有大量气泡产生、金属颗粒逐渐溶解2Al+ 3H2SO4=Al2(SO4)3+ 3H2↑ 有大量气泡产生、金属颗粒逐渐溶解Fe2O3+3H2Δ 2Fe +3H2O 红色逐渐变为银白色、试管壁有液体冶炼金属、利用氢气的还原性Fe3O4 +4H2 Δ3Fe+ 4H2O 黑色逐渐变为银白色英语翻译、试管壁有液体冶炼金属、利用氢气的还原性WO3 +3H2Δ W +3H2O 冶炼金属钨、利用氢气的还原性MoO3 +3H2ΔMo +3H2O 冶炼金属钼、利用氢气的还原性2Na+ Cl2Δ或点燃2NaCl 剧烈燃烧、黄色火焰离子化合物的形成、H2+Cl2点燃或光照 2HCl 点燃苍白色火焰、瓶口白雾共价化合物的形成、制备盐酸CuSO4 +2NaOH=Cu(OH)2↓+ Na2SO4蓝色沉淀生成、上部为澄清溶液质量守恒定律实验2C +O点燃2CO 煤炉中常见反应、空气污染物之一、煤气中毒原因2CO +O点燃2CO2蓝色火焰煤气燃烧C+ CuO 高温2Cu+ CO2↑ 黑色逐渐变为红色、产生使澄清石灰水变浑浊的气体冶炼金属2Fe2O3+ 3C 高温4Fe+ 3CO2↑ 冶炼金属Fe3O4 +2C高温3Fe+ 2CO2↑ 冶炼金属C+ CO2 高温2COCO2+H2O = H2CO3碳酸使石蕊变红证明碳酸的酸性小学三语文教学论文H2CO3 ΔCO2↑+ H2O 石蕊红色褪去Ca(OH)2 +CO2= CaCO3↓+ H2O 澄清石灰水变浑浊应用CO2检验和石灰浆粉刷墙壁CaCO3 +H2O+ CO2 = Ca(HCO3)2 白色沉淀逐渐溶解溶洞的形成,石头的风化Ca(HCO3)2Δ CaCO3↓+ H2O +CO2↑ 白色沉淀、产生使澄清石灰水变浑浊的气体水垢形成.钟乳石的形成2NaHCO3ΔNa2CO3+ H2O +CO2↑ 产生使澄清石灰水变浑浊的气体小苏打蒸馒头CaCO3 高温 CaO +CO2↑ 工业制备二氧化碳和生石灰CaCO3 +2HCl=CaCl2+ H2O +CO2↑ 固体逐渐溶解、有使澄清石灰水变浑浊的气体实验室制备二氧化碳、除水垢初中化学方程式汇总一、氧气的性质:(1)单质与氧气的反应:(化合反应)1. 镁在空气中燃烧:2Mg+ O2点燃 2MgO2. 铁在氧气中燃烧:3Fe+ 2O2点燃 Fe3O43. 铜在空气中受热:2Cu+ O2加热 2CuO4. 铝在空气中燃烧:4Al +3O2 点燃2Al2O35. 氢气中空气中燃烧:2H2 +O2 点燃 2H2O6. 红磷在空气中燃烧(研究空气组成的实验):4P +5O2点燃 2P2O57. 硫粉在空气中燃烧: S +O2 点燃 SO28. 碳在氧气中充分燃烧:C +O2点燃 CO29. 碳在氧气中不充分燃烧:2C +O2点燃 2CO(2)化合物与氧气的反应:10. 一氧化碳在氧气中燃烧:2CO+O2点燃 2CO211. 甲烷在空气中燃烧:CH4 +2O2点燃 CO2 +2H2O12. 酒精在空气中燃烧:C2H5OH +3O2点燃 2CO2 +3H2O(3)氧气的来源:13.玻义耳研究空气的成分实验 2HgO 加热 Hg +O2 ↑14.加热高锰酸钾:2KMnO4加热 K2MnO4+ MnO2 +O2↑(实验室制氧气原理1)15.过氧化氢在二氧化锰作催化剂条件下分解反应: H2O2MnO22H2O+ O2↑(实验室制氧气原理2)二、自然界中的水:16.水在直流电的作用下分解(研究水的组成实验):2H2通电2H2↑+O2 ↑17.生石灰溶于水英语六级作文:CaO +H2O == Ca(OH)218.二氧化碳可溶于水: H2O+CO2==H2CO3三、质量守恒定律:19.镁在空气中燃烧:2Mg+ O2点燃 2MgO20.铁和硫酸铜溶液反应:Fe+ CuSO4 === FeSO4+ Cu21.氢气还原氧化铜:H2 +CuO 加热 Cu +H2O22. 镁还原氧化铜:Mg+ CuO 加热 Cu +MgO四、碳和碳的氧化物:(1)碳的化学性质23. 碳在氧气中充分燃烧:C + O2点燃 CO224.木炭还原氧化铜:C + 2CuO 高温 2Cu+ CO2↑25.焦炭还原氧化铁:3C + 2Fe2O3高温 4Fe + 3CO2↑(2)煤炉中发生的三个反应:(几个化合反应)26.煤炉的底层:C +O2 点燃 CO227.煤炉的中层:CO2+ C 高温 2CO28.煤炉的上部蓝色火焰的产生:2CO +O2点燃 2CO2(3)二氧化碳的制法与性质:29.大理石与稀盐酸反应(实验室制二氧化碳):CaCO3+ 2HCl == CaCl2+ H2O +CO2↑30.碳酸不稳定而分解:H2CO3 == H2O +CO2↑31.二氧化碳可溶于水: H2O +CO2== H2CO332.高温煅烧石灰石(工业制二氧化碳):CaCO3高温 CaO+ CO2↑ 33.石灰水与中学历史教学园地二氧化碳反应(鉴别二氧化碳):Ca(OH)2 +CO2 === CaCO3↓+H2O(4)一氧化碳的性质:34.一氧化碳还原氧化铜:CO+ CuO 加热 Cu +CO2 35.一氧化碳的可燃性:2CO +O2点燃 2CO2其它反应:36.碳酸钠与稀盐酸反应(灭火器的原理):Na2CO3 2HCl == 2NaCl+ H2O +CO2↑五、燃料及其利用:37.甲烷在空气中燃烧:CH4 +2O2点燃 CO2 +2H2O 38.酒精在空气中燃烧:C2H5OH +3O2 点燃 2CO2 +3H2O 39.氢气中空气中燃烧:2H2+ O2点燃 2H2O六、金属(1)金属与氧气反应:40.镁在空气中燃烧:2Mg+ O2点燃 2MgO41.铁在氧气中燃烧:3Fe +2O2点燃 Fe3O442. 铜在空气中受热:2Cu +O2加热 2CuO43. 铝在空气中形成氧化膜:4Al+ 3O2 = 2Al2O3(2)金属单质酸 -------- 盐氢气(置换反应)44. 锌和稀硫酸Zn+ H2SO4 = ZnSO4+ H2↑45. 铁和稀硫酸Fe +H2SO4 = FeSO4 +H2↑46. 镁和稀硫酸Mg +H2SO4 = MgSO4+ H2↑47. 铝和稀硫酸2Al+ 3H2SO4 = Al2(SO4)3 +3H2↑48. 锌和稀盐酸Zn+ 2HCl == ZnCl2+ H2↑49. 铁和稀盐酸Fe +2HCl == FeCl2 +H2↑50. 镁和稀盐酸Mg +2HCl == MgCl2+ H2↑51.铝和稀盐酸2Al+ 6HCl == 2AlCl3 +3H2↑(3)金属单质盐怎样学好高中物理(溶液) ------- 新金属新盐52. 铁和硫酸铜溶液反应:Fe +CuSO4 == FeSO4 +Cu53. 锌和硫酸铜溶液反应:Zn +CuSO4 ==ZnSO4 +Cu54. 铜和硝酸汞溶液反应:Cu +Hg(NO3)2 == Cu(NO3)2 +Hg(3)金属铁的治炼原理:55.3CO +2Fe2O3 高温 4Fe +3CO2↑七、酸、碱、盐1、酸的化学性质(1)酸金属 -------- 盐氢气(见上)(2)酸金属氧化物-------- 盐水56. 氧化铁和稀盐酸反应:Fe2O3 +6HCl ==2FeCl3 +3H2O57. 氧化铁和稀硫酸反应:Fe2O3 +3H2SO4 == Fe2(SO4)3 +3H2O58. 氧化铜和稀盐酸反应:CuO +2HCl ==CuCl2 +H2O59. 氧化铜和稀硫酸反应:CuO+ H2SO4 == CuSO4+ H2O(3)酸碱 -------- 盐水(中和反应)60.盐酸和烧碱起反应:HCl +NaOH == NaCl+H2O61. 盐酸和氢氧化钙反应:2HCl+ Ca(OH)2 == CaCl2+2H2O62. 氢氧化铝药物治疗胃酸过多:3HCl +Al(OH)3 == AlCl3 +3H2O63. 硫酸和烧碱反应:H2SO4+ 2NaOH == Na2SO4 +2H2O(4)酸盐 -------- 另一种酸另一种盐64.大理石与稀盐酸反应:CaCO3+2HCl == CaCl2 +H2O+ CO2↑ 65.碳酸钠与稀盐酸反应: Na2CO3 +2HCl == 2NaCl+ H2O+ CO2↑ 66.碳酸氢钠与稀盐酸反应:NaHCO3 +HCl== NaCl+H2O+ CO2↑ 67. 硫酸和氯化钡溶液反应:H2SO4 +BaCl2 == BaSO4↓+2HCl 2、碱的幼儿园小班音乐教案化学性质(1)碱非金属氧化物 -------- 盐水68.苛性钠暴露在空气中变质:2NaOH+CO2 == Na2CO3+ H2O 69.苛性钠吸收二氧化硫气体:2NaOH +SO2 == Na2SO3 +H2O 70.苛性钠吸收三氧化硫气体:2NaOH+ SO3 == Na2SO4 +H2O 71.消石灰放在空气中变质:Ca(OH)2+ CO2 == CaCO3↓+H2O 72. 消石灰吸收二氧化硫:Ca(OH)2 +SO2 == CaSO3↓+ H2O (2)碱酸-------- 盐水(中和反应,方程式见上)(3)碱盐 -------- 另一种碱另一种盐73. 氢氧化钙与碳酸钠:Ca(OH)2 +Na2CO3 == CaCO3↓+ 2NaOH 3、盐的化学性质(1)盐(溶液)金属单质------- 另一种金属另一种盐74. 铁和硫酸铜溶液反应:Fe+ CuSO4 == FeSO4 +Cu(2)盐酸-------- 另一种酸另一种盐75.碳酸钠与稀盐酸反应: Na2CO3 +2HCl == 2NaCl +H2O+ CO2↑ 碳酸氢钠与稀盐酸反应:NaHCO3 +HCl== NaCl+ H2O +CO2↑(3)盐 碱 -------- 另一种碱 另一种盐76. 氢氧化钙与碳酸钠:Ca(OH)2 +Na 2CO 3 == CaCO 3↓+ 2NaOH (4)盐 盐 ----- 两种新盐77.氯化钠溶液和硝酸银溶液:NaCl +AgNO 3 == AgCl↓+NaNO 3 78.硫酸钠和氯化钡:Na 2SO 4 +BaCl 2 == BaSO4↓+2NaCl一、其他反应类型1、二氧化碳通入澄清石灰水中:CO 2 + Ca(OH)2 == CaCO 3↓+ H 2O2、氢氧化钠在空气中变质:CO 2+ 2NaOH = Na 2CO 3 + H 2O3、氢氧化钠溶液吸收二氧化硫:SO 2 + 2NaOH ==Na 2SO 3+ H 2O4、一氧化碳还原氧化铜:CO + CuO Cu + CO 25、酒精燃烧:C 2H 5OH + 3O 2 2CO 2 + 3H 2O6、甲烷燃烧:CH 4 + 2O 2 CO 2 + 2H 2O△点燃 点燃。
初三总复习初三化学方程式大全

初三总复习初三化学方程式大全1、镁在空气中燃烧:2Mg+O2 2MgO2、铁在氧气中燃烧:3Fe+2O2 Fe3O43、铝在空气中燃烧:4Al+3O2 2Al2O34、氢气在空气中燃烧:2H2+O2 2H2O5、红磷在空气中燃烧:4P+5O2 2P2O56、硫粉在空气中燃烧:S+O2 SO27、碳在氧气中充分燃烧:C+O2 CO28、碳在氧气中不充分燃烧:2C+O2 2CO9、二氧化碳通过灼热碳层:C+CO2 2CO10、一氧化碳在氧气中燃烧:2CO+O2 2CO211、二氧化碳和水反应(二氧化碳通入紫色石蕊试液):CO2+H2O==H2CO312、生石灰溶于水:CaO+H2O==Ca(OH)213、无水硫酸铜作干燥剂:CuSO4+5H2O==CuSO4•5H2O14、钠在氯气中燃烧:2Na+Cl2 2NaCl分解反应15、实验室用双氧水制氧气:2H2O2 2H2O+O2↑16、加热高锰酸钾:2KMnO4 K2MnO4+MnO2+O2↑17、水在直流电的作用下分解:2H2O 2H2↑+O2↑18、碳酸不稳定而分解:H2CO3==H2O+CO2↑19、高温煅烧石灰石(二氧化碳工业制法):CaCO3 CaO+CO2↑置换反应20、铁和硫酸铜溶液反应:Fe+CuSO4==FeSO4+Cu21、锌和稀硫酸反应(实验室制氢气):Zn+H2SO4==ZnSO4+H2↑22、镁和稀盐酸反应:Mg+2HCl==MgCl2+H2↑23、氢气还原氧化铜:H2+CuO Cu+H2O24、木炭还原氧化铜:C+2CuO 2Cu+CO2↑25、水蒸气通过灼热碳层:H2O+C H2+CO26、焦炭还原氧化铁:3C+2Fe2O3 4Fe+3CO2↑其他27.氢氧化钠溶液与硫酸铜溶液反应:2NaOH+CuSO4==Cu(OH)2↓+Na2SO428、甲烷在空气中燃烧:CH4+2O2 CO2+2H2O29、酒精在空气中燃烧:C2H5OH+3O2 2CO2+3H2O30、一氧化碳还原氧化铜:CO+CuO Cu+CO231、一氧化碳还原氧化铁:3CO+Fe2O3 2Fe+3CO232、二氧化碳通过澄清石灰水(检验二氧化碳):Ca(OH)2+CO2==CaCO3↓+H2O33、氢氧化钠和二氧化碳反应(除去二氧化碳):2NaOH+CO2==Na2CO3+H2O34、石灰石(或大理石)与稀盐酸反应(二氧化碳的实验室制法):CaCO3+2HCl==CaCl2+H2O+CO2↑35、碳酸钠与浓盐酸反应(泡沫灭火器的原理):Na2CO3+2HCl==2NaCl+H2O+CO2↑。
铝铁化学方程式

七.期中复习一、Al的有关反应1.2 Al2O3 4 Al +3 O2↑电解法制铝(加入冰晶石Na3AlF6降低氧化铝的熔点,做助熔剂)2. 2 Al +6 H2 2 Al(OH)3+3 H2↑3.2 Al +Fe2O3 2 Fe +Al2O3铝热反应(焊接)(冶炼难熔金属)4.2 Al +6 HCl2AlCl3+3 H2↑2 Al +2 NaOH(稀)+2 H2O 2 NaAlO2+3 H2↑二、铝盐的有关反应5.AlCl3+3 H2O Al(OH)3+3 HCl 水解反应Al2(SO4)3+6 NaHCO3 2 Al(OH)3↓+ 3 Na2SO4+6 CO2↑泡沫灭火器6.AlCl3+3 NH3·H2O Al(OH)3↓+ 3 NH4Cl 实验室制备Al(OH)3 AlCl3+3 NaOH(少量)Al(OH)3↓+ 3 NaClAlCl3+4 NaOH(过量)NaAlO2+3 NaCl +2 H2O三、Al(OH)3的有关反应Al3++3OH-Al(OH)3H++AlO2--+H2O碱式电离酸式电离7.NaAlO2+H2O Al(OH)3两性氢氧化物2 Al(OH)3Al2O3+3 H2O 制备Al2O3四、Al(OH)3的制备8.NaAlO2+HCl(少量)+H2O Al(OH)3↓+NaCl2 NaAlO2+CO2+3H2O 2 Al(OH)3↓+Na2CO3较强酸制弱酸AlCl3+3 NH3·H2O Al(OH)3↓+ 3 NH4Cl 实验室制备Al(OH)3AlCl3+3 NaOH(少量)Al(OH)3↓+ 3 NaClAl3++3 AlO2-+6 H2O 4 Al(OH)3↓五、Al2O3的两性9.Al2O3+2 NaOH 2 NaAlO2+H2O Al2O3两性氧化物Al 2O 3 + 6HCl 2 AlCl 3 + 3H 2O Al 2O 3两性氧化物一、Fe 的有关反应 Fe →Fe 2+1.Fe + S FeS Fe + I 2FeI 22. Fe + 2HClFeCl 2 + H 2↑ Fe + H 2SO 4FeSO 4 + H 2↑3. Fe + CuSO 4FeSO 4 + Cu Fe + 2Ag(NO 3)2Fe(NO 3)2 + 2Ag 4. Fe + 2FeCl 33FeCl 2 Fe + 2 Fe(NO 3)33 Fe(NO 3)2Fe →Fe 3+5.2 Fe + 3Cl 23 2 Fe + 3Br 236.Fe + 4 HNO 3(稀)Fe(NO 3)3 + NO ↑+ 2 H 2O HNO 3量多3 Fe (稀) 3 Fe(NO 3)24 H 2O Fe 量多7.3 Fe + 2 O 2 3O 4 3 Fe + 4 H 2O(g)Fe 3O 4 + 4 H 2二.Fe 2+→Fe 3+8. Cl 2 + 2FeCl 22FeCl 39. 还原性:I - > Fe 2+ > Br - > Cl -2 FeBr 2 +3 Cl 2(过量) 2 FeCl 3 + 2 Br 2 6 FeBr 2 + 3 Cl 2(少量) 2 FeCl 3 +4 FeBr 3 FeI 2 + Cl 2(少量) 2 FeCl 2 + I 2 2 FeI 2 + 3Cl 2(过量) 2 FeCl 3 + 2I 210.4 Fe(OH)2 + O 2 + 2 H 2O 4 Fe(OH)3 白色→灰绿→红褐三.Fe 3+→Fe 2+11.2 FeCl 3 + Cu 2 FeCl 2 + CuCl 2 腐蚀铜版 2 FeCl 3 + 2HI2 FeCl 2 + 2 HCl + I 2 2 FeCl3 + H 2S 2 FeCl 2 + S ↓+2 HCl四.其他 12.2 Fe(OH)33 H 2O13.Fe 2O 3 + + 3 CO 2 工业炼铁主要的化学方程式 14.Fe 3O 4 + 3 + FeCl 2 + 4 H 2O15.Fe 3+ + 3SCN -[Fe(SCN)3](血红色) 鉴定Fe 3+离子练习:1. 黑火药是中国古代四大发明之一,它的爆炸反应为: 2KNO 3+3C+S−−→−引燃A+N 2↑+3CO 2↑(已配平)(1)生成物A 的电子式为: ,属于 晶体。
高二化学镁,铝和铁化学方程式总结
高二化学镁,铝和铁化学方程式总结
高二化学镁,铝和铁化学方程式总结
1、碳酸氢钙溶液受热分解Ca(HCO3)2
=CaCO3↓+CO2↑+H2o
2、氯化镁和氨水MgCl2 + 2NH3·H2O =
Mg(OH)2+2NH4Cl
3、铝和氢氧化钠溶液
2Al+2NaOH+2H2o=2NaAlO2+3H2↑
4、铝热反应4Al+3MnO2=3Mn+2Al2O3(高温)
5、氧化铝和盐酸Al2O3 + 6HCl = 2AlCl3 + 3H2O
6、氧化铝和氢氧化钠溶液Al2O3 + 2NaOH = 2NaAlO2 + H2O
7、氢氧化铝受热分解2Al(OH)3=Al2O3+3H2O
8、氢氧化铝和盐酸Al(OH)3+3HCl=AlCl3+3H2O
9、氢氧化铝和氢氧化钠溶液
Al(OH)3+NaOH=NaAlO2+2H2O
10、三氯化铝和过量氨水
AlCl3+3NH3+3H2O=Al(OH)3↓+3NH4Cl
11、三氯化铝和过量氢氧化钠
AlCl3+4NaOH=NaAlO2+3NaCl+2H2o
12、铁和水蒸气3Fe+4H2O=Fe3O4+4H2↑
13、铁和足量的稀盐酸Fe + 2HCl = FeCl2 + H2↑
14、铁和足量的稀硝酸
Fe+4HNO3=Fe(NO3)3+NO↑+2H2o
15、铁(完全过量)和少量的稀硝酸
3Fe+8HNO3=3Fe(NO3)2+2NO↑+4H2o 16、氢氧化铁受热分解2Fe(OH)3=Fe2O3+3H2o。
最新整理铁、铝化学方程式(全)知识讲解
铁、铝化学方程式一、铁1.与O 2反应:3Fe+2O 2−−→−点燃Fe 3O 42.与Cl 2反应:2Fe+3Cl 2−−→−点燃2FeCl 33.与Br 2反应:2Fe+3Br 2−−→−点燃2FeBr 34.与I 2反应:Fe+I 2−−→−点燃FeI 25.与S 反应:Fe+S −→−∆FeS +Q 6.加热下与浓H 2SO 4反应:2Fe+6H 2SO 4(浓)−→−∆2Fe 2(SO 4)3+3SO 2↑+6H 2O 7.加热下与稀HNO 3反应:Fe+4HNO 3−→−∆Fe(NO 3)3+NO ↑+2H 2O 8.高温下与水蒸气反应:3Fe+4H 2O(g)−−→−高温Fe 3O 4+4H 2↑二、铁的氢氧化物(一)Fe(OH)28.被氧气氧化:4Fe(OH)2+O 2+2H 2O →4Fe(OH)39.制取:FeSO 4+2NaOH →Na 2SO 4+Fe(OH)2↓(二)Fe(OH)3 10.受热分解:2Fe(OH)3−→−∆Fe 2O 3+3H 2O 11.制取:Fe 3++OH —→Fe(OH)3↓ 三、铁盐和亚铁盐(一)Fe 2+12.和Cl 2反应:Fe 2++ Cl 2→2Fe 3++2Cl —13.和H 2O 2反应:2H ++2Fe 2++H 2O 2→2Fe 3++2H 2O(二)Fe 3+14.和Fe 反应:2Fe 3++Fe →3Fe 2+15.和Cu 反应:Fe 3++Cu →Cu 2++Fe 2+16.和I —反应:2Fe 3++2I —→2Fe 2++I 217.和SCN —反应:Fe 3++3SCN —↔Fe(SCN)3四、铝18.与Cl 2反应:2Al+3Cl 2−−→−点燃2AlCl 3 19.与S 反应:2Al+3S −→−∆Al 2S 3 20.与O 2反应:4Al+3O 2→2Al 2O 3(常温下生成氧化膜)4Al+3O 2−−→−点燃2Al 2O 3(纯氧中剧烈燃烧)21.毛刷实验:2Al+3Hg(NO 3)2→2Al(NO)3+3Hg ,4Al+3O 2→2Al 2O 322.与水反应:2Al+6H 2O →2Al(OH)3+3H 2↑ 23.与浓HNO 3反应:Al+6HNO 3(浓)−→−∆Al(NO 3)3+3NO 2↑+3H 2O 24.与NaOH 反应:2Al+2NaOH+2H 2O →2NaAlO 2+3H 2↑ 25.铝热反应:2Al+Fe 2O 3−−→−高温Al 2O 3+2Fe 五、氧化铝26.与HCl 反应:Al 2O 3+6HCl →2AlCl 3+3H 2O27.与NaOH 反应:Al 2O 3+2NaOH →2NaAlO 2+H 2O(以上相应的离子方程式对应系数相同)六、氢氧化铝28.酸、碱式电离:H 2O+ AlO 2—+H +↔Al(OH)3↔Al 3++3OH —29.与HCl 反应:Al(OH)3+3HCl →AlCl 3+3H 2O30.与NaOH 反应:Al(OH)3+NaOH →NaAlO 2+2H 2O(以上相应的离子方程式对应系数相同) 31.受热分解:2Al(OH)3−→−∆Al 2O 3+3H 2O 32.制备方法:(1)Al 3+与碱(NH 3·H 2O )反应:AlCl 3+3NH 3·H 2O →Al(OH)3↓+3NH 4Cl(2)AlO 2—与酸(CO 2+H 2O )反应:(CO 2少量)2NaAlO 2+CO 2+3H 2O →Na 2CO 3+2Al(OH)3↓(CO 2过量)NaAlO 2+CO 2+2H 2O →NaHCO 3+Al(OH)3↓(3)双水解反应(Al 3++AlO 2—):AlCl 3+3NaAlO 2+6H 2O →4Al(OH)3↓+3NaCl七、铝盐33.明矾净水原理:Al 3++3H 2O ↔Al(OH)3(胶体)+3H +34.AlCl 3与NaOH 反应:(1)向AlCl 3中加NaOH :AlCl 3+3NaOH →Al(OH)3↓+3NaCl (少量) Al(OH)3+NaOH →NaAlO 2+2H 2O (过量)总反应:AlCl 3+4NaOH →NaAlO 2+2H 2O+3NaCl(2)向NaOH 中加AlCl 3:AlCl 3+4NaOH →NaAlO 2+2H 2O+3NaCl (少量) AlCl 3+3NaAlO 2+6H 2O →4Al(OH)3↓+3NaCl (过量)八、偏铝酸盐35.偏铝酸盐的水解:AlO 2—+2H 2O →Al(OH)3 +OH— 36.与HCl 反应:(1)向NaAlO 2加HCl :NaAlO 2+HCl+H 2O →Al(OH)3↓+NaCl (少量) Al(OH)3+3HCl →AlCl 3+3H 2O (过量)总反应:NaAlO 2+4HCl →AlCl 3+2H 2O+NaCl(2)向HCl 加NaAlO 2:NaAlO 2+4HCl →AlCl 3+2H 2O+NaCl (少量) AlCl 3+3NaAlO 2+6H 2O →Al(OH)3↓+3NaCl (过量)37.总结:Al 3+↔碱强酸Al(OH)3↔强碱酸AlO 2—。
常用物质的化学名称及化学式
精心整理常用物质的化学名称、化学式及反应的化学方程式:一、单质:1、常见气体:氧气:O2氢气:H2氯气:Cl2氮气:N22、稀有气体:氦气:He氖气:Ne氩气:Ar3、金属和非金属单质(1)金属单质:锂:Li铍:Be钠:Na镁:Mg铝:Al钾:K钙:Ca铜:Cu铁:Fe锌:Zn钡:Ba 银:Ag汞:Hg(2)非金属单质:碳:C硅:Si磷:P硫:S二、化合物二、制取气体的化学方程式:1(1)2KClO 3↑(2)2MnO 4+MnO 2+O 2↑(3)2H 2O 2(4)2H 22(1)(2)(3)2(4)3、制取氢气的化学方程式:(1)镁、铝、铁、锌与稀盐酸反应制取H 2:Mg +2HCl =MgCl 2+H 2↑2Al +6HC l =2AlCl 3+3H 2↑ (24(1(2Na 2注意:①往NaOH 溶液中通入CO 2,会发生反应2NaOH+CO 2=====Na 2CO 3+H 2O ;若继续通入Na 2CO 3+H 2O +CO 2===2NaHCO 3而2CO 3+H 2O +CO 2↑②往Ca(OH)2溶液中通入CO 2,会发生反应Ca(OH)2+CO 2====CaCO 3↓+H 2O 若继续通入CO 2,CaCO 3会逐渐溶解,则会发生反应CaCO 3+2===2Ca(HCO 3)2Ca(HCO 3)3↓+H 2O +CO 2↑形成钟乳石、石笋等5、生成陈定的化学方程式:(1)生成BaSO4白色沉淀,不溶于稀HNO3。
离子方程式:Ba2++SO42—=BaSO4↓Ba(OH)2+H2SO4=BaSO4↓+2H2OBa(NO3)2+H2SO4=BaSO4↓+2HNO3Ba(OH)2+Na2SO4=BaSO4↓+2NaOHBa(NO3)2+Na2SO4=BaSO4↓+2NaNO3Ba(OH)2+CuSO4=BaSO4↓+Cu(OH)2↓Ba(NO3)2+CuSO4=BaSO4↓+Cu(NO3)2Ba(OH)2+K2SO4=BaSO4↓+2KOHBa(NO3)2+K2SO4=BaSO4↓+2KNO3 BaCl2+H2SO4=BaSO4↓+2HClBaCl2+Na2SO4=BaSO4↓+2NaClBaCl2+CuSO4=BaSO4↓+CuCl2(2)生成AgCl白色沉淀,不溶于稀HNO3。
高中化学方程式钠,铝,铁全部
钠及其化合物的化学方程式一、钠1、钠在氧气中燃烧:2Na+O2Na2O22、钠在氯气中燃烧:2Na+Cl22NaCl3、钠常温条件下和氧气反应:4Na+O22Na2O4、钠和硫共热:2Na+S Na2S5、钠和水反应:2Na+2H2O2NaOH+H2↑6、钠和稀盐酸反应:2Na+2HCl2NaCl+H2↑7、钠投入到硫酸铜溶液中:2Na+CuSO4+2H2O Na2SO4+CuOH2↓+H2↑8、向氯化铝溶液中加入少量的钠:6Na+2AlCl3+6H2O6NaCl+2AlOH3↓+3H2↑9、向氯化铝溶液中加入足量的钠:4Na+AlCl3+2H2O NaAlO2+3NaCl+2H2↑10、钠在高温条件下与四氯化钛反应:4Na+TiCl44NaCl+Ti二、氧化钠1、氧化钠和水反应:Na2O+H2O=2NaOH2、氧化钠与二氧化碳反应:Na2O+CO2Na2CO33、氧化钠与盐酸反应:Na2O+2HCl2NaCl+H2O4、向硫酸铜溶液中加入氧化钠:Na2O+CuSO4+H2O CuOH2↓+Na2SO45、向氯化铝溶液中加入少量的氧化钠:3Na2O+2AlCl3+3H2O2AlOH3↓+6NaCl6、向氯化铝溶液中加入足量的氧化钠:2Na2O+AlCl3NaAlO2+3NaCl三、过氧化钠1、过氧化钠与水反应:2Na2O2+2H2O4NaOH+O2↑2、过氧化钠与二氧化碳反应:2Na2O2+2CO22Na2CO3+O2↑3、过氧化钠与盐酸反应:2Na2O2+4HCl4NaCl+2H2O+O2↑4、向硫酸铜溶液中加入过氧化钠:2Na2O2+2CuSO4+2H2O===2CuOH2↓+2Na2SO4+O2↑5、向氯化铝溶液中加入少量的过氧化钠:6Na2O2+4AlCl3+6H2O4AlOH3↓+12NaCl+3O2↑6、向氯化铝溶液中加过量的过氧化钠:2Na2O2+AlCl3+2H2O NaAlO2+3NaCl+O2↑7、过氧化钠与硫酸亚铁溶液反应:4Na2O2+4FeSO4+6H2O4FeOH3↓+4Na2SO4+O2↑四、氢氧化钠1、铝与氢氧化钠溶液反应:2Al+2NaOH+2H2O2NaAlO2+3H2↑2、氯气通入氢氧化钠溶液中:Cl2+2NaOH NaCl+NaClO+H2O3、氯气通入热的浓氢氧化钠溶液中:3Cl2+6NaOH5NaCl+NaClO3+3H2O4、硫和氢氧化钠溶液共热:3S+6NaOH2Na2S+Na2SO3+3H2O5、硅溶于氢氧化钠溶液中:Si+2NaOH+H2O Na2SiO3+2H2↑6、氧化铝溶于氢氧化钠溶液中:Al2O3+2NaOH2NaAlO2+H2O7、向氢氧化钠溶液中通入少量的二氧化碳:2NaOH+CO2Na2CO3+H2O8、向氢氧化钠溶液中通入过量的二氧化碳:NaOH+CO2NaHCO39、向氢氧化钠溶液中通入少量的二氧化硫:2NaOH+SO2Na2SO3+H2O10、向氢氧化钠溶液中通入过量的二氧化硫:NaOH+SO2NaHSO311、五氧化二磷与氢氧化钠溶液反应:P2O5+6NaOH2Na3PO4+3H2O12、二氧化氮和氢氧化钠溶液反应:2NO2+2NaOH NaNO2+NaNO3+H2O13、一氧化氮、二氧化氮和氢氧化钠溶液反应:NO+NO2+2NaOH2NaNO2+H2O14、将二氧化硅溶于氢氧化钠溶液中:2NaOH+SiO2Na2SiO3+H2O15、三氧化硫和氢氧化钠溶液反应:SO3+2NaOH Na2SO4+H2O16、盐酸和氢氧化钠溶液反应:HCl+NaOH NaCl+H2O17、醋酸和氢氧化钠溶液反应:CH3COOH+NaOH CH3COONa+H2O18、向氢氧化钠溶液中通入少量的硫化氢:H2S+2NaOH Na2S+2H2O19、向氢氧化钠溶液中通入足量的硫化氢:H2S+NaOH NaHS+H2O20、硫酸和氢氧化钠溶液反应:H2SO4+2NaOH Na2SO4+2H2O21、磷酸溶液氢氧化钠溶液反应:H3PO4+3NaOH Na3PO4+3H2O22、将氢氧化铝溶于氢氧化钠溶液中:AlOH3+NaOH NaAlO2+2H2O23、向硝酸银溶液中加入氢氧化钠溶液:AgNO3+NaOH AgOH ↓+NaNO324、向硫酸铜溶液中加入氢氧化钠溶液:CuSO4+2NaOH Na2SO4+CuOH2↓25、向氯化铁溶液中加入氢氧化钠溶液:FeCl3+3NaOH FeOH3↓+3NaCl26、向氯化铝溶液中加入少量氢氧化钠溶液:AlCl3+3NaOH AlOH3↓+3NaCl27、向氯化铝溶液中加入足量氢氧化钠溶液:AlCl3+4NaOH NaAlO2+3NaCl+2H2O28、向氯化铵溶液加入氢氧化钠溶液,加热:NH4Cl+NaOH NaCl+NH3↑+H2O29、向碳酸氢铵溶液中加入少量氢氧化钠溶液共热:NH4HCO3+NaOH NaHCO3+NH3↑+H2O30、向碳酸氢铵溶液中加入足量氢氧化钠溶液共热:NH4HCO3+2NaOH Na2CO3+NH3↑+2H2O31、碳酸氢钠溶液与氢氧化钠溶液混合:NaHCO3+NaOH Na2CO3+H2O32、向碳酸氢钙溶液中加入少量氢氧化钠溶液:CaHCO32+NaOH CaCO3↓+NaHCO3+H2O33、向碳酸氢钙溶液中加入过量氢氧化钠溶液:CaHCO32+2NaOH CaCO3↓+Na2CO3+2H2O34、向碳酸氢镁溶液中加入少量的氢氧化钠溶液:MgHCO32+2NaOH MgOH2↓+2NaHCO335、向碳酸氢镁溶液中加入过量的氢氧化钠溶液:MgHCO32+4NaOH MgOH2↓+Na2CO3+2H2O五、氯化钠1、氯化钠溶液与硝酸银溶液混合:NaCl+AgNO3AgCl↓+NaNO32、氯化钠固体和浓硫酸共热:NaCl+H2SO4Na2SO4+2HCl↑3、电解饱和的氯化钠溶液:2NaCl+2H2O2NaOH+H2↑+Cl2↑4、电解氯化钠的熔融液:2NaCl2Na+Cl2↑六、碳酸钠1、碳酸钠溶液与澄清石灰水反应:Na2CO3+CaOH2CaCO3↓+2NaOH2、碳酸钠溶液与氯化钡溶液混合:Na2CO3+BaCl2BaCO3↓+2NaCl3、碳酸钠溶液呈碱性:Na2CO3+H2O NaHCO3+NaOH4、碳酸钠溶液滴入少量的盐酸:Na2CO3+HCl NaHCO3+NaCl5、碳酸钠溶液滴入足量的盐酸:Na2CO3+2HCl2NaCl+CO2↑+H2O6、碳酸钠溶液中加入醋酸:Na2CO3+2CH3COOH2CH3COONa+CO2↑+H2O7、碳酸钠溶液中通入二氧化碳气体:Na2CO3+CO2+H2O2NaHCO38、向饱和的碳酸钠溶液中通入二氧化碳气体:Na2CO3+CO2+H2O2NaHCO39、碳酸钠溶液与氯化铝溶液混合:3Na2CO3+2AlCl3+3H2O2AlOH3↓+6NaCl+3CO2↑10、碳酸钠溶液与氯化铁溶液混合:3Na2CO3+2FeCl3+3H2O2FeOH3↓+6NaCl+3CO2↑七、碳酸氢钠1、碳酸氢钠溶液呈碱性:NaHCO3+H2O H2CO3+NaOH2、碳酸氢钠溶液滴入盐酸:NaHCO3+HCl NaCl+CO2↑+H2O3、碳酸氢钠溶液滴入醋酸:NaHCO3+CH3COOH CH3COONa+CO2↑+H2O4、碳酸氢钠溶液与氯化铝溶液混合:3NaHCO3+AlCl3AlOH3↓+3NaCl+3CO2↑5、碳酸氢钠溶液与氯化铁溶液混合:3NaHCO3+FeCl3FeOH3↓+3NaCl+3CO2↑6、碳酸氢钠溶液与氢氧化钠溶液混合:NaHCO3+NaOH Na2CO3+H2O7、碳酸氢钠溶液中加入过量氢氧化钙溶液:NaHCO3+CaOH2 =CaCO3↓+NaOH+H2O8、碳酸氢钠溶液中加入少量氢氧化钙溶液: 2NaHCO3+CaOH2 =CaCO3↓+Na2CO3+2H2O9、碳酸氢钠受热分解:2NaHCO3Na2CO3+CO2↑+H2O铝及其化合物的化学方程式 一、铝1、铝在氧气中燃烧:4Al +3O 22Al 2O 32、铝在氯气中燃烧:2Al +3Cl 22AlCl 33、铝和硫共热:2Al +3S Al 2S 34、铝与稀硫酸反应:2Al +3H 2SO 4Al 2SO 43 +3H 2 ↑5、铝和氢氧化钠溶液反应:2Al +2NaOH +2H 2O2NaAlO 2+3H 2 ↑6、铝和浓硫酸共热:2Al +6H 2SO 4Al 2SO 43 +3SO 2 ↑+6H 2O7、铝和浓硝酸共热:Al +6HNO 3AlNO 33 +3NO 2 ↑+3H 2O8、铝和稀硝酸反应:Al +4HNO 3AlNO 33 +NO ↑+2H 2O8、铝和硝酸银溶液反应:Al +3AgNO 3AlNO 33 +3Ag 9、铝与硫酸铜溶液反应:2Al +3CuSO 4Al 2SO 43 +3Cu10、铝和氧化铁高温下反应:2Al +Fe 2O 3Al 2O 3+2Fe 11、铝和四氧化三铁高温共热:8Al +3Fe 3O 44Al 2O 3+9Fe 12、铝和氧化铜高温共热:2Al +3CuO Al 2O 3+3Cu 13、铝和二氧化锰高温共热:4Al +3MnO 22Al 2O 3+3Mn二、氧化铝1、氧化铝与稀硫酸反应:Al 2O 3+3H 2SO 4Al 2SO 43 +3H 2O2、氧化铝与氢氧化钠溶液反应:Al 2O 3+2NaOH 2NaAlO 2+H 2O3、电解氧化铝的熔融液:2Al 2O 34Al +3O 2 ↑三、氢氧化铝1、氢氧化铝与稀硫酸反应:2AlOH 3 +3H 2SO 4Al 2SO 43 +6H 2O2、氢氧化铝与氢氧化钠溶液反应:AlOH 3 +NaOHNaAlO 2+2H 2O3、加热氢氧化铝:2AlOH 3 Al 2O 3+3H 2O四、硫酸铝冰晶石电解1、硫酸铝溶液与氯化钡溶液混合:Al2SO43+3BaCl22AlCl3+3BaSO4↓2、硫酸铝的水溶液呈酸性:Al2SO43+6H2O2AlOH3+3H2SO43、硫酸铝溶液中加入少量的氢氧化钠溶液:Al2SO43+6NaOH3Na2SO4+2AlOH3↓4、向硫酸铝溶液中加足量的氢氧化钠溶液:Al2SO43+8NaOH2NaAlO2+3Na2SO4+4H2O5、向硫酸铝溶液中加入少量的氢氧化钡溶液:Al2SO43+3BaOH22AlOH3↓+3BaSO4↓6、向硫酸铝溶液中加入足量的氢氧化钡溶液:Al2SO43+4BaOH2BaAlO22+3BaSO4↓+4H2O7、向明矾溶液中加入少量的氢氧化钡溶液:3BaOH2+2KAlSO422AlOH3↓+3BaSO4↓+K2SO48、向明矾溶液中加入足量的氢氧化钡溶液:KAlSO42+2BaOH2KAlO2+2BaSO4↓+2H2O9、向硫酸铝溶液中加入氨水:Al2SO43+6NH3·H2O2AlOH3↓+3NH42SO410、向硫酸铝溶液中加入碳酸钠溶液:Al2SO43+3Na2CO3+3H2O2AlOH3↓+3Na2SO4+3CO2↑11、向硫酸铝溶液中加入碳酸氢钠溶液:Al2SO43+6NaHCO32AlOH3↓+3Na2SO4+6CO2↑12、向硫酸铝溶液中加入硫化钠溶液:Al2SO43+3Na2S+6H2O2AlOH3↓+3Na2SO4+3H2S ↑13、向硫酸铝溶液中加入硫氢化钠溶液:Al2SO43+6NaHS+6H2O2AlOH3↓+3Na2SO4+6H2S ↑14、向硫酸铝溶液中加入硅酸钠溶液:Al2SO43+3Na2SiO3+6H2O2AlOH3↓+3Na2SO4+3H2SiO3↓15、向硫酸铝溶液中加入偏铝酸钠溶液:Al2SO43+6NaAlO2+12H2O3Na2SO4+8AlOH3↓五、偏铝酸钠1、偏铝酸钠溶液呈碱性:NaAlO2+2H2O AIOH3+NaOH2、偏铝酸钠溶液滴入少量盐酸:NaAlO2+HCl+H2O AlOH3↓+NaCl↓3、向偏铝酸钠溶液加入足量盐酸:NaAlO2+4HCl NaCl+AlCl3+2H2O4、向偏铝酸钠溶液通入少量二氧化碳气体:2NaAlO2+CO2+3H2O2AlOH3↓+Na2CO35、向偏铝酸钠溶液通入足量二氧化碳气体:NaAlO2+CO2+2H2O AlOH3+NaHCO36、向偏铝酸钠溶液中加入硫酸铝溶液:Al2SO43+6NaAlO2+12H2O3Na2SO4+8AlOH3↓7、向偏铝酸钠溶液中加氯化铵:NaAlO2+NH4Cl+H2O AlOH3↓+NaCl+NH3↑8、向偏铝酸钠溶液中加入氯化铁溶液:3NaAlO2+FeCl3+6H2O3AlOH3↓+FeOH3↓+3NaCl铁及其化合物的化学方程式一、铁1、铁在氧气中燃烧:3Fe+2O2Fe3O42、铁在氯气中燃烧:2Fe+3Cl22FeCl33、常温条件下铁锈的形成:4Fe+3O2+2H2O2Fe2O3·H2O4、高温条件铁与氧气反应:2Fe+O22FeO5、铁和硫共热:Fe+S FeS6、铁与水蒸气在高温条件下反应:3Fe+4H2O Fe3O4+4H27、铁与稀硫酸反应:Fe+H2SO4FeSO4+H2↑8、少量的铁与浓硫酸共热:2Fe+6H2SO4Fe2SO43+3SO2↑+6H2O9、过量的铁与浓硫酸共热:Fe+2H2SO4FeSO4+SO2↑+2H2O10、少量的铁与浓硝酸共热:Fe+6HNO3FeNO33+3NO2↑+3H2O11、过量的铁与浓硝酸共热:Fe+4HNO3FeNO32+2NO2↑+2H2O12、少量的铁与稀硝酸反应:Fe+4HNO3FeNO33+NO↑+2H2O13、过量的铁与稀硝酸反应: 3Fe+8HNO33FeNO32+2NO ↑+4H2O14、铁与硫酸铜溶液反应:Fe+CuSO4FeSO4+Cu15、铁与硝酸银溶液反应:Fe+2AgNO3FeNO32+2Ag16、铁与氯化铁溶液反应:Fe+2FeCl33FeCl2二、氧化亚铁1、氧化亚铁在空气中加热:6FeO+O22Fe3O42、氧化亚铁与一氧化碳高温反应:FeO+CO Fe+CO23、氧化亚铁与铝粉在高温下反应:3FeO+2Al Al2O3+3Fe4、氧化亚铁与稀硫酸反应:FeO+H2SO4FeSO4+H2O5、氧化亚铁与浓硫酸反应:2FeO+4H2SO4Fe2SO43+SO2↑+4H2O6、氧化亚铁与浓硝酸反应:FeO+4HNO3FeNO33+NO2↑+2H2O7、氧化亚铁与稀硝酸反应:3FeO+10HNO33FeNO33+NO ↑+5H2O三、四氧化三铁1、四氧化三铁与铝粉高温下反应:8Al+3Fe3O44Al2O3+9Fe2、四氧化三铁与一氧化碳高温下反应:Fe3O4+4CO3Fe+4CO23、四氧化三铁溶于稀盐酸:Fe3O4+8HCl FeCl2+2FeCl3+4H2O4、四氧化三铁溶于浓硫酸:2Fe3O4+10H2SO43Fe2SO43+SO2↑+10H2O5、四氧化三铁溶于浓硝酸:Fe3O4+10HNO33FeNO33+NO2↑+5H2O6、四氧化三铁溶于稀硝酸:3Fe3O4+28HNO39FeNO33+NO ↑+14H2O6、四氧化三铁溶于氢碘酸:Fe3O4+8HI3FeI2+I2+4H2O四、氧化铁1、铝和氧化铁高温下反应:2Al+Fe2O3Al2O3+2Fe2、一氧化碳和氧化铁高温下反应:Fe2O3+3CO2Fe+3CO23、氧化铁溶液稀盐酸:Fe2O3+6HCl2FeCl3+3H2O4、氧化铁与氢碘酸反应:Fe2O3+6HI2FeI2+I2+3H2O五、氢氧化亚铁1、氢氧化亚铁与稀硫酸反应:FeOH2+H2SO4FeSO4+2H2O2、氢氧化亚铁与浓硫酸反应:2FeOH2+4H2SO4Fe2SO43+SO2↑+6H2O3、氢氧化亚铁与浓硝酸反应:FeOH2+4HNO3FeNO33+NO2↑+3H2O4、氢氧化亚铁与稀硝酸反应:3FeOH2+10HNO33FeNO33+NO↑+8H2O5、氢氧化亚铁在空气中被氧化:4FeOH2+O2+2H2O4FeOH36、氢氧化亚铁隔绝空气加热:FeOH2FeO+H2O7、氢氧化亚铁在空气中加热:4FeOH2+O22Fe2O3+4H2O六、氢氧化铁1、氢氧化铁与稀硫酸反应:2FeOH3+3H2SO4Fe2SO43+6H2O2、氢氧化铁溶于氢碘酸:2FeOH3+6HI2FeI2+I2+6H2O3、加热氢氧化铁:2FeOH3Fe2O3+3H2O七、氯化亚铁1、铝与氯化亚铁溶液反应:2Al+3FeCl22AlCl3+3Fe2、锌与氯化亚铁反应:Zn+FeCl2ZnCl2+Fe3、氯化亚铁暴露在空气中变质:12FeCl2+3O2+6H2O8FeCl3+4FeOH3↓4、酸化的氯化亚铁溶液中通入氧气:4FeCl2+O2+4HCl4FeCl3+2H2O5、氯化亚铁溶液中通入氯气:2FeCl2+Cl22FeCl36、氯化亚铁溶液中加入溴水:6FeCl2+3Br24FeCl3+2FeBr37、氯化亚铁溶液呈酸性:FeCl2+2H2O FeOH2+2HCl8、氯化亚铁溶液中加入氢氧化钠溶液:FeCl2+2NaOH FeOH2↓+2NaCl9、氯化亚铁溶液中加入氨水:FeCl2+2NH3·H2O FeOH2↓+2NH4Cl10、氯化亚铁溶液中加入偏铝酸钠溶液:FeCl2+2NaAlO2+4H2O FeOH2↓+2AlOH3↓+2NaCl11、氯化亚铁溶液中加入硝酸银溶液:FeCl2+2AgNO3FeNO32+2AgCl↓12、氯化亚铁溶液中加入硫化钠溶液:FeCl2+Na2S FeS↓+2NaCl13、硫酸亚铁溶液与浓硫酸反应:2FeSO4+2H2SO4Fe2SO43+SO2↑+2H2O14、硝酸亚铁溶液与浓硝酸反应:FeNO32+2HNO3FeNO33+NO2↑+H2O15、硝酸亚铁溶液与稀硝酸反应:3FeNO32+10HNO33FeNO33+NO ↑+5H2O16、酸化的氯化亚铁被过氧化氢所氧化:2FeCl2+H2O2+2HCl2FeCl3+2H2O17、过氧化钠与氯化亚铁溶液反应:4Na2O2+4FeCl2+6H2O4FeOH3↓+8NaCl+O2↑18、次氯酸钠溶液与氯化亚铁溶液反应2FeCl2+5NaClO+5H2O2FeOH3↓+5NaCl+4HClO八、氯化铁1、少量的锌和氯化铁溶液反应:Zn+2FeCl32FeCl2+ZnCl22、过量的锌与氯化铁溶液反应:3Zn+2FeCl33ZnCl2+2Fe3、铁与氯化铁溶液反应:Fe+2FeCl33FeCl24、铜和氯化铁溶液反应:Cu+2FeCl32FeCl2+CuCl25、向氯化铁溶液中通入二氧化硫:2FeCl3+SO2+2H2O2FeCl2+H2SO4+2HCl6、氯化铁溶液呈酸性:FeCl3+3H2O FeOH3+3HCl7、氯化铁溶液中加入氢氧化钠溶液:FeCl3+3NaOH FeOH3↓+3NaCl8、向氯化铁溶液中加入氨水:FeCl3+3NH3·H2O FeOH3↓+3NH4Cl9、向氯化铁溶液中加入碳酸钠溶液:2FeCl3+3Na2CO3+3H2O2FeOH3↓+6NaCl+3CO2↑10、向氯化铁溶液中加入碳酸氢钠溶液:FeCl3+3NaHCO3FeOH3↓+3NaCl+3CO2↑11、向氯化铁溶液中加入偏铝酸钠溶液:FeCl3+3NaAlO2+6H2O FeOH3↓+3AlOH3↓+3NaCl12、向氯化铁溶液中加入次氯酸钠溶液:FeCl3+3NaClO+3H2O FeOH3↓+3NaCl+3HClO13、向氯化铁溶液中通入硫化氢:2FeCl3+H2S2FeCl2+S↓+2HCl14、向氯化铁溶液中加入氢碘酸:2FeCl3+2HI2FeCl2+I2+2HCl15、向氯化铁溶液中加入少量的硫化钠溶液:2FeCl3+Na2S2FeCl2+S↓+2NaCl16、向氯化铁溶液中加入过量的硫化钠溶液:2FeCl3+3Na2S2FeS↓+S↓+6NaCl17、氯化铁溶液与碘化钾溶液混合:2FeCl3+2KI2FeCl2+I2+2KCl18、氯化铁溶液与硝酸银溶液混合:FeCl3+3AgNO33AgCl↓+FeNO3319、氯化铁溶液中加入硫氰化钾溶液:FeCl3+3KSCN FeSCN3+3KCl20、氧化镁投入到氯化铁溶液中: 3MgO+2FeCl3+3H2O3MgCl2+2FeOH321、氢氧化镁投入到氯化铁溶液中:3MgOH2+2FeCl33MgCl2+2FeOH3。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
铁、铝化学方程式
一、铁
1.与O 2反应:3Fe+2O 2−−→−点燃
Fe 3O 4 2.与Cl 2反应:2Fe+3Cl 2−−→−点燃
2FeCl 3 3.与Br 2反应:2Fe+3Br 2−−→−点燃
2FeBr 3 4.与I 2反应:Fe+I 2−−→−点燃
FeI 2 5.与S 反应:Fe+S −→−∆
FeS +Q 6.加热下与浓H 2SO 4反应:2Fe+6H 2SO 4(浓)−→−∆
2Fe 2(SO 4)3+3SO 2↑+6H 2O 7.加热下与稀HNO 3反应:Fe+4HNO 3−→−
∆
Fe(NO 3)3+NO ↑+2H 2O 8.高温下与水蒸气反应:3Fe+4H 2O(g)−−→−高温Fe 3O 4+4H 2↑ 二、铁的氢氧化物
(一)Fe(OH)2
8.被氧气氧化:4Fe(OH)2+O 2+2H 2O →4Fe(OH)3
9.制取:FeSO 4+2NaOH →Na 2SO 4+Fe(OH)2↓
(二)Fe(OH)3
10.受热分解:2Fe(OH)3−→−
∆
Fe 2O 3+3H 2O 11.制取:Fe 3++OH —→Fe(OH)3↓
三、铁盐和亚铁盐
(一)Fe 2+
12.和Cl 2反应:Fe 2++ Cl 2→2Fe 3++2Cl —
13.和H 2O 2反应:2H ++2Fe 2++H 2O 2→2Fe 3++2H 2O
(二)Fe 3+
14.和Fe 反应:2Fe 3++Fe →3Fe 2+
15.和Cu 反应:Fe 3++Cu →Cu 2++Fe 2+
16.和I —反应:2Fe 3++2I —→2Fe 2++I 2
17.和SCN—反应:Fe3++3SCN— Fe(SCN)3
18.与Cl 2反应:2Al+3Cl 2−−→−点燃
2AlCl 3 19.与S 反应:2Al+3S −→−∆
Al 2S 3 20.与O 2反应:4Al+3O 2→2Al 2O 3(常温下生成氧化膜)
4Al+3O 2−−→−点燃
2Al 2O 3(纯氧中剧烈燃烧) 21.毛刷实验:2Al+3Hg(NO 3)2→2Al(NO)3+3Hg ,4Al+3O 2→2Al 2O 3
22.与水反应:2Al+6H 2O →2Al(OH)3+3H 2↑
23.与浓HNO 3反应:Al+6HNO 3(浓)−→−∆
Al(NO 3)3+3NO 2↑+3H 2O 24.与NaOH 反应:2Al+2NaOH+2H 2O →2NaAlO 2+3H 2↑
25.铝热反应:2Al+Fe 2O 3−−→
−高温
Al 2O 3+2Fe 五、氧化铝
26.与HCl 反应:Al 2O 3+6HCl →2AlCl 3+3H 2O
27.与NaOH 反应:Al 2O 3+2NaOH →2NaAlO 2+H 2O
(以上相应的离子方程式对应系数相同)
六、氢氧化铝
28.酸、碱式电离:H 2O+ AlO 2—+H +↔Al(OH)3↔Al 3++3OH —
29.与HCl 反应:Al(OH)3+3HCl →AlCl 3+3H 2O
30.与NaOH 反应:Al(OH)3+NaOH →NaAlO 2+2H 2O
(以上相应的离子方程式对应系数相同) 31.受热分解:2Al(OH)3−→−
∆
Al 2O 3+3H 2O 32.制备方法:
(1)Al 3+与碱(NH 3·H 2O )反应:AlCl 3+3NH 3·H 2O →Al(OH)3↓+3NH 4Cl
(2)AlO 2—与酸(CO 2+H 2O )反应:(CO 2少量)2NaAlO 2+CO 2+3H 2O →Na 2CO 3+2Al(OH)3↓
(CO 2过量)NaAlO 2+CO 2+2H 2O →NaHCO 3+Al(OH)3↓
(3)双水解反应(Al 3++AlO 2—):AlCl 3+3NaAlO 2+6H 2O →4Al(OH)3↓+3NaCl
33.明矾净水原理:Al3++3H2O↔Al(OH)3(胶体)+3H+
34.AlCl3与NaOH反应:
(1)向AlCl3中加NaOH:AlCl3+3NaOH→Al(OH)3↓+3NaCl(少量)
Al(OH)3+NaOH→NaAlO2+2H2O(过量)
总反应:AlCl3+4NaOH→NaAlO2+2H2O+3NaCl
(2)向NaOH中加AlCl3:AlCl3+4NaOH→NaAlO2+2H2O+3NaCl(少量)
AlCl3+3NaAlO2+6H2O→4Al(OH)3↓+3NaCl(过量)八、偏铝酸盐
35.偏铝酸盐的水解:AlO2—+2H2O→Al(OH)3 +OH—
36.与HCl反应:
(1)向NaAlO2加HCl:NaAlO2+HCl+H2O→Al(OH)3↓+NaCl(少量)
Al(OH)3+3HCl→AlCl3+3H2O(过量)
总反应:NaAlO2+4HCl→AlCl3+2H2O+NaCl
(2)向HCl加NaAlO2:NaAlO2+4HCl→AlCl3+2H2O+NaCl(少量)
AlCl3+3NaAlO2+6H2O→Al(OH)3↓+3NaCl(过量)
37.总结:Al3+↔碱强酸Al(OH)3↔强碱酸AlO2—
如有侵权请联系告知删除,感谢你们的配合!。
