第3章《物质构成的奥秘》
沪教版九年级化学第三章《物质构成的奥秘》知识点归纳整理
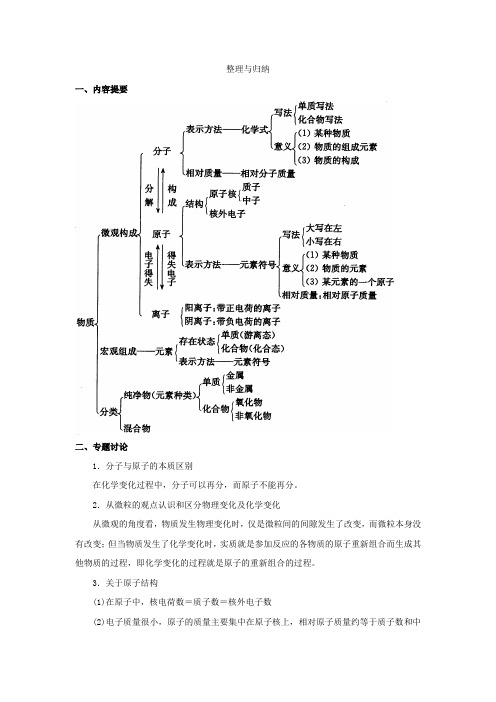
整理与归纳一、内容提要二、专题讨论1.分子与原子的本质区别在化学变化过程中,分子可以再分,而原子不能再分。
2.从微粒的观点认识和区分物理变化及化学变化从微观的角度看,物质发生物理变化时,仅是微粒间的间隙发生了改变,而微粒本身没有改变;但当物质发生了化学变化时,实质就是参加反应的各物质的原子重新组合而生成其他物质的过程,即化学变化的过程就是原子的重新组合的过程。
3.关于原子结构(1)在原子中,核电荷数=质子数=核外电子数(2)电子质量很小,原子的质量主要集中在原子核上,相对原子质量约等于质子数和中子数之和;(3)原子的种类是由核内质子数决定的,元素的化学性质是由原子的最外层电子数决定的。
4.化学式表示的意义宏观上:(1)表示某物质;(2)表示该物质是由哪些元素组成的。
微观上:(1)表示该物质的一个分子或一个原子;(2)由分子构成的物质还表示一个分子的构成情况;5.有关化学式的计算(1)计算化合物中原子个数之比我们知道,化学式中,元素符号右下角的数字就是表示该元素原子的个数,因此这些数字的比值就是化合物中原子个数之比。
如Fe3O4中,铁原子和氧原子个数比3∶4,CaCO3中,钙、碳、氧原子个数比为1∶1∶3。
(2)计算化合物中各元素质量比以Fe3O4为例,可知其中铁原子与氧原子的个数比为3∶4,可设铁原子个数为3k,氧原子个数为4k;可以通过查表得到铁的相对原子质量为56,氧的相对原子质量为16,则铁元素的质量和氧元素的质量比为Fe∶O=3k×56∶4k×16=21∶8。
故在某一种化合物中,各元素质量之比就是各元素的原子个数与它的相对原子质量之间的比值。
(3)计算化合物中某一元素的质量分数三、思维启迪多少克碳酸氢铵(NH4HCO3)与400 g硝酸铵(NH4NO3)含氮元素质量相同?解析:解答本题,要先分别算出NH4HCO3和NH4NO3中氮元素的质量分数,再算出400 g NH4NO3中含氮元素的质量。
2024年新沪教版九年级上册化学课件 第3章 物质构成的奥秘第1节 构成物质的微观粒子

举例 远处可闻到花香;湿衣服晾干
基本性质
举例
分子之间有空隙
同种分子化学性质相 同,不同种分子化学性 质不同
如氧气和液氧是由同种分子构成的,它 们的化学性质相同,都具有助燃性;过 氧化氢和水的分子构成不同,化学性质 不同
C
A.分子的种类变多 C.分子间的空隙变小
B.每个水分子体积变大 D.每个水分子质量变大
[解析] 水蒸气变成冰晶的过程是物理变化(由气态变成固态), 分子本身不改变,主要是分子间的空隙变小。
3.从宏观和微观的角度区分纯净物和混合物
宏观
微观(分子的观点)
实例
只由一种 纯净物
物质组成
由同种分子构成的物质 (只含有一种分子,有固定的 性质)
氧气中只含 有氧分子
宏观
由两种或 两种以上 混合物 物质混合 而成
科学家经过长期研究证实,构成物质的微观粒子有分子、原子和离子。
典例1 下列物质由分子构成的是( C )
A.金
B.金刚石
C.水
D.氯化钠
[解析] 金是由金原子直接构成的;金刚石是由碳原子直接构成的; 水是由水分子构成的;氯化钠是由离子构成的。故选C。
1.分子 (1)大量分子聚集成物质 分子是构成物质的一种微观粒子,大量的分子 聚集在一起,形成了我们能感知到的物质。如 水是由大量的水分子聚集而成的。
特别提醒
对原子的理解
典例3 如图所示是电解水反应的微观示意图,该图说明了( B )
A.水分子是由氢分子和氧分子构成的 B.水分子在化学反应中可以再分 C.化学反应的实质是分子重新组合的过程 D.分子是化学变化中的最小微观粒子
(4)分子和原子的区别与联系
分子
原子
概念 由分子构成的物质,分子是保 原子是化学变化中的最小 持其化学性质的最小微观粒子 微观粒子
第3章物质构成的奥秘总结提升课件---2024-2025学年九年级化学沪教版(全国)(2024)上册

和钠离子
的化学性质不同
1
2
3
25
26
27
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
19
20
21
22
23
24
返回目录
22. (2022·贺州)某元素X的原子序数为 a ,能够形成X n-,另一元素
Y能够形成与X n-具有相同电子层结构的Y m+,则元素Y的原子核内质
子数是( B )
A. a + m - n
7
8
9
10
11
12
13
14
15
16
17
18
19
20
21
22
23
24
返回目录
21. 下列因果关系错误的是(
C )
A. 因为分子构成不同,所以水和过氧化氢的化学性质不同
B. 因为质子数不同,所以碳原子和氮原子所属的元素种类不同
C. 因为碳原子的排列方式不同,所以金刚石和石墨的性质完全不同
D. 因为电子层数及最外层电子数不同,所以钠原子
B. 原子核都是由质子和中子构成的
C. 原子得到或失去电子变成离子
D. 分子的质量一定比原子的质量大
1
2
3
25
26
27
4
5
6
7
8
9
10
11
12
13
14
15
16
17
18
19
20
21
22
23
24
返回目录
九年级化学全册-第三章《物质构成的奥秘》教案-(新版)沪教版

第三章物质构成的奥秘第1节构成物质的基本微粒3。
1 构成物质的基本微粒第1课时教学目标1. 认识物质的微粒性:物质由微粒构成的,微粒不断运动,微粒之间有间隔;2.知道微粒运动快慢、微粒间隔大小的影响因素,微粒间隔大小与物质状态的关系。
3。
能用微粒的观点来解释某些常见的现象4.掌握物质性质与微粒之间的关系:微粒的性质决定了物质的化学性质;教学重点能从微观上认识微粒的性质教学难点能从微观上认识微粒的性质教学过程:【预习交流】一、回顾、预习与交流1.高锰酸钾固体的颜色为_______,高锰酸钾溶液______色。
2.冰、水、水蒸气是同种物质吗?___________;干冰和冰是同种物质吗?____3.水的电解和水的蒸发是同种变化吗?你能解释吗?4.汞俗称水银,可作为温度计的材料,你能解释原因吗?水能否作为制作温度计的材料呢?夏天,高速行驶的汽车容易爆胎,你知道原因吗?【导入】通过第一章和第二章的学习,我们已初步认识了什么是化学,也初步了解了身边最常见的一些物质――空气、氧气、二氧化碳、水等的性质、变化、用途以及制取途径。
各种各样的物质构成的五彩缤纷的宏观世界:这么多物质是怎么构成的呢?为什么不同的物质之间有些性质千差万别,有些物质性质却很相似呢?为什么同一种物质会发生不同的变化呢?这些问题都与物质的构成有关.【创设情境】同学们,上课之前我们进行一次比赛,请各组同学在10s之内把桌上的纸条尽你们可能分成最小块,尽量保证每次均分,开始!适当评价、引入,当学生感到很难再分割下去时,追问:还能继续分吗?(感受物质无限可分的哲学思想)二、合作~研讨~点拨活动一、探究物质的可分性[观察实验]高锰酸钾溶于水[现象记录]①固体颗粒逐渐_____。
②溶液的颜色__________[交流讨论]产生上述现象的原因[结论]物质由极其微小的_________构成活动二、探究构成物质的微粒的性质[观察实验] 见课本中p63的“观察与思考"[现象记录] 【实验1】说明氨水能使酚酞试液变_____。
第三章《物质构成的奥秘》中考复习

• 知识回顾 :
• 考点5 化合价与化学式
• 常见元素化合价(记口诀)
• 在化合物中,氢元素通常显 价,氧元素通常显 价。
• 2、用
表示纯净物组成的式子叫化学式。
• 1、化合物中,元素的正价与负价代数和为 ,据此可依据化 学式推断元素的化合价和根据化合价检查化学式书写是否正确。
• 2、根据 可计算相对分子质量,各元素的质量比及其某元 素的质量分数。
+17 2 8 7
+8 2 6
+19 2 8 8 1
+18 2 8 8
•
A.
B. C.
D.
二、典型题
• 例3.保持氢气化学性质的粒子是( )
• A H B H20 C H2 D 2H
• 例4.下列符号只有微观意义的是( )
A.Cl2 B.2N2
C.Cu D.CO2
• 例5. 由解放军某研究所研制的小分子团水是
• (A)Ti可以表示一个钛原子 (B)Ti4+核外有26个电子 • (C)TiO2中含有氧分子 (D)CaTiO3属于金属氧化物
• 例6. 由我国著名科学家、中国科学院院士张青莲教授主 持测定了铟、铱、锑、铕等几种元素的相对原子质量新 值,其中他测定核电荷数为63的铕元素的相对原子质量 的新值为152。则下列说法正确的是
(7)四个四氧化三铁分子(4Fe3O4) (8)3个亚铁离子(3Fe2+)
1. 某元素A的原子结构示意图为
该元素原子的核电荷数为 16
,
原子的最外层电子数是 6
,A属 非金属
元
素。(填金属、非金属或稀有气体),A原子通过得失电子而形成
的离子的符号是 S2-
人教版九年级化学第三章复习《物质构成的奥秘》(共21张PPT)

C.50
D.272
16 3 2、某原子结构示意图如右,该原子的核电荷数为_____,核外有______ 8 6 个电子层,第二层上有______个电子,最外层上有______个电子。该
原子在化学变化中容易_得___到__(“得到”或“失去”)电子。
+16 28 6
四.离子的形成 钠 + 氯气 Na Cl2
课题3元素
一、元素
质子数相同的一类原子的总称元素是宏观概念,只 概念: 讲种类,不讲个数。
金属元素:Fe、Cu、Al、Au…… 分类: 非金属元素:O、H、N、Cl……
意义:
稀有气体元素;He、Ne、Ar…… 宏观: 表示一种元素或一种物质 微观: 表示该元素的一个原子
符号: 用元素拉丁文名称的第一个大写字母来表示,若几种元素的 第一个字母相同时,就附加一个小写字母来区别,这样的符 号叫元素符号。第一个字母必须大写,第二个字母必须小写。
钠原子Na +11 2 8 1
失 电 子 钠离子Na+ +11 2 8
点燃 氯化钠 NaCl
氯原子Cl
+17 2 8 7
得 电 子
+17 2 8 8 氯离子Cl-
Na+Cl- 氯化钠
Na Cl
四.离子的形成
概念:带电荷的原子(或原子团) 带负电荷的原子叫做阴离子。如:O2- 、S2-、 F-
分类: 带正电荷的原子叫做阳离子。如:H+ 、Na+、Mg2+、Al3+
芦老师的课堂
复习课
第三单元
物质构成的奥秘
课题1分子和原子
一.分子
概念:分子是保持物质化学性质的一种粒子。
沪教版九年级全册(新)第三章《物质构成的奥秘》优秀教学案例
3. 设计相关实验,让学生亲自动手操作,培养学生的实践能力,提高学生对物质构成的认识。
4. 引导学生运用分子理论分析化学现象,培养学生运用科学方法解决问题的能力。
(三)情感态度与价值观
1. 培养学生对化学学科的兴趣,激发学生探索物质世界奥秘的热情。
5. 教学内容与过程:本案例在教学过程中注重知识的系统性和连贯性,通过多媒体手段生动形象地展示原子结构、元素周期表等知识点,使学生能够更好地理解和掌握知识。同时,通过小组讨论、总结归纳等环节,巩固所学知识,提高学生的应用能力。
2. 问题导向:本案例通过设计一系列问题,引导学生自主探究物质构成的奥秘,激发学生的思维,培养学生的批判性思维和问题解决能力。
3. 小组合作:本案例将学生分成小组,进行合作研究,培养学生的团队合作精神,提高学生的沟通能力和协作能力,使学生在实践中学习和成长,培养学生的自我评价能力,激发学生的学习动力,同时教师对学生的学习成果进行评价,提供反馈,帮助学生提高。
(三)学生小组讨论
1. 布置讨论任务:“请小组成员共同探讨水是由什么组成的?”
2. 学生分组讨论,鼓励他们提出自己的观点和疑问。
3. 教师巡回指导,参与学生的讨论,解答他们的疑问。
(四)总结归纳
1. 引导学生总结本节课所学的原子结构、元素周期表、分子与化合物等知识点。
2. 强调物质构成的奥秘与现实生活的联系,激发学生的应用意识。
沪教版九年级全册(新)第三章《物质构成的奥秘》优秀教学案例
一、案例背景
沪教版九年级全册(新)第三章《物质构成的奥秘》优秀教学案例,以物质构成的奥秘为主题,旨在让学生了解物质的微观构成,探索物质世界的奥秘。本章节内容主要包括原子结构、元素周期表、分子与化合物等知识点,涉及学科为化学。
2024年中考化学一轮复习导学案:《第3章 物质构成的奥秘》
《第3章物质构成的奥秘》复习教学案【复习目标】1、知道分子、原子、离子的联系和区别;会用微粒知识解释一些问题。
2、能从组成上区分纯净物和混合物、单质和化合物,从组成上区分识别氧化物;3、了解元素的概念、意义;化学式的含义,能正确书写物质的化学式,能根据化学式进行有关计算。
4、熟记常见元素的化合价,掌握化合价的原则及其应用;【复习重点】化学式的书写和应用【自主复习】围绕知识结构网络,复习并记熟第三章知识点,准备默写!!【课堂活动】活动一、物质的构成和组成1、分子、原子、离子有哪些相同点?有哪些不同点?联系怎样?2、用微粒的知识解释化学变化和物理变化?混合物和纯净物?3、原子结构怎样?4、相对原子质量如何计算?相对分子质量如何计算?例题1、对下列事实的解释,不合理的是()A.通过气味辨别氮气和氨气分子是运动的,不同分子的性质不同B.氧气经压缩储存在钢瓶中压强增大,分子之间的间隔变小C.干冰升华为二氧化碳气体状态变化,分子大小随之变化D.蔗糖在热水中溶解更快温度越高,分子运动速率越大例题2、某反应前后分子变化的微观示意图如下,下列说法正确的是()A.反应物与生成物共有5种物质B.反应后原子的个数增多C.该图可示意SO2与O2的反应D.该反应属于分解反应例题3、从分子的角度分析并解释下列事实,不正确的是()选项事实解释A 碘酒是混合物由不同种分子构成B 端午时节粽飘香分子在不断运动着C 气体受热膨胀温度升高,分子自身体积增大D 固体碘受热升华碘分子间的间隔变大例题4、铈(Ce)是一种常见的稀土元素,已知铈原子的原子核内有58个质子和82个中子,该原子的核外电子数为()A.24 B.58 C.82 D.140活动二、元素与化学式1、元素与原子的区别和联系?2、自然界中元素分布怎样?3、元素符号和化学式表示的含义有哪些?4、单质和化合物化学式如何书写?5、化学符号周围的数字含义相同吗?各代表意义是什么?例题5、某同学对有关化学符号中数字的含义有如下理解,其中错误的是 ( )A .Ca 2+中的“2”表示一个钙离子带两个单位正电荷B .2CO 中的“2”表示两个一氧化碳分子C .Mg +2O 中的“2”表示氧化镁中镁元素的化合价为+2价D .CO 2中的“2”表示一个氧分子由两个氧原子构成例题6、下列化学用语既能表示一种元素,又能表示一个原子,还能表示一种物质的是( )A .H 2B .AlC .OD .CH 3OH活动三、化学式的应用A aB b 的相对分子质量=a ×A 的相对原子质量+b ×B 的相对原子质量A 元素的质量B 元素的质量=a ×A 的相对原子质量b ×B 的相对原子质量A 元素的质量分数=a ×A 的相对原子质量A aB b 的相对分子质量×100% A 元素的质量=物质A a B b 的质量×A 元素的质量分数 例题7、阿司匹林分子式为C 9H 8O 4,下列关于阿司匹林说法正确是( )A .H 、O 原子个数比为1:8B .相对分子质量为180C .阿司匹林中含21种元素D .氧元素的质量分数最小例题8、据报道,“毒淀粉”是在淀粉中添加了对人体有害的马来酸(C 4H 4O 4).马来酸是无色晶体,能溶于水.下列关于马来酸的说法中正确的是( )A .马来酸属于氧化物 B .马来酸由三种元素组成 C .马来酸中碳元素的质量分数最大 D . 5%的马来酸溶液中氧元素的质量分数为2.76% 例题8、人体缺乏维生素C (简写“Vc ”)会患坏血病。
人教版初三化学第三章物质构成的奥秘知识点总结
第三单元物质构成的奇妙课题1 分子和原子一、构成物质的微粒:分子、原子、离子1、由分子构成的物质:例如水、二氧化碳、氢气、氧气等物质2、由原子构成的物质:金属、稀有气体、金刚石、石墨等物质3、有离子构成的物质:氯化钠硫酸锌4〔显著特征:含有 4 3 344等原子团〕4、物质构成的描绘:物质由××分子〔或原子、离子〕构成。
例如:铁由铁原子构成;氧气由氧分子构成。
氯化钠由氯离子和钠离子构成二、分子1、根本性质:⑴质量、体积都很小;⑵在不停地运动〔及温度有关〕。
温度越高,运动速率越快例:水的挥发、品红的扩散、闻到气味等;⑶分子间存在间隔。
同一物质气态时分子间隔最大,固体时分子间隔最小;物体的热胀冷缩现象就是分子间的间隔受热时增大,遇冷时变小的原因。
⑷同种物质间分子的性质一样,不同物质间分子的性质不同。
分子一样物质一样,分子不同物质不同2、分子的构成:分子由原子构成。
分子构成的描绘:①××分子由××原子和××原子构成。
例如:水分子由氢原子和氧原子构成②一个××分子由几个××原子和几个××原子构成。
例如:一个水分子由一个氧原子和二个氢原子构成3、含义:分子是保持物质化学性质的最小微粒。
例:氢分子是保持氢气化学性质的最小粒子,水分子是保持水的化学性质的最小粒子。
4、从分子和原子角度来区分以下几组概念⑴物理变更及化学变更由分子构成的物质,发生物理变更时,分子种类不变。
发生化学变更时,分子种类发生了变更。
〔学会从分子和原子的角度描绘物理变更和化学变更〕⑵纯净物及混合物由分子构成的物质,纯净物由同种分子构成;混合物由不同种分子构成。
⑶单质及化合物单质的分子由同种原子构成;化合物的分子由不同种原子构成。
三、原子1、含义:原子是化学变更中最小的微粒。
例:氢原子、氧原子是电解水中的最小粒子组合成新的分子。
沪教版九年级化学上册第三章《物质构成的奥秘》测试卷(含答案)
沪教版九年级化学上册第三章《物质构成的奥秘》测试卷(含答案)一、选择题1. [2021南京中考]在压强为101 kPa时,将1 L氧气置于密闭容器中降温,变为淡蓝色液体。
下列关于该过程的说法正确的是( )A.氧分子的体积变小B.氧分子的质量变小C.氧分子的数目变少D.氧分子间的间隔变小2. [2021安徽中考]富氢水指富含氢分子的水,在医学、体育等领域有重要用途。
下列有关富氢水的说法,正确的是( )A.属于纯净物B.含氢、氧两种元素C.所含氢分子不运动D.与水的性质完全相同3.硝酸铵(NH4NO3)是一种肥效较高、使用广泛的氮肥,下列关于硝酸铵中氮元素化合价的判断,正确的是( )A.-4,+6B.+1,+1C.-3,+5D.无法确定4.化学式 H2O2能表示多种意义,下列说法错误的是( )A.表示过氧化氢这种物质B.表示过氧化氢由氢元素和氧元素组成C.表示1个过氧化氢分子D.表示过氧化氢由2 个H 原子和2 个O原子构成5.下列有关化合价的说法中,正确的是( )A.在NaCl和HCl中,氯元素均为-1价B.在原子团N O3-中,各元素化合价代数和为零C.一种元素在同一种化合物里,一定显相同的化合价D.非金属元素在化合物里,一定显负价6. [2021成都中考改编]下列化学用语表达正确的是( )A.P +52O 5:磷元素在五氧化二磷中显+5价B.2O 3: 6个氧原子C.氯化钠:ClNaD.铜离子:Cu +7. [2021河北中考]氮化镓是生产5G 芯片的关键材料之一。
氮的原子结构示意图和镓在元素周期表中的信息如图所示,下列说法错误的是( )A.镓是金属元素B.氮原子的核内质子数为7C.镓元素的相对原子质量是69.72 gD.氮化镓中氮元素的化合价为-38. [2021福建中考改编]大蒜素(C 6H 10S 2O)能抑制和杀灭多种细菌。
下列有关大蒜素的说法,错误的是( )A.氢元素的质量分数最大B.由4种元素组成C.1个分子由19个原子构成D.碳元素与氧元素的质量比为9∶29. [2021邵阳中考改编]推理是学习化学的一种常用方法,下列推理正确的是 ( )A.阴离子带负电荷,则带负电荷的粒子一定是阴离子B.单质只含一种元素,则只含一种元素的物质一定是单质C.元素的种类是由质子数决定的,则质子数相同的原子一定属于同种元素D.原子核由质子和中子构成,则原子核中一定含有中子10. 下列有关分子和原子的说法正确的是( )A.分子能保持物质的化学性质,原子不能保持物质的化学性质B.相同的原子能构成分子,不同的原子不能构成分子C.相同的原子可能构成不同的分子D.在化学变化中,分子和原子的种类都不发生改变11. [2021常德中考改编]如图是5种微粒的结构示意图,下列说法不正确的是( )A.上述5种微粒只涉及4种元素B.②③⑤表示的微粒性质较稳定C.①②④属于原子,③⑤属于阴离子D.④⑤对应元素组成化合物的化学式为NaCl二、非选择题12. 依据下列化学符号中数字“2”所表示的意义,把符合题意的序号填在横线上。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第3章《物质构成的奥秘》测试卷一.选择题(共25小题)1.从分子的角度解释下列现象,错误的是()A.花香四溢﹣﹣分子不断运动B.一滴水约有1.67×1021个水分子﹣﹣分子很小C.氢气燃烧﹣﹣分子发生变化D.汽油挥发﹣﹣分子体积变大2.下列对原子、分子、离子的认识,错误的是()A.分子由原子构成,原子是不能再分的最小粒子B.相同原子可以构成不同的分子C.在原子中,原子核内的质子数等于核外电子数D.分子、原子、离子都是构成物质的粒子3.建立宏观与微观的联系是化学常用的思维方式。
下列是对宏观事实的微观解释,错误的是()A.八月桂花飘香﹣﹣分子在不断地运动B.干冰升华﹣﹣分子间的间隔变大了C.电解水生成氢气和氧气﹣﹣水中含有氢分子和氧分子D.硫在氧气中燃烧比空气中更剧烈﹣﹣在氧气中硫接触到的氧分子更多4.小明同学对探究分子性质的实验(图1)进行了改进,如图2所示,在T形三通管的粗玻璃管里,固定一根湿润的酚酞纱布条,将浓氨水滴入T形三通管的细弯管处,然后用橡皮帽封闭管口。
一会儿,就观察到ba段纱布条变成红色。
以下有关实验的说法错误的是()A.图2比图1的实验更环保、更节约B.图2中bc段纱布始终不会变红C.图1和图2的实验均能证明分子在不断的运动D.若将图2中装有浓氨水的细弯管处浸入冰水中,纱布变红的时间会变长5.推理是学习化学的一种重要方法,下列推理正确的是()A.质子和中子构成原子核,则原子核都是由质子和中子构成B.物质都是由元素组成,同种元素可以组成纯净物,则不同种元素只可以组成混合物C.同种分子的化学性质相同,则不同种分子的化学性质一定不同D.分子、原子不显电性,由他们构成的物质也不显电性,而离子带电,则由离子构成的物质是显电性的6.物质都是微观粒子构成的,下列说法错误的是()A.在化学变化中,分子可以再分,而原子不可再分B.带正电的离子是阳离子C.只有分子能构成物质D.质子数相同的一类原子属于同种元素7.有一种铀原子核内有92个质子、143个中子,则该铀原子的核外电子数是()A.235B.143C.92D.518.镆(Mc)是115号元素,该元素名称与2017年5月9日正式发布,镆有多种同位素原子,如Mc﹣288和Mc﹣287等,下列关于镆的说法正确的是()A.Mc﹣288中含有115个中子B.Mc﹣288和Mc﹣287最大的不同是质子数不同C.Mc﹣287中含有115个电子D.镆原子如果失去1个电子则可以变成另一种元素9.下列物质中含有氧分子的是()A.水B.河水C.二氧化锰D.氯酸钾10.菠菜、红萝卜富含铁,这里的“铁”指的是()A.分子B.原子C.元素D.离子11.地壳中含量最多的元素是()A.Si B.O C.Cl D.Al12.某同学认为“O2”表示的意义有以下几种说法:①表示氧元素;②表示氧气这种物质;③表示1个氧分子;④表示2个氧原子;⑤表示氧气是一种无色气体;⑥表示1个氧分子里有2个氧原子。
其中正确的是()A.②④⑤B.②③⑥C.②③④⑤D.②③⑤⑥13.下列各组都是非金属元素的是()A.S、Si、Fe B.P、H、O C.Cu、C、Cl D.Al、C、Ca 14.陈女士在微商处购买了一款价格高昂的美白系列化妆品,使用后脸部发生溃烂,经相关机构检测发现该化妆品中汞元素远远超过安全值。
下列关于汞元素的说法正确的是()A.是非金属元素B.相对原子质量是200.6gC.质子数为80D.与其他元素的根本区别是中子数不同15.如图是某元素的原子结构示意图和该元素周期表中的单元格,下列说法不正确的是()A.该元素属于金属元素B.m=10C.该原子的大小主要决定与核外电子的运动空间D.该原子的相对原子质量为47.87g16.水被称为“生命之源”,双氧水被称为“绿色氧化剂”.下列关于它们的说法正确的是()A.都含有2个氢原子B.都含有氢元素C.都含有氢分子D.都含有氢气17.分子是构成物质的一种分子,下列有关水分子的叙述正确的是()A.“冰、水为之而寒于水,说明水和冰是两种物质B.降温时水分子的化学性质发生变化C.发生化学变化时构成水分子的原子种类发生变化D.电解水生成H2和O2说明水分子可分18.根据下列原子结构示意图,判断其化学性质相似的元素是()A.①和②B.②和③C.③和④D.①和⑤19.下列关于Na、Na+两种粒子的判断,①核电荷数相同;②核外电子数相等;③化学性质相似;④质量几乎相等;⑤质子数相等;⑥Na+比Na稳定,其中正确的是()A.①④⑤⑥B.①③④⑤⑥C.①④⑤D.②③④20.下列有关分子、原子、离子说法中,正确的是()A.原子是自然界中最小的粒子B.分子是化学变化中最小的粒子C.所有原子的原子核都由质子、中子构成D.分子、原子不显电性,离子显电性21.钚是第94号元素,钚﹣238原子的中子数为144,下列说法错误的是()A.钚属于金属元素B.钚原子质子数为94C.钚原子核外电子数为144D.常用的钚相对原子质量为23822.下列关于分子、原子的一些叙述正确的是()①原子只能构成分子,分子才能构成物质;②分子是可分的,而原子是不能再分的;③分子有一定大小和质量,而原子没有;④同种分子的性质相同,不同种分子的性质不同;⑤原子是化学变化中的最小粒子;⑥分子和原子都永远处于不同的运动状态;⑦分子、原子之间都有一定间隔.A.④⑤⑥⑦B.①②③④C.①③⑤⑦D.②④⑤⑥23.关于CO2、SO2、NO2、O2四种物质中,叙述正确的是()A.都含氧分子B.都含氧元素C.都含2个氧原子D.都含氧气24.下列化学符号既表示该种元素,又表示该种元素的一个原子,还可以表示该种物质的是()A.O B.H2 C.He D.H2O25.不同元素之间最本质的区别是()A.质子数不同B.中子数不同C.电子数不同D.质量大小不同二.填空题(共8小题)26.将分子、原子、原子核、质子、中子或电子,分别填入下列有关空格内:(1)构成物质的粒子有多种,有的物质是由构成的,如铁、汞等;有的物质是由构成的,如氮气、水等.(2)氧化汞是保持氧化汞化学性质的最小粒子,在化学变化中,氧化汞分解成汞和氧,汞直接构成汞,每两个氧构成一个氧,无数个氧构成氧气.(3)氧原子中心有一个带8个单位正电荷的,核外有8个在一定范围的空间里作高速运动,由于每个带一个单位负电荷,每个带一个单位正电荷,不带电,所以整个不显电性.(4)由于和的相对质量约为1,氧的相对原子质量为16,可知氧的原子核内有8个和8个个中子.27.化学兴趣小组的同学在探究分子的特征时设计了如图所示的实验,请你参与他们的探究活动,回答有关问题:烧杯A中盛有10mL浓氨水;在烧杯B、C中分别盛有20mL蒸馏水,并分别滴加3滴酚酞试液于蒸馏水中,得到无色溶液。
用只大烧杯把A、B两烧杯罩在一起,几分钟后,观察现象。
(1)实验中观察到的现象是。
请你用分子的知识解释出现该现象的原因。
(2)由该实验可知氨水具有的性质是:。
(3)实验中烧杯C的作用是。
(4)该装置有一个明显的不足之处是,你的改进建议是。
28.在分子、原子、原子核、质子、中子、电子这些粒子中选择符合条件的填在相应的横线上。
(1)能保持氧气化学性质的是氧,能保持铁的化学性质的是铁;(2)化学变化中最小的粒子是;(3)不显电性的是。
29.如图是金属钠和氯气反应生成氯化钠的徵观示意图,根据图示回答下列问题。
(1)钠原子在反应中(填“失去”、“得到”)电子;(2)构成氯化钠的粒子是;(3)由原子核外电子层数与元素所在周期表中的周期数相同可知,氯元素在元素周期表中应排在第周期。
30.请用微观的知识回答下列问题.(1)钠原子和钠离子两者的化学性质不同是因为(2)H2O和H2O2化学性质不同的原因是.31.用“分子”、“原子”“元素”“离子”填入下列空格.(1)水是由水构成(2)铜是由铜组成(3)氧气是由氧构成(4)氧分子是由氧构成(5)氯化钠是由钠和氯构成.32.用化学符号填空:(1)地壳中含量最多的元素是;(2)生物体含量最多的金属元素是;(3)地壳中含量最多的金属元素是,其次是。
33.据《自然》杂质报道,科学家研制出一种以元素锶的原子做钟摆的钟是世界上最精确的钟。
如图A是锶元素在周期表中的相关信息,如图B是锶元素形成的一种粒子的结构示意图。
(1)锶元素的相对原子质量为。
(2)图B中X=,该粒子的符号是。
(3)如图1表示的微粒中,与Sr化学性质相似的是(填序号)。
三.实验探究题(共1小题)34.图Ⅰ是小娅按课本进行的一个化学实验,在实验时同学们闻到了一股难闻的刺激性气味。
于是小明对原实验装置进行了改进,装置如图Ⅱ。
【实验操作】a.向B、C、E三支试管分别加入5mL的蒸馏水,各滴入1~2滴无色酚酞溶液,振荡,观察溶液颜色b.在A、D试管中分别加入2mL浓氨水,立即用带橡皮塞的导管按实验图Ⅱ连接好,并将D试管放置在盛有热水的烧杯中,观察几分钟。
【分析讨论】:(1)E试管放有酚酞溶液的目的是;(2)进行操作b时观察到的现象是;(3)由此可以得到的有关分子的性质是①;②;(4)对比改进前的实验,改进后实验的优点是。
(5)小婷认为还需加对比试验排除是水是否参加反应的干扰,你认为小婷的说法(填正确或错误)理由是。
四.解答题(共1小题)35.在分子、原子、原子核、质子、中子、电子等粒子中,找出符合下列条件的粒子,填在相应的横线上:(1)能保持物质化学性质的粒子是.(2)化学变化中的最小粒子是.(3)带正电荷的粒子是.(4)不显电性的粒子是.(5)决定原子质量大小的粒子主要是.。
