甲烷
甲烷

资料ata
二、甲烷的分子组成和结构
分子式:CH4
H
H
电子式: H C H
H
结构式:H C H
H
结构式:用短线来表示一对共用电子的图式
问题:从甲烷的电子式是否可以推断甲烷分子中 碳原子和四个氢原子都在同一个平面上?
甲烷分子的空间结构
球棍模型
比例模型
立体结构: 正四面体型,C原子位于中心,四个H 原子位于正四面体的四个顶点。 4个C-H键的键 长和强度相等,夹角相等(键角是109028/)。
乙烷
HHH ||| H-C-C-C-H || | HH H
丙烷
几种烷烃的球棍模型及对应的结构式
丁烷
丁烷:H H H H
|||| H-C-C-C-C-H
|||| HHHH
异丁烷
异丁烷:
H |
H--C--H
H
H
|
|
H-C——C——C-H
||
|
HH H
相同点
只含C、H两种元素,每个碳以 四个单键与其它原子相结合。
构的现象叫同分异构现象。 具有同分异构现象的化合物互称为同分异
构体。
正丁烷和异丁烷互为同分异构体。
正戊烷、异戊烷和新戊烷互为同分异构体。
C5H12
CH3CH2CH2CH2CH3
CH3CHCH2CH3 CH3
CH3 CH3CCH3
CH3
问:三种物质的沸点是否相同? 正>异>新
一般带有支链越多的同分异构体,熔沸点越低
2
③取代反应,在光照条件下进行,产物更复杂
例如: CH 3CH 3 Cl 2 光照 会产生9种取代产物。
一氯取代反应的通式:
甲烷
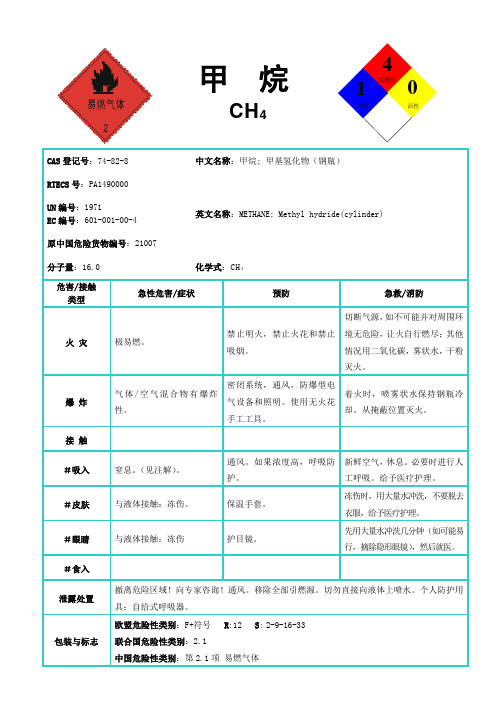
易燃性41活性毒性甲 烷CH 4CAS 登记号:74-82-8 中文名称:甲烷; 甲基氢化物(钢瓶) RTECS 号:PA1490000UN 编号:1971EC 编号:601-001-00-4 英文名称:METHANE; Methyl hydride(cylinder) 原中国危险货物编号:21007分子量:16.0 化学式:CH 4危害/接触 类型急性危害/症状 预防 急救/消防火 灾 极易燃。
禁止明火,禁止火花和禁止吸烟。
切断气源,如不可能并对周围环境无危险,让火自行燃尽;其他情况用二氧化碳,雾状水,干粉灭火。
爆 炸气体/空气混合物有爆炸性。
密闭系统,通风,防爆型电气设备和照明。
使用无火花手工工具。
着火时,喷雾状水保持钢瓶冷却。
从掩蔽位置灭火。
接 触#吸入窒息。
(见注解)。
通风。
如果浓度高,呼吸防护。
新鲜空气,休息。
必要时进行人工呼吸。
给予医疗护理。
#皮肤 与液体接触:冻伤。
保温手套。
冻伤时,用大量水冲洗,不要脱去衣服,给予医疗护理。
#眼睛 与液体接触:冻伤 护目镜。
先用大量水冲洗几分钟(如可能易行,摘除隐形眼镜),然后就医。
#食入泄露处置撤离危险区域!向专家咨询!通风。
移除全部引燃源。
切勿直接向液体上喷水。
个人防护用具:自给式呼吸器。
包装与标志 欧盟危险性类别:F+符号 R :12 S : 2-9-16-33联合国危险性类别:2.1 中国危险性类别:第2.1项 易燃气体应急响应运输应急卡:TEC(R)-20G1F。
美国消防协会法规:H1(健康危险性);F4(火灾危险性);R0(反应危险性)储存耐火设备(条件)。
阴凉场所。
沿地面和天花板通风。
重要数据物理状态、外观:无色压缩或液化气体,无气味。
物理危险性:气体比空气轻。
职业接触限值:阈限值:(C1-C4链烷烃气体)1000ppm(时间加权平均值)(美国政府工业卫生学家会议,2005年)。
最高容许浓度未制定标准。
接触途径:该物质可通过吸入吸收到体内。
甲烷完整PPT课件

目录
• 甲烷基本概念与性质 • 甲烷制备方法与工艺流程 • 甲烷燃烧反应与能量转换原理 • 甲烷储存运输技术发展现状与挑战 • 甲烷在工业生产和生活中应用案例 • 实验操作注意事项与安全防护措施
01
甲烷基本概念与性质
甲烷定义及分子式
甲烷定义
最简单的有机化合物,由碳和氢 元素组成。
燃烧反应方程式及条件
甲烷燃烧反应方程式
CH4 + 2O2 → CO2 + 2H2O
燃烧条件
需要足够的氧气供应和一定的点燃温度。
能量转换原理及效率分析
能量转换原理
甲烷燃烧时,化学能转化为热能和光 能。
效率分析
燃烧效率受氧气供应、燃烧温度、燃 烧室设计等因素影响,高效燃烧技术 可提高能量转换效率。
环保性能评估及排放标准
与卤素单质发生取代反应,生成卤代 烃。
甲烷在自然界中存在形式
天然气
甲烷是天然气的主要成分,广泛存在于地下 岩石储层中。
沼气
在沼泽地带、污水沟、动物粪便等环境中, 由微生物发酵产生。
煤层气
赋存在煤层中的甲烷,以吸附状态存在于煤 基质颗粒表面。
重要性及应用领域
能源领域
作为燃料,广泛应用于 民用、工业、交通等领
Байду номын сангаас域。
化工原料
用于生产合成氨、甲醇 、甲醛等化工产品。
温室气体
甲烷是一种重要的温室 气体,对全球气候变化
有重要影响。
其他应用
用作制冷剂、发泡剂等 。
02
甲烷制备方法与工艺流程
天然气分离法
01
02
03
天然气成分及性质
天然气主要由甲烷组成, 同时含有少量乙烷、丙烷 等烃类以及硫化氢、二氧 化碳等非烃类成分。
甲烷知识介绍

甲烷知识介绍甲烷在自然界的分布很广,甲烷是最简单的有机物,是天然气,沼气,坑气等的主要成分。
也是含碳量最小(含氢量最大)的烃,也是天然气、沼气、油田气及煤矿坑道气的主要成分。
它可用来作为燃料及制造氢气、碳黑、一氧化碳、乙炔、氢氰酸及甲醛等物质的原料。
甲烷,化学式CH4,是最简单的烃,由一个碳和四个氢原子通过sp3杂化的方式组成,分子结构呈正四面体结构,四个键的键长相同键角相等。
在标准状态下甲烷是一无色无味气体。
一些有机物在缺氧情况下分解时所产生的沼气其实就是甲烷。
甲烷主要是作为燃料,如天然气和煤气,广泛应用于民用和工业中。
作为化工原料,可以用来生产乙炔、氢气、合成氨、碳黑、硝氯基甲烷、二硫化碳、一氯甲烷、二氯甲烷、三氯甲烷、四氯化碳和氢氰酸等。
天王星的大气层也存在甲烷和氢气。
据德国核物理研究所的科学家经过试验发现,植物和落叶都产生甲烷,而生成量随着温度和日照的增强而增加。
另外,植物产生的甲烷是腐烂植物的10到100倍。
他们经过估算认为,植物每年产生的甲烷占到世界甲烷生成量的10%到30%。
行星中发现甲烷据国外媒体报道,美国天文学家19日宣布,他们首次在太阳系外一颗行星的大气中发现了甲烷,这是科学家首次在太阳系外行星探测到有机分子,从而增加了确认太阳系外存在生命的希望。
该小组还证实了先前的猜测,即这颗名叫HD 189733b的行星的大气中有水。
甲烷是创造适合生命存在的条件中,扮演重要角色的有机分子。
美国宇航局喷气推进实验室的天文学家,利用绕轨运行的“哈勃”太空望远镜得到了一张行星大气的红外线分光镜图谱,并发现了其中的甲烷痕迹。
甲烷最基本的氧化反应就是燃烧:CH4+2O2→CO2+2H2O甲烷的含氢量在所有烃中是最高的,达到了25%,因此相同质量的气态烃完全燃烧,甲烷的耗氧量最高。
点燃纯净的甲烷,在火焰的上方罩一个干燥的烧杯,很快就可以看到有水蒸气在烧杯壁上凝结。
倒转烧杯,加入少量澄清石灰水,振荡,石灰水变浑浊。
甲烷

3、甲烷分子中的四个氢原子可逐一被取代, 故甲烷的卤代物并非一种,而是4种卤代物的混合物。
CH4 + Cl2
光
CH3Cl + HCl
一氯甲烷(无色气体)
CH3Cl + Cl2 光 CH2Cl2 + HCl 二氯甲烷
石灰水变浑浊, 证明有CO2生成。
温州网讯----2007年鹿城区黄龙街道双桥
村上一窨井“发火”,一路人不幸坠入窨井,脸上
都是血,头发、眉毛已被烧焦,衣裤也被炸烂。窨井
边注的意路面: 点被燃震甲得多烷处前龟必裂须,验几纯十,公斤否重则的会窨爆井炸盖。飞出 10多米远(思,考摔:成两什半么。时一候目甲击烷者会说,爆当炸时最窨强井烈盖?飞) 起
16gx25℅ 1g/mol
=4mol
CH4
交流与讨论:
2.写出甲烷分子的分子式,电子式和结构式
分子式
电子式
结构式
CH4
空间立体结构:
键角 109°28′
球棍模型
科学实验证明:甲烷分子呈正四面体结构, C原子位于正四面体的中心,
四个氢原子位于正四面体的顶点上。
C—H键的键长和键ຫໍສະໝຸດ (109°28′)相同。反应物 生成物 电子转移
反应特点
有机物+单质 有机物+HX
一般生成两种化合物 没发生电子转移, 不是氧化还原反应 很多反应是可逆反应, 副反应较多,用“→” 连接
置换反应
Zn+H2SO4=ZnSO4+H2↑ 单质跟化合物反应,生成 另一种化合物和单质的反应。
一种单质和一种化合物
甲烷化学知识点总结

甲烷化学知识点总结1. 结构特点甲烷的分子结构呈正四面体形,碳原子位于正四面体的中心,四个氢原子位于四个顶点上。
由于甲烷分子的结构稳定,碳-碳和碳-氢的键的键长和键角都是固定的,这也是甲烷分子具有特殊性质的原因之一。
2. 物理性质甲烷是一种无色、无臭的气体,在常温常压下为气体态,但在极低温下可以冷凝成液体或固体。
甲烷的密度小于空气,燃烧时产生的气体比空气轻,容易聚集在上部,具有爆炸危险。
甲烷具有较高的燃烧热值,是一种常用的燃料。
3. 化学性质(1)燃烧反应甲烷是一种良好的燃料,在氧气的存在下能够发生燃烧反应产生二氧化碳和水。
甲烷的燃烧是一个放热反应,生成的燃烧热可以被利用作为能源。
CH4 + 2O2 → CO2 + 2H2O(2)氧化反应当甲烷与氧气在高温条件下反应时,可以生成一氧化碳和水。
2CH4 + 3O2 → 2CO + 4H2O这是一种不完全燃烧反应,生成的一氧化碳具有毒性,会对环境和人体健康造成危害。
(3)氧化反应在空气中,甲烷还可以与氮气发生氧化反应,生成一些氮氧化物。
这些氮氧化物是大气中的污染物之一,对环境具有一定的危害。
CH4 + 2N2 → 2N2O + N24. 化学反应(1)卤代反应由于甲烷分子中的碳原子电负性较小,碳-氢键的键能较高,因此甲烷分子不容易进行化学反应。
但在适当的条件下,如在紫外光的照射下,可以进行卤代反应。
CH4 + Cl2 → CH3Cl + HCl(2)氧化反应在高温或催化剂的作用下,甲烷可以氧化成一氧化碳、二氧化碳和水等产物。
CH4 + O2 → CO + 2H2OCH4 + 2O2 → CO2 + 2H2O(3)加成反应甲烷还可以通过加成反应与其他烃类发生反应,生成更复杂的有机化合物。
CH4 + C2H4 → C2H6这些化学反应使得甲烷可以作为重要的有机合成原料,在化工领域有着广泛的应用。
5. 生产工艺目前,甲烷的生产主要有天然气提取和合成气制甲烷两种途径。
甲烷知识

简介:甲烷是无色,无味,易燃烧气体,窒息性的气味。
钢瓶装高压压缩气体。
溶解性:微溶于水,溶于醇、乙醚。
,密度(标准状况)0.717克/升,沸点-161.5℃,熔点-182.48℃。
燃烧热(kJ/mol):889.5、临界温度(℃):-82.6、临界压力(MPa):4.59。
闪点(℃):-188、引燃温度(℃):538。
在一定条件下,甲烷能发生卤代反应(Cl2,Br2)和热分解(分解成C、H2、C2H2等)等反应。
甲烷燃烧时火焰呈青白色。
沼气、坑气、天然气的主要成分是甲烷。
天然气中的甲烷经低温和加压液化,可以用特殊船舶越洋运输。
甲烷的化学性质甲烷性质稳定,跟酸性KMnO4溶液或溴水均不发生反应。
点燃甲烷和空气的混合气会发生爆炸。
甲烷在空气里的爆炸极限是5.3~14.0%(体积),在氧气里的爆炸极限是5.4~59.2%(体积)。
商品详细工业甲烷纯度规格电子气纯度规格甲烷的应用甲烷用作热水器、燃气炉热值测试标准燃料甲烷用于生产可燃气体报警器的标准气,校正气甲烷用作太阳能电池,非晶硅膜气相化学沉积的碳源甲烷用作医药化工合成的生产原料注意事项甲烷本身对人体没有特殊毒作用,只是在浓度高时有麻醉效应。
当空气中含量大时,也能造成缺氧、窒息,引起中毒症状。
当甲烷浓度大于10%时产生眼睛和前额的受压感,浓度更高时,开始出现呼吸急促、疲劳、恶心、呕吐等窒息症状,并能导致失去知觉。
泄漏气体时,要用强制通风的方法使其浓度在爆炸范围以下。
漏气的钢瓶如果无法堵漏,则要转移到空旷地方放宅,或者装适当的灯头燃烧。
瓶装气体产品为高压充装气体,使用时应经减压降压后方可使用。
包装的气瓶上均有使用的年限,凡到期的气瓶必须送往有部门进行安全检验,方能继续使用。
每瓶气体在使用到尾气时,应保留瓶内余压在0.5MPa,最小不得低于0.25MPa 余压,应将瓶阀关闭,以保证气体质量和使用安全。
瓶装气体产品在运输储存、使用时都应分类堆放,严禁可燃气体与助燃气体堆放在一起,不准靠近明火和热源,应做到勿近火、勿沾油腊、勿爆晒、勿重抛、勿撞击,严禁在气瓶身上进行引弧或电弧,严禁野蛮装卸。
甲烷知识点

第三章 有机化合物第一节 甲烷知识点一 有机物一、有机化合物:绝大多数含碳的化合物称为有机化合物,简称有机物。
像CO 、CO 2、碳酸、碳酸盐、金属碳化物、金属氰化物等少数化合物,由于它们的组成和性质跟无机化合物相似,因而一向把它们作为无机化合物。
性质和反应 有机物无机物溶解性 多数不溶于水,易溶于有机溶剂,如油脂溶于汽油,煤油溶于苯。
多数溶于水,而不溶于有机溶剂,如食盐、明矾溶于水。
耐热性 多数不耐热;熔点较低,(400°C 以下)。
如淀粉、蔗糖、蛋白质、脂肪受热分解;C 20H 42熔点36.4°C,尿素132°C 。
多数耐热难熔化;熔点一般很高。
如食盐、明矾、氧化铜加热难熔,NaCl 熔点801°C 。
可燃性 多数可以燃烧,如棉花、汽油、天然气都可以燃烧。
多数不可以燃烧,如CaCO 3、MnCl 2不可以燃烧。
电离性 多数是非电解质,如酒精、乙醚、苯都是非电解质、溶液不电离、不导电。
多数是电解质,如盐酸、氢氧化钠、氯化镁的水溶液是强电解质。
化学反应一般复杂,副反应多,较慢,如生成乙酸乙酯的酯化反应在常温下要16年才达到平衡。
石油的形成更久一般简单,副反应少,反应快,如氯化钠和硝酸银反应瞬间完成。
二、有机物的主要特点大多数有机物属于分子晶体,1、难溶于水易溶于酒精、汽油、苯等有机溶剂。
2、易燃烧。
3、大多数是非电解质,难电离。
4、熔点低,易熔化。
5、反应慢、反应复杂、副反应多。
6.不易导电有机反应比较复杂,反应速率慢,一般需加热或使用催化剂,常伴有副反应,因而所得产品往往是混合物。
三、有机物中碳的成键特征1. 有机物中都含有碳原子,碳原子有4个价电子,每个碳原子不仅能与其他原子形成4个共价键,而且碳碳之间也可以以共价键相结合形成可长可短的碳链;碳链可以是直链或带直链或形成环状。
2. 在有机化合物中,碳原子的4个价电子全部参与成键,它总是形成4个键,其成键方式为或或注:有机物种类繁多主要是由碳原子的成键特点和碳原子间的结合方式决定的。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第五章
烃
1、定义:仅含碳和氢两种元素的有机物称 为碳氢化合物,又称烃。 2、种类:根据结构不同, 可分为烷烃、烯烃、炔 烃、芳香烃等。
第一节 甲 烷
一、甲烷的组成与结构
经过科学实验证明甲烷分子的结 构是正四面体结构,碳原子位于正四 面体的中心,4个氢原子分别位于正四 面体的4个顶点上(键角是109028/)。
[例4] 在光照条件下,将等物质的 量的甲烷与Cl2充分反应,得到的混 合物中物质的量最多的物质是 [ D ] A.CH3Cl B.CH2Cl2 C.CCl4 D.HCl
[例5] 将20mL0.1mol/L的NaOH溶液与 10mL0.1mol/L醋酸混合后加强热,最后得 到的固体是 [ D ] A.NaOH B.NaOH和CH3COONa C.CH3COONa D.Na2CO3
二、有机物的主要性质特点
1、大多数有机物难溶于水,易溶于有机溶剂。
2、绝大多数有机物受热容易分解,而且容易燃烧。 3、绝大多数有机物不易导电,熔点低。 4、有机物的反应复杂,一般比较慢,常常伴 有副反应发生。 有机物的以上性质特点与其 结构 密切相关。
比较尿素和碳酸
结构简式:
尿素
碳酸
分子式:
CO(NH2)2
1、氧化反应:
甲烷与高锰酸钾不发 生反应,也不与溴水 发生反应。
2、受热分解: 在隔绝空气的情况下,加热至 10000C,甲烷分解生成炭黑和氢气。
3、取代反应:
有机物分子里的某些原子或原子团被其他原子 或原子团所代替的反应叫做取代反应
取代反应与置换反应的比较
取代反应
可与化合物发生取代, 生成物中不一定有单质
例8、把体积相同的甲烷和氯气充入 一个集气瓶中,光照一段时间后,发 现气体的黄绿色变浅,集气瓶壁上有 淡黄绿色液滴,此时,集气瓶内的物 质最多可能有[ D ] A.四种 B.五种 C.六种 D.七种
例9、.下列事实中能证明甲烷分 子是以碳原子为中心的正四面体 结构的 [ C ] A.CH2Cl2有两种不同的结构 B.在常温常压下CH2Cl2是液体 C.CH2Cl2只有一种空间结构 D.CH2Cl2是一种极性分子
发展材料
课堂练习
1、下列物质中属于有机物的是:( B 2、下列说法中不正确 的是:(
、C )
)
A、二氧化碳 B、尿素 C、酒精 D、碳酸氢铵
B
A、大多数有机物 难溶于水,易溶于汽油、酒精、苯等有 机溶剂。
B、有机物的熔点低,受热易分解,都能燃烧。
C、绝大多数有机物是非电解质,不易导电。
D、有机物的化学反应比较复杂,一般较慢,且常伴有副 反应发生。
已知有一化合物仅含碳氢两种元素,碳氢质量 比是9:2,在标准状况下,密度为1.964克/升, 试写出该化合物的分子式。
典型例习题
[例1] 、下列有关有机化合物组成的叙 D 述正确的是[ ] A.所有含碳元素的物质都是有机化合物 B.有机化合物指所有的含碳化合物 C.CO、CO2是含碳化合物,所以它们是 有机化合物 D.有机物中一定含碳元素
H2CO3
无机物
有机物
结论: 有机物和无机物并无绝对的界限。
原因: 1、碳原子含有4个价电子,可以跟其它原子 形成4个共价键;
.. C H H: : ..
H
H
H
H
C
H
H
2、碳原子相互之间能以共价键结合形成长的碳链。
ห้องสมุดไป่ตู้
C
C
C C C
C C C C
C C C
裨益健康 增产食物
增加能源
化学—中心学科
改善环境
有机物
阅读与思考
1、什么是有机物?其组成元素有哪些? 2、有机物与无机物是否为毫无关系的两类物质? 3、有机物种类繁多的原因何在? 4、有机物有哪些特点?这些特点与什么密切相关? 5、有机物对发展国民经济和提高人民生活具有 什么意义?
一、什么叫有机物?
含有碳元素的化合物为有机物。 1、定义: ( 但碳的氧化物、碳酸、碳酸盐、 碳的金属化合物等看作无机物。) 2、组成元素:碳、氢、氧、氮、硫、磷、卤素等 主要元素 其他元素
例10、某种甲烷和氢气的混合气体VL, 完全燃烧需要氧气的体积在相同状况 下也是VL,则原混合气体中,甲烷和 氢气的体积比是 [ ] B A.1∶1 B.1∶2 C.2∶1 D.3∶1
二、甲烷的物理性质
甲烷是无色、无臭的气 体,密度是0.717g/L(标准 状况),极难溶于水。 甲烷是池沼底部产生的 沼气和煤矿的坑道所产生的 气体的主要成分。这些甲烷 都是在隔绝空气的情况下, 由植物残体经过微生物发酵 的作用而生成的。
三、甲烷的化学性质
通常情况下,甲烷稳定,如与强酸、 强碱和强氧化剂等一般不发生化学反应。 在特定条件下甲烷能与某些物质发生化 学反应,如可以燃烧和发生取代反应等。
置换反应
反应物、生成物中一定 有单质
反应能否进行受催化剂、 在水溶液中进行的置换反 温度、光照等外界条件影 应遵循金属活动性顺序 响较大 逐步取代,产物较复杂 反应产物简单
补充:甲烷的实验室制法
原料: 无水醋酸钠固体 、碱石灰
实验原理: CaO CH 3COONa NaOH CH 4 Na 2CO3
[例6] 在CH4分子结构中,四个碳氢 键 [ B] A.在同一平面上 B.形成一个正四面体的立体结构 C.键长、键能相等 D.键角均为120°
例7、某物质在空气中充分燃烧生成 CO2和H2O,则该物质[ D ] A.只含碳元素 B.只含氧元素 C.只含碳、氧两种元素 D.一定含碳、氢元素,可能含氧 元素
发生装置: 固+固 加热 收集装置: 排水法;向下排空气法
(NaOH、CaO)
CaO的作用:
1、干燥剂(吸收反应中的水分产生)
2、疏松剂(使生产的CH4易于外逸)
3、防止试管破裂(防止NaOH在高温下 与玻璃反应)
四、存在与用途
上海城市居民所使用的燃料主要是管道煤气, 但某些地区已开始使用东海天然气作为居民燃 料。管道煤气的主要成分是CO、H2和少量烃类, 天然气的主要成分是CH4。燃烧相同体积的管 道煤气和天燃气,消耗空气体积较大的是 。 如果将燃烧管道煤气的灶具改烧天然气,灶具 的改进方法是 (填增大或减小)进风 口。如不作改进可能产生的不良后果 是 。
[例2] 在人类已知的化合物中,品
种最多的是 [ D ] A.过渡元素的化合物 B.第二主族元素的化合物 C.第三主族元素的化合物 D.第四主族元素的化合物 E.第五主族元素的化合物
[例3] 某有机物在氧气中充分燃烧,生成 的水蒸气和二氧化碳的物质的量比为1∶1, 由此可以得出结论 [ ] BE A.该有机物分子中C、H、O原子个数比 为1∶2∶3 B.分子中C、H原子个数比为1∶2 C.有机物中必定含氧 D.有机物中必定不含氧 E.无法判断有机物中是否含氧
