碳负离子反应ppt课件
合集下载
13 碳负离子的反应

(
)
O
O
(1) C2H5ONa (2) H
1. OH
H5C2OC(CH2)4COC2H5
(
)
2. H
+
(
)
CH3COCH2COOC2H5
1)NaH 2)C6H5COCl
1)OH
(
)
2)H /
+
(
)
O
O
(1) NaH (2) H
CH3CCH3 + CH3(CH2)3CH2COC2H5
(
)
CH2CH2COOC2H5 H3C CH CH2CH2COOC2H5
取代甲基酮( 取代甲基酮 应用广泛)
取代乙酸
O H CH3 C C CH3 CH2CH2CH3
CH3 O H O (1) C2 H5ONa 2 C C C OC2H5 (2) CH3CH2CH2 Br (1) C2H5 ONa (2) CH3I (1) OH-/H2O (2) H3O+ TM
取代环烷基甲基酮
O
O
CH3CCH2COC2H5
OH
-
OOH
O
O CH3COOH + -CH2COC2H5
CH3C-CH2COC2H5
O CH3COO- + CH3COC2H5
OH-
H+
2 CH3COOH + C2H5OH
• 在合成上的应用
O CH3CCH2COOC2H5 C2H5ONa O CH3CH2CH2Br CH3CCHCOOC2H5
CH2(CO2C2H5)2
(1) C2H5ONa (2) CH3CH2 CH2Br
(1) C2H5ONa (2) CH3I
《碳负离子的反应》课件

防护措施
禁止事项
应急处理
废弃物处理
实验时需佩戴实验服、 护目镜等防护装备。
禁止在实验过程中饮食 、吸烟等行为。
熟悉实验中可能发生的 意外情况及处理方法。
按规定正确处理实验废 弃物。
实验废弃物的处理
分类处理
根据废弃物的性质进行分类, 如有机废弃物、无机废弃物等
。
回收利用
部分废弃物可进行回收利用, 以节约资源。
副产物的生成。
06
碳负离子反应的实验操作 与安全注意事项
实验操作规程
01
02
03
04
实验前的准备
确保实验室环境整洁,检查实 验器材是否齐全、完好。
试剂取用
按照需求适量取用,避免浪费 或不足。
操作步骤
按照规定的顺序进行实验操作 ,不可省略或颠倒。
数据记录
实时记录实验数据,确保准确 无误。
安全注意事项
安全处置
对于无法回收利用的废弃物, 需按照规定进行安全处置。
记录存档
对废弃物的处理过程进行记录 ,并存档备查。
THANKS
感谢观看
自由基反应
总结词
自由基反应是碳负离子与自由基的反 应,通常发生在碳负离子的未共用电 子对被自由基的空轨道接收的过程中 。
详细描述
在自由基反应中,碳负离子与自由基 相互作用,形成新的碳-碳键或碳-自 由基键。这种反应通常在高温或光照 条件下进行,有利于自由基的形成和 反应。
光化学反应
总结词
光化学反应是碳负离子在光的作用下发 生的化学反应,通常需要特定波长的光 照射。
β-羟基酸酯的合成
总结词
β-羟基酸酯是有机合成中的一种特殊结构, 碳负离子可以用于合成β-羟基酸酯。
有机化学课件--羧酸衍生物涉及碳负离子的反应及在合成中应用

碳负离子的形成反应
通过质子化、脱质子化和分子内断裂等反应,碳负离子可以由碳中心引起的 电子重新组合而形成。
碳负离子的反应类型
1
加成反应
2
碳负离子可以与底物中的亲电中心发生
加成反应,以构建更复杂的有机分子结
3
构。
亲核取代反应
碳负离子可与亲核试剂发生取代反应, 用于构建新的碳-碳和碳-其他原子键。
脱质子化反应
有机化学课件--羧酸衍生 物涉及碳负离子的反应及 在合成中应用
本课件将深入探讨羧酸衍生物的结构、碳负离子的反应以及其在有机合成中 的重要应用。
羧酸衍生物的基本结构
了解羧酸衍生物的结构是理解其反应及应用的基础。羧酸的含氧官能团带有 一对孤对电子,使其成为独特的化学实体。
碳负离子是什么
碳负离子是具有孤对电子的碳原子,其带负电荷的性质使其成为化学反应中 的重要中间体。
碳负离子通过脱质子化反应与质子酸反 应,生成分子的亲核部分。
羧酸衍生物中碳负离子的应用
酮合成
通过脱羧或其他反应,碳负离子可用于酮的合成, 提供新的药物和材料研究领域的突破。
酯化反应
碳负离子参与酯化反应,用于合成酯类化合物, 广泛应用于食品、香料和涂料行业。
烯烃合成
醋酸根离子的脱羧反应可生成烯烃,为制备高附 加值化学品提供了一种高效方法。
总结和要点
通过了解羧酸衍生物中碳负离子的反应和应用,我们能够更好地理解有机合 成中的关键步骤和策略,为创新和发展提供重要的参考。
卤代反应
通过卤代反应,羧酸衍生物中的碳负离子可ຫໍສະໝຸດ 与 卤代试剂发生反应,生成有机卤化物。
合成中使用碳负离子的案例
苯甲酸的醇合成
碳负离子参与醇形成反应,将苯 甲酸转化为苯甲醇,用于生产香 料和药物。
碳负离子的反应

官能团转化反应
卤代烃的水解反应
卤代烃在碱性条件下生成碳负离 子,与水发生亲核取代反应生成 醇。
酯的水解反应
酯在碱性条件下生成碳负离子, 与水发生亲核取代反应生成羧酸 和醇。
立体选择性反应
烯烃的顺反异构化反应
在光照或加热条件下,烯烃与卤素发生 加成反应生成卤代烷,卤代烷在碱性条 件下生成碳负离子,再与另一分子烯烃 发生亲核加成反应,生成具有立体选择 性的顺反异构体。
碳负离子的反应
汇报人:XX
• 碳负离子概述 • 碳负离子的反应类型 • 碳负离子在有机合成中的应用 • 碳负离子的反应机理与动力学 • 碳负离子的实验方法与检测技术 • 碳负离子的应用前景与挑战
01
碳负离子概述
定义与性质
定义
碳负离子是指带有负电荷的碳原子, 通常表示为$C^-$。它是许多有机化 学反应中的重要中间体。
自由基反应
自由基引发
在某些条件下,如高温或过氧化物存在下,碳负离子可以引发自由基链式反应。通过均裂产生自由基,进而引发 后续的自由基传递和终止步骤。
自由基加成
碳负离子可以作为自由基受体,与自由基发生加成反应。例如,在烯烃的自由基加成反应中,碳负离子与烯烃中 的双键发生加成,生成新的自由基中间体。
电化学反应
性质
碳负离子具有亲核性,可以与亲电试 剂发生反应。它的稳定性取决于其所 处的化学环境,如溶剂、温度、pH值 等。
结构与稳定性
结构
碳负离子的结构通常是一个或多个碳 原子通过共价键与其他原子或基团相 连,并带有一个负电荷。这个负电荷 可以通过共振结构进行分散,从而提 高其稳定性。
稳定性
碳负离子的稳定性与其结构密切相关 。一般来说,具有较大共轭体系或能 够通过共振稳定化的碳负离子更稳定 。例如,苯基负离子比甲基负离子更 稳定。
碳负离子反应

穿戴防护装备:实验过程中必须穿戴防护 服、手套、护目镜等防护装备。
实验环境:实验应在通风良好的实验室中 进行避免在密闭空间内进行。
实验材料:实验材料应妥善保管避免接触 皮肤和眼睛。
实验操作:实验过程中应严格按照实验 步骤进行操作避免操作不当导致危险。
实验废弃物:实验结束后应妥善处理实验 废弃物避免环境污染。
碳负离子反应是合 成有机化合物的重 要方法之一广泛应 用于药物合成、材 料科学等领域。
碳负离子反应的机 理包括亲核加成、 亲核取代、亲核消 除等。
碳负离子反应的分类
碳负离子反应可以分为两类:亲核碳负离子反应和亲电碳负离子反应 亲核碳负离子反应是指碳负离子作为亲核试剂与亲电试剂发生反应 亲电碳负离子反应是指碳负离子作为亲电试剂与亲核试剂发生反应 碳负离子反应在合成化学中具有广泛的应用如合成有机化合物、药物合成等
碳负离子反应的特点
碳负离子是一种重要的有机合成中间体 碳负离子反应具有高度选择性和立体选择性 碳负离子反应可以生成多种类型的有机化合物 碳负离子反应在合成化学中具有广泛的应用
碳负离子反应的原理
碳负离子反应的化学键特征
碳负离子反应是一种化学反应其中 碳原子失去电子形成负离子。
碳负离子反应的化学键特征还与反 应条件、反应物浓度等因素有关。
碳负离子反应的研究趋势和展望
研究热点:碳负离子反应在材料科学、化学合成等领域的应用 研究方法:理论计算、实验验证相结合的研究方法 研究挑战:如何提高碳负离子反应的效率和选择性 研究展望:未来可能会在能源、环保等领域取得突破性进展
碳负离子反应的研究方法和手段
实验方法:通过实验观察碳负离子反应的过程和结果 理论研究:通过理论推导和计算来研究碳负离子反应的机理和规律 模拟计算:通过计算机模拟来研究碳负离子反应的条件和影响因素 合作研究:与其他研究机构或企业合作共同推进碳负离子反应的研究
有机化学碳负离子的反应
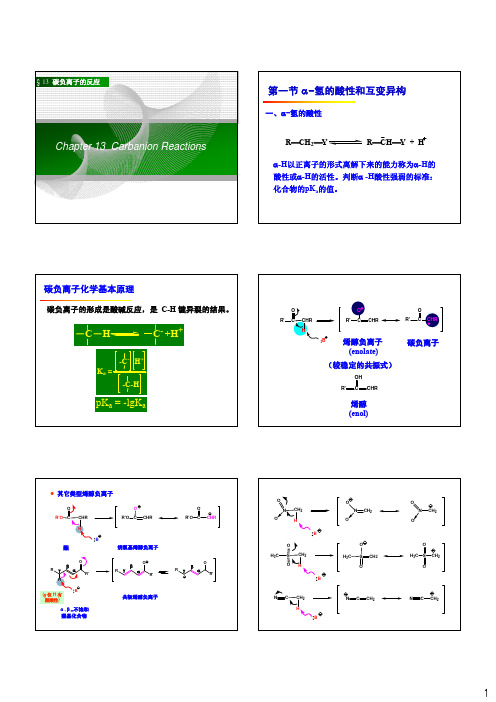
O R'O C
CHR
H
B
酯
O R'O C CHR
烷氧基烯醇负离子
O
β
Rγ
α
R'
H
B (γ 位 H 有
弱酸性)
α,β-不饱和 羰基化合物
β
O
Rγ
α
R'
共轭烯醇负离子
O R'O C CHR
O β
Rγ
α
R'
O
N CH2
O
H
B
O H3C S CH2
OH
B
N C CH2 H B
O N CH2
O
O
H3C
S CH2 O
¾芳醛中羰基化合物的反应活性受电子效应和空间结 构位置的影响,空间位阻较大时它将起主要的作用。
¾当苯环上为烷基时,由于烷基是给电子的基团,又 有位阻使反应物羰基活性下降,反应难以进行,产率 也低。
¾邻位甲基的位阻十分明显,导致不发生反应。
¾当苯环上有吸电子基团时有利于反应进行,不仅反 应的速度加快,并且产率也大大增加。
新型强碱
z 1. LDA 二异丙基胺锂 z 2. LHMDS六甲基二硅胺锂 z 3. LATMP四甲基哌啶锂
特点: z 1. 碱性强pKa大于33 z 2. 能溶解于非极性溶剂 z 3. 位阻大亲核性差
二、互变异构
O R' C CHR
H
O R' C CHR
B 烯醇负离子 (enolate)
(较稳定的共振式)
COOH
−CH=O + H2C
COOH
NH3,C2H5OH -H2O
COOH −CH=CHC
第一章 碳负离子反应ppt

O R C CH 2 O EtO
O H+ C OEt
-
COOEt
-
O R C CH 2 C
+ COOEt
OCEt O R C CH 2 O C O C OEt O R C CH2 O C OEt
-CO EtO-
导向或致活
β-酮酯中亚甲基因有两个活化氢,酸性增加可以在较
温和的条件下进行其它反应,化合物中酯基可以水
化下,丁二酸酯或α-羟基取代的丁二酸酯却能和酮
羰基反应(Stobbe反应),机理:
EtO2C EtO2C CH2CH2 CH
CO2Et
EtO
EtOHEtLeabharlann 2CCH R2CO
R
CH2 CH CO2Et
CO2Et
COOEt CH2 CO2Et
CH2
CO2Et + R2CO
C O
R
Stobbe缩合
CH 3 CO 2Et O
1.3.2分子间酯缩合-克莱森(Claisen)缩合
两个酯的缩合和醇醛缩合区别:在于羰基加成后,前
者脱去RO-,成为酮酯,而后者获得质子,形成羟酮。
O CH3C O OEt + CH3C OEt EtO-O
O CH 2 C OEt
CH 3C
H+
O CH3CCH 2CO 2Et + EtOH
-
RCO
R2C
-O
C
CO 2Et
R2C O
H C
CO2Et
α,β-环氧酸酯在碱催化下水解得到缩水甘油酸。 后者在酸存在下,迅速脱羧重排为醛。
R2C O H C CO2Et H2O 碱催化 R2C O CHCOOH (1) H + (2) CO2 R2C O CH2 重排
O H+ C OEt
-
COOEt
-
O R C CH 2 C
+ COOEt
OCEt O R C CH 2 O C O C OEt O R C CH2 O C OEt
-CO EtO-
导向或致活
β-酮酯中亚甲基因有两个活化氢,酸性增加可以在较
温和的条件下进行其它反应,化合物中酯基可以水
化下,丁二酸酯或α-羟基取代的丁二酸酯却能和酮
羰基反应(Stobbe反应),机理:
EtO2C EtO2C CH2CH2 CH
CO2Et
EtO
EtOHEtLeabharlann 2CCH R2CO
R
CH2 CH CO2Et
CO2Et
COOEt CH2 CO2Et
CH2
CO2Et + R2CO
C O
R
Stobbe缩合
CH 3 CO 2Et O
1.3.2分子间酯缩合-克莱森(Claisen)缩合
两个酯的缩合和醇醛缩合区别:在于羰基加成后,前
者脱去RO-,成为酮酯,而后者获得质子,形成羟酮。
O CH3C O OEt + CH3C OEt EtO-O
O CH 2 C OEt
CH 3C
H+
O CH3CCH 2CO 2Et + EtOH
-
RCO
R2C
-O
C
CO 2Et
R2C O
H C
CO2Et
α,β-环氧酸酯在碱催化下水解得到缩水甘油酸。 后者在酸存在下,迅速脱羧重排为醛。
R2C O H C CO2Et H2O 碱催化 R2C O CHCOOH (1) H + (2) CO2 R2C O CH2 重排
碳负离子课件PPT

碳负离子的电子结构
碳负离子的电子结构是稳定的,其价 电子数为6,具有一个空轨道,可以 接受电子。
碳负离子可以通过接受电子而形成稳 定的负离子,这与其电子结构有关。
碳负离子的电子构型为1s²2s²2p⁶, 其最外层电子构型与C原子相同。
碳负离子的光谱性质
01
碳负离子在光谱中表现出特征的 吸收和发射光谱,这些光谱可以 用于研究碳负离子的结构和性质 。
碳负离子的合成方法
碳负离子的合成方法有多种, 如通过醇、醚、胺等的酸式分 解、通过重氮化合物或卡宾的 反应等。
在合成碳负离子时,需要选择 适当的反应条件和试剂,以确 保合成的高效性和产物的纯度。
合成碳负离子时需要注意安全 问题,如避免使用有毒有害的 试剂和避免产生危险的气体等。
03
碳负离子的物理性质
碳负离子对水环境的影响
净化水质
碳负离子具有吸附和还原 作用,能够去除水中的重 金属离子和有害有机物, 提高水质。
促进水生生物生长
碳负离子可以提供水生生 物所需的营养物质,促进 水生生物的生长和繁殖。
调节水体酸碱度
碳负离子可以与水中的氢 离子反应,调节水体的酸 碱度,维持水体的生态平 衡。
碳负离子对土壤环境的影响
提高土壤肥力
碳负离子可以促进土壤中有机物 的分解和转化,提高土壤的肥力。
改善土壤结构
碳负离子可以与土壤中的矿物质 发生反应,形成有益的土壤结构, 提高土壤的保水能力和透气性。
抑制土壤污染
碳负离子可以吸附和固定土壤中 的重金属离子和有害有机物,降
低土壤污染的风险。
05
碳负离子的未来发展
碳负离子在新能源领域的应用
碳负离子的形成
通过共价键的断裂形成
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
醛酮+α-卤代酸酯 + 强碱=α,β-环氧酸酯
该反应的意义在于环氧生成物经过后续反应可 以制备新的醛酮
10
11
复习重要反应:Michael addition
请翻回α,β不饱和醛酮复习机理。该机理也 是一个碳负离子机理,属于要求内容。
12
内容扩展: 除了α,β不饱和醛酮以外,该反应α, β不饱和酯、 α,β不饱和腈都能发生。
酰基化
教材上讨论了用碱和溶剂的问题,但即使反应存 在很多问题,醇钠事实上仍然是比较常用的碱, 因此以后的条件统一写醇钠,溶剂可以不写。 26
烷基化
27
3.在合成上的应用
主要用途是合成甲基酮类衍生物 也可以合成其他一些有甲基酮主干结构的化
合物
乙酰乙酸 乙酯的残 留片段
烷化时引 入的卤代 烷部分
28
36
合成分析:
一元酸:
37
二元酸:
38
39
环酸(3-6元环)
40
用丙二酸二乙酯合成 (04年 药大 研)
41
第四节 烯胺的反应
复习:烯胺(见醛酮)
酸性条件
仲胺多环状
四氢吡咯 吗啉
六氢吡啶42
烯胺的烷化和酰化
p-π共轭 给烯胺带来了部分碳负离子性质
43
44
书写步骤: 1 成烯胺 2 成醛酮 特征—在原醛酮的α位置取代
31
长链多卤烃通过三乙的自环合
该类反应为成环的又一个重要方法。反应时要注 意控制量比:三乙1mol,卤烃1mol,碱2mol。否 则可能发生三乙分子间交联。
32
结构类似物的反应
β—羰基酯具有类似三乙的结构,可以发生 和三乙相似的反应。
33
分析:
34
二、丙二酸二乙酯
制法:
35
合成步骤基本和三乙一样,先烷化再水解。
碳负离子的反应
第一节 碳负离子的稳定因素、
α-氢的酸性
烷负离子——碱性极强,极不稳定
α—位引入吸电子基,分散负电荷,有利负离子 的稳定
2
• α-羰基的物质为负离子同时在诱导和共轭上都提
供了特殊的稳定性
复习回顾:醛酮的互变异构
互变异构
多羰基化合物对异构提供了特殊的稳定性。
3
O CH3CCH3
OO C2H5OCCH2COC2H5
2-丁烯醛
反应物要求: 含有-H的醛(酮较难)
反应条件: 稀碱 6
• 羟(醛一缩)合普的尔金衍反生应类型
Perkin Reaction
(二)克脑文戈尔缩合
Knoevenagel Condensation
(三)达森反应
Darzen Reaction
7
(二)Knoevenagel Condensation 活泼亚甲基
反应需要活 泼卤代烷: 碘甲烷、烯 丙卤代物、 苄卤代物、
α-卤代酸酯
45
力了! 16
Dieckmann Condensation (狄克曼缩 合)
分子内酯缩合反应成五元或六元环的β-酮酸酯
产物有α-H,有继续反应的可能 有水解脱羧的可能
17
交叉缩合
不同的具α-H 的酯进行酯缩合时,可能有 四种产物,在合成上无意义
18
常见的用于交叉缩合的酯
19
酮酯缩合
酮α-氢的酸性强于酯的α-氢,在碱性催化剂作 用下酮提供α-氢形成烯醇负离子,作为亲核试剂 进攻酯发生亲核加成-消除反应,生成β-二羰基
甲基酮衍生物合成分析和实例:
由三乙和合适卤代物合成
分析: (1) 产物为甲基酮,合成时一定要经过酮式分解。 (2) 将目标产物的结构与丙酮比较,确定引入基团。 (3) 最后确定合成路线。写全反应步骤和反应条件。
注意:当引入基团不同时,通常是先引入体积较大 的基团。
29
30
合成双羰基化合物
+ 3C化合物
OO CH3CCH2COC2H5
OH
0.00015
CH2 CCH3
OH O
0.1
C2H5OC CHCOH3C CHCOC2H5
OO CH3CCH2CCH3
OO C6H5CCH2CCH3
OH O CH3C CHCCH3
OH O C6H5C CHCCH3
76.0
90.0
4
对结果的一些讨论: 1 强吸电子、大共轭体系的存在有利于形成更
反应用碱为醇钠、季铵碱、氢氧化钾/钠等各种强碱
13
二、克莱森缩合—Claisen condensation
三乙(乙酰乙酸乙酯)的制备
有α-H的酯
强碱——至少是醇钠级别的碱 14
机理
PKa 11
PKa 16
15
只有一个α-H的酯 反应情况比较特殊
强碱,加强第一 步的转化率
反应到这里,没有α-H来提供单向酸碱反应的动
化合物。
20
各种酯缩合被常用于增加碳链和官能团的各种反应
21
22
逆分析
23
第三节 β-二 羰基化合物的烷化、酰化
和在合成中的应用
一 乙酰乙酸乙酯
二 丙二酸二乙酯
24
一 乙酰乙酸乙酯
1.分解方式:酸式分解和酮式分解 酸式分解—有替代方法,不重要
酮式分解—合成的一个重要方法
25
2. 烷基化和酰基化
Y或Y' = COR , COOR , COOH , CN , NO2等 弱碱
使用(吡啶、哌啶、胺)等有机弱碱,目的是为 了抑制羟醛缩合的副反应
8
• 高活性的醛易与各种活泼亚甲基物质反应
• 酮需要和酸性更强的亚甲基反应
1,3双官能团化合
物经常有脱羧等后
续反应,被广泛地
用于合成
9
(三) Darzen Reaction
加稳定的烯醇式。 2 酸性和烯醇式比例基本有一致性。 3 会影响反应的立体化学——因为烯醇式是一 个平面型。
5
第二节 缩合反应
一、 羟醛缩合
O
H
α
CH3 C H + CH2 CHO
OH CH3CHCH2CHO △
稀 NaOH 4~5 ℃
OH
CH3CHCH2CHO β-羟基丁醛 (醇醛)
CH3CH CHCHO + H2O
该反应的意义在于环氧生成物经过后续反应可 以制备新的醛酮
10
11
复习重要反应:Michael addition
请翻回α,β不饱和醛酮复习机理。该机理也 是一个碳负离子机理,属于要求内容。
12
内容扩展: 除了α,β不饱和醛酮以外,该反应α, β不饱和酯、 α,β不饱和腈都能发生。
酰基化
教材上讨论了用碱和溶剂的问题,但即使反应存 在很多问题,醇钠事实上仍然是比较常用的碱, 因此以后的条件统一写醇钠,溶剂可以不写。 26
烷基化
27
3.在合成上的应用
主要用途是合成甲基酮类衍生物 也可以合成其他一些有甲基酮主干结构的化
合物
乙酰乙酸 乙酯的残 留片段
烷化时引 入的卤代 烷部分
28
36
合成分析:
一元酸:
37
二元酸:
38
39
环酸(3-6元环)
40
用丙二酸二乙酯合成 (04年 药大 研)
41
第四节 烯胺的反应
复习:烯胺(见醛酮)
酸性条件
仲胺多环状
四氢吡咯 吗啉
六氢吡啶42
烯胺的烷化和酰化
p-π共轭 给烯胺带来了部分碳负离子性质
43
44
书写步骤: 1 成烯胺 2 成醛酮 特征—在原醛酮的α位置取代
31
长链多卤烃通过三乙的自环合
该类反应为成环的又一个重要方法。反应时要注 意控制量比:三乙1mol,卤烃1mol,碱2mol。否 则可能发生三乙分子间交联。
32
结构类似物的反应
β—羰基酯具有类似三乙的结构,可以发生 和三乙相似的反应。
33
分析:
34
二、丙二酸二乙酯
制法:
35
合成步骤基本和三乙一样,先烷化再水解。
碳负离子的反应
第一节 碳负离子的稳定因素、
α-氢的酸性
烷负离子——碱性极强,极不稳定
α—位引入吸电子基,分散负电荷,有利负离子 的稳定
2
• α-羰基的物质为负离子同时在诱导和共轭上都提
供了特殊的稳定性
复习回顾:醛酮的互变异构
互变异构
多羰基化合物对异构提供了特殊的稳定性。
3
O CH3CCH3
OO C2H5OCCH2COC2H5
2-丁烯醛
反应物要求: 含有-H的醛(酮较难)
反应条件: 稀碱 6
• 羟(醛一缩)合普的尔金衍反生应类型
Perkin Reaction
(二)克脑文戈尔缩合
Knoevenagel Condensation
(三)达森反应
Darzen Reaction
7
(二)Knoevenagel Condensation 活泼亚甲基
反应需要活 泼卤代烷: 碘甲烷、烯 丙卤代物、 苄卤代物、
α-卤代酸酯
45
力了! 16
Dieckmann Condensation (狄克曼缩 合)
分子内酯缩合反应成五元或六元环的β-酮酸酯
产物有α-H,有继续反应的可能 有水解脱羧的可能
17
交叉缩合
不同的具α-H 的酯进行酯缩合时,可能有 四种产物,在合成上无意义
18
常见的用于交叉缩合的酯
19
酮酯缩合
酮α-氢的酸性强于酯的α-氢,在碱性催化剂作 用下酮提供α-氢形成烯醇负离子,作为亲核试剂 进攻酯发生亲核加成-消除反应,生成β-二羰基
甲基酮衍生物合成分析和实例:
由三乙和合适卤代物合成
分析: (1) 产物为甲基酮,合成时一定要经过酮式分解。 (2) 将目标产物的结构与丙酮比较,确定引入基团。 (3) 最后确定合成路线。写全反应步骤和反应条件。
注意:当引入基团不同时,通常是先引入体积较大 的基团。
29
30
合成双羰基化合物
+ 3C化合物
OO CH3CCH2COC2H5
OH
0.00015
CH2 CCH3
OH O
0.1
C2H5OC CHCOH3C CHCOC2H5
OO CH3CCH2CCH3
OO C6H5CCH2CCH3
OH O CH3C CHCCH3
OH O C6H5C CHCCH3
76.0
90.0
4
对结果的一些讨论: 1 强吸电子、大共轭体系的存在有利于形成更
反应用碱为醇钠、季铵碱、氢氧化钾/钠等各种强碱
13
二、克莱森缩合—Claisen condensation
三乙(乙酰乙酸乙酯)的制备
有α-H的酯
强碱——至少是醇钠级别的碱 14
机理
PKa 11
PKa 16
15
只有一个α-H的酯 反应情况比较特殊
强碱,加强第一 步的转化率
反应到这里,没有α-H来提供单向酸碱反应的动
化合物。
20
各种酯缩合被常用于增加碳链和官能团的各种反应
21
22
逆分析
23
第三节 β-二 羰基化合物的烷化、酰化
和在合成中的应用
一 乙酰乙酸乙酯
二 丙二酸二乙酯
24
一 乙酰乙酸乙酯
1.分解方式:酸式分解和酮式分解 酸式分解—有替代方法,不重要
酮式分解—合成的一个重要方法
25
2. 烷基化和酰基化
Y或Y' = COR , COOR , COOH , CN , NO2等 弱碱
使用(吡啶、哌啶、胺)等有机弱碱,目的是为 了抑制羟醛缩合的副反应
8
• 高活性的醛易与各种活泼亚甲基物质反应
• 酮需要和酸性更强的亚甲基反应
1,3双官能团化合
物经常有脱羧等后
续反应,被广泛地
用于合成
9
(三) Darzen Reaction
加稳定的烯醇式。 2 酸性和烯醇式比例基本有一致性。 3 会影响反应的立体化学——因为烯醇式是一 个平面型。
5
第二节 缩合反应
一、 羟醛缩合
O
H
α
CH3 C H + CH2 CHO
OH CH3CHCH2CHO △
稀 NaOH 4~5 ℃
OH
CH3CHCH2CHO β-羟基丁醛 (醇醛)
CH3CH CHCHO + H2O
