土壤硝化作用强度讲义的测定
矿化、硝化与反硝化实验方法

土壤矿化、硝化与反硝化1.矿化培养矿化培养试验采用风干土淹水密闭培养法,预培2 周来消除干土效应。
称取过20 目筛风干土5g,每层土样称取3份,分别置于10×180 mm 的试管中。
将试管平放于桌面上小心滚动,使管中土面倾斜,用移液管缓缓加入5 ml去离子水。
加水后检查各试管中的土壤是否完全润湿,并尽量驱出土中的空气,然后用橡皮塞密封管口,置于25o C 的培养箱中恒温培养,约每周换气一次,并驱除土中气体(在培养后期换气的时间间隔可长一些);分别于淹水后第0 周、1,3 周、5 周、7 周、10 周、14周时进行取样测定土壤中的铵态氮的含量,每层土样测定3 管,作为3 个重复。
测定时用20ml 2.5 mol/L KCl 将管中土壤全部洗入100ml 三角瓶中,振荡1 小时后静置半小时过滤,将滤液储存在塑料瓶中备测。
(1)每个培养管吸取培养溶液:5ml去离子水(2) 培养周期:预培2 周,分别于淹水后第0 周、2 周、4 周、6 周、8 周、10 周和12 周时进行取样测定土壤中的铵态氮的含量,每层土样测定3 管,作为3 个重复。
(3) 培养结束处理:测定时用20ml 2.5 mol/L KCl 将管中土壤全部洗入100ml三角瓶中,振荡1 小时后静置半小时过滤,将滤液储存在塑料瓶中备测。
2.土壤硝化试验方法如下:称取5g 过20 目筛的每层供试土样各2份,分别放入10×180 mm 的试管中,其中0天培养则不加铵,另外第7天、14 天、21 天和28 天分别取样的分别加入1.125 mgN (NH4)2SO4溶液,然后加水至田间持水量的80%,瓶口用塑料薄膜封口以减少水分损失,称重后置于25o C 的培养箱中恒温培养。
预培3 天后,对不加铵的分别加22.7ml 2.2mol/L KCL 溶液,振荡1 小时后,过滤到干净的塑料瓶中,测定铵态氮和硝态氮的含量作为初始量;而对加铵培养瓶称重,通气30 分钟并补充水分至原重,然后继续恒温培养,并开始计算时间,每隔3 天对加铵培养瓶通气一次并称重补充水分至原重,在正式培养后的第7天、14 天、21 天和28 天分别取样,每层土样各取3 瓶作为3 个重复,分别加25ml 2 mol/L KCL溶液,振荡1 小时后,过滤到干净的塑料瓶中,测定铵态氮和硝态氮的含量。
土壤中硝氮、氨氮测定方法
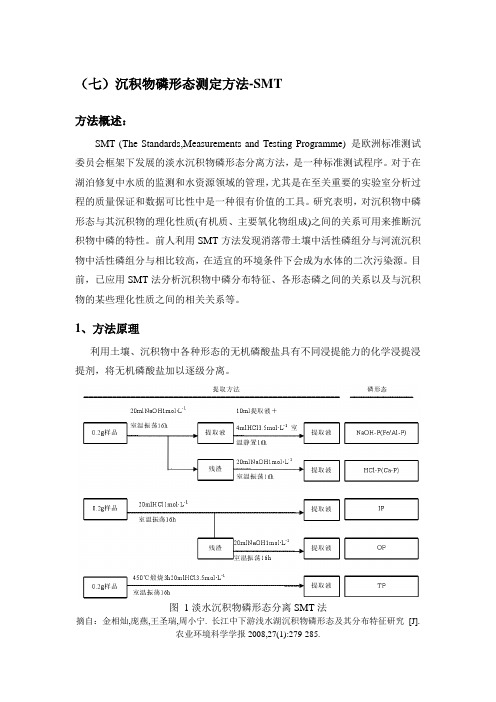
(七)沉积物磷形态测定方法-SMT方法概述:SMT (The Standards,Measurements and Testing Programme) 是欧洲标准测试委员会框架下发展的淡水沉积物磷形态分离方法,是一种标准测试程序。
对于在湖泊修复中水质的监测和水资源领域的管理,尤其是在至关重要的实验室分析过程的质量保证和数据可比性中是一种很有价值的工具。
研究表明,对沉积物中磷形态与其沉积物的理化性质(有机质、主要氧化物组成)之间的关系可用来推断沉积物中磷的特性。
前人利用SMT方法发现消落带土壤中活性磷组分与河流沉积物中活性磷组分与相比较高,在适宜的环境条件下会成为水体的二次污染源。
目前,已应用SMT法分析沉积物中磷分布特征、各形态磷之间的关系以及与沉积物的某些理化性质之间的相关关系等。
1、方法原理利用土壤、沉积物中各种形态的无机磷酸盐具有不同浸提能力的化学浸提浸提剂,将无机磷酸盐加以逐级分离。
图1淡水沉积物磷形态分离SMT法摘自:金相灿,庞燕,王圣瑞,周小宁. 长江中下游浅水湖沉积物磷形态及其分布特征研究[J].农业环境科学学报2008,27(1):279-285.2、需要的设备与实验条件紫外分光光度计、高压灭菌锅3、所需试剂及操作步骤(一)所需要的试剂(1)5N H2SO4:70mL浓硫酸-500mL水中,置于常温下保存;(2)酒石酸锑钾溶液:准确称取1.3715g酒石酸锑钾于500mL容量瓶中,溶解定容,充分摇匀后将该溶液贮存在棕色或其他试剂瓶(玻璃瓶)中,将其置于4℃下保存。
(3)钼酸铵溶液:准确称取40g钼酸铵于1000mL容量瓶中,加适量水待其完全溶解后加水稀释至刻度线,充分摇匀后将该溶液贮存在棕色或其他试剂瓶(玻璃瓶)中,将其置于冰箱中于4℃下保存。
(4)抗坏血酸溶液:准确称取17.6g抗坏血酸1000mL容量瓶中,加适量水待其完全溶解后加水稀释至刻度线,充分摇匀后将该溶液贮存在棕色或其他试剂瓶(玻璃瓶)中,将其置于冰箱中于4℃下保存。
土壤中硝化抑制剂DMPP含量的气相色谱测定法

收稿日期:2007-07-06; 修订日期:2007-09-09 基金项目:中 科 院 知 识 创 新 工 程 重 要 方 向 项 目 (KZCX3-SW-445); 国 家 科 技 支 撑 计 划 项 目 (2006BAD10B00) 作者简介:房娜娜(1982-),女,河南新乡人,硕士研究生,主要从事土壤植物营养与土壤肥料方面的研究工作。 Tel:024-83970357; E-mail:fangnana0373@ * 通讯作者:E-mail: wuzj@
表 1 不同萃取剂的峰面积 Table 1 Results of apex area for different extractants
序号 Serial number
溶剂 Extractants
1
氯仿
2
甲苯
3
ቤተ መጻሕፍቲ ባይዱ
环己烷
4
正庚烷
5
石油醚
峰面积 Apex area (μV s) 23949.000 2857.667 16086.667 14271.000 20242.333
第 39 卷第 6 期 2008 年 12 月
土壤通报 Chinese Journal of Soil Science
Vol . 39 , No . 6 Dec . , 2008
土壤中硝化抑制剂 DMPP 含量的气相色谱测定法
房娜娜 1,2,武志杰 1*,陈利军 1,陈 光 3,史云峰 1,2
(1.中国科学院 沈阳应用生态研究所,辽宁沈阳 110016;2.中国科学院 研究生院,北京 100039;3.沈阳化工研究院,辽宁 沈阳 110021)
算其在不同温度下的日平均降解速率。
6.262 6.863 11.566
稳定性肥料中硝化抑制剂作用效果的检测方法

稳定性肥料中硝化抑制剂作用效果的检测方法徐英龙;张蕾;杨明;房娜娜;石元亮【摘要】以硝化抑制率作为评价指标,研究了影响硝化抑制剂抑制效果测定方法的主要因素,包括氮土比、培养时间以及土壤类型等.确立了测定稳定性肥料中硝化抑制剂抑制作用效果的最佳检测方法:称取风干后的棕壤200 g,以氮土比1.15:1 000准确称取样肥,并将其充分混匀,以25%的含水量,在30 ℃培养箱中培养.选择自培养开始的第9、12、15 d测定土壤中硝态氮(包括亚硝态氮)的质量分数.该检测方法提高了评价效率和准确度.%Based on the nitrification inhibitory rate as evaluating indicator,the factors that affect the inhibiting efficiency evaluation of nitrification inhibitor were studied,which including:soil nitrogen ratio,incubation time and soil types and etc.A rapid detection method was established for evaluating the efficiency of nitrification inhibitor in stabilized fertilizers:200 g of dried brown soil were weighed,and then the amount of fertilizer were weighed according to the nitrogen and soil ratio at 1.15: 1 000.The mixed soil and fertilizer were cultured in the incubator at 30 ℃with 25%the water content.Soilnitrate(including nitrite)content was measured at the 9,12,15 day.The detection method increased the evaluating efficiency and accuracy.【期刊名称】《中国土壤与肥料》【年(卷),期】2017(000)002【总页数】5页(P157-161)【关键词】检测方法;硝化抑制剂;硝化抑制率;稳定性肥料【作者】徐英龙;张蕾;杨明;房娜娜;石元亮【作者单位】中国科学院沈阳应用生态研究所,辽宁沈阳 110016;中国科学院沈阳应用生态研究所,辽宁沈阳 110016;中国科学院沈阳应用生态研究所,辽宁沈阳110016;中国科学院沈阳应用生态研究所,辽宁沈阳 110016;中国科学院沈阳应用生态研究所,辽宁沈阳 110016【正文语种】中文【中图分类】S143.1;S14-33稳定性肥料是通过一定工艺在肥料造粒过程中加入脲酶抑制剂和(或)硝化抑制剂,能延缓施入土壤的尿素水解和进一步抑制铵态氮向硝态氮转化,而减少氮的挥发和流失,使肥效期得到延长的一类含氮肥料[1]。
土壤硝化作用强度测定

土壤硝化作用强度测定
一、原理
将定量的土壤接种到硝化细菌培养基中,由于土壤中硝化细菌的作用,是亚硝酸氧化成硝酸,用培养基中亚硝酸的消失量占原始培养基中亚硝酸含量的百分比作为硝化作用强度的指标。
亚硝酸能与格利斯试剂反应产生一种紫红色的化合物,该显色反应不易受硝态氮的干扰。
二、药品器材
1.硝化细菌培养基:NaNO2 1g MgSO4·7H2O 0.03g MnSO4·4H2O 0.01g K2HPO40.75g
Na2CO3(无水)1g NaH2PO40.25g超纯水1000ML
2.格利斯试剂:溶液一,称取磺胺酸0.5g,溶于150ml醋酸溶液(30%)中,保存于棕色
瓶中。
溶液二,称取α-萘胺0.5g,加入50ml蒸馏水中,煮沸后,缓缓加入30%的醋酸溶液150ml,保存于棕色瓶中。
3.亚硝酸根标准溶液:称取 1.500g分析纯亚硝酸那于烧杯中,加蒸馏水溶解后定容至
1000ml,此溶液亚硝酸根离子浓度为1mg/ml。
用时以此液配成亚硝酸根标准溶液(亚硝酸根离子浓度为0.01mg/ml)。
三、步骤
1.在150ml三角瓶中装30ml硝化细菌培养基,灭菌。
2.冷却后的培养基中接种1/10土壤悬液1ml,于28℃恒温培养15d,取出三角瓶过滤。
3.用比色法测定滤液中的亚硝酸含量。
四、硝化作用强度
硝化作用强度=(原始培养基中亚硝酸根含量-培养后培养基中亚硝酸根含量)/原始培养基中亚硝酸根含量*100%。
凯氏定氮法 标准-概述说明以及解释

凯氏定氮法标准-概述说明以及解释1.引言1.1 概述凯氏定氮法是一种常用的分析方法,用于确定物质中的氮含量。
该方法基于凯氏反应,即将有机或无机物中的氮转化为氨,再通过氨测定确定氮的含量。
凯氏定氮法简单、灵敏度高,并能够适用于各种类型的样品。
文章的概述部分旨在介绍凯氏定氮法的基本背景和重要性。
首先,我们将对凯氏定氮法的原理和相关的基本步骤进行阐述。
接着,我们将探讨凯氏定氮法在不同领域中的广泛应用,并特别关注其在环境科学、农业和食品安全等领域的应用情况。
凯氏定氮法具有一些独特的优点,如操作简便、成本低廉、准确性高等。
然而,同时我们也必须认识到凯氏定氮法存在一定的局限性,如对某些有机物的测定存在困难等。
针对这些问题,本文还将展望凯氏定氮法未来的发展方向,并探讨可能的改进和创新。
总而言之,本文将全面介绍凯氏定氮法的原理、步骤和应用,并对其优点、局限性进行评估。
通过深入了解凯氏定氮法,我们可以更好地理解其在实际应用中的潜力和局限性,并为其未来的研究和应用提供参考。
文章结构部分的内容可以如下所示:1.2 文章结构本文将按照以下结构来展开对凯氏定氮法的介绍和分析:第一部分,引言,将对凯氏定氮法进行概述,简要介绍该方法的背景和相关概念。
同时,本部分还将描述文章的目的,即通过对凯氏定氮法的详细介绍和分析,帮助读者更好地理解和应用该方法。
第二部分,正文,将重点介绍凯氏定氮法的原理、步骤和应用。
2.1小节将详细阐述凯氏定氮法的原理,包括氛围压降法和热导法两种常见的方法。
2.2小节将详细描述凯氏定氮法的步骤,包括样品的预处理、试剂的选择和实验操作等。
2.3小节将探讨凯氏定氮法在不同领域的应用,例如土壤分析、环境监测等,以及其在实际应用中的优点和限制。
第三部分,结论,将对凯氏定氮法进行总结并展望其未来的发展。
3.1小节将概述凯氏定氮法的优点,如准确性高、灵敏度好等。
3.2小节将强调凯氏定氮法的局限性,如样品处理过程中的误差、仪器设备的限制等。
(新)土壤硝化作用强度的测定

实验程序3
(用比色法测定滤液中的亚硝酸根含量)
结果计算
NO2-(mg/30mL)=X(mg/mL) ×比色体积×稀 释倍数 ×10-3
式中X(mg/mL)——由标准曲线查知 10-3——换算为mg
土壤硝化作用强度
计算公式:
原始培养基中NO2- 量-培养基中NO2- 量 硝化作用强度= ×100% 原始培养基中NO2- 量
思考题
什么叫硝化作用?硝化作用由哪
两类细菌参与? 根据硝酸细菌培养基的组成成分, 硝酸细菌属何种营养类型? 本实验的原理是什么? 实验中要注意什么?
实验二十三
结
束
菌培养基中,每组接2只三角瓶过 滤立即用以测定原始培养液中亚硝 酸根含量,另一支三角瓶置于280C 温室中培养15d. 培养结束,取出三角瓶,培养液进 行过滤。
实验程序3
(用比色法测定滤液中的亚硝酸根含量) 取滤液1mL于50mL容量瓶中,稀释至约 40mL,加入1mL格利斯试剂Ⅰ,放置 10min。再加入1mL格利斯试剂Ⅱ和 1mL2%醋酸钠溶液,显色后稀释至刻度, 放置10min后,用分光光度计(波长 520nm)比色测定。 亚硝酸银标准曲线的绘制 吸取压硝酸银 标准液0、1、2、3、4、5mL,分别放 入50mL容量瓶中,定容。与待测样品同 样条件进行比色,以浓度为横坐标,以光 密度为纵坐标绘制标准曲线。
实验材料2
格利斯试剂: 1. 溶液Ⅰ 称取对氨基苯磺酸0.5g,溶于 150ml30%醋酸溶液中,保存于棕色瓶中。 2.溶液Ⅱ 称取α-萘胺0.5g,加入50mL 蒸馏水中,煮沸后,缓缓加入30%的醋酸 溶液150mL,保存于棕色瓶中。 亚硝酸银标准液 称取1.5000g分析纯亚 硝酸钠于烧杯中,加蒸馏水溶解后洗入 1000mL容量瓶中 ,再加蒸馏水至刻度, 摇匀。用时以此液稀释成标准液(每mL含 0.01mg的NO2-)
硝化作用强度的测定

6.亚硝酸根标准曲线的绘制,吸取亚硝酸根标准液0、1、2、3、4、5ml分别放入50ml容量瓶中,定容,与待测样品同样条件进行比色,以浓度为横坐标,以OD值为纵坐标绘制标准曲线。
三、实验步骤
培养基的配置及1/10土壤悬液的制备-----接种培养-----用比色法测定滤液中的亚硝酸根含量。
1.在150ml三角瓶中装30ml硝酸细菌培养基,灭菌每组2瓶。
2.在150ml三角瓶中装45ml蒸馏水,并放入少许玻璃珠,灭菌每组1瓶。
3.称5g土于45ml三角瓶中,震荡5分钟。
4.取1ml于硝酸细菌培养基中,每组接2瓶,其中一瓶立即过滤用以测定原始培养基中亚硝酸根含量,另一瓶置于28温箱培养15天,培养结束,取出三角瓶,培养液进行过滤。
硝化作用强度的测定
一、目的要求
掌握硝化强度的测定方法,了解土壤中氮素如何有效利பைடு நூலகம்及对环境污染的影响。
二、实验材料
样品:新鲜土样
培养基:硝化作用第二阶段培养基
亚硝酸钠1克;硫酸镁0.03克;硫酸锰0.01克
磷酸氢二钾0.75克;碳酸钙3.0克;水1000毫升
格里斯试剂:
1.溶液Ⅰ:称取对氨基苯磺酸0.5g(0.05g)溶于150ml(15ml) 30%醋酸溶液中,保存于棕色瓶中。
四、结果计算
NO2–(mg/30ml)=X(ug/ml)*比色体积*稀释倍数*10-3
X(由标准曲线查知)10-3(换算为ml)
土壤消化强度=原始培养基中NO2–量—培养基中NO2–量
