2021年碳酸钠与碳酸氢钠性质比较
碳酸钠与碳酸氢钠的区别

碳酸钠与碳酸氢钠的区别
碳酸钠,俗名苏打、纯碱、洗涤碱,化学式:Na2CO3,普通情况下为白色粉末,为强电解质。
密度为2.532g/cm3,熔点为851°C,易溶于水,具有盐的通性。
碳酸氢纳为白色粉末,或不透明单斜晶系细微结晶。
比重2.159。
无臭、味咸,可溶于水,微溶于乙醇。
其水溶液因水解而呈微碱性,受热易分解,在65℃以上迅速分解,在270℃时完全失去二氧化碳,在干燥空气中无变化,在潮湿空气中缓慢分解。
用作食品工作的发酵剂、汽水和冷饮中二氧化碳的发生剂、黄油的保存剂。
可直接作为制药工业的原料,用于治疗胃酸过多。
还可用于电影制片、鞣革、选矿、冶炼、金属热处理,以及用于纤维、橡胶工业等。
同时用作羊毛的洗涤剂、泡沫灭火剂,以及用于农业浸种等。
1。
碳酸钠和碳酸氢钠

一、碳酸钠(Na2CO3)
俗名:纯碱、苏打
物理性质 • 1、颜色状态:白色粉末 • 2、水溶性:易溶于水
化学性质
1、热稳定性:稳定。 2、酸性(速度较慢): Na2CO3+2HCl===2NaCl+CO2 +H2O 3、与CaCl2溶液反应: Na2CO3 + CaCl2 ===2NaCl+CaCO3 4、碱性:强于碳酸氢钠
4、 碱性:弱于碳酸钠
三、用途
• 碳酸钠常用于玻璃,制皂,造纸,纺织等 工业,生活中的洗涤剂。
• 碳酸氢钠常用于发酵粉,医疗上中和胃酸。
参考方法:
• 若是固体, • 1、观察状态:碳酸钠为白色固体粉末,碳酸
氢钠为白色细小的晶体。
• 2、观察溶解性:加适量的水碳酸钠全部溶解, 碳酸氢钠不能全部溶解。
• 3、加热:质量减少,且产生使澄清石灰水变 浑浊的气体的是碳酸氢钠。
• 若是溶液, • 1、向两溶液中滴加稀盐酸:一开始没有明 显现象,一会才有气泡冒出的是碳酸钠, 一开始就会有气泡生成的是碳酸氢钠。 • 2、向两溶液中加入氯化钡或氯化钙溶液: 有白色沉淀的是碳酸氢钠。
碳酸钠粉末
纯碱
碳酸氢钠晶体ຫໍສະໝຸດ 小苏打二、碳酸氢钠( NaHCO3)
俗名:小苏打
物理性质 • 1、颜色状态:白色单斜晶体 • 2、水溶性:溶于水
化学性质
1、热稳定性:不稳定。 2NaHCO3===Na2CO3 +CO2 +H2O 2、酸性(速度较快): NaHCO3+HCl===NaCl+CO2 +H2O 3、与CaCl2溶液反应: NaHCO3 与 CaCl2 不反应
碳酸氢钠和碳酸钠

碳酸氢钠和碳酸钠
化学式和化学性质
1、热稳定性:碳酸钠加热不分解,碳酸氢钠加热易分解成碳酸钠,
水和二氧化碳;
2、水溶解性:碳酸钠的溶解度大于碳酸氢钠;
3、与二氧化碳的反应:碳酸钠能跟二氧化碳(与水)化合生成碳酸氢钠,而碳酸氢钠不反应;
4、与氢氧化钠的反应:碳酸氢钠能跟氢氧化钠反应生成碳酸钠和水,而碳酸氢钠不反应;
5、与氯化钙的反应:碳酸钠跟氯化钙(或氯化钡)溶液易生成碳酸盐
沉淀,而碳酸氢钠跟盐类稀溶液不易生成沉淀6、与苯酚的反应:碳酸钠
能与苯酚反应生成苯酚钠和碳酸氢钠,而碳酸氢钠不与苯酚反应。
碳酸钠与碳酸氢钠性质的比较教程文件

与可溶性钙盐、 钡盐反应
产生白色沉淀
不反应
与碱 烧 碱
反应
石灰水
不反应
O H H3 C C O 3 2 O H 2 O
C2aC3O 2 Ca3 CO 产生白色沉淀
转化
用途
可用于玻璃、造纸、纺织等工 业;可做洗涤剂等。
可用于灭火机、发酵剂、医药等。
侯小杰
碳 酸 钠 和 碳 酸 氢 钠 的 用 途
碳酸钠与碳酸氢钠性质的比较
侯小杰
碳酸钠和碳酸氢钠的性质比较
实验探究 ②碳酸钠和碳酸氢钠与盐酸反应的比较
结论:
NaHCO3与稀盐酸 的反应要比
Na2CO3与稀盐酸 的反应剧烈得多。
侯小杰
碳酸钠和碳酸氢钠的性质比较
实验探究 碳酸钠和碳酸氢钠的性质比较
③碳酸钠和碳酸氢钠的热稳定性比较 结论: NaHCO3受热易 分解,而Na2CO3 比较稳定。
侯小杰
俗名 色态 溶解性
热稳定性
Na2CO3
苏打、纯碱
白色粉末
NaHCO3
小苏打
细ቤተ መጻሕፍቲ ባይዱ白色晶体
侯小杰
俗名 色态 溶解性
热稳定性
Na2CO3
苏打、纯碱 白色粉末
NaHCO3
小苏打 细小白色晶体
碳酸钠比碳酸氢钠易溶于水
稳定
2 Na 3 H N 2 C C a 3 O C O 2 O H 2 O
侯小杰
此课件下载可自行编辑修改,仅供参考! 感谢您的支持,我们努力做得更好!谢谢
侯小杰
产生白色沉淀
不反应
与碱 烧 碱
反应
石灰水
不反应
O H H3 C C O 3 2 O H 2 O
碳酸钠与碳酸氢钠对比表格PPT课件
NaHCO3
NaHCO3+HCl=NaCl+ H2O +
HCO3-+H+=H2O+CO2↑
CO2↑
B 与碱反应
Na2CO3
与NaOH不反应, 无现象
NaHCO3+NaOH=Na2CO3+H2O NaHCO3 HCO3-+OH -=CO32-+H2O
反应,但无明显现象
Na2CO3:
易与Ba(OH)2、Ca(OH)2 反应生成碳酸盐沉 淀和NaOH
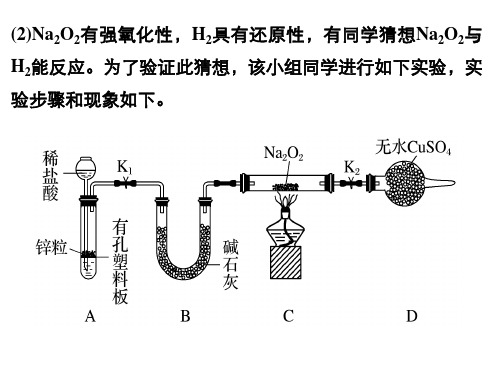
(2)Na2O2有强氧化性,H2具有还原性,有同学猜想Na2O2与 H2能反应。为了验证此猜想,该小组同学进行如下实验,实 验步骤和现象如下。
碳酸钠与碳酸氢钠性质的比较
名称
碳酸钠
碳酸氢钠
①俗名 纯碱、苏打 小苏打
②色态
白色粉末 白色细小晶体
③溶解性
>
④溶液碱性
>
⑤与酸反应速率 ⑥与BaCl2反应 ⑦NaOH反应 ⑧ Ca(OH)2反应
<
白色沉淀
不反应 白色沉淀
无现象 反应 白色沉淀
碳酸钠与碳酸氢钠性质的比较
名称
碳酸钠
碳酸氢钠
①溶于水放热
>
②热稳定性
>
③相互转化
Na2CO3
CO2 + H2O
(1)固体: 加热 (2)溶液: NaOH
NaHCO3
A、与 酸 反 应
Na2CO3+2HCl=2NaCl+H2O+CO2↑
Na2CO3 CO32 -+2H+= H2O + CO2↑
Na2CO3+Ca(OH)2=CaCO3 +2NaOH
碳酸钠与碳酸氢钠对比表

碳酸钠与碳酸氢钠对照表
1 / 1
碳酸钠和碳酸氢钠的性质比较
名称 碳酸钠( Na 2CO 3)
碳酸氢钠( NaHCO 3 )
俗名
色 态
白色晶体
渺小白色晶体
易溶于水(但比
Na CO
),溶
水溶性
易溶于水,溶液呈
性
23 溶解度
液呈 性
稳固性 稳固,但结晶碳酸钠( Na 2 CO 3 10 H 2 O ) 不稳固,受热易分解,方程式: 易风化
与 H +反 少许 H +: 少许 H +: 应
足量 H +: 足量 H +: 与碱反
与 Ca(OH)
现象:
与
现象:
应
离子方程式:
离子方程式:
2
Ca(OH)2
与 NaOH 离子方程式:
与 NaOH
离子方程式:
与盐 CaCl 2
CaCl 2
反响
硫 酸 硫 酸
铝
铝
主要用 玻璃 造纸
制造 清洗
发酵 医药 灭火器
途
互相转 化
等浓度 PH 大小 比较
鉴识 Na 2 CO 3 NaHCO 3 的方法。
碳酸钠和碳酸氢钠性质比较ppt课件

7
二、化学性质
2、与 酸 反 应
结论:
等质量的碳酸钠和碳酸氢钠都易与酸反 应,但是碳酸氢钠与酸反应产生气体速度 快且多。
8
二、化学性质
溶解性
碳酸钠比碳酸氢钠易溶于水
4
结论:
Na2CO3
NaHCO3
碱性: Na2CO3 〉NaHCO3
5
二、化学性质
1、热稳定性
结论:
① NaHCO3不稳定,受热可分解 ② Na2CO3 稳定, 受热不分解
应用: 此性质可鉴别Na2CO3固体和NaHCO3固体
6
分组合作探究等质量的Na2CO3和 NaHCO3与盐酸的反应
3、与碱 反 应
4、与 盐 反 应
结论:
碳酸钠与氯化钙反应生成白色沉淀; 碳酸氢钠与氯化钙不反应
应用: 此性质可鉴别Na2CO3溶液和NaHCO3溶液
9
俗名 色态 溶解性 热稳定性
Na2CO3
NaHCO3
苏打、纯碱
小苏打
白色粉末
细小白色晶体
碳酸钠比碳酸氢钠易溶于水
稳定
受热易分解
与酸反应 2H++CO32-=CO2↑+H2O
1.下列说法中不正确的是
()
D
A.相同条件下, Na2CO3比NaHCO3易溶于水 B.Na2CO3比NaHCO3稳定 C. 饱和的Na2CO3溶液比NaHCO3溶液的碱性强
D.物质的量相等的Na2CO3和NaHCO3分别与足量稀盐酸反
【最新】碳酸钠和碳酸氢钠

【最新】碳酸钠和碳酸氢钠
碳酸钠和碳酸氢钠是在人们上中学时就熟知的两种化学用品,虽然它们只差一个字,但是还是有一定的区别。
碳酸钠又叫纯碱,是重要的有机化学品之一,俗名叫“苏打”,易溶于水,溶液呈较强的碱性,可以水解油脂,因此可以用来做洗涤剂,清洁油污,也可用来做肥皂。
碳酸氢钠俗名“小苏打”,为弱碱,可以中和盐酸,反应快速且柔和,因此也被作为胃药,内服后,治疗胃酸过多的症状。
一、碳酸钠和碳酸氢钠的性质
1、碳酸钠外观呈白色粉末,加热至815°C才融化但不分解,稳定性较强,受热不易分解。
工业碳酸钠具有弱刺激性和腐蚀性,如果皮肤不小心碰到其溶液,请立即用大量水溶液冲洗,如果误服碳酸钠,请立即漱口,并饮用牛奶或者鸡蛋,以减轻溶液中碱性物质对消化系统的腐蚀。
另外碳酸钠也可以作为食用纯碱,主要用来软化肉质,泡软干货。
还可以用来蒸馒头,可迅速中午面点发酵产生的酸性物质,但是也不能过多使用。
2、碳酸氢钠外观呈白色细小晶体,性质不稳定、固体碳酸氢钠受热即分解成水和二氧化碳。
在50多度的热水既可融化分解,小苏打可破坏肉质纤维结构,使肉质松软膨胀,鲜嫩爽滑,也可以用来制作蛋糕、面点等,原因是其分解产生的气体可以使馒头、包子等食物多孔松软。
二、碳酸钠和碳酸氢钠的区别
总体说来,碳酸钠有一定的化学腐蚀性,不可经常大量接触。
而碳酸氢钠性质更温和,在平时生活使用中,请注意分清。
— 1 —。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
*欧阳光明*创编 2021.03.07
一、 Na2CO3与 NaHCO3性质比较
二、Na2CO3与 NaHCO3的相互转化
三、如何区分Na2CO3与 NaHCO3
1、加热观察是否分解:能够分解产生能使澄清石灰水变浑浊的无色无味的气体的为NaHCO3,不分解的为Na2CO3
2、取等质量的固体(或等浓度等体积的Na2CO3与NaHCO3的溶液)分别与盐酸,反应观察剧烈程度,剧烈的为NaHCO3
3、加CaCl2,看是否有沉淀生成;有沉淀生成的为Na2CO3,无沉淀生成的为NaHCO3
四、CO32—与HCO3—的检验方法
①CO32—的检验方法:先加CaCl2溶液,产生白色沉淀,再加稀盐酸沉淀溶解并产生无色
无味的能使澄清石灰水变浑浊的气体
②HCO3—的检验方法:先加CaCl2溶液,无现象,再加稀盐酸产生无色无味的能使澄清石灰水变浑浊的气体
*欧阳光明*创编 2021.03.07。
