表面现象PPT课件
合集下载
表面现象

G r Vm ( ' p RTr r
开尔文公式
8prdr 2 p 2 4pr dr r
Vm M r
开尔文公式解释日常生活中的现象:(P289) 人工降雨的原理
(3)液体的润湿与铺展 P
(l/g)
N
M
P298 例题
8.4 溶液的表面吸附
(1)溶液表面的吸附现象
溶液的表面吸附是指——溶质在表面 层中与本体溶液中浓度不同的现象。
溶质 溶剂
溶液 正吸附:溶质在表面的浓度大于本体浓度 (可溶性有机化合物,如醇、醛、酸、酯等)
负吸附:溶质在表面的浓度小于本体浓度
(无机电解质,如无机盐和不挥发性无机酸、碱等)
pdV dA
pdV dA
p
dA
dV
2
A 4pr
4 3 V pr 3
8prdr 2 p 2 4pr dr r
拉普拉斯公式
附加压力与液体的表面张力成正比,与曲率半径成反比。
a. 对空气中的液滴(凸液面), p'= p+Δp
b. 液体中的气泡(凹液面), P =p‘+Δp c. 水平液面, p'=p d. 对液泡, 泡内气压比泡外的要大,其差值为Δp=4σ/r
(s/g) O
O
(s/l)
接触角与各表面张力的关系
接触角:σ(l-g)与σ(s-l)的夹角。 平衡时有: (s g ) (s l ) (l g ) cos
0
(s g ) (s l ) cos (l g )
(s g ) (s l ) cos (l g )
P291 用毛细管现象解释锄地保墒的原理。
开尔文公式
8prdr 2 p 2 4pr dr r
Vm M r
开尔文公式解释日常生活中的现象:(P289) 人工降雨的原理
(3)液体的润湿与铺展 P
(l/g)
N
M
P298 例题
8.4 溶液的表面吸附
(1)溶液表面的吸附现象
溶液的表面吸附是指——溶质在表面 层中与本体溶液中浓度不同的现象。
溶质 溶剂
溶液 正吸附:溶质在表面的浓度大于本体浓度 (可溶性有机化合物,如醇、醛、酸、酯等)
负吸附:溶质在表面的浓度小于本体浓度
(无机电解质,如无机盐和不挥发性无机酸、碱等)
pdV dA
pdV dA
p
dA
dV
2
A 4pr
4 3 V pr 3
8prdr 2 p 2 4pr dr r
拉普拉斯公式
附加压力与液体的表面张力成正比,与曲率半径成反比。
a. 对空气中的液滴(凸液面), p'= p+Δp
b. 液体中的气泡(凹液面), P =p‘+Δp c. 水平液面, p'=p d. 对液泡, 泡内气压比泡外的要大,其差值为Δp=4σ/r
(s/g) O
O
(s/l)
接触角与各表面张力的关系
接触角:σ(l-g)与σ(s-l)的夹角。 平衡时有: (s g ) (s l ) (l g ) cos
0
(s g ) (s l ) cos (l g )
(s g ) (s l ) cos (l g )
P291 用毛细管现象解释锄地保墒的原理。
第十一章 表面现象

即内压为p1=p0 +2/
=101325+2×58.9×10-3÷(10-6/2)
=3.369×105Pa
按克-克方程,可求得水过热蒸气压 3.369×105Pa时沸点
Ln(3.369×105/101325)=(-40660/8.314)(1/T-
1/373)
T=410.6K
即过热410.6-373.2=37.4K
6.
在293K时,当水银被分散成半径为1×107cm的微小汞粒时其蒸汽压为多少?这时气 体中饱和水银蒸汽含量以mg/cm3计算有多 少?(已知293K时一般状态下水银蒸汽压 为1.73×10-4kPa、气体中饱和水银蒸汽含量 为14.3mg/m3,水银表面张力为471.6×103N/m。)
按Kelvin公式 RTln(Pr/P0)=2M/r0 RTln(Pr/P0)=2×471.6×10-3×200.6×10-3/(1×10-
9×13.6×103)
=13870.6
Pr/P0 =297.08 Pr =297.08 ×2.73×10-4×103=51.39Pa (即半径为1×10-7cm水银微粒的蒸气压) 因蒸气压之比等于其含量之比,故
pr/p0 =297.08=m/14.3 M=4248mg/m3
7.
在298K时,已知平均半径为3×10-5cm的石 膏(CaSO4)微粒,在水中溶解度为 18.2mmol/dm3;半径大于2×10-4cm的颗粒 与普通硫酸钙溶解度相同为15.33mmol/dm3; 若石膏的摩尔体积为59cm3;试计算固体硫 酸钙与水之间的界面张力?
根据Kelvin公式
RTln(Cr/C0)=2 SH /rS= 2 SVm·s/r S =(RTr/2Vm·s)ln(Cr/C0)
第七章表面现象

这些力的作 用最终会使液 滴成球形. 滴成球形.
(三)毛细现象 毛细现象是证明表面张力存在的一个典型的例子, 毛细现象是证明表面张力存在的一个典型的例子, 是证明表面张力存在的一个典型的例子 正是表面张力引起的弯曲液面的附加压力使得和毛细 管壁润湿的液体沿毛细管上升. 管壁润湿的液体沿毛细管上升. 2σ cosθ h= ρ液gR 当液体可以润湿毛细管壁, 当液体可以润湿毛细管壁,即形 凹形液面时 成凹形液面时,θ < 90°,h > 0,毛 ° , 细管内液面上升; 细管内液面上升; 若液体不能润湿毛细管壁, 若液体不能润湿毛细管壁,即形 凸液面时 成凸液面时,θ > 90°,h < 0,毛细 ° , 管内液面下降,低于正常液面. 管内液面下降,低于正常液面.
三,表面张力与温度的关系 温度升高,界面张力下降,当达到临界温度 温度升高,界面张力下降,当达到临界温度Tc 界面张力趋向于零.这可用热力学公式说明: 时,界面张力趋向于零.这可用热力学公式说明:
运用麦克司韦关系式,可得: 运用麦克司韦关系式,可得:
S σ = A T , p ,nB T A, p ,nB
如果在活动边框上挂一重物, 如果在活动边框上挂一重物, 使重物质量W 与边框质量W 使重物质量 2与边框质量 1所产 生的重力F与总的表面张力大小相 生的重力 与总的表面张力大小相 等方向相反,则金属丝不再滑动. 等方向相反,则金属丝不再滑动. 上述现象表明:在液体表面存 上述现象表明: 在着一种使液面收缩的力, 在着一种使液面收缩的力,称为表 面张力.它的方向和表面相切, 面张力.它的方向和表面相切,垂 直作用在单位长度线段上的表面收 缩力. 缩力.
二,曲面的蒸气压 (一)弯曲液面的蒸气压——开尔文公式 弯曲液面的蒸气压 开尔文公式 用热力学的基本原理可以导出在指定温度下液体 的蒸气压和曲率半径之间的关系. 的蒸气压和曲率半径之间的关系. 的球形液滴或气泡,在温度T 曲率半径为 r 的球形液滴或气泡,在温度 下的 蒸气压为 pr* ,液体在此温度下的正常蒸气压为 p*
(三)毛细现象 毛细现象是证明表面张力存在的一个典型的例子, 毛细现象是证明表面张力存在的一个典型的例子, 是证明表面张力存在的一个典型的例子 正是表面张力引起的弯曲液面的附加压力使得和毛细 管壁润湿的液体沿毛细管上升. 管壁润湿的液体沿毛细管上升. 2σ cosθ h= ρ液gR 当液体可以润湿毛细管壁, 当液体可以润湿毛细管壁,即形 凹形液面时 成凹形液面时,θ < 90°,h > 0,毛 ° , 细管内液面上升; 细管内液面上升; 若液体不能润湿毛细管壁, 若液体不能润湿毛细管壁,即形 凸液面时 成凸液面时,θ > 90°,h < 0,毛细 ° , 管内液面下降,低于正常液面. 管内液面下降,低于正常液面.
三,表面张力与温度的关系 温度升高,界面张力下降,当达到临界温度 温度升高,界面张力下降,当达到临界温度Tc 界面张力趋向于零.这可用热力学公式说明: 时,界面张力趋向于零.这可用热力学公式说明:
运用麦克司韦关系式,可得: 运用麦克司韦关系式,可得:
S σ = A T , p ,nB T A, p ,nB
如果在活动边框上挂一重物, 如果在活动边框上挂一重物, 使重物质量W 与边框质量W 使重物质量 2与边框质量 1所产 生的重力F与总的表面张力大小相 生的重力 与总的表面张力大小相 等方向相反,则金属丝不再滑动. 等方向相反,则金属丝不再滑动. 上述现象表明:在液体表面存 上述现象表明: 在着一种使液面收缩的力, 在着一种使液面收缩的力,称为表 面张力.它的方向和表面相切, 面张力.它的方向和表面相切,垂 直作用在单位长度线段上的表面收 缩力. 缩力.
二,曲面的蒸气压 (一)弯曲液面的蒸气压——开尔文公式 弯曲液面的蒸气压 开尔文公式 用热力学的基本原理可以导出在指定温度下液体 的蒸气压和曲率半径之间的关系. 的蒸气压和曲率半径之间的关系. 的球形液滴或气泡,在温度T 曲率半径为 r 的球形液滴或气泡,在温度 下的 蒸气压为 pr* ,液体在此温度下的正常蒸气压为 p*
物理化学第十章表面现象

P = P 0 + P
P = P 0 P
图10-8 弯曲液面的附加压力
§10-3 弯曲液面的附加压力和毛细现象 这种弯曲液面内外的压力差,就称之为附加压力,用 P 来表示。
P = P内 P外 = P P 0
附加压力的方向总是指向曲率中心。 二、拉普拉斯(Laplace)方程 附加压力的大小与弯曲液面曲率半径有关 。
Ga = γ s l (γ s g + γ l g ) = Wa'
图10-4 沾湿过程
§10-2 润湿现象与接触角
则此过程中, Wa' 即称为沾湿功。 对于一个自发过程来讲, Wa' > 0 。 Wa' 外
W a' 所做的最大功。
ቤተ መጻሕፍቲ ባይዱ是液固沾湿时,系统对
值愈大,液体愈容易润湿固体。
(2)浸湿(immersional wetting) 所谓浸湿是指当固体浸入液体中,气—固界面完全被 固—液界面所取代的过程。如图10-5所示: 在恒温恒压可逆情况下,将具有单位表面积的固体 浸入液体中,气—固界面转变为液固界面,在该过 程中吉布斯函数的变化值为 Gi = γ s l γ s g = Wi
γ s g = γ s l + γ l g cos θ
cos θ =
γ
sg
γ
sl
γ l g
1805年杨氏(TYoung)曾得到此式,故称其为杨氏方程。 1)当 θ > 90 0 时, cosθ < 0 即 γ s g < γ s l
G = γ s l γ s g > 0
γ s g > γ s l 2)当θ < 90 0 时, θ > 0 cos 液体润湿固体过程中能自动发生,液体有扩大固—液界面的趋势,
P = P 0 P
图10-8 弯曲液面的附加压力
§10-3 弯曲液面的附加压力和毛细现象 这种弯曲液面内外的压力差,就称之为附加压力,用 P 来表示。
P = P内 P外 = P P 0
附加压力的方向总是指向曲率中心。 二、拉普拉斯(Laplace)方程 附加压力的大小与弯曲液面曲率半径有关 。
Ga = γ s l (γ s g + γ l g ) = Wa'
图10-4 沾湿过程
§10-2 润湿现象与接触角
则此过程中, Wa' 即称为沾湿功。 对于一个自发过程来讲, Wa' > 0 。 Wa' 外
W a' 所做的最大功。
ቤተ መጻሕፍቲ ባይዱ是液固沾湿时,系统对
值愈大,液体愈容易润湿固体。
(2)浸湿(immersional wetting) 所谓浸湿是指当固体浸入液体中,气—固界面完全被 固—液界面所取代的过程。如图10-5所示: 在恒温恒压可逆情况下,将具有单位表面积的固体 浸入液体中,气—固界面转变为液固界面,在该过 程中吉布斯函数的变化值为 Gi = γ s l γ s g = Wi
γ s g = γ s l + γ l g cos θ
cos θ =
γ
sg
γ
sl
γ l g
1805年杨氏(TYoung)曾得到此式,故称其为杨氏方程。 1)当 θ > 90 0 时, cosθ < 0 即 γ s g < γ s l
G = γ s l γ s g > 0
γ s g > γ s l 2)当θ < 90 0 时, θ > 0 cos 液体润湿固体过程中能自动发生,液体有扩大固—液界面的趋势,
表面现象
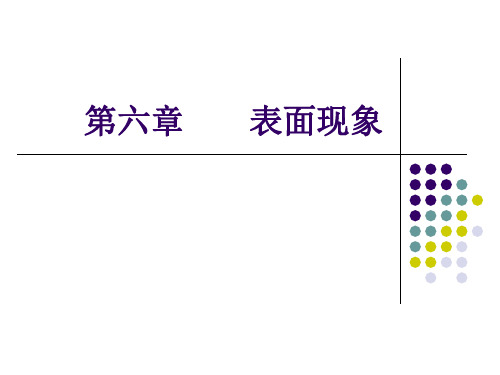
g -l
若σs-g-σs-l =σg-l ,cos=1,= 0,完全润湿; 若 σs-g-σs-l < σg-l , 0< cos < 1, 0 < < 90,润
湿; 若σs-g < σs-l , cos < 0, 90 < < 180,不润湿
防雨设备, 农药配制, 机械润滑, 矿物浮选, 注水采油, 金属焊接, 印染及洗涤等方面都与润湿有关。 药物制剂中很多方面要用到润湿,如外用的散剂, 片剂中的崩解剂,注射瓶中的针剂。
第六章
表面现象
引 言
•界面: 两相的接触面. 其中一相为气相的界 面习惯上称为表面. •界面现象是自然界中普遍存在的基本现象, 如润湿现象,毛细现象, 过饱和(过冷, 过热等) 现象, 吸附现象等. •产生界面现象的主要原因是处于界面层中的 分子与物质内部的分子存在力场上的差异, 两 者的化学势大小不相等. •高度分散的物质具有巨大的界面积,往往产生 明显的界面效应.
固定的 障片
可移动 的障片
• 油酸单分子膜示意图
二、表面活性剂的分类
阴离子表面活性剂 如肥皂 RCOONa 离子型表 面活性剂
阳离子表面活性剂
如胺盐 C18H37NH3+Cl-
表面活性 物质分类
非离子型 表面活性剂
两性表面活性剂
如氨基酸型R-NH-H2COOH 如聚乙二醇类 HOCOH2[CH2OCH2]nCH2OH
σ
I 无机酸, 碱, 盐等.
σ0
Ⅱ 有机酸, 醇, 酯, 醚, 酮等.
Ⅲ 肥皂, 合成洗 涤剂等. c
• 水溶液表面张力与溶质浓度的关系
二、吉布斯吸附等温式
c d 吉布斯吸附等温式: RT dc T
表面现象的含义
表面现象的含义
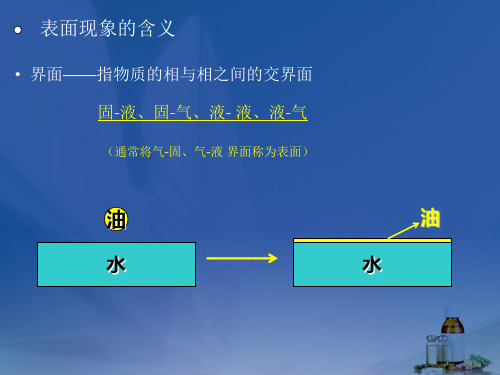
• 界面——指物质的相与相之间的交界面 固-液、固-气、液- 液、液-气
(通常将气-固、气-液 界面称为表
• 表面(界面)现象——指在物质相与相之间的表面上,由于表 面分子与内部分子性质的差异,而产生的一系列物理化学现象
气相 表面
液相
液相分子对表面层分子的引力远大于气相分子对它的引力,因而表面层分子 受到一个垂直于液体表面并指向液体内部的合力,该力试图将它拉向液体内 部
表面现象在药剂中应用
• 在药物的提取和精制、发酵过程
中经常出现的过冷、过热、吸附、
解吸附、发泡、消泡、胶体形成
与破坏等各种界面或表面现象;
活性炭——吸附
水 (蒸 加气 热蒸 )馏
表面现象在药剂中应用
• 具体剂型如薄膜制剂、静脉注射乳状液、固体分散剂等剂型制 备过程中也会出现表面现象;
• 皮肤给药的透皮吸收、难溶性药物的胃肠道释放和吸收等均与 表面现象有着密切的关系。
物理化学第九章--表面现象

p0
A
ps
p0 − ps
ps
p0
附加压力总是指向曲面的球心
A
溶液
9.2.2 Laplace 公式 在毛细管内充满液体,管端有的球状液滴半径为 ′与之平衡。 在毛细管内充满液体,管端有的球状液滴半径为R′与之平衡。 液滴所受总压为: 液滴所受总压为 对活塞稍加压力: 对活塞稍加压力 液滴体积增加dV 液滴体积增加 相应表面积增加dA 相应表面积增加 s 克服附加压力p 克服附加压力 s所做的功等于可 逆增加表面积的Gibbs自由能 自由能 逆增加表面积的
边长10 → 边长 -2m→10-9m,比表面增长了一千万倍。 ,比表面增长了一千万倍。 高度分散的物质系统具有巨大的表面积, 高度分散的物质系统具有巨大的表面积,往往产生明显 的界面效应,因此必须充分考虑界面性质对系统的影响。 的界面效应,因此必须充分考虑界面性质对系统的影响。
9.1.2 表面自由能 表面功 δWf,R= γdAS ( )T,P,nB δWf,R= (dG)T,P,R
溶液的过饱和现象— 溶液的过饱和现象
亚 稳 状 态
液体的过冷现象— 液体的过冷现象
毛细凝聚
9.4 溶液的表面吸附
9.4.1 表面活性物质与非表面活性物质 (1) 非表面活性物质 无机盐和不挥发的酸、 无机盐和不挥发的酸、碱 (2) 表面活性物质 碳链较短的脂肪酸、 碳链较短的脂肪酸、醇、 胺等有机化合物。 酮、醛、胺等有机化合物。 (3) 表面活性剂 碳氢链中含有8个碳以上的 碳氢链中含有 个碳以上的 有机酸的各种盐 转折处的极小值 转折处的极小值 : 杂质的影响
p↑,气体分子易被液面吸附 ↑ 气体分子易被液面吸附; 一般p↑ 液体的 一般 ↑,液体的γ↓,因为 p↑,气体在液体中的溶解度增加。 ↑ 气体在液体中的溶解度增加。
第五节表面现象

二、表面吸附
表面吸附:物质在两相界面上浓度与内部浓度不同的现象。 吸附剂:吸附其他物质的物质。 吸附质:被吸附的物质。 1.固体表面的吸附
表面的原子—表面张力—吸引分子、离子—聚集—减小表面 张力—降低表面能—稳定。 当其他条件相同时,固体表面积越大,固体吸附剂的吸附能 力就越大。
2.液体表面的吸附
ቤተ መጻሕፍቲ ባይዱ
疏水基团
亲水基团
(二)表面活性物质的应用
1.乳化剂 使乳浊液稳定的物质 乳化作用:乳化剂所起的作用 乳剂:由水、油和乳化剂形成的乳浊液。
乳剂类型
水包油型(O/W) 油包水型(W/O)
乳剂示意图 (a)O/W(b)W/O
表面活性物质的应用
2.润湿剂 润湿:液体在固体表面粘附的现象。 润湿剂:能改善润湿程度的表面活性物质。
第五节
表面现象
表面:物体与空气或与其本身的蒸气接触的面。 如水面、桌面。 界面:物体与另一个凝聚相接触的面。 如水与油接触的面。 表面现象:一切界面上所发生的现象。 一、表面张力与表面能
图1-3 表面张力
表面张力:表面分子受到的指向内部的力。
表面能:液体表面层分子比内部分子所多出的能量。 表面张力越大,表面能就越高;表面积越大,表面能也越高。
基本性质、应用
液体表面也会因某种溶质的加入而产生吸附,使液体表面张 力发生相应的变化。 表面活性物质(表面活性剂):能够显著降低液体表面张力 的物质。 表面惰性物质:能增大液体表面张力的物质。
三、表面活性物质
表面活性物质:能够显著降低水的表面张力的物质 (一)表面活性物质的基本性质 结构特点——分子中同时有疏水基团(烷烃基) 和亲水基团(羧基、氨基)。 例如:肥皂(高级脂肪酸钠)
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
.
19
第九章 表面现象
9.2 弯曲液面下的附加压力和弯曲液面上的蒸气压
9.2.1 弯曲液面下的附加压力
9.2.1.1 弯曲液面下的附加压力
(1)平面
表面张力的方向与液面
相切,如果液面是水平的,
则表面张力也是水平的。平
衡时,沿环形面积AB周界
的表面张力相互抵消,此时
液体表面内外的压力相等,
即
p=p0
第九章 表面现象
.
1
第九章 表面现象
.
2
第九章 表面现象
9.1 比表面吉布斯自由能和表面张力
9.2 弯曲液面下的附加压力和弯曲液 面上的蒸气压
9.3 溶液的表面吸附
9.4 表面活性物质 9.5 液-固界面的润湿作用 9.6 固体表面对气体的吸附
9.7 固体在溶液中的吸附
.
3
第九章 表面现象
界面:两相的接触面
比表面:表示物质分散程度的物理量。单位 体积或单位质量的物质所具有的表
面积,单位是m-1或m2·kg -1。 用符号S0表示
S0
A V
或
S0
A m
式中A是体积为V(m3)或质量为m(kg)的物质 所具有的总表面积。
.
11
第九章 表面现象 系统的分散程度很高时,表面现象不能忽略 例:大水滴分散成微小水滴
WdA
式中σ为比例系数,它在数值上等于当T,P及 组成恒定的条件下,增加单位表面积时所必须 对体系做的可逆非体积功。
.
15
第九章 表面现象
在定温定压可逆条件下
WdG T,p
因此 G
A T , p
单位J·m-2
比表面吉布斯σ的物理意义: (1) 在定温定压和组成恒定的条件下,增加单位 表面积引起系统吉布斯自由能的增量。 (2) 当以可逆方式增加新表面时,环境对系统所 做的表面功转化为表面层分子的吉布斯自由能。
A
B
.
20
第九章 表面现象 (2)凸面或凹面
对于弯曲液面,
沿AB周界上的表面张
力不是水平的,其方
向垂直于周界且与液
面相切。平衡时,表
面张力将产生一合力,
指向曲面曲率半径的 中心,此时液面内外
A
压差,即附加压力
p内p外p
.
B
A
B
21
第九章 表面现象
9.2.1.2 拉普拉斯公式
(1)在毛细管内充满液体,管 端有半径为R′的球状液滴与之平 衡。外压为 p0 ,附加压力为 Δp, 液滴所受总压为
1. 注:
2. (1) 纯液体的表面张力通常是指液体与其饱
和
31.. (2) 了如本果身共蒸存气的的另空一气相接为触其时他测物得质的时数,据则。因
为
2.
另一相中的其他物质对液体表面层分子
的
31.. (3) 作作用用力在不液同—,液所或以液表—面固张界力面也上就的可张能力有称
相为
42..
当 界大面的张变力化。。
(2) 它们是两个不同的概念,都是客观存在并
相
(3) 互联系的,是从不同的角度来反映系统的
表 (14.) (2) 是面强特度征性。质,数值与物质的种类,共存另
一
2.
相温的度性升质高以,及表温面度张、力压下力降等,因即素有关 。 0
T p
压力升高,表面张力下降,即
p
T
0
.
18
第九章 表面现象
(3)Δp方向指向曲率半径的中心。
.
24
第九章 表面现象
解释常见现象:
(1)液滴为何呈球形或椭球形
出现不规则的弯曲形状的液滴, 在液面不同部位,其弯曲方向和曲 率都不同,由此产生的附加压力也 不同,在凸面处附加压力指向液体 内部,而在凹面处则指向相反的方 向,这种不平衡的力必将迫使液滴 变形。
r
拉普拉斯公式
.
23
第九章 表面现象
9.2.1.2 拉普拉斯公式 关于拉普拉斯公式:
(1)附加压力与液面曲率半径有关。液滴愈小, 所受到的附加压力愈大。
(2)当弯曲液面为凸面时,r>0,Δp>0,即凸 面下液体所受到的压力比平面下要大;当液面为凹 面时,r<0,Δp<0,即凹面下液体所受到的压力比 平面下要小。如液面为平面,可以认为r →∞,故 Δp=0,这时液面下压力等于外压力。
气-液界液-固界面 液-液界面
与气体接触的 界面也称表面 即,气液表
面 和气固表
面
.
4
第九章 表面现象
气-液界面
.
5
第九章 表面现象
气-固界面
.
6
第九章 表面现象
液-液界面
.
7
第九章 表面现象
液-固界面
.
8
第九章 表面现象
液-液界面
.
9
第九章 表面现象
关于界面:
p0+Δp (2)对活塞稍加压力,将毛细管 内液体压出少许,使液滴体积增 加dV,相应地其表面积增加dA。 环境克服附加压力所作的功与可 逆增加表面积的吉布斯自由能增 加相等。
.
22
第九章 表面现象 9.2.1.2 拉普拉斯公式
pdVdA
A4r2 d A 8rdr
V4r3dV4r2dr
3
因此 p 2
(1)界面并不是两相接触的几何面,它有一 定的厚度,厚度为纳米级,大约是单分子层或 几个分子层。
(2)界面两侧的两相中物质的物理性质和化学 性质是不同的,但在相界面处,物质的性质又 和两相内部物质的性质都不相同。界面是系统 中特殊的部分。
.
10
第九章 表面现象
9.1 比表面吉布斯自由能和表面张力
9.1.1 比表面
分成1021个
半径1cm
总表面积 1.26×10-3 m2 比表面积 3×10-1m2·kg-1
1
.
半径1nm
1.26×104m2 3×106 m2·kg-
12
第九章 表面现象
9.1.2 比表面吉布斯自由能
任何两相界面上的分子所处的环境与本体内部的 分子不同,相界面的分子所处力场不对称。
处在液体表面上的分 子所受的合力不等于 零,其合力垂直于液
.
16
第九章 表面现象
9.1.3 表面张力
实验:金属丝移
动dx的距离扩
展皂膜,皂膜
有上下两个面,
因此
F2l
F 2l
表面张力:在相表面的切面上,垂直作用于表面
上任意单位长度切线上的表面紧缩力,
单位是N·m-1。
.
17
第九章 表面现象
比表面吉布斯自由能与表面张力:
(1) 数值上相同,量纲相同,但物理意义不同。
面而指向液体内部。
.
13
第九章 表面现象
由于液体表面分子的受力不均,在没有其 它作用力存在时,所有的液体都有缩小表面积 的自发趋势。
相反,若要扩展液体的表面,即把一部分分 子从内部移到表面上来,就必须克服液体内部分 子之间的吸引力而对系统做功,此功称为表面功。
.
14
第九章 表面现象
在温度、压力和组成恒定时,可逆地扩展 液体表面积,环境对系统所做的表面功δW′应 与增加的表面积dA成正比。若以 表示比例系 数,则
