初中化学用语全
化学用语集锦
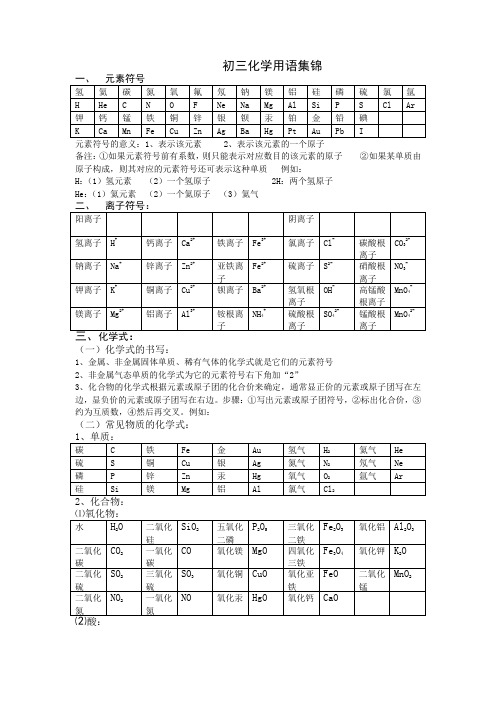
初三化学用语集锦元素符号的意义:1、表示该元素 2、表示该元素的一个原子备注:①如果元素符号前有系数,则只能表示对应数目的该元素的原子②如果某单质由原子构成,则其对应的元素符号还可表示这种单质例如:H:(1)氢元素(2)一个氢原子 2H:两个氢原子He:(1)氦元素(2)一个氦原子(3)氦气(一)化学式的书写:1、金属、非金属固体单质、稀有气体的化学式就是它们的元素符号2、非金属气态单质的化学式为它的元素符号右下角加“2”3、化合物的化学式根据元素或原子团的化合价来确定,通常显正价的元素或原子团写在左边,显负价的元素或原子团写在右边。
步骤:①写出元素或原子团符号,②标出化合价,③约为互质数,④然后再交叉。
例如:(二)常见物质的化学式:其他:过氧化氢 H2O2甲烷 CH4乙醇 C2H5OH 醋酸CH3COOH 葡萄糖C6H12O6尿素 CO(NH2)2O附录一、常见物质的颜色1、固体的颜色2、溶液中离子的颜色3、沉淀的颜色二、火焰的颜色三、离子的共存离子能否共存取决于两种离子相遇后能否生成水、气体或沉淀,如能生成上述物质则离子不能共存。
常见的有:1、H+和OH-会反应会生成H2O2、NH4+和OH-生成NH3和H2O3、H+和CO32-会生成H2CO3,分解后生成H2O和CO2气体4、Ca2+和CO32-会生成CaCO3沉淀,Cu2+、Fe3+与OH-会生成Cu(OH)2、Fe(OH)3沉淀,Ag+与Cl-生成AgCl沉淀,Ba2+与SO42-、CO32-生成BaSO4和BaCO3沉淀。
初中全部化学方程式方程式:4H2O+3Fe 高温Fe3O4+4H2式量: 72 168 232 8描述:赤热的铁跟水蒸气反应生成四氧化三铁和氢气。
方程式:4FeS2+11O2 高温2Fe2O3+8SO2式量: 480 352 320 512描述:燃烧硫铁矿(主要成分是FeS2)生成Fe2O3和SO2方程式:C+O2 点燃CO2式量: 12 32 44 描述:碳在氧气中充分燃烧方程式:S+O2 点燃SO2式量: 32 32 64 描述:硫粉在空气中燃烧方程式:4P+5O2 点燃2P2O5式量: 124 160 284 描述:红磷在空气中燃烧方程式:3Fe+2O2 点燃Fe3O4式量: 168 64 232 描述:铁在氧气中燃烧方程式:2C2H2+5O2 点燃4CO2+2H2O式量: 52 160 176 36 描述:方程式:CH4+2O2 点燃CO2+2H2O式量: 16 64 44 36 描述:甲烷在空气中燃烧方程式:2H2+O2 点燃2H2O式量: 4 32 36 描述:氢气中空气中燃烧方程式:2Mg+O2 点燃2MgO式量: 48 32 80 描述:镁在空气中燃烧方程式:2Cu+O2 △2CuO式量: 127 32 159 描述:铜在空气中受热方程式:4Al+3O2 △2Al2O3式量: 108 96 204 描述:铝在空气中燃烧方程式:2KClO3 △2KCl+3O2↑式量: 245 149 96描述:加热氯酸钾方程式:2KClO3MnO2△2KCl+3O2↑式量: 245 149 96描述:加热氯酸钾(有少量的二氧化锰)方程式:2KMnO4 △K2MnO4+MnO2+O2↑式量: 316 197 87 32 描述:加热高锰酸钾方程式:NH4HCO3 △NH3↑+H2O+CO2↑式量: 79 17 18 44 描述:方程式:Cu2(OH)2CO3 △2CuO+CO2↑+H2O式量: 221 159 44 18描述:加热碱式碳酸铜方程式:2HgO △2Hg+O2↑式量: 434 402 32 描述:方程式:2H2O 电解2H2↑+2O2↑式量: 36 4 64描述:水在直流电的作用下分解方程式:Zn+H2SO4 ZnSO4+H2↑式量: 65 98 161 2描述:锌和稀硫酸方程式:Mg+H2SO4 MgSO4+H2↑式量: 24 98 120 2描述:镁和稀硫酸方程式:Zn+2HCl ZnCl2+H2↑式量: 65 73 136 2描述:锌和稀盐酸方程式:Fe+2HCl FeCl2+H2↑式量: 56 73 127 2描述:铁和稀盐酸方程式:ZnO+2HCl ZnCl2+H2O 式量: 81 73 136 18描述:方程式:8Al+3Fe3O4 点燃9Fe+4Al2O3式量: 216 696 504 408 描述:方程式:Al2O3+3H2SO4 Al2(SO4)3+3H2O 式量: 102 294 342 54描述:方程式:CuO+H2 △Cu+H2O式量: 79.5 2 63.5 18描述:氢气还原氧化铜方程式:CuSO4+2NaOH Na2SO4+Cu(OH)2↓式量: 159.5 80 142 97.5描述:方程式:Fe3O4+4CO 高温3Fe+4CO2式量: 232 112 168 176描述:一氧化碳还原四氧化三铁方程式:Fe2(SO4)3+6NaOH 2Fe(OH)3↓+3Na2SO4式量: 400 240 214 426 描述:方程式:MnO2+4HCl △MnCl2+2H2O+Cl2↑式量: 87 146 126 36 71 描述:方程式:2C2H6+7O2 点燃4CO2+6H2O式量: 60 224 176 108描述:方程式:Cu+4HNO3 Cu(NO3)2+2NO2↑+2H2O 式量: 63.5 252 187.5 92 36描述:方程式:Zn+CuSO4 ZnSO4+Cu式量: 65 159.5 161 63.5描述:方程式:2Al+3H2SO4 Al2(SO4)3+3H2↑式量: 54 294 342 6描述:铝和稀硫酸方程式:C2H4+3O2 点燃2CO2+2H2O式量: 28 96 88 36描述:方程式:2Na+2H2O 2NaOH+H2↑式量: 46 36 80 2描述:方程式:CO2+C 高温2CO式量: 44 12 56 描述:方程式:CuO+CO △Cu+CO2式量: 79.5 28 63.5 44 描述:一氧化碳还原氧化铜方程式:2CO+O2 点燃2CO2式量: 56 32 88 描述:一氧化碳在氧气中燃烧方程式:2CuO+C △2Cu+CO2↑式量: 159 12 127 44 描述:木炭还原氧化铜方程式:2Fe2O3+3C 高温4Fe+3CO2↑式量: 320 36 224 132 描述:焦炭还原氧化铁方程式:CO2+H2O H2CO3 式量: 44 18 62描述:二氧化碳溶解于水方程式:H2CO3 H2O+CO2↑式量: 62 18 44描述:碳酸不稳定而分解方程式:CaCO3 高温CaO+CO2↑式量: 100 56 44描述:高温煅烧石灰石方程式:CaCO3+CO2+H2O Ca(HCO3)2式量: 100 44 18 162描述:方程式:Ca(HCO3)2 CaCO3↓+H2O+CO2↑式量: 162 100 18 44描述:方程式:CaCO3+2HCl CaCl2+H2CO3式量: 100 73 111 62描述:方程式:CaCO3+2HCl CaCl2+H2O+CO2↑式量: 100 73 111 18 44描述:大理石与稀盐酸反应方程式:C+H2O 高温CO+H2↑式量: 12 18 28 2描述:方程式:Na2CO3+2HCl 2NaCl2+H2O+CO2↑式量: 106 73 188 18 44 描述:碳酸钠与稀盐酸反应方程式:C2H5OH+3O2 点燃2CO2+3H2O式量: 46 96 88 54 描述:酒精在空气中燃烧方程式:2CH3OH+3O2 点燃2CO2+4H2O式量: 64 96 88 72 描述:方程式:Fe+H2SO4 FeSO4+H2↑式量: 56 98 152 2描述:方程式:Fe+CuSO4 FeSO4+Cu 式量: 56 159.5 152 63.5描述:方程式:Fe2O3+6HCl 2FeCl3+3H2O式量: 160 219 325 54描述:方程式:Cu(OH)2+2HCl CuCl2+2H2O式量: 97.5 73 134.5 36描述:方程式:AgNO3+HCl AgCl↓+HNO3式量: 170 36.5 143.5 63描述:方程式:Fe2O3+3H2SO4 Fe2(SO4)3+3H2O 式量: 160 294 400 54描述:方程式:Cu(OH)2+H2SO4 CuSO4+2H2O式量: 97.5 98 159.5 36描述:方程式:BaCl2+H2SO4 BaSO4↓+2HCl式量: 208 98 233 73描述:方程式:ZnO+2HNO3 Zn(NO3)2+H2O式量: 81 126 189 18描述:方程式:Mg(OH)2+2HNO3 Mg(NO3)2+2H2O 式量: 58 126 148 36描述:方程式:CuO+H2SO4 CuSO4+H2O式量: 79.5 98 159.5 18描述:方程式:NaOH+HCl NaCl+H2O式量: 40 36.5 58.5 18描述:方程式:2NaOH+CO2 Na2CO3+H2O式量: 80 44 106 18描述:方程式:2NaOH+SO2 Na2SO3+H2O式量: 80 64 126 18描述:方程式:2NaOH+H2SO4 Na2SO4+2H2O式量: 80 98 142 36描述:方程式:NaOH+HNO3 NaNO3+H2O式量: 40 63 85 18描述:方程式:2NaOH+CuSO4 Cu(OH)2↓+Na2SO4 式量: 80 159.5 97.5 142描述:方程式:3NaOH+FeCl3 Fe(OH)3↓+3NaCl式量: 120 162.5 107 175.5描述:方程式:CaO+H2O Ca(OH)2式量: 56 18 74描述:生石灰(CaO)溶于水生成熟石灰Ca(OH)2方程式:Ca(OH)2+SO3 CaSO4+H2O式量: 74 80 136 18描述:方程式:Ca(OH)2+CO2 CaCO3↓+H2O式量: 74 44 100 18描述:方程式:Ca(OH)2+Na2CO3 CaCO3↓+2NaOH 式量: 74 106 100 80描述:方程式:2NaOH+SO3 Na2SO4+H2O式量: 80 80 142 18描述:方程式:Zn+CuSO4 ZnSO4+Cu式量: 65 159.5 161 63.5描述:方程式:Hg(NO3)2+Cu Cu(NO3)2+Hg式量: 325 63.5 187.5 201描述:方程式:NaOH+NH4NO3 NaNO3+NH3↑+H2O 式量: 40 80 85 17 18。
初中化学用语(全)
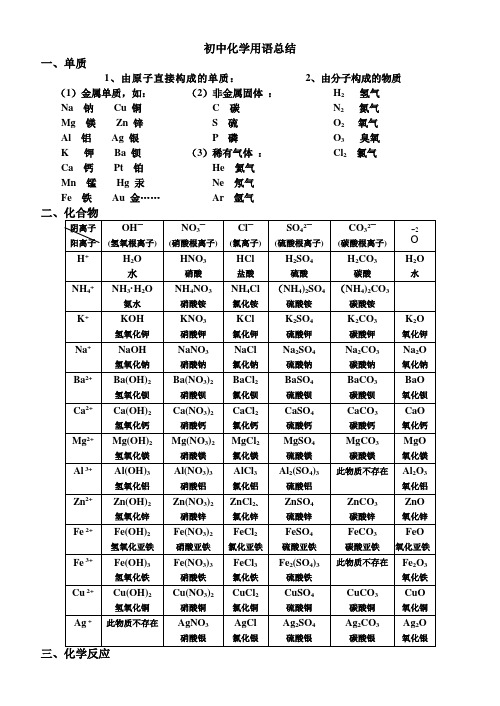
初中化学用语总结一、单质1、由原子直接构成的单质:2、由分子构成的物质(1)金属单质,如:Na 钠Cu 铜Mg 镁Zn 锌Al 铝Ag 银K 钾Ba 钡Ca 钙Pt 铂Mn 锰Hg 汞Fe 铁Au 金……(2)非金属固体:C 碳S 硫P 磷(3)稀有气体:He 氦气Ne 氖气Ar 氩气H2氢气N2氮气O2 氧气O3臭氧Cl2氯气(一)、化合反应:“多变一”1、氯化氢和氨气反应:氯化铵氨气氯化氢−→−+ Cl NH NH HCl 43===+2、红磷燃烧: 五氧化二磷氧气磷点燃−−→−+ 522O P 2O 5P 4点燃+ 3、硫的燃烧: 二氧化硫氧气硫点燃−−→−+ 22SO O S 点燃+ 4、铁在氧气中燃烧:四氧化三铁点燃氧气铁−−→−+ 432O e F O 2e F 3点燃+5、镁的燃烧: 氧化镁氧气镁点燃−−→−+ O Mg 2O 2Mg 2点燃+ 6、铝的燃烧: 氧化铝氧气铝点燃−−→−+ 322O Al 2O 34Al 点燃+7、铜在空气中加热:氧化铜氧气铜加热−−→−+ O Cu 2O Cu 22△+8、氢气的燃烧: 水氧气氢气点燃−−→−+ O H 2O 2H 222点燃+ 9、木炭燃烧: 二氧化碳氧气碳点燃−−→−+ 22CO O C 点燃+ 10、碳在不足量氧气中燃烧:一氧化碳氧气碳点燃−−→−+ CO 2O C 22点燃+ 11、一氧化碳的燃烧:二氧化碳氧气一氧化碳点燃−−→−+ 22CO 2O CO 2点燃+12、二氧化碳溶于水:碳酸水二氧化碳→+13、生石灰遇水反应:氢氧化钙水氧化钙→+(二)、分解反应:“一变多”1、氧化汞加热分解: 氧气汞氧化汞加热+−−→− ↑+2O Hg 2Og H 2△2、过氧化氢催化分解:氧气水过氧化氢二氧化锰+−−−−→− ↑+22O Mn 22O O H 2O 2H 23、高锰酸钾加热分解:氧气二氧化锰锰酸钾高锰酸钾加热++−−→−4、氯酸钾与二氧化锰混合加热:5、电解水: 氢气氧气水通电+−−→− ↑+↑222O H 2O2H 通电6、碳酸分解: 二氧化碳水碳酸+→7、碱式碳酸铜(孔雀石)热分解:水二氧化碳氧化铜碱式碳酸铜加热++−−→−8、电解熔融氧化铝制铝:氧气铝氧化铝通电+−−→− ↑+232O 3Al 4O l A 2通电9、碳酸钙高温分解: 二氧化碳氧化钙碳酸钙高温+−−→− ↑+23CO O a C aCO C 高温(三)、置换反应:“单质+化合物 — 化合物+单质 A+BC — AC+B ”1、 氢气还原氧化铜:铜水氧化铜氢气加热+−−→−+2、 碳还原氧化铜:铜二氧化碳氧化铜碳高温+−−→−+ 金属活动顺序:3、 镁与稀盐酸反应:氢气氯化镁盐酸镁+→+4、 铝与稀盐酸反应:氢气氯化铝盐酸铝+→+5、 锌与稀盐酸反应:氢气氯化锌盐酸锌+→+6、 铁与稀盐酸反应:氢气氯化亚铁盐酸铁+→+7、 镁与稀硫酸反应:氢气硫酸镁稀硫酸镁+→+8、 锌与稀硫酸反应:氢气硫酸锌稀硫酸锌+→+ 9、 铝与稀硫酸反应:氢气硫酸铝稀硫酸铝+→+10、铁与稀硫酸反应:氢气硫酸亚铁稀硫酸铁+→+11、铝与硫酸铜反应:铜硫酸铝硫酸铜铝+→+12、铁与硫酸铜反应:铜硫酸亚铁硫酸铜铁+→+13、铁与氯化铜反应:铜氯化亚铁氯化铜铁+→+(四)、复分解反应:1、氯化钾与硝酸银反应:氯化银硝酸钾硝酸银氯化钾+→+2、盐酸与硝酸银反应:氯化银硝酸硝酸银盐酸+→+3、氧化铜与硫酸反应:水硫酸铜硫酸氧化铜+→+4、氧化镁与硫酸反应:水硫酸镁硫酸氧化镁+→+5、氧化铁与盐酸反应:水氯化铁盐酸氧化铁+→+6、盐酸与氢氧化钠反应:水氯化钠氢氧化钠盐酸+→+7、硫酸与氢氧化钠反应:水硫酸钠氢氧化钠硫酸+→+ 8、硝酸与氢氧化铜反应:水硝酸铜氢氧化铜硝酸+→+9、氯化钡与硫酸反应:水硫酸钡硫酸氯化钡+→+ 9、氯化钡与碳酸钠反应:氯化钠碳酸钡碳酸钠氯化钡+→+10、氢氧化钠硫酸铜反应:硫酸铜氢氧化铜硫酸铜氢氧化钠+→+11、氢氧化钙与氯化铁反应:氯化钙氢氧化铁氯化铁氢氧化钙+→+(五)、其他反应: 1、汽车尾气催化转换:氮气二氧化碳一氧化氮一氧化碳+−−→−+铂、钯22dP t P N CO 2NO2CO 2++,2、二氧化碳与氢氧化钙反应(澄清石灰水变浑浊):水碳酸钙氢氧化钙二氧化碳+→+3、大理石与盐酸反应:二氧化碳水氯化钙盐酸碳酸钙++→+4、甲烷(天然气的主要成分)燃烧:水二氧化碳氧气甲烷点燃+−→−+O H 2CO O 2CH 2224++点燃5、一氧化碳还原氧化铁:二氧化碳铁一氧化碳氧化铁高温+−−→−+ 232CO 32Fe COO e F ++高温6、一氧化碳还原氧化铜:二氧化碳铜一氧化碳氧化铜加热+−−→−+ 2CO u C COCuO ++加热10、碳酸氢铵与氢氧化钙混合:氨气水碳酸钙氢氧化钙碳酸氢铵++→+11、硫酸铵与氢氧化钠溶液混合加热:氨气水硫酸钠氢氧化钠硫酸铵△++−→−+(NH 4)2SO 4+2NaOH Na 2SO 4+ H 2O + NH 3·H 2O7、葡萄糖在酶作用下的反应:水二氧化碳氧气葡萄糖酶+−→−+。
初中化学必背知识点打印版

初中化学必背知识点打印版一、化学用语。
1. 元素符号。
- 前20号元素:氢(H)、氦(He)、锂(Li)、铍(Be)、硼(B)、碳(C)、氮(N)、氧(O)、氟(F)、氖(Ne)、钠(Na)、镁(Mg)、铝(Al)、硅(Si)、磷(P)、硫(S)、氯(Cl)、氩(Ar)、钾(K)、钙(Ca)。
- 常见金属元素:铁(Fe)、铜(Cu)、锌(Zn)、银(Ag)、金(Au)、汞(Hg)等。
2. 化学式。
- 单质化学式。
- 金属单质:用元素符号表示,如铁(Fe)、铜(Cu)等。
- 固态非金属单质:一般用元素符号表示,如碳(C)、硫(S)等;但碘(I₂)除外。
- 稀有气体:用元素符号表示,如氦气(He)、氖气(Ne)等。
- 气态非金属单质:在元素符号右下角写上表示分子中所含原子数的数字,如氢气(H₂)、氧气(O₂)、氮气(N₂)等。
- 化合物化学式。
- 书写原则:正价在前,负价在后,根据化合物中正负化合价代数和为零的原则确定原子个数比。
- 例如:水(H₂O),其中氢元素化合价为 + 1,氧元素化合价为 - 2;氯化钠(NaCl),钠元素化合价为+1,氯元素化合价为 - 1。
3. 化学方程式。
- 书写原则。
- 一是必须以客观事实为基础;二是要遵守质量守恒定律,等号两边各原子的种类和数目必须相等。
- 例如:- 镁在空气中燃烧:2Mg + O₂{点燃}{===}2MgO。
- 实验室制取氧气:- 加热高锰酸钾:2KMnO₄{}{===}K₂MnO₄+MnO₂+O₂↑。
- 过氧化氢分解:2H₂O₂{MnO_2}{===}2H₂O+O₂↑。
- 化学方程式的意义。
- 质的方面:表示反应物、生成物和反应条件。
如氢气和氧气在点燃条件下反应生成水。
- 量的方面:- 宏观上:表示反应物、生成物之间的质量比。
在2H₂+O₂{点燃}{===}2H₂O中,氢气、氧气和水的质量比为4:32:36 = 1:8:9。
- 微观上:表示反应物、生成物之间的粒子个数比。
100个化学用语

100个化学用语1. 元素 (element)2. 化合物 (compound)3. 分子 (molecule)4. 原子 (atom)5. 反应 (reaction)6. 酸 (acid)7. 碱 (base)8. 盐 (salt)9. 溶液 (solution)10. 晶体 (crystal)11. 气体 (gas)12. 液体 (liquid)13. 固体 (solid)14. 离子 (ion)15. 化学键 (chemical bond)16. 反应速率 (reaction rate)17. 摩尔质量 (molar mass)18. 摩尔浓度 (molar concentration)19. 反应平衡 (chemical equilibrium)20. 离子化 (ionization)21. 电离度 (ionization degree)22. 化学式 (chemical formula)23. 反应机制 (reaction mechanism)24. 化学平衡 (chemical balance)25. 比较分析 (comparative analysis)26. 氧化还原反应 (redox reaction)27. 酸碱中和反应 (acid-base neutralization reaction)28. 氧化剂 (oxidizing agent)29. 还原剂 (reducing agent)30. 晶体结构 (crystal structure)31. 电子亲和力 (electron affinity)32. 电离能 (ionization energy)33. 共价键 (covalent bond)34. 极性 (polarity)35. 热力学 (thermodynamics)36. 核化学 (nuclear chemistry)37. 催化剂 (catalyst)38. 光催化 (photocatalysis)39. 量子力学 (quantum mechanics)40. 电子结构 (electronic structure)41. 有机化合物 (organic compound)42. 无机化合物 (inorganic compound)43. 生物化学 (biochemistry)44. 放射性 (radioactive)45. 电解质 (electrolyte)46. 晶体缺陷 (crystal defect)47. 热分析 (thermal analysis)48. 光谱学 (spectroscopy)49. 核磁共振 (nuclear magnetic resonance)50. 红外光谱 (infrared spectroscopy)51. 质谱 (mass spectrometry)52. 光电子能谱 (photoelectron spectroscopy)53. 光谱分析 (spectral analysis)54. 电化学 (electrochemistry)55. 电导率 (conductivity)56. 比色法 (colorimetry)57. 密度 (density)58. 粘度 (viscosity)59. 热容 (heat capacity)60. 摩尔吸光度 (molar absorptivity)61. 晶体学 (crystallography)62. 热力学循环 (thermodynamic cycle)63. 化学动力学 (chemical kinetics)64. 反应速度常数 (rate constant)65. 反应活化能 (activation energy)66. 催化作用 (catalysis)67. 氧化态 (oxidation state)68. 还原态 (reduction state)69. 链式反应 (chain reaction)70. 增溶剂 (cosolvent)71. 电解 (electrolysis)72. 电解槽 (electrolytic cell)73. 化学计量 (stoichiometry)74. 氧化数 (oxidation number)75. 比例法 (proportional method)76. 酸碱指示剂 (acid-base indicator)77. 沉淀 (precipitate)78. 污染物 (pollutant)79. 溶解度 (solubility)80. 毒性 (toxicity)81. 晶体生长 (crystal growth)82. 光催化剂 (photocatalyst)83. 酸碱滴定 (acid-base titration)84. 沸点 (boiling point)85. 熔点 (melting point)86. 比热容 (specific heat capacity)87. 催化剂活性 (catalyst activity)88. 化学反应平衡常数 (chemical equilibrium constant)89. 氧化物 (oxide)90. 电子云 (electron cloud)91. 分子轨道 (molecular orbital)92. 电子转移 (electron transfer)93. 能带 (band)94. 离子晶体 (ionic crystal)95. 配位化合物 (coordination compound)96. 可燃性 (flammability)97. 气液平衡 (gas-liquid equilibrium)98. 表面张力 (surface tension)99. 热解 (pyrolysis)100. 溶剂 (solvent)。
初中化学用语汇总

初中化学用语汇总1. 原子:构成分子的最小粒子。
2. 元素:由同种原子组成的物质。
4. 分子:由两个及以上原子组成的不带电荷的粒子。
6. 原子量:一个原子质量单位。
8. 周期表:元素根据其原子核结构的排列方式排列的表格。
9. 金属:具有良好的导电性和热传导性质的物质。
11. 金属元素:处于周期表左侧的元素。
16. 原子核:由质子和中子组成的原子中心部分。
17. 共价键:由电子对共享形成的键。
18. 离子键:带正电荷和负电荷之间的相互作用。
21. 化学键:元素通过共享或转移电子形成的化学物质的力。
22. 化学式:用元素符号表示化合物的组成。
23. 反应物:在化学反应中参与反应的物质。
25. 化学反应:物质之间的化学相互作用。
26. 酸:会释放出氢离子的物质。
28. 盐:由阳离子和阴离子组成的离子化合物。
30. 溶解:由固体或气体转变为液体。
31. 溶质:溶解在溶剂中的物质。
34. 沉淀:在溶液中形成的固体颗粒。
36. 电离:在溶液中将电解质分解为离子。
39. 化学平衡:反应物和生成物在化学反应中达到平衡状态。
40. 配位化合物:由中心金属离子和其它分子和离子中的原子和分子共价结合而成的化合物。
41. 化学式计算:根据化学式计算元素的质量。
42. 摩尔质量:化学式中一个摩尔的质量。
43. 密度:单位体积内的物质质量。
44. 燃烧:化合物与氧气彻底反应的化学反应。
46. 温度:温度代表了物体内部分子的平均运动速度。
47. 热力学系统:研究热和压力与化学反应之间的关系。
48. 热能:热能是物体或系统储存的能量。
49. 热动力学:热的能量学,研究物质内部热运动的规律。
50. 热量:由于温度差异而流动的能量。
51. 热容:物质单位质量的温度变化时吸收或释放的热量。
52. 热传导:热能通过物质的传递。
53. 热平衡:两个物体之间热能的交换达到相同的温度。
54. 热力学第一性原理:能量守恒。
55. 内能:热力学系统内分子内部相互作用引起的能量总和。
九年级常见化学用语和化学方程式

九年级常见化学用语和化学方程式五、课本中的化学方程式:第二单元:1、红磷在氧气中燃烧4 P + 5 O2 2 P2O52、碳在氧气中燃烧 C + O2CO23、硫在氧气中燃烧S + O2 SO24、铁在氧气中燃烧 3 Fe + 2 O2Fe3O45、铝在氧气中燃烧 4 Al + 3 O2 2 Al2O36、用过氧化氢制氧气 2 H2O2 2 H2O + O2↑7、用高锰酸钾制氧气2KMnO4K2MnO4+ MnO2+ O2↑8、用氯酸钾和二氧化锰的混合物制氧气 2 KClO3 2 KCl + 3 O2↑第三单元:9、水通电分解(电解水) 2 H2O 2 H2↑+ O2↑10、汞受热2Hg+O22HgO11、氧化汞受热分解2HgO2Hg+O2↑12、氢气在空气中燃烧 2 H2 + O2 2 H2O13、氢气还原氧化铜H2 + CuO Cu + H2O第四单元:第五单元:14、铁和硫酸铜溶液反应Fe + CuSO 4FeSO4 + Cu15、碳酸钠和盐酸反应Na 2CO3+2HCl2NaCl+H2O+CO2↑16、镁条在空气中燃烧 2 Mg + O2 2 MgO17、高温煅烧石灰石(二氧化碳的工业制法)CaCO3CaO + CO2↑第六单元:2 CO18、碳在氧气中不充分燃烧 2 C + O2 (不足)19、碳跟氧化铜反应 C + 2 CuO 2 Cu + CO2↑20、碳跟氧化铁反应 3 C + 2 Fe2O3 4 Fe + 3 CO2 ↑21、碳跟二氧化碳反应C+CO22CO+ 2HCl CaCl2 + CO2↑+ H2O22、实验室制取二氧化碳CaCO23、二氧化碳与水反应CO 2 + H2O H2CO324、碳酸分解H 2CO3CO2 ↑+ H2O25、二氧化碳与氢氧化钙溶液反应(二氧化碳的检验方法)CO 2 + Ca(OH)2CaCO3↓+ H2O26、一氧化碳燃烧 2 CO + O2 2 CO227、一氧化碳还原氧化铜CO +CuO Cu + CO228、一氧化碳还原氧化铁 3 CO +Fe2O3 2 Fe + 3 CO2第七单元:29、甲烷燃烧CH4 + 2 O2CO2 + 2 H2O30、酒精燃烧C2H5OH + 3 O2 2 CO2 + 3 H2O第八单元:31、镁和稀盐酸反应镁和稀硫酸反应Mg + 2 HCl MgCl+ H2↑Mg + H2SO4MgSO4 + H2↑32、锌和稀盐酸反应锌和稀硫酸反应(实验室制取氢气)Zn + 2 HCl ZnCl+ H2↑Zn + H2SO4ZnSO4 + H2↑33、铁和稀盐酸反应铁和稀硫酸反应+ H2↑Fe + H2SO4FeSO4 + H2↑Fe + 2 HCl FeCl34、铝和稀盐酸反应铝和稀硫酸反应+3H2↑2Al+ 3H2SO4Al2(SO4)3 +3 H2↑2Al+6HCl2AlCl35、铝和硫酸铜溶液反应 2 A l + 3 CuSO 4Al2(SO4)3 + 3CuCu(NO3)2 + 2 Ag36、铜和硝酸银溶液反应Cu + 2 AgNO第十单元:37、铁锈与稀盐酸反应铁锈与稀硫酸反应FeO3+6HCl2FeCl3+3H2O Fe2O3+3H2SO4Fe2(SO4)3+3H2O38、氧化铜与稀硫酸反应H2SO4+ CuO Cu SO4+ H2O39、氧化钙与水的反应CaO+HO Ca(OH)240、氢氧化钠溶液与二氧化碳反应2NaOH+CO 2Na2CO3+H2O41、二氧化硫与氢氧化钠溶液反应2NaOH+SO 2Na2SO3+H2O42、三氧化硫与氢氧化钠溶液反应2NaOH+SO 3Na2SO4+H2O43、氢氧化钠与盐酸反应氢氧化钠与硫酸反应NaOH+HCl NaCl+H 2O 2NaOH+H2SO4Na2SO4+H2O44、氢氧化钙与盐酸反应氢氧化钙与硫酸反应+2HCl CaCl2+2H2O Ca(OH)2+H2SO4CaSO4+2H2OCa(OH)第十一单元:45、碳酸氢钠与盐酸反应NaHCO 3+HCl NaCl+H2O+CO2↑CO3+Ca(OH)2CaCO3↓+2NaOH46、碳酸钠溶液与氢氧化钙溶液反应Na初中化学常见物质的颜色(后面是物质化学式或物质名称,前面是颜色)1. 常见物质的颜色:多数气体为无色,多数固体化合物为白色,多数溶液为无色。
初三化学常化学用语必背

初三化学常化学用语必背“化学是一门记忆加实验的科学”,这也许不太符合一些同学的思维习惯。
下面是小偏整理的初三化学常化学用语必背,感谢您的每一次阅读。
初三化学常化学用语必背一、熟记下列元素名称及符号: 1、H氢O氧 N氮 Cl氯 C碳 P 磷 S硫 2、K钾 Ca钙 Na钠 Mg镁 Al铝 Zn锌 Fe铁 Cu铜 Hg汞 Ag 银 Mn锰 Ba钡二、熟记下列物质的化学式: 1、单质: H2氢气 O2氧气 N2氮气 C碳 P磷 S硫 Fe铁 Cu铜 Hg汞 2、化合物 (1)氧化物:H2O水CO2二氧化碳CO一氧化碳SO2二氧化硫SO3三氧化硫P2O5五氧化二磷 Fe2O3氧化铁Fe3O4四氧化三铁 CaO氧化钙 MgO氧化镁 CuO氧化铜 ZnO氧化锌 FeO氧化亚铁MnO2二氧化锰-Na2O氧化钠(2)酸:HCl盐酸H2SO4硫酸HNO3硝酸 H2CO3碳酸 -H2SO3亚硫酸(3)碱:NaOH氢氧化钠KOH氢氧化钾Ca(OH)2氢氧化钙Ba(OH)2氢氧化钡 Cu(OH)2氢氧化铜Fe(OH)3氢氧化铁Fe(OH)2氢氧化亚铁Al(OH)3氢氧化铝Mg(OH)2氢氧化镁(4)盐:NaCl氯化钠Na2CO3碳酸钠NaHCO3碳酸氢钠 CaCO3碳酸钙 CaCl2氯化钙 KCl氯化钾ZnCl2氯化锌AgCl氯化银FeCl3氯化铁FeCl2氯化亚铁AlCl3氯化铝 BaCl2氯化钡 Na2SO4硫酸钠CuSO4硫酸铜FeSO4硫酸亚铁Fe2(SO4)3硫酸铁ZnSO4硫酸锌BaSO4硫酸钡KClO3氯酸钾KMnO4高锰酸钾K2MnO4锰酸钾KNO3硝酸钾 Ag NO3硝酸银 Cu(NO3)2硝酸铜-NH4Cl氯化铵-NH4NO3硝酸铵-(NH4)2SO4硫酸铵- NH4HCO3碳酸氢铵(5)有机物:CH4甲烷C2H5OH乙醇(酒精) C6H12O6葡萄糖(C6H10O5)n淀粉 -CO(NH2)2尿素三、熟记下列元素在化合物中的化合价:(1) 正价(多为金属)+1 +1 +1 +1 +2 +2 +2 +2 +2 +3 +2 +3 H K Na Ag Ca Mg Zn Ba Cu Al Fe(FeO) Fe(Fe2O3) (2) 负价(非金属)-2 -1 -2 O Cl S (3) 原子团+1 -1 -1 -1 -1 -2 -2 -2 -3 -1 NH4 OH NO3 ClO3 MnO4(KMnO4) CO3 SO4 SO3 PO4 HCO3四、熟记下列常用离子(比较与相应化合价的联系)(1)阳离子H+ K+ Na+ Ca2+ Fe2+ Mg2+ Cu2+ Fe3+(2)阴离子Cl- OH - NO3- CO32- SO4 2-五、熟记下列化学方程式:(一)化合反应(A+B→C):1、木炭在氧气中燃烧:C+O2 点燃CO2 2、硫在氧气中燃烧:S+O2 点燃SO2 3、镁在空气中燃烧:2Mg+O2 点燃 2MgO 4、铁在氧气中燃烧: 3Fe+2O2 点燃 Fe3O4 5、磷在氧气中燃烧:4P+5O2 点燃2P2O5 6、铜在空气中加热:2Cu+O2 △ 2CuO 7、氢气在氧气中燃烧:2H2+O2 点燃 2H2O8、一氧化碳在空气中燃烧:2CO+O2 点燃2CO2 9、碳不充分燃烧:2C+O2(不充分)点燃2CO 10、二氧化碳通过灼热的碳层:CO2 + C 高温2CO 11、二氧化碳与水反应:CO2+H2O === H2CO3-12、三氧化硫溶于水:SO3+H2O === H2SO4 (酸雨的成因)13、生石灰和水化合:CaO+H2O === Ca(OH)2(二)分解反应(C→A+B):14 过氧化氢用二氧化锰作催化剂分解(实验室制O2):2H2O2 2 H2O + O2↑15、氯酸钾与二氧化锰共热(实验室制O2):2KClO3 2KCl+3O2↑ 16、加热高锰酸钾:2KMn O4 △ K2MnO4 + MnO2 + O2↑ 17、电解水:2H2O通电2H2↑ + O2↑18、碳酸不稳定分解:H2CO3 === H2O + CO2↑19、高温煅烧石灰石:CaCO3 高温 CaO + CO2↑-20、氢氧化铜受热分解:Cu(OH)2 △ CuO + H2O(三)置换反应(A+BC→B+AC):21、锌和稀硫酸反应(实验室制H2):Zn+H2SO4 === ZnSO4 + H2↑ 22、锌和盐酸的反应:Zn+2HCl === ZnCl2 + H2↑ 23、铁和盐酸: Fe+2HCl === FeCl2 + H2↑ 24、铁和稀硫酸:Fe+H2SO4 === FeSO4 + H2↑ 25、氢气还原氧化铜:H2+CuO △ Cu + H2O26、氢气还原氧化铁:3H2 + Fe2O3 △ 2Fe + 2H2O27、木炭还原氧化铜:C+2CuO高温2Cu + CO2↑ 28、焦碳还原氧化铁:3C+2Fe2O3 高温4Fe+3CO2↑ 29、铁和硫酸铜溶液:Fe + CuSO4 === Cu + FeSO4 30、铜和硝酸银溶液:Cu + 2AgNO3 === 2Ag + Cu(NO3)231、铝和稀硫酸:2Al+3H2SO4 === Al2(SO4)3 + 3H2↑32、铝和硫酸铜溶液:2Al + 3CuSO4 === 3Cu + Al2(SO4)3-33、钠和水反应:2Na+2H2O === 2NaOH+H2↑(四)复分解反应(AB+CD→AD+CB):34、大理石和稀盐酸(实验室制CO2):CaCO3 + 2HCl === CaCl2 + H2O + CO2↑ 35、碳酸钠和盐酸(灭火器原理):Na2CO3 + 2HCl === 2NaCl + H2O + CO2↑36、碳酸氢钠和盐酸:NaHCO3 + HCl === NaCl + H2O + CO2↑37、碳酸钾(草木灰)和盐酸:K2CO3 + 2HCl === 2KCl + H2O + CO2↑38、盐酸和氢氧化钠(中和反应):HCl + NaOH === NaCl + H2O 39、硫酸和氢氧化钠溶液:H2SO4 + 2NaOH === Na2SO4 + 2H2O 40、硫酸与氯化钡溶液:H2SO4 + BaCl2 === BaSO4↓(白)+ 2HCl 41、盐酸与硝酸银溶液:HCl + AgN O3 === AgCl↓(白)+ HNO342、氢氧化钠和硫酸铜:2NaOH+CuSO4 === Cu(OH)2↓(蓝色) + Na2SO443、氢氧化钠和氯化铁溶液:3NaOH+FeCl3 === Fe(OH)3↓(红褐色)+ 3NaCl44、碳酸钠和石灰水:Na2CO3 + Ca(OH)2 === CaCO3↓ + 2NaOH45、硫酸钠和氯化钡:Na2SO4 + BaCl2 === BaSO4↓ + 2NaCl 46、氯化钠和硝酸银:NaCl + AgNO3 === AgCl↓ + NaNO347、氢氧化铝和盐酸(中和胃酸):Al(OH)3 + 3HCl === AlCl3 + 3H2O 48、氢氧化镁和盐酸(去除水垢):Mg(OH)2 + 2HCl === MgCl2 + 2 H2O 49、盐酸除铁锈:Fe2O3 + 6HCl === 2FeCl3 + 3H2O 50、氧化铜和硫酸:CuO + H2SO4 === CuSO4 + H2O -51、硝酸铵和氢氧化钠:NH4NO3 + NaOH △ NaNO3 + H2O + NH3↑(五)其他:52、二氧化碳使澄清石灰水变浑浊(实验室用于鉴定CO2):CO2 + Ca(OH)2 === CaCO3↓ + H2O 53、二氧化碳通入氢氧化钠溶液(实验室用于吸收CO2): CO2 + 2NaOH === Na2CO3 + H2O 54、用氢氧化钠溶液吸收三氧化硫:SO3 + 2NaOH === Na2SO4 + H2O 55、一氧化碳还原氧化铜:CO + CuO △ Cu + CO256、一氧化碳还原氧化铁(炼铁):3CO + Fe2O3 高温 2Fe + 3CO257、甲烷在空气中燃烧:CH4 + 2O2 点燃 CO2 + 2H2O 58、乙醇在空气中燃烧:C2H5OH+3O2 点燃 2CO2+3H2O-59、葡萄糖在人体组织中氧化:C6H12O6 + 6O2 =酶6CO2+6H2O化学学习经典方法技巧一:形成网络,优化忆技巧二:突出关键,浓缩记忆技巧三:分析对比,理解记忆技巧四:形象比喻,增强记忆技巧五:口诀韵语,灵活记忆技巧六:前后联想,巩固记忆“化学是一门记忆加实验的科学”,这也许不太符合一些同学的思维习惯。
初中化学用语(全)

初中化学方程式总结一、化合反应:“多变一”2、红磷燃烧:522O P 2O 5P 4点燃+3、硫的燃烧:22SO O S 点燃+4、铁在氧气中燃烧:432O e F O 2e F 3点燃+5、镁的燃烧:O Mg 2O 2Mg 2点燃+6、铝的燃烧:322O Al 2O 34Al 点燃+7、铜在空气中加热:O Cu 2O Cu 22△+8、氢气的燃烧:O H 2O 2H 222点燃+9、木炭燃烧:22CO O C 点燃+10、碳在不足量氧气中燃烧:CO 2O C 22点燃+11、一氧化碳的燃烧:22CO 2O CO 2点燃+12、二氧化碳溶于水:13、生石灰遇水反应:二、分解反应:“一变多”1、氧化汞加热分解: 氧气汞氧化汞加热+−−→− ↑+2O Hg 2Og H 2△ 2、过氧化氢催化分解:氧气水过氧化氢二氧化锰+−−−−→− ↑+22O Mn 22O O H 2O 2H 23、高锰酸钾加热分解:氧气二氧化锰锰酸钾高锰酸钾加热++−−→− 4、氯酸钾与二氧化锰混合加热:5、电解水: 氢气氧气水通电+−−→− ↑+↑222O H 2O2H 通电6、碳酸分解: 二氧化碳水碳酸+→7、碱式碳酸铜(孔雀石)热分解:水二氧化碳氧化铜碱式碳酸铜加热++−−→−8、电解熔融氧化铝制铝:氧气铝氧化铝通电+−−→− ↑+232O 3Al 4O l A 2通电9、碳酸钙高温分解: 二氧化碳氧化钙碳酸钙高温+−−→− ↑+23CO O a C aCO C 高温 10、碳酸氢钠分解:氧气铝氧化铝通电+−−→− ↑++22323CO Na 2Na CO O H HCO V11、碳酸氢铵分解: 二氧化碳氧化钙碳酸钙高温+−−→− ↑+2O Hg 2Og H 2△(三)、置换反应:“单质+化合物 — 化合物+单质 A+BC — AC+B ”1、 氢气还原氧化铜:铜水氧化铜氢气加热+−−→−+2、 碳还原氧化铜:铜二氧化碳氧化铜碳高温+−−→−+3、 氢气还原氧化铁:铜二氧化碳氧化铜碳高温+−−→−+4、 碳还原氧化铁:铜二氧化碳氧化铜碳高温+−−→−+金属活动顺序:5、 镁与稀盐酸反应:氢气氯化镁盐酸镁+→+6、 铝与稀盐酸反应:氢气氯化铝盐酸铝+→+7、 锌与稀盐酸反应:氢气氯化锌盐酸锌+→+8、 铁与稀盐酸反应:氢气氯化亚铁盐酸铁+→+9、 镁与稀硫酸反应:氢气硫酸镁稀硫酸镁+→+10、 锌与稀硫酸反应:氢气硫酸锌稀硫酸锌+→+11、 铝与稀硫酸反应:氢气硫酸铝稀硫酸铝+→+10、铁与稀硫酸反应:氢气硫酸亚铁稀硫酸铁+→+11、铝与硫酸铜反应:铜硫酸铝硫酸铜铝+→+12、铁与硫酸铜反应:铜硫酸亚铁硫酸铜铁+→+13、铁与氯化铜反应:铜氯化亚铁氯化铜铁+→+(四)、复分解反应:1、氯化钾与硝酸银反应:氯化银硝酸钾硝酸银氯化钾+→+2、盐酸与硝酸银反应:氯化银硝酸硝酸银盐酸+→+3、氧化铜与硫酸反应:水硫酸铜硫酸氧化铜+→+4、氧化镁与硫酸反应:水硫酸镁硫酸氧化镁+→+5、氧化铁与盐酸反应:水氯化铁盐酸氧化铁+→+6、盐酸与氢氧化钠反应:水氯化钠氢氧化钠盐酸+→+7、硫酸与氢氧化钠反应:水硫酸钠氢氧化钠硫酸+→+8、硝酸与氢氧化铜反应:水硝酸铜氢氧化铜硝酸+→+9、氯化钡与硫酸反应:水硫酸钡硫酸氯化钡+→+9、氯化钡与碳酸钠反应:氯化钠碳酸钡碳酸钠氯化钡+→+10、氢氧化钠硫酸铜反应:硫酸铜氢氧化铜硫酸铜氢氧化钠+→+11、氢氧化钙与氯化铁反应:氯化钙氢氧化铁氯化铁氢氧化钙+→+(五)、其他反应:1、汽车尾气催化转换:氮气二氧化碳一氧化氮一氧化碳+−−→−+铂、钯 22d P t P N CO 2NO2CO 2++,2、二氧化碳与氢氧化钙反应(澄清石灰水变浑浊):水碳酸钙氢氧化钙二氧化碳+→+3、大理石与盐酸反应:二氧化碳水氯化钙盐酸碳酸钙++→+4、甲烷(天然气的主要成分)燃烧:水二氧化碳氧气甲烷点燃+−→−+O H 2CO O 2CH 2224++点燃5、一氧化碳还原氧化铁: 二氧化碳铁一氧化碳氧化铁高温+−−→−+ 232CO 32Fe COO e F ++高温 6、一氧化碳还原氧化铜:二氧化碳铜一氧化碳氧化铜加热+−−→−+ 2CO u C CO CuO ++加热10、碳酸氢铵与氢氧化钙混合:氨气水碳酸钙氢氧化钙碳酸氢铵++→+11、硫酸铵与氢氧化钠溶液混合加热:氨气水硫酸钠氢氧化钠硫酸铵△++−→−+(NH 4)2SO 4+2NaOH Na 2SO 4+ H 2O + NH 3·H 2O7、葡萄糖在酶作用下的反应:水二氧化碳氧气葡萄糖酶+−→−+。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
初中化学用语总结
一、单质
1、由原子直接构成的单质:
2、由分子构成的物质
(1)金属单质,如:
Na 钠 Cu 铜
Mg 镁 Zn 锌
Al 铝 Ag 银
K 钾 Ba 钡
Ca 钙 Pt 铂
Mn 锰 Hg 汞
Fe 铁Au 金……(2)非金属固体:
C 碳
S 硫
P 磷
(3)稀有气体:
He 氦气
Ne 氖气
Ar 氩气
H
2
氢气
N
2
氮气
O
2
氧气
O
3
臭氧
Cl
2
氯气
二、化合物
三、化学反应
(一)、化合反应:“多变一”
1、氯化氢和氨气反应:氯化铵氨气氯化氢−→−
+ Cl NH NH HCl 43===+ 2、红磷燃烧: 五氧化二磷氧气磷点燃
−−→−+ 522O P 2O 5P 4点燃+ 3、硫的燃烧: 二氧化硫氧气硫点燃
−−→−+ 22SO O S 点燃+ 4、铁在氧气中燃烧:四氧化三铁点燃氧气铁−−→−+ 432O e F O 2e F 3点燃+
5、镁的燃烧: 氧化镁氧气镁点燃
−−→−+ O Mg 2O 2Mg 2点燃+ 6、铝的燃烧: 氧化铝氧气铝点燃
−−→−+ 322O Al 2O 34Al 点燃+ 7、铜在空气中加热:氧化铜氧气铜加热
−−→−+ O Cu 2O Cu 22△+ 8、氢气的燃烧: 水氧气氢气点燃
−−→−+ O H 2O 2H 222点燃+
9、木炭燃烧: 二氧化碳氧气碳点燃
−−→−+ 22CO O C 点燃+ 10、碳在不足量氧气中燃烧:一氧化碳氧气碳点燃
−−→−+ CO 2O C 22点燃+ 11、一氧化碳的燃烧:二氧化碳氧气一氧化碳点燃
−−→−+ 22CO 2O CO 2点燃+ 12、二氧化碳溶于水:碳酸水二氧化碳→+
13、生石灰遇水反应:氢氧化钙水氧化钙→+
(二)、分解反应:“一变多”
1、氧化汞加热分解: 氧气汞氧化汞加热
+−−→− ↑+2O Hg 2O g H 2△
2、过氧化氢催化分解:氧气水过氧化氢二氧化锰
+−−−−→− ↑+22O Mn 22O O H 2O 2H 2 3、高锰酸钾加热分解:
4、氯酸钾与二氧化锰混合加热:
5、电解水: 氢气氧气水通电
+−−→− ↑+↑222O H 2O 2H 通电
6、碳酸分解: 二氧化碳水碳酸+→
7、碱式碳酸铜(孔雀石)热分解:
8、电解熔融氧化铝制铝:氧气铝氧化铝通电+−−→− ↑+232O 3Al 4O l A 2通电
9、碳酸钙高温分解: 二氧化碳氧化钙碳酸钙高温+−−→− ↑+23CO O a C aCO C 高温
(三)、置换反应:“单质+化合物 — 化合物+单质 A+BC — AC+B ”
1、氢气还原氧化铜:铜水氧化铜氢气加热
+−−→−+ 2、碳还原氧化铜:铜二氧化碳氧化铜碳高温+−−→−+
金属活动顺序:
3、镁与稀盐酸反应:氢气氯化镁盐酸镁+→+
4、铝与稀盐酸反应:氢气氯化铝盐酸铝+→+
5、锌与稀盐酸反应:氢气氯化锌盐酸锌+→+
6、铁与稀盐酸反应:氢气氯化亚铁盐酸铁+→+
7、镁与稀硫酸反应:氢气硫酸镁稀硫酸镁+→+
8、锌与稀硫酸反应:氢气硫酸锌稀硫酸锌+→+
9、铝与稀硫酸反应:氢气硫酸铝稀硫酸铝+→+
10、铁与稀硫酸反应:氢气
+
铁+
→
稀硫酸
硫酸亚铁
11、铝与硫酸铜反应:铜
+
→
硫酸铝
硫酸铜
铝+
12、铁与硫酸铜反应:铜
+
铁+
→
硫酸铜
硫酸亚铁
13、铁与氯化铜反应:铜
+
→
氯化亚铁
氯化铜
铁+
(四)、复分解反应:
1、氯化钾与硝酸银反应:氯化银
+
氯化钾+
→
硝酸钾
硝酸银
2、盐酸与硝酸银反应:氯化银
→
+
硝酸银
硝酸
盐酸+
3、氧化铜与硫酸反应:水
+
→
硫酸铜
硫酸
氧化铜+
4、氧化镁与硫酸反应:水
+
硫酸镁
→
硫酸
氧化镁+
5、氧化铁与盐酸反应:水
→
+
盐酸
氯化铁
氧化铁+
6、盐酸与氢氧化钠反应:水
→
盐酸+
+
氯化钠
氢氧化钠
7、硫酸与氢氧化钠反应:水
→
+
氢氧化钠
硫酸+
硫酸钠
8、硝酸与氢氧化铜反应:
9、氯化钡与硫酸反应:水
+
氯化钡+
→
硫酸钡
硫酸
9、氯化钡与碳酸钠反应:
10、氢氧化钠硫酸铜反应:硫酸铜
→
+
氢氧化钠+
氢氧化铜
硫酸铜
11、氢氧化钙与氯化铁反应:氯化钙
→
+
氯化铁
氢氧化钙+
氢氧化铁
(五)、其他反应:
1、汽车尾气催化转换:
2、二氧化碳与氢氧化钙反应(澄清石灰水变浑浊):
3、大理石与盐酸反应:
4、甲烷(天然气的主要成分)燃烧:
5、一氧化碳还原氧化铁:
6、一氧化碳还原氧化铜:
10、碳酸氢铵与氢氧化钙混合:氨气
+
+
碳酸氢铵+
→
水
碳酸钙
氢氧化钙
11、硫酸铵与氢氧化钠溶液混合加热:氨气
−→
−
+
+
硫酸钠
水
氢氧化钠
硫酸铵△+
(NH
4)
2
SO
4
+2NaOH Na
2
SO
4
+ H
2
O+ NH
3
·H
2
O
7、葡萄糖在酶作用下的反应:水
二氧化碳
氧气
葡萄糖酶+
−→
−
+。
