高考化学-专题18物质结构与性质
高考化学复习专题检测—物质结构与性质(含解析)

高考化学复习专题检测—物质结构与性质(含解析)一、选择题(本题包括25小题,每小题2分,共50分,每小题只有一个选项符合题意)1.(2023·黑龙江省绥化市第九中学高三质检)已知在一定条件下,SO2也能体现其氧化性,例如:2H2S+SO2=3S+2H2O,下列化学用语使用正确的是()A.SO2的VSEPR模型:B.HS-电离的离子方程式:HS-+H2O H2S+OH-C.基态硫原子p x轨道的电子云轮廓图:D.基态氧原子最外层电子的轨道表示式:【答案】C【解析】A项,二氧化硫中心原子S的价层电子对数为3,有1对孤电子对,S杂化类型为sp2,VSEPR模型为平面三角形,A错误;B项,HS-电离的离子方程式HS-H++S2-,B错误;C项,基态硫原子P x轨道的电子云轮廓为哑铃型,C正确;D项,基态氧原子最外层电子的轨道表示式:,D错误;故选C。
2.(2023·江苏省南京市江宁区高三期中)尿素CO(NH2)2是一种高效化肥,也是一种化工原料。
反应CO2+2NH3CO(NH2)2+H2O可用于尿素的制备。
下列有关说法不正确...的是()A.NH3与CO(NH2)2均为极性分子B.N2H4分子的电子式为C.NH3的键角大于H2O的键角D.尿素分子σ键和π键的数目之比为6∶1【答案】D【解析】A项,NH3分子为三角锥形,为极性分子,CO(NH2)2中的N原子与NH3中的N成键方式相同,所以二者均为极性分子,A正确;B项,N原子的最外层电子数为5个,要达到稳定结构,N2H4的电子式为:,B正确;C项,NH3分子中有3个σ键,1对孤电子对,H2O分子中有2个σ键和2对孤电子对,孤电子对与成键电子对之间的排斥力大于成键电子对之间的排斥力,所以H2O的键角小于NH3中的键角,C正确;D项,1个单键1个σ键,1个双键1个σ键和1个π键,尿素中含有6个单键和1个双键,7个σ键和1个π键,尿素分子σ键和π键的数目之比为7∶1,D错误;故选D。
物质结构与性质(选择题)-2023年新高考化学真题题源解密(解析版)

专题十二物质结构与性质目录:2023年真题展现考向一分子的极性和共价键的极性考向二杂化类型和空间构型考向三电负性和电离能考向四晶胞及其计算考向五晶胞类型判断真题考查解读近年真题对比考向一电离能、电负性的应用考向二 杂化轨道及空间构型考向三 共价键的极性与分子极性的判断考向四 晶体类型判断考向五 晶胞粒子数与晶体化学式判断命题规律解密名校模拟探源易错易混速记考向一分子的极性和共价键的极性1(2023·山东卷第3题)下列分子属于极性分子的是()A.CS 2B.NF 3C.SO 3D.SiF 42(2023·浙江选考第12题)共价化合物Al 2Cl 6中所有原子均满足8电子稳定结构,一定条件下可发生反应:Al 2Cl 6+2NH 3=2Al NH 3 Cl 3,下列说法不正确的是()A.Al 2Cl 6的结构式为B.Al 2Cl 6为非极性分子C.该反应中NH 3的配位能力大于氯D.Al 2Br 6比Al 2Cl 6更难与NH 3发生反应3(2023·浙江选考第10题)X 、Y 、Z 、M 、Q 五种短周期元素,原子序数依次增大。
X 的2s 轨道全充满,Y 的s 能级电子数量是p 能级的两倍,M 是地壳中含量最多的元素,Q 是纯碱中的一种元素。
下列说法不正确的是()A.电负性:Z >XB.最高正价:Z <MC.Q 与M 的化合物中可能含有非极性共价键D.最高价氧化物对应水化物的酸性:Z >Y物质结构与性质(选择题)-2023年新高考化学真题题源解密(解析版)4(2023·新课标卷第12题)“肼合成酶”以其中的Fe 2+配合物为催化中心,可将NH 2OH 与NH 3转化为肼(NH 2NH 2),其反应历程如下所示。
下列说法错误的是()A.NH 2OH 、NH 3、H 2O 均为极性分子B.反应涉及N -H 、N -O 键断裂和N -H 键生成C.催化中心的Fe 2+被氧化为Fe 3+,后又被还原为Fe 2+D.将NH 2OH 替换为ND 2OD ,反应可得ND 2ND 2考向二杂化类型和空间构型5(2023·辽宁卷第6题)在光照下,螺呲喃发生开、闭环转换而变色,过程如下。
物质结构与性质综合题-2023年新高考化学真题(解析版)

物质结构与性质综合题目录:2023年真题展现考向一考查杂化轨道、空间结构、晶体类型、晶胞计算考向二考查同素异形体、晶体类型、杂化轨道、晶胞计算考向三考查电子排布式、电负性、空间结构、杂化轨道、晶胞计算考向四考查电子排布式、电离能、空间结构、晶胞计算考向五考查电子排布式、杂化轨道、晶胞计算真题考查解读近年真题对比考向一考查电子排布式、杂化轨道、空间构型、晶胞计算考向二考查电子排布式、键角、电负性、杂化轨道、晶胞计算考向三考查轨道表示式、电离能、杂化轨道、晶胞计算考向四考查电子排布式、元素周期表、配位键、氢键、相似相溶考向五考查电子排布式、键角、氢键、晶胞计算考向六考查电离能、几何构型、轨道表示式、顺磁性物质命题规律解密名校模拟探源易错易混速记考向一考查杂化轨道、空间结构、晶体类型、晶胞计算1(2023·浙江选考第17题)硅材料在生活中占有重要地位。
请回答:(1)Si (NH 2)4分子的空间结构(以Si 为中心)名称为,分子中氮原子的杂化轨道类型是。
Si (NH 2)4受热分解生成Si 3N 4和NH 3,其受热不稳定的原因是。
(2)由硅原子核形成的三种微粒,电子排布式分别为:①[Ne ]3s 23p 2、②[Ne ]3s 23p 1、③[Ne ]3s 23p 14s 1,有关这些微粒的叙述,正确的是。
A.微粒半径:③>①>②B.电子排布属于基态原子(或离子)的是:①②C.电离一个电子所需最低能量:①>②>③D.得电子能力:①>②(3)Si 与P 形成的某化合物晶体的晶胞如图。
该晶体类型是,该化合物的化学式为。
2(2023·山东卷第16题)卤素可形成许多结构和性质特殊的化合物。
回答下列问题:物质结构与性质综合题-2023年新高考化学真题(解析版)(1)-40℃时,F2与冰反应生成HOF利HF。
常温常压下,HOF为无色气休,固态HOF的晶体类型为,HOF水解反应的产物为(填化学式)。
2015高考化学总复习分章测试卷:原子结构与性质

专题18 原子结构与性质一、选择题1.在基态多电子原子中,关于核外电子能量的叙述错误的是( ) A .最易失去的电子能量最高 B .电离能最小的电子能量最高C .p 轨道电子能量一定高于s 轨道电子能量D .在离核最近区域内运动的电子能量最低 2.下列有关物质结构的表述正确的是( )A .次氯酸的电子式:H ··Cl ···· ··O ······B .氮原子轨道表示式为:C .氯原子的最外层电子排布式为3s 23p 5D .钠离子的结构示意图:3.具有如下电子层结构的电子,其相应元素一定属于同一主族的是( ) A .3p 能级上有2个未成对电子的原子和4p 能级上有2个未成对电子的原子 B .3p 能级上只有1个空轨道的原子和4p 能级上只有1个空轨道的原子 C .最外层电子排布为1s 2的原子和最外层电子排布为2s 22p 6的原子 D .最外层电子排布为1s 2的原子和最外层电子排布为2s 2的原子4.下表列出了某短周期元素R 的各级电离能数据(用I 1、I 2……表示,单位为kJ·mol-1)。
下列关于元素①R 的最高正价为+3价②R 元素位于元素周期表中第ⅡA 族 ③R 元素第一电离能大于同周期相邻元素 ④R 元素基态原子的电子排布式为1s 22s 2 A .①② B .②③ C .③④ D .①④5.现有四种元素的基态原子的电子排布式如下:①1s 22s 22p 63s 23p 4; ②1s 22s 22p 63s 23p 3;③1s 22s 22p 3; ④1s 22s 22p 5。
则下列有关比较中正确的是( )A .第一电离能:④>③>②>①B.原子半径:④>③>②>①C.电负性:④>③>②>①D.最高正化合价:④>③=②>①6.气态电中性基态原子的原子核外电子排布发生如下变化,吸收能量最多的是()A.1s22s22p63s23p2→1s22s22p63s23p1B.1s22s22p63s23p3→1s22s22p63s23p2C.1s2s22p63s23p4→1s22s22p63s23p3D.1s22s22p63s23p6d104s24p2→1s22s22p63s23p6d104s24p17.下列关于元素电负性大小的比较中,不正确的是()A.O<S<Se<Te B.C<N<O<FC.P<S<O<F D.K<Na<Mg<Al二、非选择题8.下面是s能级和p能级的原子轨道图,试回答下列问题:(1)s电子的原子轨道呈球形,每个s能级有1个原子轨道;p电子的原子轨道呈哑铃形,每个p能级有3个原子轨道。
高考化学物质结构与性质
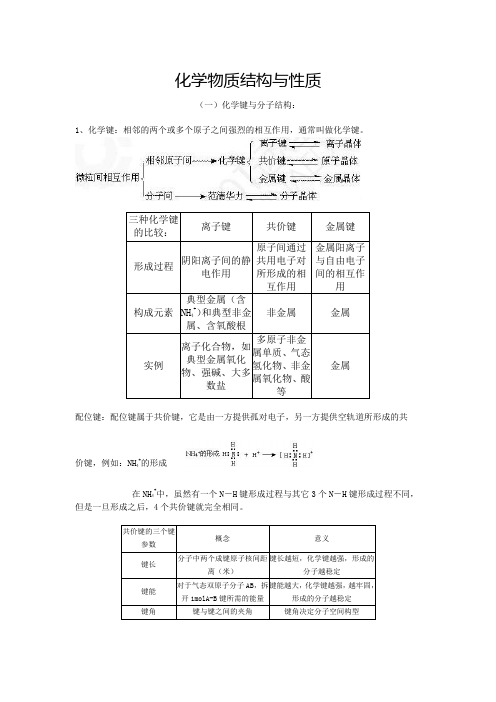
化学物质结构与性质(一)化学键与分子结构:1、化学键:相邻的两个或多个原子之间强烈的相互作用,通常叫做化学键。
配位键:配位键属于共价键,它是由一方提供孤对电子,另一方提供空轨道所形成的共价键,例如:NH 4+的形成在NH 4+中,虽然有一个N -H 键形成过程与其它3个N -H 键形成过程不同,但是一旦形成之后,4个共价键就完全相同。
键长、键能决定共价键的强弱和分子的稳定性:原子半径越小,键长越短,键能越大,分子越稳定。
共价键按成键形式可分为σ键和π键两种,σ键主要存在于单键中,π键主要存在于双键、叁键以及环状化合物中。
σ键较稳定,而π键一般较不稳定。
共价键具有饱和性和方向性两大特征。
2、分子结构:价层电子对互斥理论:把分子分成两大类:一类是中心原子上的价电子都用于形成共价键。
如CO2、CH2O、CH4等分子中的C原子。
它们的立体结构可用中心原子周围的原子数来预测,概括如下:另一类是中心原子上有孤对电子(未用于形成共价键的电子对)的分子。
如H2O和NH3中心原子上的孤对电子也要占据中心原子周围的空间,并参与互相排斥。
因而H2O分子呈V型,NH3分子呈三角锥型。
杂化轨道理论:在形成多原子分子的过程中,中心原子的若干能量相近的原子轨道重新组合,形成一组新的轨道,这个过程叫做轨道的杂化,产生的新轨道叫杂化轨道。
据参与杂化的s轨道与p轨道的数目,存在sp3、sp2、sp三种杂化。
杂化轨道理论分析多原子分子(离子)的立体结构价层电子对互斥模型判断简单分子或离子的空间构型说明:(1)等电子原理是指原子总数相同,价电子总数相同的分子或离子,对于主族元素而言,价电子就是其最外层电子数,即为最外层电子总数相等。
这一类分子或离子具有相似的化学键特征、分子结构以及部分物理性质相似,但一般情况下,化学性质并不相似。
同样,化学键相似,并不是指键角等一定相同。
利用等电子原理可判断一些简单分子或离子的主体构型,如:CO2、CNS-、NO2+、N3-的原子总数均为3,价电子总数均为16,因此,它们的空间构型均为直线型。
2017年高考真题-专题18+物质结构与性质(选修)Word版含解析

4龜十八物质徘构島艘肩1. 【2017新课标1卷】(15分)钾和碘的相关化合物在化工、医药、材料等领域有着广泛的应用。
回答下列问题:(1) ___________________________________________________________ 元素K的焰色反应呈紫红色,其中紫色对应的辐射波长为____________________________________________ nm (填标号)。
A. 404.4B. 553.5C. 589.2D. 670.8E. 766.5(2) ______________________________________________________ 基态K原子中,核外电子占据最高能层的符号是_____________________________________________________ ,占据该能层电子的电子云轮廓图形状为___________ 。
K和Cr属于同一周期,且核外最外层电子构型相同,但金属K的熔点、沸点等都比金属Cr低,原因是 ______________________________ 。
(3) __________________________________________________________________________ X射线衍射测定等发现,bAsF6中存在I;离子。
I;离子的几何构型为___________________________________ ,中心原子的杂化形式为___________________ 。
(4) KIO;晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立方结构,边长为a=0.446 nm ,晶胞中K、1、0分别处于顶角、体心、面心位置,如图所示。
K与O间的最短距离为 _______ nm,与K紧邻的O个数为____________ 。
(5) ______________________________________________________________ 在KIO;晶胞结构的另一种表示中,I处于各顶角位置,则K处于_________________________________________位置,O处于_______【参考答案】(1) A ( 2) N 球形K的原子半径较大且价电子数较少,金属键较弱(3) V 形sp3(4) 0.315 12 (5)体心棱心【解析】⑴紫色漩长400才4芳眄因此选项岛正确.(2両位于第四刪IA族」电子占据最高能层罡第四爲尺卩N层』最后一亍电子垣充在壬能级上』电子云轮廊图対球形j K的原子半彳耳衣于G的半径,且价电子数卡抄,金属键较乱因此K的熔钛海点.比G佻⑶耳与0为互为等电子检OF2属于V形,因此I;几何构型为V形,其中心原子的杂化类型为sp3; (4)根据晶胞结构,K与0间的最短距离是面对角线的一半,即为、上0 446 nm= 0.315nm ,根据晶胞的结构,距离2K最近的O的个数为12个;(5)根据KIO3的化学式,以及晶胞结构,可知K处于体心,O处于棱心。
【高考化学】2023年高考化学真题——物质结构与性质 元素推断

2023年高考化学真题 ——物质结构与性质 元素推断1.(2023·山东卷)下列分子属于极性分子的是 A .2CS B .3NF C .3SO D .4SiF【答案】B【详解】A .CS 2中C 上的孤电子对数为12×(4-2×2)=0,σ键电子对数为2,价层电子对数为2,CS 2的空间构型为直线形,分子中正负电中心重合,CS 2属于非极性分子,A 项不符合题意;B .NF 3中N 上的孤电子对数为12×(5-3×1)=1,σ键电子对数为3,价层电子对数为4,NF 3的空间构型为三角锥形,分子中正负电中心不重合,NF 3属于极性分子,B 项符合题意;C .SO 3中S 上的孤电子对数为12×(6-3×2)=0,σ键电子对数为3,价层电子对数为3,SO 3的空间构型为平面正三角形,分子中正负电中心重合,SO 3属于非极性分子,C 项不符合题意;D .SiF 4中Si 上的孤电子对数为12×(4-4×1)=0,σ键电子对数为4,价层电子对数为4,SiF 4的空间构型为正四面体形,分子中正负电中心重合,SiF 4属于非极性分子,D 项不符合题意; 答案选B 。
2.(2023·北京卷)中国科学家首次成功制得大面积单晶石墨炔,是碳材料科学的一大进步。
下列关于金刚石、石墨、石墨炔的说法正确的是A.三种物质中均有碳碳原子间的σ键B.三种物质中的碳原子都是3sp杂化C.三种物质的晶体类型相同D.三种物质均能导电【答案】A【详解】A.原子间优先形成σ键,三种物质中均存在σ键,A项正确;B.金刚石中所有碳原子均采用3sp杂化,石墨中所有碳原子均采用2sp杂化,石墨炔中苯环上的碳原子采用2sp杂化,碳碳三键上的碳原子采用sp杂化,B项错误;C.金刚石为共价晶体,石墨炔为分子晶体,石墨为混合晶体,C项错误;D.金刚石中没有自由移动电子,不能导电,D项错误;故选A。
高考化学物质结构与性质

2、分子性质 (1)分子得极性 ①分子构型与分子极性得关系
类型 实例 键得极性 空间构型 分子极性
X2
H2、N2 非极性键 直线形 非极性分子
XY HCl、NO 极性键
XY2 (X2Y)
CO2、CS2
极性键
直线形 极性分子 直线形 非极性分子
XY2
SO2 极性键
V形
(X2Y) H2O、H2S 极性键
b.配位键的表示:常用“―→”来表示配位键,箭头指向
接受孤电子对的原子,如 NH4+可表示为
,
在 NH+ 4 中,虽然有一个 N—H 键形成的过程与其他 3 个 N—H 键形成的过程不同,但是一旦形成之后,4 个共价 键就完全相同。
③配合物 如[Cu(NH3)4]SO4
配位体有孤电子对,如H2O、NH3、CO、F-、Cl-、CN-等。 中心原子有空轨道,如Fe3+、Cu2+、Zn2+、Ag+等。
高考化学物质结构与性质
栏目索引
考点一 基态原子得核外电子排布 考点二 元素得电离能和电负性 考点三 两大理论与分子构型 考点四 微粒作用与分子性质 考点五 微粒作用与晶体结构
考点一 基态原子得核外电子排布 1、排布规律
知识精讲
(1)能量最低原理:基态原子核外电子优先占据能量最低
得原子轨道,如Ge:1s22s22p63s23p63d104s24p2。
(3)无机含氧酸分子得酸性 无机含氧酸可写成(HO)mROn,如果成酸元素R相同,则n 值越大,R得正电性越高,使R—O—H中O得电子向R偏移, 在水分子得作用下越易电离出H+,酸性越强,如 HClO<HClO2<HClO3<HClO4。
3、范德华力、氢键、共价键得比较
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
专题18 物质结构与性质1.锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。
回答下列问题: (1)基态Ge 原子的核外电子排布式为[Ar]________,有________个未成对电子。
(2)Ge 与C 是同族元素,C 原子之间可以形成双键、叁键,但Ge 原子之间难以形成双键或叁键。
从原子结构角度分析,原因是________________________________________。
(3)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因_________________。
(4)光催化还原CO 2制备CH 424Zn 、Ge 、O 电负性由大至小的顺序是________。
(5)Ge 单晶具有金刚石型结构,其中Ge 原子的杂化方式为________,微粒之间存在的作用力是________。
(6)晶胞有两个基本要素:①原子坐标参数,表示晶胞内部各原子的相对位置。
如图为Ge 单晶的晶胞,其中原子坐标参数A 为(0,0,0);B 为(12,0,12);C 为(12,12,0)。
则D 原子的坐标参数为________。
②晶胞参数,描述晶胞的大小和形状。
已知Ge 单晶的晶胞参数a =565.76 pm ,其密度为________g·cm -3(列出计算式即可)。
对照晶胞图示,坐标系以及A 、B 、C 点坐标,选A 点为参照点,观察D 点在晶胞中位置(体对角线14处),由B 、C 点坐标可以推知D 点坐标。
②类似金刚石晶胞,1个晶胞含有8个锗原子,ρ=8×736.02×565.763×107g·cm-3。
答案:(1)3d 104s 24p 22(2)Ge 原子半径大,原子间形成的σ单键的键长较长,pp 轨道肩并肩重叠程度很小或几乎不能重叠,难以形成π键(3)GeCl 4、GeBr 4、GeI 4的熔、沸点依次增高。
原因是分子结构相似,相对分子质量依次增大,分子间相互作用力逐渐增强(4)O>Ge>Zn (5)sp 3共价键(6)①(14,14,14) ②8×736.02×565.763×1072.东晋《华阳国志·南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。
回答下列问题:(1)镍元素基态原子的电子排布式为________,3d 能级上的未成对电子数为________。
(2)硫酸镍溶于氨水形成[Ni(NH 3)6]SO 4蓝色溶液。
①[Ni(NH 3)6]SO 4中阴离子的立体构型是________。
②在[Ni(NH 3)6]2+中Ni 2+与NH 3之间形成的化学键称为________,提供孤电子对的成键原子是________。
③氨的沸点________(填“高于”或“低于”)膦(PH 3),原因是________;氨是________分子(填“极性”或“非极性”),中心原子的轨道杂化类型为________。
(3)单质铜及镍都是由________键形成的晶体;元素铜与镍的第二电离能分别为:I Cu =1 958 kJ·mol -1、I Ni =1 753 kJ·mol -1,I Cu >I Ni 的原因是___________________。
(4)某镍白铜合金的立方晶胞结构如图所示。
①晶胞中铜原子与镍原子的数量比为________。
②若合金的密度为d g·cm -3,晶胞参数a =________nm 。
答案:(1)1s 22s 22p 63s 23p 63d 84s 2或[Ar]3d 84s 22(2)①正四面体 ②配位键 N ③高于 NH 3分子间可形成氢键 极性 sp 3(3)金属 铜失去的是全充满的3d 10电子,镍失去的是4s 1电子 (4)①3∶1 ②⎣⎢⎡⎦⎥⎤2516.02×1023×d 13×1073.砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料等。
回答下列问题: (1)写出基态As 原子的核外电子排布式________。
(2)根据元素周期律,原子半径Ga________As ,第一电离能Ga________As 。
(填“大于”或“小于”) (3)AsCl 3分子的立体构型为________,其中As 的杂化轨道类型为________。
(4)GaF 3的熔点高于1 000℃,GaCl 3的熔点为77.9℃,其原因是____________。
(5)GaAs 的熔点为1 238℃,密度为ρ g·cm -3,其晶胞结构如图所示。
该晶体的类型为________,Ga 与As 以________键键合。
Ga 和As 的摩尔质量分别为M Ga g·mol -1和M As g·mol -1,原子半径分别为r Ga pm 和r As pm ,阿伏加德罗常数值为N A ,则GaAs 晶胞中原子的体积占晶胞体积的百分率为________。
解析:本题考查物质结构与性质知识,意在考查考生对相关原理的应用能力。
(1)根据构造原理可写出基态As 原子的核外电子排布式。
(2)同周期主族元素从左到右,原子半径逐渐减小,第一电离能呈增大趋势。
Ga 的原子半径大于As ,Ga 的第一电离能小于As 。
(3)AsCl 3的中心原子(As 原子)的价层电子对数为(5+1×3)/2=4,所以是sp 3杂化。
AsCl 3的立体构型为三角锥形。
(4)根据晶体类型比较熔点。
一般来说,离子晶体的熔点高于分子晶体的熔点。
(5)根据晶胞结构示意图可以看出,As 原子与Ga 原子形成了空间网状结构的晶体,结合GaAs 的熔点知GaAs 是原子晶体。
首先用均摊法计算出1个晶胞中含有As 原子的个数:8×1/8+6×1/2=4,再通过观察可知1个晶胞中含有4个Ga 原子。
4个As 原子和4个Ga 原子的总体积V 1=4×(43π×10-30×r 3As +43π×10-30×r 3Ga )cm 3;1个晶胞的质量为4个As 原子和4个Ga 原子的质量之和,即(4M As N A +4M Ga N A)g ,所以1个晶胞的体积V 2=4ρN A(M As +M Ga )cm 3。
最后V 1/V 2即得结果。
答案:(1)[Ar]3d 104s 24p 3(2)大于 小于 (3)三角锥形 sp 3(4)GaF 3为离子晶体,GaCl 3为分子晶体 (5)原子晶体 共价4π×10-30N A ρr 3Ga +r 3AsM Ga +M As×100%4.碳及其化合物广泛存在于自然界中。
回答下列问题:(1)处于一定空间运动状态的电子在原子核外出现的概率密度分布可用________形象化描述。
在基态14C 原子中,核外存在________对自旋相反的电子。
(2)碳在形成化合物时,其键型以共价键为主,原因是________。
(3)CS 2分子中,共价键的类型有________,C 原子的杂化轨道类型是________,写出两个与CS 2具有相同空间构型和键合形式的分子或离子________。
(4)CO 能与金属Fe 形成Fe(CO)5,该化合物的熔点为253 K ,沸点为376 K ,其固体属于________晶体。
(5)碳有多种同素异形体,其中石墨烯与金刚石的晶体结构如图所示:①在石墨烯晶体中,每个C 原子连接________个六元环,每个六元环占有________个C 原子。
②在金刚石晶体中,C 原子所连接的最小环也为六元环,每个C 原子连接________个六元环,六元环中最多有________个C 原子在同一平面。
答案:(1)电子云 2(2)C有4个价电子且半径小,难以通过得或失电子达到稳定电子结构(3)σ键和π键sp CO2、SCN-(或COS等)(4)分子(5)①3 2 ②12 45.A、B、C、D为原子序数依次增大的四种元素,A2-和B+具有相同的电子构型;C、D为同周期元素,C核外电子总数是最外层电子数的3倍;D元素最外层有一个未成对电子。
回答下列问题:(1)四种元素中电负性最大的是________(填元素符号),其中C原子的核外电子排布式为________。
(2)单质A有两种同素异形体,其中沸点高的是________(填分子式),原因是________;A和B的氢化物所属的晶体类型分别为________和________。
(3)C和D反应可生成组成比为1∶3的化合物E,E的立体构型为________,中心原子的杂化轨道类型为________。
(4)化合物D2A的立体构型为________,中心原子的价层电子对数为________,单质D与湿润的Na2CO3反应可制备D2A,其化学方程式为________。
(5)A和B能够形成化合物F,其晶胞结构如图所示,晶胞参数a=0.566 nm,F的化学式为________;晶胞中A原子的配位数为________;列式计算晶体F的密度(g·cm-3)________。
答案:(1)O 1s22s22p63s23p3(或[Ne]3s23p3)(2)O3O3相对分子质量较大,范德华力大分子晶体离子晶体(3)三角锥形sp3(4)V形 4 2Cl2+2Na2CO3+H2O===Cl2O+2NaHCO3+2NaCl(或2Cl2+Na2CO3===Cl2O+CO2+2NaCl)(5)Na2O 84×62 g·mol-1-3-73×6.02×1023mol-1=2.27 g·cm6.填写下列空白。
(1)周期表前四周期的元素a、b、c、d、e,原子序数依次增大。
a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同族;e的最外层只有1个电子,但次外层有18个电子。
回答下列问题:b、c、d中第一电离能最大的是________(填元素符号),e的价层电子轨道示意图为________。
(2)现有部分前36号元素的性质或原子结构如下表。
①R________________________________________________________________________。
②S元素的常见化合价为________,原因是____________________________________________________________________________________________________________。
