第七章光致电子转移(ppt)
光化学——电子转移页PPT文档

1983年授予H.Taube的诺贝尔化学奖,表彰他在 无机化学体系中氧化还原反应机制的开创性研究;
1988年由H.Michel,J.Deisenhofer及R.Huber共 享,诺贝尔化学奖表彰他们在阐明细菌光合作用 反应中详细机理方面的贡献,而这一过程所涉及 的机制也与光诱导的电子转移过程相关。
式中:
ΔG0为电子转移反应的自由能变化值; λ为电子转移前后电子给体与受体的内部结 构以及周围溶剂分子的取向调整所需要的 重组能;
HDA为电子转移前后的电子轨道偶合常数, 一般取决于电子给体和受体的中心距离而 与介质的性质无关。
通过对电子转移反应速率的研究,推出一
个极为简单的公式,可用以描述电子转移 反应活化能G*与反应中自由能变化ΔG0以 及总的重组能λ之间的关系:
第五章 电子转移
电子转移是最基本和最重要的化学反应 之一。它在物理学(半导体,显微扫描技 术)、合成(光)化学、分子生物学 (DNA 的降解与修复,酶催化等)、超分 子化学、材料科学以及显像技术等领域扮 演着极为重要的角色。
大半个世纪以来,人们对电子转移反应进 行了卓有成效的实验和理论研究。在过去的 二十多年,诺贝尔化学奖被多次授予给从事 电子转移相关工作的科学家,这不仅反映了 电子转移在这些领域中的突出地位和重要作 用,而且也说明它巨大的科学和实用价值。
二、太阳能电池
人工模拟光合作用的研究都是在均相溶 液中进行,光能被转化为化学能。光伏电 池是直接将光能转化为电能,其原理本质 上也是光诱导的电荷分离,但是是在非均 相的界面间在两种不同导电性能的物质界 面,如半导体P-N结、不同半导体或半导体 金属界面等产生的电荷分离
三 光催化分解水制氢
氢气是一种非常清洁的替代能源。与不可再生能
光诱导电荷转移

6/28/2019
分子间电荷转移态
电子转移也可以发生在具有不同得失电子能力的分子之间,反应 的产物。在受到光激发时,一个电子从电子给体(D)转移到电子受 体(A)并形成给体自由基阳离子(D•+)和受体自由基阴离子(A•-)的过 程。
6/28/2019
分子前线轨道解释光电转移
6/28/2019
6/28/2019
谢谢!!!
李尚 2014.09.27
基本概念
光控 分子开关
荧光探针
荧光
• 处于基态的分子吸收光能后,跃迁到激 发态,返回到基态的过程,发出荧光
• 荧光探针是建立在光谱化学和光学波导与测量技术基 础上,选择性的将分析对象的化学信息连续转变为分 析仪器易测量的荧光信号的分子测量装置。
• 分子开关是指一种具有双稳态的分子,通过施加一定的影响, 分子可以在两种状态之间进行可逆转换。指基于外部因素的 改变对分子荧光发射强度的影响而构建的一种分子开关。
分子内电荷转移态(ICT)
光诱导下电子转移可以发生在分子内部,即电子由给体单元向 受体单元转移,反应的产物通常称为。一是用于发射荧光, 另一部 分则用于和外来刺激相作用
6/28/2019
光诱导电荷转移在有机分子中的应用
6/28/2019
( 1) 光敏感类器件: 可用于分子 科学及生命科学研究, 作为敏感 探针来考察所研究体系的性质、 行为和变化。 ( 2) 光开关类器件: 可用作控制 性器件以及用于对收集数据的加 工、处理等方面。
( 2) 两个部分间应通过一共同的枢纽点相互联系或竞争; ( 3) 电子转移和电荷转移是这类器件化合物发生作用的重要机制。
6/28/2019
分子开关条件
光致电子转移反应机理的研究及应用

光致电子转移反应机理的研究及应用光致电子转移反应(PET)是一种利用光能激发组分之间电子的转移过程的物理化学反应。
通过光激发,低能电子从一个电子受体跃迁到一个电子供体分子上,导致分子结构的改变。
PET反应机理和应用在化学和生物领域具有广泛的研究价值和应用前景。
PET反应机理的研究主要关注于电子受体和电子供体之间的相互作用。
在可见光范围内,电子供体通常会吸收光能并转移给电子受体分子,从而产生带电粒子的转移。
电子供体与电子受体之间的距离和取向对于光激发和电子转移速率至关重要。
而分子的结构、电子亲和力和自旋态等因素也会影响PET反应的发生和速率。
PET反应具有很强的应用潜力。
在有机合成领域,PET反应可以用于合成新颖的有机分子,尤其是许多有机光敏物质。
例如,PET反应可以用于制备具有捕光功能的配合物、荧光探针和电子传递材料。
这些有机光敏物质在光子学器件、传感器、荧光显微镜和化学分析等领域有广泛的应用。
另外,PET反应还可以用于有机光化学催化,如光催化水分解、CO2转化和有机反应的可见光催化。
在生物学领域,PET反应具有研究荧光蛋白发光性质和信号传递的重要意义。
蛋白质结构中的芳香氨基酸残基,如色氨酸和酪氨酸,通常可以作为电子供体或电子受体,参与到PET反应中。
通过研究PET反应,可以揭示生物大分子的能量和电子转移机理,从而深入了解光合作用、荧光蛋白发光机制以及酶催化反应等生物过程。
在光学材料领域,PET反应也被用于制备具有特殊光学性质的材料。
例如,将PET技术应用于制备光电存储材料、光学传感器和光子晶体材料,可以增强材料的光学性能和调控光学信号传输。
总之,光致电子转移反应机理和应用的研究对于开发新的有机合成方法、理解光敏分子行为、揭示生物大分子的光生物学过程以及开发新型光学材料具有重要意义。
随着科学技术的发展,PET反应在化学、生物和材料科学中的应用前景将继续拓展,为实现更多的科技突破和创新提供了新的思路和方法。
光致电子转移反应机理的研究及应用

光致电子转移反应机理的研究及应用光致电子转移反应是一种在光照条件下发生的一种动力学过程,通过吸收光能激发电子而实现电子转移的反应。
在这种反应中,光能被吸收后,分子中的一个电子从基态(基本能级)跃迁到激发态(高能级),并在激发态下发生反应。
这种反应机制在生物体内以及有机合成领域都有着广泛的应用。
光致电子转移反应的机理可以分为两类:单电子转移和多电子转移。
在单电子转移反应中,一个电子从一个分子转移到另一个分子或原子上,从而产生自由基中间体。
这种反应通常用于光化学反应和有机合成领域。
在多电子转移反应中,多个电子参与反应,形成更复杂的物质结构或化合物。
这种反应通常用于生物体内的能量传递或电子传递等过程中。
研究光致电子转移反应的机理对于理解光化学反应、生物体内能量传递等过程至关重要。
通过实验方法、计算模拟等手段,可以揭示反应物、产物及中间体的结构、构型和电子结构,并推导出反应的速率常数、热力学参数等重要信息。
这些信息对于优化反应条件、设计新的药物分子、光催化剂等具有重要的指导意义。
在应用方面,光致电子转移反应已经被广泛应用于生物医药、环境保护、材料科学等领域。
在生物医药领域,光疗法利用光致电子转移反应杀灭癌细胞,成为一种新型的肿瘤治疗方法。
在环境保护领域,光催化技术利用光致电子转移反应降解有机污染物,净化水体和大气。
在材料科学领域,光催化材料和光敏材料利用光致电子转移反应制备具有特殊性能的材料。
综上所述,光致电子转移反应机制的研究和应用具有广阔的前景和潜力。
通过深入理解光致电子转移反应的机理,可以开发出更有效的光化学反应、生物医药和环境保护技术,并为人类社会的可持续发展做出贡献。
因此,有必要继续深入研究光致电子转移反应机制,以推动相关领域的发展和创新。
第七章、光致电子转移

能, 图中的λ则为重组能。它是在电子转移过程中,体系从平 衡的反应物态转变到平衡的产物态,因分子内核位置的变化 (包括键长和键角变化)所需的能量( λ内),以及当分子处 于溶剂环境中时,其周围溶剂分子因电子转移而引起的能量变 化( λ外)。它们可分别称为内重组能和外重组能。如下式所示: λ = λ内+ λ外
A-L-B
h
电子转移 A*-L-B
A+.- L- B- .
k ET = ν exp (-ΔG≠/ RT)
ΔG≠ = (ΔG 0 + λ) 2 / 4λ λ = λ内 + λ外
kET - 速度常数 λ - 重组能 ΔG≠-活化能 ΔG 0 - 自由能
E A*-L- B
3
Eop 2
14 A -L- B
Solvent molecules in fluctuation – constant change in energy of donor-acceptor complex
At critical solvent configuration q*, D*A complex has same free energy as D+A-
电子转移过程发生于众多的研究体系和对象, 包括:
在溶液中或在胶体中的有机分子;
在不同的界面如金属/ 液体、半导体/ 液体以及液 体/ 液体界面的电子转移过程;
绿色植物的光合作用和生命体系内蛋白质的氧化 还原反应等。近年来发展得极其迅速的分子
What is the Electron-Transfer ?
D,A
k1
D+ACRIP
光致电子转移
地球上几乎所有的生物都要依赖细菌或植物的光合作用生存。
在光合作用反应中 心,阳光触发一系列电子转移过程,引起电荷分离,最终在生物膜上形成质子梯 度。
从而,光量子的自由能存储下来,继而用于生成高能量的三磷酸腺苷(ATP )。
这些与光合作用相关的PET 过程稍后将在第12章中详细讨论。
这里我们先来了解一下光的吸收对分子的氧化还原性质的影响。
分子吸收一个光 子后,一个电子跃迁至高能量能级,分子成为激发态,给电子能力比基态更强, 可作为还原剂。
同时,电子的激发也在最高已占分子轨道中留下一个电子空穴, 分子的得电子能力也更强,可作为氧化剂。
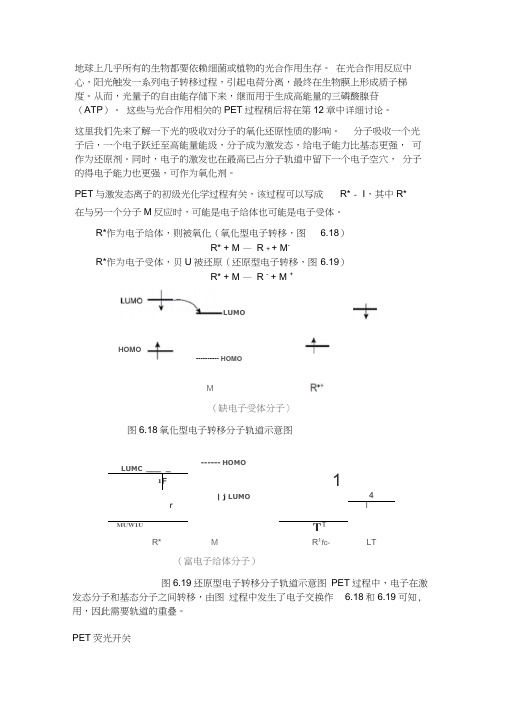
PET 与激发态离子的初级光化学过程有关,该过程可以写成 R* - I ,其中R* 在与另一个分子M 反应时,可能是电子给体也可能是电子受体。
R*作为电子给体,则被氧化(氧化型电子转移,图6.18)R* + M — R + + M -R*作为电子受体,贝U 被还原(还原型电子转移,图 6.19)R* + M — R - + M +(缺电子受体分子〉 图 6.18氧化型电子转移分子轨道示意图 LUMC ___ _------ HOMO 1 1 F| j LUMO4 rI MUW1UTT R*M R 1 f c- LT (富电子给体分子)图6.19还原型电子转移分子轨道示意图 PET 过程中,电子在激发态分子和基态分子之间转移,由图 过程中发生了电子交换作用,因此需要轨道的重叠。
PET 荧光开关LUMO---------- HOMOM6.18和6.19可知, HOMO用于阳离子荧光探针(包括H +)的分子是不发光的,但与阳离子结合后则可发 卄、|/ 丿光。
探针分子内有一个荧光发色团 (荧光团),该荧光团连接在一个带有给电子基团 的阳离子受体上。
受体向荧光团发生 PET 过程,荧光团因此猝灭(图6.20 )。
阳离子受体与阳离子连接后,电子转移受阻,荧光团重新发光。
因此 PET 传感 器可以作为分子开关。
光化学——电子转移页PPT文档

荧光共振能量转移(FRET)(Fluorescence / Förster resonance energy transfer) 是比较分子间距离与分子直径的有效工具, 广泛用于研究各种涉及分子间距离变化的 生物现象, 可以定量测量两个发光基团之间的距离, 在蛋白质空间构象、蛋白与蛋白间相互作 用、核酸与蛋白间相互作用以及其它一些
光诱导电子转移基本理论 目前,光诱导电子转移基本理论主要上有两种:
一是直接以反应自由能变化值ΔG0的正负直接判断电子转移
反应能否发生的能否发生的Rehm-Weller方程
二是以电子转移反应的活化能和自由能的相对大小来判断电
子转移反应能否发生的Marcus理论。
1956年,Marcus提出了电子转移反应 理论。该理论认为:电子转移反应速率取 决于电子给体与电子受体间的距离,反应 自由能的变化以及反应物与周围溶剂重组 能的大小,电子转移速率常数可表示为:
一个激发的分子与其基态相比通常是一 个更好的电子供体(Donor)或者电子受体 (Acceptor),通过电子的转移,它会“敏化” 或者永久改变其邻近分子的化学物理性质。
电子转移的分类
典型的 PET 体系是由三部分组成 包含电子给体(D)的主体分子 通过一间隔基 B(或是桥基) 和电子受体(A)相连而成。
方面的研究中得到广泛应用。
J(λ)表示光谱重叠积分
FRET的应用: ⑴、可用于研究蛋白质以及蛋白复合体的结构和 空间构象与布局
⑵、研究蛋白质的折叠 蛋白质折叠是一个非常繁杂的过程,因为它涉及 到大量的途径来将无数去折叠构象连接成为唯一 的天然构象。在用实验方法来探索各个途径所占 比例的漫长过程中,FRET已经能够测量自由状态 的单分子蛋白折叠的表面自由能特征,这些数据 在其他方法是难以得到的。
光致电子转移

Rehm-Weller 的经验结果,和 Marcus 理论所得到的 log k 对ΔG0 作图,即反应速度常数和电子转移驱动力的关系,分别列出如下:
(a) 1012
Marcus theory
kq / mol-1. dm3.s-1
(b)
Rehm-Weller equation
kr s-1
10
10
1010
C为一数值不大的常数
如DG0 <0 , 则电子转移过程能够发生
激发态和基态的氧化还原性质
Reductive and oxidative electron transfers
电子转移可在一个络合物的中间体内发生。即可在中间体内发生有效、而非绝 热的物种电子态的变化
D* + A
[D
*
, A]
[ D+ , A-]
按Marcus的理论,在非绝热势能面图中,电子是以谐振振荡频率,来回运动于 反应物的抛物线,每一周期则可穿越过渡态两次。因此,只有很小的(电子偶合)机 会,使体系过渡到产物态去。这一状况称为 非-绝热的限定。而在量子力学中,对它 的描述是借助于一级微扰理论,即通过谐振微扰,而得到Fermi黄金规则。如下式:
反应物DA与产物D+A- 沿反应标的非绝热势能面
Lippy 和Marcus 的电子转移模式
Lippy
Marcus
重 组 能 可从势能图中,等能反应(ΔG=0)下,反应物与产物的平衡几何形状 间的垂直分离值,来加以表示。可以看出,如果不存在有预重组的情况下,重组能 应当也是一个在电子转移过程中需要加以克服的“能垒”—— 早期Libby模型
Weller公式的应用:
G = Eox. - Ered
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
电子转移过程发生于众多的研究体系和对象, 包括:
在溶液中或在胶体中的有机分子;
在不同的界面如金属/ 液体、半导体/ 液体以及液 体/ 液体界面的电子转移过程;
绿色植物的光合作用和生命体系内蛋白质的氧化 还原反应等。近年来发展得极其迅速的分子
What is the Electron-Transfer ?
按 Rehm-Weller 公式可以计算出 DG0
D D G 0= E o x-E re d- E 0 ,0-C
式中, EOX 电子给体的氧化电位 Ered 电子受体的还原电位 DE0,0 为激发所提供的能量 C为一数值不大的常数
如DG0 <0 , 则电子转移过程能够发生
激发态和基态的氧化还原性质
Photo-induced Electron-Transfer
Excitation of Donor
Excitation of Donor
Photo-induced Electron-Transfer
Excitation of Acceptor
Excitation of Acceptor
激发态电子转移示意图
D ,A k1
D +A C R IP
k2 D + S A -
kx SSR IP
而这种转换的速度,则取决于一系列条件,包括:温度, D-A间 相互作用,以及它们与溶剂分子间的相互作用等。
电荷分离的速度常数k1依赖于溶剂的极性 例:D—蒽为电子给体,A—四硝基甲烷
k1=108(二氯甲烷) k1=1010(正己烷)
Marcus理论
Weller公式
Marcus electron transfer theory
Marcus electron transfer theory
D*A
D+A-
kQ
Zexp
对于SSRIP,它还有着比CRIP更髙的溶剂化重组能。
除溶剂的影响外,还须考虑电子转移与能量转移间的平衡问题。 因为激发的电子给体或受体,还可能存在下列的三种过程:
D*
kD
D + h (发光或其他)
A* D* + A
kA kET k -ET
h(发光或其他) D + A*(能量转移过程)kBiblioteka T [ A ] > kD 或
电子转移猝灭 常数和扩散速度 常数相接近。
因此通过猝灭常数测定,可判断过程的性质。
电子转移能否发生与电子给体与受体的氧化/还原电位有关!
G = E o x .-E r e d - E 0 ,0
Weller公式的应用:
如 G<0,则电子转移过程能够发生.
什么是电子转移过程的驱动力?
过程的自由能变化 DG0 可看作为驱动力,
C值--在溶液中粒子间的库仑作用项,这里取 0.2
Examples of electron donors and acceptors in the excited state
电子转移的两种理论
电子转移的两种理论:
Weller公式和Marcus理论。 Weller公式是由实验得出的结果 而Marcus理论则是从理论得到的
Chrysene
ΔS值约为0.04 Gibbs/mol
有关电子转移的平衡存在着下列关系:
D * + A
ket k-et
D + +A -
在气相中,基态条件下的电子转移可有下式:
在气相中,激发态条件下的电子转移可有下式:
ED*(即 E*)则为辐射所提供的帮助。(也可写成ΔE0,0)。
有关电子转移过程的平衡,可有下式:
光诱导电子转移过程,与电子交换能量转移不同, 它可形成离子自由基对(ionic radical pair )
不同的电子转移方式
通过空间的电子转移, Through space 电子给体和受体间的直接接触, Direct contact 通过键的电子转移, Through bond
Outer-Sphere Electron-Transfer
当
or
时,能量转移将会发生
k-ET [ D] > kA
[ D] [ A* ]
kET
KET
[ D*] [ A ]
k -ET
GET = DGETRT ln-K RE TlnKET
DG DH TDS
ET
ET
ET
对于刚性体系,由于熵变ΔS的减小,因此ΔS可忽略不计,上式可写成:
GET
HET
Naphthalene
ket D* + A
k–et
D+• + A•
ΔGet = Eo(D+/D) – Eo(A/A-) – ΔHet- TΔSoet
当激发物种处于溶液中时,则电子转移的ΔG将包括除气相中的结果外,还 应考虑溶剂的影响,如前述的SSRIP以及相关的重组能等,例:
Weller 经验公式,ΔGet = Eo(D+/D) – Eo(A/A-) – ΔE0,0 – C
D
CRIP
D+
A
A-
SSRIP
图. 在溶液中电子受体与给体间的电子转移,和不同离子自由基对的形成
Contact Radical Ion Pair (CRIP) & Solvent Separated Radical Ion Pair (SSRIP)
D* A
D+
A-
CRIP SSRIP
可以认为,在溶液中 CRIP 与SSRIP间存在着相互转换的关系:
Reductive and oxidative electron transfers
电子转移可在一个络合物的中间体内发生。即可在中间体内发生有效、而 非绝热的物种电子态的变化
D * + A [ D * ,A ] [ D + ,A - ] D + + A -
式中 [ ] 内即是所谓的络合体。但由于有溶剂分子存在,因此事情就并不如此简单。 这里存在有接触的离子自由基对(contact radical ionic pair, CRIP),以及溶剂分子 分离的离子自由基对(solvent separated radical ionic pair,SSRIP)
Through space
Inner-Sphere Electron-Transfer
Direct contact
Electron-Transfer via a Bridge
Through bond
荧光猝灭的电子转移和能量转移机理
荧光猝灭 过程,可有 1)电子转移 猝灭,和 2)能量转移 猝灭。
