大学有机化学反应方程式总结较全完整版
有机化学方程式(70个)

有机化学基础反应方程式汇总1. 甲烷(烷烃通式:C n H 2n +2)甲烷的制取:CH 3CaO △2CO 3+CH 4↑(1)氧化反应甲烷的燃烧:CH 4+2O 2 点燃CO 2+2H 2O甲烷不可使酸性高锰酸钾溶液及溴水褪色。
(2)取代反应CH 4+Cl 光照3Cl(一氯甲烷)+HClCH 3Cl+Cl 光照2Cl 2(二氯甲烷)+HClCH 2Cl 2+Cl 光照3(三氯甲烷)+HCl (CHCl 3又叫氯仿)CHCl 3+Cl 光照4(四氯化碳)+HCl(3)分解反应甲烷分解:CH 高温22. 乙烯(烯烃通式:C n H 2n )乙烯的制取:CH 3CH 2浓硫酸170℃2=CH 2↑+H 2O(消去反应)(1)氧化反应乙烯的燃烧:CH 2=CH 2+3O 点燃2+2H 2O乙烯可以使酸性高锰酸钾溶液褪色,发生氧化反应。
(2)加成反应与溴水加成:CH 2=CH 2+Br 2Br —CH 2Br与氢气加成:CH 2=CH 2+H 2催化剂CH 3CH 3 与氯化氢加成:CH 2=CH 2+HCl 催化剂CH 3CH 2Cl 与水加成:CH 2=CH 2+H 2O催化剂CH 3CH 2OH(3)聚合反应 乙烯加聚,生成聚乙烯:n CH 2=CH 2催化剂 [CH 2—CH 2 ] n 适当拓展:CH 3CH =CH 2+Cl 3׀ Cl CH -׀ ClCH 2 CH 3CH =CH 2+H 2催化剂CH 3CH 2CH 3 CH 3CH =CH 2+HCl 催化剂CH 3CH 2CH 2Cl 或CH 3׀ ClCHCH 3 CH 3CH =CH 2+H 2O 催化剂CH 3CH 2CH 2OH 或CH 3׀ OHCHCH 3 n CH 2=CH -CH 3催化剂 [CH 2—׀ CH 3CH ] n (聚丙烯) 3. 乙炔(炔烃通式:C n H 2n-2)乙炔的制取:CaC 2+2H 2 CH ↑+Ca(OH)2(1)氧化反应乙炔的燃烧:HC ≡CH+5O 点燃2+2H 2O乙炔可以使酸性高锰酸钾溶液褪色,发生氧化反应。
大学有机化学方程式总结

大学有机化学方程式总结
1. 碳氢化合物的烷烃类反应
1.1 卤代烃和氢化钠的反应
碳氢化合物(卤代烃)与氢化钠反应生成相应的烷烃,并释放出相应的卤化钠。
反应方程式如下:
R-X + NaH -> R-H + NaX
1.2 卤代烃和氢化亚铜的反应
碳氢化合物(卤代烃)与氢化亚铜反应生成相应的烷烃,并释放出相应的卤化铜。
反应方程式如下:
R-X + 2Cu2O + 2Cu -> R-H + 3Cu2X2
2. 醇类的酯化反应
2.1 醇与羧酸的酯化反应
醇与羧酸反应生成相应的酯,并释放出相应的水。
反应方程式如下:
R-OH + R'-COOH -> R'-COOR + H2O
2.2 醇与酸酐的酯化反应
醇与酸酐反应生成相应的酯,并释放出相应的酸。
反应方程式如下:
R-OH + R'-COO-CO-R'' -> R'-COOR + R''-COOH
3. 烯烃的加成反应
3.1 烯烃与卤素的加成反应
烯烃与卤素反应生成相应的二卤代烃。
反应方程式如下:
R-CH=CH2 + X2 -> R-CH2-CHX-CH2-X
3.2 烯烃与负氧化剂的加成反应
烯烃与负氧化剂反应生成相应的环氧化合物。
反应方程式如下:
R-CH=CH2 + [O] -> R-CH2-CH2-O-CH2-CH2-R
以上是一些大学有机化学方程式的总结,希望对您有帮助。
参考文献:
1. 有机化学方程式实验室手册,XX大学化学系,20XX年。
有机化学反应公式

有机化学反应公式
有机化学反应式是一个比较广泛的题目,因为有机化学反应式包括了很多不同的反应类型和反应条件。
以下是一些常见的有机化学反应式,但请注意,这并不是完整的有机化学反应式列表。
烷烃的燃烧反应:CH4 + 2O2 →CO2 + 2H2O
烷烃的氯代反应:CH4 + Cl2 →CH3Cl + HCl
烯烃的加成反应:CH2=CH2 + H2 →CH3CH3
烯烃的氧化反应:CH2=CH2 + O2 →CH3CHO
烯烃的聚合反应:nCH2=CH2 →-[-CH2-CH2-]n-
苯的硝化反应:C6H6 + HNO3 →C6H5NO2 + H2O
苯的磺化反应:C6H6 + H2SO4 →C6H5SO3H + H2O
醇的酯化反应:CH3OH + CH3COOH →CH3COOCH3 + H2O
酮的还原反应:2CH3COCH3 + H2 →CH3CH(OH)CH3
醛的氧化反应:CH3CHO + O2 →CH3COOH
以上只是有机化学反应式的一部分,有机化学是一个非常广泛和复杂的领域,有许多其他的反应和机制。
大学有机方程式总结_有机反应总结

化学竞赛有机方程式总结烷烃的化学反应:⒈卤代(F 2,I 2不可作卤化剂)CH 4+Cl 2−→−γh CH 3Cl+CH 2Cl 2+CHCl 3+CCl 4+HCl CH 3CH 2CH 3+Cl 2 −−−→−︒)25(h C γCH 3CHClCH 3(57%)+CH 3CH 2CH 2Cl(43%) ⒉氧化(略)烯烃的化学反应:⒈加卤素:CH 3CH=CH 2+Br 2−−→−4CCl CH 3CHBr -CH 2Br⒉加氢卤酸:CH 3CH=CH 2+HBr →CH 3CHBr -CH 3 符合马氏规则⒊与无机酸:CH 3CH=CH 2+H 2SO 4→CH 3CH(OSO 3H)-CH 3CH 3CH=CH 2+HOCl →CH 3CH(OH)-CH 2Cl⒋与水加成:CH 3CH=CH 2−−→−42SO H CH 3CH(OSO 3H)-CH 3−−→−O H 2CH 3CH(OH)CH 3 ⒌与硼烷加成:CH 3CH=CH 2−−→−62H B (CH 3CH 2CH 2)3B −−−→−)O(OH H -2CH 3CH 2CH 2OH顺式加成,反马氏取向生成1︒醇 ⒍过氧化物存在下,反马氏取向:CH 3CH=CH 2+HBr →−−−→−过氧化物CH 3CH 2CH 3Br HCl 、 HI 无此反应⒎催化加氢成烷烃:用Pt,Pd,Ni 等⒏高锰酸钾氧化:碱性:CH 3CH=CH 2+KMnO 4−−→−-OH CH 3CH(OH)CH 2OH+MnO 2+KOH酸性:CH 3CH=CH 2+KMnO 4−−→−∆+/H CH 3COOH+CO 2↑⒐臭氧化: R O RRC=CHR ′−→−3OC CHR ′→ 可根据产物推断反应物结构R O -O 故多用于双键位置判定′COOH′CHO′CH 2OH⒑催化氧化:CH 2=CH 2+O 2−−−→︒C 300-CH 2-CH 2 OCH 2=CH 2+O 2−−−−→−22CuCl~PdCl CH 3CHO 多用于工业生产 ⒒α-取代反应: 氯代:CH 2=CHCH 3−−−−→−︒C600-/400Cl 2CH 2=CH -CH 2Cl 溴代:CH 2=CHCH 3−−→−NBS CH 2=CH -CH 2Br ⒓重排:(CH 3)3CCH=CH 2−−→−HCl (CH 3)2CClCH(CH 3)2(主)+(CH 3)3CCHClCH 3(次) 这一重排是由于分步加成和第一步中,由H +对双键的加成生成碳正离子,其稳定性3︒>2︒>1︒,故在可能的情况下,它将以重排的方式趋于更稳定的状态。
(完整版)大学有机化学反应方程式总结(较全).doc
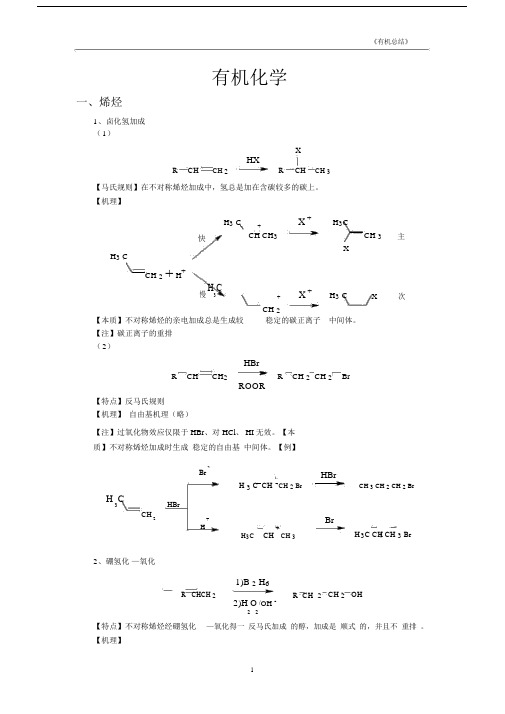
有机化学一、烯烃1、卤化氢加成 ( 1)XHXRCHCH 2R CHCH 3【马氏规则】在不对称烯烃加成中,氢总是加在含碳较多的碳上。
【机理】H 3 C+X +H 3CCH 3主快CH CH 3XH 3 CCH 2+ H +慢H 3C+X +H 3 CX次CH 2 【本质】不对称烯烃的亲电加成总是生成较稳定的碳正离子 中间体。
【注】碳正离子的重排( 2)HBrR CHCH 2 R CH 2 CH 2 BrROOR【特点】反马氏规则 【机理】 自由基机理(略)【注】过氧化物效应仅限于 HBr 、对 HCl 、 HI 无效。
【本质】不对称烯烃加成时生成 稳定的自由基 中间体。
【例】BrH 3 C CH CH 2 BrH 3CHBrCH2+H+H 3CCH CH 3HBrCH 3 CH 2 CH 2 BrBrH 3C CH CH 3 Br2、硼氢化 —氧化1)B 2 H 6R CHCH 2R CH 2 CH 2 OH2)H O /OH -2 2【特点】不对称烯烃经硼氢化 —氧化得一 反马氏加成 的醇,加成是 顺式 的,并且不 重排 。
【机理】H 3CH 3CH 3CCHCH 2CHCH 3CHCH 3HBH 2HBH 2HBH 2H 3CCH 3CH=CH 2-CH 2CH 2CH 3O OH-CH CH 2(CH 3 CH 2 CH 2 )3BH 3 CH 2CH 2C BO OHHBH 2CH 2CH 2CH 3CH 2CH 2CH 3CH 2 CH 2 CH 3+-H 3 CH 2 CH 2 C BOHOH 3CH 2CH 2 C -OCH 2CH 2CH 3B-CH CH CH3OOHHO O22CH 2CH 2CH 3HOO -B(OCH 2CH 2CH 3)3BOCH 2 CH 2CH 3OCH 2CH 2CH 3B(OCH 2 CH 2 CH 3 )3+3NaOH 3NaOH3HOCH 2CH2CH33+Na 3BO3【例】1)BH 3OH H2)H 2O 2/OH -CH3HCH33、 X 2 加成BrBr 2 /CCl 4CCCC Br【机理】Br BrBrBr -Br+C +C BrCCC CC CBrBr H 2OBr +BrC+C C-HCC C+2【注】通过机理可以看出,反应先形成三元环的溴鎓正离子,然后亲和试剂进攻从背面进攻,不难看出是反式加成。
有机化学方程式汇总

有机化学方程式汇总有机化学反应方程式汇总1.甲烷与氯气的反应:CH4 + Cl2 → CH3Cl + HClCH3Cl + Cl2 → CH2Cl2 + HClCH2Cl2 + Cl2 → CCl4 + HCl(分步取代)燃烧:CH4 + 2O2 → CO2 + 2H2O2.烷烃的燃烧通式:CnH2n+2 + (3n+1)O2 → nCO2 + (2n+2)H2O3.甲烷的热分解:CH4 高温 C + 2H24.烷烃的热分解:C4H10 → C2H4 + C2H6C4H10 → CH4 + C3H65.乙烯实验室制法:XXX H2SO4 → CH2=CH2 ↑(浓硫酸为催化剂和脱水剂)点燃:CH2=CH2 + 3O2 → 2CO2 + 2H2O6.乙烯的燃烧:CH2=CH2 + 3O2 → 2CO2 + 2H2O7.乙烯通入溴水中:CH2=CH2 + Br2 → CH2BrCH2Br8.乙烯和氢气加成:催化剂:CH3CH=CH2 + H2 → CH3CH2CH39.乙烯和HCl的反应:催化剂:CH2=CH2 + HCl → CH3CH2Cl10.乙烯水化制乙醇:CH2=CH2 + H2O → CH3CH2OH11.乙烯催化氧化制备乙醛:催化剂:2CH2=CH2 + O2 → 2CH3CHO加热加压:CH2―CH2―n―CH2―CH―12.乙烯的加聚反应:催化剂:n CH2=CH2 → (-CH2-CH2-)n13.制取聚丙烯:催化剂:n CH3CH=CH2 → (-CH2-CH(CH3)-)n14.1,3-丁二烯的加成反应:1,2加成:CH2=CH-CH=CH2 + Cl2 → CH2Cl-CH(Cl)-CH=CH2 Cl + Cl2 → Cl21,4加成:Cl完全加成+ 2Cl2 → Cl3CCCl315.1,3-丁二烯的加成反应:n CH2=C-CH=CH2 → (-CH2-C=CH-CH2-)n-CH316.乙炔的制取:CaC2 + 2H2O → C2H2 ↑ + Ca(OH)2点燃:2C2H2 + 5O2 → 4CO2 + 2H2O18.乙炔的燃烧公式为O(l) + 2600 kJ,表示在氧气存在下,乙炔会燃烧并释放出2600千焦的能量。
(完整版)有机化学方程式汇总

有机化学反应方程式汇总1. 甲烷与氯气CH 4+Cl 2CH 3Cl+HCl CH 3Cl+Cl 2CH 2Cl 2+HClCH 2Cl 2+Cl 2CHCl 3+HCl CHCl 3+Cl 2CCl 4+HCl (分步取代)2. 甲烷的燃烧3. 烷烃的燃烧通式4. 甲烷的热分解 CH 4−−→−高温C+2H 25. 烷烃的热分解6. 乙烯实验室制法 CH 3CH 2OH H 2O + CH 2=CH 2 ↑(浓硫酸:催化剂,脱水剂)7. 乙烯的燃烧8. 乙烯通入溴水中9. 乙烯和氢气加成10. 乙烯和HCl 的反应 11. 乙烯水化制乙醇 12. 乙烯催化氧化制备乙醛13. 乙烯的加聚反应 14. 制取聚丙烯 CH 4 + 2O CO 2 + 2H 2O燃烧C n H 2n+2 + O n CO 2 + (n + 1)H 2O 3n+1 2燃烧△C 4H C 2H 4+C 2H 6△C 4H CH 4 + C 3H 6CH 2=CH 2 + 3O 2 2CO 2 + 2H 2O点燃2CH 2=CH 2 + O 2CH 3CHO催化剂加热加压CH 3CH=CH 2 + H CH 3CH 2CH 3催化剂CH 2=CH 2 + Br 2 CH 2BrCH 2BrCH 2=CH 2 + HCl CH3CH 2Cl 催化剂CH 2=CH 2 + H 2O CH 3CH 2OH催化剂―CH 2―CH 2―nn CH 2=CH 2催化剂―CH 2――nn CH 2=CH ―CH 催化剂15. 1,3-丁二烯的加成反应 1,2加成1,4加成完全加成16. 1,3-丁二烯的加成反应 17. 乙炔的制取 CaC 2+2H 2O →C 2H 2↑+Ca(OH)218. 乙炔的燃烧19. 乙炔通入溴水中20. 乙炔与氢气的加成反应21. 乙炔水化制备乙醛22. 聚氯乙烯的制备23. 苯的燃烧 24. 苯与液溴反应(FeBr 3作催化剂)25. 苯的硝化反应Cl+ Cl 2催化剂+ Cl 2催化剂Cl+ 2Cl 2催化剂Cl ClCl―CH 2―C=CH ―CH 2―nn CH 2=C ―CH=CH 2催化剂CH 3CH 32 C 2H 2 + 5 O 4 CO 2 + 2 H 2O (l) + 2600 kJ点燃1, 2 - 二溴乙烷HC CH +Br BrC C Br Br H H 1, 1 , 2 , 2 - 四溴乙烷+Br BrC C Br BrH H C C Br Br H Br Br H 催化剂HC CH+H 2H 2C CH 2CH ≡CH + HCl CH 2=CHCl 催化剂氯乙烯CH ≡CH + H 2O乙醛3C C OH 催化剂聚氯乙烯H 2C CHCln -CH 2-CH --Cln 点燃+ 15 O 12 CO 2 + 6 H 2O2+ Br 溴苯NO 226. 苯的磺化反应27. 苯与氢气加成生成环己烷28. 苯与氯气的加成反应29. 苯的同系物被高锰酸钾酸性溶液氧化30.甲苯和氯气的取代反应31. 甲苯的硝化反应32. 甲苯和氢气的加成反应33. 溴乙烷水解 CH 3CH 2Br + NaOH CH 3CH 2OH + NaBr34. 溴乙烷消去反应 CH 3CH 2Br +NaOH CH 2=CH 2↑ + NaBr + H 2O35. 乙醇与钠反应 2CH 3CH 2OH + 2Na 2CH 3CH 2ONa + H 2↑36. 乙醇催化氧化 2CH 3CH 2OH + O 2 2CH 3CHO + 2H 2O37. 乙醇的燃烧 CH 3CH 2OH +3O 2→2CO 2 + 3H 2OH 2O,△ Cu △醇 △HO SO 3+△+ H 2O3H 苯磺酸催化剂2△ClCl Cl ClClCl + 3 Cl 2光照C H KMnO 4 (H +)CH 3HO NO 2+ 3浓硫酸+ 3 H 2OCH 3NO 2NO 2O 2N2,4,6-三硝基甲苯 (TNT)+ 3 H CH 3CH 3CH 3CH 3Cl+ Cl + HClFeCH 3ClCH 3+ Cl + HClFe38. 乙醇与浓氢溴酸的反应 CH 3CH 2OH +HBr →CH 3CH 2Br + H 2O39. 乙醇脱水(分子内、分子间) CH 3CH 2OH CH 2=CH 2 ↑+H 2O (消去反应)2CH 3CH 2OH CH 3CH 2—O —CH 2CH 3+ H 2O (取代反应)40. 苯酚的电离方程式 41. 苯酚与NaOH 溶液反应42. 苯酚与金属钠反应 43. 苯酚和碳酸钠溶液反应44. 苯酚钠和盐酸反应 45. 苯酚钠溶液中通入CO 2气体46. 苯酚和浓溴水反应(苯酚的定性检验和定量测定方法)47. 苯酚的硝化反应48. 苯酚与FeCl 3溶液49. 苯酚的加成反应浓H 2SO 4 140℃OH电离O -+ H+OH + NaOHONa + H 2OOH 2 + 2Na ONa 2 + H OH + Na 2CO ONa + NaHCO 3+ HCl OH + NaClONa + CO 2 + H 2OH + NaHCO 3ONa OH+ 3 HNO + 3 H 2OOHNO 2O 2NNO 2浓硫酸苦味酸OHFeCl 3溶液紫色,易溶于水的物质OHOH+ 3 H 2Ni环己醇OH+ 3 Br OHBr BrBr+ 3 HBr50. 苯酚的缩聚反应n + n + n H 2O2OHH C OH n51.苯酚的酯化反应52. 乙醛的加成反应(还原反应) 53. 乙醛的氧化反应—燃烧反应54. 乙醛的催化氧化反应 55. 乙醛与银氨溶液的反应 ③ CH 3CHO + 2 [Ag(NH 3)2]+3COO - + NH 4+3 + H 2O56. 乙醛与Cu(OH)2悬浊液反应57. 乙醛的制备方法乙醇氧化法乙烯氧化法乙炔水化法58. 醛的加成反应(还原反应)59. 醛的催化氧化反应OH+ CH 3COOH + H 2OOOCCH3乙酸酐CH 3CHO + H 23CH 2OH 2CH 3CHO + 5O 4CO 2 + 4H 2O点燃2 CH 3CHO + O 3COOH① Ag + + NH 3·H 2O AgOH + NH 4+② AgOH + 2 NH ·H 2O [Ag(NH3)2]+ + OH - + 2 H 2O2 CH 3CH 2OH + O 3CHO + 2 H 2O + H 23CHOHC CH 2 + O 22 CH 3CHO 加热 加压H 2C CH 2催化剂2R―CHO + O 2―COOHR ―CHO + H 2―CH 2OHCH 3CHO + 2 Cu(OH)23COOH + Cu 2O + 2 H 2OCu 2+ + 2 OH - Cu(OH)260. 醛与银氨溶液的反应 61. 醛与Cu(OH)2悬浊液反应 62. 甲醛的银镜反应 63. 甲醛与Cu(OH)2悬浊液反应 64. 乙酸与氢氧化铜悬浊液 2CH 3COOH + Cu(OH)2 = (CH 3COO)2Cu + 2H 2O65. 乙酸乙酯制取(用饱和碳酸钠溶液收集)CH 3COOH + CH 3CH 2OHCH 3COOC 2H 5 + H 2O66. 乙二酸和乙二醇反应C ―OH ∣C ―OH OOHO ―CH 2∣HO ―CH 2+ + 2H 2O 浓硫酸C C O CH 2CH 2O O OnHOOC ―COOH + nHOCH 2―CH 2OH + 2nH 2O ―C ―C ―OCH 2―CH 2O ―O On浓硫酸67. 乙醇和硝酸酯化CH 3CH 2OH + HNO 3 CH 3CH 2ONO 2 + H 2O浓硫酸68. 乙酸乙酯的水解CH 3COOC 2H 5 + H 2O CH 3COOH + CH 3CH 2OH 稀硫酸CH 3COOC 2H 5 + NaOH ==== CH 3COONa + CH 3CH 2OH69. 甲酸钠与银氨溶液反应HCOONa +2Ag(NH 3)2OH NH 4OCOONa +2Ag ↓+3NH 3↑+H2O浓硫酸△R ―CHO + 2Cu(OH)2 R ―COOH + Cu 2O ↓ + 2H 2OR ―CHO + 2Ag(NH 3)2OH R ―COONH 4 + 2Ag ↓ + 3NH 3 + H 2O HCHO + 4 Cu(OH)2 CO 2 + 2 Cu 2O + 5 H 2O HCHO + 4 [Ag(NH 3)2]+ + 4 OH - (NH 4)2CO 3 + 4 Ag + 6 NH 3 + 2 H 2O70.甲酸钠与新制氢氧化铜反应HCOONa+2Cu(OH)2+ NaOH Na2CO3+Cu2O↓+3H2O71.葡萄糖的银镜反应CH2OH(CHOH)4CHO+2Ag(NH3)2OHCH2OH(CHOH)4COONH4+2Ag↓+3NH3↑+H2O72.葡萄糖与新制氢氧化铜反应CH2OH(CHOH)4CHO+2Cu(OH)2 +NaOH CH2OH(CHOH)4COONa+Cu2O↓+3H2O 73. 蔗糖水解C12H22O11 + H2O 催化剂C 6H 12O6 + C6H12O6蔗糖葡萄糖果糖74. 麦芽糖水解C12H22O11 + H2O 催化剂2C6H12O6麦芽糖葡萄糖75. 淀粉水解(C6H10O5)n + nH2O 催化剂nC6H12O6淀粉葡萄糖76. 纤维素水解(C6H10O5)n + nH2O 催化剂nC6H12O6纤维素葡萄糖77. 工业制取肥皂(皂化反应)C17H35COO―CH2∣C17H35COO―CH∣C17H35COO―CH2+ 3NaOH 3 C17H35COONa +HO―CH2∣HO―CH∣HO―CH278.油酸甘油酯硬化79.工业制造乙苯 + CH2=CH280.制造硝酸纤维的反应81.甲苯与高锰酸钾酸性溶液反应5 +6KMnO4+9H2SO4→ 5 +3K2SO4+ 6MnSO4+ 14H2O82.甘油制取炸药83.甲醛与苯酚反应制取酚醛树脂代表物之间的转化关系:CH3CH3CH2=CH2 CH=CH CH2=CHCl CH3CH 2OHCH 2BrCH2BrCH2OHCH2OHCHOCHOCOOHCOOH[ CH2—CH ]nClCH3CHO CH3COOHCH3COOC2H5CH3CH2BrO=CO=CCH2CH2OO。
有机化学反应方程式小结

有机化学反应方程式小结一.取代反应1.CH4+Cl2--光→CH3Cl+HCl2.C2H6+Cl2--光→C2H5Cl+HCl3.C6H6+Br2—Fe→C6H5Br+HBr4.C2H5OH+HBr--加热→C2H5Br+H2O5.C6H6+HNO3--H2SO4水浴加热→C6H5NO2+H2O6.C6H5Cl+H2O--NaOHCu,高温,加压→C6H5OH+HCl7.C2H5Cl+H2O—NaOH→C2H5OH+HCl8.CH3COOC2H5+H2O—稀硫酸,加热→CH3COOH+C2H5OH9.(C17H35COO)3C3H5+3NaOH→C3H5(OH)3+3C17H35COOH10.2CH3CH2OH+2Na→2CH3CH2ONa+H211.2C6H5OH+2Na→2C6H5ONa+H2↑12.2CH3COOH+2Na→2CH3COONa+H2↑(分子间脱水)C2H5OH+C2H5OH--浓H2SO4,140℃→C2H5OC2H5+H2O二.加成反应13.CH2=CH2+H2→Ni,加热→CH3CH314.CH2=CH2+HCl--催化剂,加热→CH3CH2Cl15.C2H2+H2--Ni,加热→CH2=CH216.C2H2+2H2--Ni,加热→CH3CH317.C2H2+2HCl--催化剂,加热→CH3CHCl218.CH2=CH-CH=CH2+Br2→CH2=CH-CHBr-CH2Br19.CH2=CH-CH=CH2+Br2→CH2Br-CH=CH-CH2Br20.CH2=CH-CH=CH2+2Br2→BrCH2-CHBr-CHBr-CH2Br21.CH3CHO+H2–Ni→CH3CH2OH22.CH2OH-(CHOH)4-CHO+H2--Ni→CH2OH-(CHOH)4-CH2OH23.C6H6+3H2—Ni→C6H12(环己烷)24.C6H6+3Cl2--光→C6H6Cl625.CH2=CH2+H2O--H2SO4,加热,加压→CH3CH2OH三.消去反应26.CH3CH2OH--浓H2SO4,170℃→CH2=CH2↑+H2O27.CH3CH2Br+NaOH--醇,加热→CH2=CH2↑+NaBr+H2O四.酯化反应(取代反应)28.CH3COOH+CH3CH2OH--浓H2SO4,加热→CH3COOC2H5+H2O29.C3H5(OH)3+3HNO3--浓H2SO4→C3H5(ONO2)3+3H2O五.水解(卤代烃、酯、油脂的水解见上,亦是取代反应)30.CH3COONa+H2O→CH3COOH+NaOH31.CH3CH2ONa+H2O→CH3CH2OH+NaOH32.C6H5ONa+H2O→C6H5OH+NaOH33.C17H35COONa+H2O→C17H35COOH+NaOH34.(C6H10O5)n+nH2O--H2SO4,加热→nC6H12O6六.氧化反应35.2C2H5OH+O2--Cu或Ag,加热→2CH3CHO+2H2O36.C6H12O6+6O2→6CO2+6H2O+热37.2CH3CHO+O2→2CH3COOH38.CH3CHO+2[Ag(NH3)2]OH→CH3COONH4+2Ag↓+3NH3+H2O39.CH3CHO+2Cu(OH)2加热→CH3COOH+Cu2O↓+2H2O40.CH2OH(CHOH)4CHO+2[Ag(NH3)2]OH→CH2OH(CHOH)4COONH4+2Ag↓+3NH3+H2O41.CH2OH(CHOH)4CHO+2Cu(OH)2--加热→CH2OH(CHOH)4COOH+Cu2O↓+2H2O42.HCOOH+2[Ag(NH3)2]OH→NH4HCO3+2Ag↓+3NH3+H2O43.HCOOH+2Cu(OH)2加热→CO2+Cu2O↓+3H2O44.HCOONa+2[Ag(NH3)2]OH→NaHCO3+4NH3+2Ag↓+H2O45.HCOONH4+2[Ag(NH3)2]OH→NH4HCO3+2Ag↓+4NH3+H2O46.HCOOR+2[Ag(NH3)2]OH→NH4OCOOR+2Ag↓+3NH3+H2O47.HCHO+2[Ag(NH3)2]OH→HCOONH4+2Ag↓+3NH3+H2O48.HCHO+4[Ag(NH3)2]OH→NH4HCO3+4Ag↓+7NH3+2H2O49.HCHO+4Cu(OH)2加热→CO2+2Cu2O↓+5H2O七.还原反应50.CH3COCH3+H2--Ni→CH3CHOHCH360.HCHO+H2--Ni→CH3OH51.C6H5CH=CH2+4H2--Ni→C6H11CH2CH3八.加聚反应52.nCH2=CH2→[CH2-CH2]n53.nCH3-CH=CH2→[CH-CH2]n67.nCH2=C-COOCH3→[CH2-C]n68.nCH2=C-CH=CH2→[CH2-C=CH-CH2]n九.缩聚反应氨基酸合成蛋白质。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
大学有机化学反应方程式总结较全Document serial number【NL89WT-NY98YT-NC8CB-NNUUT-NUT108】有机化学一、烯烃1、卤化氢加成 (1)CHCH 2RHXCHCH 3RX【马氏规则】在不对称烯烃加成中,氢总是加在含碳较多的碳上。
【机理】CH 2CH 3CH +CH 3CH 3X +CH 3CH 3X+H +CH 2+C3X +CH 3X主次【本质】不对称烯烃的亲电加成总是生成较稳定的碳正离子中间体。
【注】碳正离子的重排 (2)CHCH 2RCH 2CH 2R BrHBrROOR【特点】反马氏规则【机理】 自由基机理(略)【注】过氧化物效应仅限于HBr 、对HCl 、HI 无效。
【本质】不对称烯烃加成时生成稳定的自由基中间体。
【例】CH 2CH3BrCH CH 2BrC H 3CH +CH 3C H 3HBrBrCH 3CH 2CH 2BrCH BrCH 3C H 32、硼氢化—氧化CHCH 2RCH 2CH 2R OH1)B 2H 62)H 2O 2/OH-【特点】不对称烯烃经硼氢化—氧化得一反马氏加成的醇,加成是顺式的,并且不重排。
【机理】CH2CH 33H 323H 32CH CH 2CH 3HBH 2CH CH=CH (CH 3CH 2CH 2)3B-H 3CH 2CH 2C22CH 3CH 2B OCH2CH 2CH 3H 3CH 2CH 2CCH 2CH 2CH 3+OH -OHB-OC H 2CH 2CH 3CH 2CH 2CH 3H 3CH 2CH 2OBOC H 2CH 2CH 3CH 2CH 2CH 3OC H 2CH 2CH 3HOO -B(OCH 2CH 2CH 3)3B(OCH 2CH 2CH 3)3+3NaOH 3NaOH3HOC H 2CH 2CH 33+Na 3BO 32【例】CH 31)BH 32)H 2O 2/OH -CH 3HHOH3、X 2加成CCBr /CClCC BrBr【机理】CC CC Br BrC CBr +CC Br OH 2+-H +CC Br OH【注】通过机理可以看出,反应先形成三元环的溴鎓正离子,然后亲和试剂进攻从背面进攻,不难看出是反式加成。
不对称的烯烃,亲核试剂进攻主要取决于空间效应。
【特点】反式加成 4、烯烃的氧化1)稀冷高锰酸钾氧化成邻二醇。
3H 33H3稀冷KMnO433M n O OOO H 2O 3H 33H 3 2)热浓酸性高锰酸钾氧化C C H R R 2R 1KMnO 4H +CRR 1O +R 2COHO3)臭氧氧化C C H R R 2R 1CRR 1O +R 2CHO1)O 32)Zn/H 2O4)过氧酸氧化C C HR R 2R 1ROOOH21C CH R R 2R121Ag+O 25、烯烃的复分解反应CH 2RCH 2R 1+催化剂C H 2CH 2RR 1【例】OC H2CH 2C 6H 5OC 6H 5+C H 2CH 26、共轭二烯烃 1)卤化氢加成CH CH 2HXCH 3XCH 2CH 3X高温1,4加成为主低温1,2加成为主2)狄尔斯-阿德尔(Diels-Alder )反应【描述】共轭二烯烃和烯烃在加热的条件下很容易生成环状的1,4加成产物。
【例】CH 2CH 2+O OO苯∆O OOCH 2CH 2+苯∆C H OCH 2C H O二、脂环烃1、环丙烷的化学反应【描述】三元环由于张力而不稳定,易发生加成反应开环,类似碳碳双键。
H /Ni CH 2CH 2CH 2HHCH 2CH 2CH 2Br Br CH 2CH 2CH 2H OH CH 2CH 2CH 2HX【特点】环烷烃都有抗氧化性,可用于区分不饱和化合物。
【注】遵循马氏规则 【例】CH3CH 2CH CH 2HBrCH 32、环烷烃制备1)武兹(Wurtz )反应【描述】通过碱金属脱去卤素,制备环烷烃。
【例】C C XX C 2H 5OHCCCH 2XCH 2X 双键的保护2)卡宾①卡宾的生成A 、多卤代物的α消除X 3CH+-N aOH a,R -LiC XX+X-+H YB 、由某些双键化合物的分解CO H 2C :N 2H 2C :Cl 2H 2C :Cl-H 2OH 2+Cl2C Cl++++CO 2②卡宾与烯烃的加成反应【特点】顺式加成,构型保持 【例】Cl CH/NaOH相转移催化剂Cl ClCH 3CH 3Br CH/KOC(CH )3HOC(CH 3)33H3③类卡宾【描述】类卡宾是一类在反应中能起到卡宾作用的非卡宾类化合物,最常用的类卡宾是ICH 2ZnI 。
C H2I 2Cu(Zn)I C H 2ZnI+制备【特点】顺式加成,构型保持 【例】CH I Zn(Cu)CH 3CH 3CH I 3H 3三、炔烃1、还原成烯烃 1)、顺式加成R 2R 1R 1R2Cat=[P b/BaSO4,P b/CaC O 3,Ni 3B...](C H 3COO)2NiNaBH 4Ni 3BH 2Cat2)、反式加成R 2R 1H 2CatR 1R 2Cat=[Na/ 液氨...]2、亲电加成 1)、加X 2R 2R 1Br 2R 2R 1BrBr【机理】中间体Br+R 2R 1【特点】反式加成 2)、加HXCHR2HBrC CH 3BrCH 3BrRR HBrR R BrH(一摩尔的卤化氢主要为反式加成)3)、加H 2OCHRH 2OHgSO 4/H2SO 4O CH 3RCH RO重排【机理】CH RC+Hg+HRHg2+H 2OR HHg +OH 2+-H+R HHg +OH R HHg +OHH +O CH 3R重排【特点】炔烃水合符合马式规则。
【注】只有乙炔水合生成乙醛,其他炔烃都生成相应的酮。
3、亲核加成 1)、OCH 3CH CH+OOHCH 3Zn(CH 3COO)CH 2CH OCCH 3OCH 3OH+CH 3COOCH 3HCHO H+CH 2维尼纶合成纤维就是用聚乙烯醇甲酯2)、CH CH+HC NNH 4Cl,CuCl 2aqCH 2CNNN CH 3C H 3CH 3CH 3NCCN CH 2CN2CHCN人造羊毛3)、CH CH+C 2H 5OH碱150℃~180℃/压力CH 2CHOC 2H 54、聚合CH CH2Cu 2Cl 2NH 4Cl CH 2CH C CHC H CH3Cu 2Cl 2NH 4ClCH 2CH CHCH 2C H CH3金属羰基化合物C H CH3Ni(CN)25、端炔的鉴别CCHRCC -RAgC CH RC C -R CuCu(NH )+Ag(NH )+白色红色【注】干燥的炔银和炔铜受热或震动时易发生爆炸,实验完毕,应立即加浓硫酸把炔化物分解。
6、炔基负离子CC-RNa+1°烷基(2)H 2OR -L(L=X,OTs)R 1:(1)OR CR O(1)(2)H 2OC CR R 1CCRCH 2CH R 1OHCCRC R 1OHR 2C HCH NaNH C H C-Na+CH 3C H 3OH OCH COHCH 3CH 3H Pb/BaSO 4CH 3CH 2CH 3OHAl O CH 3C2CH 2三、芳烃1、苯的亲电取代反应 1)卤代+FeBr 3Br+BrHBr 22)硝化+NO 2+H 2OHN O 3浓H 2SO 4浓3)磺化+SO 3H+H 2OH 2SO( 7%SO 3 )SO 3HH +4)傅-克(Friedel-Crafts)反应 ①傅-克烷基化反应+RClAlCl 3RRCl+AlCl 3AlC l 4++R CH 2+RCH 2++HR++HR+++AlC l 4+R++HC lAlC l 3【注】碳正离子的重排,苯环上带有第二类定位基不能进行傅-克反应。
【例】+CH 3ClAlCl 3CH 3CH3+CH 3ClCH 3CH 3AlCl 3CH 3CH 3CH3CH 2Cl 2+2AlCl3CH 1Cl 3+3AlCl3②傅-克酰基化反应+RO Cl AlCl 3OR+OO O RRAlCl 3OR+RCOOH【例】CH 3CH 2COClAlCl 3CH 3OZn -HgHCl浓CH3+O OOAlCl 3COOHO2、苯环上取代反应的定位效应1)第一类定位基,邻对位定位基,常见的有:NR 2NH RNH 2OHHNC ROORCRO OR ArX(F,C l,Br,I)2)第二类定位基,间位定位基, 常见的有:NR 3NO 2CF 3Cl 3COOHCOROCNSO 3HCH OCOR【注】第一类定位基除卤素外,均使苯环活化。
第二类定位基使苯环钝化。
卤素比较特殊,为弱钝化的第一类定位基。
3、苯的侧链卤代CH3FehCH 3ClCH 3Cl+CH 2ClCH 3NBSCH 2Br【机理】自由基机理 4、苯的侧链氧化1)用高锰酸钾氧化时,产物为酸。
【描述】苯环不易被氧化,当其烷基侧链上有α氢的时候,则该链可被高锰酸钾等强氧化剂氧化,不论烷基侧链多长。
结果都是被氧化成苯甲酸。
CH KMnO H +COOH【例】C CH3CH 3CH 3CH 3KMnO H C CH 3CH 3CH 3COOH2)用CrO 3+Ac 2O 为氧化剂时,产物为醛。
【例】CH 3NO2CrO /Ac OCH(OAc)NO 2CHONO 23)用MnO 2为氧化剂时,产物为醛或酮。
CH 3MnO H 2SO 4CHOCH2CH 3MnO H 2SO 4CH 3O5、萘αβ【特点】萘的亲电取代反应,主要发生在α位,因为进攻α位,形成的共振杂化体较稳定,反应速度快。
【例】HNO 3H 2SO 4NO2Br 2CCl 4BrH 2SO 4SO 3HSO 3HCH 3HNO 3HOAcCH 3NO 2CH 3HNO 3HOAcCH 3NO 2NO 2HNO 3H 2SO 4NO 2NO 2NO 2NO 2+四、卤代烃1、取代反应 (1)水解R XOH -ROHR XRSH SH -(2)醇解R XROR 1R 1ONaR XRSR 1R 1SNa(3)氰解RR S R1CN -C 2H 5OH(4)氨解RX RNH 2NH 3RXNH 3R 3N(5)酸解R XR1COOR R 1COO -(6)与炔钠反应R X+R 1CC-C C RR 1(7)卤素交换反应RXNaI丙酮R I2、消除反应 (1)脱卤化氢 ①β-消除CH CH 2RClHαβNaOH乙醇RCHCH 2【注】当有多种β-H 时,其消除方向遵循萨伊切夫规律,即卤原子总是优先与含氢较少的β碳上的氢一起消除。
