乙酸性质
乙酸的物理性质

有强烈刺激性气味无色液体, 有强烈刺激性气味无色液体, 沸点117.9℃, 熔点 ℃ 熔点16.6℃; 沸点 ℃ 易溶于水、又叫冰醋酸
2、乙酸的分子结构 乙酸的分子式__________, 乙酸的分子式 C2H4O2 , 结构式
2CH3COO H+Na2CO3= 2CH3COONa H2O+CO2↑ 写出醋酸除水垢的化学方程式: 写出醋酸除水垢的化学方程式: 2CH3COO H+CaCO3= (CH3COO)2Ca H2O+CO2↑
(2)乙酸的酯化反应 ) 实验步骤: 实验步骤:药品及添加 的先后顺序:乙醇、浓硫酸、 ____________________________ 的先后顺序:乙醇、浓硫酸、乙酸 实验现象:____________________________ 实验现象:碳酸钠饱和溶液的上方有无色透明 的油状液体产生, 的油状液体产生,并可闻到香味 ________________________________________ 在有浓硫酸存在、加热的条件下, 在有浓硫酸存在、加热的条件下,乙醇与 结论: 结论:______________________________ 乙酸发生反应 ____________________________
CH3COO H+HOC2H5
浓硫酸 △
CH3COOC2H5+H2O
含酯的水果 -
如何测出乙酸与乙醇反应, 如何测出乙酸与乙醇反应,哪种物 质提供-H,哪种物质提供-OH? 质提供 ,哪种物质提供 ? 同位素原子示踪法
浓硫酸 △
CH3CO 18O H+HOC2H5
乙酸的存储方式

乙酸的存储方式乙酸(CH3COOH)是一种无色透明的有机酸。
它广泛应用于制药、食品、化妆品、农药、涂料等各个领域。
但由于其有毒、挥发性强等特点,乙酸的存储方式也尤为重要。
一、乙酸的性质和特点首先,我们需要了解乙酸的性质和特点。
乙酸是一种弱酸,pKa为4.76,易溶于水,挥发性强,有刺激性气味。
乙酸的蒸汽可以形成易燃性混合物,导致火灾和爆炸。
同时,乙酸还具有腐蚀性,其浓度越高,对金属、皮肤、黏膜等的腐蚀性也越强。
二、乙酸的包装方式根据乙酸的特点,我们应当选择正确的包装方法。
乙酸的包装材料应具备抗腐蚀、防漏、耐压、耐高温、耐低温等特点。
一般常用的包装材料有聚乙烯塑料瓶、玻璃瓶、铁桶、刚玉瓷瓶等。
其中,聚乙烯塑料瓶是常见的包装材料之一,因其价格低廉、重量轻、可靠性高,所以成为了绝大多数乙酸包装的选择。
三、乙酸的储存环境除了选择适当的包装材料之外,乙酸的储存环境也尤为重要。
乙酸应储存在阴凉、干燥、通风良好的仓库中,远离热源、点火源、易燃物、氧化剂等,避免与其它物质接触。
若有泄漏的情况,应立即采取相应应急措施,保证人员安全和储存环境不受损坏。
四、乙酸的储存时间乙酸的储存时间主要受环境因素和包装材料的影响。
在正确的储存环境下,乙酸的储存时间可以达到数年。
但若储存条件不当,则会导致乙酸被降解,从而出现气味异变、浑浊、析出沉淀等现象。
因此,建议在储存前检查包装材料、储存环境等因素,并定期检查。
五、乙酸的处理如果乙酸已经超过储存期限、密封不良、出现异味、变色等情况,则需要进行处理。
一般来说,将其小心、谨慎地倒入防爆容器中,然后交给专业的处理机构。
在处理前,我们也需要了解当地的相关法律法规和处理要求,以避免环境和人员的损害。
结语乙酸的正确存储方式,不仅可以保证其长期使用,而且还能预防事故的发生。
因此,我们应该对乙酸的性质、包装方式、储存环境等做到充分了解,并加强自身的安全意识,从而确保乙酸的合理利用。
乙酸用途性质

乙酸用途性质乙酸(又称醋酸)是一种常见的有机酸,化学式为CH3COOH。
它是无色液体,具有刺激性气味和酸味。
乙酸广泛用于各个领域,具有多种用途和性质。
首先,乙酸是一种重要的工业化学品。
它是许多有机化合物的原料和中间体。
乙酸可以通过发酵、化学合成、氧化醇等多种方法制备。
工业上最常用的生产乙酸的方法是通过由乙烯氧化得到乙醛,然后进一步氧化得到乙酸。
乙酸的一个主要用途是作为食品添加剂。
醋酸钠、醋酸钙等乙酸盐广泛用于食品工业中的酱料、调味品、罐头等产品中,以增加食品的酸味和延长保质期。
此外,乙酸还可以用作面包、饼干等烘焙食品发酵剂的原料。
乙酸还被广泛用于制药工业。
许多药品的合成过程中需要使用乙酸作为催化剂、溶剂或中间体。
例如,乙酸可以用于合成水杨酸、水合氯醛等药物原料。
此外,乙酸还可以用于制备麻醉药物如乙醚和氯仿等。
除了食品和药品工业,乙酸还在纺织工业中发挥重要作用。
乙酸可以用作丝绸和纤维染色的溶剂和媒染剂。
它可以改善染料在纤维上的分散性和渗透性。
此外,乙酸还可以用于纤维的酯化和脱酯等处理过程。
乙酸还是制备涂料、油漆和胶粘剂的重要成分之一。
乙酸树脂是一种优良的涂料基材,具有良好的耐候性、耐热性和耐化学腐蚀性。
乙酸也可以用作制备丙烯酸酯树脂和醛酸树脂等的原料。
此外,乙酸还有许多其他的用途。
它可以用作金属清洗剂,用于去除金属上的氧化物和污垢。
乙酸还可以用于制备酯、醚、酰胺等有机化合物。
乙酸的盐,如乙酸铜、乙酸铝等,具有抗菌、杀菌、防腐等作用,可以用于制备木材防腐剂、涂料添加剂等。
总之,乙酸广泛用于食品添加剂、制药工业、纺织工业、涂料工业等多个领域,并具有多种用途和性质。
随着科学技术的不断发展,乙酸的应用前景将更为广阔。
乙酸

中文名: 乙酸;冰醋酸英文名: Acetic acid glacial 别名: Glacial acetic acid分子结构:分子式: C2H4O2分子量: 60.05物理化学性质熔点:16-16.5ºC沸点:117-118ºC水溶性:MISCIBLE折射率:1.3715闪点:40ºC密度:1.048性质描述:无色透明液体。
熔点16.635℃沸点117.9℃,相对密度1.0492(20/4℃)折射率1.3716闪点(开杯)57℃自燃点465℃粘度11.83mPa·s(20℃)纯乙酸在16℃以下时,能结成冰状固体,故称冰醋酸。
与水、乙醇、苯和乙醚混溶,不溶于二硫化碳。
当水加到乙酸中,混合后的总体积变小,密度增加。
分子比为1:1,进一步稀释,不再发生上述体积的改变。
有刺激性气味。
安全信息安全说明:S23:不要吸入蒸汽。
S26:万一接触眼睛,立即使用大量清水冲洗并送医诊治。
S45:出现意外或者感到不适,立刻到医生那里寻求帮助(最好带去产品容器标签)。
危险品标志: C:腐蚀性物质危险类别码: R10:易燃。
R35:会导致严重灼伤。
危险品运输编号: UN2789其他信息产品应用:生产方法及其他形式存在;排泄物和血液中以游离酸的形式存在。
许多微生物可以将不同的有机物通过发酵转化为乙酸。
中国古代就有关于制醋的记载,早在公元前,人类已能用酒经各种乙酸菌氧化发酵制醋,19世纪后期,发现将木材干馏可以获得乙酸。
1911年,在德国建成了世界上第一套乙醛氧化生产乙酸的工业装置。
不久又研究发展了低碳烃氧化生产乙酸的方法。
1960年原联邦德国采用甲醇在高压(20MPa)下经羰基化制乙酸的方法。
随后,美国孟山都公司采用铑络合物催化剂(以碘化物作助催化剂),使甲醇羰基化制乙酸的压力降到0.3-3.0MPa,并于1970年建成生产能力135kt乙酸的甲醇低压羰基化工业装置。
由于该法技术经济先进,从70年代中期起新建的大厂多采用甲醇低压羰基化法。
乙酸的性质

2、乙酸性质
物理性质 颜色:无色 气味:刺激性气味 状态:液体 溶解性:易溶于水、乙醇 密度:几乎与水相等
乙酸 结构式: 结构简式:
化学式:
酸性
实验3-4
①酒精灯的使用 ②试管加热液体 ③饱和Na2CO3溶液
饱和Na2CO3溶液的作用
①降低乙酸乙酯的溶解度, 便于分层 ②除去挥发出来的乙酸 ③溶解挥发出来的乙醇
2CH3COOH + Na2CO3 = 2CH3COONa + H2O+ CO2↑
2CH3COOH +Na2O= 2CH3COONa +H2O
C2H4O2
H
H H
↑
+CO2
2CH3COOH +Na2O= 2CH3COONa +H2O
H O CH3 C O CH2CH3 + H2O O CH3 C OH
酯化反应
有人认为酯化反应属于取代 酯化反应属于取代反应 反应,你觉得对吗?
水解反应
完成下列酸与醇的酯化反应及酯水解反应 酸:甲酸、乙酸、丙酸
醇:甲醇、乙醇、丙醇
O CH3 CH3 O C CHCH3
+ H 2O
O
NaOH溶液
CH3 C OH+ ຫໍສະໝຸດ O CH2CH3CH3COOH
CH3COO- + H+
NaOH溶液
+ HO CH2CH3
新版高中化学讲义:乙酸

一、乙酸的物理性质颜色 气味 状态 熔点 沸点 溶解性 无色强烈刺激性气味液体16.6℃117.9℃易溶于水和乙醇乙酸又称醋酸,当温度低于16.6℃时,乙酸就凝结为类似于冰一样的晶体,所以纯净的乙酸又称冰醋酸。
二、乙酸的结构分子式 结构式 结构简式官能团【答案】C 2H 4O 2CH 3COOH羧基(或—COOH)三、乙酸的化学性质 1.弱酸性(1)电离方程式:CH 3COOHCH 3COO - + H +(2)酸的通性:①使紫色石蕊溶液变红;②与活泼金属(如Zn)、金属氧化物(如CuO)、碱(如NaOH)、 某些盐(如CaCO 3)反应。
(3)酸性强弱:HCl >CH 3COOH >H 2CO 3第21讲 乙酸知识导航知识精讲(4)应用:除水垢CaCO3 + 2CH3COOH === Ca(CH3COO)2 + CO2↑+ H2O 2.酯化反应实验装置实验步骤在一支试管中加入3 mL乙醇,然后边振荡试管边慢慢加入2 mL浓H2SO4和2 mL乙酸,再加入几片碎瓷片。
连接好装置,用酒精灯小心加热,将产生的蒸气经导管通到饱和Na2CO3溶液的液面上。
实验现象饱和Na2CO3溶液的液面上有无色透明的油状液体生成,且能闻到香味。
实验结论①乙酸与乙醇在浓H2SO4存在且加热的条件下,反应生成了不溶于水的物质。
②化学方程式:____________________________________________________【答案】CH3COOH + CH3CH2OH CH3COOCH2CH3 + H2O乙酸乙酯的物理性质:颜色气味状态密度溶解性无色透明有芳香气味油状液体比水小难溶于水,易溶于有机溶剂四、酯化反应的概念与原理1.定义:酸与醇反应生成酯和水的反应,叫酯化反应。
2.特点:酯化反应属于取代反应,也是可逆反应,乙酸乙酯会与水发生水解反应生成酸和醇。
3.原理:酸脱羟基,醇脱氢。
五、酯酯的官能团是酯基(,或写作—COOR),很多鲜花和水果的香味都来自酯。
【知识解析】羧酸的性质(以乙酸为例)
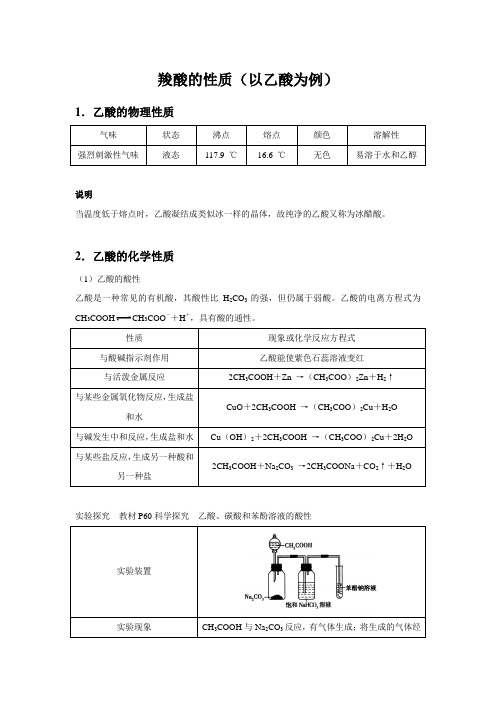
羧酸的性质(以乙酸为例)1.乙酸的物理性质说明当温度低于熔点时,乙酸凝结成类似冰一样的晶体,故纯净的乙酸又称为冰醋酸。
2.乙酸的化学性质(1)乙酸的酸性乙酸是一种常见的有机酸,其酸性比H2CO3的强,但仍属于弱酸。
乙酸的电离方程式为CH3COOH CH3COO-+H+,具有酸的通性。
实验探究教材P60科学探究乙酸、碳酸和苯酚溶液的酸性酸性:CH3COOH>H2CO3>(2)酯化反应用同位素示踪法探究酯化反应中的脱水方式。
用含有示踪原子的CH3CH218OH与CH3COOH反应,经测定,产物中含有示踪原子,说明酯化反应的脱水方式是“酸脱羟基醇脱氢”名师提醒(1)注意乙醇、乙酸和浓硫酸三种液体的混合顺序,不可先加浓硫酸。
(2)实验时应加碎瓷片并小火加热,防止暴沸及副反应的发生。
(3)导气管兼冷凝的作用,防止未反应的乙酸和乙醇挥发损失。
导管末端不可伸入液体中,防止出现倒吸。
(4)饱和碳酸钠溶液的作用是减少乙酸乙酯的溶解、中和挥发出的乙酸、溶解挥发出的乙醇。
酯化反应是醇和羧酸反应生成酯和水的一类反应,属于取代反应。
发生酯化反应时醇羟基中的氢原子与羧酸分子中的—OH结合生成水,其余部分连接成酯。
3.羧酸的化学性质羧酸的化学性质与乙酸相似,主要取决于羧基官能团。
发生化学反应时,羧酸分子中易断裂的化学键如图3-3-1所示。
图3-3-1①处:O—H键断裂时,易电离出H+,使羧酸表现出酸性;②处:C—O键断裂时,羧基中的一OH易被取代,如酯化反应;③处:C—H键断裂时,α-H易被取代,如RCH2COOH+Cl2RCHClCOOH+HCl。
典例详析例1(2019四川成都检测)巴豆酸的结构简式为CH3CH=CHCOOH。
现有①HCl ②溴的四氯化碳溶液③纯碱溶液④2-丁醇⑤酸性KMnO4溶液,根据巴豆酸的结构特点,判断在一定条件下能与巴豆酸反应的物质是A.②④⑤B.①③④C.①②③④D.①②③④⑤解析◆因为巴豆酸中含有,,所以巴豆酸可以与HCl、Br2发生加成反应,也可以被酸KMnO4溶液氧化;因为巴豆酸中含有—COOH,所以其可与2-丁醇发生酯化反应,也可与Na2CO3反应。
乙酸-生活中两种常见的有机物

-4-
一廿日
-5-
一、乙酸物理性质
色态: 无色液体 气味: 有强烈刺激性气味 沸点: 117.9℃ (易挥发) 熔点: 16.6℃ (无水乙酸又称为:冰醋酸) 溶解性: 和水任意比互溶,易溶于有机溶剂
-6-
二、乙酸的分子结构
分子式:C2H4O2
结构式:
HO
H CC O H
结构简式: CH3COOH
饱和一元羧酸:CnH2nO2(n≥1) 甲酸(蚁酸):HCOOH 乙二酸(草酸):HOOC-COOH 苯甲酸(安息香酸): COOH
-33-
六、酯类
酯是有芳香气味的液体,存 在于各种水果和花草中。如 梨里含有乙酸异戊酯,苹果 和香蕉里含有异戊酸异戊酯 等。酯的密度一般小于水, 并难溶于水,易溶于乙醇和 乙醚等有机溶剂。酯可用作 溶剂,也可用作制备饮料和
红葡萄酒密封储存时间越长,质量越好,原因是什么?
-14-
厨师烧鱼时常加醋并加点酒,这样鱼的味道 就变得香醇,特别鲜美。你知道其中的奥秘吗?
-15-
探究实验:乙酸的酯化反应
实验操作要点: (1)饱和碳酸钠溶液的体 积约为2手指高度,导管不 能插入液面(试管下面垫上 抹布) (2)乙酸乙酯层大约有1手 指层高时停止加热。 (3)闻产物的气味后充分 震荡试管再闻产物的气味
探究酯化反应的可能脱水方式
+ + CH3COOH
HOCH2CH3
浓硫
△
酸
CH3COOCH2CH3
H2O
+ + CH3COOH
HOCH2CH3
浓硫
△
酸
CH3COOCH2CH3
H2O
同位素示踪法
浓硫酸
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
课[提问]:我们已学过醇、醛等物
质的重要性质,请同学们找出它
们之间的相互关系。
【板书】:
CH3CH2OH CH3CHO
CH3COOH
[讲述]:乙醛的氧化产物乙酸是
一种重要的有机酸,在日常生活
中我们也经常用到它。
[展示]:食用醋样品,让学生闻
气味。
[讲述]:普通食醋中含有3%—5%
的乙酸,所以乙酸又叫醋酸。
这
节课就来研究乙酸的结构和性
质。
[板书]:乙酸的性质
思考,
写
式。
倾听。
观察。
[设问]:乙酸是强酸还是弱酸?[板书]:二、化学性质
酸性:
CH3COOH CH3COO-+H+
证明:在醋酸中加入鸡蛋壳有气泡冒出
H2CO3<CH3COOH
学质酯化反应:
浓硫酸的作用:催化剂、吸水
剂。
[设问]:乙酸与乙醇反应时可能
的脱水的方式有几种?
[板书]:可能的脱水方式:
倾听记忆
讨
见解。
[设问] 在发生化学反应时,乙酸的
主要断键方式有几种?学
总结。
