2020年高中物理竞赛辅导课件★★ 准静态过程 功 热量
合集下载
准静态过程 功 热量 内能 热力学第一定律 等体过程 等压过程 摩尔热容等温过程和绝热过程

V2 V
Qp
E2
E1
W
等压膨胀过程:气体吸收的热 量,一部分用于内能的增加, 一部分用于对外作功。
p
等 压
p
( p,V2 ,T2 )
2
( p,V1,T1)
1
压
W
缩
o V2
V1 V
Qp
E1
W
E2
等压压缩过程:外界对气体作 的功和内能的减少均转化为热 量放出。
等压过程中,W 与 △E始终同号
Q
m' M
解 1)等温过程
W12 '
RT ln V2 ' V1
2.80104 J
2)氢气为双原子气体
(i 2) i 1.40
T2
T1
(V1 V2
)
1
753K
p
p2
2 T2
p2' T2' T1
Q0
p1
2'
T1
T 常量 1
o V2 V2' V1 10 V1 V
怎么求?
由热力学第一定律
dQT dWT pdV
Q T
WT
p RT
V2 V1
pdV
V
p
p1
1 ( p1,V1,T )
p2
( p2 ,V2 ,T )
2
o V1 dV V2 V
恒
温
谁做功?
热
源
T
QT
WT
V2
V1
RT V
dV
RT
ln V2 V1
RT ln p1
2020高中物理竞赛辅导课件(基础热力学)6功 热量(共18张PPT)

(A)
例4.要使一热力学系统的内能增加,可以通 过____________或___________两种方式,或 者两种方式兼用来完成. 热力学系统的状态发生变化时,其内能的改变 量只决定于______,而与_______无关.
外界对系统作功 向系统传递热量 始末两个状态 所经历的过程
谢谢观看!
热量
热是物体中大量微粒机械运动的宏观表现
热量从温度高的物体传递到温度低的物体 或者从物体的高温部分传到低温部分 一定热量的产生(或消失)总是伴随着等 量的其他某种形式能量(如机械能、电能) 的消失(或产生)
热力学第一定律
绝热功与系统的内能 热量定义 热力学第一定律
绝热功与系统的内能
如果一个系统经过一个过程,其状态的变化完全是由 于机械的或电磁的作用,则称此过程为绝热过程。在 绝热过程中外界对系统所作的功为绝热功。
2020高中物理竞赛
基础热力学篇
功 热量
热力学过程 功 热量
热力学过程
当系统的状态随时间变化时,
我们就说系统在经历一个热力
学过程,简称过程。
理想气体自由膨胀
驰豫时间:系统平衡态破坏后需要经过一段 时间才能达到新的平衡态
非静态过程:在热力学过程中系统经历 的是一系列非平衡态
准静态过程:在热力学过程进行中的 每一时刻,系统都处于平衡态
气体自由膨胀过程
初态
真空
末 态
功
力学中
dW
F
ds
dW Pe Sdl dV Sdl
dW PedV
功的图示
在无摩擦准静态过程中 dW PdV
系统体积由V1变为V2,外界对系统作总功为
W V2 PdV
V1
系统对外界所作的功 W
例4.要使一热力学系统的内能增加,可以通 过____________或___________两种方式,或 者两种方式兼用来完成. 热力学系统的状态发生变化时,其内能的改变 量只决定于______,而与_______无关.
外界对系统作功 向系统传递热量 始末两个状态 所经历的过程
谢谢观看!
热量
热是物体中大量微粒机械运动的宏观表现
热量从温度高的物体传递到温度低的物体 或者从物体的高温部分传到低温部分 一定热量的产生(或消失)总是伴随着等 量的其他某种形式能量(如机械能、电能) 的消失(或产生)
热力学第一定律
绝热功与系统的内能 热量定义 热力学第一定律
绝热功与系统的内能
如果一个系统经过一个过程,其状态的变化完全是由 于机械的或电磁的作用,则称此过程为绝热过程。在 绝热过程中外界对系统所作的功为绝热功。
2020高中物理竞赛
基础热力学篇
功 热量
热力学过程 功 热量
热力学过程
当系统的状态随时间变化时,
我们就说系统在经历一个热力
学过程,简称过程。
理想气体自由膨胀
驰豫时间:系统平衡态破坏后需要经过一段 时间才能达到新的平衡态
非静态过程:在热力学过程中系统经历 的是一系列非平衡态
准静态过程:在热力学过程进行中的 每一时刻,系统都处于平衡态
气体自由膨胀过程
初态
真空
末 态
功
力学中
dW
F
ds
dW Pe Sdl dV Sdl
dW PedV
功的图示
在无摩擦准静态过程中 dW PdV
系统体积由V1变为V2,外界对系统作总功为
W V2 PdV
V1
系统对外界所作的功 W
2020年高中物理竞赛(力学篇)01运动的描述:描述质点运动的四个物理量(共12张PPT)

2020全国高中奥林匹克竞赛 物理
力学篇 (基础版)
P
一. 描述质点运动的四个物理量
1.位置矢量(单位:米)
位置矢量(位矢): r 运动方程: r r(t)
O
vΓ
r(t)
Δs
P 2
2.位移:
r r2 r1 r(t2) r(t1)
P 1
v
rv 1
Δrvr
Г
2
直角 坐标系中
r
r
xi
( x2
v1 Δv
v2
或位矢对时间的二阶导数
r、av
描述质点运动状态的物理量 描述质点运动状态变化的物理量
直角坐标系中
加速度
a
dv
dv x
i
dv y
j
dv z
k
dt dt dt
dt
axi ay j azk
加速度大小
a a
a
2 x
a
2 y
az
2
任意曲线运动都可以视为沿x,y,z轴的三个各自独 立的直线运动的叠加(矢量加法)。
速度大小
v v
vx2
v
2 y
vz2
平均速度
v
r
x
i
y
j
z
k
t t t t
vxi vy j vzk
v
v(t )
速率(单位:米/秒)
平均速率
v s t
瞬时速率 v lim s ds t0 t dt
P
r r Q
O r r
注意 速度是矢量,速率是标量。
一般情况 v v (s r)
单向直线运动情况
——运动的独立性原理或运动叠加原理
力学篇 (基础版)
P
一. 描述质点运动的四个物理量
1.位置矢量(单位:米)
位置矢量(位矢): r 运动方程: r r(t)
O
vΓ
r(t)
Δs
P 2
2.位移:
r r2 r1 r(t2) r(t1)
P 1
v
rv 1
Δrvr
Г
2
直角 坐标系中
r
r
xi
( x2
v1 Δv
v2
或位矢对时间的二阶导数
r、av
描述质点运动状态的物理量 描述质点运动状态变化的物理量
直角坐标系中
加速度
a
dv
dv x
i
dv y
j
dv z
k
dt dt dt
dt
axi ay j azk
加速度大小
a a
a
2 x
a
2 y
az
2
任意曲线运动都可以视为沿x,y,z轴的三个各自独 立的直线运动的叠加(矢量加法)。
速度大小
v v
vx2
v
2 y
vz2
平均速度
v
r
x
i
y
j
z
k
t t t t
vxi vy j vzk
v
v(t )
速率(单位:米/秒)
平均速率
v s t
瞬时速率 v lim s ds t0 t dt
P
r r Q
O r r
注意 速度是矢量,速率是标量。
一般情况 v v (s r)
单向直线运动情况
——运动的独立性原理或运动叠加原理
9.4准静态过程中功和热量的计算 课件-2020-2021学年高中物理竞赛
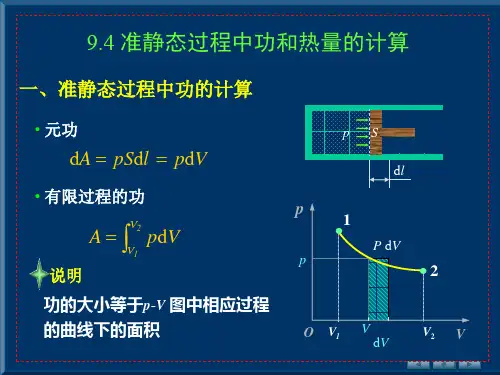
• 有限过程的功
A V2 pdV V1
说明 功的大小等于p-V 图中相应过程 的曲线下的面积
pS
dl
p
•1
P dV
p
•2
O V1
V dV
V2 V
二、 准静态过程中热量的计算
1. 热容 热容
物体温度升高1 K 所吸收的热量
比热容 单位质量的物体温度升高1 K 所吸收的热量
摩尔热容
1 mol 理想气体,经某一过程 x,吸热 Q,温度变化 T
违背第二定律开尔文表述
假设不成立
三、 热力学第二定律的实质,就是揭示了自然界的一 切自发过程都是单方向进行的不可逆过程。
9.11 卡诺定理
1. 在温度分别为T1 与T2 的两个给定热源之间工作的一切可 逆热机,其效率 相同,都等于可逆卡诺热机的效率,即
1 Q2 1 T2
Q1
T1
2. 在相同的高、低温热源之间工作的一切不可逆热机,其
Cx
lim
T 0
Q T
注意: 热容是过程量
2. 热量计算
mol 气体,经历某一个准静态过程 x,温度由 T1 变化 到 T2 ,吸热 Qx
Qx
T2 T1
CxdT
Cx —— 摩尔热容
若Cx与温度无关时(摩尔热容),则
Q Cx (T2 T2 )
9.3 功 热量 内能 热力学第一定律
热力学系统与外界传递能量的两种方式 做功 传热
94准静态过程中功和热量的计算一准静态过程中功的计算lpsaddvpddl?元功sp?21vvvpadovp1v2v??12dv?有限过程的功功的大小等于pv图中相应过程的曲线下的面积说明vppdv二准静态过程中热量的计算1
A V2 pdV V1
说明 功的大小等于p-V 图中相应过程 的曲线下的面积
pS
dl
p
•1
P dV
p
•2
O V1
V dV
V2 V
二、 准静态过程中热量的计算
1. 热容 热容
物体温度升高1 K 所吸收的热量
比热容 单位质量的物体温度升高1 K 所吸收的热量
摩尔热容
1 mol 理想气体,经某一过程 x,吸热 Q,温度变化 T
违背第二定律开尔文表述
假设不成立
三、 热力学第二定律的实质,就是揭示了自然界的一 切自发过程都是单方向进行的不可逆过程。
9.11 卡诺定理
1. 在温度分别为T1 与T2 的两个给定热源之间工作的一切可 逆热机,其效率 相同,都等于可逆卡诺热机的效率,即
1 Q2 1 T2
Q1
T1
2. 在相同的高、低温热源之间工作的一切不可逆热机,其
Cx
lim
T 0
Q T
注意: 热容是过程量
2. 热量计算
mol 气体,经历某一个准静态过程 x,温度由 T1 变化 到 T2 ,吸热 Qx
Qx
T2 T1
CxdT
Cx —— 摩尔热容
若Cx与温度无关时(摩尔热容),则
Q Cx (T2 T2 )
9.3 功 热量 内能 热力学第一定律
热力学系统与外界传递能量的两种方式 做功 传热
94准静态过程中功和热量的计算一准静态过程中功的计算lpsaddvpddl?元功sp?21vvvpadovp1v2v??12dv?有限过程的功功的大小等于pv图中相应过程的曲线下的面积说明vppdv二准静态过程中热量的计算1
高二物理竞赛功、热量 课件

无限小过程 系统无限小 做功值,它 不表示对 A 的全微分
功,热均为在过程中传递的能量,即过程量。 内能为状态函数。
5
对于理想气体,内能只与温度有关:
E i RT
2 对于准静态过程,。
注意:一个系统与外界的热传递不一定引起系统本身温 度的变化。 例1:等温过程(膨胀或压缩)
热库T
6
等温过程
1. 过程特征 系统温度保持不变,即 dT = 0,T = const.
(3) A —— 系统对外界做功,A 为正值,即A > 0; 外界对系统做功,A 为负值,即A < 0 (即系统对外做负功)。
4
对于任一无限小的过程(即初态与末态相距很近的过 程),热力学第一定律应写为:
dQ = dE + dA
无限小过程 的无限小热 量,它不表 示对Q 的全 微分
无限小过程 内能的增量
对于1mol物质,分别有摩尔定压热容Cp,m 和摩尔定体热容 CV,m 。 对于1kg物质,分别有定压比热 cp 和定体比热 cV 。
14
Cm
dQ m dT
1 dQ
dT
M
或:Cm = Mc
注意:由于dQ是一个过程量,故同一种理想气体在不同的
过程中,热容、比热容及摩尔热容是不同的。
13
定压热容:系统在压强保持不变的过程中的热容,记为
Cp。
Cp
dQ dT p
定体热容:系统在体积保持不变的过程中的热容,记为Cv。
CV
dQ dT V2来自系统经历一有限的准静态过程,体积由V1 变为 V2,则 系统对外界所做的总功为:
A dA V2 pdV V1
以气体膨胀做功为例,气体从初态( I )变化到末态(Ⅱ)用 上式求出的功的大小,根据定积分的意义可知,即为 p-V 状态图过程曲线下的面积。
2020年高中物理竞赛-热学A(联赛版)04热力学第一定律:应用(共12张PPT)

CV molT
RTVmol Vmol b
2a Vmol
H0
H p
T
H Vmol
T
Vmol p
T
2aVmol (Vmol b)2 RTbVm3ol 2a(Vmol b)2 RTVm3ol
从摩尔焓得:
H Vmol
T
2a(Vmol b)2 RTbVm2ol Vm2ol (Vmol b)2
3
RbT1 2a
1
与试验比较: 包科达书,p172
上转换温度:T1u 2a / Rb 下转换温度:T1d 2a / 9Rb
最大压强:p1 / T1 0 p10 a / 3b2 对应温度: T10 8a / 9Rb
Q
的热量称为该系统的热容 (C)。特殊标度下
C lim T 0 T
有:比热容 (c)、 摩尔热容 (Cmol)、等.
等体过程 V 0 Q (U pV )V (U )V
CV
lim (Q)V T 0 T
lim (U )V T 0 T
U T V
等压过程 Qp (U pV ) p [(U pV )] p 定义焓 (Enthalpy, 状态函数) H U pV (Q) p (H ) p
实验表明:常温常压下节流后,一般气体温度下降(T2 < T1), 氢、氦等气体温度上升(T2 > T1)。这种气体节流膨胀后温度发生 变化的现象称为节流效应,也称焦耳—汤姆逊效应,且T2 < T1 的 称为正效应, T2 > T1 的称为负效应。
定义: T1 T2 , 0 正效应(电冰箱),反之,负效应
2020高中物理竞赛
热学A
第二节 热力学第一定律的应用 (一)准静态过程
05准静态过程内能热量和功
2
Байду номын сангаас
准静态过程只有在进行的 “ 无限缓慢 ” 的条件 下才可能实现。 下才可能实现。实际过程则要求系统状态发生变化的 特征时间远远大于弛豫时间τ才可近似看作准静态过 特征时间远远大于弛豫时间 才可近似看作准静态过 程。 对于一个平衡态,我们可以用状态参量来描述。 对于一个平衡态,我们可以用状态参量来描述。 作为准静态过程中间状 P A 态的平衡态, 态的平衡态 , 具有确定的状 态参量值。 态参量值。 对 于 简 单 系 统 可 用 P—V 图 V 过程曲线 上的一点来表示这个平衡态。 上的一点来表示这个平衡态 。 B 系统的准静态变化过程可用P 系统的准静态变化过程可用 P— o 图上的一条曲线表示。 V图上的一条曲线表示。 V 非准静态过程不能用状态图上的一条曲线来表示。 非准静态过程不能用状态图上的一条曲线来表示。 准静态过程是一种理想的极限, 准静态过程是一种理想的极限,但作为热力学 的基础,我们要着重讨论它。 的基础,我们要着重讨论它。 3
5
2.气体作功的计算 . 只考虑无摩擦准静态过程的功。 只考虑无摩擦准静态过程的功。 b b 由功的定义: 由功的定义: = A dA = Fdr cosθ
P
dV S
∫
压力 F = PS 元功
a
∫
a
dx
dA = Fdx = PSdx= PdV dA = PdV 体积变化从 V1—V2,在整个 P 1
因热量与过程有关,故同一系统, 因热量与过程有关,故同一系统,在不同过程中 的热容量有不同的值。常用的定容热量与定压热容量。 的热容量有不同的值。常用的定容热量与定压热容量。 等容过程:引入等容摩尔热容 V,表示在等容过程中, 等容过程:引入等容摩尔热容C 表示在等容过程中 表示在等容过程中, 等容过程 容摩尔热容 1 mol 气体升高单位温度所吸收的热量。 气体升高单位温度所吸收的热量。
Байду номын сангаас
准静态过程只有在进行的 “ 无限缓慢 ” 的条件 下才可能实现。 下才可能实现。实际过程则要求系统状态发生变化的 特征时间远远大于弛豫时间τ才可近似看作准静态过 特征时间远远大于弛豫时间 才可近似看作准静态过 程。 对于一个平衡态,我们可以用状态参量来描述。 对于一个平衡态,我们可以用状态参量来描述。 作为准静态过程中间状 P A 态的平衡态, 态的平衡态 , 具有确定的状 态参量值。 态参量值。 对 于 简 单 系 统 可 用 P—V 图 V 过程曲线 上的一点来表示这个平衡态。 上的一点来表示这个平衡态 。 B 系统的准静态变化过程可用P 系统的准静态变化过程可用 P— o 图上的一条曲线表示。 V图上的一条曲线表示。 V 非准静态过程不能用状态图上的一条曲线来表示。 非准静态过程不能用状态图上的一条曲线来表示。 准静态过程是一种理想的极限, 准静态过程是一种理想的极限,但作为热力学 的基础,我们要着重讨论它。 的基础,我们要着重讨论它。 3
5
2.气体作功的计算 . 只考虑无摩擦准静态过程的功。 只考虑无摩擦准静态过程的功。 b b 由功的定义: 由功的定义: = A dA = Fdr cosθ
P
dV S
∫
压力 F = PS 元功
a
∫
a
dx
dA = Fdx = PSdx= PdV dA = PdV 体积变化从 V1—V2,在整个 P 1
因热量与过程有关,故同一系统, 因热量与过程有关,故同一系统,在不同过程中 的热容量有不同的值。常用的定容热量与定压热容量。 的热容量有不同的值。常用的定容热量与定压热容量。 等容过程:引入等容摩尔热容 V,表示在等容过程中, 等容过程:引入等容摩尔热容C 表示在等容过程中 表示在等容过程中, 等容过程 容摩尔热容 1 mol 气体升高单位温度所吸收的热量。 气体升高单位温度所吸收的热量。
10-1 准静态过程 功 内能和热量
总热量:
Q Q
10-1 准静态过程 功 内能和热量
10.2
热力学第一定律
第10章 热力学定律
10.2.1 热力学第一定律 某一过程,系统从外界吸热 Q,对外 界做功 A,系统内能从初始态 E1变为 E2,则由能量守恒:
A ΔE Q
内能是状态量, A、 Q是过程量
对微元过程:
Q dE A
热一律的另一种表述: 第一类永动机制不成 对准静态过程: Q E2 E1
V2
V1
pdV
10.2.2 热容
C
Q
dT
单位:J/mol· K
• 摩尔热容量 C ,
• 比热容 c , 单位:J/kg· K
Q 为过程量
C为过程量
经常用到1摩尔物质在等体过程以及在等压过程中的热 容量,称为摩尔定体热容和摩尔定压热容,分别定义 为:
CV ,m
i R 2
C P ,m
i2 R 2
2i i
i=3
单原子气体:
双原子气体: 多原子气体:
1.67
i=5
i=6
1.40
1.33
用 C
V ,m
CP,mγ值和实验比较,常温下符合很好
t 200 C
CV ,m R 2
P 1.01105 pa
CP ,m R 2
P
A
(PB,VB,TB)
V2
V1
pdV
O
VA
dV
VB
V
说明 δA>0:系统对外做功 系统所作的功在数值上 等于P-V 图上过程曲线 以下的面积。
作功与过程有关 。
p 下,气体准静态地由体积 V1 例 计算在等压 的过程系统对外界所做的功。
高中物理竞赛课件 第七章 热力学基础 (共67张PPT)
E i RT dE i RdT
2
2
CP
dQP dT
dQP
dE
PdV
i 2
RdT
RdT
PV RT d(PV) PdV VdP PdV RdT
14
单原子:i 3 双原子:i 5 多原子:i 6 二、三种等值过程
5
3
7
5
8
6
1.等容过程 特征:dV 0 dA 0
p
过程方程:
(1)状态d的体积Vd; (2)整个过程对外所做的功;
(3)整个过程吸收的热量.
p
2p1
c
解: (1)由绝热过程方程:
TcVc 1 TdVd 1
p1
ab
d
1
得:Vd
Tc Td
1
Vc
根据题意:
Td
Ta
p1V1 R
o v1 2v1
v
Vc 2V1
Tc
pcVc R
4 p1V1 R
4Ta
5
3
27
(2)整个过程对外所做的功;
真空
T
T0
2V0
∵绝热过程
(E E0) A 0
而 A=0
V0 1T0 (2V0) 1T T P0V0 P(2V0) P
E E0 (T T0)
始末两态满足 P0V0 P(2V0)
状态方程
T0
T
P
1 2
P0
26
例7-4 1mol单原子理想气体,由状态a(p1,V1)先等压加热至体积增大1倍,再等体加热至压 力增大1倍,最后再经绝热膨胀,使其温度降至初始温度,如图所示,试求:
i 2 1
1
i
物理课件4.14.2准静态过程功热量
当外界对系统所做的功为正时 ,系统能量增加;当外界对系 统所做的功为负时,系统能量 减少。
03 准静态过程热量的计算
CHAPTER
热量的定义
热量
在热传递过程中,系统之 间由于温差而发生的能量 转移的量度。
单位
在国际单位制中,热量的 单位是焦耳(J)。
热量与温度的关系
热量与温度变化量成正比 ,即 ΔQ = m × c × ΔT, 其中 m 是质量,c 是比热 容,ΔT 是温度变化量。
当 θ = 90° 时,cosθ = 0,表示力不 做功,即 W = 0。
当 θ > 90° 时,cosθ < 0,表示力做 负功,即 W < 0。
准静态过程功的物理意义
准静态过程功的物理意义是表 示系统能量的转化或转移。
在准静态过程中,系统能量的 变化量等于外界对系统所做的 功,是 描述力的空间效果的一个物理量 。
02
它等于力与物体在力的方向上通 过的位移的乘积。
准静态过程功的计算公式
准静态过程功的计算公式为:W = Fs cosθ,其中 F 是力,s 是位移,θ 是力与位移之间的夹角。
当 θ < 90° 时,cosθ > 0,表示力 做正功,即 W > 0。
准静态过程与动态过程的比较
动态过程能量耗散大,系统状态 随时间变化显著;准静态过程能 量耗散小,系统状态随时间变化
缓慢。
动态过程需要更多的外部能量输 入来维持系统状态的改变;准静
态过程则不需要。
在热力学计算中,准静态过程的 热力学性质更容易计算和处理。
02 准静态过程功的计算
CHAPTER
功的定义
准静态过程热量的计算公式
准静态过程
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
5
2020年高中物理竞赛辅导课件★★
一 准静态过程(理想化的过程)
从一个平衡态到另一平衡态所经过的每 一中间状态均可近似当作平衡态的过程 .
砂子 活塞 气体
p
p1 1 ( p1,V1,T1)
p2
2 ( p2 ,V2 ,T2 )
o V1 V2 V
1
二 功(过程量)
1 功是能量传递和转换的量度,它引 起系统热运动状态的变化.
T1 Q T2
4
物理学
第五版
13-1 准静态过程 功 热量
功与热量的异同
(1)都是过程量:与过程有关;
(2)等效性:改变系统热运动状态作用相同;
1 cal = 4.18 J , 1 J = 0.24 cal
(3)功与热量的物理本质不同 .
宏观运动
功 分子热运动
热量
分子热运动
分子热运动
第十三章 热力学基础
宏观运动能量
热运动能量
2
物理学
第五版
13-1 准静态过程 功 量
2 准静态过程功的计算
dW Fdl pSdl
dW pdV
W V2 pdV V1
注意: 作功与过程有关 .
第十三章 热力学基础
3
三 热 量(过程量)
通过传热方式传递能量的量度,系统 和外界之间存在温差而发生的能量传递 .
T1 T2
