2017版高考化学一轮复习:章末冲关评价练12
2017版高考化学人教版(全国)一轮复习:真题专训第十二章 专题课时6有机合成与推断

专题课时6有机合成与推断1.(2015·广东理综,30)有机锌试剂(R-ZnBr)与酰氯()偶联可用于制备药物Ⅱ:(1)化合物Ⅰ的分子式为________________.(2)有关化合物Ⅱ,下列说法正确的是________(双选)。
A.可以发生水解反应B.可与新制Cu(OH)2共热生成红色沉淀C.可与FeCl3溶液反应显紫色D.可与热的浓硝酸和浓硫酸混合液反应(3)化合物Ⅲ含3个碳原子,且可发生加聚反应。
按照途径1合成路线的表示方式,完成途经2中由Ⅲ到Ⅴ的合成路线:_________________________________(标明反应试剂,忽略反应条件)。
(4)化合物Ⅴ的核磁共振氢谱中峰的组数为________,以H替代化合物Ⅵ中的ZnBr,所得化合物的羧酸类同分异构体共有________种(不考虑手性异构)。
(5)化合物Ⅵ和Ⅶ反应可直接得到Ⅱ,则化合物Ⅶ的结构简式为________________.解析(1)根据化合物Ⅰ的结构简式即可得出其分子式为C12H9Br。
(2)结合流程图中化合物Ⅱ的结构简式可知,化合物Ⅱ的分子中含有酯基,能发生水解反应,A项正确;化合物Ⅱ的分子中不含醛基,不能与新制的Cu(OH)2共热生成红色沉淀,B项错误;化合物Ⅱ的分子中不含有酚羟基,与FeCl3溶液反应不显紫色,C项错误;化合物Ⅱ的分子中含有苯环,可与热的浓硝酸和浓硫酸混合液发生苯环上的取代反应,D项正确。
(3)化合物Ⅲ含有3个碳原子且可发生加聚反应,说明化合物Ⅲ含有碳碳双键,结合化合物Ⅵ的结构简式及化合物V 生成化合物Ⅵ的反应条件可知,化合物V为BrCH2CH2COOCH2CH3,故化合物Ⅲ为含3个碳原子且含有碳碳双键的CH2===CHCOOH,化合物Ⅳ为BrCH2CH2COOH,故由化合物Ⅲ合成化合物Ⅴ的合成路线为CH2===CHCOOH 错误!BrCH2CH2COOH错误!BrCH2CH2COOCH2CH3;(4)根据化合物V的结构简式和对称性,可知其分子中等效氢原子有4种,故核磁共振氢谱中峰的组数为4;以H替代化合物Ⅵ中的ZnBr,所得化合物为CH3CH2COOCH2CH3,其中属于羧酸类同分异构体为C4H9-COOH,丁基有4种同分异构体,故C4H9-COOH共有4种羧酸类同分异构体。
《世纪金榜》2017版高考化学一轮总复习2012年高考分类题库人教大纲版考点1氧化还原反应

此题库为Word版,请按住Ctrl,滑动鼠标滚轴,调节合适的观看比例,点击右上角的关闭按钮可返回目录。
考点1 氧化还原反应一、选择题1.(2012·四川高考·13)向27.2 g Cu和Cu2O的混合物中加入某浓度的稀硝酸0.5 L,固体物质完全反应,生成NO和Cu(NO3)2。
在所得溶液中加入1.0 mol·L-1的NaOH溶液1.0 L,此时溶液呈中性,金属离子已完全沉淀,沉淀质量为39.2 g。
下列有关说法不正确的是( )A.Cu与Cu2O的物质的量之比为2∶1B.硝酸的物质的量浓度为2.6 mol·L-1C.产生的NO在标准状况下的体积为4.48 LD.Cu、Cu2O与硝酸反应后剩余HNO3为0.2 mol【解题指南】解答本题时可以按照以下流程【解析】选B。
根据题意得到的金属离子的沉淀为氢氧化铜0.4 mol,根据元素守恒可以确定原混合物中有铜0.2 mol,有氧化亚铜0.1 mol,将溶液变成中性时消耗氢氧化钠1 mol,沉淀铜离子只消耗了0.8 mol,因此反应过程中硝酸过量0.2 mol,由于固体混合物与硝酸的反应为氧化还原反应,该反应过程中铜元素的化合价均升高为+2价,化合价升高了0.4+0.2=0.6(mol),硝酸中氮原子的化合价由+5价降低为+2价,因此生成的一氧化氮的物质的量为0.2 mol,根据氮元素守恒可以判断原溶液中硝酸的物质的量为1.2 mol,浓度为2.4 mol·L-1。
2.(2012·上海高考·11) 工业上将氨气和空气的混合气体通过铂-铑合金网发生氨氧化反应,若有标准状况下V L氨气完全反应。
并转移n个电子,则阿伏加德罗常数(N A)可表示为( )【解题指南】解答本题时应该注意以下几点:(1)氨的催化氧化的方程式为:4NH3+5O24NO+6H2O(2)反应为氧化还原反应,得失电子守恒。
2017版高考化学一轮复习 真题专训 第十二章 有机化学基础 基础课时2 烃和卤代烃 新人教版

基础课时2 烃和卤代烃1.(2015·北京,10)合成导电高分子材料PPV的反应:下列说法正确的是( )A.合成PPV的反应为加聚反应B.PPV与聚苯乙烯具有相同的重复结构单元C. 和苯乙烯互为同系物D.通过质谱法测定PPV的平均相对分子质量,可得其聚合度解析合成PPV的反应是缩聚反应,A项错误;聚苯乙烯可表示为,B 项错误;两种有机物中含的碳碳双键的数目不同,因此不是同系物,C项错误;通过质谱法可测定PPV的平均相对分子质量,又知道单体的相对分子质量,因此可得该高分子的聚合度,D项正确。
答案D,2.(2015·上海化学,10)卤代烃的制备有多种方法,下列卤代烃不适合由相应的烃经卤代反应制得的是( )解析可由环己烷发生取代反应产生。
可由2,2-二甲基丙烷发生取代反应产生,可由与HCl发生取代反应产生,而不适合用与Cl2发生取代反应产生,C正确。
可由2,2,3,3-四甲基丁烷发生取代反应产生。
答案 C3.(2015·重庆化学,10)某“化学鸡尾酒”通过模拟臭虫散发的聚集信息素可高效诱捕臭虫,其中一种组分T可通过下列反应路线合成(部分反应条件略)。
(1)A的化学名称是________,A→B新生成的官能团是________。
(2)D的核磁共振氢谱显示峰的组数为________。
(3)D→E的化学方程式为__________________________________________。
(4)G与新制的Cu(OH)2发生反应,所得有机物的结构简式为________。
(5)L可由B与H2发生加成反应而得,已知R1CH2Br+NaC≡CR2―→R1CH2C≡CR2+NaBr,则M的结构简式为________。
(6)已知R 3C≡C R 4――-----------→Na ,液NH 3,则T 的结构简式为________。
解析 (1)根据A 的结构简式可知化学名称是丙烯,A→B 新生成的官能团是溴原子。
新新2017版高考化学一轮复习 章末冲关评价练4 第4章 非金属及其化合物

非金属及其化合物(时间:45分钟分值:100分)一、选择题(每小题5分,共50分)1.(2016·四川绵阳模拟)在氯化钡溶液中通入SO2,溶液澄清,若将溶液分装于两支试管中,第一支加入氯水,另一支加入烧碱溶液,下列有关叙述不正确的是( ) A.两支试管中生成相同的白色沉淀B.第一支试管的白色沉淀为硫酸钡C.本次实验表明SO2具有还原性D.SO2通入氯化钡溶液中没有发生反应,表明弱酸不能制取强酸【解析】SO2被氯水氧化生成硫酸根离子,硫酸根离子与钡离子反应生成硫酸钡沉淀;SO2与烧碱溶液反应生成亚硫酸根离子,亚硫酸根离子与钡离子反应生成亚硫酸钡沉淀,A 项错误。
【答案】 A2.化学与生活、社会密切相关。
下列说法正确的是( )A.光纤通信使用的光缆的主要成分是晶体Si,太阳能电池使用的材料主要是SiO2B.氨很容易液化,液氨汽化吸收大量的热,所以液氨常用作制冷剂C.高锰酸钾溶液、酒精、双氧水都能杀菌消毒,消毒原理相同,都利用了强氧化性D.SO2可以用来漂白纸浆、毛、丝、草帽辫,增白食品等【解析】光纤通信使用的光缆的主要成分是SiO2,太阳能电池使用的材料主要是Si,A错误;酒精能杀菌消毒是利用其使蛋白质变性,C错误;SO2不能用来增白食品,D错误。
【答案】 B3.下列现象或事实不能用同一原理解释的是( )A.浓硝酸和氯水用棕色细口试剂瓶保存B.硫化钠和亚硫酸钠固体长期暴露在空气中变质C.Cl2和SO2都能使品红溶液褪色D.SO2和FeSO4溶液都能使KMnO4溶液褪色【解析】浓硝酸和氯水用棕色细口试剂瓶保存都是为了防止光照时发生分解反应,A 原理相同;硫化钠和亚硫酸钠固体长期暴露在空气中,都会被氧化而变质,B原理相同;Cl2能使品红溶液褪色是因为HClO具有强氧化性,SO2能使品红溶液褪色是因为SO2具有漂白性,C不能用同一原理解释;SO2和FeSO4都有还原性,能将KMnO4还原而使KMnO4溶液褪色,D原理相同。
【步步高】(全国)2017版高考化学一轮复习 第12章 物质结构与性质(选考)单元综合检测卷 新人教版

第十二章物质结构与性质(选考)考生注意:1.本试卷共4页。
2.答卷前,考生务必用蓝、黑色字迹的钢笔或圆珠笔将自己的姓名、班级、学号填写在相应位置上。
3.本次考试时间100分钟,满分100分。
1.(10分)(2015·西安市西工大附中高考一模)MnO2是碱锰电池材料中最普通的正极材料之一,在活性材料MnO2中加入CoTiO3纳米粉体,可以提高其利用率,优化碱锰电池的性能。
(1)写出基态Mn原子的核外电子排布式________________________。
(2)CoTiO3晶体结构模型如图1,在CoTiO3晶体中1个Ti原子、1个Co原子周围距离最近的O原子数目分别为________个、________个。
(3)二氧化钛(TiO2)是常用的、具有较高催化活性和稳定性的光催化剂,常用于污水处理。
O2在其催化作用下,可将CN-氧化成CNO-,进而得到N2。
与CNO-互为等电子体的分子、离子化学式分别为________、________(各写一种)。
(4)三聚氰胺是一种含氮化合物,其结构简式如图2,三聚氰胺分子中氮原子轨道杂化类型是______;1 mol三聚氰胺分子中σ键的数目为________。
三聚氰胺的相对分子质量与硝基苯的相近,但三聚氰胺的熔点比硝基苯的高,其原因是________________________________________________________________________。
2.(12分)(2015·银川市宁大附中高三期末)(1)中国古代四大发明之一——黑火药,它的爆炸反应为2KNO3+3C+S===A+N2↑+3CO2↑(已配平)。
①除S外,其余元素的电负性从大到小依次为______________________。
②在生成物中,A的晶体类型为________;含极性共价键的分子中中心原子的杂化轨道类型为________________。
高考复习方案(全国卷)2017版高考化学一轮复习 测评手册(无答案)新人教版
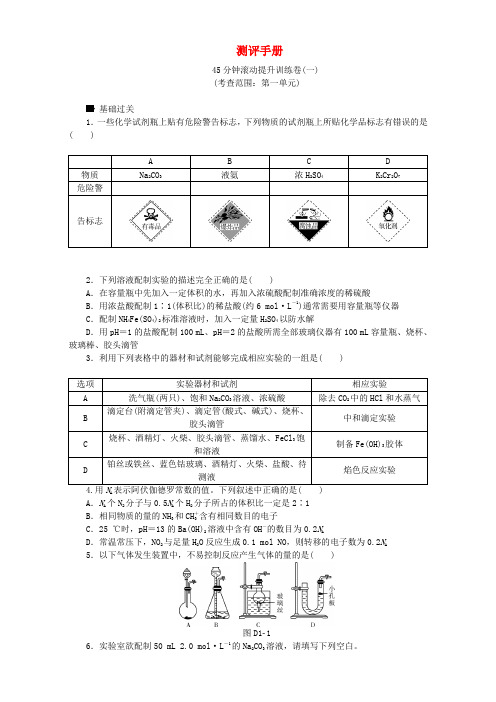
测评手册45分钟滚动提升训练卷(一)(考查范围:第一单元)基础过关1.一些化学试剂瓶上贴有危险警告标志,下列物质的试剂瓶上所贴化学品标志有错误的是( )2.下列溶液配制实验的描述完全正确的是( )A.在容量瓶中先加入一定体积的水,再加入浓硫酸配制准确浓度的稀硫酸B.用浓盐酸配制1∶1(体积比)的稀盐酸(约6 mol·L-1)通常需要用容量瓶等仪器C.配制NH4Fe(SO4)2标准溶液时,加入一定量H2SO4以防水解D.用pH=1的盐酸配制100 mL、pH=2的盐酸所需全部玻璃仪器有100 mL容量瓶、烧杯、玻璃棒、胶头滴管3.利用下列表格中的器材和试剂能够完成相应实验的一组是( )4.用A表示阿伏伽德罗常数的值。
下列叙述中正确的是( )A.N A个N2分子与0.5N A个H2分子所占的体积比一定是2∶1B.相同物质的量的NH3和CH+3含有相同数目的电子C.25 ℃时,pH=13的Ba(OH)2溶液中含有OH-的数目为0.2N AD.常温常压下,NO2与足量H2O反应生成0.1 mol NO,则转移的电子数为0.2N A5.以下气体发生装置中,不易控制反应产生气体的量的是( )图D116.实验室欲配制50 mL 2.0 mol·L-1的Na2CO3溶液,请填写下列空白。
(1)若用无水碳酸钠配制,则需Na2CO3的质量是________,称取Na2CO3固体常用的仪器是________。
(2)若用碳酸钠晶体(Na2CO3·10H2O)配制,则需晶体的质量是________。
(3)若用5 mol·L-1的Na2CO3溶液配制,则需该Na2CO3溶液的体积是______mL,量取该Na2CO3溶液常用的仪器是______。
定容时俯视刻度线读数,所得溶液浓度________(填“偏高”“偏低”或“不变”)。
(4)从上述配制的溶液中取出10 mL,其中Na2CO3的物质的量浓度是______________,含有Na2CO3的质量是________。
2017化学鲁科版一轮天天练:第12周 课时作业·周周清含解析
周六排查训练(本栏目内容,在学生用书中以独立形式分册装订!)[高考题重组]判断正误(正确的打“√”,错误的打“×”)1.(1)稀醋酸中加入少量醋酸钠能增大醋酸的电离程度(2015·重庆理综,3A)()(2)25 ℃时,等体积等浓度的硝酸与氨水混合后,溶液pH=7(2015·重庆理综,3B)()(3)25 ℃时,0.1 mol·L-1的硫化氢溶液比等浓度的硫化钠溶液的导电能力弱(2015·重庆理综,3C)()(4)25 ℃时,用醋酸溶液滴定等浓度NaOH溶液至pH=7,V醋酸<V NaOH(2013·重庆理综,2B)()(5)稀醋酸加水稀释,醋酸的电离程度增大,溶液的pH减小(2012·重庆理综,10B)()(6)中和等体积、等物质的量浓度的盐酸和醋酸所消耗的n(NaOH)相等(2012·福建理综,10C)()(7)CH3COOH溶液加水稀释后,溶液中c(CH3COOH)c(CH3COO-)的值减小(2013·江苏化学,11C)()(8)室温下,对于0.1 mol·L-1的氨水,加水稀释后,溶液中c(NH+4)·c(OH-)变大(2013·福建理综,8B)()答案:(1)×(2)×(3)√(4)×(5)×(6)√(7)√(8)×2.(1)酸式滴定管装标准溶液前,必须先用该溶液润洗(2014·新课标全国卷Ⅰ,12B)()(2)酸碱滴定实验中,用待滴定溶液润洗锥形瓶以减小实验误差(2014·新课标全国卷Ⅰ,12C)()(3)测定NaOH溶液浓度,可用滴定管、锥形瓶、烧杯、NaOH溶液、0.100 0 mol·L-1盐酸达到目的(2014·安徽理综,9D)()(4)用蒸馏水润湿的试纸测溶液的pH,一定会使结果偏低(2014·大纲全国卷,6D)()(5)(2014·山东理综,10B)()(6)50 ℃时,pH=4的醋酸中,c(H+)=4.0 mol·L-1(2013·广东理综,12A)()(7)50 ℃时,pH=12的纯碱溶液中,c(OH-)=1.0×10-2mol·L-1(2013·广东理综,12C)()(8)在蒸馏水中滴加浓硫酸,K W不变(2013·天津理综,5A)()(9)NaCl溶液和CH3COONH4溶液均显中性,两溶液中水的电离程度相同(2013·天津理综,5D)()(10)25 ℃与60 ℃时,水的pH相等(2012·福建理综,10B)()(11)用0.200 0 mol·L-1NaOH标准溶液滴定HCl与CH3COOH的混合液(混合液中两种酸的浓度均约为0.1 mol·L-1),至中性时,溶液中的酸未被完全中和(2012·浙江理综,12C)()答案:(1)√(2)×(3)×(4)×(5)×(6)×(7)×(8)×(9)×(10)×(11)√[高考题汇编]3.(2014·山东理综,13)已知某温度下CH3COOH和NH3·H2O的电离常数相等,现向10 mL浓度为0.1 mol/L的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中()A.水的电离程度始终增大B.c(NH+4)/c(NH3·H2O)先增大再减小C.c(CH3COOH)与c(CH3COO-)之和始终保持不变D.当加入氨水的体积为10 mL时,c(NH+4)=c(CH3COO-)解析:A项,CH3COOH溶液中滴加氨水,水的电离程度先增大等恰好完全反应后水的电离程度再减小;B项,c(NH+4)/c(NH3·H2O)=K b/c(H+),K b不变,H+浓度不断减小,c(NH+4)/c(NH3·H2O)值始终增大,B错;C中随着氨水不断滴加,c(CH3COOH)与c(CH3COO -)之和变小;D中当加入氨水的体积为10 mL时,CH3COOH和NH3·H2O恰好完全反应,电离常数相等,所以醋酸铵呈中性,c(NH+4)=c(CH3COO-)。
新新高考化学一轮复习 章末冲关评价练12 有机化学基础
有机化学基础(时间:45分钟分值:100分)一、选择题(每小题6分,共30分)1.咖啡酸具有止血功效,存在于多种中药中,其结构简式如图。
则下列有关说法正确的是( )A.该物质苯环上一氯代物有2种B.1 mol该物质可以与1.5 mol碳酸钠溶液反应生成1.5 mol CO2C.既能发生取代反应,也能发生加成反应D.所有碳原子不可能都在同一个平面上【解析】A项,该物质苯环上的一氯代物有3种,错误;B项,该有机物中酚羟基、—COOH均能与Na2CO3反应,但只有—COOH能生成CO2,错误;D项,苯环及其所连的12个原子共平面,碳碳双键及所连的原子共平面,通过碳碳单键的旋转两平面可能重合,故所有碳原子可能共平面,错误。
【答案】 C2.(2016·杭州模拟)儿茶素(其结构简式如图所示)是茶叶的主要活性成分,具有抗氧化、抗菌、除臭等作用。
R′=H或OH)下列说法正确的是( )A.常温下,儿茶素不溶于水,也不溶于有机溶剂B.儿茶素能与FeCl3溶液发生显色反应C.1 mol儿茶素最多可与4 mol NaOH反应D.儿茶素一定不能发生水解反应【解析】A项,该物质在常温下不易溶于水,但能溶于有机物溶剂,错误;B项,儿茶素分子中含有酚羟基,能与FeCl3溶液发生显色反应,正确;C项,该分子中最多含有8个酚羟基和1个酯基,均可与NaOH溶液反应,所以1 mol 儿茶素最多可与9 mol NaOH反应,错误;D项,若R是则该分子中存在酯基,可以发生水解反应,错误。
【答案】 B3.(2016·武汉调研)某饱和一元酯C5H10O2在酸性条件下水解生成甲和乙两种有机物,乙在铜的催化作用下能被氧化为醛,满足以上条件的酯有( )A.6种B.7种C.8种D.9种【解析】乙在铜的催化作用下能被氧化成醛,说明乙为醇,且其所含的羟基在端位碳原子上,满足该条件的醇有甲醇、乙醇、1丙醇、1丁醇、2甲基1丙醇,甲醇对应生成的酯有2种,为正丁酸甲酯和异丁酸甲酯,其他醇对应生成的酯均只有1种,故满足条件的酯共有6种。
2017版高考化学一轮复习:章末冲关评价练7
章末冲关评价练(七)(时间:45分钟分值:100分)一、选择题(每小题5分,共40分)1.100 ℃时,将0.1 mol N2O4置于1 L密闭的烧瓶中,然后将烧瓶放入100 ℃的恒温槽中,烧瓶内的气体逐渐变为红棕色:N2O4(g) 2NO2(g)。
下列选项不能说明上述反应在该条件下已经达到平衡状态的是()A.烧瓶内气体的密度不再变化B.烧瓶内气体的颜色不再变化C.烧瓶内气体的压强不再变化D.烧瓶内气体的平均相对分子质量不再变化【解析】判断一个可逆反应是否达到平衡,一般根据“可变量不再变化”来判断。
ρ=m/V,由质量守恒可知气体质量不会改变,题中固定了容器体积,所以密度始终不会改变,无法判断反应是否达到平衡状态。
【答案】 A2.一定条件下,可逆反应:X(g)+3Y(g) 2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),反应达到平衡时,X、Y、Z的浓度分别为0.1 mol·L -1、0.3 mol·L-1、0.08 mol·L-1。
则下列判断不正确的是()A.c1∶c2=1∶3B.平衡时,Y和Z生成速率之比为3∶2C.X、Y的转化率不相等D.c1的取值范围为0<c1<0.14 mol·L-1【解析】设X转化的浓度为x mol·L-1,X(g)+3Y(g) 2Z(g)起始浓度(mol·L-1) c1c2c3转化浓度(mol·L-1) x3x2x平衡浓度(mol·L-1) 0.1 0.3 0.08则:c1∶c2=(x+0.1)∶(3x+0.3)=1∶3,A正确;平衡时,正、逆反应速率相等,则Y和Z的生成速率之比为3∶2,B正确;反应前后X、Y气体的浓度比相同,符合反应化学计量数之比,所以达到平衡状态时转化率相同,C 错误;若起始时反应向逆反应方向进行,则0<c 1<0.1 mol·L -1,如反应向正反应方向进行,则0.1 mol·L -1<c 1<0.14 mol·L -1,则0<c 1<0.14 mol·L -1,D 正确。
2017版高考化学一轮复习:章末冲关评价练5
章末冲关评价练(五)(时间:45分钟分值:100分)一、选择题(每小题5分,共50分)1.用9943Tc给低产油田作“钡透”,能实现原油的增产增收。
下列有关9943Tc的说法中正确的是()A.9943Tc与9743Tc互为同素异形体B.9943Tc含有43个中子C.9943Tc与9743Tc的物理性质、化学性质均相同D.9943Tc的中子数比电子数多13【解析】9943Tc与9743Tc互为同位素,不是互为同素异形体,A项错误;9943Tc含有56个中子,B项错误;9943Tc与9743Tc的物理性质不同、化学性质相同,C项错误;99Tc含有56个中子、43个电子,D项正确。
43【答案】 D2.(2013·全国大纲卷)下列关于同温同压下的两种气体12C18O和14N2的判断正确的是()A.体积相等时密度相等B.原子数相等时具有的中子数相等C.体积相等时具有的电子数相等D.质量相等时具有的质子数相等【解析】A.根据阿伏加德罗定律,同温同压下,同体积的任何气体含有相同的分子数,即气体的物质的量相同,但由于12C18O与14N2摩尔质量不相等,故质量不相等,密度也不相等。
B.二者都是双原子分子,原子数相等时二者的物质的量相等,二者所含中子数不相等,1个12C18O分子含有16个中子,1个14N2分子含有14个中子。
C.同温同压下,同体积的气体的物质的量相等,且1分子12C18O与14N2中均含有14个电子,故12C18O与14N2具有的电子数相等。
D.12C18O与14N2质子数相等,质量相等的二者物质的量不相等,含有的质子数也不相等。
【答案】 C3.(2016·河北衡水调研)下列说法中,不正确的是()A.短周期元素中,最外层电子数是其电子层数两倍的元素共有3种B.第三周期元素的离子半径大小比较:Cl->S2->Na+>Mg2+>Al3+C.日本福岛核电站释放出的放射性核素131I、132I、133I互为同位素D.相同条件下,通过测定同浓度的Na2CO3溶液和Na2SO4溶液的pH,可比较C和S的非金属性强弱【解析】短周期元素中,最外层电子数是其电子层数两倍的元素共有3种,每周期1种,A正确;同周期元素的阴离子半径大于阳离子半径,核外电子排布相同时核电荷数大的离子半径小,硫离子半径应该大于氯离子半径,B不正确;同种元素的不同原子互为同位素,C正确;通过测定同浓度的Na2CO3溶液和Na2SO4溶液的pH,得到碳酸和硫酸的酸性强弱,从而得到C和S的非金属性强弱,D正确。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
章末冲关评价练(十二)(时间:45分钟分值:100分)一、选择题(每小题6分,共30分)1.咖啡酸具有止血功效,存在于多种中药中,其结构简式如图。
则下列有关说法正确的是()A.该物质苯环上一氯代物有2种B.1 mol该物质可以与1.5 mol碳酸钠溶液反应生成1.5 mol CO2C.既能发生取代反应,也能发生加成反应D.所有碳原子不可能都在同一个平面上【解析】A项,该物质苯环上的一氯代物有3种,错误;B项,该有机物中酚羟基、—COOH均能与Na2CO3反应,但只有—COOH能生成CO2,错误;D项,苯环及其所连的12个原子共平面,碳碳双键及所连的原子共平面,通过碳碳单键的旋转两平面可能重合,故所有碳原子可能共平面,错误。
【答案】 C2.(2016·杭州模拟)儿茶素(其结构简式如图所示)是茶叶的主要活性成分,具有抗氧化、抗菌、除臭等作用。
R′=H或OH)下列说法正确的是()A.常温下,儿茶素不溶于水,也不溶于有机溶剂B.儿茶素能与FeCl3溶液发生显色反应C.1 mol儿茶素最多可与4 mol NaOH反应D.儿茶素一定不能发生水解反应【解析】A项,该物质在常温下不易溶于水,但能溶于有机物溶剂,错误;B项,儿茶素分子中含有酚羟基,能与FeCl3溶液发生显色反应,正确;C项,该分子中最多含有8个酚羟基和1个酯基,均可与NaOH溶液反应,所以1 mol 儿茶素最多可与9 mol NaOH反应,错误;D项,若R是则该分子中存在酯基,可以发生水解反应,错误。
【答案】 B3.(2016·武汉调研)某饱和一元酯C5H10O2在酸性条件下水解生成甲和乙两种有机物,乙在铜的催化作用下能被氧化为醛,满足以上条件的酯有() A.6种B.7种C.8种D.9种【解析】乙在铜的催化作用下能被氧化成醛,说明乙为醇,且其所含的羟基在端位碳原子上,满足该条件的醇有甲醇、乙醇、1-丙醇、1-丁醇、2-甲基-1-丙醇,甲醇对应生成的酯有2种,为正丁酸甲酯和异丁酸甲酯,其他醇对应生成的酯均只有1种,故满足条件的酯共有6种。
【答案】 A4.(2016·南昌一模)某天然拒食素具有防御非洲大群蚯蚓的作用,其结构简式如图(未表示出原子或原子团的空间排列)。
该拒食素与下列某试剂充分反应,所得有机物分子的官能团种数减少,则该试剂是()A.H2B.Cu(OH)2悬浊液C.HBr D.Br2的CCl4溶液【解析】该有机物中含有碳碳双键、醛基2种官能团,与氢气充分反应所得有机物中含羟基1种官能团,A项符合题意;与Cu(OH)2悬浊液反应所得有机物中含碳碳双键、羧基2种官能团,官能团种数不变,B项不符合题意;分别与HBr、Br2发生加成反应,所得有机物中含Br原子、醛基2种官能团,官能团种数不变,C项、D项不符合题意。
【答案】 A5.(2016·山西考前监测)布洛芬属于丁苯丙酸的一种,是世界卫生组织推荐的儿童抗炎退烧药,其结构如图所示。
下列说法不正确的是( )A.布洛芬的分子式为C 13H 18O 2B .布洛芬与苯甲酸(C 6H 5COOH)互为同系物C .丁苯丙酸共有12种可能的结构D .布洛芬能发生加成、取代等反应【解析】 根据已知结构可知布洛芬的分子式为C 13H 18O 2,A 项正确;布洛芬与苯甲酸中含有1个苯环、1个羧基,且分子组成相差6个“CH 2”原子团,故它们属于同系物,B 项正确;丁基有4种结构,分别为—CH 2CH 2CH 2CH 3、丙酸基有2种结构,分别为—CH 2CH 2COOH 、两个取代基在苯环上有邻、间、对3种位置关系,故丁苯丙酸的可能结构有4×2×3=24(种),C 项错误;布洛芬分子中含有苯环,可发生加成反应,苯环上的H 和烷基上的H 可被取代,D 项正确。
【答案】 C二、非选择题(共4大题,70分)6.(18分)(2016·湖北八校联考)烃A 的质谱图中,质荷比最大的数值为42。
碳氢两元素的质量比为6∶1,其核磁共振氢谱有三个峰,峰的面积比为1∶2∶3。
A 与其他有机物之间的关系如下图所示:已知:CH 2===CH 2――→KMnO 4/OH -HOCH 2CH 2OH ,回答下列问题:(1)F 的结构简式为________________________________________。
(2)有机物C 中的官能团名称为_______________________________。
(3)指出下列转化的化学反应类型:A →B____________,E →G____________。
(4)写出C 与新制的氢氧化铜悬浊液反应的化学方程式:_________________________________________________________。
(5)E 在一定条件下可以相互反应生成一种六元环有机物,则此反应的化学方程式为_________________________________________________________。
(6)与E 互为同分异构体,且属于酯类的有机物,除CH 3OCOOCH 3、CH 3CH 2OCOOH 外还有________种(分子中无O —O 键)。
【解析】 本题考查有机化合物的官能团的性质、有机反应类型、有机合成等。
烃A 的质谱图中,质荷比最大的数值为42,即A 的相对分子质量为42,碳氢两元素的质量比为6∶1,则碳氢原子个数比为612∶11=1∶2,所以A 的分子式为C 3H 6,其核磁共振氢谱有三个峰,峰的面积比为1∶2∶3,则A 的结构简式为CH 3CH===CH 2,A 发生加聚反应可得F 为,根据题中信息可知,A 被高锰酸钾氧化成B 为CH 3CHOHCH 2OH ,B 发生氧化反应生成C 为CH 3COCHO ,C 发生氧化反应再酸化得D 为CH 3COCOOH ,D 与氢气发生加成反应生成E 为CH 3CHOHCOOH ,E 发生缩聚反应得高聚物G 。
(1)根据上面的分析可知,F 的结构简式为。
(2)C 为CH 3COCHO ,C 中含有的官能团名称为羰基和醛基。
(3)根据上面的分析可知,A →B 为氧化反应,E →G 为缩聚反应。
(4)C 为CH 3COCHO ,C 与新制的氢氧化铜悬浊液反应的化学方程式为CH 3COCHO +2Cu(OH)2+NaOH ――→△CH 3COCOONa +Cu 2O ↓+3H 2O 。
(5)E 为CH 3CHOHCOOH 含有羧基和醇羟基,E 在一定条件下可以相互发生酯化反应生成一种六元环有机物,反应的化学方程式为+2H 2O 。
(6)与CH 3CHOHCOOH 互为同分异构体,且属于酯类的有机物,除CH 3OCOOCH 3、CH 3 CH 2 OCOOH 外还有HOCH 2 COOCH 3、HCOOCH 2CH 2OH 、HCOOCH 2OCH 3、HCOOCH(OH)CH 3、CH 3COOCH 2OH 共5种。
【答案】 (1) (2)羰基(或酮基)、醛基△(3)氧化反应缩聚反应(4)CH3COCHO+2Cu(OH)2+NaOH――→CH3COCOONa+Cu2O↓+3H2O+2H2O7.(18分)(2016·贵州八校二次联考)已知①C7H10O4是六元环状化合物,②一个碳原子上连两个羟基不稳定,脱水生成,有下列合成路线。
请回答下列问题:(1)反应1的反应类型____________,反应2的反应类型____________。
(2)C2H4O3分子中所含官能团的名称________。
(3)写出B的结构简式________________,C的结构简式________________。
(4)C2H2Cl4→A的化学方程式__________________________________________________________________________________________________________________。
(5)C5H12O2―→C5H10O2的化学方程式__________________________________________________________________________________________________________________。
(6)C5H10O2的同分异构体中,属于酯类的同分异构体有________种。
【解析】根据题给合成路线中各物质的转化关系,由C2H2Cl4在碱性条件下水解生成A和A在酸性条件下生成C2H4O3,结合题给信息②,可确定A为HOCH2COONa,进而确定C2H4O3的结构简式为HOCH2COOH,C2H2Cl4的结构简式为CH2ClCHCl3;由C5H10能发生加成反应,说明其中有一个碳碳双键,反应1为C5H10与溴的加成反应,反应2为C5H10Br2在碱性条件下水解生成C5H12O2,C5H12O2中有两个相邻的羟基,由C5H12O2氧化的最终产物C5H10O3可知,C5H10O3中有一个羟基和一个羧基,即C5H12O2中有一个羟基不能被氧化,据此可确定其结构简式为CH3CH2C(CH3)OHCH2OH,进而顺推出C5H10O2为CH3CH2C(CH3)OHCHO,C5H10O3为CH3CH2C(CH3)OHCOOH和C5H10O3的缩聚产物C为【答案】(1)加成反应水解(取代)反应(2)羟基和羧基(4)CH 2ClCHCl 3+5NaOH ――→△HOCH 2COONa +4NaCl +2H 2O(5)2CH 3CH 2C(CH 3)OHCH 2OH +O 2――→催化剂2CH 3CH 2C(CH 3)OHCHO +2H 2O (6)98.(16分)(2016·湖南十三校联考)已知:①乙醛甲基上的氢原子的活性都很强,可与甲醛发生如下反应:CH 3CHO +HCHO 催化剂HOCH 2CH 2CHO ……③醇可与浓氢卤酸共热反应生成卤代烃。
现由乙烯和丙二酸等物质为原料来合成G ,合成路线如下:(1)写出下列物质的结构简式:A.________;C.________;G .________。
(2)写出下列反应的反应类型:Ⅲ.________________________________; Ⅳ.____________。
(3)写出A ―→B 的化学反应方程式:__________________________________________________________________________________________________________________。
