高分子化学实验报告
苯丙乳液——高化实验报告

苯乙烯
分子式 分子量 C7H12O 128.17 2 沸点 145.7 用量 12ml
丙烯酸 丁酯
分子式 分子量
高ium lauryl sulfate 熔点 204-207
C12H25 288.38 O4SNa 沸点 --用量 0.2g
1.09 摩尔数 0.0008 密度 1.98 摩尔数 0.002 密度 2.44 摩尔数 ---
2
性状 无色透明油状液体 溶解性 不溶于水,溶于 醇、醚等多数有机 溶剂 性状 无色透明液体 溶解性 不溶于水,可混溶 于乙醇、乙醚 性状
毒性 对眼和上呼吸道粘膜有 刺激和麻醉作用。 备注 苯乙烯:丙烯酸丁酯 =2:3(体积比) 毒性 其蒸气或雾对眼睛、粘 膜和呼吸道有刺激作用 备注 苯乙烯:丙烯酸丁酯 =2:3(体积比) 毒性
在已准确称重的小铝箔皿中 滴入约 1g 的产品,滴加 1 滴 TBC,准确称重后,放入 烘箱内,几天后取出冷却, 称重,计算固含量。 将乳液在洁净的玻璃板上, 置于常温下成膜,观察膜的 完整性和透明性。
铝箔 0.182g,滴加了 1.03g 乳液,最后总重为 0.377g, 固含量为 18.9%
我的膜大部分比较平整,不 玻璃板的洁净程度对成膜好 粘,但有些地方涂得不够均 坏有很大影响。成膜机理见 匀,因为层数没涂一致。 最后的实验结果分析。 AlCl3 的破乳机理,实际上 与胶体的聚沉类似,Al3+离 我的乳液迅速生成白色浆状 子的聚沉能力最强,与胶粒 物,后立刻聚集成为橡胶状 界面上的十二烷基硫酸钠结 弹性物质,用手挤压可以渗 合后,胶粒之间斥力减小, 出较多水分 因而聚沉成为颗粒,甚至成 为大块固体。
聚合体系变蓝是因为粒径达 到了一定水平,光线散射而 得。 共聚要考虑竞聚率,因此选 用半连续法对最终产品的性 能更有利。 蓝色不明显说明粒径增大。 补加引发剂,是防止聚合中 后期自由基被包围而使得增 长减缓,单体过度堆积而使 得胶粒溶胀,这也是半连续 法的一个重要工艺。 有油花说明还可以继续反 应,但量很少,几乎看不出 来。 TBC 为阻聚剂,防止乳液在 烘箱中继续聚合,理论固含 量应为 20.4%,这说明仍有 一些单体未能反应。
高吸水树脂的制备——高化实验报告
高分子化学实验报告
水。当渗透压差消失时,树脂便达到了吸水平衡。 3.影响高吸水性树脂吸水倍率的因素有哪些? 答:影响因素很多。从原料上考虑,有单体的类别、中和度,还有交联剂、引发剂的 类型和用量;从聚合过程上考虑,有聚合温度、聚合时间、加料方式等;从成品的角度考 虑,有结构助剂、防老化剂的用量等等。 九、 实验心得
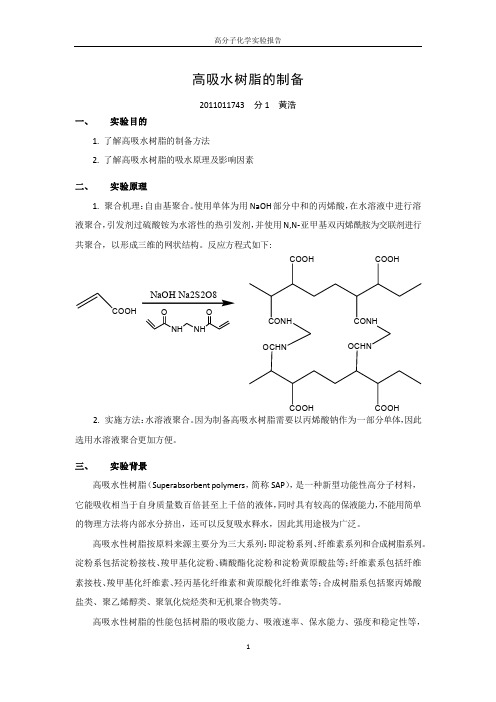
COOH COOH
NaOH Na2S2O8
COOH O NH NH OCHN OCHN O CONH CONH
COOH
CO因为制备高吸水树脂需要以丙烯酸钠作为一部分单体, 因此 选用水溶液聚合更加方便。 三、 实验背景
高吸水性树脂 (Superabsorbent polymers, 简称 SAP) , 是一种新型功能性高分子材料, 它能吸收相当于自身质量数百倍甚至上千倍的液体, 同时具有较高的保液能力, 不能用简单 的物理方法将内部水分挤出,还可以反复吸水释水,因此其用途极为广泛。 高吸水性树脂按原料来源主要分为三大系列: 即淀粉系列、 纤维素系列和合成树脂系列。 淀粉系包括淀粉接枝、 羧甲基化淀粉、 磷酸酯化淀粉和淀粉黄原酸盐等; 纤维素系包括纤维 素接枝、 羧甲基化纤维素、 羟丙基化纤维素和黄原酸化纤维素等; 合成树脂系包括聚丙烯酸 盐类、聚乙烯醇类、聚氧化烷烃类和无机聚合物类等。 高吸水性树脂的性能包括树脂的吸收能力、吸液速率、保水能力、强度和稳定性等,
3
高分子化学实验报告
下图分别为聚合得到的凝胶(左)和切割得到的胶块(右) :
下图分别为烘干后的吸水树脂(左,薄膜态)和吸水饱和后的树脂(右,胶冻态) :
六、
注意事项 1. 本实验为研究型实验, 中和度、 交联度和引发剂用量都为可选条件, 在实验前应明
确分工,并进行详细记录,我们将中和度和交联剂用量作为了变量。 2. 在中和过程中, 氢氧化钠水溶液应滴加到丙烯酸中, 使其缓慢放热。 中和度用摩尔 比计算。 3. 在聚合过程中不可搅动溶液,聚合之后应用去离子水洗涤,而不是自来水。
高分子化学实验报告

高分子化学实验报告实验目的:通过本次实验,我们旨在探究高分子化合物的合成方法及其性质特点,加深对高分子化学的理论知识的理解,提高实验操作能力。
实验原理:高分子化合物是由许多重复单元组成的大分子化合物,其合成方法主要包括聚合反应和缩聚反应。
聚合反应是通过单体分子之间的共价键形成高分子链,而缩聚反应则是通过小分子间的共价键形成高分子链。
高分子化合物的性质特点包括分子量大、熔点高、溶解性差等。
实验步骤:1. 实验前准备,准备所需试剂和设备,确保实验环境整洁。
2. 聚合反应实验,将单体A和单体B按一定摩尔比例混合,加入催化剂,在适当温度下进行反应,得到高分子化合物。
3. 缩聚反应实验,将小分子C和小分子D按一定摩尔比例混合,加入催化剂,在适当温度下进行反应,得到高分子化合物。
4. 高分子化合物性质测试,测试所得高分子化合物的分子量、熔点、溶解性等性质。
实验结果与分析:通过实验,我们成功合成了两种不同结构的高分子化合物,分别进行了性质测试。
实验结果表明,聚合反应所得高分子化合物具有较高的分子量和熔点,而缩聚反应所得高分子化合物溶解性较差。
这与高分子化合物的性质特点相吻合。
实验结论:本次实验通过聚合反应和缩聚反应成功合成了两种高分子化合物,并对其性质进行了测试。
实验结果表明,高分子化合物的合成方法和性质与理论知识相符合。
通过本次实验,我们加深了对高分子化学的理论知识的理解,提高了实验操作能力。
实验注意事项:1. 实验操作时要注意安全,避免接触有害物质。
2. 实验设备要保持干净整洁,避免杂质对实验结果的影响。
3. 实验操作要仔细,按照实验步骤进行,避免操作失误导致实验失败。
总结:通过本次实验,我们对高分子化学有了更深入的了解,实验结果验证了理论知识的正确性。
在今后的学习和研究中,我们将继续深入探究高分子化学领域,不断提高自己的实验技能和理论水平。
以上就是本次高分子化学实验的实验报告,谢谢阅读!。
高分子聚合反应实验报告

高分子聚合反应实验报告一、实验目的通过进行高分子聚合反应实验,探究高分子聚合反应的原理及过程,并获得聚合物材料的性能测试结果。
二、实验原理高分子聚合反应是指通过一系列化学反应将单体分子逐渐连接成大分子的过程。
其中,自由基聚合反应是最常见的一种高分子聚合反应类型。
自由基聚合反应中,通常使用引发剂将稳定的自由基中间体引发聚合反应。
聚合反应的过程包括引发、传递和终止三个步骤。
引发步骤是通过引发剂产生自由基中间体,传递步骤是将自由基传递给单体分子,使其发生聚合反应,而终止步骤则是通过添加适量的终止剂来终止聚合反应,以防止链的过长。
三、实验步骤1. 实验前准备:准备实验所需的试剂和仪器设备。
2. 合成聚合物样品:按照实验方案中的比例混合单体和引发剂,加入适量的溶剂,通过恒温反应器进行反应。
3. 分离和提取聚合物:通过溶剂溶解和萃取等步骤,将聚合物从反应体系中分离和提取出来。
4. 聚合物性能测试:对提取得到的聚合物样品进行性能测试,包括分子量、熔点、玻璃化转变温度等方面的测试。
5. 结果记录和分析:将实验得到的数据进行整理、记录和分析,得出实验结论。
四、实验结果与讨论根据实验步骤进行实验后,得到了聚合物样品,并对其进行了性能测试。
实验结果显示,聚合物样品的分子量在一定范围内,熔点和玻璃化转变温度符合预期的范围。
这表明实验中成功合成了目标聚合物,并具备一定的热稳定性和物理性能。
五、实验结论通过高分子聚合反应实验,成功合成了目标聚合物。
实验结果表明,该聚合物具备一定的热稳定性和物理性能。
实验所采用的反应方案和操作步骤得到了验证,并为后续相似实验提供了指导和参考。
六、实验心得通过本次实验,我对高分子聚合反应的原理和过程有了更深入的理解。
同时,我也了解到了实验操作的重要性和细节处理的必要性。
在今后的实验中,我将更加注重实验操作的规范性和细致性,以获得更准确的实验结果。
七、参考文献[1] 参考文献1[2] 参考文献2[3] 参考文献3以上为本次高分子聚合反应实验报告,感谢您的耐心阅读。
高分子化学实验报告

摘要离子交换法是液相中的离子和固相中离子间所进行的的一种可逆性化学反应,当液相中的某些离子较为离子交换固体所喜好时,便会被离子交换固体吸附,为维持水溶液的电中性,所以离子交换固体必须释出等价离子回溶液中。
离子交换树脂一般呈现多孔状或颗粒状,其大小约为0.5~1.0m m,其离子交换能力依其交换能力特征可分:(1)强酸型阳离子交换树脂:主要含有强酸性的反应基如磺酸基(-S O3H),此离子交换树脂可以交换所有的阳离子。
(2)弱酸型阳离子交换树脂:具有较弱的反应基如羧基(-C O O H基),此离子交换树脂仅可交换弱碱中的阳离子如C a2+、M g2+,对于强碱中的离子如N a+、K+等无法进行交换。
阳离子交换树脂大都含有磺酸基(—S O3H)、羧基(—C O O H)或苯酚基(—C6H4O H)等酸性基团,其中的氢离子能与溶液中的金属离子或其他阳离子进行交换。
例如苯乙烯和二乙烯苯的高聚物经磺化处理得到强酸性阳离子交换树脂,其结构式可简单表示为R—S O3H,式中R代表树脂母体,其交换原理为:2R—S O3H+C a2+=(R—S O3)2C a+2H+关键词:阳离子交换树脂酸性基团金属离子氢离子磺化树脂母体ABSTRACTIo n ex c h an ge p ro c es s i s a re v e rs i bl e ch e m i c al r e a ct i on be t w e en t h e l i q ui d ph as e and s ol i d p ha s e,wh en s om e o f t h e i on i s p r e f e r ed b y t h e i o n ex ch an ge s ol i d,wi l l b e a bs o rb e d b y t h e i o n ex c h an ge s ol i d. In o r d e r t o m a i nt ai n t h e el e ct ri c n e ut r al i t y o f w a t e r s ol ut i on, s o i o n ex ch an ge sol i d m u s t r e l e a s e t he e qu al i on b a c k t o s o l u t i o n.Io n e x c h an ge r es i n ge n er a l l y p r e s en t s a s m ul t i p l e ho l es o r p a rt i cl e s h ap e, i t s si z e i s ab ou t0.5 ~ 1.0m m,t h e i o n ex c h an ge c a p a ci t y c a n b e di vi d e d i nt o2p a rt s b y i t s ex c h an ge c ap a c i t y c h a r a ct e ri st i cs:(1)St ro n g-a ci d c a t i on ex ch an ge r es i n: m ai n l y c o n t ai ns s t ro n g a c i d r e a ct i on m e di u m su c h a s s ul f on i c a c i d gro up(- S O3H ),t hi s i on ex c ha n ge r es i n c a n ex c ha n ge al l c at i o ns.(2)We ak-a ci d ca t i on ex c ha n ge r e s i n: ha vi n g a w e a k er r e a c t i on m e d i u m su ch as c ar b ox yl(-C O O H),t hi s i on ex ch a n ge re s i n c a n o nl y e x ch a n ge c a t i o ns i n t h e a l k al i su c h a s C a2+,M g2+, for t hose i n st ro n g al ka l i s u ch as Na+,K+c a nno t ex ch an ge d.M os t o f c a t i o n ex c h an ge r e si n c ont a i ni n g s ul fo ni c a ci d (-S O3H), c a r b ox yl(-C O O H)o r a p h en ol-b as e d(-C6H4O H)a nd o t he r a ci di c gr o u ps, wh i ch h yd r o ge n i o ns c an ex c h a n ge w i t h m et a l i o ns i n s ol ut i on o r ot h e r c at i o n. S u c h as s t yr e n e a nd t he s t r on g a c i d c at i on ex c h an ge r e si n o bt a i n ed b y d i v i n yl be nz e n e p ol ym e r t h ro u gh t he s ul f on at i on,a nd i t s st r uc t u r e c a n b e s i m pl y e x p r es s e d a s R-S O3H, w h e r e R r ep r e se nt s t h e r es i n m at r i x, t h e p ri n ci p l e o f t h e ex c h an ge i s:2R—S O3H+C a2+=(R—S O3)2C a+2H+K E Y WO R DS:C at i on ex c h an ge r es i n, A c i di c gr ou ps,M et al i o ns, H yd r o ge n i o n,S u l fo n at e d r esi n m at ri x前言离子交换树脂是一种具有网状立体结构、且不溶于酸、碱和有机溶剂的固体高分子化合物.离子交换树脂的单元结构由两部分组成。
BPO的精制实验报告

高分子化学实验报告2014级高分子(2)班姓名:杨磊学号:1414171037实验名:过氧化苯甲酰(BPO)的精制一、实验目的1)了解高分子化学自由基聚合过程中引发剂的精制的原理和方法。
2)掌握利用重结晶的方法精制过氧化苯甲酰(BPO)。
二、实验原理过氧化苯甲酰(BPO)为白色结晶性粉末,熔点103~105摄氏度,溶于乙醚、丙酮、氯仿和苯等有机溶剂,易燃烧,受撞击、热、摩檫会爆炸。
常用的过氧化苯甲酰由于长期保存部分分解,因此在用于聚合前要先进行精制,通常采用的方法是重结晶,以氯仿为溶剂,甲醇为沉淀剂进行BPO的精制,在结晶过程中温度过高会爆炸,应注意控制温度。
过氧化苯甲酰在不同溶剂中的溶解度如下:重结晶原理:利用被提纯物质在不同溶剂中的溶解度不同提纯固体物质,是杂质在热滤时被出去或是在冷却后被留在母液中从而达到提纯固体化合物的目的。
本实验中BPO在氯仿中溶解度较大,在甲醇中溶解度较小,BPO溶解在氯仿中后,再将溶液滴入到甲醇中,由于BPO在氯仿中的溶解度远远大于在甲醇中的溶解度,因此可以将BPO结晶析出。
三、实验药品及仪器药品:过氧化苯甲酰、氯仿、甲醇仪器:布氏漏斗、烧杯、玻璃棒、纱布、量筒四、实验步骤及现象体,触摸烧杯外壁有冰凉感,略微带有一点刺激性气味晶体晶形稍有破坏,但仍能观察出较为明显的针状晶形五、实验结果得到白色针状晶体六、产率计算1)烘干后的BPO:0.59g2)产率计算:0.59/3.00*100%=19.67%七、差分析及讨论1)结晶产物上层晶膜不呈针状,晶体较小,没能长成较大的针状晶体。
析:可能有部分杂质参与了结晶,在将BPO的氯仿溶液加入到甲醇中的时候一边加一边旋转了烧杯,没有在同一个点加入,可能引起了较多晶核的出现,形成了一些细小的点状晶粒,导致了之后的结晶竞争较强,不能很好的形成较大的漂亮的针状晶体;在讲溶液拿到风扇下去吹的时候也们有较好的保持平稳,烧杯晃动的过程中可能也会形成些许晶核,导致结晶长不大。
环氧树脂的固化——高化实验报告

环氧树脂的固化2011011743 分1 黄浩一、实验目的1.了解高分子化学反应的基本原理及特点2.了解环氧树脂的制备及固化反应的原理、特点二、实验原理环氧树脂(epoxy resins),是指分子中带有两个或两个以上环氧基的低分子量物质及其交联固化产物的总称,是一种热固性树脂。
其最重要的一类是双酚A型环氧树脂,它是由环氧氯丙烷与双酚A 在氢氧化钠作用下聚合而成:如下图所示,双酚A环氧树脂中末端的活泼的环氧基和侧羟基赋予树脂反应活性,使它可以与交联剂作用,从而交联成三维结构,即固化;双酚A的苯环骨架提供强韧性和耐热性,亚甲基链赋予树脂柔韧性,这使得它的综合性能优异,可以用作特种塑料;羟基和醚键的高度极性,使环氧树脂分子与相邻界面产生了较强的分子间作用力,而且因环氧基的高活性,使得它固化速度很快,从而可以作为粘结剂,商业上称作“万能胶”。
因为环氧树脂在未固化前是呈热塑性的线型结构,要实现它的各种功能,必须加入固化剂,与环氧树脂的环氧基等反应,变成网状结构的大分子,成为不溶不熔的热固性成品。
固化剂的种类很多,可以根据分子结构分为如下三类:1、胺类固化剂:胺类固化剂可分为脂肪胺型和芳香胺型。
脂肪胺型使用比较普遍,硬化速度快、黏度低、使用方便,但固化剂本身的毒性较大、易升华,固化后形成的胶层脆性大、粘结强度不高、耐热性和介电性较差等。
芳香胺型形成的固化物可在100~150℃长期使用,粘接强度高,耐化学试剂和耐老化性能好,但作为结构胶使用韧性不够,还需要增韧改性。
根据有机化学的知识,要使环氧开环成羟基,必须使用一二级胺,因为它们含有活泼氢原子,使环氧基开环生成羟基,生成的羟基再与环氧基起醚化反应,最后生成网状或体型聚合物。
三级胺只可进行催化开环,环氧树脂的环氧基被叔胺开环变成阴离子而非羟基,一般而言,不直接用作固化剂,常常与酸酐类固化剂联用。
2、酸酐类固化剂:硬化反应较平稳,硬化过程中放热少,使用寿命长,毒性较小,硬化后树脂的力学性能较好。
PVA的制备——高化实验报告

聚乙烯醇的制备——PVAc的合成和醇解2011011743 分1 黄浩一、实验目的1.通过乙酸乙烯酯的溶液聚合,了解溶液聚合原理及过程。
2.掌握用于制备维尼纶的聚乙酸乙烯酯工艺条件的特点。
3.了解高分子化学反应的基本原理及特点。
4.了解聚醋酸乙烯酯醇解反应的原理、特点及影响醇解反应的因素。
二、实验原理(一)PVAc合成:1.聚合机理:自由基聚合。
醋酸乙烯酯是低活性单体、高活性自由基,容易发生链转移,一般转移至醋酸基的端甲基处,如向大分子转移则形成交联产物、向单体和溶剂转移则降低分子量。
为了控制链转移以控制分子量,需要对温度进行控制,温度升高则链转移反应增加,降低分子量,温度降低则反应速率降低,因此要选择适当的反应温度。
因为链转移的存在,聚乙酸乙烯酯(PVAc)为非结晶性聚合物,玻璃化温度较低,性脆,并且呈现出冷流,不能用作塑料制品。
2.实施方法:溶液聚合。
溶液聚合体系由单体、引发剂和溶剂组成,具有反应均匀、聚合热易散发、容易控温、分子量分布均匀等优点。
但同时,溶液聚合也存在着一些缺点,如自由基向溶剂进行链转移,导致分子量降低;单体浓度相对本体聚合降低,使得聚合速率降低;增加了溶剂分离的步骤,增加了工业生产的成本,等等。
因此,溶液聚合通常用于聚合物溶液直接使用的场合,如涂料、粘合剂、合成纤维纺丝液等。
3.聚合条件:本实验使用AIBN为引发剂,甲醇为溶剂,控制聚合温度为70℃,最后通过水浸+水洗的方法,将聚合物与溶剂和单体分离。
AIBN是热引发的引发剂,根据半衰期选择聚合温度在70℃附近;为使聚合终点得以判断,选择低沸点溶剂甲醇,以其气化的气泡来监测体系粘度。
反应方程式如下:O O**OOnn(二)PVAc醇解:本实验为高分子反应,酯的醇解,即酯交换反应,在碱催化下进行。
高分子反应由于链团的屏蔽和分子扩散的阻碍,以及邻基效应、几率效应和溶解度效应等,反应程度普遍不高,与小分子反应存在较大差别。
由于“乙烯醇”易异构化为乙醛,不能通过理论单体“乙烯醇”的聚合来制备聚乙烯醇,只能通过聚乙酸乙烯酯的醇解或水解反应来制备,而醇解法制成的PVA 精制容易,纯度较高,主产物的性能较好,因此工业上通常采用醇解法。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
高分子化学实验报告
实验目的:
本实验旨在通过合成高分子材料聚苯乙烯(PS),探究高分子化学
的原理与制备方法。
实验原理:
聚苯乙烯是一种常见的塑料,具有良好的机械性能和耐化学腐蚀性。
它是通过苯乙烯单体的自由基聚合反应制备而成的。
聚合反应是一种
链式反应,包括起始、传递和终止三个步骤。
在起始步骤中,通过投
入引发剂(如过氧化苯甲酰)引发苯乙烯的自由基聚合。
在传递步骤中,自由基在聚合过程中转移。
在终止步骤中,反应中止,形成分子
量各异的聚合物。
实验步骤:
1. 首先准备实验所需材料,如苯乙烯单体、过氧化苯甲酰等。
2. 在实验室操作台上搭建聚合反应设备,包括反应釜、冷却装置和
搅拌装置。
3. 按照一定的配方将苯乙烯单体、引发剂和溶剂加入反应釜中。
4. 打开搅拌装置,开始搅拌混合,保持适当的反应温度和时间。
5. 实验结束后,将反应混合物抽滤、洗涤清洁,并用真空干燥法将
聚苯乙烯产物制成固体。
实验结果与分析:
通过实验可得到聚苯乙烯固体产物,并通过质谱仪等仪器进行表征。
经过测定,聚苯乙烯的分子量、熔点、拉伸强度等参数可以得到。
根
据实验结果可以判断聚苯乙烯的合成反应达到预期效果。
实验讨论:
聚苯乙烯是一种常见的高分子材料,具有广泛的应用前景。
本实验
中所使用的反应条件仅为示例,实际生产中需要根据具体要求进行优化。
此外,聚苯乙烯的性能还可以通过改变反应条件、引入共聚单体
等手段进行调控。
结论:
本实验通过合成聚苯乙烯,探究了高分子化学的原理与制备方法。
通过实验我们得到了聚苯乙烯的固体产物,并对其进行了表征。
该实
验有助于加深对高分子化学的理解,并为相关应用领域的研究提供了
基础。
参考文献:
[1] Smith, J. M., & Johnson, D. B. (2018). Polymer Science and Technology. Academic Press.
[2] Cowie, J. M. (2007). Polymers: Chemistry and Physics of Modern Materials. CRC Press.
附注:本实验报告仅为示例,具体内容根据实际实验情况进行调整。
实验操作中需严格遵守实验室安全规范,并在有资质指导人员的指导
下进行。
