-热力学基础总结
热 力 学 基 础 总 结
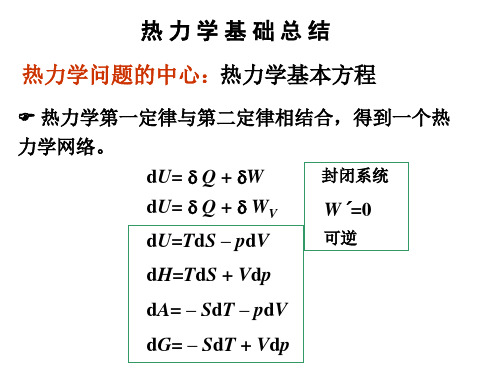
(CB)
;
(
A nB
)T
,v,nc
(CB)
;
(
G nB
)T
,V
,nc
; (CB)
(
U nB
)
S ,V
,nc
V
(CB)
;
( nB
)T , p,nc
H
(CB)
;
( nB
) S , p,nc
; (CB)
A ( nB )T , p,nc (CB) ;
解: 偏摩尔量:
; ; ; H
( nB )T , p,nc (CB)
• 热力学量变换法(变量变换法)就是将不能用实 验直接测量的量转换为用实验量或状态方程表 示的关系的基本方法。
变量变换法
从研究工作需要来看:
变量变换法是在学科发展中形成的科学方法。 通常在研究工作中会提出许多科学命题,为 寻求解决问题的思路或设计实验,总要想法 进行命题的转换,以利用已有信息或通过实 验进行分析,其间变量变换就是一个有效的 方法,今以实例说明。
解:在水的正常沸点时 1= 2;
在温度为 373.15K 及 202 650 Pa 下
因为 所以
故
(
Gm* p
)T
Vm
>0
3> 1
4> 2
4> 3> 2= 1。
4> 3。
计算题
1 一定量纯理想气体由同一始态,分别经绝热可逆 膨胀至(T2,p2, V2)和经绝热不可逆膨胀至(T2',p2',V2')
=
nCV,m dT T
p dV T V
dG= – SdT + Vdp dGT= Vdp
变量变换法
工热知识点总结

工热知识点总结一、理论基础1. 热力学基础热力学是研究热现象和能量转化规律的科学,其研究对象包括热力学系统的状态、过程和相互作用等。
热力学定律包括热力学第一、二、三定律,它们分别描述了能量守恒、熵增加和温度不可降的规律。
2. 热传导热传导是指物质内部热能的传递,根据导热介质的不同,可分为导热、导电、导磁等传导方式。
热传导的计算公式为热传导方程,其中包括热传导系数、温度梯度和距离梯度等。
在实际工程中,热传导的计算可以通过有限元分析、数值模拟等方法得到。
3. 对流传热对流传热是指通过流体的流动使热能传递的过程,可以是强迫对流或自然对流。
对流传热的传热系数和换热器的设计是工热领域的重要内容。
4. 热辐射热辐射是指物体由于温度差而发出或吸收的电磁波,热辐射的计算需要考虑辐射率、温度、表面发射率等参数。
热辐射通常可以通过辐射传热方程来描述,实际工程中可以应用黑体辐射、灰体辐射等模型进行计算。
二、热力学系统1. 封闭系统封闭系统是指不与外界交换物质,但与外界进行能量交换的系统。
热力学系统通常可以根据其与外界的物质交换情况分为封闭系统、开放系统和孤立系统。
2. 开放系统开放系统是指既与外界进行能量交换,又与外界进行物质交换的系统。
例如,蒸汽锅炉和汽轮机系统就是开放系统。
3. 孤立系统孤立系统是指既不与外界交换物质,也不与外界进行能量交换的系统。
孤立系统是理论假设中的一个重要模型,可以用于研究理想化的热力学系统。
三、热力学循环1. 卡诺循环卡诺循环是理想化的热力学循环模型,其效率最高,可用于分析和比较各种热力学循环系统的性能。
卡诺循环包括等温膨胀、绝热膨胀、等温压缩和绝热压缩四个过程,可以用来分析热机和热泵的性能。
2. 布雷顿循环布雷顿循环是一种热力学循环,广泛应用于蒸汽轮机、汽轮机和制冷机等系统。
布雷顿循环包括等压加热、等压膨胀、等压冷却和等压压缩四个过程,可以用来分析蒸汽发电系统和空气压缩系统的性能。
3. 斯特林循环斯特林循环是一种理想化的热力学循环模型,包括等温定压加热、绝热膨胀、等温定压冷却和绝热压缩四个过程。
热工基础的期末总结

热工基础的期末总结一、热力学部分1. 热力学基础知识的学习热力学是研究热能与其他形式能量之间相互转化和传递的一门学科。
在学习过程中,我通过课堂的学习、书籍和网上资料的查阅,对热力学的基本概念、热力学系统和热力学性质等方面有了初步的了解。
2. 热力学基本定律热力学基本定律是热力学的核心内容,也是热工基础的重点。
本课程主要学习了热力学的三大基本定律:热力学第一定律、热力学第二定律和热力学第三定律。
通过对这些定律的学习和应用,我能够分析和计算热力学系统的能量转移和能量转化过程。
3. 热力学过程和热力学循环热力学过程是指系统在一定条件下发生的能量传递和物理性质发生变化的过程。
热力学循环是指系统在一定路径下变化,最终回到初始状态的过程。
通过学习这些内容,我能够对热力学过程和热力学循环进行分析和计算,从而了解能量转移和物理性质变化的规律。
4. 热力学性质的计算热力学性质是指描述系统热力学状态和性质的量,如温度、压力、体积等。
在学习过程中,我学习了热力学性质的计算方法,如状态方程、热容、焓、熵等。
通过对热力学性质的计算,我能够确定系统的热力学状态和性质。
二、传热学部分1. 传热学的基本概念和模型传热学是研究热量如何从高温区向低温区传递的学科。
在学习过程中,我学习了传热学的基本概念和模型,如传热方式、传热模型和传热原理等。
2. 传热方式和传热模型传热方式是指热量传递的途径,主要包括传导、对流和辐射。
传热模型是指用来描述传热过程的数学模型,如传热定律和传热方程等。
在学习过程中,我对这些内容进行了深入的学习和了解。
3. 传热计算方法在传热学中,计算方法是非常重要的,主要包括传热计算和传热换热器的计算。
传热计算是指通过传热方程和传热模型对传热过程进行计算和分析。
传热换热器的计算是指对传热器的传热性能和换热器的几何参数进行计算和设计。
通过学习和掌握这些计算方法,我能够对传热系统进行分析和设计。
三、实践操作在本学期的热工基础课程中,我还进行了一些实践操作和实验课程。
化学热学知识点总结

化学热学知识点总结一、热力学基本概念热力学是研究物体内部能量和物质间能量相互转化的物理学科,并且研究物体内能量的传递和扩散规律以及热现象的规律。
热力学研究的主要对象是热、功和能量。
热是由于温度差引起的能量传递。
功是由于力的作用引起的能量转化。
能量是物体具有的使其能够进行工作的物理量(如物体的动能、势能、内能等)。
热力学的热、功和能量是相互联系、相互转化的。
二、状态函数状态函数是在描述过程时与路径无关的,只与初始和终了状态有关的函数。
例如,压强、温度、体积等。
状态函数的改变与路径无关,只与初末状态有关,与路径无关意味着状态函数的变化值与过程取向无关,所以状态函数的变化必须是由初末状态决定的。
状态函数的改变与路径无关因为它们的改变只与初末态有关。
但对于某些状态函数来说,虽然它与系统的性质本身无关,但是它的改变却能使心理特性发生变化。
三、热力学定律热力学定律是热力学的基本规律,它描述了能量的转化和传递规律。
热力学定律包括零法则、第一定律、第二定律、第三定律。
零法则:如果两个系统与第三个系统分别处于热平衡状态,那么这两个系统之间也一定处于热平衡。
第一定律:能量守恒,即能量不能被创造或消灭,只能从一个物体转移到另一个物体,或从一个形式转化为另一形式。
它也可以表述为:系统的内能增量等于系统所吸收的热量与所作的功的代数和。
第二定律:热能不可能自发地从低温物体传递到高温物体,热力学过程不可逆的方向是从低温物体向高温物体传递热量的方向。
第三定律:当温度接近绝对零度时,是熵趋于常数。
这意味着,不可能通过有限数量次的操作使任何系统冷却至绝对零度。
四、热力学方程热力学方程是描述物质热力学性质的方程,其中包括理想气体状态方程、范德华方程等。
理想气体状态方程为P = nRT。
范德华方程为(P + a/V^2)(V - b) = RT。
热力学方程不仅可以用于计算压强、温度、体积等参数的关系,还可以从中推导出其他热力学性质的关系。
高中物理知识点总结热力学基础

高中物理知识点总结热力学基础IMB standardization office【IMB 5AB- IMBK 08- IMB 2C】一.教学内容:热力学基础(一)改变物体内能的两种方式:做功和热传递1. 做功:其他形式的能与内能之间相互转化的过程,内能改变了多少用做功的数值来量度,外力对物体做功,内能增加,物体克服外力做功,内能减少。
2. 热传递:它是物体间内能转移的过程,内能改变了多少用传递的热量的数值来量度,物体吸收热量,物体的内能增加,放出热量,物体的内能减少,热传递的方式有:传导、对流、辐射,热传递的条件是物体间有温度差。
(二)热力学第一定律1. 内容:物体内能的增量等于外界对物体做的功W和物体吸收的热量Q 的总和。
2. 表达式:。
3. 符号法则:外界对物体做功,W取正值,物体对外界做功,W取负值,吸收热量Q 取正值,物体放出热量Q取负值;物体内能增加取正值,物体内能减少取负值。
(三)能的转化和守恒定律能量既不能凭空产生,也不能凭空消失,它只能从一种形式转化为另一种形式或从一个物体转移到另一个物体。
在转化和转移的过程中,能的总量不变,这就是能量守恒定律。
(四)热力学第二定律两种表述:(1)不可能使热量由低温物体传递到高温物体,而不引起其他变化。
(2)不可能从单一热源吸收热量,并把它全部用来做功,而不引起其他变化。
热力学第二定律揭示了涉及热现象的宏观过程都有方向性。
(3)热力学第二定律的微观实质是:与热现象有关的自发的宏观过程,总是朝着分子热运动状态无序性增加的方向进行的。
(4)熵是用来描述物体的无序程度的物理量。
物体内部分子热运动无序程度越高,物体的熵就越大。
(五)说明的问题1. 第一类永动机是永远无法实现的,它违背了能的转化和守恒定律。
2. 第二类永动机也是无法实现的,它虽然不违背能的转化和守恒定律,但却违背了热力学第二定律。
(六)能源和可持续发展1. 能量与环境(1)温室效应:化石燃料燃烧放出的大量二氧化碳,使大气中二氧化碳的含量大量提高,导致“温室效应”,使得地面温度上升,两极的冰雪融化,海平面上升,淹没沿海地区等不良影响。
大学热学物理知识点总结

大学热学物理知识点总结1.热力学基本定律热力学基本定律是热学物理的基础,它包括三个基本定律,分别是热力学第一定律、热力学第二定律和热力学第三定律。
(1)热力学第一定律热力学第一定律是能量守恒定律的热学表述,它规定了热力学系统能量的守恒性质。
简单地说,热力学第一定律表明了热力学系统能量的增减只与系统对外界做功和与外界热交换有关。
热力学第一定律的数学表达式为ΔU=Q-W,其中ΔU表示系统内能的增量,Q表示系统吸热的大小,W表示系统对外界所作的功。
由此可以看出,系统的内能变化量等于吸收热量减去做的功。
(2)热力学第二定律热力学第二定律是热力学系统不可逆性的表述,它规定了热力学系统内部的熵增原理,即系统的熵不会减小,而只会增加或保持不变。
简单地说,热力学第二定律表明了热力学系统内部的任何一种热力学过程都是不可逆的。
这意味着热力学系统永远无法使热量全部转化为功,总会有一部分热量被转化为无效热。
热力学第二定律还表明了热力学过程的方向性,即热量只能从高温物体传递到低温物体,而不能反向传递。
(3)热力学第三定律热力学第三定律规定了当温度趋于绝对零度时,任何物质的熵都将趋于一个有限值,这个有限值通常被定义为零。
简单地说,热力学第三定律表明了在绝对零度时,任何系统的熵都将趋于零。
热力学第三定律的提出对于热学物理的研究具有非常重要的意义,它为我们理解热学系统的性质提供了重要的基础。
2.热力学过程热力学过程是指热力学系统内部发生的一系列变化,包括各种状态参数的变化和热力学系统对外界的能量交换。
常见的热力学过程有等温过程、绝热过程、等容过程和等压过程等。
这些过程在日常生活以及工业生产中都有着广泛的应用。
(1)等温过程等温过程是指在恒定温度下进行的热力学过程。
在等温过程中,系统对外界做的功和吸收的热量之比是一个常数。
这意味着等温过程的压强和体积成反比,在P-V图上表现为一条双曲线。
常见的等温过程有等温膨胀和等温压缩等。
(2)绝热过程绝热过程是指在无热交换的情况下进行的热力学过程。
热学内容知识点总结
热学内容知识点总结热学的主要内容包括热力学和热传导学。
热力学是热学的基础,它研究热量和功的相互转化过程,以及物质在不同温度下的性质和行为。
热传导学则是研究热量在物体中的传播和传递规律。
此外,热学还涉及到热辐射和相变等内容。
热学在工程技术中有着广泛的应用,如热力机械、制冷空调、火箭发动机等都是依据热学原理来设计和工作的。
在热学的学习过程中,有一些重要的知识点需要我们重点掌握。
下面我们就来总结一下热学的重要知识点。
1. 热力学基本概念热学的基本概念包括热平衡、热容量、热力学系统、热力学过程等。
热平衡是指在相互接触的物体之间,不存在能量的净交换,它们的温度不再发生变化的状态。
热容量是物体对热量的吸收能力的度量,它是指物体温度升高一个度所需的热量。
热力学系统是研究的对象,可以是封闭系统、开放系统或孤立系统。
热力学过程是指系统从一个状态变为另一个状态的过程,包括等容过程、等压过程、等温过程、绝热过程等。
2. 热力学定律热学定律是热学研究的基础,包括热力学第一定律、热力学第二定律、热力学第三定律等。
热力学第一定律是能量守恒定律的推论,它表明热量和功是可以相互转化的。
热力学第二定律是热过程方向性的定律,它表明热量不会自发地从低温物体传到高温物体,也就是热量不会自发地从冷的地方传到热的地方。
热力学第三定律则是介绍了绝对零度的概念,它规定在绝对零度时物体的熵为零。
3. 热力学循环热力学循环是指一个系统在不断地被热源加热和被冷源散热的过程中所经历的一系列热力学过程。
热力学循环包括卡诺循环、斯特林循环、布雷顿循环等。
卡诺循环是一个理想的热力学循环,它由等温膨胀、绝热膨胀、等温压缩、绝热压缩四个过程组成。
卡诺循环具有最高的效率,它为热机的效率提供了理论上的极限。
4. 热力学参数热力学参数是热学研究中的重要内容,包括温度、热量、功、熵等。
温度是物体内能的一种度量,它是物体热平衡状态的一种指标。
热量是热能的转移形式,它是物体之间由于温度差产生的能量交换。
热力学基础知识点总结
热力学基础知识点总结
热力学是研究能量转化与传递规律的科学,主要包括以下基础知识点:
1. 系统与环境:热力学研究的对象是一个被称为系统的物体、组织或区域,而系统与其周围的一切被称为环境。
2. 状态量与过程量:状态量是描述系统状态的量,如温度、压力、体积等,它们只依赖于系统的初始和最终状态;而过程量是描述系统变化过程中的性质,如热量、功等。
3. 热平衡与温度:当两个物体处于热平衡时,它们之间不存在热量的净传递,此时它们的温度相等。
4. 热传递与热传导:热传递是指热量从高温物体流向低温物体的过程,可以通过热传导、辐射和对流等方式实现。
热传导是通过物质分子间的碰撞传递热量的过程。
5. 热容与比热容:热容是指物体吸收或释放单位温度变化所需的热量,而比热容是单位质量物质所需的热量。
6. 理想气体状态方程:理想气体状态方程描述了理想气体的压力、体积和温度之间的关系,常用的方程有理想气体状态方程
(PV=nRT)和绝热过程公式(PV^γ=常数)。
7. 熵与熵增:熵是描述系统无序度的物理量,熵增原理表明在孤立系统中,熵总是增加的。
8. 热力学第一定律:热力学第一定律是能量守恒定律在热力学中的表现,它表明能量可以从一个形式转化为另一个形式,但总能量守恒。
9. 热力学第二定律:热力学第二定律是描述热量传递方向性的原理,它指出热量只能从高温物体传递到低温物体,不会自发地从低温物体传递到高温物体。
10. 吉布斯自由能:吉布斯自由能是描述系统在恒温、恒压条件下的可用能量,通过最小化吉布斯自由能可以预测系统的平衡态。
这些是热力学基础知识点的概述,它们在热力学的研究和应用中扮演着重要的角色。
热统期末知识点总结
热统期末知识点总结一、热力学基础知识1. 热力学系统:封闭系统、开放系统、孤立系统2. 热力学过程:等容过程、等压过程、等温过程、绝热过程3. 热力学第一定律:能量守恒定律4. 热力学第二定律:热力学不可逆定律5. 热力学第三定律:绝对零度不可达定律二、热力学状态方程1. 理想气体状态方程:PV=nRT2. 绝热方程:PV^γ=常数3. van der Waals方程:(P+a/V^2)(V-b)=RT三、热力学过程1. 等容过程:ΔU=Q,W=02. 等压过程:ΔU=Q-PΔV,W=PΔV3. 等温过程:Q=W,ΔU=04. 绝热过程:Q=0,ΔU=−W四、热力学循环1. 卡诺循环:由等温膨胀、绝热膨胀、等温压缩、绝热压缩四个过程组成的热力学循环2. 卡诺循环效率:η=1- T2/T13. 高效率循环:例如布雷顿循环、热力循环等五、熵和熵增原理1. 熵:系统的无序程度的度量2. 熵增原理:孤立系统的熵不会减少六、热力学定值1. 等温线:PV=常数2. 等容线:P/T=常数3. 等熵线:PV^(γ-1)=常数4. 绝热线:P*V^γ=常数七、不可逆循环1. 单级制冷机和热泵2. 制冷系数和制冷效率3. 制冷系统和热泵系统的效率八、传热1. 传热方式:导热、对流、辐射2. 热传导方程:Q=κAΔT/Δx3. 对流换热方程:Q=mcΔT4. 辐射换热:∈AσT^4九、热力学关系1. 准静态过程:在系统进行状态变化的过程中,系统每一瞬间的参数都可以近似看作平衡的过程2. 等压过程、等容过程、绝热过程的特点及实际应用3. 内能、焓、熵等热力学量的物理意义和计算公式十、热力学定律1. 卡诺定理:卡诺热机效率只与工作物质两个温度有关2. 克劳修斯不等式:任何两个热机无法达到或超过Carnot热机效率3. 热力学循环ΔS=0:卡诺循环4. 有用工作和抽取热5. 充分条件为ΔU=0十一、工程应用1. 蒸汽发动机2. 内燃机3. 空气压缩机总结:热态学是描述热力学性质以及热力学基本定律的一门学科,它研究热力学定态下物质的性质及其变化。
热力学重点知识总结(期末复习必备)
热力学重点知识总结(期末复习必备)热力学重点知识总结 (期末复必备)1. 热力学基本概念- 热力学是研究物质和能量转化关系的科学领域。
- 系统:研究对象,研究所关注的物体或者物质。
- 环境:与系统相互作用的外部世界。
- 边界:系统与环境之间的分界面。
2. 热力学定律第一定律:能量守恒定律- 能量既不会凭空产生,也不会凭空消失,只会在不同形式之间转化。
- $\Delta U = Q - W$,其中 $U$ 表示内能,$Q$ 表示传热量,$W$ 表示对外界做功。
第二定律:热力学箭头定律- 热量不会自发地从低温物体传递到高温物体,而是相反的方向。
- 热量自发地会沿着温度梯度从高温物体传递到低温物体。
- 第二定律的一个重要应用是热机效率计算:$\eta =\frac{W}{Q_H}$,其中 $Q_H$ 表示从高温热源吸收的热量,$W$ 表示对外界做的功。
第三定律:绝对零度定律- 温度无法降低到绝对零度,即 $0$K 是一个温度的下限。
- 第三定律提供了热力学的温标基准,即绝对温标。
3. 热力学过程绝热过程- 绝热过程是指在过程中不与环境发生热量交换的过程。
- 绝热过程中,系统的内能会发生改变,但传热量为零。
等温过程- 等温过程是指在过程中系统与环境保持恒定的温度。
- 在等温过程中,系统的内能不变,但会发生热量交换。
绝热可逆过程- 绝热可逆过程是指绝热过程与可逆过程的结合。
- 在绝热可逆过程中,系统不仅不与环境发生热量交换,还能够在过程中达到热力学平衡。
4. 热力学系统分类封闭系统- 封闭系统是指与环境隔绝,但能够通过物质和能量交换来进行工作的系统。
开放系统- 开放系统是指与环境可以进行物质和能量交换的系统,也称为流体系统。
孤立系统- 孤立系统是指与环境既不进行物质交换,也不进行能量交换的系统。
5. 热力学熵- 熵是热力学中一个重要的物理量,表示系统的无序程度或混乱程度。
- 熵的增加反映了系统的混乱程度的增大,熵的减少反映了系统的有序程度的增大。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
-热力学基础总结
一、热力学第一定律(封闭系统,任何过程)(封闭系统微变过程)
二、热力学第二定律
1、热力学第二定律的数学表达式,Clausius不等式:
> 为不可逆=为可逆
2、熵的定义式
三、状态函数及其关系式
1、状态函数关系式:(定义式)H = U + pV || || G = A + pV + + TS TS
2、热力学的四个基本方程:(适用条件:恒定组成,只作体积功的封闭系统)
3、对应系数关系式:
4、Maxwell关系式:
;;;;
四、各种判据的比较:
判据熵判据(S判据)亥姆霍兹自由能判据(A判据)吉布斯自由能判据(G判据)系统孤立系统封闭系统封闭系统适用条件任何过程恒温恒容且非体积功W’=0恒温恒压且非体积功W’=0自发方向dSsio=dSsys+ dSsur>0<0<0平衡状态dSiso=dSsys+ dSsur=0
五、各种热力学函数的计算公式:
1、体积功的计算(1)、定义式:
(2)、反抗恒定外压过程:
(3)、可逆过程:
(4)、理想气体恒温过程:
(5)、有气体参加的相变过程:体系在恒温恒压下由凝聚相转变为气相(6)、绝热过程:
2、热效应的计算(1)、恒容热:
(封闭系统,恒定W′= 0)(2)、恒压热:
(封闭系统,恒压,)(3)、理想气体恒温可逆过程:
(4)、绝热过程:
3、热力学能的计算(1)、封闭系统,任何过程:
(2)、理想气体恒温过程:=0 (3)、均相物质变温过程:(4)、绝热过程:
4、焓变的计算(1)、封闭系统:
(2)、理想气体恒温过程:=0(3)、均相物质变温过程:(4)、恒压过程:
(5)、可逆相变过程:
(6)、不可逆相变过程设计过程完成。
5、熵变的计算(1)、熵的定义式:
(2)、理想气体的恒温过程:
(3)、恒压变温过程的熵变:
若可视为常数,则(4)、恒容变温过程的熵变:
若可视为常数时,则(5)、理想气体同时改变的过程的熵变:
(6)、绝热可逆过程:,绝热不可逆过程的熵变,设计过程计算。
(7)、理想气体恒温恒压下混合过程的熵变:
(8)、可逆相变过程的熵变:,不可逆相变过程的熵变需设定过程完成。
6、ΔA和ΔG的计算(1)、定义式:
和或:
和(2)、恒温过程:
(3)、理想气体恒温过程:(4)、等熵过程:
(5)、可逆相变过程和的计算:,(6)、不可逆相变过程:设计另一途径,使相变在可逆的条件下进行。
7、理想气体绝热可逆过程方程:适用条件:理想气体;绝热可逆过程;不做非体积功,缺一不可。
六、热力学基本概念
1、热力学性质(广度性质,强度性质)
2、状态及状态函数(定义及特点);
3、热容(定义,恒压热容,恒容热容);
4、热力学能;
5、卡诺循环;
6、热机效率:;理想热机:
7、熵的物理意义;
8、熵增大原理;
9、最小亥姆霍兹自由能原理;
10、最小吉布斯自由能原理;
11、热力学第二定律的表述;。
