有机物C5-C1沸点
有机化合物沸点高低的判断

有机化合物沸点高低的判断有机化合物的沸点高低,这可真是个有趣的话题啊!你知道吗,就好像人有高矮胖瘦之分,有机化合物的沸点也各不相同呢!这其中的奥秘可不少。
先来说说碳原子数吧。
一般情况下,碳原子数越多,沸点往往就越高。
这就好比是一支队伍,人越多,那场面就越大,越不容易散掉。
那些碳原子多的有机化合物,就像是一支庞大的队伍,需要更高的能量才能让它们“解散”,也就是达到沸点。
再看看分子间的作用力。
这就如同人与人之间的关系一样,如果关系紧密,那可就不容易分开啦!有机化合物分子间的作用力越大,沸点也就越高。
比如醇类,它们之间可以形成氢键,就像好朋友紧紧拉着手,所以沸点就相对较高。
还有啊,支链的多少也会影响沸点呢!支链多了,就好像一个人身上挂满了各种零碎,行动起来就没那么顺畅了。
有机化合物也是如此,支链多会让分子变得不那么规整,分子间的接触就没那么紧密了,沸点也就相应降低了。
想想看,烷烃不就是个很好的例子吗?直链烷烃的沸点随着碳原子数增加而升高,但是相同碳原子数的烷烃,支链越多沸点越低。
这不就像是在比较谁更“厉害”一样吗?再比如说芳香烃,苯的沸点就比甲苯低一些,这又是为什么呢?不就是因为甲苯多了个甲基嘛!这小小的一个甲基,却能让沸点发生变化,是不是很神奇呢?有机化合物的世界就是这么奇妙,这么丰富多彩!每一种有机化合物都有它独特的性质和沸点。
我们通过研究它们,可以更好地了解这个世界,更好地利用它们。
所以啊,不要小看这些小小的有机化合物,它们蕴含的奥秘可多着呢!有机化合物沸点高低的判断真的很重要,它能让我们更深入地理解化学反应、物质的性质等等。
我们应该认真去探索,去发现其中的乐趣和价值!。
五氯乙烷_沸点_概述说明以及解释

五氯乙烷沸点概述说明以及解释1. 引言1.1 概述本篇文章旨在探讨五氯乙烷的沸点特性,并对其进行深入的分析和解释。
五氯乙烷是一种常见的有机化合物,其性质和应用领域备受关注。
了解其沸点的测定方法、范围以及影响因素,对于加深我们对五氯乙烷的认识具有重要意义。
1.2 文章结构本文共分为四个部分进行论述,即引言、正文、结果与讨论以及结论。
其中,正文部分介绍了五氯乙烷的性质并阐述了液体沸点与气体沸点的概念;随后详细解析了测定五氯乙烷沸点的方法。
在结果与讨论部分,我们将对五氯乙烷的沸点范围及其影响因素进行解析,并说明不同环境条件下其沸点变化情况。
最后,我们将比较五氯乙烷与其他物质的沸点,并展望它在应用领域中可能发挥的作用。
1.3 目的本文主要目的有三个方面:首先,通过介绍五氯乙烷的性质,使读者对该化合物有一个全面的了解;其次,阐述液体沸点与气体沸点的概念,帮助读者理解五氯乙烷在不同状态下发生相变的原理;最后,探究测定五氯乙烷沸点的方法,并分析其沸点范围及受影响因素,以期为相关实际应用提供指导和有价值的评价。
2. 正文:2.1 五氯乙烷的性质介绍五氯乙烷是一种有机化合物,分子式为C2Cl5H和分子量为201.3 g/mol。
它是无色液体,在常温下具有刺激性气味。
五氯乙烷主要用作工业溶剂和农药成分,具有较高的挥发性和不容易挥发的特点。
2.2 液体沸点与气体沸点的概念液体沸点是指在给定压力下,液体开始转变为气体状态(也称为饱和蒸汽)的温度。
而气体沸点则是指在标准大气压下,液体开始转变为气体状态的温度。
2.3 五氯乙烷的沸点测定方法五氯乙烷的沸点可以通过实验测定来确定。
一个常用的方法是采用常压蒸馏法。
该方法中,将样品加入装有热源的容器中,在恒定压力下进行加热。
当样品温度上升时,在某一温度达到液体与饱和蒸汽平衡时,开始观察到液体汽化,此时该温度即为五氯乙烷的沸点。
此外,还可以使用气相色谱法进行沸点测定。
该方法利用了不同物质在不同温度下的沸点差异,在分析仪器中通过气相色谱柱将五氯乙烷样品加热至其开始挥发的温度,记录并分析挥发物质的特征峰,从而确定沸点。
有机化合物熔点沸点测定

搅拌器 双浴法测熔点
液态样品气化过程示意图
五、实验关键
1、实验操作关键
(1)熔点测定 ①熔点管本身要干净,管壁不能太厚,封口要
均匀、圆滑,不能漏气。 ②样品一定要干燥,并要研成细粉末,往毛细
管内装样品时,一定要反复冲撞致密,管外样品 要用软纸擦干净。
③升温速度不宜太快,开始升温时速度可稍快 些(5℃/min),接近该样品熔点或沸点时,升温速 度要慢(1~2℃/min),应快速、准确读取温度数。
加热纯固体化合物的过程中,有一段时间温度 不变,即固体开始熔化直至固体全部转化为液体时, 此时出现的现象是晶体表面开始湿润,继而样品开 始塌陷且部分透明,当固体全部熔化时即成透明液 体,温度就会迅速上升。要想精确测定熔点,则在 接近熔点时升温的速度不能太快,必须严格控制加 热速度,以每分钟升高1~2℃为宜。
导热液液面应 高于上容
(2)沸点测定装置 烧杯水浴加热
沸点管内液体中心与 温度计球部中心在同一平面
温度计不能与 烧杯底部接触
试样的液面在 浴液液面之下
六、实验结果
1 、熔点测定
实验现象描述:
结论:纯净化合物混有杂质时熔点
,
熔程
。
测定次数
1
初熔 全熔
④第二次测定时,要等浴温冷至其熔点以下约 30℃左右再进行。
(2)沸点测定
①准确判断液体处于沸腾状态时,液态试样的 现象。
②准确观察毛细管口最后一个气泡欲进而出的 状态,及时读数。
③液态样品的沸点必需多次测定,以平均值报 道。
④防止沸点管中试样溶液蒸干,应及时补充。
2、使用实验装置的注意事项 (1)熔点测定装置
纯液体有机化合物在一定的压力下具有确定的沸 点;但具有固定沸点的液体不一定都是纯净的化合物, 当两种或两种以上的物质按一定的组成比形成的混合物 在一定温度下沸腾,这种混合物称为共沸物或恒沸混合 物,如95.6%乙醇+4.4%的水,沸点为78.16℃。
常用有机化合物的物理常数
144.19 1.0989 96
288
折射率
20
nD
在水中
—
02.(冷)
—
3.3(20℃)
1.3714 ∞
1.3288 ∞
1.4214 不溶
1.484 100(17℃) (1.602) ∞(热)
—
0.06(热)
1.42662 不溶
1.4507 溶
1.4641 3.6(20℃)
1.5011 0.07(22℃)
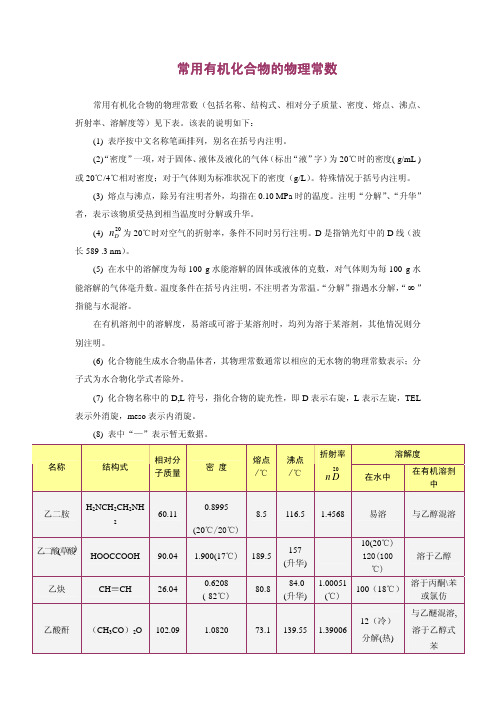
常用有机化合物的物理常数
常用有机化合物的物理常数(包括名称、结构式、相对分子质量、密度、熔点、沸点、
折射率、溶解度等)见下表。该表的说明如下:
(1) 表序按中文名称笔画排列,别名在括号内注明。
(2)“密度”一项,对于固体、液体及液化的气体(标出“液”字)为 20℃时的密度( g/mL )
或 20℃/4℃相对密度;对于气体则为标准状况下的密度(g/L)。特殊情况于括号内注明。
顺式:— 反式 1.203
(162.14)n —
123.11 1.2037
62.50
0.9104
64.52
0.8978
157.02 1.4950
熔点 /℃
123~124
71 68.5 分解 5.7 -153.8 -136.4
-30.82
沸点 /℃
295
— 293 — 210.8 -13.37 12.37
表示外消旋,meso 表示内消旋。
(8) 表中“—”表示暂无数据。
名称
结构式
相对分 子质量
密度
熔点 /℃
沸点 /℃
折射率
20
nD
溶解度
在水中
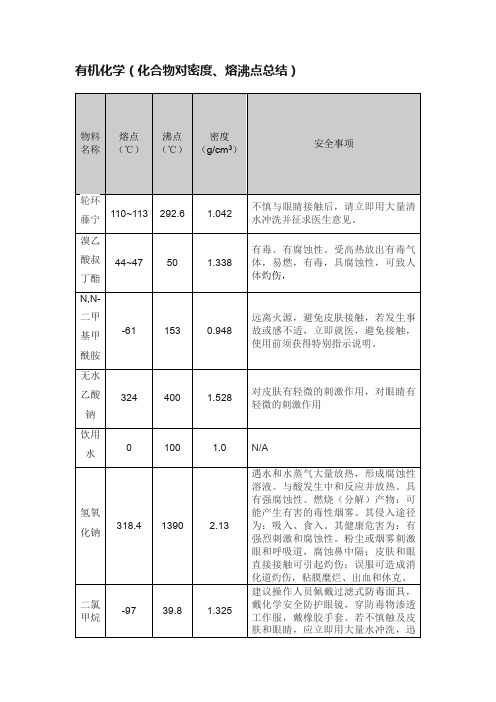
有机化学(化合物对密度、熔沸点总结)
153
0.948
远离火源,避免皮肤接触,若发生事故或感不适,立即就医,避免接触,使用前须获得特别指示说明。
无水乙酸钠
324
400
1.528
对皮肤有轻微的刺激作用,对眼睛有轻微的刺激作用
饮用水
0
100
1.0
N/A
氢氧化钠
318.4
1390
2.13
遇水和水蒸气大量放热,形成腐蚀性溶液。与酸发生中和反应并放热。具有强腐蚀性。燃烧(分解)产物:可能产生有害的毒性烟雾。其侵入途径为:吸入、食入。其健康危害为:有强烈刺激和腐蚀性。粉尘或烟雾刺激眼和呼吸道,腐蚀鼻中隔;皮肤和眼直接接触可引起灼伤;误服可造成消化道灼伤,粘膜糜烂、出血和休克。
有机化学(化合物对密度、熔沸点总结)
物料名称
熔点(℃)
沸点(℃)
密度(g/cm3)
安全事项
轮环藤宁
110~113
292.6
1.042
不慎与眼睛接触后,请立即用大量清水冲洗并征求医生意见。
溴乙酸叔丁酯
44~47
50
1.338
有毒。有腐蚀性。受高热放出有毒气体,易燃,有毒,具腐蚀性,可致人体灼伤,
N,N-二甲基甲酰胺
二氯甲烷
-97
3பைடு நூலகம்.8
1.325
建议操作人员佩戴过滤式防毒面具,戴化学安全防护眼镜,穿防毒物渗透工作服,戴橡胶手套。若不慎触及皮肤和眼睛,应立即用大量水冲洗,迅速就医。
甲基叔丁基醚
-110
55.2
0.74
建议操作人员佩戴过滤式防毒面具,戴化学安全防护眼镜,穿防毒物渗透工作服,戴橡胶手套。若不慎触及皮肤和眼睛,应立即用大量水冲洗,迅速就医。
有机化和物的沸点高低

有机化和物的沸点高低有一定的规律,现总结如下:一、同系物沸点大小判断,一般随着碳原子数增多,沸点增大。
如甲烷<乙烷<丙烷<丁烷<戊烷<.....二、链烃同分异构体沸点大小判断,一般支链越多,沸点越小。
如:正戊烷>异戊烷>新戊烷三、芳香烃的沸点大小判断,侧链相同时,临位>间位>对位。
如:临二甲苯》间二甲苯》对二甲苯四、对于碳原子数相等的烃沸点大小判断,烯烃<烷烃<炔烃五、同碳原子的脂肪烃的衍生物沸点大小判断,烯烃的衍生物沸点低于烷烃的同类衍生物。
如:油酸的沸点<硬脂酸。
六、不同类型的烃的含氧衍生物的沸点比较,相对分子质量相近的脂肪羧酸>脂肪醇>脂肪醛,七、酚和羧酸与它们对应的盐沸点比较,酚和羧酸<对应盐的沸点。
如乙酸<乙酸钠八、分子量相近的烃的沸点一般低于烃的衍生物。
例1、下列沸点大小,前者低,后者高的是().A、苯酚和苯酚钠B、软脂酸和油酸C、丁烯和乙烯D、丁烷和2-甲基丙烷解析:A对,苯酚盐的熔沸点大于苯酚;B错,软脂酸常温固态,油酸常温液态,碳原子相近的高级一元脂肪酸,烃基中C=C越多,沸点越低;C错,同系物中C数越多,沸点越高;D错,同类同分异构体,支链多,沸点低。
答案是A。
点评:本题考查不同情况不同物质之间沸点的大小,考查的范围大,知识跨度大,知识零散,决定沸点高低的因素不同,从理论的角度、平时积累和生活的实践多角度理解,总结规律。
例2、(08年宁夏)下列说法错误的是().A.乙醇和乙酸都是常用调味品的主要成分B.乙醇和乙酸的沸点和熔点都比C2H6、C2H4的沸点和熔点高C.乙醇和乙酸都能发生氧化反应D.乙醇和乙酸之间能发生酯化反应,酯化反应和皂化反应互为逆反应解析:A对,乙醇和乙酸分别是日常生活中料酒和食醋的主要成分;B对,乙醇和乙酸分子极性强,分子之间可以形成氢键,而C2H6、C2H4非极性分子,所以前者熔沸点远远高于后者;C对,氧化反应种类繁多,乙醇和乙酸都能燃烧;D错,皂化反应仅指高级脂肪酸甘油酯在碱性条件下的水解反应,乙酸乙酯在碱性条件下的水解不叫皂化反应。
常用有机无机溶剂的沸点、溶解性和毒性

常用溶剂的沸点、溶解性和毒性溶剂名称沸点(101.3kPa溶解性毒性液氨-33.35℃特殊溶解性:能溶解碱金属和碱土金属剧毒性、腐蚀性液态二氧化硫-10.08溶解胺、醚、醇苯酚、有机酸、芳香烃、溴、二硫化碳,多数饱和烃不溶剧毒甲胺-6.3是多数有机物和无机物的优良溶剂,液态甲胺与水、醚、苯、丙酮、低级醇混溶,其盐酸盐易溶于水,不溶于醇、醚、酮、氯仿、乙酸乙酯中等毒性,易燃二甲胺7.4是有机物和无机物的优良溶剂,溶于水、低级醇、醚、低极性溶剂强烈刺激性石油醚不溶于水,与丙酮、乙醚、乙酸乙酯、苯、氯仿及甲醇以上高级醇混溶与低级烷相似乙醚34.6微溶于水,易溶与盐酸.与醇、醚、石油醚、苯、氯仿等多数有机溶剂混溶麻醉性戊烷36.1与乙醇、乙醚等多数有机溶剂混溶低毒性二氯甲烷39.75与醇、醚、氯仿、苯、二硫化碳等有机溶剂混溶低毒,麻醉性强二硫化碳46.23微溶与水,与多种有机溶剂混溶麻醉性,强刺激性溶剂石油脑与乙醇、丙酮、戊醇混溶较其他石油系溶剂大丙酮56.12与水、醇、醚、烃混溶低毒,类乙醇,但较大1,1-二氯乙烷57.28与醇、醚等大多数有机溶剂混溶低毒、局部刺激性氯仿61.15与乙醇、乙醚、石油醚、卤代烃、四氯化碳、二硫化碳等混溶中等毒性,强麻醉性甲醇64.5与水、乙醚、醇、酯、卤代烃、苯、酮混溶中等毒性,麻醉性,四氢呋喃 THF66优良溶剂,与水混溶,很好的溶解乙醇、乙醚、脂肪烃、芳香烃、氯化烃吸入微毒,经口低毒1,4-二氧六环101.32能与水及多数有机溶剂混溶,仍溶解能力很强微毒,强于乙醚2~3倍己烷68.7甲醇部分溶解,比乙醇高的醇、醚丙酮、氯仿混溶低毒。
麻醉性,刺激性三氟代乙酸71.78与水,乙醇,乙醚,丙酮,苯,四氯化碳,己烷混溶,溶解多种脂肪族,芳香族化合物1,1,1-三氯乙烷74与丙酮、、甲醇、乙醚、苯、四氯化碳等有机溶剂混溶低毒类溶剂四氯化碳76.75与醇、醚、石油醚、石油脑、冰醋酸、二硫化碳、氯代烃混溶氯代甲烷中,毒性最强乙酸乙酯77.112与醇、醚、氯仿、丙酮、苯等大多数有机溶剂溶解,能溶解某些金属盐低毒,麻醉性乙醇78.3与水、乙醚、氯仿、酯、烃类衍生物等有机溶剂混溶微毒类,麻醉性丁酮79.64与丙酮相似,与醇、醚、苯等大多数有机溶剂混溶低毒,毒性强于丙酮苯80.1难溶于水,与甘油、乙二醇、乙醇、氯仿、乙醚、、四氯化碳、二硫化碳、丙酮、甲苯、二甲苯、冰醋酸、脂肪烃等大多有机物混溶强烈毒性环己烷80.72与乙醇、高级醇、醚、丙酮、烃、氯代烃、高级脂肪酸、胺类混溶低毒,中枢抑制作用乙睛81.6与水、甲醇、乙酸甲酯、乙酸乙酯、丙酮、醚、氯仿、四氯化碳、氯乙烯及各种不饱和烃混溶,但是不与饱和烃混溶中等毒性,大量吸入蒸气,引起急性中毒异丙醇82.4与乙醇、乙醚、氯仿、水混溶微毒,类似乙醇1,2-二氯乙烷83.48与乙醇、乙醚、氯仿、四氯化碳等多种有机溶剂混溶高毒性、致癌乙二醇二甲醚85.2溶于水,与醇、醚、酮、酯、烃、氯代烃等多种有机溶剂混溶。
化合物的物理性质

化合物的物理性质《烷烃的物理性质》一. 物质的状态室温下,C1-C4为气体,C5-C16为液体,C17以上是固体。
二.熔点和沸点烷烃的熔点和沸点都很低,并且熔点和沸点随分子量的增加而升高。
但值得注意的是:(1)对同数碳原子的烷烃来说,结构对称的分子熔点高。
因为结构对称的分子在固体晶格中可紧密排列,分子间的色散力作用较大,因而使之熔融就必须提供较多的能量。
(2)含偶数碳原子的正烷烃比奇数碳原子的熔点高。
这主要取决于晶体中碳链的空间排布情况。
X光证明,固体正烷烃的碳链在晶体中伸长为锯齿形,奇数碳原子的链中两端的甲基处在同一边,而偶数碳原子的链中,两端的甲基处在相反的位置,从而使这种碳链比奇数碳链的烷烃可以彼此更为靠近,于是它们之间的色散力就大些。
烷烃的沸点上升比较有规则,每增加一个CH2基,上升20-30℃,越到高级系列上升越慢。
在相同碳原子数的烷烃中,直链的沸点比带支链的高,这是由于在液态下,直链的烃分子易于相互接近,而有侧链的烃分子空间阻碍较大,不易靠近。
三. 比重、溶解度、折光率(略)环烷烃的物理性质在常温常压下环丙烷及环丁烷为气体,环戊烷为液体,高级环烷烃为固体。
环烷烃的熔点较同数碳原子的直链烷烃高,因为环烷烃比直链烷烃在晶格中排列更紧密。
环烷烃的密度为0.688~0.853g•c m-3 。
环烷烃不溶于水。
一些环烷烃的熔点和沸点见表3-2。
表3.2 环烷烃的熔点、沸点、张力能(kJ·mol-1)和每一个-CH2-单元的燃烧热(kJ·mol-1 )《芳烃的物理性质》苯及其同系物大多为液体,故有特殊的香气,但它们的蒸气有毒。
高浓度的苯蒸气作用于中枢神经,引起急性中毒。
长期接触低浓度的苯蒸气能损害造血器官。
因此,应尽量注意少接触苯。
有时可以用甲苯代替苯作溶剂,因少量甲苯在人体中可以与甘氨酸作用被人体中酶催化形成马尿酸(C6H5CONHCH2CO2H)而排出体外,故甲苯毒性相对较小。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
C=C=C
沸点 -161.49℃ -88.63℃ -42.07℃
-0.5℃
备注
-11.73℃ 30.074℃
烷烃
27.852℃
9.503
-32.8℃
12.51℃ 环烷烃
49.262℃
-103.71℃ -47.70℃
-34.5℃
C=C-C-C
-6.26℃
15
顺丁烯
16
反丁烯
17
异丁烯
C C=C-C=C
30 3-甲基-1,2-丁二烯
C C-C=C=C
31
反-戊二烯
H C=C C=C
CH
48.26℃ 34.07℃ 40.85℃ 68.119℃
32
顺-戊二烯
C C=C C=C
HH
44.07℃
1、对于炔烃、C=C=C类化合物化学性质极活泼,炼油行业一般不产生。 2、环烷烃而言,只有五元环、六元环较稳定,易存在。 3、C=C-C=C(丁二烯)一般富产于大乙烯装置,催化、焦化一般不产生。 4、正构烷烃沸点随C数增加而增加,但支链增加,沸点降低。
18
1,2丁二烯
19
1,3丁二烯
20
正戊烯
21
顺二戊烯
22
反二戊烯
23
2-甲基-1-丁烯
24
2-甲基-2-丁烯
25
3-甲基-1-丁烯
CC C=C
HH
HC C=C
CH
C C=C-C
C=C=C-C C=C-C=C C=C-C-C-C
C CC=C
HH
H CC=C
CH
C C=C-C-C
C C-C=C-C
C C-C-C=C
序号 1 2 3
5 6 6
7
化合物 甲烷 乙烷 丙烷
正丁烷
异丁烷
正戊烷 异戊烷
新戊烷
8
环丙烷
9
环丁烷
10
环戊烷
11
乙烯
12
丙烯
13
丙二烯
14
正丁烯
结构简式 CH4 C-C
C-C-C C-C-C-C
C C-C-
C-C-C-C-C
C C-C-C-C
C C-C-C
C
C C-C
C-C C-C C CC C-C
3.72℃
0.88℃
-6.9℃ 10.85℃ -4.5℃ 29.968℃ 36.942℃
36.353℃
31.163℃
烯烃
38.568℃
20.061℃
26
1,2-戊二烯
C=C=C-C-C
44.85℃
27
1,4-戊二烯
C=C-C-C=C
25.90℃
28
2,3-戊二烯
C-C=C=C-C
29 2-甲基-1,3-丁二烯
