原子核外电子排布的规律练习题
原子的核外电子排布和结构示意图及其强化练习
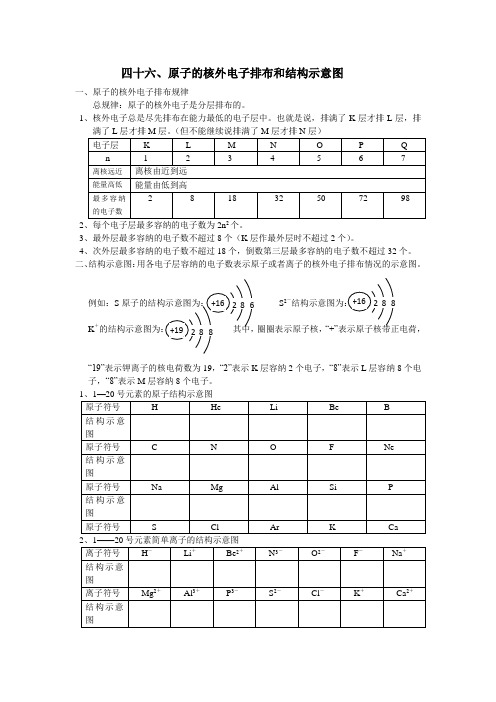
四十六、原子的核外电子排布和结构示意图一、原子的核外电子排布规律总规律:原子的核外电子是分层排布的。
1、核外电子总是尽先排布在能力最低的电子层中。
也就是说,排满了K 层才排L 层,排满了L 层才排M 层。
(但不能继续说排满了M 层才排N 层)2、每个电子层最多容纳的电子数为2n 个。
3、最外层最多容纳的电子数不超过8个(K 层作最外层时不超过2个)。
4、次外层最多容纳的电子数不超过18个,倒数第三层最多容纳的电子数不超过32个。
二、结构示意图:用各电子层容纳的电子数表示原子或者离子的核外电子排布情况的示意图。
例如:SS 2-K +“+”“19”表示钾离子的核电荷数为19,“2”表示K 层容纳2个电子,“8”表示L 层容纳8个电子,“8”表示M 层容纳8个电子。
3、具有2电子的微粒:He, Li+, Be2+, H2具有10电子的微粒:Ne、N3-、O2-、F-、Na+、Mg2+、Al3+、CH4、NH3、H2O、HF、H3O+、NH4+、OH-、NH2-、具有18电子的微粒:、Ar、P3-、S2-、Cl-、K+、Ca2+、SiH4、PH3、H2S、HCl、C2H6、N2H4、H2O2、F2、HS-、O22-、三、强化练习1、某主族元素的原子有5个电子层,最外层只有1个电子,下列描述中正确的是()A、其单质常温下跟水反应不如钠剧烈B、其原子半径比钾原子半径小C、其碳酸盐易溶于水D、其氢氧化物不能使氢氧化铝溶解2、下列四种元素中,其单质氧化性最强的是()A、原子含有最外层电子数最多的第二周期元素B、位于周期表中第三周期ⅢA族的元素C的元素D、原子结构示意图为的元素3、氢化钠(NaH)+1价,NaH与水反应放出氢气。
下列叙述中,正确的是()A、NaH在水中显酸性B、NaH中氢负离子的电子层排布与氦原子的相同C、NaH中氢负离子半径比锂离子半径小D、NaH中氢负离子可被还原成氢气4、用R代表短周期元素,R原子最外层的电子数是最内层电子数的2倍。
高中化学人教版必修2-原子核外电子排布习题附解析

原子核外电子排布一、选择题1.下列叙述正确的是()A.电子的能量越低,运动区域离核越远B.核外电子的分层排布即是核外电子的分层运动C.稀有气体元素原子的最外层都排有8个电子D.当M层是最外层时,最多可排布18个电子答案 B解析电子的能量越低,离核越近,故A错;He原子最外层只有2个电子,故C错;原子最外层电子数不能超过8个,故D错。
2.下列化学符号表示正确的是()A.中子数为6的碳原子符号:66CB.中子数为22的钙离子符号:4220Ca2+C.氟离子的结构示意图:D.干冰的化学式:H2O答案 B解析中子数为6的C原子质量数为12,故其符号为126C,故A错;中子数为22的Ca2+的质量数为42,故其符号为4220Ca2+,故B正确;氟离子的结构示意图:,故C 错;干冰的化学式为CO2,故D错。
3.已知最外层电子数相等的元素的原子具有相似的化学性质。
氧元素原子的核外电子分层排布示意图为,下列原子中,与氧元素原子化学性质相似的是()答案 D解析由核外电子分层排布示意图可知:氧元素原子最外层电子数为6,氖元素原子最外层电子数为8,碳元素原子最外层电子数为4,镁元素原子最外层电子数为2,硫元素原子最外层电子数为6;根据最外层电子数相等的元素原子化学性质相似,可知与氧元素原子化学性质相似的是硫。
4.[2015·太原高一检测]下列叙述正确的是()A.核外电子排布完全相同的两种粒子的化学性质一定相同B.单原子形成的离子一定具有稀有气体元素原子的核外电子排布C.核外电子排布相同的两种原子一定属于同种元素D.可能存在质子数和电子数都相同的阳离子和阴离子答案 C解析1H、2H化学性质相同,而O2-、Na+虽核外电子排布完全相同,但其化学性质不同,A项错误;H+核外电子数是0,B项错误;核外电子排布相同的不同原子必定是同位素关系,C项正确;如果阴、阳离子的电子数相同,则其质子数必定不同,反之亦然,D项错误。
1.2.1原子核外电子的排布课后作业2

原子核外电子的排布一、选择题1.下列叙述中,正确的是()A.在多电子的原子里,能量高的电子通常在离核近的区域内运动B.核外电子总是先排在能量低的电子层上,例如只有排满了M层后才排N层C.某原子M层上电子数为L层电子数的4倍D.某离子的核电荷数与最外层电子数相等2.关于原子结构的叙述正确的是()A.所有的原子核都是由质子和中子构成的B.原子的最外层电子数不超过8C.稀有气体原子的最外层电子数均为8D.原子的次外层电子数都是83.下列各原子结构示意图中所表示的核外电子排布正确的是()4.已知W粒子的结构示意图为,下列关于它的说法不正确的是()A.y=2B.若x=18,则z=8C.若x=14,则其氢化物的化学式为H2WD.若x=17,则其最高价氧化物的化学式为W2O75.下列说法中,肯定错误的是()A.某原子K层上只有1个电子B.某原子M层上电子数为L层上电子数的4倍C.某离子M层上和L层上的电子数均为K层的4倍D.某原子的核电荷数与最外层电子数相等6.下列化学符号表示同一种元素的是()①3517X②3717X③④A.①③B.①②③C.②③D.①②③④7.已知最外层电子数相同的原子具有相似的化学性质。
氧原子的核外电子分层排布示意图为,下列原子中,与氧原子化学性质相似的是()8.下列叙述中,正确的是()A.核外电子排布完全相同的两种微粒,其化学性质一定相同B.凡单原子形成的离子,一定具有稀有气体元素原子的核外电子排布C.核外电子排布相同的两原子一定属于同种元素D.任一阴离子的核外电子排布一定与其上一周期稀有气体元素原子的核外电子排布相同9.某短周期元素的原子最外层电子数是次外层电子数的3倍,那么该原子()A.有3个电子层B.有2个电子层C.最外层电子数是8D.核电荷数是1010.下列说法中,正确的是()A.原子最外层电子少于3个的元素均是金属元素B.原子核外能量越低的电子离核越远,能量越高的电子离核越近C.两个简单微粒的电子层排布完全相同,则它们一定是同一种元素D.在短周期元素中,原子最外层电子数等于电子层数的元素是H、Be、Al11.已知元素X、Y的核电荷数分别是a和b,它们的离子X m+和Y n-的核外电子排布相同,则下列关系式中正确的是()A.a=b+m+nB.a=b-m+nC.a=b+m-nD.a=b-m-n12.短周期元素A和B,其中A元素的原子最外层电子数是a,次外层电子数是b;B元素的原子M层电子数是(a-b),L层电子数是(a+b),则A、B两种元素形成的化合物的化学式可能表示为()A.B3A2B.AB2C.A3B2D.BA213.短周期元素中,A元素原子最外层电子数是次外层电子数的2倍;B元素原子最外层电子数是其内层电子总数的3倍;C元素原子M层电子数等于其L层电子数的一半;D 元素原子最外层有1个电子,D的阳离子与B的阴离子电子层结构相同,则这4种元素原子序数关系中正确的是()A.C>D>B>AB.D>B>A>CC.A>D>C>BD.B>A>C>D二、非选择题14.根据下列A、B、C、D、E五种粒子(原子或离子)的结构示意图,回答有关问题:(1)五种粒子中,属于原子的是________,属于离子的是_________。
化学 原子结构 核外电子排布练习答案以及解析

原子结构 核外电子排布练习答案以及解析1答案及解析:答案:B解析:真题探源:教材P31:用A Z X 表示原子组成[质量数()A =质子数() Z +中子数()N ];教材P29:原子(离子)的结构示意图。
思路点拨:A 项中,原子符号中, A 表示质量数,该氧原子为188O ,C 项中, 2S -的核外电子数为8,该示意图表示硫原子核外电子排布;D 项中,“2Na S ”由阴、阳离子组成,不存在2Na S 分子。
2答案及解析:答案:D解析:A.元素符号左下角表示的是原子核内的质子数,原子核内的质子数等于该元素的原子序数,所以该元素的原子序数是116,正确。
B.在原子符号的左上角表示的该元素原子的质量数,质量数就是质子数与中子数的和,所以该原子的中子数是293116177-=,正确。
C.对于元素的原子来说,原子核内的质子数等于原子核外的电子数,等于元素的原子序数,所以该原子的原子核外电子数116,正确。
D.293只表示该同位素原子的质量数,由于不知道该元素有几种同位素原子,各种同位素原子的含量是多少,因此不能确定该元素的相对原子质量,错误。
3答案及解析:答案:B解析:A 项,中子数=质量数-质子数,它们的质子数均为83,质量数分别为209和210,故它们的中子数分别为126和127, A 项错误,D 项错误;B 项,二者的质子数相同,质量数不同,它们互为同位素,B 项正确;C 项,二者的核外电子数均为83,C 项错误。
4答案及解析:答案:A解析:5答案及解析:答案:C解析:由离子所带的电荷可知, 231molRO -中核外电子的物质的量比质子的物质的量多2mol,由题意可知, 234gRO -中核外电子的物质的量比质子的物质的量多0.1mol,故231molRO -的质量为24200.1mol g g mol⨯=,则23RO -的相对原子质量=R 的相对原子质量+3x16=80,则R 的相对原子质量为32。
人教版化学必修二第一章第二节原子核外电子的排布练习含参考答案

原子核外电子的排布周末作业1.下列关于原子核外电子排布规律的说法错误的是( )A. K层是能量最低的电子层B.原子失电子时先失去能量低的电子C.核外电子总是优先排布在能量较低的电子层上D. N层为次外层时,最多可容纳的电子数为182.下列叙述不正确的是( )A.在多电子原子里,核外电子的能量不同B.原子核外的电子按其能量不同分层排布C.电子的能量越低,运动区域离核越远D. M层电子的能量大于L层电子的能量3.排布在下列各电子层上的一个电子,所具有的能量最低的是( )A. K层B. L层C. M层D. N层4.核电荷数为16的元素和核电荷数为4的元素的原子相比较,前者下列数据是后者4倍的是( )①电子数 ②最外层电子数 ③电子层数 ④次外层电子数A.①④B.①③④C.①②④D.①②③④5.关于原子核外电子排布的下列叙述正确的是( )A.原子核外电子的能量按K、L、M、N电子层的顺序依次减小B.原子核外次外层电子数不超过18个,倒数第三层不超过32个C.某原子的K电子层为最外层,该电子层最多可容纳8个电子D.某原子核外有三个电子层,其L层为次外层,最多可容纳18个电子6.某元素原子的核电荷数是电子层数的五倍,其质子数是最外层电子数的三倍,该元素的原子核外电子排布是( )A. 2、5 B. 2、7C. 2、8、5D. 2、8、77.下列微粒的结构示意图,正确的是( )A. Mg2+:B. Cl:C. Ar:D. K:8.某化合物XY2的Y-的粒子示意图可能是( )A.B.C.D.9.某元素的核外有三个电子层,其最外层电子数是次外层电子数的一半,则此元素是( ) A.硫B.碳C.硅 D.氯10.下列叙述中不正确的是( )A. K层电子数为奇数的所有主族元素所在族的序数与该元素原子的K层电子数相等B. L层电子数为奇数的所有主族元素所在族的序数与该元素原子的L层电子数相等C. L层电子数为偶数的所有主族元素所在族的序数与该元素原子的L层电子数相等D.M层电子数为奇数的所有主族元素所在族的序数与该元素原子的M层电子数相等11.某元素原子的最外层电子数为次外层电子数的3倍,则该元素原子核内质子数为( ) A. 3 B. 7 C. 8 D. 1012.下列各微粒:①H3O+、NH、Na+;②OH-、NH、F-;③O、Na+、Mg2+;④CH4、NH3、H2O具有相同质子数和相同电子数的一组是( )A.①②③B.①②④C.②③④D.①③④13.核外电子层结构相同的一组粒子是( )A.Mg2+、Al3+、Cl-、NeB.Na+、F-、S2-、ArC.K+、Ca2+、S2-、ArD.Mg2+、Na+、Cl-、S2-14.根据1~20号元素原子的核外电子排布的特点,确定元素的种类。
第2讲 原子核外电子排布的规律练习题

第二讲原子核外电子的排布规律练习题一、核外电子的排布规律在含有多个电子的原子里,电子的能量并不相同,能量低的电子通常在离核近的区域运动,能量高的电子通常在离核远的区域运动。
我们常用电子层来表明。
离核最近的叫第一层,离核稍远的叫第二层,依次类推,由近及远叫三、四、五、六、七层,也可依次把它们叫做K、L、M、N、O、P、Q层。
核外电子的分层运动,又叫核外电子的分层排布。
如图。
科学研究证明,电子一般总是尽先排布在能量最低的电子层里,即最先排布K层,当K层排满后,再排布L层,依次类推。
1-20号元素原子的电子层排布核电荷数元素名称元素符号各电子层的电子数核电荷数元素名称元素符号各电子层的电子数K L M N K L M N12345678910氢氦锂铍硼碳氮氧氟氖HHeLiBeBCNOFNe122 12 22 32 42 52 62 72 811121314151617181920钠镁铝硅磷硫氯氩钾钙NaMgAlSiPSClArKCa2 8 12 8 22 8 32 8 42 8 52 8 62 8 72 8 82 8 8 12 8 8 2核外电子排布的一般规律是:①各电子层最多容纳的电子数目是2n2;②最外层电子数目不超过8个(K层为最外层时不超过2个),次外层电子数目不超过18个,倒数第三层电子数目不超过32个;③核外电子总是尽先排布在能量最低的电子层里,然后再由里往外依次排布在能量逐步升高的电子层里。
1-18号元素的原子结构示意图。
1.结构示意图(原子、离子)2.电子式(原子、离子)[课堂练习]写出下列微粒的结构示意图和电子式:结构示意图:Na+;Cl-;Ar ;K+;N ;O 电子式:S2-;K+;S;P ;He 。
练习一、选择题1.以下说法正确的是()A.原子是最小的粒子B.所有粒子都带中子C.原子呈电中性,所以原子不含电荷D.原子质量主要集中在原子核上2.下列说法中不正确的是()A.原子中电子在核外运动没有确定的轨道B.电子云中小黑点的疏密表示电子在核外某处出现机会的多少C.离原子核越近的电子越不容易失去D.在原子中,除最外层电子层,每层上的电子数必符合2n2个3.下列各关系式中,正确的是()A.中性原子中:核外电子数=核内中子数B.中性原子中:核内质子数=核外电子数C.在R2-中:电子数=核内质子数-2D.在R2+中:电子数=核内质子数+24.在构成原子的各种微粒中,决定原子种类的是()A.质子数 B.中子数 C.质子数和中子数 D.核外电子数5. M层有2个价电子的元素A和L层有5个价电子的元素B,组成稳定的化合物,该化合物的式量为()A.88 B.40 C.100 D.726.有X和Y两种元素,且X3-和Y n+的电子数相等,若X的核电荷数为z,则Y的核电荷数为()A.z-n-3B.z-n+3C.z+n+3D.z+n-37.下列粒子结构示意图正确的是()3+-D.Na8.某元素原子L层电子数比K层电子数多5个,该元素的最高正化合价为()A.+5 B.+6 C.+7 D.无最高正化合价9.下列各组粒子中,具有相同核外电子排布的是()A.F-,ArB.Ca2+,AlC.K+,S2-D.Mg2+,Cl+10.若a A n+和b B2-两种离子的核外电子层结构相同,则a等于()A.b+n+2B.b+n-2C.b-n-2D.b-n+211.与Ar的核外电子排布相同的离子,跟与Ne的核外电子排布相同的离子,所形成的化合物是A.CaF2B.HClC.Na2OD.H2O12.有X和Y两种元素,且X3-和Y n+的电子数相等,若X的核电荷数为z,则Y的核电荷数为()A.z-n-3B.z-n+3C.z+n+3D.z+n-313.今有A、B、C三种元素,A、C元素原子的最外层电子数分别是6、2,B元素原子最外层电子数是内层电子数的2倍,A原子比B原子多一个电子层,C原子比B原子少一个电子层,这三种元素分别是()A.S Si Be B.O C Mg C.O Si Ca D.S C He14.几种微粒具有相同的核电荷数,则可说明( )A.可能属于同一种元素B.一定是同一种元素C.彼此之间一定是同位素D.核外电子个数一定相等15.已知R2+离子核外有a个电子,b个中子,表示R原子符号正确的是()A.ba R B.22-+-baaRC.22+++baaR D.baa+-2R16.下列说法中错误的是()A.质量数相同的原子,其化学性质一定相同B.质子数相同的微粒,其核外电子排布也相同C.金属性越活泼,其原子在反应中越易失去电子D.非金属性越活泼,其阴离子越难失去电子17.在核电荷数为1—20元素的原子中,次外层电子数为最外层电子数2倍的元素是( ) A.核电荷数为3的元素B.核电荷数为14的元素C.核电荷数为6的元素D.核电荷数为16的元素18.某离子的原子核里有n个质子,该离子的电子层排布与氖原子相同,则它所带的电荷数可能是()A.n-10 B.10-n C.n+10 D.n/1019.元素X的原子核外M电子层有3个电子,元素Y2-离子核外共有18个电子,则这两种元素可形成的化合物为( )A.XY2B.X2Y C.X2Y3D.X3Y220.下列叙述中,正确的是()A.两种微粒,若核外电子排布完全相同,则其化学性质一定相同B.凡单原子形成的离子,一定具有稀有气体元素原子的核外电子排布C.两原子,如果核外电子排布相同,则一定属于同种元素D.阴离子的核外电子排布一定与上周期稀有气体元素原子的核外电子排布相同二、填空题19X在其化合物中,最高正价为,负价为。
物质结构与性质一有关核外电子排布规律综合考点训练

2023届高三化学高考备考二轮复习物质结构与性质一有关核外电子排布规律综合考点训练一、单选题1.具有下列电子层结构的原子成离子,其对应元素一定属于同一周期的是A.两原子核外全部都是s电子B.3p能级上只有一个空轨道的原子和3p能级上只有一个未成对电子的原子C.原子核外M层上的s、p能级都充满电子,而3d能级上没有电子的两种原子D.最外层电子排布为263s3p的原子和最外层电子排布为263s3p的离子2.“21世纪是钛的世纪”,钛是一种性能非常优越的金属,在能源、航天、医疗等方面有重要应用。
已知钛原子序数为22,位于第四周期,最外层有2个电子。
则其次外层电子数为A.2B.8C.10D.183.下列说法正确的是A.原子核外各电子层最多能容纳的电子数为n2B.同一主族中,第三周期和第四周期元素原子的核电荷数都相差8C.位于第四周期第IV A族的元素为金属元素D.门捷列夫在1869年提出了元素的性质随着原子序数的递增而呈周期性变化的规律4.一般情况下,前者无法决定后者的是A.原子核外电子排布——元素在周期表中的位置B.弱电解质的相对强弱——相同温度、相同浓度下电离度的大小C.分子间作用力的大小——分子稳定性的高低D.物质内部储存的能量高低——化学反应的热效应5.下列有关原子核外电子的说法错误的是A.每个电子层作为最外层时,最多可容纳8个电子B.电子在核外是分层排布的C.电子不停地做高速运动D.离原子核近的电子能量低,离原子核远的电子能量高6.下列说法中正确的是A.某微粒核外电子排布为2、8、8结构,则该微粒一定氩原子B.最外层电子达到稳定结构的微粒只能是稀有气体的原子C.F-、Na+、A13+是与Ne原子具有相同电子层结构的离子D .某元素原子的最外层只有2个电子,则该元素一定是金属元素7.下列说法正确的是A .最外层有2个电子的原子都是金属原子B .同一周期元素的原子,半径越小越容易失去电子C .同一主族的元素的氢化物,相对分子质量越大,它的沸点一定越高D .非金属元素呈现的最高化合价不超过该元素原子的最外层电子数8.已知:34Se (硒)与S 为同族元素。
高中化学 《原子核外电子的排布》同步练习

现吨市安达阳光实验学校原子核外电子的排布1.(高考卷) 是常规核裂变产物之一,可以通过测大气或水中的含量变化来监测核电站是否发生放射性物质泄漏。
下列有关131 53I的叙述中错误的是( )A .的化学性质与相同B .的原子序数为53C .的原子核外电子数为78D .的原子核内中子数多于质子数解析:选C 。
与互为同位素,二者的化学性质相同;的原子序数为53,原于核外电子数为53,中子数为131-53=78,则的原子核内中子数多于质子数。
2.核电荷数小于或于18的元素中,原子的最外层电子数是其余电子总数一半的元素种类有( )A.1种B.2种C.3种D.4种解析:选B。
在1~18号元素中,符合题给要求的元素原子的电子排布依次为2、1和2、8、5。
3.(高一质检)原子核外每个电子层上均含有2n2个电子的元素是( ) A.Be B.CC.Ar D.Ne解析:选D。
原子核外每个电子层上均含有2n2个电子的元素必须具备每层电子排布:K层2个,L层8个,当有3个电子层时,电子数为18>8(原子的最外层电子数不超过8个),所以只有Ne符合要求。
4.某粒子结构示意图为,若该粒子为离子,则它所带的电荷数可能为( )①8-n②n-8 ③10-n④n-10A.①② B.①③C.③④ D.②④解析:选C。
若该微粒为阳离子,其所带电荷数为n-10,若为阴离子,其所带电荷数为10-n。
5.已知A元素原子的核电荷数大于B元素原子的核电荷数,但两种元素的原子具有相同数目的电子层,A元素原子最外层电子数为B元素的两倍,A元素原子M层电子数为K层电子数的3倍,C元素原子的核电荷数是电子层数的4倍,其质子数为最外层电子数的6倍。
请完成下列空白:(1)A的原子结构示意图为________;A元素的名称为________。
(2)B的原子结构示意图为________;B元素的名称为________。
(3)C的离子结构示意图为________;C元素的名称为________。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
第二讲原子核外电子的排布规律练习题
一、核外电子的排布规律
在含有多个电子的原子里,电子的能量并不相同,能量低的电子通常在离核近的区域运动,能量高的电子通常在离核远的区域运动。
我们常用电子层来表明。
离核最近的叫第一层,离核稍远的叫第二层,依次类推,由近及远叫三、四、五、六、七层,也可依次把它们叫做K、L、M、N、O、P、Q层。
核外电子的分层运动,又叫核外电子的分层排布。
如图。
科学研究证明,电子一般总是尽先排布在能量最低的电子层里,即最先排布K层,当K层排满后,再排布L层,依次类推。
核外电子排布的一般规律是:①各电子层最多容纳的电子数目是2n2;②最外层电子数目不超过8个(K层为最外层时不超过2个),次外层电子数目不超过18个,倒数第三层电子数目不超过32个;③核外电子总是尽先排布在能量最低的电子层里,然后再由里往外依次排布在能量逐步升高的电子层里。
1-18号元素的原子结构示意图。
1.结构示意图(原子、离子)
2.电子式(原子、离子)
[课堂练习]写出下列微粒的结构示意图和电子式:
结构示意图:Na+;Cl-;Ar ;K+;N ;O 电子式:S2-;K+;S;P ;He 。
练习
一、选择题
1.以下说法正确的是()
A.原子是最小的粒子
B.所有粒子都带中子
C.原子呈电中性,所以原子不含电荷
D.原子质量主要集中在原子核上
2.下列说法中不正确的是()
A.原子中电子在核外运动没有确定的轨道
B.电子云中小黑点的疏密表示电子在核外某处出现机会的多少
C.离原子核越近的电子越不容易失去
D.在原子中,除最外层电子层,每层上的电子数必符合2n2个
3.下列各关系式中,正确的是()
A.中性原子中:核外电子数=核内中子数
B.中性原子中:核内质子数=核外电子数
C.在R2-中:电子数=核内质子数-2
D.在R2+中:电子数=核内质子数+2
4.在构成原子的各种微粒中,决定原子种类的是()
A.质子数 B.中子数 C.质子数和中子数 D.核外电子数
5. M层有2个价电子的元素A和L层有5个价电子的元素B,组成稳定的化合物,该化合物的式量为()
A.88 B.40 C.100 D.72
6.有X和Y两种元素,且X3-和Y n+的电子数相等,若X的核电荷数为z,则Y的核电荷数为()
A.z-n-3
B.z-n+3
C.z+n+3
D.z+n-3
7.下列粒子结构示意图正确的是()
3+
-
D.Na
8.K
A.B.+6
9.
A.F-,Ar
B.Ca2+,Al
C.K+,S2-
D.Mg2+,Cl+
10.若a A n+和b B2-两种离子的核外电子层结构相同,则a等于()
A.b+n+2
B.b+n-2
C.b-n-2
D.b-n+2
11.与Ar的核外电子排布相同的离子,跟与Ne的核外电子排布相同的离子,所形成的化合物是
A.CaF2
B.HCl
C.Na2O
D.H2O
12.有X和Y两种元素,且X3-和Y n+的电子数相等,若X的核电荷数为z,则Y的核电荷数为()
A.z-n-3
B.z-n+3
C.z+n+3
D.z+n-3
13.今有A、B、C三种元素,A、C元素原子的最外层电子数分别是6、2,B元素原子最外层
电子数是内层电子数的2倍,A原子比B原子多一个电子层,C原子比B原子少一个电子层,这三种元素分别是()
A.S Si Be B.O C Mg C.O Si Ca D.S C He
14.几种微粒具有相同的核电荷数,则可说明( )
A.可能属于同一种元素B.一定是同一种元素
C.彼此之间一定是同位素D.核外电子个数一定相等
15.已知R2+离子核外有a个电子,b个中子,表示R原子符号正确的是()
A.b
a R B.2
2
-
+
-
b
a
a
RC.2
2
+
+
+
b
a
a
R D.b
a
a
+
-2
R
16.下列说法中错误的是()
A.质量数相同的原子,其化学性质一定相同
B.质子数相同的微粒,其核外电子排布也相同
C.金属性越活泼,其原子在反应中越易失去电子
D.非金属性越活泼,其阴离子越难失去电子
17.在核电荷数为1—20元素的原子中,次外层电子数为最外层电子数2倍的元素是( ) A.核电荷数为3的元素B.核电荷数为14的元素
C.核电荷数为6的元素D.核电荷数为16的元素
18.某离子的原子核里有n个质子,该离子的电子层排布与氖原子相同,则它所带的电荷数可能是()
A.n-10 B.10-n C.n+10 D.n/10
19.元素X的原子核外M电子层有3个电子,元素Y2-离子核外共有18个电子,则这两种元素可形成的化合物为( )
A.XY2B.X2Y C.X2Y3D.X3Y2
20.下列叙述中,正确的是()
A.两种微粒,若核外电子排布完全相同,则其化学性质一定相同
B.凡单原子形成的离子,一定具有稀有气体元素原子的核外电子排布
C.两原子,如果核外电子排布相同,则一定属于同种元素
D.阴离子的核外电子排布一定与上周期稀有气体元素原子的核外电子排布相同
二、填空题
19X在其化合物中,最高正价为,负价为。
23.元素
9
24.V、W、X、Y、Z五种元素,它们的核电荷数依次增大,且都小于20。
其中:X、Z是金属元素;
V和Z元素原子的最外层都只有一个电子;W和Y元素原子的最外层电子数相同,且W元素原子L层电子数是K层电子数的3倍;X元素原子的最外层电子数是Y元素原子最外层电子数的一半。
由此推知(填元素符号):V是___________,W是____________,X是____________,Y 是____________,Z是____________。
25.有几种元素的微粒的最外电子层结构如图所示,其中:
(1)某电中性微粒一般不和其他元素的原子反应,这种微
粒符号是________。
其电子式是
(2)某微粒的盐溶液,加入AgNO3溶液时会出现白色浑浊,这种微粒符
号是_______。
26.A元素原子M电子层上有6个电子。
B元素与A元素的原子核外电子层数相同,B元素的原子最外电子层只有1个电子。
(1)B元素的原子结构示意图为________________。
A离子的电子式。
(2)A、B两元素形成的化合物的名称是________
27.在1—18号元素中,电子总数是最外层电子数二倍的元素是;最外层电子数是次外层电子数二倍的是;次外层电子数是最外层电子数二倍的是。
28.下列各题中的物质均由核电荷数为1—10的元素组成,请填写化学式。
(1)只有两个原子核和两个电子组成的分子是;
(2)1个最外层有4个电子的原子,和2个最外层有6个电子的原子结合的分子是;(3)1个最外层有5个电子的原子和3个只有1个电子的原子结合的分子是;(4)由3个最外层是6个电子的原子结合而形成的分子是;
(5)由两个原子核10个电子结合而成的分子是,由五个原子核10个电子结合而成的分子是,
29.某金属元素R原子的质量数为52,已知R n+离子含有28个中子和21个电子,则R显+n价时的氢氧化物,其化学式为。
30.A原子的L层比B原子的L层少3个电子,B原子核外电子总数比A原子核外电子总数多5个,则A、B可能是什么元素?写出推断过程。
