高考化学钠及其化合物综合题汇编附答案解析
高考化学钠及其化合物综合经典题附答案
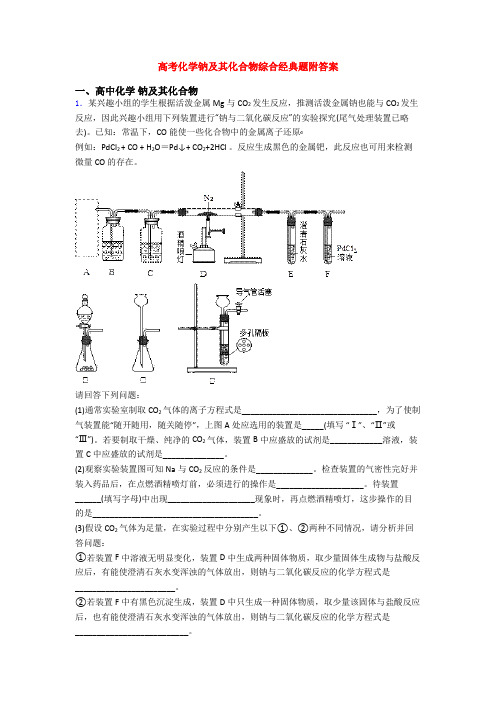
高考化学钠及其化合物综合经典题附答案一、高中化学钠及其化合物1.某兴趣小组的学生根据活泼金属Mg与CO2发生反应,推测活泼金属钠也能与CO2发生反应,因此兴趣小组用下列装置进行“钠与二氧化碳反应”的实验探究(尾气处理装置已略去)。
已知:常温下,CO能使一些化合物中的金属离子还原例如:PdCl2 + CO + H2O=Pd↓+ CO2+2HCl 。
反应生成黑色的金属钯,此反应也可用来检测微量CO的存在。
请回答下列问题:(1)通常实验室制取CO2气体的离子方程式是_______________________________,为了使制气装置能“随开随用,随关随停”,上图A处应选用的装置是_____(填写“Ⅰ”、“Ⅱ”或“Ⅲ”)。
若要制取干燥、纯净的CO2气体,装置B中应盛放的试剂是____________溶液,装置C中应盛放的试剂是______________。
(2)观察实验装置图可知Na与CO2反应的条件是_____________。
检查装置的气密性完好并装入药品后,在点燃酒精喷灯前,必须进行的操作是____________________。
待装置______(填写字母)中出现____________________现象时,再点燃酒精喷灯,这步操作的目的是______________________________________。
(3)假设CO2气体为足量,在实验过程中分别产生以下①、②两种不同情况,请分析并回答问题:①若装置F中溶液无明显变化,装置D中生成两种固体物质,取少量固体生成物与盐酸反应后,有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式是_______________________。
②若装置F中有黑色沉淀生成,装置D中只生成一种固体物质,取少量该固体与盐酸反应后,也有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式是__________________________。
高考化学钠及其化合物综合经典题附答案

高考化学钠及其化合物综合经典题附答案一、高中化学钠及其化合物1.某兴趣小组的学生根据活泼金属Mg与CO2发生反应,推测活泼金属钠也能与CO2发生反应,因此兴趣小组用下列装置进行“钠与二氧化碳反应”的实验探究(尾气处理装置已略去)。
已知:常温下,CO能使一些化合物中的金属离子还原例如:PdCl2 + CO + H2O=Pd↓+ CO2+2HCl 。
反应生成黑色的金属钯,此反应也可用来检测微量CO的存在。
请回答下列问题:(1)通常实验室制取CO2气体的离子方程式是_______________________________,为了使制气装置能“随开随用,随关随停”,上图A处应选用的装置是_____(填写“Ⅰ”、“Ⅱ”或“Ⅲ”)。
若要制取干燥、纯净的CO2气体,装置B中应盛放的试剂是____________溶液,装置C中应盛放的试剂是______________。
(2)观察实验装置图可知Na与CO2反应的条件是_____________。
检查装置的气密性完好并装入药品后,在点燃酒精喷灯前,必须进行的操作是____________________。
待装置______(填写字母)中出现____________________现象时,再点燃酒精喷灯,这步操作的目的是______________________________________。
(3)假设CO2气体为足量,在实验过程中分别产生以下①、②两种不同情况,请分析并回答问题:①若装置F中溶液无明显变化,装置D中生成两种固体物质,取少量固体生成物与盐酸反应后,有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式是_______________________。
②若装置F中有黑色沉淀生成,装置D中只生成一种固体物质,取少量该固体与盐酸反应后,也有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式是__________________________。
全国高考化学钠及其化合物的综合高考真题汇总附答案

全国高考化学钠及其化合物的综合高考真题汇总附答案一、高中化学钠及其化合物1.某兴趣小组的学生根据Mg与CO2反应原理推测钠也能在CO2中燃烧,为了确定其产物并进行试验论证,某同学设计了下列装置进行试验(已知PdCl2能被CO还原为Pd),请回答下列问题:(1)上图装置2中应盛放__________溶液.(2)为了使反应随开随用,随关随停,上图方框内应选用_____装置(填上图字母代号).(3)检查装置的气密性完好并装好药品后,在点燃酒精灯前,应先进行1装置的操作,待装置______(填数字编号)中出现_______________现象时,再点燃酒精灯.(4)①若装置6中有黑色沉淀(Pd)生成,装置4中残留固体(只有一种物质)加盐酸后有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式为_________.②若装置6中溶液无明显现象,装置4中残留固体(有两种物质)加盐酸后有能澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式为_____________.【答案】饱和碳酸氢钠 C 5 澄清石灰水变浑浊的 2Na+2CO2Na2CO3+CO4Na+3CO22Na2CO3+C【解析】【分析】【详解】(1)根据二氧化碳的实验室制法可知二氧化碳中可能含有HCl气体,所以应除去HCl,则装置B中盛放的溶液是饱和碳酸氢钠溶液;答案为:饱和碳酸氢钠;(2)为了使反应随开随用,随关随停,上图方框内应选用C装置,因为C装置可以达到固液分离的目的,起到随开随用,随关随停的作用;答案为:C;(3)因为该实验是验证二氧化碳与Na的反应,所以应排除空气中的氧气,所以先通入二氧化碳使5中澄清石灰水变浑浊后,再点燃酒精灯;答案为:澄清石灰水变浑浊的;5;(4)①若装置6中有黑色沉淀(Pd)生成,装置4中残留固体(只有一种物质)加盐酸后有能使澄清石灰水变浑浊的气体放出,说明该固体是碳酸钠,则Na与二氧化碳反应生成CO和碳酸钠,化学方程式是2Na+2CO2Na2CO3+CO;答案为: 2Na+2CO2Na2CO3+CO;②若装置6中溶液无明显现象,说明无CO生成,装置4中残留固体(有两种物质)加盐酸后有能澄清石灰水变浑浊的气体放出,则一种固体为碳酸钠,另一种是C单质,化学方程式是4Na+3CO22Na2CO3+C。
全国高考化学钠及其化合物推断题的综合高考真题分类汇总附详细答案

全国高考化学钠及其化合物推断题的综合高考真题分类汇总附详细答案一、钠及其化合物1.由三种元素组成的化合物A ,按如下流程进行实验。
气体B 为纯净物,溶液C 焰色反应为砖红色,气体E 能使湿润的红色石蕊试纸变蓝。
请回答:(1)组成A 的三种元素是________,A 的化学式是________。
(2)固体A 与足量稀盐酸反应的化学方程式是________。
(3)气体E 与甲醛在一定条件可生成乌洛托品(学名:六亚甲基四胺),该反应的化学方程式是________(乌洛托品可以用分子式表示)。
【答案】Ca 、H 、N 2Ca HN 2422Ca HN 5HCl 2CaCl H NH Cl +=+↑+ 34NH 6HCHO +→(或6124C H N )26H O +【解析】【分析】 溶液C 焰色反应为砖红色说明溶液C 中含有Ca 元素,可知沉淀F 为CaCO 3,4.00g 碳酸钙的物质的量为 4.00g=0.04mol 100g/mol ,根据元素守恒可知固体A 中含有Ca 元素,其质量为0.04mol×40g/mol=1.60g ;气体E 能使湿润的红色石蕊试纸变蓝说明气体E 为NH 3,所以溶液D 中含有NH 4+,根据元素守恒可知溶液C 中含有N 元素,固体A 中含有N 元素;气体B 为纯净物,其物质的量为0.448L=0.02mol 22.4L/mol ,固体A 中Ca 元素的质量为1.60g ,则其他元素为1.90g-1.60g=0.30g ,可先假设E 为一种常见的气体,若该气体为NO 、NO 2、O 2,则固体A 中另外一种元素为O ,而0.02mol NO 或NO 2或O 2所含氧元素的质量均大于0.30g ,故不合理,若该气体为H 2,固体A 中另外一种元素为H ,则符合题意,同时可以参考CaH 2与水的归中反应生成氢气。
【详解】(1)根据分析可知固体A 中的三种元素为:Ca 、N 、H ;Ca 的常见化合价为+2价,已知固体A 中Ca 元素的物质的量为0.04mol ,质量为1.60g ,N 元素的和H 元素质量为0.04g 共0.30g ,N 的相对原子质量为14,氢的相对原子质量为1,据此可推测A 的化学式可能为Ca 4N 2H 2,化为最简整数比为2Ca HN ;(2)根据产物可知A 与盐酸反应的产物中含有NH 4+,H 2,Ca 2+,根据电子守恒和元素守恒可知方程式为:2422Ca HN 5HCl 2CaCl H NH Cl +=+↑+;(3)气体E 为为NH 3,甲醛为HCHO ,根据元素守恒可知方程式为:34NH 6HCHO +→(或6124C H N )26H O +。
高考化学压轴题专题复习—钠及其化合物的综合附答案解析

高考化学压轴题专题复习—钠及其化合物的综合附答案解析一、高中化学钠及其化合物1.纯碱、烧碱等是重要的化工原料。
(1)利用如图所示装置可间接证明二氧化碳与烧碱溶液发生了反应。
将A与B连接,打开止水夹,将胶头滴管中的液体挤入烧瓶,此时的实验现象是______。
若其它操作不变,将A与C连接,可观察到的现象是_______。
(2)向100 mL2 mol/L的NaOH 溶液中通入一定量CO2,结晶,得到9.3 g白色固体,该白色固体的组成是_______(写化学式)。
设计实验确认该白色固体中存在的阴离子,试完成下列方案。
实验操作实验现象结论①取少量白色固体于试管中,加____________足量水溶解,再加足量BaCl2溶液②过滤,取2 mL滤液于试管____________中,滴加酚酞(3)现代工业常以氯化钠为原料制备纯碱,部分工艺流程如下:已知NaHCO3在低温下溶解度较小。
反应I为:NaCl+CO2+NH3+H2O NaHCO3↓+NH4Cl,处理母液的两种方法如下。
①向母液中加入石灰乳,可将其中_____循环利用,同时得到融雪剂_____。
②向母液中通入NH3,加入细小的食盐颗粒并降温,可得到NH4Cl晶体。
试写出通入NH3后,溶解度较小的酸式碳酸盐转变为溶解度较大的碳酸盐的离子方程式:______________。
【答案】水沿导管由广口瓶进入烧瓶广口瓶中的长导管口有气泡产生 NaOH和Na2CO3产生白色沉淀原白色固体中有CO32-存在溶液变红溶液中含有氢氧化钠 NH3 CaCl2 HCO3—+NH3=NH4++H2O【解析】【分析】(1)CO2与NaOH反应生成Na2CO3,烧瓶内压强减小;(2)先根据钠原子守恒,通过极值法确定白色固体的组成;根据题中所给试剂,要首先利用中性溶液BaCl2检验出碳酸钠,并将碳酸根离子全部沉淀,再通过检验溶于的pH来确定是否含有NaOH;(3)①根据流程可知,母液中含有氯化铵,加入石灰乳后可以生成氨气;②碳酸氢钠溶于水,母液为碳酸氢钠饱和溶液,向母液中通入氨气,氨气与碳酸氢钠反应碳酸钠和碳酸铵。
全国高考化学钠及其化合物推断题的综合高考真题汇总含答案解析

全国高考化学钠及其化合物推断题的综合高考真题汇总含答案解析一、钠及其化合物1.甲、乙、丙均为化合物,其中甲为淡黄色的固体,乙常温下为无色无味液体,丙为常见的无色无味气体,它们有如下图的转化关系,已知D为黄绿色气体,按要求回答下列问题:(1)甲物质为____________(填化学式)。
(2)乙与甲反应的化学方程式为____________,丙与甲反应的化学方程式为____________。
(3)D能使湿润的有色布条褪色,其褪色原因是____________(结合化学反应方程式描述原因)。
(4)D可用于制取“84”消毒液,反应的化学方程式为____________,也可用于工业上制取漂白粉,反应的化学方程式为____________,但漂白粉保存不当易变质,变质时涉及到的化学方程式为____________。
【答案】Na2O2 2Na2O2+2H2O=4NaOH+O2↑ 2Na2O2+2CO2=2Na2CO3+O2Cl2+H2O=HCl+HClO、 HClO有漂白性 Cl2+2NaOH=NaClO+NaCl+H2O2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O Ca(ClO)2+H2O+CO2=CaCO3↓+2HClO,2HClO2HCl+O2↑【解析】【分析】甲、乙、丙均为化合物,甲为淡黄色的固体,乙常温下为无色无味液体,丙为常见的无色无味气体,甲能既能与乙反应也能与丙反应,可知甲为Na2O2,乙为H2O,丙为CO2,则A 为NaOH,B为O2,C为Na2CO3,D为黄绿色气体,则D为Cl2,D(Cl2)与A(NaOH)反应生成NaCl、NaClO,F的溶液能与丙(CO2)反应C与I,则F为NaClO、E为NaCl、I为HClO,G与C(Na2CO3)反应得到E(NaCl)与丙(CO2),则G为HCl,据此解答。
【详解】根据上述分析可知:甲为Na2O2,乙为H2O,丙为CO2,A为NaOH,B为O2,C为Na2CO3,D为Cl2,E为NaCl,F为NaClO,G为HCl,I为HClO。
高考化学 钠及其化合物综合试题附详细答案

高考化学钠及其化合物综合试题附详细答案一、高中化学钠及其化合物1.甲、乙两同学分别用如图所示装置测定空气中氧气的含量。
先用弹簧夹夹住橡胶管,点燃钠,伸入瓶中并塞上瓶塞。
待钠熄灭并冷却后,打开弹簧夹,观察广瓶内水面的变化情况:(1)上述实验过程中发生反应的化学方程式为__________________________________。
(2)甲同学实验中广瓶内水面上升明显小于瓶内空气体积的15,乙同学实验中广瓶内水面上升明显大于瓶内空气体积的15,下列对这两种现象解释合理的是________A.甲同学可能使用的钠的量不足,瓶内氧气没有消耗完B.甲同学可能未塞紧瓶塞,钠熄灭冷却后外界空气进入瓶内C.乙同学可能没有夹紧弹簧夹,钠燃烧时瓶内部分空气受热从导管逸出D.乙同学可能插入燃烧匙太慢,塞紧瓶塞之前瓶内部分空气受热逸出(3)在实验室里,某同学取一小块金属钠做钠与水反应的实验。
将钠投入水中后,钠熔化成一个小球,根据这一现象你能得出的结论是①__________,②__________,【答案】2Na+O2Na2O2 ABCD 钠与水反应放出热量钠的熔点低【解析】【分析】(1)钠在加热条件下与氧气反应生成过氧化钠,据此写出化学反应方程式即可,注意条件;(2)A.若钠的量不足,则氧气消耗不完,造成进水量少于容器容积的量;B.若瓶塞未塞紧,钠熄灭冷却,瓶内气体收缩,外面的空气会进入瓶内,使气体得到补充;C.若弹簧夹未夹紧,钠燃烧时,瓶内气体膨胀,使部分气体从导管口逸出;D.若插入燃烧匙太慢,钠燃烧时,瓶内气体膨胀,在塞紧瓶塞前,瓶内部分气体从瓶口逸出;(3)依据钠熔化成一个小球可知反应放出热量,钠的熔点低。
【详解】(1)钠在加热条件下与氧气反应生成过氧化钠,化学反应方程式为: 2Na+O2Na2O2;(2)A.钠的量不足,瓶内氧气没有消耗完,导致氧气剩余,故瓶内水面上升高度达不到,选项A正确;B.瓶塞末塞紧,钠熄灭冷却时外界空气进入瓶内,导致瓶内压强过大,水面上升高度达不到,选项B正确;C.没夹紧弹簧夹,钠燃烧时瓶内部分空气受热从导管逸出,导致瓶内压强减小,水面上升高度超出,选项C正确;D.插入燃烧匙太慢,塞紧瓶塞之前,瓶内部分空气受热逸出,导致瓶内压强减小,水面上升高度超出,选项D正确;答案选ABCD;(3)将钠投入水中后,钠熔化成一个小球,根据这一现象你能得出的结论是①钠与水反应放出热量,②钠的熔点低。
全国高考化学钠及其化合物推断题的综合高考真题分类汇总含详细答案

全国高考化学钠及其化合物推断题的综合高考真题分类汇总含详细答案一、钠及其化合物1.已知甲、乙、丙为常见单质,A、B、C、D、E、F、G、X均为常见的化合物;B和X的摩尔质量相同,E的相对分子质量比D的相对分子质量大16,在一定条件下,各物质相互转化关系如下图所示。
请按要求填空:(1)丙的化学式是_______,G的化学式是_________。
(2)写出有关变化的化学方程式:甲 + 乙:___________;D + 丙:_______。
(3)B与X的水溶液反应生成C和乙的离子方程式是________________________。
【答案】O2 SO3 2Na + S Na2S 2Na2SO3+ O2= 2Na2SO4 Na2O2+S2-+2H2O=4OH-+S↓+2Na+【解析】【分析】单质甲、乙均能分别与单质丙连续两次反应,可能是单质甲、乙分别被O2连续两次氧化,生成不同的氧化物,则丙是O2;氧化物B与水反应能放出O2,则B是Na2O2,那么C是NaOH,A是Na2O,甲是Na;又因B和H的摩尔质量相同,则X是Na2S,那么乙是S,F 是SO2,G是SO3;由E的相对分子质量比D的相对分子质量大16可知D是Na2SO3,E是Na2SO4。
【详解】(1)由以上分析可知丙是O2,G是SO3;故答案为:O2,SO3;(2)甲 + 乙的反应为钠与硫共热反应生成硫化钠,反应的化学方程式为2Na +S Na 2S;D + 丙的反应为亚硫酸钠与氧气反应生成硫酸钠,反应的化学方程式为2Na 2SO3+ O2= 2Na2SO4,故答案为:2Na + S Na2S;2Na2SO3+ O2= 2Na2SO4;(3)过氧化钠与氯化钠的水溶液发生氧化还原反应生成氢氧化钠和硫,反应的离子方程式为Na2O2+S2-+2H2O=4OH-+S↓+2Na+,故答案为:Na2O2+S2-+2H2O=4OH-+S↓+2Na+。
2.A、B、C、D、E、X是中学常见的无机物,存在如下图转化关系(部分生成物和反应条件略去)。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
高考化学钠及其化合物综合题汇编附答案解析一、高中化学钠及其化合物1.某兴趣小组的学生根据活泼金属Mg与CO2发生反应,推测活泼金属钠也能与CO2发生反应,因此兴趣小组用下列装置进行“钠与二氧化碳反应”的实验探究(尾气处理装置已略去)。
已知:常温下,CO能使一些化合物中的金属离子还原例如:PdCl2 + CO + H2O=Pd↓+ CO2+2HCl 。
反应生成黑色的金属钯,此反应也可用来检测微量CO的存在。
请回答下列问题:(1)通常实验室制取CO2气体的离子方程式是_______________________________,为了使制气装置能“随开随用,随关随停”,上图A处应选用的装置是_____(填写“Ⅰ”、“Ⅱ”或“Ⅲ”)。
若要制取干燥、纯净的CO2气体,装置B中应盛放的试剂是____________溶液,装置C中应盛放的试剂是______________。
(2)观察实验装置图可知Na与CO2反应的条件是_____________。
检查装置的气密性完好并装入药品后,在点燃酒精喷灯前,必须进行的操作是____________________。
待装置______(填写字母)中出现____________________现象时,再点燃酒精喷灯,这步操作的目的是______________________________________。
(3)假设CO2气体为足量,在实验过程中分别产生以下①、②两种不同情况,请分析并回答问题:①若装置F中溶液无明显变化,装置D中生成两种固体物质,取少量固体生成物与盐酸反应后,有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式是_______________________。
②若装置F中有黑色沉淀生成,装置D中只生成一种固体物质,取少量该固体与盐酸反应后,也有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式是__________________________。
(4)请用文字简要说明你判断②中D装置生成固体的成分是钠的正盐或酸式盐的理由。
_________________________________。
【答案】CaCO3 + 2H+= Ca2++ H2O + CO2↑Ⅲ饱和NaHCO3浓H2SO4高温(或强热) 扭开装置Ⅲ中导气管活塞 E 澄清的石灰水变浑浊排出该装置中的空气 4Na +3CO22Na2CO3+ C 2Na + 2CO2Na2CO3+ CO 生成正盐。
因为根据质量守恒定律可知,反应物共有三种元素,没有氢元素,因此不能生成酸式盐。
【解析】【分析】(1)实验室通常用大理石或石灰石和稀盐酸反应制取二氧化碳,反应不需要加热,大理石和石灰石的主要成分是碳酸钙,能和稀盐酸反应生成氯化钙、水和二氧化碳;Ⅲ装置能使反应随时进行或停止,原理是:关闭开关时,试管中的气体增多,压强增大,把液体压入长颈漏斗,固体和液体分离,反应停止;打开开关时,气体导出,试管中的气体减少,压强减小,液体和固体混合,反应进行;(2)高温条件下,钠能和氧气反应;二氧化碳能使澄清石灰水变浑浊;(3)根据提供的信息可以判断反应进行情况;(4)化学反应遵循质量守恒定律,即反应前后元素种类、原子种类和总个数都不变.【详解】(1)通常实验室制取CO2气体的化学方程式是:CaCO3+2HCl═CaCl2+H2O+CO2↑;Ⅲ装置能使反应随时进行或停止,原理是:关闭开关时,试管中的气体增多,压强增大,把液体压入长颈漏斗,固体和液体分离,反应停止;打开开关时,气体导出,试管中的气体减少,压强减小,液体和固体混合,反应进行;若要制取干燥、纯净的CO2气体,装置B中应盛放的试剂是饱和碳酸氢钠溶液,这是因为饱和碳酸氢钠溶液不能和二氧化碳反应,能和稀盐酸反应生成氯化钠、水和二氧化碳,从而可以除去二氧化碳中的氯化氢气体;装置C中应盛放的试剂是浓硫酸,用来除去二氧化碳中的水蒸气;(2)观察实验装置图可知Na与CO2反应的条件是高温;检查装置的气密性完好并装入药品后,在点燃酒精喷灯前,必须进行的操作是通入一会儿二氧化碳气体,待装置E中出现浑浊现象时,再点燃酒精喷灯,这步操作的目的是防止钠和空气中的氧气反应;(3)①若装置F中溶液无明显变化,装置D中生成两种固体物质,取少量固体生成物与盐酸反应后,有能使澄清石灰水变浑浊的气体放出,说明反应生成了碳酸钠,则钠与二氧化碳反应生成碳酸钠和碳,反应的化学方程式是:3CO2+4Na2Na2CO3+C;②若装置F中有黑色沉淀生成,装置D中只生成一种固体物质,说明反应生成了一氧化碳,取少量该固体与盐酸反应后,也有能使澄清石灰水变浑浊的气体放出,说明反应生成了碳酸钠,则钠与二氧化碳反应生成碳酸钠和一氧化碳,反应的化学方程式是:2CO2+2Na Na2CO3+CO;(4)②中D装置生成固体的成分是钠的正盐的理由是:反应物中不含有氢元素,因此生成物中不含有氢元素,即生成的固体不可能是碳酸氢钠。
2.某兴趣小组的学生根据Mg与CO2反应原理推测钠也能在CO2中燃烧,为了确定其产物并进行试验论证,某同学设计了下列装置进行试验(已知PdCl2能被CO还原为Pd),请回答下列问题:(1)上图装置2中应盛放__________溶液.(2)为了使反应随开随用,随关随停,上图方框内应选用_____装置(填上图字母代号).(3)检查装置的气密性完好并装好药品后,在点燃酒精灯前,应先进行1装置的操作,待装置______(填数字编号)中出现_______________现象时,再点燃酒精灯.(4)①若装置6中有黑色沉淀(Pd)生成,装置4中残留固体(只有一种物质)加盐酸后有能使澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式为_________.②若装置6中溶液无明显现象,装置4中残留固体(有两种物质)加盐酸后有能澄清石灰水变浑浊的气体放出,则钠与二氧化碳反应的化学方程式为_____________.【答案】饱和碳酸氢钠 C 5 澄清石灰水变浑浊的 2Na+2CO2Na2CO3+CO4Na+3CO22Na2CO3+C【解析】【分析】【详解】(1)根据二氧化碳的实验室制法可知二氧化碳中可能含有HCl气体,所以应除去HCl,则装置B中盛放的溶液是饱和碳酸氢钠溶液;答案为:饱和碳酸氢钠;(2)为了使反应随开随用,随关随停,上图方框内应选用C装置,因为C装置可以达到固液分离的目的,起到随开随用,随关随停的作用;答案为:C;(3)因为该实验是验证二氧化碳与Na的反应,所以应排除空气中的氧气,所以先通入二氧化碳使5中澄清石灰水变浑浊后,再点燃酒精灯;答案为:澄清石灰水变浑浊的;5;(4)①若装置6中有黑色沉淀(Pd)生成,装置4中残留固体(只有一种物质)加盐酸后有能使澄清石灰水变浑浊的气体放出,说明该固体是碳酸钠,则Na与二氧化碳反应生成CO和碳酸钠,化学方程式是2Na+2CO2Na2CO3+CO;答案为: 2Na+2CO2Na2CO3+CO;②若装置6中溶液无明显现象,说明无CO生成,装置4中残留固体(有两种物质)加盐酸后有能澄清石灰水变浑浊的气体放出,则一种固体为碳酸钠,另一种是C单质,化学方程式是4Na+3CO22Na2CO3+C。
答案为:4Na+3CO22Na2CO3+C;3.往100mL的NaOH溶液中通入2CO充分反应后,在减压和较低温度下,小心地将溶液蒸干,得到白色固体M。
通入的2CO的体积V(标准状况)与M的质量W的关系如下图所示。
试解答下列问题:(1)A点时,白色固体M的化学式为_________,通入的2CO的体积为_________mL(标准状况下,下同)。
(2)C点时,白色固体M的化学式为__________,通入的2CO的体积为__________mL。
(3)B点时M的组成成分为_________,物质的量之比为_________,通入的2CO的体积为__________mL。
(4)该NaOH溶液的物质的量浓度为_________。
【答案】Na2CO3 1120 NaHCO3 2240 Na2CO3、NaHCO3 1:3 1792 1mol/L【解析】【分析】由图知NaOH质量为4 g,物质的量为0.1 mol,完全转化为Na2CO3时,Na2CO3质量为0.1mol×12×106g/mol=5.3 g,完全转化为NaHCO3时,NaHCO3质量为0.1mol×84g/mol=8.4g,故A点白色固体M为Na2CO3,C点白色固体M为NaHCO3,根据碳原子守恒可得n(CO2),根据V=nV m计算二氧化碳体积;图B点时M的质量为7.16 g,5.3<7.16<8.4,知M由Na2CO3和NaHCO3组成,设在B点时Na2CO3物质的量为x,NaHCO3物质的量为y,根据钠离子守恒、二者质量之和列方程计算x、y的值,根据V=nV m计算二氧化碳体积;根据c=nV计算NaOH溶液的物质的量浓度。
【详解】由图知NaOH质量为4 g,物质的量为0.1 mol,完全转化为Na2CO3时,Na2CO3质量为0.1mol×12×106g/mol=5.3 g,完全转化为NaHCO3时,NaHCO3质量为0.1mol×84g/mol=8.4g,故A点白色固体M为Na2CO3,C点白色固体M为NaHCO3;(1)由上述分析可知,A点白色固体M为Na2CO3,需CO2体积为0.1 mol×12×22.4L•mol−1=1.12L=1120 mL,故答案为:Na2CO3;1120;(2)由上述分析可知,C点白色固体M为NaHCO3,需CO2体积为0.1 mol×22.4L•mol−1=2.24L=2240 mL,故答案为:NaHCO3;2240;(3)图B点时M的质量为7.16 g,5.3<7.16<8.4,知M由Na2CO3和NaHCO3组成;设在B点时Na2CO3物质的量为xmol,NaHCO3物质的量为ymol,则:2x+y=0.1,106x+84y=7.16,解得x=0.02,y=0.06,n(Na2CO3):n(NaHCO3)= 0.02mol:0.06mol=1:3,故V(CO2)=(0.02 mol+0.06 mol)×22.4L•mol−1=1.792L=1792 mL,故答案为:Na2CO3、NaHCO3;1:3;1792;(4)该NaOH溶液的物质的量浓度为0.1mol0.1L=1mol/L,故答案为:1mol/L。
【点睛】本题根据图像判断出开始时氢氧化钠的质量及利用假设法判断A、C两点白色固体的成分是解题关键。
