化合价与化学式(金)
沪教版初三化学----化合价和化学式

沪教版初三化学----化合价和化学式一、化合价1. 化合价的概念:各种元素在相互化合形成化合物时原子之间都有固定的化合数目,我们把元素的这种性质成为化合价。
(1).化合价有正有负。
(2).化合价的表示方法:在元素符号的正上方用“+”,“-”的数字表示。
符号在前,数字在后。
2.一般规律(1)、在化合物里,金属元素通常显正价(氢显+1价),非金属元素显负价(氧显-2价)(2)、在化合物里,各元素正负化合价的代数和等于零(3)、在单质分子里,元素的化合价为零二、常见元素的化合价1.常见原子的化合价如下名称氢氧碳硫钠镁铁铜氯钙符号H O C S Na Mg Fe Cu Cl Ca根价+1-2+2 +4+4 +6 -2+1+2+2 +3+2-1+2常见元素的化合价口诀:钾钠氢银正一价,钙镁锌钡正二价;氟氯溴碘负一价,通常氧是负二价;铜正一正二铝正三,铁有正二和正三;碳有正二和正四,硫有负二正四和正六2、原子团(1) 原子团:某些元素的原子集合在一起作为一个整体参加化学反应,它所起的作用和一个原子一样,这样的原子集团称为原子团。
(2) 掌握几个常见原子团的主要化合价名称铵根氢氧根硝酸根硫酸根碳酸根磷酸根碳酸氢根亚硫酸根符号NH4OH NO3SO4CO3PO4HCO3SO3根价+1-1-1-2-2-3-1-2(3) 原子团化合价记忆口诀:负一氢氧和硝酸负二硫酸碳酸根负三磷酸正一铵三、根据化合价书写化学式1.原则:在化合物里,各元素正负化合价的代数和等于零2.步骤:(1)正价元素写左边,负价元素写右边(2)标示相应元素的化合价,求出绝对值的最小公倍数(3)求出相应原子的个数,将原子个数比化成最简比写在元素符号的右下角例1 写出下列物质的化学式硫酸亚硫酸盐酸硝酸碳酸磷酸硫酸钡硫酸铜硫酸钾碳酸钠硫酸镁碳酸氢钠碳酸钙碳酸锌硝酸银硝酸钡氯化银硝酸钾碳酸钾氯化汞过氧化氢氯酸钾氯化钾锰酸钾硫酸铁氢氧化铜氢氧化镁氢氧化钙氨水硫酸亚铁课堂练习1.下列化学式中,书写正确的是()A.二氧化硫O2SB.四氧化三铁3FeO4C.氧气OD.二氧化碳CO22. 写出下列常见物质的化学式。
常见的元素化合价 化学式

亚
亚
FeSO4
碳酸 铜
CuCO3
碳酸 银
Ag2CO3
铁
铁
硝 AgNO3 硫 K2SO4 高锰 KMnO4 锰酸 K2MnO4
第6页
酸
酸
酸钾
钾
银
钾
常见的元素符合、化合价、离子符合、化学式
一、常见元素名称与符号:
原子 元素 元素 原子 元素 元素 原子 元素 元素
序数 名称 符号 序数 名称 符号 序数 名称 符号
1.单质
名称
化学 式
名称
化学 式
名称
化学
化学
名称
式
式
氦气
氖气
氩气
锰
氪气
氙气
氡气
铅
第8页
氟气
氯气
液溴
汞
碘
氧气
氢气
铂
氮气
臭氧
石墨、金 金
刚石
单晶
红磷、白
硫磺
钨
硅
磷
钙
钾
镁
银
铝
钠
铁
锌
铜
2.氯化物〔盐〕
名称
化学 式
名称
化学
化学
名称
式
式
名称
化学 式
氯化 氢
氯化钾
氯化 钠
氯化亚 铁
氯化 银
氯化钡
氯化 铜
氯化铁
氯化 钙
H2O2
一氧 化碳
二氧化
二氧化
二氧化
CO
CO2
SO2
NO2
碳
硫
氮
三氧
五氧化
一氧化
四氧化
SO3
P2O5
初中常见化合价化学式及化学方程式
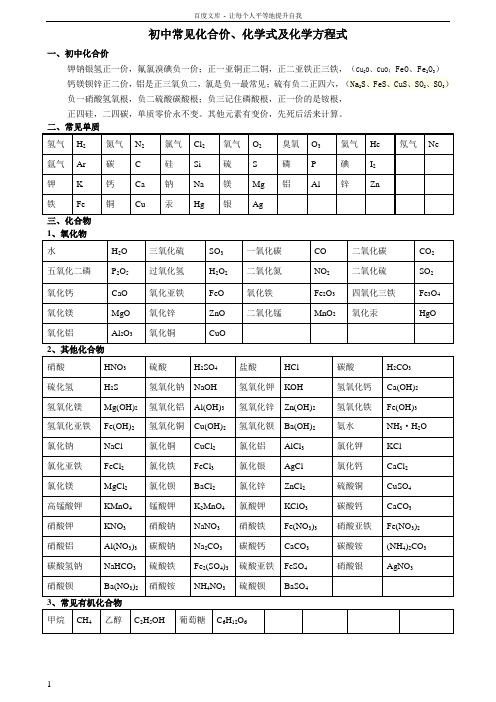
初中常见化合价、化学式及化学方程式一、初中化合价钾钠银氢正一价,氟氯溴碘负一价;正一亚铜正二铜,正二亚铁正三铁,(Cu2O、CuO;FeO、Fe2O3)钙镁钡锌正二价,铝是正三氧负二,氯是负一最常见;硫有负二正四六,(Na2S、FeS、CuS、SO2、SO3)负一硝酸氢氧根,负二硫酸碳酸根;负三记住磷酸根,正一价的是铵根,正四硅,二四碳,单质零价永不变。
其他元素有变价,先死后活来计算。
三、化合物初中化学方程式全(已配平)一、化合反应1、镁在空气中燃烧:2Mg+O2点燃2MgO2、铁在氧气中燃烧:3Fe+2O2点燃Fe3O43、铝在空气中燃烧:4Al+3O2点燃2Al2O34、氢气在空气中燃烧:2H2+O2点燃2H2O5、红磷在空气中燃烧:4P+5O2点燃2P2O56、硫粉在空气中燃烧:S+O2点燃SO27、碳在氧气中充分燃烧:C+O2点燃 CO28、碳在氧气中不充分燃烧:2C+O2点燃2CO9、二氧化碳通过灼热碳层:C+CO2高温2CO10、一氧化碳在氧气中燃烧:2CO+O2 点燃2CO211、二氧化碳和水反应(二氧化碳通入紫色石蕊试液):CO2+H2O=H2CO312、生石灰溶于水:CaO+H2O=Ca(OH)213、无水硫酸铜作干燥剂:CuSO4+5H2O=CuSO4·5H2O14、钠在氯气中燃烧:2Na+Cl2点燃2NaCl二、分解反应15、实验室用双氧水制氧气:2H2O2MnO22H2O+O2↑16、加热高锰酸钾:2KMnO4△K2MnO4+MnO2+O2↑17、水在直流电的作用下分解:2H2O通电2H2↑+O2↑18、碳酸化学性质不稳定而分解:H2CO3=H2O+CO2↑19、高温煅烧石灰石(二氧化碳工业制法):CaCO3高温CaO+CO2↑20、加热氯酸钾分解:2KClO3=2KCl+3O2↑21、氧化汞加热分解:2HgO△2Hg+O2↑三、置换反应(单质+化合物→新的单质+新的合化物)22、锌和稀盐酸反应(实验室制氢气):Zn+2HCl=ZnCl2+H2↑锌和稀硫酸反应(实验室制氢气):Zn+H2SO4=ZnSO4+H2↑23、镁和稀盐酸反应:Mg+2HCl=MgCl2+H2↑镁和稀硫酸反应:Mg+H2SO4=MgSO4+H2↑24、铁和稀盐酸反应:Fe+2HCl=FeCl2+H2↑铁和稀硫酸反应:Fe+H2SO4=FeSO4+H2↑25、铝和稀盐酸反应:2Al+6HCl=2AlCl3+3H2↑铝和稀硫酸反应:2Al+3H2SO4=Al2(SO4)3+3H2↑26、铁和硫酸铜溶液反应:Fe+CuSO4 =FeSO4+Cu铝和硫酸铜溶液反应:2Al+3CuSO4=Al2(SO4)3+3Cu27、铜和硝酸银反应:Cu+2AgNO3=Cu(NO3)2+2Ag28、氢气还原氧化铜:H2+CuO△Cu+H2O29、木炭还原氧化铜:C+2CuO高温 2Cu+CO2↑30、焦炭还原氧化铁:3C+2Fe2O高温 4Fe+3CO2↑31、水蒸气通过灼热碳层:H2O+C高温 H2+CO四、复分解反应复分解反应是由两种互相交换成分,生成另外两种化合物的反应。
常见元素的化合价口诀

常见元素的化合价口诀:氢钠钾银正一价,钙钡镁锌正二价,一二铜,二三铁,二四六硫二四碳,三铝四硅三五磷,变价还有锰氯氮。
一价氯氢钾钠银,二价氧钡钙镁锌,三铝四硅五氮磷,二三铁,二四碳,二四六硫价齐全。
铜汞二价最常见,化合价要记清,莫忘单质价为零!化合价:一价钾钠氯银,二价钡镁钙锌,三铝四硅五价磷,六硫七锰八为零,一铜二铁加亚名,单质为零,氢正一,氧负二,氢氧优先,不变价优先,遇正必负。
一价氢锂钾钠银;二价氧钙钡镁锌。
三铝四硅五价磷,变价元素记在心。
二三铁,二四碳,一七氯,三五氮。
二四六硫要分清,铜汞一二也都有。
单质元素价为零负一硝酸氢氧根,负二碳酸硫酸根。
负三记住磷酸根,正一价的是铵根。
根价口诀编辑口诀1一价铵根硝酸根;氢氯酸根氢氧根。
高锰酸根氯酸根;高氯酸根醋酸根。
二价硫酸碳酸根;氢硫酸根锰酸根。
暂记铵根为正价;负三有个磷酸根。
口诀2负一硝酸氢氧根,负二硫酸碳酸根,只有正一是铵根,还有负三磷酸根。
(适合初中生用)综合口诀编辑口诀一氟氯溴碘负一价;正一氢银与钾钠。
氧的负二先记清;正二镁钙钡和锌。
正三是铝正四硅;下面再把变价归。
全部金属是正价;一二铜来二三铁。
锰正二四与六七;碳的二四要牢记。
非金属负主正不齐;氯的负一正一五七。
氮磷负三与正五;不同磷三氮二四。
硫有负二正四六;边记边用就会熟。
周期表必须要有节奏才能记住:氢氦锂铍硼碳氮/氧氟氖/钠镁铝硅/磷硫氯氩/钾钙/按照这个节奏读几遍就记住了,初中记到20号就可以了啊溶解性表要用记少排多法:氢离子是全溶的,下面就不讲了,氢氧根氨钾钠钡溶,硝酸根全溶,氯离子银不溶,硫酸根离子钡不溶,碳酸根氨钾钠溶,微溶的可以先不管用化合价写化学式的原则:正价前,负价后;(金前非后,氧右非左):Al O+3 -2化合价,标上头;Al O先略简,后交叉;Al2O3代数和,等于零。
(+3*2)+(-2*3)=0。
金属元素、化合价、化学式
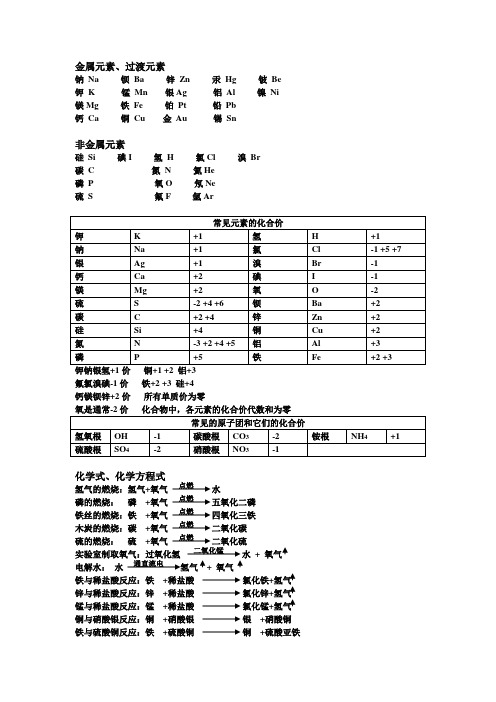
金属元素、过渡元素
钠 Na 钡 Ba 锌 Zn 汞 Hg 铍 Be 钾 K 锰 Mn 银Ag 铝 Al 镍 Ni 镁Mg 铁 Fe 铂 Pt 铅 Pb 钙 Ca 铜 Cu 金 Au 锡 Sn
非金属元素
硅 Si 碘I 氢 H 氯Cl 溴 Br 碳 C 氮 N 氦He 磷 P 氧O 氖Ne 硫 S 氟F 氩Ar
钾钠银氢+1价 铜+1 +2 铝+3 氟氯溴碘-1价 铁+2 +3 硅+4 钙镁钡锌+2价 所有单质价为零
化学式、化学方程式
氢气的燃烧:氢气+氧气 水 磷的燃烧: 磷 +氧气 五氧化二磷
铁丝的燃烧:铁 +氧气 四氧化三铁 木炭的燃烧:碳 +氧气 二氧化碳
硫的燃烧: 硫 +氧气 二氧化硫 实验室制取氧气:过氧化氢 水 + 氧气
电解水: 水 + 氧气
铁与稀盐酸反应:铁 +稀盐酸 氯化铁+氢气 锌与稀盐酸反应:锌 +稀盐酸 氯化锌+氢气 锰与稀盐酸反应:锰 +稀盐酸 氯化锰+氢气 铜与硝酸银反应:铜 +硝酸银 银 +硝酸铜 铁与硫酸铜反应:铁 +硫酸铜 铜 +硫酸亚铁
点燃
点燃 点燃
点燃 点燃
二氧化锰 通直流电。
化学式与化合价知识点归纳

化学式与化合价知识点归纳
化学式是表示化合物组成的一种符号表示法,由元素符号和原子所含个数(用希腊字母的下标表示)组成。
化合价是指元素在化合物中存在时所能与其它元素组成化合物的能力。
化合价可以是正的、负的或零。
以下是一些化合价的规律和知识点:
1. 单质的化合价一般为零,即自身与自身结合时,元素的化合价为零。
2. 碱金属(IA族元素例如Li、Na、K等)的化合价一般为+1,即它们一般失去一个电子形成+1价离子。
3. 碱土金属(IIA族元素例如Be、Mg、Ca等)的化合价一般为+2,即它们一般失去两个电子形成+2价离子。
4. 氢(H)的化合价一般为+1,但在金属化物中,其化合价为-1。
5. 氧(O)的化合价一般为-2,但在过氧化物(如H2O2)中,其化合价为-1。
6. 卤素(VIIA族元素如F、Cl、Br等)的化合价一般为-1。
7. 在一个化合物中,各个元素的化合价相加等于零。
例如,在H2O中,H的化合价为+1,O的化合价为-2,两者相加等于0。
8. 通过化学式可以推测出元素的化合价。
例如,Fe2O3表示二氧化铁,O的化合价为-2,那么Fe的化合价可以通过推算得到为+3。
9. 某些元素(如过渡金属元素)的化合价可以变化,例如,铁(Fe)的化合价可以是+2或+3,铜(Cu)的化合价可以是+1或+2。
以上是一些常见的化学式与化合价相关的知识点,希望对你有帮助!。
初中化学化合价和化学式总结(2篇)

初中化学化合价和化学式总结化学式与化合价要掌握的内容:能用化学式正确表示某些常见物质的组成记住常见元素及原子团的化合价要能根据化合价书写化学式及根据化学式判断元素化合价能利用相对原子质量、相对分子质量进行物质组成的简单计算能看懂常见商标中用化学式表示的物质成分及含量初步学会根据化学式计算相对分子质量、各元素的质量比或根据质量比求化学式、计算指定元素的质量分数1化学式1.概念:用元素符号和数字表示物质组成的式子【注意】每种纯净物的组成是固定不变的,所以,一种物质的化学式只有一个2.化学式表示的含义(一般包括宏观和微观)化学式的含义以H2O为例宏观表示一种物质表示水这种物质表示该物质有哪些元素组成的表示水由氧元素和氢元素组成微观表示该物质的一个分子或者一个原子表示一个水分子由分子构成的物质,还可以表示一个分子的构成情况表示一个水分子中由____个氢原子和____个氧原子构成备注:在化学式与元素符号前加上大于1的数字,都只具有微观意义,即只代表几个微观的微粒3.化学式的写法和读法2化合价含义:由于形成化合物的元素有固定的原子个数比,所以化学上就用“化合价”来表示原子之间相互化合的数目化合物中各元素的化合价通常是在化学式中各元素符号或原子团的正上方标记,一般把“+”“-”写在前,价数写在后。
如元素化合价与离子表示方法的区别和联系离子符号化合价正负号及数值标的位置元素符号的右上角元素符号的正上方正、负号及数值书写顺序数值在前,正、负号在后正、负号在前,数值在后联系离子所带电荷与化合价数值是一致的,已知离子符号可推测该元素的化合价,已知化合价也可以确定离子所带电荷和电性实例Mg2+、Ca2+、Cl-化合价的一般规律①单质中,元素的化合价为0,在化合物中,正、负化合价代数和为0②在化合物中,氢元素的化合价通常为+1价,氧元素的化合价通常显示-2价③金属元素在化合物里显正价,非金属元素在和金属元素化合时,通常显负价④一些元素在不同物质中可显不同的化合价,如Fe有+2、+3价,S有-2、+4、-6价备注:这里介绍两种化合价口诀供给同学们记忆:口诀1:一价钾钠氯氢银;二价氧钙钡镁锌;三铝四硅五价磷;二三铁,二四碳,二四六硫都齐全,铜汞二价最常见。
初中化学化合价口诀表

初中化学化合价口诀表一、概述化学化合价是指元素在化合物中的价态或化合物中各元素的正、负电荷的比例关系。
初中化学中,我们需要掌握一些常见元素的化合价,能够通过化合价口诀来快速准确地确定元素的化合价。
本文将介绍常见元素的化合价口诀表,供初中化学学习者参考。
二、主要元素的化合价1. 碱金属元素(IA族元素)•氢(H):氢化物(H-)中氢的化合价为-1。
•钾(K)、钠(Na):一价阳离子,其化合价为+1。
2. 碱土金属元素(IIA族元素)•铍(Be):二价阳离子,其化合价为+2。
•镁(Mg):二价阳离子,其化合价为+2。
3. 铜、银、金(IB、IIB、VIB族元素)•铜(Cu):由于具有两种化合价态,可根据具体情况确定。
–铜在阳离子中的化合价为+2。
–铜在氧化物中的化合价为+1。
•银(Ag)、金(Au):由于只有一种化合价态,其化合价分别为+1。
4. 卤素元素(VIIA族元素)•氟(F):一种化合价态,其化合价为-1。
•氯(Cl)、溴(Br)、碘(I):均为一价阴离子,其化合价为-1。
5. 第16、17、18族元素•氧(O):一种化合价态,其化合价为-2。
•硫(S):根据实际情况可有多种化合价态,一般为2、4、6。
•氮(N):根据实际情况可有多种化合价态,一般为-3、+3、+5。
6. 第1、2、13、14族元素•氢(H):正离子时,氢的化合价为+1。
•碳(C)、硅(Si):根据实际情况可有多种化合价态。
三、化合价口诀表化合价口诀表是帮助我们记忆元素化合价的一种方法。
下面是常见元素的化合价口诀表:1.氢除负一,银金加一。
2.氧氟氯溴碘,氧负二级加一线。
3.金银铜铁,只有单一态。
4.碱土金属被二抹,除铬锌盖球袋。
5.氨氮亏三只脚,邦硅磷锡老大巧。
6.钙锶镭四两铺,吃饭就来氧边走。
通过这些简洁的句子,我们可以快速记忆常见元素的化合价,辅助我们在化学计算和化学式写法中省去繁琐的查阅过程。
四、小结初中化学化合价口诀表是学习初中化学中化合价的有效辅助工具之一。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
依据:化合物里正负化合价代数和为0.
+
练习:已知SO4为-2价,求FeSO4中铁元素的化合价.
可变价元素的化合价必须根据计算才能确定。
三、根据化合价求化学式
例题3:已知磷为+5价,氧为-2价,写出磷的这种 化合物的化学式。
解: 1.写出组成的元素:正价在前,负价在后, 2.求正负化合价绝对值的最小公倍数→
1.元素符号之前加数字不再表示某元素,不再有 宏观的意义,只表示原子的个数。 2.化学式前加数字也不再表示该物质, 不具有宏观的意义,只表示分子的个数。
练一练
表示2个水分子 用元素符号或化学式填空 4CO2 (1) 4个二氧化碳分子 2H O 2 (2)7个铁原子 7Fe (3)1个氧分子 O2 表示每个水分子 (4)5个硫原子 5S 中有2个氢原子
2.在化合物里,正负化合价的代数和为0.
3.元素的化合价是元素的原子在形成化合物时表现 出来的一种性质。因此, 在单质分子里,元素的化合价为0.
一些常见元素化合价口诀
一价金属钾钠银 氢一氧二单质零 二价金属钙镁钡锌 铝为正三要记清
一些常见原子团的化合价
负一硝酸氢氧根 负三记住磷酸根 负二硫酸碳酸根 正一价的是铵根
化合价的表示方法:O 化合价
-2
Mg 离子
+2
表示 标在元素符号的正上 标在元素符号的右上 角 左数字右符号 方法 方 左符号右数字 符号 +3 -2 +2 Al3+、O2-、Mg2+
Al、O、Mg
联系
同种元素的化合价与离子的电荷, 通常数值相等,正负相同,位置相反。
2Mg
+2
镁元素的化合价为+2价
化学式的书写必须依据实验的结果
表示水这种 物质
表示一个 水分子
表示水由氢 元素和氧元 素组成
表示一个 水分子由2个 氢原子和1个 氧原子构成
CO2 表示 (1)二氧化碳这种物质;
模仿着说一说:CO2
(2)二氧化碳由氧元素和碳元素组成。 (3)一个二氧化碳分子;
(4)一个二氧化碳分子由2个氧原子和1个碳原子 构成;
2.表达意义
①表示一种物质
宏观意义:
②表示一种物质的元素组成 ③表示物质的一个分子 ④表示物质一个分子的构成情况
微观意义:
符号H、2H、H2、2H2各具有什么意义?
① H表示氢元素或一个氢原子。
② 2H表示2个氢原子。
③ H2表示氢气这种物质;氢气是由氢元素组成; 一个氢分子;每个氢分子由2个氢原子构成。 ④ 2H2表示两个氢分子
2个镁原子
2Mg2+
镁离子带2个单位的正电荷
2个镁离子 2H2O
-2
水中的氧元素为-2价
一个水分子中含有两个氢原子 2个水分子
化 合 价 的 一 般 规 律
1、化合价有正负之分。 (1)在化合物中,氢通常显+1价,氧通常显-2价。 (2)金属元素跟非金属元素化合时,金属元素 显正价,非金属元素显负价。 (3)同种元素在不同化合物中可显示不同的 化合价;同种元素在同一化合物中也能显示 不同的化合价。
64×2+(16+1)×2+12来自+16×3=222求划线元素的质量分数
H2O CO2 KMnO4 K2MnO4 NH4NO3 Cu2(OH)2CO3
11.1% 27.3 % 40.5 % 39.6 % 35 %
57.5 %
+5 P
-2 O
5×2=10
3.求各元素的原子数:最小公倍数/正价数(或负价数)=原子个数
P:10/5=2
O:10/2=5
P2O5 +5×2+(-2)×5=0
4.原子个数写在元素符号右下角:→ 5.检查正误:正负化合价代数和为0 →
十字交叉法写化学式:
一排顺序二标价. 价数交叉写右下. 约简价数作角码. 总价为零去检查.
3.化学式的写法与读法
金属单质: Cu Fe Hg Mg
由原子 构成 单 质
非金属固态单质: C P S Si 稀有气体单质: He Ne Ar
直接用元素符 号表示化学式
由分子构成: H2 O2 N2 Cl2 用元素符号及其右下角的数字表示
氧化物的化学式: 如:CO2 SO2 P2O5 Fe3O4 MnO2 化 合 物 氧元素在后,另一种元素在前 金属元素和非金属组成的化合物:
如:NaCl KCl HgO MgO 金属元素在前,非金属元素在后
一 般 从 右 到 左 读 作 某 化 某
有 时 还 要 读 出 原 子 的 个 数
练一练
写出下列物质的化学式
铜 磷 氦气 四氧化三铁 氯化钠
Cu Au
金
P S
硫
He Ne
氖气
Fe3O4 HgO
氧化汞
NaCl KCI
氯化钾
读出下列物质的名称
练习:
1.下列化学式中,书写错误的是 ( A) (A)氧化钙(OCa)(B)氧化镁(MgO) (C)三氯化铁 (FeCl3)
(D)三氧化硫(SO3)
2.化学式Fe3O4的读法是 ( C )
(A)铁三氧四 (B)三铁化四氧
(C)四氧化三铁 (D)三氧化二铁
练习3
指出下列各图所表示的意义,并用 化学符号表示出来:
1、写符号 2、标化合价 P O P
+5
O
-2
+5 -2
3、化合价绝对值交叉放置元素符号右下角 4、约简 5、检查
P2 O5
练习:
已知:Al为+3价,O为-2价,写出它们的化学式
已知:C为+4价,O为-2价 ,写出它们的化学式 已知:Ca为+2价,OH为-1价,写出它们的化学式 已知:Mg为+2价,SO4为-2价,写出它们的化学式
39:55:64 78:55:64 28:4:48 128:80:2:12
求相对分子质量
H2O CO2 KMnO4 K2MnO4 NH4NO3 Cu2(OH)2CO3 1×2+16=18 12+16×2=44 39+55+16×4=158
39×2+55+16×4=197 14+1×4+14+16×3=80
一、给元素或原子团标化合价
例题1:标出下列划线部分的化合价。
+1
H2O
—1
NaCl
—1
+1
+1
K2S
—2
MgO
+1
+2
Al2O3
—2
+3
NaOH AgNO3 ZnSO4
NH4Cl CaCO3
二、根据化学式求化合价
例题2:已知O为-2价,求Fe2O3中铁元素的化合价. 解:设Fe2O3中铁元素的化合价为X 2X+(-2)× 3=0 X= 3
课题4
化学式与化合价
一、化学式
1、定义:用元素符号和数字的组 合表示物质组成的式子。
如:水的化学式为 H2O 氧气的化学式为 O2 二氧化碳的化学式为 CO2
①任何物质都有化学式吗?
只有纯净物才能用化学式表示其组成
②同种物质可以有不同的化学式吗?
一种物质只能用一个化学式来表示
③化学式可以任意的书写吗?
三、根据化学式计算
1、原子个数比: 脚标比
相对原子质量之和 2、相对分子质量(Mr): 3、元素质量比:
相对原子质量×原子个数比
4、元素的质量分数:
求原子个数比和元素质量比
2: 1 H2O 1: 2 CO2 KMnO4 1: 1 : 4 K2MnO4 2: 1 : 4 NH4NO3 2: 4: 3 Cu2(OH)2CO3 2:5:2:1 2:16 12:32
2H
3O2 2H2 4O 3SO2 Cu 2O2
4下图表示气体分子的示意图,图中红圆圈和蓝圆 圈分别表示两种不同质子数的原子,其中表示化合 物的是( D )
一些物质组成元素的原子个数比
物质
原子个数比
HCl
H2O
NaCl
Fe2O3
1:1
2:1
1:1
2:3
二、化合价
化学上用“化合价”来表示原子之间 相互化合的数目。
