《还原糖的鉴定》PPT课件
合集下载
高二生物实验一生物组织中还原糖脂肪、蛋白质的鉴定ppt

蛋白质的鉴定:
蛋白质的鉴定:
选材:黄豆种子(蛋白液) 制备组织样液:大豆组织研磨液或蛋白质稀释液
双缩脲试剂A2ml
呈色反应:组织样液2ml(无色)
震荡摇匀 双缩脲试剂 B3~4滴
紫色 结论:组织样液中有蛋白质
练习:
1、(2003年全国卷)在过氧化氢酶中加入双缩脲试
剂,其结果应该是
C
A、产生气泡 B、溶液呈蓝色
①甘蔗的茎 ②油菜籽 ③花生种子 ④梨 ⑤甜菜的块根 ⑥豆浆 ⑦鸡蛋清
A、 ④ ② ⑥ B 、⑤ ③ ⑦ C、 ① ② ⑥ D、 ④ ③ ⑥
1_植物组织成分.swf
呈色反应(加刚配置的斐林试剂)蓝色 砖红色
结论:植物组织中含有还原糖
脂肪的鉴定:
脂肪的鉴定:
取材:花生种子(浸泡3~4h),将子叶削成薄片
①取最理想的薄片
制片 ②在薄片上滴苏丹Ⅲ染液(2~3min)
③去浮色(用50﹪酒精) ④ 制成临时装片
观察:低倍镜下寻找到已着色的圆形小颗粒,然后 用高倍镜观察,可看到橘黄色圆形小颗粒 结论:脂肪能被苏丹Ⅲ染液染成橘黄色。
实验一
生物组织中还原糖、 脂肪、蛋白质的鉴定
实验原理:
实验原理:
1、还原性糖+斐林试剂 加热 砖红色沉淀
2、脂肪+苏丹Ⅲ 染液 橘黄色
脂肪+苏丹 Ⅳ 染液 红色
3、蛋白质+双缩脲试剂
紫色
方法步骤:
还原糖的鉴定:
方法步骤:
还原糖的鉴定:
选材:含糖量较高、白色或近于白色的植物组织
制备组织液 (制浆 过滤 取液)
C、溶液呈紫色 D、产生砖红色沉淀
2、用斐林试剂可以鉴定还原糖的存在,用双缩脲试 剂可以鉴定蛋白质的存在,在医学上,还常用上 述两种试剂进行疾病的诊断。能够诊断的疾病是D
《还原糖的测定》PPT课件

250------样品溶液的总体积,mL。
食品安全检验技术(理化部分) 食品中还原糖的测定
2、高锰酸钾滴定法
该法适用于各类食品中还原糖的测定,对于深色样液也 同样适用。这种方法的主要特点是准确度高,重现性好, 这两方面都优于直接滴定法。但操作复杂、费时。 (1)原理
将还原糖与过量的碱性酒石酸铜溶液反应,还原糖使 二价铜还原为氧化亚铜沉淀。经过滤取得氧化亚铜,用硫 酸铁溶液将其氧化溶解,而三价铁盐被定量地还原为亚铁 盐,再用高锰酸钾标准液滴定所产生的亚铁盐。根据高锰 酸钾标准溶液消耗量计算得氧化亚铜量,从检索表中查得 与氧化亚铜量相当的还原糖量,即可计算样品中的还原糖 含量。
ⅳ、汽水等含二氧化碳的饮料:吸取样品100.0mL于蒸 发皿中,在水浴上除去二氧化碳后,转移入250mL容量 瓶中,并用水洗涤蒸发皿,洗液并入容量瓶中,再加水 至刻度,混匀备用。
食品安全检验技术(理化部分) 食品中还原糖的测定
② 测定 吸取50.00mL处理后的样品溶液于400mL烧杯中,加碱
性酒石酸铜甲、乙液各25mL,盖上表面皿,置电炉上加热, 使其在4分钟内沸腾,再准确沸腾2分钟,趁热用铺好石棉的 古氏坩埚或G4垂融坩埚抽滤,并用60℃热水洗涤烧杯及沉 淀,至洗液不呈碱性为止。将坩埚放回原400mL烧杯中,加 25mL硫酸铁溶液及25mL水,用玻璃棒搅拌使氧化亚铜完全 溶解,以高锰酸钾标准溶液滴定至微红色为终点。记录高锰 酸钾标准溶液消耗量。
食品安全检验技术(理化部分) 食品中还原糖的测定
试剂
① 碱 性 酒 石 酸 铜 甲 液 : 称 取 15g 硫 酸 铜 ( C uSO4·5H2O) 及 0.05g次甲基蓝,溶于水中并稀释到1000 mL ②碱性酒石酸铜乙液:取50g酒石酸钾钠及75g氢氧化钠,溶 于 水 中 , 再 加 入 4g 亚 铁 氰 化 钾 , 完 全 溶 解 后 , 再 用 水 稀 到 1000 mL,储存于橡胶塞玻璃瓶内。 ③乙酸锌溶液:称取21.9g乙酸锌[Zn(CH3COO)2·2H2O],加3 mL冰醋酸 ,加水溶解并稀释1000 mL。 ④ 106g/L 亚 铁 氰 化 钾 溶 液 : 称 取 106.g 亚 铁 氰 化 钾 [K4Fe(CN)6·3H2O],溶于水中,稀释至100mL。 ⑤葡萄糖标准液:准确称取1.000 g干燥至恒量的 纯葡萄糖, 加水溶解后加入5 mL 盐酸,并以水稀释至1000 mL。 ⑥ 盐酸。
还原糖的检测和观察优选PPT文档
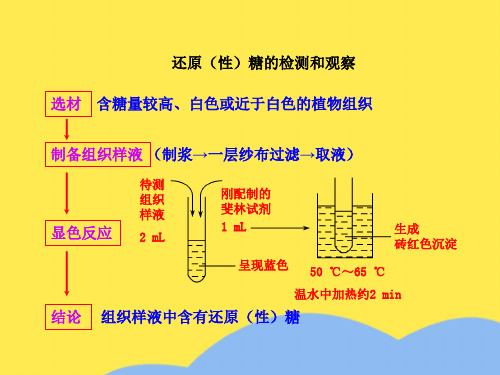
刚配制的 斐林试剂 1 mL
呈现蓝色 50 ℃~65 ℃
生成 砖红色沉淀
温水中加热约2 mi测和观察
选材 含糖量较高、白色或近于白色的植物组织
制显备色组反织 应样液 (制浆→一层纱布过滤→取液) 含组还组还( 组还含含组组还 组组还含还 含组组还含含 组组含组(含组还组(组还组含组还还糖织原织原制织原糖糖织织原织织原糖原糖织织原糖糖织织糖织制糖织原织制织原织糖织原原量 样 ( 样 ( 浆样 ( 量 量 样 样 (样 样 ( 量 (量 样 样 ( 量 量样 样 量 样 浆 量 样 ( 样 浆 样 ( 样 量 样 ( (较液性液性→ 液性较较液液性 液液性较性 较液液性较较 液液较液→较液性液→液性液较液性性高中)中)一 中)高高中中) 中中)高) 高中中)高高 中中高中一高中)中一中)中高中))、含糖含糖层 含糖、、含含糖 含含糖、糖 、含含糖、、 含含、含层、含糖含层含糖含、含糖糖白有的有的纱 有的白白有有的 有有的白的 白有有的白白 有有白有纱白有的有纱有的有白有的的色还检还检布 还检色色还还检 还还检色检 色还还检色色 还还色还布色还检还布还检还色还检检或原测原测过 原测或或原原测 原原测或测 或原原测或或 原原或原过或原测原过原测原或原测测近(和(和滤 (和近近((和 ((和近和 近((和近近 ((近(滤近(和(滤(和(近(和和于性观性观性观于于性性观性性观于观于性性观于于性性于性于性观性性观性于性观观→ →→白)察)察)察白白))察 ))察白察 白))察白白 ))白)白)察))察)白)察察取 取取色糖糖糖色色糖糖糖糖色色糖糖色色 糖糖色糖色糖糖糖糖色糖液 液液的的的的的的的 的的的) ))植植植植植植植 植植植物物物物物物物 物物物组组组组组组组 组组组待组样2织织织织织织织 织织织测织液mL
项目4-6食品中还原糖的测定ppt课件

〔2〕含脂食品〔如乳酪、巧克力、蛋黄酱杏仁糖等〕 石油醚脱脂→水提取
〔3〕含大量淀粉和糊精的食品 〔如粮谷制品、某些蔬菜、调味品〕
70%~75%的乙醇溶液提取,沉淀淀粉和糊精,不需求除 蛋白
❖ 〔4〕含酒精和二氧化碳的液体样品 ❖ 通常蒸发至原体积的1/3~1/4,以除去酒精和二氧化碳。
❖ 但是酸性食品,在加热之前应预先用氢氧化纳调理样品溶液 至中性,以防止低聚糖被部分水解。
❖ 常用的除铅剂有草酸钠、草酸钾、硫酸钠、磷酸钠、磷酸氢二纳等。
❖ ③本法是根据一定量的碱性酒石酸铜溶液〔铜离子量一定〕耗费的样液 量来计算样液中复原糖含量,反响体系中铜离子的含量是定量的根底, 所以样品在处置时,不能用铜盐〔硫酸铜-氢氧化钠〕作为廓清剂。
子工程一
黄酒中复原糖的测
定
直接滴定法 GB/T 5009.7-2021
常模糊不清。 特点:试剂用量少,操作和计算都比较简便、快速,滴定终点
比较明显
详细任务义务分解
义务1:仪器设备及试剂的预备 义务2:样品预处置 义务3:样品复原糖含量测定 义务4:结果结果数据处置 义务5:填写检验报告单
义务一、仪器设备及试剂的预备
试剂:
费林试剂甲液:(15.00g无水硫酸铜+0.05g次甲基蓝→1000mL)
Determination of carbohydate in foods
引言
❖ 食品中糖类测定是食品的主要分析工程之一,在食品工业中具有非常重 要的意义。
❖ 1、食品加工中常需求控制一定量的糖酸比 ❖ 2、糖果中糖的组成及比例直接关系到其风味和质量 ❖ 3、糖的焦糖化作用及羰氨反响既可使食品获得诱人的色泽和风味,又
❖ 〔5〕固体样品 ❖ 40~50℃的水提,温度高可溶性多糖溶出,添加廓清负担
〔3〕含大量淀粉和糊精的食品 〔如粮谷制品、某些蔬菜、调味品〕
70%~75%的乙醇溶液提取,沉淀淀粉和糊精,不需求除 蛋白
❖ 〔4〕含酒精和二氧化碳的液体样品 ❖ 通常蒸发至原体积的1/3~1/4,以除去酒精和二氧化碳。
❖ 但是酸性食品,在加热之前应预先用氢氧化纳调理样品溶液 至中性,以防止低聚糖被部分水解。
❖ 常用的除铅剂有草酸钠、草酸钾、硫酸钠、磷酸钠、磷酸氢二纳等。
❖ ③本法是根据一定量的碱性酒石酸铜溶液〔铜离子量一定〕耗费的样液 量来计算样液中复原糖含量,反响体系中铜离子的含量是定量的根底, 所以样品在处置时,不能用铜盐〔硫酸铜-氢氧化钠〕作为廓清剂。
子工程一
黄酒中复原糖的测
定
直接滴定法 GB/T 5009.7-2021
常模糊不清。 特点:试剂用量少,操作和计算都比较简便、快速,滴定终点
比较明显
详细任务义务分解
义务1:仪器设备及试剂的预备 义务2:样品预处置 义务3:样品复原糖含量测定 义务4:结果结果数据处置 义务5:填写检验报告单
义务一、仪器设备及试剂的预备
试剂:
费林试剂甲液:(15.00g无水硫酸铜+0.05g次甲基蓝→1000mL)
Determination of carbohydate in foods
引言
❖ 食品中糖类测定是食品的主要分析工程之一,在食品工业中具有非常重 要的意义。
❖ 1、食品加工中常需求控制一定量的糖酸比 ❖ 2、糖果中糖的组成及比例直接关系到其风味和质量 ❖ 3、糖的焦糖化作用及羰氨反响既可使食品获得诱人的色泽和风味,又
❖ 〔5〕固体样品 ❖ 40~50℃的水提,温度高可溶性多糖溶出,添加廓清负担
还原糖蛋白质脂肪的鉴定PPT课件

4、 另一支试管内装入蛋清组织液的作用是( )
11
三、脂肪的鉴定:
1、 取一粒浸泡3~4小时的花生种子,去皮后纵切下一些薄片(注意刀片不要 划伤手指) 2、 用毛笔将最薄的一片移到洁净的载玻片的正中央 3、 向花生薄片上滴2~3滴苏丹Ⅲ染液,染色2~3分钟后用吸水纸吸去薄片周 围的染液(染色的时间一定把握好) 4、 在薄片上滴1~2滴50%的酒精以洗去浮色,用吸水纸吸去周围的酒精 5、 在薄片上滴1~2滴蒸馏水,盖上盖玻片(盖玻片不要平放,应倾斜一定的 角度下放,以免产生气泡,若有气泡,可在一边滴蒸馏水另一边用吸水纸 吸水至无气泡止) 6、 用低倍镜寻找装片的最薄处(1~2层)并将这部分移到视野的正中央,观 察已着色的圆形小颗粒。 7、 换用高倍镜观察(注意:在使用显微镜的过程中显微镜一定要平放不可 倾斜)
4
蛋白质的鉴定原理 鉴定生物组织中是否含有 蛋白质时,常用双缩脲法,使用的是双缩脲 试剂。双缩脲试剂的成分是质量浓度为0.1 g /mL的氢氧化钠溶液和质量浓度为0.01 g/ mL的硫酸铜溶液。在碱性溶液(NaOH)中, 双缩脲(H2NOC—NH—CONH2)能与Cu2+作 用,形成紫色或紫红色的络合物,这个反应 叫做双缩脲反应。由于蛋白质分子中含有很 多与双缩脲结构相似的肽键,因此,蛋白质 可与双缩脲试剂发生颜色反应。
6
器材
显微镜、双面刀片、试管、试管夹、大 烧杯、酒精灯、三脚架、石棉网、试管 架、载玻片、吸水纸、电炉。7源自试剂配制:
斐林试剂 甲液 氢氧化钠的质量浓度0.1g/ml的溶液 乙液 硫酸铜的质量浓度0.05g/ml的溶液 使用时临时配制,将4滴~5滴乙液滴入2ml甲液中,配完立即使用。 与斐林试剂原理一样的本尼迪试剂配制后可长久保存,配方如下:无水硫酸铜1.74g溶于 100ml热水中冷却后加至150ml。取柠檬酸钠173g,无水碳酸钠100g和600ml水共热,溶 解后冷却并加水至850ml。再将冷却的150ml硫酸铜溶液倾入即可。 苏丹III溶液的配制 称取0.1g苏丹III或IV干粉,溶于50ml丙酮中,再加入70%酒精50ml即可使用。 苏丹Ⅳ溶液的配制 称取0.1 g苏丹Ⅳ干粉,溶于50 mL丙酮中,再加入体积分数为70%的 酒精50 mL,充分混合后即可使用。 双缩脲试剂的配制: 取10g氢氧化钠放入量筒中,加水至100ml,待充分溶解后倒入试剂瓶中,配成氢氧化钠的 质量浓度为0.1g/ml的溶液,瓶口上塞上胶塞,贴上标签:试剂A 取1g硫酸铜放入量筒中,加水至100ml,待充分溶解后倒入试剂瓶中,配成硫酸铜的质量 浓度为0.01g/ml的溶液(蓝色),瓶口上塞上胶塞,贴上标签:试剂B
11
三、脂肪的鉴定:
1、 取一粒浸泡3~4小时的花生种子,去皮后纵切下一些薄片(注意刀片不要 划伤手指) 2、 用毛笔将最薄的一片移到洁净的载玻片的正中央 3、 向花生薄片上滴2~3滴苏丹Ⅲ染液,染色2~3分钟后用吸水纸吸去薄片周 围的染液(染色的时间一定把握好) 4、 在薄片上滴1~2滴50%的酒精以洗去浮色,用吸水纸吸去周围的酒精 5、 在薄片上滴1~2滴蒸馏水,盖上盖玻片(盖玻片不要平放,应倾斜一定的 角度下放,以免产生气泡,若有气泡,可在一边滴蒸馏水另一边用吸水纸 吸水至无气泡止) 6、 用低倍镜寻找装片的最薄处(1~2层)并将这部分移到视野的正中央,观 察已着色的圆形小颗粒。 7、 换用高倍镜观察(注意:在使用显微镜的过程中显微镜一定要平放不可 倾斜)
4
蛋白质的鉴定原理 鉴定生物组织中是否含有 蛋白质时,常用双缩脲法,使用的是双缩脲 试剂。双缩脲试剂的成分是质量浓度为0.1 g /mL的氢氧化钠溶液和质量浓度为0.01 g/ mL的硫酸铜溶液。在碱性溶液(NaOH)中, 双缩脲(H2NOC—NH—CONH2)能与Cu2+作 用,形成紫色或紫红色的络合物,这个反应 叫做双缩脲反应。由于蛋白质分子中含有很 多与双缩脲结构相似的肽键,因此,蛋白质 可与双缩脲试剂发生颜色反应。
6
器材
显微镜、双面刀片、试管、试管夹、大 烧杯、酒精灯、三脚架、石棉网、试管 架、载玻片、吸水纸、电炉。7源自试剂配制:
斐林试剂 甲液 氢氧化钠的质量浓度0.1g/ml的溶液 乙液 硫酸铜的质量浓度0.05g/ml的溶液 使用时临时配制,将4滴~5滴乙液滴入2ml甲液中,配完立即使用。 与斐林试剂原理一样的本尼迪试剂配制后可长久保存,配方如下:无水硫酸铜1.74g溶于 100ml热水中冷却后加至150ml。取柠檬酸钠173g,无水碳酸钠100g和600ml水共热,溶 解后冷却并加水至850ml。再将冷却的150ml硫酸铜溶液倾入即可。 苏丹III溶液的配制 称取0.1g苏丹III或IV干粉,溶于50ml丙酮中,再加入70%酒精50ml即可使用。 苏丹Ⅳ溶液的配制 称取0.1 g苏丹Ⅳ干粉,溶于50 mL丙酮中,再加入体积分数为70%的 酒精50 mL,充分混合后即可使用。 双缩脲试剂的配制: 取10g氢氧化钠放入量筒中,加水至100ml,待充分溶解后倒入试剂瓶中,配成氢氧化钠的 质量浓度为0.1g/ml的溶液,瓶口上塞上胶塞,贴上标签:试剂A 取1g硫酸铜放入量筒中,加水至100ml,待充分溶解后倒入试剂瓶中,配成硫酸铜的质量 浓度为0.01g/ml的溶液(蓝色),瓶口上塞上胶塞,贴上标签:试剂B
食品的测定实验一:食品中还原糖的测定ppt课件

同时平行操作三份,后滴定的葡萄糖或其他还原糖标准溶 液的体积应控制在0.5~1.0mL以内,否则。增加预加量, 重新滴定。
Page 6 2019年7月5日9时32分
(三)样品溶液预备滴定
吸取5.0mL碱性酒石酸铜甲液及5.0mL乙液,置于150mL三 角锥瓶,加水10mL,加入玻璃珠2粒,摇匀,在电炉上加 热至沸,趁热以先快后慢的速度,从滴定管中滴加试样溶 液,并保持溶液沸腾状态,待溶液颜色变浅时,以每两秒 1滴的迅速滴定,直至溶液蓝色刚好褪去为终点,记录样 品溶液消耗体积。当样液中还原糖浓度过高时应适当稀释, 再进行测定,使每次滴定消耗样液的体积控制在与标定碱 性酒石酸铜溶液时所消耗的还原糖标准溶液的体积相近, 约在10mL左右,记录消耗样液的总体积,作为正式滴定参 考用。
Page 7 2019年7月5日9时32分
(四)、样品溶液正式滴定
吸取5.0mL碱性酒石酸甲液及5.0mL乙液,置于 150mL三角锥瓶,加水10mL,加入玻璃珠2粒, 从滴定管加入比预备测定体积少1mL的样品溶液 至三角锥瓶,摇匀,同上法滴定至终点。同法 平行操作三份。
Page 8 2019年7月5日9时32分
实验一: 食品中还原糖的测定
标准依据: GB/T5009.7-2003食品中还原糖的测定
Page 1 2019年7月5日9时32分
一、目的要求 1、学习直接滴定法测定还原糖的原理,并掌握其测定的操作技
术。 2、通过对实验结果的分析,了解影响测定准确性的因素。
二、实验原理 将等量的碱性酒石酸铜甲液,乙液混合时,立即生成天蓝色
后加入5mL盐酸,并以水稀释至1000mL。此溶液每毫升相当于1.0mg葡萄糖。 7、果糖标准溶液:按试剂6配制操作,配制每毫升标准溶液相当于1.0mg果糖。 8、乳糖标准溶液:按试剂6配制操作,配制每毫升标准溶液相当于1.0mg的乳糖。 9、转化糖标准溶液:准确称取0.9500g纯蔗糖,用100mL水溶解,置于具塞三角瓶
Page 6 2019年7月5日9时32分
(三)样品溶液预备滴定
吸取5.0mL碱性酒石酸铜甲液及5.0mL乙液,置于150mL三 角锥瓶,加水10mL,加入玻璃珠2粒,摇匀,在电炉上加 热至沸,趁热以先快后慢的速度,从滴定管中滴加试样溶 液,并保持溶液沸腾状态,待溶液颜色变浅时,以每两秒 1滴的迅速滴定,直至溶液蓝色刚好褪去为终点,记录样 品溶液消耗体积。当样液中还原糖浓度过高时应适当稀释, 再进行测定,使每次滴定消耗样液的体积控制在与标定碱 性酒石酸铜溶液时所消耗的还原糖标准溶液的体积相近, 约在10mL左右,记录消耗样液的总体积,作为正式滴定参 考用。
Page 7 2019年7月5日9时32分
(四)、样品溶液正式滴定
吸取5.0mL碱性酒石酸甲液及5.0mL乙液,置于 150mL三角锥瓶,加水10mL,加入玻璃珠2粒, 从滴定管加入比预备测定体积少1mL的样品溶液 至三角锥瓶,摇匀,同上法滴定至终点。同法 平行操作三份。
Page 8 2019年7月5日9时32分
实验一: 食品中还原糖的测定
标准依据: GB/T5009.7-2003食品中还原糖的测定
Page 1 2019年7月5日9时32分
一、目的要求 1、学习直接滴定法测定还原糖的原理,并掌握其测定的操作技
术。 2、通过对实验结果的分析,了解影响测定准确性的因素。
二、实验原理 将等量的碱性酒石酸铜甲液,乙液混合时,立即生成天蓝色
后加入5mL盐酸,并以水稀释至1000mL。此溶液每毫升相当于1.0mg葡萄糖。 7、果糖标准溶液:按试剂6配制操作,配制每毫升标准溶液相当于1.0mg果糖。 8、乳糖标准溶液:按试剂6配制操作,配制每毫升标准溶液相当于1.0mg的乳糖。 9、转化糖标准溶液:准确称取0.9500g纯蔗糖,用100mL水溶解,置于具塞三角瓶
还原糖含量的测定ppt课件
3显色和比色按下表操作管号还原糖总糖样品量ml2010蒸馏水ml010dns试剂ml1515加热同时一起在沸水浴中加热5min冷却立即用流动冷水冷却至室温蒸馏水ml215215吸光值a540结果处理以以12号管的吸光值分别在标准曲线上查出相应的还原糖毫克数
实验六 还原糖和总糖含量的测定 (3,5-二硝基水杨酸比色法)
方可离开。 7、值日生打扫干净实验室后,方可离开。
13
4
5
操作步骤 1、绘制葡萄糖标准曲线
管号
0 1 2 3456
葡萄糖液(ml) 0 0.2 0.4 0.6 0.81.6 1.4 1.2 1.0 0.8
DNS试剂(ml) 1.5 1.5 1.5 1.5 1.5 1.5 1.5
加热
同时一起在沸水浴中加热5min*
9
待水解液冷却至室温后加入1滴酚酞指示 剂,用6mol/L NaOH中和至微红色,在 4000rpm、5分钟条件下离心,得到的上 清液转移到100ml容量瓶中,用蒸馏水定 容至刻度,上下颠倒几次混匀溶液,作为 总糖待测液。
10
(3)显色和比色,按下表操作
管号 样品量(ml) 蒸馏水(ml) DNS试剂(ml) 加热
8
(2)提取样品中的总糖: 准确称取0.1g食用面粉放置于100ml三角 瓶中,加入10ml 6mol/L HCl及15ml蒸馏 水,沸水浴30分钟(注意不能把水烧干)。 用滴管吸取1~2滴水解液于白瓷板上,加1 滴I-KI溶液,如显示出蓝色说明水解不完全, 可适当延长沸水浴时间;若不显蓝色,则 说明水解完全。
7
2、测定样品中还原糖和总糖含量。
(1)提取样品中的还原糖:
准确称取1g食用面粉放置于100ml三角瓶 中,加少量蒸馏水调成糊状,再加入50ml 蒸馏水,摇匀,置于50℃水浴条件下20分 钟,使还原糖浸出;在4000rpm、5分钟条 件下进行离心,得到的上清液倒入100ml容 量瓶中,用蒸馏水定容至刻度,上下颠倒 几次将溶液混匀,作为还原糖待测液。
实验六 还原糖和总糖含量的测定 (3,5-二硝基水杨酸比色法)
方可离开。 7、值日生打扫干净实验室后,方可离开。
13
4
5
操作步骤 1、绘制葡萄糖标准曲线
管号
0 1 2 3456
葡萄糖液(ml) 0 0.2 0.4 0.6 0.81.6 1.4 1.2 1.0 0.8
DNS试剂(ml) 1.5 1.5 1.5 1.5 1.5 1.5 1.5
加热
同时一起在沸水浴中加热5min*
9
待水解液冷却至室温后加入1滴酚酞指示 剂,用6mol/L NaOH中和至微红色,在 4000rpm、5分钟条件下离心,得到的上 清液转移到100ml容量瓶中,用蒸馏水定 容至刻度,上下颠倒几次混匀溶液,作为 总糖待测液。
10
(3)显色和比色,按下表操作
管号 样品量(ml) 蒸馏水(ml) DNS试剂(ml) 加热
8
(2)提取样品中的总糖: 准确称取0.1g食用面粉放置于100ml三角 瓶中,加入10ml 6mol/L HCl及15ml蒸馏 水,沸水浴30分钟(注意不能把水烧干)。 用滴管吸取1~2滴水解液于白瓷板上,加1 滴I-KI溶液,如显示出蓝色说明水解不完全, 可适当延长沸水浴时间;若不显蓝色,则 说明水解完全。
7
2、测定样品中还原糖和总糖含量。
(1)提取样品中的还原糖:
准确称取1g食用面粉放置于100ml三角瓶 中,加少量蒸馏水调成糊状,再加入50ml 蒸馏水,摇匀,置于50℃水浴条件下20分 钟,使还原糖浸出;在4000rpm、5分钟条 件下进行离心,得到的上清液倒入100ml容 量瓶中,用蒸馏水定容至刻度,上下颠倒 几次将溶液混匀,作为还原糖待测液。
还原糖的鉴定(最全版)PTT文档
B液 质量浓度为的CuSO4溶液 2、双缩脲试剂
A液 质量浓度的NaOH溶液
B液 质量浓度的CuSO4溶液 3、苏丹III
苏丹III干粉,溶于100mL体积分数为95%的酒 精中,待全部溶解后再使用。
四、实验步骤 1、可溶性还原糖的鉴定
制备生物组织样液 取材、研磨、过滤 取样
取2ml组织样液注入试管
砖红色沉淀
4、观察。
2、脂肪+苏丹III A液 质量浓度为的NaOH溶液
A液 质量浓度的NaOH溶液 取2ml组织样液注入试管
橘黄色
脂肪+苏丹IV
红色
3、蛋白质+双缩脲试剂
紫色反应
二、实验材料:
鉴定的有机物
滴入3~4滴双缩脲
适宜材料
选用的材料
某些化学试剂能够使生物组织中的有关有机化合物,产生特定的颜色反应。
还原糖的鉴定
显微镜的使用
1、安放; 3、调焦;
2、对光; 4、观察。
实验一: 生物组织中可溶性还原糖、脂肪、 蛋白质的鉴定
一、实验原理:
如用酒精灯直接加热,Cu2O沉淀颗粒较小,呈现黄色。
某些化学试剂能够使生物组织中的有关有机化 加热(煮沸2min),观察
可溶性还原糖的鉴定原理: 加热(煮沸2min),观察
花生种子
取一支试管注入
加热(煮沸2min),观察
如用酒精灯直接加热,Cu2O沉淀颗粒较小,呈现黄色。
B液 质量浓度的CuSO4溶液
Байду номын сангаас蛋白质
富含蛋白质的 生物组织
豆浆
• 深入原理
1.可溶性还原糖的鉴定原理:
生物组织中常见的可溶性糖有葡萄糖、果糖、 麦芽糖、蔗糖。前三种糖分子中都含有游离的 具有还原性的半缩醛羟基,因此叫还原性糖, 而蔗糖的分子中没有,因此叫非还原性糖。
A液 质量浓度的NaOH溶液
B液 质量浓度的CuSO4溶液 3、苏丹III
苏丹III干粉,溶于100mL体积分数为95%的酒 精中,待全部溶解后再使用。
四、实验步骤 1、可溶性还原糖的鉴定
制备生物组织样液 取材、研磨、过滤 取样
取2ml组织样液注入试管
砖红色沉淀
4、观察。
2、脂肪+苏丹III A液 质量浓度为的NaOH溶液
A液 质量浓度的NaOH溶液 取2ml组织样液注入试管
橘黄色
脂肪+苏丹IV
红色
3、蛋白质+双缩脲试剂
紫色反应
二、实验材料:
鉴定的有机物
滴入3~4滴双缩脲
适宜材料
选用的材料
某些化学试剂能够使生物组织中的有关有机化合物,产生特定的颜色反应。
还原糖的鉴定
显微镜的使用
1、安放; 3、调焦;
2、对光; 4、观察。
实验一: 生物组织中可溶性还原糖、脂肪、 蛋白质的鉴定
一、实验原理:
如用酒精灯直接加热,Cu2O沉淀颗粒较小,呈现黄色。
某些化学试剂能够使生物组织中的有关有机化 加热(煮沸2min),观察
可溶性还原糖的鉴定原理: 加热(煮沸2min),观察
花生种子
取一支试管注入
加热(煮沸2min),观察
如用酒精灯直接加热,Cu2O沉淀颗粒较小,呈现黄色。
B液 质量浓度的CuSO4溶液
Байду номын сангаас蛋白质
富含蛋白质的 生物组织
豆浆
• 深入原理
1.可溶性还原糖的鉴定原理:
生物组织中常见的可溶性糖有葡萄糖、果糖、 麦芽糖、蔗糖。前三种糖分子中都含有游离的 具有还原性的半缩醛羟基,因此叫还原性糖, 而蔗糖的分子中没有,因此叫非还原性糖。
检测生物组织中的还原性糖、脂肪和蛋白质ppt 中图版精选教学PPT课件
生物组织中的有机物与某些化学试剂能够产生特定的颜色反应:
1.葡萄糖+班氏试剂
砖红色沉淀
2.脂肪+苏丹Ⅲ染液―→橘黄色
3.蛋白质+双缩脲试剂―→紫色
1.还原糖的鉴定
2.脂肪的鉴定
3.蛋白质的鉴定
实验中所用的试剂: (1)班氏试剂 配制方法为: ①甲液:无水硫酸铜1.74 g(含水的硫酸铜也可,用量须另行计算)溶于100 mL热水中,冷却后稀释至150 mL。 ②乙液:取柠檬酸钠173 g,无水碳酸钠100 g和600 mL水共热,溶解后冷 却并加水至850 mL。 ③将甲液倒入乙液中,边倒边搅拌。此试剂配好后可长期使用。 实质:Cu2+与还原性糖共热生成砖红色沉淀。
(4)两支试管中的溶液都变为紫色 (5)酶的化学本质是蛋白质
第 一 单 元 有 机 体 中 的 细 胞
,又何必对未知的前方魂牵梦萦?生活中,其实我们每个人都有目标,并且我们的奋斗,都是为了能离它更近。奋斗努力,快步走行,无可厚非,但是我想,人生在路上行走,本应该走走停
生 物 同时,适时的放慢脚步,看看你的身(边,中看图看你版的周·必围,修欣1赏)一下沿途的美丽风景,也许里面就有会你想要的东西。不要为了追求物质财富,不要忙于到达目的地,只顾疲于奔跑,而错过了
多开心和快乐。人生不如意事十之八九,如若我们不抱怨,湖涂一些,淡然一点,烦恼就会少些,日子即便是平庸,但也能活得踏实、安稳、快乐。在时间的渡口,我们都是匆匆的过客,多
生香,。
走在人生路上,最宝贵的是你的微笑。人的一生会遭遇许多坎坷,经历许多风雨,纵然前面充满荆棘,也必须走下去。微笑着,无论是在平淡的日子里,还是在迷茫低落的时候,都让自 笑着,证明了你对未来充满着信心,眼前的困难只是暂时的,没什么可畏惧!微笑着,证明了你的意志是无比的坚强,既然确定了目标就去奋斗,一切的阻挠都显得可笑和无力,丝毫都不能
1.葡萄糖+班氏试剂
砖红色沉淀
2.脂肪+苏丹Ⅲ染液―→橘黄色
3.蛋白质+双缩脲试剂―→紫色
1.还原糖的鉴定
2.脂肪的鉴定
3.蛋白质的鉴定
实验中所用的试剂: (1)班氏试剂 配制方法为: ①甲液:无水硫酸铜1.74 g(含水的硫酸铜也可,用量须另行计算)溶于100 mL热水中,冷却后稀释至150 mL。 ②乙液:取柠檬酸钠173 g,无水碳酸钠100 g和600 mL水共热,溶解后冷 却并加水至850 mL。 ③将甲液倒入乙液中,边倒边搅拌。此试剂配好后可长期使用。 实质:Cu2+与还原性糖共热生成砖红色沉淀。
(4)两支试管中的溶液都变为紫色 (5)酶的化学本质是蛋白质
第 一 单 元 有 机 体 中 的 细 胞
,又何必对未知的前方魂牵梦萦?生活中,其实我们每个人都有目标,并且我们的奋斗,都是为了能离它更近。奋斗努力,快步走行,无可厚非,但是我想,人生在路上行走,本应该走走停
生 物 同时,适时的放慢脚步,看看你的身(边,中看图看你版的周·必围,修欣1赏)一下沿途的美丽风景,也许里面就有会你想要的东西。不要为了追求物质财富,不要忙于到达目的地,只顾疲于奔跑,而错过了
多开心和快乐。人生不如意事十之八九,如若我们不抱怨,湖涂一些,淡然一点,烦恼就会少些,日子即便是平庸,但也能活得踏实、安稳、快乐。在时间的渡口,我们都是匆匆的过客,多
生香,。
走在人生路上,最宝贵的是你的微笑。人的一生会遭遇许多坎坷,经历许多风雨,纵然前面充满荆棘,也必须走下去。微笑着,无论是在平淡的日子里,还是在迷茫低落的时候,都让自 笑着,证明了你对未来充满着信心,眼前的困难只是暂时的,没什么可畏惧!微笑着,证明了你的意志是无比的坚强,既然确定了目标就去奋斗,一切的阻挠都显得可笑和无力,丝毫都不能
还原性糖的测定课件
《还原性糖的测定》PPT课件
3.试剂 p68 ① 碱性酒石酸铜甲液:硫酸铜+次甲基蓝. ② 碱性酒石酸铜乙液:酒石酸钾钠 + NaOH + 亚铁氰化钾 ③ 乙酸锌溶液 ④ 亚铁氰化钾溶液 ⑤ 葡萄糖标准溶液:准确称取经 98 ~ 100 ℃ 干燥至恒重的无水葡萄糖1.0000g,加水溶解后移入1000 m1容量瓶中,加入5m1盐酸(防止微生物生长)。
பைடு நூலகம்还原性糖的测定》PPT课件
GB/T 5009.7—2003《食品中还原糖的测定》 1. 直接滴定法(先标定再测定) 2. 高锰酸钾法
《还原性糖的测定》PPT课件
粗纤维的测定 P58
粗纤维是植物性食品的主要成分之一,广泛存在于各种植物体内。化学上不是单一组分,是混合物。 1. 粗纤维——主要成分是纤维素、半纤维素、木质素及少量含N物。集中存在于谷类的麸、糠、秸杆、果蔬的表皮等处。 对稀酸、稀碱难溶,人体不能消化利用的部分。
化学法
还原糖法
碘量法
比色法
《还原性糖的测定》PPT课件
第二节 可溶性糖类的测定
一、可溶性糖类的提取和澄清 食品中可溶性糖类通常是指葡萄糖、果糖等游离单糖及蔗糖等低聚糖。一般须将样品磨碎、浸渍成溶液(提取液),经过滤后再测定。 (一)提取 1. 常用的提取剂有水及乙醇溶液。 2. 提取液制备的原则 ⑴ 取样量与稀释倍数的确定,使(0.5—3.5mg / ml)。 ⑵ 含脂肪的食品,须经脱脂后再用水提取。
膳食纤维素测定仪
《还原性糖的测定》PPT课件
二、不溶性膳食纤维的测定
1.原理 样品经热的中性洗涤剂浸煮后,残渣用热蒸馏水充分洗涤,除去样品中游离淀粉、蛋白质、矿物质,然后加入α一淀粉酶溶液以分解结合态淀粉,再用蒸馏水、丙酮洗涤,以除去残存的脂肪、色素等,残渣经烘干,即为中性洗涤纤维 (不溶性膳食纤维)。
3.试剂 p68 ① 碱性酒石酸铜甲液:硫酸铜+次甲基蓝. ② 碱性酒石酸铜乙液:酒石酸钾钠 + NaOH + 亚铁氰化钾 ③ 乙酸锌溶液 ④ 亚铁氰化钾溶液 ⑤ 葡萄糖标准溶液:准确称取经 98 ~ 100 ℃ 干燥至恒重的无水葡萄糖1.0000g,加水溶解后移入1000 m1容量瓶中,加入5m1盐酸(防止微生物生长)。
பைடு நூலகம்还原性糖的测定》PPT课件
GB/T 5009.7—2003《食品中还原糖的测定》 1. 直接滴定法(先标定再测定) 2. 高锰酸钾法
《还原性糖的测定》PPT课件
粗纤维的测定 P58
粗纤维是植物性食品的主要成分之一,广泛存在于各种植物体内。化学上不是单一组分,是混合物。 1. 粗纤维——主要成分是纤维素、半纤维素、木质素及少量含N物。集中存在于谷类的麸、糠、秸杆、果蔬的表皮等处。 对稀酸、稀碱难溶,人体不能消化利用的部分。
化学法
还原糖法
碘量法
比色法
《还原性糖的测定》PPT课件
第二节 可溶性糖类的测定
一、可溶性糖类的提取和澄清 食品中可溶性糖类通常是指葡萄糖、果糖等游离单糖及蔗糖等低聚糖。一般须将样品磨碎、浸渍成溶液(提取液),经过滤后再测定。 (一)提取 1. 常用的提取剂有水及乙醇溶液。 2. 提取液制备的原则 ⑴ 取样量与稀释倍数的确定,使(0.5—3.5mg / ml)。 ⑵ 含脂肪的食品,须经脱脂后再用水提取。
膳食纤维素测定仪
《还原性糖的测定》PPT课件
二、不溶性膳食纤维的测定
1.原理 样品经热的中性洗涤剂浸煮后,残渣用热蒸馏水充分洗涤,除去样品中游离淀粉、蛋白质、矿物质,然后加入α一淀粉酶溶液以分解结合态淀粉,再用蒸馏水、丙酮洗涤,以除去残存的脂肪、色素等,残渣经烘干,即为中性洗涤纤维 (不溶性膳食纤维)。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
用其它热源加热不易控制温度,很容易 导致反应失败,而且斐林试剂里的蓝色 氢氧化铜沉淀热稳定性较差,受热 (80℃以上)很容易分解生成黑色的氧 化铜沉淀和水,不能生成砖红色氧化亚 铜沉淀。
反应过程
热水浴 还原糖(葡萄糖、果糖) +菲林试
变色
剂 2-3min
2.用斐林试剂鉴定可溶性还原糖 时,溶液颜色变化过程 为
生物组织中普遍存在的还原糖种类较多, 常见的有葡萄糖、果糖、麦芽糖。它们的 分子内都含有还原性基团(游离醛基或游 离酮基)。这些还原性基团能够与试剂中 的基团反应,并有明显的现象。
还原糖与菲林试剂反应过程
水浴加热
还原糖(葡萄糖、果糖)+菲林试剂 ?
砖红色
2-3min
鉴定可溶性还原糖为什么要 水浴加热?
A.浅蓝色 棕色 砖红色
B.无色 浅蓝色 棕色
C.砖红色 D.棕色
浅蓝色 绿色
棕色 无色
实验步骤
斐林试剂由质量浓度为0.1g/mL的氢氧化 钠溶液和质量浓度为0.05g/mL的硫酸铜 溶液配制而成,二者混合后,立即生成淡 蓝色的Cu(OH)2沉淀。Cu(OH)2与加入的葡 萄糖在加热的条件下,能够生成砖红色的 Cu2O沉淀,而葡萄糖本身则氧化成葡萄糖 酸。
2、下列哪组试剂在使用过程中,必须加热:
A.斐林试剂鉴定可溶性还原糖的过程中 B.苏丹Ⅲ染液在鉴定动物组织中的脂肪时 C.双缩脲试剂鉴定蛋白质时
D.碘化钾溶液鉴定淀粉时 ( A )
3 还原糖与菲林试剂生成的产物是()
A CuO B Cu2O C Cu D CuO2
生物组织中可溶性 还原糖的鉴定实验
白糖
盐
味精
还原糖的鉴定方法
1 物理学方法:观察颜色、状态、气味; 直接品尝
小苏打/NaHCO3 元明粉/Na2SO4
葡萄糖
还原糖的鉴定方法
1 物理学方法:观察颜色、状态、气味; 直接品尝
2 化学方法: 斐林试剂、班氏试剂、银氨溶液等.
化学方法鉴定原理
二、实验步骤与现象
1.可溶性还原糖
选材:含糖量较高的白色或近于白色,苹果、梨最好 。
制浆:去皮、切块、研磨
制备组织样液: 过滤:(用单层纱布)
显色反应
取液:(2mL)
现象:
1、为什么要选白色或近于白色的材料进行试验? 答:减少试验材料对试验现象的干扰,使得试验
现象明显。
2、为什么加入组织样液与菲林试剂后溶液或显 蓝色?
答:菲林试剂中的Cu(OH)2在溶液中显蓝色。
反应式
CH2OH—(CHOH)4—CHO+2Cu(OH)2 →
CH2OH—(CHOH)4—COOH+Cu2O↓+2H2O 砖红色沉淀
三种试剂现象对比
试剂 菲林试剂 班氏试剂 银氨溶液
现象
砖红色 沉淀
砖红色沉 淀
出现银镜
课堂练习:
1、某些单子叶植物,如韭菜、鸢尾的叶子内含 有大量的可溶性还原糖,但这些单子叶植物的叶 子不宜作实验材料,原因是:这些叶子的颜色较深, 对还原性糖与斐林试剂的颜色反应起遮蔽作用
反应过程
热水浴 还原糖(葡萄糖、果糖) +菲林试
变色
剂 2-3min
2.用斐林试剂鉴定可溶性还原糖 时,溶液颜色变化过程 为
生物组织中普遍存在的还原糖种类较多, 常见的有葡萄糖、果糖、麦芽糖。它们的 分子内都含有还原性基团(游离醛基或游 离酮基)。这些还原性基团能够与试剂中 的基团反应,并有明显的现象。
还原糖与菲林试剂反应过程
水浴加热
还原糖(葡萄糖、果糖)+菲林试剂 ?
砖红色
2-3min
鉴定可溶性还原糖为什么要 水浴加热?
A.浅蓝色 棕色 砖红色
B.无色 浅蓝色 棕色
C.砖红色 D.棕色
浅蓝色 绿色
棕色 无色
实验步骤
斐林试剂由质量浓度为0.1g/mL的氢氧化 钠溶液和质量浓度为0.05g/mL的硫酸铜 溶液配制而成,二者混合后,立即生成淡 蓝色的Cu(OH)2沉淀。Cu(OH)2与加入的葡 萄糖在加热的条件下,能够生成砖红色的 Cu2O沉淀,而葡萄糖本身则氧化成葡萄糖 酸。
2、下列哪组试剂在使用过程中,必须加热:
A.斐林试剂鉴定可溶性还原糖的过程中 B.苏丹Ⅲ染液在鉴定动物组织中的脂肪时 C.双缩脲试剂鉴定蛋白质时
D.碘化钾溶液鉴定淀粉时 ( A )
3 还原糖与菲林试剂生成的产物是()
A CuO B Cu2O C Cu D CuO2
生物组织中可溶性 还原糖的鉴定实验
白糖
盐
味精
还原糖的鉴定方法
1 物理学方法:观察颜色、状态、气味; 直接品尝
小苏打/NaHCO3 元明粉/Na2SO4
葡萄糖
还原糖的鉴定方法
1 物理学方法:观察颜色、状态、气味; 直接品尝
2 化学方法: 斐林试剂、班氏试剂、银氨溶液等.
化学方法鉴定原理
二、实验步骤与现象
1.可溶性还原糖
选材:含糖量较高的白色或近于白色,苹果、梨最好 。
制浆:去皮、切块、研磨
制备组织样液: 过滤:(用单层纱布)
显色反应
取液:(2mL)
现象:
1、为什么要选白色或近于白色的材料进行试验? 答:减少试验材料对试验现象的干扰,使得试验
现象明显。
2、为什么加入组织样液与菲林试剂后溶液或显 蓝色?
答:菲林试剂中的Cu(OH)2在溶液中显蓝色。
反应式
CH2OH—(CHOH)4—CHO+2Cu(OH)2 →
CH2OH—(CHOH)4—COOH+Cu2O↓+2H2O 砖红色沉淀
三种试剂现象对比
试剂 菲林试剂 班氏试剂 银氨溶液
现象
砖红色 沉淀
砖红色沉 淀
出现银镜
课堂练习:
1、某些单子叶植物,如韭菜、鸢尾的叶子内含 有大量的可溶性还原糖,但这些单子叶植物的叶 子不宜作实验材料,原因是:这些叶子的颜色较深, 对还原性糖与斐林试剂的颜色反应起遮蔽作用
