β内酰胺酶抑制剂的临床应用
β-内酰胺类抗生素β内酰胺酶抑制剂复方制剂临床应用专家共识(2020年版)

β-内酰胺类抗生素β内酰胺酶抑制剂复方制剂临床应用专家共识(2020年版)一、概述革兰阴性菌及少数革兰阳性菌对β-内酰胺类抗生素耐药的最重要机制是产生各种β-内酰胺酶。
β-内酰胺酶抑制剂能够抑制部分β-内酰胺酶,避免β-内酰胺类抗生素被水解而失活。
因此,β-内酰胺类抗生素/β-内酰胺酶抑制剂复方制剂(简称β-内酰胺酶抑制剂复方制剂)是临床治疗产β-内酰胺酶细菌感染的重要选择。
我国临床使用的β-内酰胺酶抑制剂复方制剂的种类和规格繁多,临床工作者对该类制剂的特点了解参差不齐,临床不合理使用问题比较突出。
二、主要β-内酰胺酶及产酶菌流行情况β-内酰胺酶是由细菌产生的,能水解β-内酰胺类抗生素的一大类酶。
β-内酰胺酶种类繁多,有多种分类方法,最主要的分类方法有两种:一、是根据β-内酰胺酶的底物、生化特性及是否被酶抑制剂所抑制的功能分类法(Bush分类法),其将β-内酰胺酶分为青霉素酶、广谱酶、超广谱β-内酰胺酶(ESBLs)、头孢菌素酶(AmpC酶)和碳青霉烯酶等;二、是根据β-内酰胺酶末端的氨基酸序列特征的分子生物学分类法(Ambler分类法),将β-内酰胺酶分为丝氨酸酶(包括A类、C类酶和D 类酶)及金属酶(B类酶)。
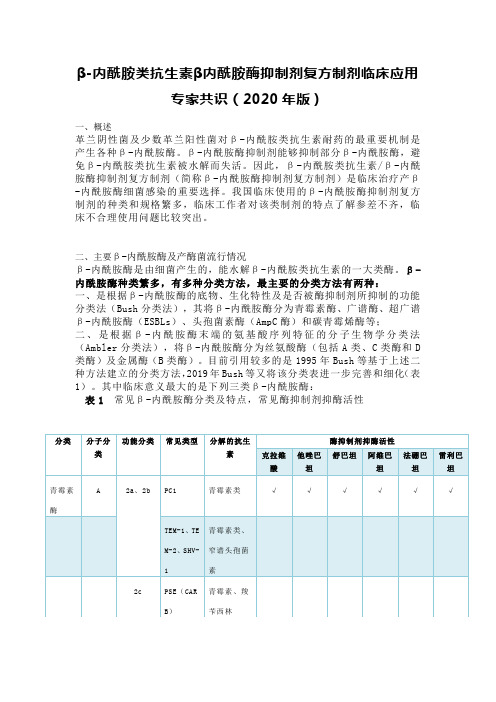
目前引用较多的是1995年Bush等基于上述二种方法建立的分类方法,2019年Bush等又将该分类表进一步完善和细化(表1)。
其中临床意义最大的是下列三类β-内酰胺酶:表1 常见β-内酰胺酶分类及特点,常见酶抑制剂抑酶活性1、ESBLs主要属2be\2br\2ber类酶,是由质粒介导的能水解青霉素类、头孢菌素及单环酰胺类等β-内酰胺类抗生素的β-内酰胺酶,其对碳青霉烯类和头霉素类水解能力弱。
ESBLs主要由肠杆菌科细菌产生,以肺炎克雷伯菌、大肠埃希菌、变形杆菌最为常见。
根据编码基因的同源性,ESBLs可分为TEM型、SHV型、CTX-M 型、OXA型和其他型共5大类型。
2、AmpC酶属C类酶,通常由染色体介导,可以被β-内酰胺类抗生素诱导。
β-内酰胺类抗生素β内酰胺酶抑制剂复方制剂临床应用专家共识

β-内酰胺类抗生素β内酰胺酶抑制剂复方制剂临床应用专家共识(2020年版)一、概述革兰阴性菌及少数革兰阳性菌对β-内酰胺类抗生素耐药的最重要机制是产生各种β-内酰胺酶。
β-内酰胺酶抑制剂能够抑制部分β-内酰胺酶,避免β-内酰胺类抗生素被水解而失活。
因此,β-内酰胺类抗生素/β-内酰胺酶抑制剂复方制剂(简称β-内酰胺酶抑制剂复方制剂)是临床治疗产β-内酰胺酶细菌感染的重要选择。
我国临床使用的β-内酰胺酶抑制剂复方制剂的种类和规格繁多,临床工作者对该类制剂的特点了解参差不齐,临床不合理使用问题比较突出。
二、主要β-内酰胺酶及产酶菌流行情况β-内酰胺酶是由细菌产生的,能水解β-内酰胺类抗生素的一大类酶。
β-内酰胺酶种类繁多,有多种分类方法,最主要的分类方法有两种:一、是根据β-内酰胺酶的底物、生化特性及是否被酶抑制剂所抑制的功能分类法(Bush分类法),其将β-内酰胺酶分为青霉素酶、广谱酶、超广谱β-内酰胺酶(ESBLs)、头孢菌素酶(AmpC酶)和碳青霉烯酶等;二、是根据β-内酰胺酶末端的氨基酸序列特征的分子生物学分类法(Ambler 分类法),将β-内酰胺酶分为丝氨酸酶(包括A类、C类酶和D类酶)及金属酶(B类酶)。
目前引用较多的是1995年Bush等基于上述二种方法建立的分类方法,2019年Bush等又将该分类表进一步完善和细化(表1)。
其中临床意义最大的是下列三类β-内酰胺酶:表1常见β-内酰胺酶分类及特点,常见酶抑制剂抑酶活性1、ESBLs主要属2be\2br\2ber类酶,是由质粒介导的能水解青霉素类、头孢菌素及单环酰胺类等β-内酰胺类抗生素的β-内酰胺酶,其对碳青霉烯类和头霉素类水解能力弱。
ESBLs主要由肠杆菌科细菌产生,以肺炎克雷伯菌、大肠埃希菌、变形杆菌最为常见。
根据编码基因的同源性,ESBLs可分为TEM型、SHV型、CTX-M型、OXA型和其他型共5大类型。
2、AmpC酶属C类酶,通常由染色体介导,可以被β-内酰胺类抗生素诱导。
常用抗菌药物的临床应用

常用抗菌药物的临床应用首都医科大学附属北京朝阳医院于晓敏一、前言抗生素是具有抗病原体活性的一大类物质,自 1940 年以来,青霉素应用于临床,现抗生素的种类已达几千种,在临床上常用的亦有几百种。
抗菌素是指对细菌和微生物具有抑制和杀灭作用的一类抗生素,而抗菌药物主要是杀灭细菌的。
抗生素是比较广义的,抗菌药物是比较专一的。
二、临床常用抗菌药物及应用要点抗生素的作用机制如( ppt4 图片所示,抗生素通过作用于细菌不同的部位从而起到抗菌的作用。
抗生素从作用上来讲,可以分为杀菌剂和抑菌剂两大类。
(一杀菌剂1. b 内酰胺类抗生素β - 酰胺类抗生素有一个共性就是均有β酰胺环可被β内酰胺酶水解而失效。
其作用机制是通过抑制细胞壁的合成,达到杀菌的目的。
影响其作用的因素有抗生素的浓度以及作用剂量、抗生素透过细胞膜的能力、对 b 内酰胺酶作用的抵抗力以及和靶位的亲和力,抗生素的血药浓度与给药方法有关,β内酰胺酶是有时间依赖性的,一般每 4~6 小时一次。
( ppt8 图片显示的是用时间浓度曲线演示β - 内酰胺酶抗生素的给药方法。
b 内酰胺类抗生素目前主要有青霉素类、头孢菌素类、碳青霉烯类、头霉素、单环类和β内酰胺酶抑制剂等。
( 1 青霉素类的药物①主要抗革兰阳性菌:对青霉毒酶不稳定,可出现严重过敏反应,治疗革兰阳性球菌(葡萄球菌除外、奈瑟菌属和梅毒的首选药物。
青霉素 V :耐酸,口服,活性较青霉素 G 差。
青霉素 G :注射,剂量 160-960 万 U/ 日 , 个别脑膜炎用量可 >1000 万 U/ 日,要分次给,每次 <500 万 U ,主要用于 G(+ 菌。
②耐酶青霉素:抗菌谱同耐青霉素酶,主要治疗产酶的金葡菌、耐甲氧西林金葡菌( MRSA 。
常用的为苯唑西林、氯唑西林。
③广谱青霉素:对革兰阳性、阴性菌均有效,对青霉素酶不稳定。
如氨苄西林和阿莫西林,对阴性菌活性强,但易被 b 内酰胺酶破坏。
β-内酰胺类抗生素β内酰胺酶抑制剂复方制剂临床应用专家共识(2020年版)
β-内酰胺类抗生素β内酰胺酶抑制剂复方制剂临床应用专家共识(2020年版)一、概述革兰阴性菌及少数革兰阳性菌对β-内酰胺类抗生素耐药的最重要机制是产生各种β-内酰胺酶。
β-内酰胺酶抑制剂能够抑制部分β-内酰胺酶,避免β-内酰胺类抗生素被水解而失活。
因此,β-内酰胺类抗生素/β-内酰胺酶抑制剂复方制剂(简称β-内酰胺酶抑制剂复方制剂)是临床治疗产β-内酰胺酶细菌感染的重要选择。
我国临床使用的β-内酰胺酶抑制剂复方制剂的种类和规格繁多,临床工作者对该类制剂的特点了解参差不齐,临床不合理使用问题比较突出。
二、主要β-内酰胺酶及产酶菌流行情况β-内酰胺酶是由细菌产生的,能水解β-内酰胺类抗生素的一大类酶。
β-内酰胺酶种类繁多,有多种分类方法,最主要的分类方法有两种:一、是根据β-内酰胺酶的底物、生化特性及是否被酶抑制剂所抑制的功能分类法(Bush分类法),其将β-内酰胺酶分为青霉素酶、广谱酶、超广谱β-内酰胺酶(ESBLs)、头孢菌素酶(AmpC酶)和碳青霉烯酶等;二、是根据β-内酰胺酶末端的氨基酸序列特征的分子生物学分类法(Ambler分类法),将β-内酰胺酶分为丝氨酸酶(包括A类、C类酶和D 类酶)及金属酶(B类酶)。
目前引用较多的是1995年Bush等基于上述二种方法建立的分类方法,2019年Bush等又将该分类表进一步完善和细化(表1)。
其中临床意义最大的是下列三类β-内酰胺酶:表1 常见β-内酰胺酶分类及特点,常见酶抑制剂抑酶活性素及单环酰胺类等β-内酰胺类抗生素的β-内酰胺酶,其对碳青霉烯类和头霉素类水解能力弱。
ESBLs主要由肠杆菌科细菌产生,以肺炎克雷伯菌、大肠埃希菌、变形杆菌最为常见。
根据编码基因的同源性,ESBLs可分为TEM型、SHV型、CTX-M 型、OXA型和其他型共5大类型。
2、AmpC酶属C类酶,通常由染色体介导,可以被β-内酰胺类抗生素诱导。
部分由质粒介导,常呈持续高水平表达。
β-内酰胺类抗生素β内酰胺酶抑制剂复方制剂临床应用专家共识(2020年版)

3-内酰胺类抗生素B内酰胺酶抑制剂复方制剂临床应用专家共识(2020年版)一、概述革兰阴性菌及少数革兰阳性菌对3 -内酰胺类抗生素耐药的最重要机制是产生各种3 -内酰胺酶。
3 -内酰胺酶抑制剂能够抑制部分3 -内酰胺酶,避免3 -内酰胺类抗生素被水解而失活。
因此,3 -内酰胺类抗生素/ 3-内酰胺酶抑制剂复方制剂(简称3 -内酰胺酶抑制剂复方制剂)是临床治疗产3 -内酰胺酶细菌感染的重要选择。
我国临床使用的3 -内酰胺酶抑制剂复方制剂的种类和规格繁多,临床工作者对该类制剂的特点了解参差不齐,临床不合理使用问题比较突出。
二、主要3-内酰胺酶及产酶菌流行情况3-内酰胺酶是由细菌产生的,能水解3 -内酰胺类抗生素的一大类酶。
3-内酰胺酶种类繁多,有多种分类方法,最主要的分类方法有两种:一、是根据3 -内酰胺酶的底物、生化特性及是否被酶抑制剂所抑制的功能分类法(Bush分类法),其将3 -内酰胺酶分为青霉素酶、广谱酶、超广谱3-内酰胺酶(ESBLs)、头抱菌素酶(AmpC酶)和碳青霉烯酶等;二、是根据3-内酰胺酶末端的氨基酸序列特征的分子生物学分类法(Ambler分类法),将3 -内酰胺酶分为丝氨酸酶(包括A类、C类酶和D类酶)及金属酶(B类酶)。
目前引用较多的是1995年Bush等基于上述二种方法建立的分类方法,2019年Bush等又将该分类表进一步完善和细化(表1)。
其中临床意义最大的是下列三类3 -内酰胺酶:表1常见B-内酰胺酶分类及特点,常见酶抑制剂抑酶活性1、E SBLs主要属2be\2br\2ber 类酶,是由质粒介导的能水解青霉素类、头抱菌素及单环酰胺类等B -内酰胺类抗生素的B -内酰胺酶,其对碳青霉烯类和头霉素类水解能力弱。
ESBLs主要由肠杆菌科细菌产生,以肺炎克雷伯菌、大肠埃希菌、变形杆菌最为常见。
根据编码基因的同源性,ESBLs可分为TEM型、SHV型、CTX-M型、OXA型和其他型共5大类型。
β-内酰胺类抗生素β内酰胺酶抑制剂复方制剂临床应用专家共识(2020版)

β-内酰胺类抗生素β 内酰胺酶抑制剂复方制剂临床应用专家共识( 2020 年版)一、概述革兰阴性菌及少数革兰阳性菌对β-内酰胺类抗生素耐药的最重要机制是产生各种β-内酰胺酶。
β-内酰胺酶抑制剂能够抑制部分β-内酰胺酶,避免β-内酰胺类抗生素被水解而失活。
因此,β-内酰胺类抗生素/β-内酰胺酶抑制剂复方制剂(简称β-内酰胺酶抑制剂复方制剂)是临床治疗产β-内酰胺酶细菌感染的重要选择。
我国临床使用的β-内酰胺酶抑制剂复方制剂的种类和规格繁多,临床工作者对该类制剂的特点了解参差不齐,临床不合理使用问题比较突出。
二、主要β-内酰胺酶及产酶菌流行情况β-内酰胺酶是由细菌产生的,能水解β-内酰胺类抗生素的一大类酶。
β-内酰胺酶种类繁多,有多种分类方法,最主要的分类方法有两种:一、是根据β-内酰胺酶的底物、生化特性及是否被酶抑制剂所抑制的功能分类法( Bush 分类法),其将β-内酰胺酶分为青霉素酶、广谱酶、超广谱β-内酰胺酶( ESBLs)、头孢菌素酶( AmpC 酶)和碳青霉烯酶等;二、是根据β-内酰胺酶末端的氨基酸序列特征的分子生物学分类法(Ambler 分类法),将β-内酰胺酶分为丝氨酸酶(包括 A 类、C 类酶和D 类酶)及金属酶( B 类酶)。
目前引用较多的是 1995 年 Bush 等基于上述二种方法建立的分类方法,2019 年Bush 等又将该分类表进一步完善和细化(表1)。
其中临床意义最大的是下列三类β-内酰胺酶:表 1 常见β-内酰胺酶分类及特点,常见酶抑制剂抑酶活性1、ESBLs 主要属 2be\2br\2ber 类酶,是由质粒介导的能水解青霉素类、头孢菌素及单环酰胺类等β-内酰胺类抗生素的β-内酰胺酶,其对碳青霉烯类和头霉素类水解能力弱。
ESBLs 主要由肠杆菌科细菌产生,以肺炎克雷伯菌、大肠埃希菌、变形杆菌最为常见。
根据编码基因的同源性,ESBLs 可分为 TEM 型、SHV 型、CTX-M 型、OXA 型和其他型共 5 大类型。
β-内酰胺类抗生素β内酰胺酶抑制剂复方制剂临床应用专家共识(2020年版)
β-内酰胺类抗生素β内酰胺酶抑制剂复方制剂临床应用专家共识(2020年版)一、概述革兰阴性菌及少数革兰阳性菌对β-内酰胺类抗生素耐药的最重要机制是产生各种β-内酰胺酶。
β-内酰胺酶抑制剂能够抑制部分β-内酰胺酶,避免β-内酰胺类抗生素被水解而失活。
因此,β-内酰胺类抗生素/β-内酰胺酶抑制剂复方制剂(简称β-内酰胺酶抑制剂复方制剂)是临床治疗产β-内酰胺酶细菌感染的重要选择。
我国临床使用的β-内酰胺酶抑制剂复方制剂的种类和规格繁多,临床工作者对该类制剂的特点了解参差不齐,临床不合理使用问题比较突出。
二、主要β-内酰胺酶及产酶菌流行情况β-内酰胺酶是由细菌产生的,能水解β-内酰胺类抗生素的一大类酶。
β-内酰胺酶种类繁多,有多种分类方法,最主要的分类方法有两种:一、是根据β-内酰胺酶的底物、生化特性及是否被酶抑制剂所抑制的功能分类法(Bush分类法),其将β-内酰胺酶分为青霉素酶、广谱酶、超广谱β-内酰胺酶(ESBLs)、头孢菌素酶(AmpC酶)和碳青霉烯酶等;二、是根据β-内酰胺酶末端的氨基酸序列特征的分子生物学分类法(Ambler分类法),将β-内酰胺酶分为丝氨酸酶(包括A类、C类酶和D 类酶)及金属酶(B类酶)。
目前引用较多的是1995年Bush等基于上述二种方法建立的分类方法,2019年Bush等又将该分类表进一步完善和细化(表1)。
其中临床意义最大的是下列三类β-内酰胺酶:表1 常见β-内酰胺酶分类及特点,常见酶抑制剂抑酶活性1、ESBLs主要属2be\2br\2ber类酶,是由质粒介导的能水解青霉素类、头孢菌素及单环酰胺类等β-内酰胺类抗生素的β-内酰胺酶,其对碳青霉烯类和头霉素类水解能力弱。
ESBLs主要由肠杆菌科细菌产生,以肺炎克雷伯菌、大肠埃希菌、变形杆菌最为常见。
根据编码基因的同源性,ESBLs可分为TEM型、SHV型、CTX-M型、OXA型和其他型共5大类型。
2、AmpC酶属C类酶,通常由染色体介导,可以被β-内酰胺类抗生素诱导。
β-内酰胺酶抑制剂复合制剂
加强药物相互作用研究
提高患者用药依从性
对于与其他药物可能发生相互 作用的情况,医生应加强药物 相互作用的研究,了解具体作 用机制,避免不良反应的发生 。
向患者充分说明用药的重要性 和注意事项,提高患者的用药 依从性,减少不良反应的发生 。
THANKS
感谢观看
加强β-内酰胺酶抑制剂复合制剂耐药性的研 究,为耐药性问题的解决提供科学依据。
06
β-内酰胺酶抑制剂复合制剂的挑战和
解决方案
挑战分析
耐药性
随着时间的推移,细菌对β-内酰胺酶抑制剂复合制剂的耐药性逐 渐增强,导致药物治疗效果下降。
药物相互作用
与其他药物同时使用时,β-内酰胺酶抑制剂复合制剂可能会与其他 药物发生相互作用,影响疗效。
β-内酰胺酶抑制剂复合制 剂
• 引言 • β-内酰胺酶抑制剂复合制剂的种类和
特性 • β-内酰胺酶抑制剂复合制剂的药理作
用和机制 • β-内酰胺酶抑制剂复合制剂的临床应
用和效果
• β-内酰胺酶抑制剂复合制剂的研发进 展和未来展望
• β-内酰胺酶抑制剂复合制剂的挑战和 解决方案
01
引言
背景介绍
新药研发
优化给药方案
随着对β-内酰胺酶抑制剂复合制剂作用机制 的深入了解,未来将会有更多新型的β-内酰 胺酶抑制剂复合制剂进入研发阶段。
针对不同病原体和宿主,优化β-内酰胺酶抑 制剂复合制剂的给药方案,以提高疗效和降 低副作用。
扩大适应症范围
耐药性研究
随着临床应用的不断深入,β-内酰胺酶抑制 剂复合制剂的适应症范围有望进一步扩大。
扩大抗菌谱
通过抑制β-内酰胺酶,β-内酰胺 酶抑制剂复合制剂可以扩大β-内 酰胺类抗生素的抗菌谱,使其对 一些原本耐药的细菌有效。
浅谈β-内酰胺类抗生素与酶抑制剂联用
浅谈β-内酰胺类抗生素与酶抑制剂联用【摘要】随着β-内酰胺类抗生素广泛发展,各种细菌对其耐药性随之增多,由于该类抗生素易被致病菌所产生的β-内酰胺酶水解,产酶耐药菌引起的感染已成为临床急需解决的问题。
解决此类抗生素耐药性的途径之一是通过与β-内酰胺酶抑制剂组方,恢复抗生素原有的抗菌活性和抗菌谱,从而提高其临床疗效。
1 β-内酰胺的结构与作用机制如图:β-内酰胺结构典型—青霉素结构式β-内酰胺能与青霉素结合蛋白(PBPs)结合,能抑制细胞壁粘肽合成酶,从而阻碍细胞壁粘肽合成,使细菌胞壁缺损,菌体膨胀裂解,引起细菌细胞死亡。
2 β-内酰胺类药物的分类与介绍β-内酰胺类药物是指是指氨基在内酰胺环中的β位碳原子上的一类药物。
其分类及抗菌谱见表一表一β-内酰胺类药物的分类介绍及抗菌谱分类代表药物抗菌谱天然青霉素青霉素G G+菌(球菌、杆菌)、G-球菌(脑膜炎球菌)、致病螺旋体(梅毒、钩端、鼠咬热螺旋体)半合成青霉素耐酸青霉素青霉素V 主要用于轻度细菌感染,恢复期的巩固和防止感染复发耐酶青霉素氟氯西林主要用于治疗耐青霉素金黄色葡萄球菌的严重感染,以及呼吸道感染广谱青霉素氨苄西林、羟氨苄西林用于G-杆菌感染,严重者与氨基糖苷类合用抗绿脓杆菌青霉素羧苄西林、美洛西林广谱,对绿脓杆菌作用强,不受病灶脓液影响抗G-杆菌青霉素美西林、替莫西林窄谱,对G-杆菌作用强头孢菌素第1代头孢噻吩、头孢唑啉、头孢氨苄对大多数G+ G-有效,对绿脓杆菌等感染疗效差。
主要用于耐PG的金葡菌感染第2代头孢孟多、头孢呋辛、头孢克洛对G–作用,对β-内酰胺酶稳定性大于1代,对G+菌小于一代,适用于大肠、变形、厌氧菌,肾功能不良、青霉素过敏者感染第3代头孢哌酮、头孢他定、头孢曲松、头孢噻肟对G–作用及对β-内酰胺酶稳定性大于1、2代,对G+小于1、2代,一般不作为一线抗感染药。
主要用于重症G–杆菌感染,危及生命的G–杆菌、绿脓杆菌感染第4代头孢匹罗、头孢吡肟对G+ G-厌氧菌作用及对β-内酰胺酶稳定性大于3代,主要用于耐甲氧西林金黄色葡萄球菌、肺炎球菌、阴沟杆菌、绿脓杆菌等感染其他β-内酰胺类头霉素类头孢西丁、拉氧头孢用于盆腔、腹腔、妇科、需氧厌氧混合感染碳青霉烯类亚胺培南、美罗培南对军团菌、沙眼衣原体、肺炎支原体无效,对其他菌作用强单环β-内酰胺类氨曲南对G-菌、绿脓杆菌作用强大,对G+菌、厌氧菌很弱或无效3 β-内酰胺酶作用机制β-内酰胺酶使β-内酰胺类抗生素开环失活,它通过与β-内酰胺环上的羰基共价结合,水解酰胺键使β-内酰胺类抗生素失活。
抗菌药物的临床应用(II)
第 三 代
头孢噻肟、 1970s末 头孢曲松、 头孢他啶、 头孢哌酮、 头孢地嗪
对G+菌弱于第一、二代头孢菌素, 对G-菌(如铜绿假单胞菌属、沙 雷杆菌属、不动杆菌属、消化球 菌和部分脆弱类杆菌)较第一、二 代头孢菌素强。对肠球菌属和难 辨梭状芽胞杆菌无效,对厌氧菌 作用弱
第 四 代
1980s
对肠杆菌可细菌比头孢噻肟和头 头孢匹罗、 孢他啶强,对铜绿假单胞菌弱于 头孢他啶,对G+球菌如葡萄球菌 头孢吡肟、 属、链球菌属强于第三代头孢菌 头孢克定 素,但对MRSA和厌氧菌作用仍弱。 对产AmpC酶菌(阴沟肠杆菌、弗 劳地枸橼酸菌属、沙雷氏菌属和 铜绿假单胞菌)易产生耐药。对厌 氧菌、MRSA、MRSE和产超广谱 酶(ESBLs)的感染疗效?
1960s
头孢唑林、 对青霉素酶稳定,但可被 G-菌产生的β-内酰胺酶 头孢拉定 破坏,仅适用于产青霉素 酶的金葡菌和少数G-菌。 肾毒性。 1970s中 头孢夫辛、 对G+菌弱于第一代头孢菌 头孢西丁、 素,但部分G-菌(如奈瑟 头孢美唑 菌属、部分吲哚阳性变形 杆菌、部分枸橼酸菌属和 部分肠杆菌属)较第一代头 孢菌素强。
β-内酰胺酶抑制剂
克拉维酸、舒巴坦、他(三)唑巴坦:均属不可 逆竞争性抑制剂和自杀性抑制剂。后两者可透 过血脑屏障 他唑巴坦:对青霉素酶,TEM、OXA、SHV、 PSE等质粒介导及部分染色体介导的I型酶均有 较强的抑制作用。抑酶作用他唑巴坦>克拉维 酸>舒巴坦。 β-内酰胺酶诱导作用:他唑巴坦<克拉维酸<舒 巴坦
第三代口服: 头孢克肟:对肠杆菌科作用在口服头孢菌素中 最强,但弱于环丙沙星。 400mg,qd/150mg,bid。 头孢布烯(先力腾):抗菌谱与头孢噻肟相似, 对绿脓杆菌和大部分厌氧菌无效。 400mg,qd/200mg,bid。 头孢特仑匹酯(托米伦):100mg~200mg,tid
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
(2)不可逆的竞争性抑制剂,既与β-内酰 胺竞争酶的活性部位,又与酶发生不可逆 的化学反应,使酶失去活性,如克拉维酸 、舒巴坦、他唑巴坦等;
(3)非竞争性抑制剂,不与β-内酰胺竞争 酶的催化活性部位,而在远离此部位的适 当部位与酶结合,使酶变态而丧失作用, 如甲氧西林等。
实用文档
• 抑制金黄色葡萄球菌、肺炎链球菌和奇异变形 杆菌所产生的酶。 [3]
• 其特点是能抑制革兰氏阴性菌和葡萄球菌产生 的许多β-内酰胺酶。
• 本身仅有微弱的抗菌活性,能增强青霉素类及 头孢菌素类对许多产β-内酰胺酶微生物的抗菌 活性,减少这些药物的剂量。
• 对摩根杆菌、肠杆菌和铜绿假单胞菌作用差。
实用文档
主要品种
• 哌拉西林+舒巴坦(4:1) • 血、尿及组织浓度高,适用于同时患有多
发疾病预后不良的耐药菌感染。 • 美洛西林+舒巴坦(4:1) • 对严重耐药菌感染的临床疗效与头孢吡肟
相当,在治疗胸腹腔感染、脑膜炎及泌尿 生殖系统感染中显示明显优势。
实用文档
主要品种
• 头孢哌酮+舒巴坦(1:1,4:1) • 能有效分解致病菌β-内酰胺酶,从而增强
实用文档
主要品种
• 替卡西林克拉维酸( 3:1) • 用于产酶肠杆科细菌、铜绿假单胞菌及厌
氧菌等感染; • 阿莫西林克拉维酸钾 • (2:1,4:1,5:1,7:1,10:1,14:1) • 在胃酸中稳定,主要分布在细胞外液,在
尿中的药物浓度较高,对耐氨苄西林和阿 莫西林的产β-内酰胺酶菌株作用较强,主 要用于产酶耐药菌引起的轻中度感染。
• 舒巴坦与克拉维酸的抑酶谱相似,但抑酶 作用稍弱,抗菌活性略强。
• 是金葡菌和多数革兰氏阴性杆菌的强抑制 剂。
实用文档
主要品种
• 氨苄西林+舒巴坦(1:1,2:1) • 两者协同作用使β-内酰胺酶钝化,抗菌效
力增强,常用于产酶金葡菌,流感杆菌、 卡他莫拉菌、产酶肠杆菌、厌氧菌所致各 种感染。 • 阿莫西林+舒巴坦(2:1) • 抑制细菌转肽酶,阻止细菌细胞壁合成过 程中粘肽的交联反应,破坏细胞壁的完整 性,同时促发细菌自溶系统,使菌体崩解
实用文档
主要品种
• 阿莫西林+他唑巴坦(2:1) • 改善抗生素产酶耐药的情况,主要用于治
疗呼吸道感染、尿路感染、皮肤及软组织 感染、淋巴组织感染及关节感染。
实用文档
最新进展—T—he 阿β-l维act巴am坦ase
inhibitor NXL 104 does
• 与酶可逆性共价结合n新ot型in的duβce-内am酰pC胺β酶- 抑 制剂,目前处于Ⅲ期l临ac床tam试as验e e。xpression in
实用文档
Ⅳ型
• Ⅳ型由肠杆菌属产生 • 为染色体介导 • 对β-内酰胺酶抑制剂敏感, • 主要水解底物是青霉素类,部分头孢菌素
。
实用文档
Ⅴ型
• 由肠杆菌属产生,为质粒介导的 • β-内酰胺酶抑制剂对其有效,主要水解底
物是异恶吐青霉素类。
• 注:超广谱酶是质粒介导的β-内酰胺酶。
实用文档
按作用分为三类
胺酶抑制剂对它无效 • 肠杆菌属、不动杆菌属、假单孢菌属、流
感嗜血杆菌属、枸橼酸杆菌及脆弱拟杆菌 产等。
实用文档
Ⅱ型
• 由染色体突变介导 • 主要水解底物是青霉素类 • β-内酰胺酶抑制剂(如:克拉维酸、他唑
巴坦等)对其有效, • 产酶菌为葡萄球菌属、变形杆菌属及假单
孢菌属等。
实用文档
Ⅲ型
• 由肠杆菌属产生,属质粒介导。 • 对β-内酰胺酶抑制剂敏感。 • 水解底物是青霉素类,部分头孢菌素。
实用文档
克拉维酸
实用文档
克拉维酸
• 克拉维酸是从链霉素的代谢产物中分离出 的一种抗生素。抗菌谱广,但活性很弱, 其特点是能抑制革兰氏阴性菌和葡萄球菌 产生的许多β内酰胺酶,是第一个应用于临 床的β内酰胺酶抑制剂。
• 当每一个酶分子被不可逆的钝化,约有115 个克拉维酸分子作为底物被破坏,所以其 抑制酶活性较低.
实用文档
发展历史及进程
1
β-内酰胺酶 抑制剂于 1969年开 始研制
2
克拉维酸是 从链霉菌的 培养液中分 离得到,并 于1977年 完成了全合 成
3
80年代日本 大鹏公司合 成了他唑巴 坦
4
哌拉西林他 唑巴坦上市
1969
1977 1980' 1990
实用文档
实用文档
Ⅰ型
• 主要底物是头孢菌素类 • 由染色体突变介导目前分离合成的β-内酰
实用文档
舒巴坦
实用文档
• 舒巴坦属于青霉烷砜类的β内酰胺酶抑制剂 ,也是第一个人工合成的此类抑制剂。能 与多种β内酰胺类抗生素联合使用,在较低 浓度就可产生明显的协同作用。
• 不可逆的、竞争性β-内酰胺酶抑制剂,通 过竞争β-内酰胺酶的活性部位而发挥抑酶 作用。
实用文档
• 由于舒巴坦抑酶作用随时间延长而增强, 所以也被称为进行性抑制剂。舒巴坦自身 具有一定的抗菌活性,常可单独用于淋球 菌和脑膜炎球菌的周围感染。
• 能抑制革兰阴性菌产生的各种质粒介导的 β-内酰胺酶,对染色体介导的Ⅰ型酶也有 效。
• 能增强对一般革兰氏阴性杆菌的活性,但 不能提高对绿脓杆菌的活性。
实用文档
主要品种
• 哌拉西林+他唑巴坦(4:1,8:1) • 他唑巴坦与哌拉西林有很好的药ห้องสมุดไป่ตู้学同步
性,对产酶菌和厌氧菌其抗菌活性是哌拉 西林的4~8倍,比第三代头孢菌素活性更强 。 [5] • 下呼吸道、泌尿道、腹腔内、皮肤软组织 感染
头孢哌酮对葡萄球菌、假单胞菌、脆弱拟 杆菌的活性。 • 对呼吸道、皮肤软组织及泌尿系统的中重 度感染疗效较好。
实用文档
他唑巴坦
实用文档
• 他唑巴坦是从舒巴坦的衍生物中筛选出来 的高效β内酰胺酶抑制剂。是目前临床效果 最佳的β内酰胺酶抑制剂。
• 弱的抗菌活性,具有毒性低、抑酶活性强 、稳定性好、抑酶谱广等优点。
β内酰胺酶抑制剂的临床应用
实用文档
实用文档
2
β-内酰胺酶抑制剂
• 病原菌质粒传递产生β-内酰胺酶,致使一 些药物β-内酰胺环水解而失活,是病原菌 对一些常见的β-内酰胺类抗生素(青霉素 类、头孢菌素类)耐药的主要方式。
• β-内酰胺酶抑制剂是一类β-内酰胺类药物 ,可与β-内酰胺酶发生牢固的结合而使酶 失活,和其他抗生素联用可增强其抗菌活 性,减少其用量。
