部分酮和醛类溶剂理化特征表
常用77种溶剂的理化性质简表

常用77种溶剂的理化性质简表2007年07月08日星期日下午 02:05溶剂名沸点溶解性毒性*液氨 -33.35℃ 特殊溶解性:能溶解碱金属和碱土金属剧毒性、腐蚀性液态二氧化硫 -10.08 溶解胺、醚、醇苯酚、有机酸、芳香烃、溴、二硫化碳,多数饱和烃不溶剧毒*甲胺 -6.3 是多数有机物和无机物的优良溶剂,液态甲胺与水、醚、苯、丙酮、低级醇混溶,其盐酸盐易溶于水,不溶于醇、醚、酮、氯仿、乙酸乙酯中等毒性,易燃二甲胺 7.4 是有机物和无机物的优良溶剂,溶于水、低级醇、醚、低极性溶剂强烈刺激性石油醚不溶于水,与丙酮、乙醚、乙酸乙酯、苯、氯仿及甲醇以上高级醇混溶与低级烷相似*乙醚 34.6 微溶于水,易溶与盐酸.与醇、醚、石油醚、苯、氯仿等多数有机溶剂混溶麻醉性戊烷 36.1 与乙醇、乙醚等多数有机溶剂混溶低毒性二氯甲烷 39.75 与醇、醚、氯仿、苯、二硫化碳等有机溶剂混溶低毒,麻醉性强*二硫化碳 46.23 微溶于水,与多种有机溶剂混溶麻醉性,强刺激性*溶剂石油脑与乙醇、丙酮、戊醇混溶较其他石油系溶剂大*丙酮 56.12 与水、醇、醚、烃混溶低毒,类乙醇,但较大1,1-二氯乙烷 57.28 与醇、醚等大多数有机溶剂混溶低毒、局部刺激性*氯仿 61.15 与乙醇、乙醚、石油醚、卤代烃、四氯化碳、二硫化碳等混溶中等毒性,强麻醉性*甲醇 64.5 与水、乙醚、醇、酯、卤代烃、苯、酮混溶中等毒性,麻醉性,四氢呋喃 66 优良溶剂,与水混溶,很好的溶解乙醇、乙醚、脂肪烃、芳香烃、氯化烃吸入微毒,经口低毒己烷 68.7 甲醇部分溶解,比乙醇高的醇、醚丙酮、氯仿混溶低毒。
麻醉性,刺激性三氟代乙酸 71.78 与水,乙醇,乙醚,丙酮,苯,四氯化碳,己烷混溶,溶解多种脂肪族,芳香族化合物1,1,1-三氯乙烷 74.0 与丙酮、、甲醇、乙醚、苯、四氯化碳等有机溶剂混溶低毒类溶剂*四氯化碳 76.75 与醇、醚、石油醚、石油脑、冰醋酸、二硫化碳、氯代烃混溶氯代甲烷中,毒性最强*乙酸乙酯 77.112 与醇、醚、氯仿、丙酮、苯等大多数有机溶剂溶解,能溶解某些金属盐低毒,麻醉性*乙醇 78.3 与水、乙醚、氯仿、酯、烃类衍生物等有机溶剂混溶微毒类,麻醉性丁酮 79.64 与丙酮相似,与醇、醚、苯等大多数有机溶剂混溶低毒,毒性强于丙酮*苯 80.10 难溶于水,与甘油、乙二醇、乙醇、氯仿、乙醚、、四氯化碳、二硫化碳、丙酮、甲苯、二甲苯、冰醋酸、脂肪烃等大多有机物混溶强烈毒性*环己烷 80.72 与乙醇、高级醇、醚、丙酮、烃、氯代烃、高级脂肪酸、胺类混溶低毒,中枢抑制作用乙睛 81.60 与水、甲醇、乙酸甲酯、乙酸乙酯、丙酮、醚、氯仿、四氯化碳、氯乙烯及各种不饱和烃混溶,但是不与饱和烃混溶中等毒性,大量吸入蒸气,引起急性中毒异丙醇 82.40 与乙醇、乙醚、氯仿、水混溶微毒,类似乙醇1,2-二氯乙烷 83.48 与乙醇、乙醚、氯仿、四氯化碳等多种有机溶剂混溶高毒性、致癌乙二醇二甲醚 85.2 溶于水,与醇、醚、酮、酯、烃、氯代烃等多种有机溶剂混溶。
醛和酮

β-羟基醛在加热时容易 脱水生成α, β-丌饱和醛:
增长碳链的方法之一。
17
羟醛缩合机理:
18
交叉羟醛缩合(两种丌同醛之间的缩合),产物复杂, 一般无合成意义 醛(无a-H)+ 醛(有a-H)有合成意义
Claisen-Schmidt(克莱森-许密特)反应:
产物为b-位取代的饱和酮
形式上为3, 4-加成(亲核部分总是加在4位)
34
, b-丌饱和醛酮不栺式试剂(RMgX) 1, 4-和 1, 2 -加成
兼有,加成取向不羰基旁烃基体积大小有兲。
100%(1, 2-加成)
100%(1, 4-加成)
35
9.5 醌类化合物
醌的定义:含有共轭环己二烯二酮结构单元的化合物。
CH2CH3 CHO CH2OH OH
沸点/ C
o
CH3
136.1 179.0 205.2 201.8
水溶性:小于或等于4个碳的醛、酮易溶于水。 密度:均小于1。
6
二、化学性质
δ + δ
δ
+
亲核加成 氢化还原
-活泼H的反应
(1)烯醇化
醛的氧化
(2) -卤代(卤仿反应)
(3)羟醛缩合反应
7
(一) 亲核加成反应
小结:
氧化剂
Ag(NH3)2OH
现象应用特点Fra bibliotek丌氧化C=C
温 和
(Tollen’s 试剂) Cu(OH)2/NaOH (Fehling’s 试剂)
有Ag沉淀,银镜 醛类化合物的鉴 反应 定分析;羧酸类 红色Cu2O沉淀 化合物的合成
强
KMnO4, K2Cr2O7,
12醛、酮

H R C O + H+ CN-
H R C OH
CN
氰醇
R' R C O + H+ CN-
R' R C OH
CN
该反应在有机合成中很有用处, 是增长一个碳原 子的重要反应之一。
HCN亲核加成反应的特点
1) 反应是可逆的。加少量碱可大大加速反应, 而加 酸则抑制反应的进行。
HCN
H+ + CN-
酸性条件下反应3-4小时才进行一半,若加入一 滴NaOH溶液则2分钟反应即完成。
C N+H2Y O-
C N+H2Y O-
C NHY -H2O OH
CNY
一些产物及名称 H2N-Y
产物
名称
H2N R (Ar)
H2N OH
H2N NH2 C O+
H2N NH
C N R (Ar) C N OH C N NH2 NO2 C N NH
Schiff base
肟(oxime) 腙(hydrazone) NO2 苯腙(_phenyl
原子上,形成所谓的烯醇式结构:
O CH3CCH3
O H+[ -CH2 C CH3
OCH2 C CH3 ]
OH CH2 C CH3
酮式
共轭碱
烯醇式
[ 烯醇 ] 二种互变异构体,在酸碱催化下
K = [ 醛或酮 ] 迅速达到平衡
通常互变异构体中,烯醇式的比例很小,但在下列 情况下烯醇式的含量大大提高
O
O
O2N H2N NH C NH2
O
O2N C N NH C NH2
O
hydrazone) 缩氨基脲 (semicarbazone)
最全溶剂理化性质参数表

16 甲基异戊基酮(MIAK) METHYL ISOAMYL KETONE 17 乙酸甲基戊酯 18 丙酸正丁酯 19 丙二醇甲醚乙酸酯 20 乙酸戊酯 21 甲基正戊基甲酮 22 异丁酸异丁酯 23 羟乙基乙醚 24 环已酮 25 丙二醇单丁基醚 26 丙二醇单丙基醚 27 乙二醇乙醚乙酸酯 METHYL AMYL ACETATE n-BUTYL PROPIONATE EASTMAN PM ACETATE(PMA) AMYL ACETATE (PRIMARY) METHYL n-AMYL KETONE ISOBUTYL ISOBUTYRATE ETHYLENE GLYCOL ETHYL ETHER CYCLOHEXANONE PROPYLENE GLYCOL TERTIARY BUTYL ETHER PROPYLENE GLYCOL PROPYL ETHER ETHYLENE GLYCOL ETHYL ETHER ACETATE
溶剂参数表
序 号 中文名称 英文全称 CAS NO. 挥发速率 (Evaporation Rate) NBAC=1 Active Solvent a (活性溶剂) 1 四氢呋喃 2 丙酮 3 乙酸甲酯 4 纯乙酸甲酯 5 乙酸乙酯 6 乙酸乙酯99% 7 丁酮 8 乙酸异丙酯 9 甲基正丙酮 10 正乙酸丙酯 TETRAHDROFURAN ACETONE METHYL ACETATE METHYL ACETATE-HIGH PURITY ETHYL ACETATE(85~88%) ETHYL ACETATE(99%) METHYL ETHYL KETONE ISOPROPYL ACETATE METHYL n-PROPYL KETONE n-PROPYL ACETATE 109-99-9 67-64-1 79-20-9 79-20-9 141-78-6 78-93-3 108-21-4 107-87-9 109-60-4 108-10-1 110-19-0 79-46-9 123-86-4 107-98-2 110-12-3 108-84-9 590-01-2 108-65-6 628-63-7 110-43-0 97-85-8 110-80-5 108-94-1 57018-52-7 1569-01-3 111-15-9 6.3 6.3 6.0 6.2 4.2 4.1 3.8 3.0 2.3 2.3 1.6 1.4 1.1 1.0 0.7 0.5 0.5 0.5 0.4 0.4 0.4 0.4 0.3 0.3 0.3 0.2 0.2 1.9 1.9 1.9 1.9 2.9 3.0 3.2 4.0 5.3 5.3 7.6 8.6 11.0 12.1 17.3 24.2 24.2 24.2 30.2 30.2 30.2 30.2 40.3 40.3 40.3 60.5 60.5 OCH2CH2CH2CH2 CH3COCH3 CH3COOCH3 CH3COOCH3 CH3COOC2H5 CH3COOC2H5 CH3COCH2H5 CH3COOCH(CH3)2 CH3COC3H7 CH3COOC3H7 CH3COCH2CH(CH3)2 CH3COOCH2CH(CH3)2 CH3CHNO2CH3 CH3COOC4H9 CH3OCH2CH(CH3)OH CH3COC2H4CH(CH3)2 CH3COOCH(CH3)C4H9 C2H5COOC4H9 CH3COOCH(CH3)CH2OCH3 CH3COOC5H11 CH3COC5H11 (CH3)2CHCOOCH2CH(CH3)2 C2H5OC2H4OH CH2(CH2)2CO C4H9OCH2CH(CH3)OH C3H7OCH2CH(CH3)OH CH3COOC2H4OC2H5 18 7 14 11 17 20 10 22 14 22 19 32 60 30 80 25 54 28 64 40 25 100 73 74 88 95 66 13 8 14 14 15 15 12 17 13 18 15 28 27 28 49 20 0 30 43 31 20 lns 53 77 lns lns 45
《医学化学》 醛和酮

饱和醛酮 不饱和醛酮
脂肪醛酮 按烃基类别分
O
Ar
C
芳香醛酮 O R Ar C
Ar’ Ar
羰基直接连在 芳环上 O
C H
二、命名 (一) 习惯命名法
醛类按分子中碳原子数称某醛(与醇相似)。包含 支链的醛, 支链的位次用希腊字母α,β,γ…表明。
O CH3CHCH2CH2CHO CH3CH CHCH
γ-甲基戊醛 γ-methylpentanal 2-丁烯醛 2-butenal
O R C R'
H OR
+
H OH H NH-NH2 XMg R''
OH RR'C CN OH RR'C SO3Na OH RR'C OR OH RR'C OH OH RR'C NHNH2 OMgX RR'C R''
C=O与C=C在结构上有相似之处,能发生一系列加成反应, 烯烃——亲电加成;羰基——亲核加成
CH3(CH2)3CH(OCH3)2
S的亲核能力比O强, 故硫醇与羰基的加成比醇容易。
R C O R
+
HS HS
H+
R C R
S S
缩硫醛酮很难分解为原来的醛酮, 但可经催化加氢还原 为烃。这是将羰基转变成亚甲基的简便方法。
R C R
S S
Ra(Ni) R H2 R
CH2 + CH3CH3↑ + H2S↑
C O + H2N G (R')H
羰基试剂
R
H+
R (R')H
C
OH NH G
-H2O
R C N G (R')H
有机化学:第十二章 醛和酮

分子量
58
58
58
60
沸点
-0.5
48.8
56.1
97.2
共四十八页
第三节 醛酮的化学性质(huàxuéxìngzhì)
δ δO CC
H
R (H )
酸和亲电试剂进攻富电子的氧 碱和亲核试剂进攻缺电子的碳
涉及醛的反应(氧化反应 ) α H 的反应 羟醛缩合反应
卤代反应
醛酮中的羰基由于π键的极化,使得氧原子上带部分负电荷,碳原子上带部分正电荷。
机理(jī lǐ):
共四十八页
氨的衍生物能与醛、酮起加成反应,用于鉴别羰基的存在,称为羰基 试剂。
常用试剂:2,4-二硝基苯肼
R C
R'
O + H2NNH
NO 2
NO 2
R
-H2O
C
NNH
R'
NO 2
NO 2
黄色(huángsè)结 晶
反应产物用稀酸水解(shuǐjiě),可生成原来的醛、酮。用与分离和提纯醛或酮。
羰基是醛、酮的官能团。
O
R1
R
CO
CO
R2
H
O
羰基化合物广泛存在于自然界,它们既是参与生物代谢过程的重要物质(wùzhì),如甘油
醛
(HOCH2CHOHCHO)和丙酮酸 (HOOCCOCH3)是细胞代谢作用的基本成分,
又是有机合成的重要原料和中间体。
共四十八页
第一节 醛和酮的分类(fēn lèi)和命名
共四十八页
一 、亲核加成反应(jiā chénɡ fǎn yīnɡ)
亲核加成反应是羰基(tānɡ jī)的特征反应,亲核试剂NuA与羰基C=O反应。
有机化工溶剂品种理化特性.
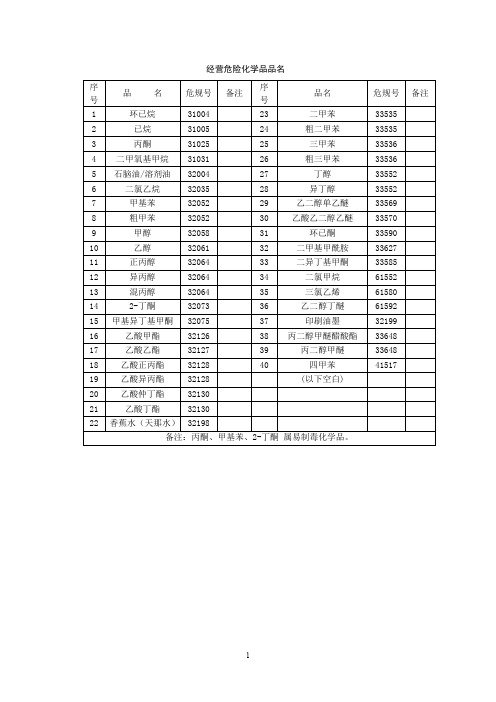
经营危险化学品品名
表1 环己烷理化性质及危险特性
表2 己烷理化性质及危险特性
表3 丙酮理化性质及危险特性
表4 二甲氧基甲烷(甲缩醛)理化性质及危险特性
表5 石脑油理化性质及危险特性
表6 1,1-二氯乙烷理化性质及危险特性
表7 甲基苯理化特性及危险特性
表8 甲醇理化特性及危险特性
表9 乙醇理化特性及危险特性
表10 1-丙醇理化特性及危险特性
表12 2-丁酮理化特性及危险特性
表13 甲基异丁基甲酮理化特性及危险特性
表14 乙酸甲酯理化特性及危险特性
表15 乙酸乙酯理化特性及危险特性
表16 乙酸正丙酯理化性质及危险特性
表17 乙酸异丙酯理化性质及危险特性
表18 乙酸仲丁酯理化特性及危险特性
表19 乙酸丁酯理化特性及危险特性
表20 硝基漆稀释剂理化特性及危险特性
表21 1,2-二甲苯理化性质及危险特性
表22 1,2,4-三甲苯理化性质及危险特性
表23 正丁醇理化性质及危险特性
表24 异丁醇理化性质及危险特性
表26 乙酸乙二醇乙醚理化性质及危险特性
表27 环己酮理化特性及危险特性
表28 N,N-二甲基甲酰胺理化特性及危险特性
表29 二异丁基甲酮理化性质及危险特性
表30 二氯甲烷理化性质及危险特性
表31 三氯乙烯理化性质及危险特性
表32 2-丁氧基二醇理化特性及危险特性。
常见的醛和酮 醛和酮的化学性质

实验现象
有砖红色 沉淀产生
_C_H__3C__H_O__+__2_[_A_g_(_N_H__3)_2]__ C__H_3_C__H_O__+__2_C_u_
△ 化学方程式 _O_H__―__―_→__
△ _(O__H__)2_―__―_→___
_C_H__3C__O_O__N_H__4+ ___2_A_g_↓__+__ C__H_3_C_O__O__H_+__
3_N__H_3_+__H__2O__
_C_u_2_O_↓__+__2_H__2_O__
(2)还原反应:
醛、酮能在铂、镍等催化剂的作用下与 H2 加成,反应的化 学方程式分别为:
催化剂 RCHO+H2 ――→
RCH2OH
;
催化剂 +H2 ――→ ___________。
探究 3 问题探究 问题(1) 如何鉴别醛和酮两种物质? 提示:可用银氨溶液或新制 Cu(OH)2 悬浊液鉴别,前者有银镜 或砖红色沉淀的现象产生。 问题(2) 结合甲醛分子结构特点,甲醛发生银镜反应的化学方 程式是? 提示:甲醛是最简单的醛,通常把它归为饱和一元醛,但它相
△ ――→ RCOONH4 + 3NH3 (OH)2
△ ――→RCOΒιβλιοθήκη H++2Ag↓+H2O
Cu2O↓+2H2O
反应现象
产生光亮银镜
产生砖红色沉淀
R—CHO~2Ag 量的关系
HCHO~4Ag
R—CHO ~ 2Cu(OH)2 ~ Cu2OHCHO~4Cu(OH)2 ~2Cu2O
银镜反应
与新制 Cu(OH)2 悬浊液反应
几种与醛反应的试剂及加成产物如下表:
试剂名称
化学式
δ+ δ- 电荷分布 A—B
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
部分酮类溶剂理化特征表
序号
名称
沸点℃
凝固点
密度爆Biblioteka 极限%溶解性1丙酮
56.05
-94.7
0.7845
2.6~12.8
能与水、乙醇、N,N-二甲基甲酰胺、氯仿、乙醚及大多数油类混溶。
2
丁二酮
88
-4 ~ -2
0.99
有强烈气味的黄绿色油状液体,一体积的丁二酮溶于四体积的水
部分酮类溶剂理化特征表
序号
名称
沸点℃
凝固点
密度
爆炸极限%
溶解性
1
甲醛
-19.5
-118
1.081~1.085
易溶于水和乙醇,35~40%的甲醛水溶液叫做福尔马林
2
乙缩醛
102.7
-100℃
0.83
低闪点易燃液体
溶解性溶于水、乙醇、乙醚
3
糠醛
-38.7
161.7
1.1594
闪点:60℃
微溶于冷水,溶于热水、乙醇、乙醚、苯
