回顾拜耳法和碱石灰烧结法
氧化铝生产3

石或锐钛矿的形态存在。物相鉴定结果表明,TiO2以
钙钛矿的形态(CaO· TiO2)存在于熟料和溶出渣中。 在熟料溶出时,CaO· TiO2基本上不参与反应。在配 制炉料时,CaO的配入量应该同时满足SiO2和TiO2 所需要的CaO量。
5.碱石灰铝土矿炉料烧结过程反应顺序
• 根据炉料在烧结过程中物相组成的变化,碱石灰铝土 矿炉料烧结过程中反应顺序为:
中灰份的数量及其组成。同时也要考虑硫所造成的碱损失,
铁铝比,这样既有利于熟料烧结成块,同时也利于熟 料窑挂窑皮的操作。生产实践经验表明,炉料铁铝比 在0.07~0.10范围较好。
• (3)碱比、钙比 烧结温度随碱比增大而升高,碱比 为0.9左右时,烧成温度范围变得很窄,不好烧结。
烧结温度随钙比升高而降低,但降低不明显。然而炉
料的碱比和钙比是由保证有用成分的最大溶出率来决 定的。
• 熟料经破碎后,用稀碱溶液在球磨机内进行粉碎湿磨溶 出,使有用成分 Na2O 和 Al2O3 转变为铝酸钠溶液,而原 硅酸钙和氧化铁形成固相赤泥,经过沉降分离,得到铝 酸钠溶液,从而达到有用成分与有害杂质分离的目的。 分离后的赤泥需经过热水充分洗涤后才能排弃,目的是
回收赤泥附液中的Na2O和Al2O3。
• 当Na2CO3、A12O3和Fe2O3同时存在时,在低温下 生成Na2O· Fe2O3的反应占优势,随着温度的升高铁
酸钠相对数量降低,而Na2O· Al2O3的数量增加。当
温度升高到900℃,Al2O3能置换Na2O· Fe2O3中的 Fe2O3生成Na2O· Al2O3。在烧结温度范围内此反应 能进行到底: Na2O· Fe2O3+ Al2O3→Na2O· Al2O3+ Fe2O3
SiO2),造成Na2O和Al2O3的损失。
铝的生产过程
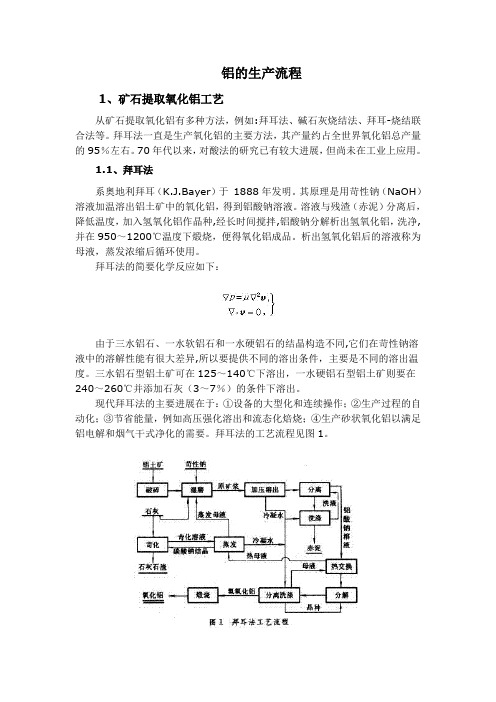
铝的生产流程1、矿石提取氧化铝工艺从矿石提取氧化铝有多种方法,例如:拜耳法、碱石灰烧结法、拜耳-烧结联合法等。
拜耳法一直是生产氧化铝的主要方法,其产量约占全世界氧化铝总产量的95%左右。
70年代以来,对酸法的研究已有较大进展,但尚未在工业上应用。
1.1、拜耳法系奥地利拜耳(K.J.Bayer)于1888年发明。
其原理是用苛性钠(NaOH)溶液加温溶出铝土矿中的氧化铝,得到铝酸钠溶液。
溶液与残渣(赤泥)分离后,降低温度,加入氢氧化铝作晶种,经长时间搅拌,铝酸钠分解析出氢氧化铝,洗净,并在950~1200℃温度下煅烧,便得氧化铝成品。
析出氢氧化铝后的溶液称为母液,蒸发浓缩后循环使用。
拜耳法的简要化学反应如下:由于三水铝石、一水软铝石和一水硬铝石的结晶构造不同,它们在苛性钠溶液中的溶解性能有很大差异,所以要提供不同的溶出条件,主要是不同的溶出温度。
三水铝石型铝土矿可在125~140℃下溶出,一水硬铝石型铝土矿则要在240~260℃并添加石灰(3~7%)的条件下溶出。
现代拜耳法的主要进展在于:①设备的大型化和连续操作;②生产过程的自动化;③节省能量,例如高压强化溶出和流态化焙烧;④生产砂状氧化铝以满足铝电解和烟气干式净化的需要。
拜耳法的工艺流程见图1。
拜耳法的优点主要是流程简单、投资省和能耗较低,最低者每吨氧化铝的能耗仅3×106千卡左右,碱耗一般为100公斤左右(以Na2CO3计)。
拜耳法生产的经济效果决定于铝土矿的质量,主要是矿石中的SiO2含量,通常以矿石的铝硅比,即矿石中的Al2O3与SiO2含量的重量比来表示。
因为在拜耳法的溶出过程中,SiO2转变成方钠石型的水合铝硅酸钠(Na2O·Al2O3·1.7SiO2·nH2O),随同赤泥排出。
矿石中每公斤SiO2大约要造成1公斤Al2O3和0.8公斤NaOH的损失。
铝土矿的铝硅比越低,拜耳法的经济效果越差。
直到70年代后期,拜耳法所处理的铝土矿的铝硅比均大于7~8。
碱石灰烧结法氧化铝生产工艺

分解母液蒸发——从过程中排除过量的水, 蒸发的循环纯碱溶液用以配制生料浆。
熟料烧结
生料的高温煅烧,制取主要含铝酸钠、铁 酸钠和硅酸二钙的熟料。 熟料烧结的最佳温度条件决定于原料的化 学及矿物组成和生了得配料比。我们在实 验室一般在1350摄氏度。 烧结完成后要磨料,磨成一定粒度的熟料。 再做下一步实验。
熟料溶出
溶出是为了使熟料中的铝酸钠转入溶液, 分离和洗涤不溶性残渣(赤泥)。 溶出:称10g熟料和碳酸钠溶液装到三口烧 瓶中,在80度条件的恒温水浴中,搅拌桨 以一定速度搅拌,溶出30min。 成分分析:全碱浓度、苛碱浓度、AO浓度、 吸光度测S
在溶出过程中,由于原硅酸钙引起的二次 反应,在溶出液中有不少的SiO2,使成品氧 化铝的质量低于规范要求。 通过测溶液的吸光度算出其硅含量。 脱硅过程实质就是是其中的SiO2转变成浓 度小的化合物沉淀析出。 脱硅法一:使SiO2成为含水铝硅酸钠析出。 脱硅法二:使SiO2成为水化石榴石析出。
烧结法的原理
用碳酸钠和石灰石按一定比例与铝土矿烧 结,可以很大程度上减轻Si2O的危害,使 Al2O3和Na2O的损失大大减少,这样就形成 了碱石灰烧结法。在处理高硅铝矿是,比 拜耳法优越。 中国现在的铝土矿品味很差,碱石灰烧结 法有很大的应用前景。
烧结法的基本流程
拜耳法生产氧化铝工艺

生产氧化铝工艺流程从矿石提取氧化铝有多种方法,例如:拜耳法、碱石灰烧结法、拜耳•烧结联合法等。
拜耳法一直是生产氧化铝的主要方法,其产量约占全世界氧化铝总产量的95%左右。
70年代以来,对酸法的研究已有较大进展,但尚未在工业上应用。
碱石灰烧结法适用于处理高硅的铝土矿,将铝土矿、碳酸钠和石灰按一定比例混合配料,在回转窑内烧结成由铝酸钠(Na2O • A12O3)、铁酸钠(Na2O • Fe2O3、原硅酸钙(2CaO • SiO2)和钛酸钠(CaO • TiO2 组成的熟料。
然后用稀碱溶液溶出熟料中的铝酸钠。
此时铁酸钠水解得到的NnOH也进入溶液。
如果溶出条件控制适当,原硅酸钙就不会大量地与铝酸钠溶液发生反应,而与钛酸钙、Fe2O3 - H2O等组成赤泥排出。
溶出熟料得到的铝酸钠溶液经过专门的脱硅过程,SQ2O形成水合铝硅酸钠(称为钠硅渣)或水化石榴石3CaO -A12O3 -xSiO2 -(6 -2x)H2O沉淀(其中x~0.1),而使溶液提纯。
把CO2气体通入精制铝酸钠溶液,和加入晶种搅拌,得到氢氧化铝沉淀物和主要成分是碳酸钠的母液。
氢氧化铝经燉烧成为氧化铝成品。
水化石榴石中的A12O3 可以再用含Na2CO3母液提取回收。
碱石灰烧结法的主要化学反应如下:烧结:A12O3+Na2CO3—- Na2O • A12O3+CO2Fe2O3+Na2CO3—- Na2O • Fe2O3+CO2SiO2+2CaCO3—- 2CaO • SiO2+2CO2TiO2+CaCO3—- CaO • TiO2+CO2熟料溶出:Na2O • A12O3+4H2O—- 2NaAl(OH)4 (溶解)Na2O • Fe2O3+2H2O—- Fe2O3 • H2O I +2NaOH (水解)脱硅:1.7 Na2SiO3+2NaAl(OH)4—- Na2O • A12O3 • 1.7SiO2 • nH2O I+3.4NaOH3 Ca(OH)2+2NaAl(OH)4+x Na2SiO3——-3CaO • A12O3 • x SiO2 • (6-2x)H2O ! +2(l+x)NaOH分解:2NaOH+CO2—-Na2CO3+H2ONaAl(OH)4—- A1(OH)3 I +NaOH中国碱石灰烧结法生产氧化铝的主要技术成就是:在熟料烧成中采用低碱比配方,在熟料溶出工艺中采用二段磨料和低分子比溶液,以抑制溶出时的副反应损失,使熟料中Na2O和AI2O3的溶出率分别达到94〜96%和92〜94%。
碱石灰烧结法

碱石灰烧结法
碱石灰烧结法(Calcination with Soda Lime Method)是一种常用的酸雨减排技术,它通过将石灰和苏打混合加热,产生二氧化碳和水蒸气,从而将酸性气体中的二氧化硫(SO2)和氮氧化物(NOx)去除。
碱石灰烧结法的工作原理是将石灰和苏打混合后,加热至约800℃的高温下进行烧结。
在烧结过程中,碱石灰与二氧化硫和氮氧化物反应生成相应的硫酸盐和硝酸盐。
然后通过洗涤和过滤等步骤,将产生的盐类分离出来,从而达到减少酸雨生成物的目的。
碱石灰烧结法相对于其他减排技术的优势在于其成本较低、操作简单,并且能够同时去除二氧化硫和氮氧化物。
然而,该方法也存在一些局限性,例如燃烧热量的损失、操作过程中可能产生的废水等问题。
总之,碱石灰烧结法是一种常用的酸雨减排技术,能够有效去除酸性气体中的二氧化硫和氮氧化物,减少酸雨的生成。
氧化铝生产的基本方法

从矿山胶带输送机送来的铝土矿直接进入预均化堆场,由堆料机纵向分层平铺于堆场,取料机从横向端面取料,以完成铝土矿均化过程。
本工序设置1条均化堆场,采用长条形双料堆,料堆293m,储量为59000t,储存天数为13天。保证堆取料机运行线路的畅通,对堆、取料机每三个月进行一次小修,每六个月进行一次大修。
中 间 状
≤44μm的粒级含量/%
20~50
10
10~20
平均直径/μm
50
80~100
50~80
安息角/(˙)
> 45
30~35
30~40
比表面积/(m2/g)
< 5
>35
>35
密度/(g/m3)
3.90
≤3.70
≤3.70
堆积密度/(g/m3)
0.95
>0.85
0.85>
四、氧化铝厂方案比较
生产规模及产品方案
石灰 铝矿石 石灰石 纯碱
第一赤泥及附液
煤
灰
洗液
洗液
热水
CO2
循环碱液
结晶碳酸钠
硅渣及附液
热水
弃赤泥
蒸汽
晶种及附液
分解母液
热水
洗涤液 热水
成品氢氧化铝
去配料
三、电解炼铝对氧化铝的质量要求
电解炼铝对氧化铝的质量要求:
1)、氧化铝的纯度;
2)、氧化铝的物理性质。
氧化铝的纯度是影响原铝质量的主要因素,同时也影响电解过程的技术经济指标。
1、氧化铝中含有更正电性元素的氧化物Fe2O3、SiO2、TiO2、V2O5等,这些元素在电解过程中将首先在阴极上析出而使铝的质量降低,同时,电解质中含有磷、钒、钛、铁等杂质,还会使电流效率降低。
氧化铝生产流程

氧化铝的生产流程从矿石提取氧化铝有多种方法,例如:拜耳法、碱石灰烧结法、拜耳-烧结联合法等。
拜耳法一直是生产氧化铝的主要方法,其产量约占全世界氧化铝总产量的95%左右。
70年代以来,对酸法的研究已有较大进展,但尚未在工业上应用。
拜耳法系奥地利拜耳(K.J.Bayer)于 1888年发明。
其原理是用苛性钠(NaOH)溶液加温溶出铝土矿中的氧化铝,得到铝酸钠溶液。
溶液与残渣(赤泥)分离后,降低温度,加入氢氧化铝作晶种,经长时间搅拌,铝酸钠分解析出氢氧化铝,洗净,并在950~1200℃温度下煅烧,便得氧化铝成品。
析出氢氧化铝后的溶液称为母液,蒸发浓缩后循环使用。
拜耳法的简要化学反应如下:由于三水铝石、一水软铝石和一水硬铝石的结晶构造不同,它们在苛性钠溶液中的溶解性能有很大差异,所以要提供不同的溶出条件,主要是不同的溶出温度。
三水铝石型铝土矿可在125~140℃下溶出,一水硬铝石型铝土矿则要在240~260℃并添加石灰(3~7%)的条件下溶出。
现代拜耳法的主要进展在于:①设备的大型化和连续操作;②生产过程的自动化;③节省能量,例如高压强化溶出和流态化焙烧;④生产砂状氧化铝以满足铝电解和烟气干式净化的需要。
拜耳法的工艺流程见图1。
拜耳法的优点主要是流程简单、投资省和能耗较低,最低者每吨氧化铝的能耗仅3×106千卡左右,碱耗一般为100公斤左右(以Na2CO3计)。
拜耳法生产的经济效果决定于铝土矿的质量,主要是矿石中的SiO2含量,通常以矿石的铝硅比,即矿石中的Al2O3与SiO2含量的重量比来表示。
因为在拜耳法的溶出过程中,SiO2转变成方钠石型的水合铝硅酸钠(Na2O·Al2O3·1.7SiO2·nH2O),随同赤泥排出。
矿石中每公斤SiO2大约要造成1公斤Al2O3和0.8公斤NaOH的损失。
铝土矿的铝硅比越低,拜耳法的经济效果越差。
直到70年代后期,拜耳法所处理的铝土矿的铝硅比均大于7~8。
拜耳法氧化铝制取工艺(含电解)

氧化铝生产工艺
拜耳法生产氧化铝
烧结法生产氧化铝
拜耳法生产氧化铝
拜耳法生产氧化铝工艺介绍
拜耳法生产氧化铝基本原理 拜耳法生产氧化铝工序
拜耳法生产氧化铝工艺流程
拜耳法生产氧化铝的基本原理
拜耳法生产氧化铝的基本原理是: (l)用NaOH溶液溶出铝土矿,所得到的铝酸钠溶液在添加 晶种、不断搅拌的条件下,溶液中的氧化铝呈氢氧化铝析出, 即种分过程。 (2)分解得到的母液,经蒸发浓缩后在高温下可用来溶出 新的铝土矿,即溶出过程。 交替使用这两个过程,就能够每处理一批矿石便得到一批氢 氧化铝,构成所谓的拜耳法循环。 用反应方程式表示如下: Al2O3(1或3)H2O+2NaOH+aq2NaAl(OH)4+aq
我国铝土矿特点
我国铝土矿资源丰富,储量大;高铝、高硅、
低铁;铝硅比较低,中低品位铝土矿居多; 多数铝土矿是一水硬铝石型铝土矿。
铝酸钠溶液
铝酸钠溶液成分
铝酸钠溶液分子比 铝酸钠溶液结构 铝酸钠溶液诱导期 铝酸钠溶液稳定性及其影响因素
铝酸钠溶液
工业铝酸钠的主要成分是NaAl(OH)4、
拜耳法生产氧化铝工序
原矿浆制备
高压溶出 赤泥分离、洗涤 晶种分解 氢氧化铝分离、洗涤 氢氧化铝焙烧
原矿浆制备
原矿浆制备的工艺流程
矿石破碎 配矿 配碱 配石灰 原矿浆液固比调整 预脱硅
原矿浆制备工艺流程
原矿浆制备的主要设备包括:
带式输送机、球磨机、矿浆磨、螺旋分级机。
铝酸钠溶液诱导期
铝酸钠溶液的诱导期即过饱和铝酸钠溶液自发分解析 出氢氧化铝的时间长短。诱导期即是在开头一段时 间内溶液不发生明显的分解,在此期间溶液主要是 发生内部变化—离子聚合或晶核开始形成。 诱导期的长短取决于溶液的组成(浓度、αK杂质和温 度)等因素。αK和浓度高以及有机物等存在时,诱 导期长。添加晶种时也有诱导期,但诱导期的延续 时间比不添加种子时短得多。以至在晶种量较多时 延续时间只有几分钟甚至完全消失。
- 1、下载文档前请自行甄别文档内容的完整性,平台不提供额外的编辑、内容补充、找答案等附加服务。
- 2、"仅部分预览"的文档,不可在线预览部分如存在完整性等问题,可反馈申请退款(可完整预览的文档不适用该条件!)。
- 3、如文档侵犯您的权益,请联系客服反馈,我们会尽快为您处理(人工客服工作时间:9:00-18:30)。
回顾:拜耳法与碱石灰烧结法
一、原理
拜耳法:K. J. Bayer 1889-1892 提出, 实质为两项专利:
•低温低ακ铝酸钠溶液, 加晶种时AH析出;
•高温高ακ铝酸钠溶液, 铝土矿的溶出。
实质:使下列反应在不同的条件下朝不同方向交替进行
Al2O3(1或3)H2O + 2NaOH + aq 2NaAl(OH)4 + aq
碱石灰烧结法:
1. 高温焙烧把铝土矿中的Al2O3与加入的纯碱Na2CO3反应形成易溶于水或稀碱的固体铝酸钠(Na2O·Al2O3),同时使杂质硅、铁、钛等生成原硅酸钙(2CaO·SiO2)、铁酸钠(Na2O·Fe2O3)、钛酸钙(CaO·TiO2)等。
2. 用调整液溶出熟料中的Na2O与Al2O3,得到铝酸钠溶液,与进入赤泥的原硅酸钙、钛酸钙以及Fe2O3·H2O等不溶性残渣分离。
3. 熟料的溶出液(粗液)进行专门的脱硅净化,脱硅后的精液碳分产出Al2O3。
碳分母液蒸发浓缩后返回配料。
二、流程
拜耳法:四个循环,六个工序
原矿浆制备、高压溶出(循环一)、溶出矿浆稀释和赤泥分离和洗涤(循环二)、晶种分解(循环三)、AH分级与洗涤、AH煅烧、母液蒸发及苛化(循环四)等。
碱石灰烧结法:九个工序,六个比
九个工序:生料浆制备;熟料烧结;熟料溶出;赤泥分离及洗涤;粗液脱硅;精液碳酸化分解;氢氧化铝分离与洗涤;氢氧化铝的煅烧;分解母液蒸发浓缩六个比:碱比(Na2CO3/Al2O3+Fe2O3);钙比(CaO/SiO2);铝硅比(A/S);铁铝比(F/A);生料浆液固比;溶出液固比
三、溶出主要反应
拜耳法:
1.主反应:三水铝石:Al(OH)3 + NaOH + aq = NaAl(OH)4 + aq
一水铝石:AlOOH + NaOH + aq = NaAl(OH)4 + aq
2. SiO2:
溶解:Al2O3·2SiO2·2H2O + 6NaOH + aq → 2NaAl(OH)4 + 2Na2SiO3 + aq
析出: 1.7Na2SiO3 + 2NaAl(OH)4+ aq → Na2O·Al2O3·1.7SiO2·H2O↓+ 3.4NaOH + H2O
①引起Al2O3和Na2O 的损失;
②形成钠硅渣,进入成品AH,影响产品质量;
③钠硅渣在生产设备和管道上,特别是在预热器、压煮器等换热设备表面上
析出成为结疤,使传热系数大大降低,增加能耗和清理工作量。
④大量的硅酸钠大形成增加赤泥量,并且可能成为极分散的细悬浮液,不利
于赤泥的分离和洗涤。
措施:预脱硅
3. 含硫矿物及铁矿
a-FeOOH→ a-Fe2O3 +H2O (针铁矿变为赤铁矿,有利)
2FeCO3+2NaOH → Fe(OH)2+Na2CO3 (菱铁矿反苛化,高度分散的Fe(OH)2) 4Fe(OH)2→ Fe3O4+Fe O+ 3H2O+H2↑(磁铁矿污染铝酸钠溶液)
3FeO + H2O → Fe3O4 +H2↑ (绿泥石,有害)
黄铁矿(硫的存在形态,胶体,污染铝酸钠溶液,降低赤泥沉降性能,有害)
1.反苛化和形成钠的含硫化合物,损失苛性碱,且蒸发时析出钠盐;
2.高度分散的FeO 、FeS和Fe3O4难分离,影响产品质量;沉降性能变坏。
3.不凝性气体增加,导致溶出器有效容积减少;
4.腐蚀设备:
Fe+Na2S2O3+2NaOH →Na2S+Na2SO4+Fe(OH)2
Fe(OH)2+Na2S → Na2[FeS2(OH)2] ·2H2O
措施:控制S含量(拜耳法S%<0.7%);加氧化剂(漂白粉和NaNO3)。
4. TiO2
3TiO2+2NaOH+aq=Na2O·3TiO2·2.5H2O+aq
①与碱反应,导致Na2O损失;
②太酸钠薄膜的形成包裹矿石表面,降低溶出率;
③赤泥沉降性能变差,在加热器表面形成结垢,降低传热效率。
措施:添加石灰使之形成钙钛矿(CaO·TiO2):
2CaO+TiO2+2H2O=2CaO·TiO2·2H2O
由于钛酸钙结晶粗大松脆,易脱落,所以氧化铝溶出不受影响,并且消除了生成钛酸钠所造成的碱损失。
5. 添加石灰(CaO)的作用
矿石中含有少量的CaO,主要来源于工艺流程中添加的石灰。
CaO是拜耳法溶出过程中必须添加的物质,作用为:
添加CaO是消除TiO2的危害有效措施:
2CaO+TiO2+2H2O=2CaO·TiO2·2H2O
避免了钛酸钠的生成,从而消除了TiO2的危害,显著提高氧化铝的溶
出速率和浸出率。
促进针铁矿转变为赤铁矿,使其中的氧化铝充分溶出,并使赤泥沉降性能改善
活化一水硬铝石的溶出反应。
生成水化石榴石,减小氧化钠的损失,降低碱耗。
碱石灰烧结法:
1.NaAlO2+2H2O=NaAl(OH)4(90℃,3~5min,100 g/L S,Nc, Ns,稳定性)
2.2NaFeO2+2H2O=2NaOH+Fe2O3·H2O(低铁,低苛性比值溶出)
3.CA+NaOH→C3AH6+……C12A7+NaOH→C3AH6+……
CA+Na2CO3+aq→2NaAl(OH)4+CaCO3+aq
C12A7+Na2CO3+aq→NaAl(OH)4+CaCO3+NaOH+aq
C3AH6+Na2CO3+aq →NaAl(OH)4+CaCO3+NaOH+aq
4. C2F+aq →C3FH6+Fe(OH)3+aq
CF+NaAl(OH)4+aq →C3AH6+Fe(OH)3+aq
CF+H2O →Ca(OH)2+Fe(OH)3
Ca(OH)2+Fe(OH)3→C3FH1.5+H2O (注:铁酸钙溶出速度<原硅酸钙)二次反应:
1.2CaO·SiO2+1.17H2O= 2CaO·SiO2 · 1.17H2O (致密膜)
2CaO·SiO2 +2Na2CO3+aq=Na2SiO3+2CaCO3↓+2NaOH+aq
2CaO·SiO2+2NaOH+aq=2Ca(OH)2↓+ Na2SiO3 +aq
Ca(OH)2 + Na2SiO3 +a q= 2CaO·SiO2 · H2O (致密膜)
这些反应都不致造成二次反应损失。
1. 3Ca(OH)2+2NaAl(OH)4=3CaO·Al2O3·6H2O+2NaOH
2. 3CaO·Al2O3·6H2O+x Na2SiO3= 3CaO·Al2O3·x SiO2 ·(6-2x)H2O+2x NaOH
(x=0.5~0.8)
3. (2+n)NaAl(OH)4+2Na2SiO3+aq=Na2O·Al2O3 ·2SiO2 ·n Na Al(OH)4 ·x H2O +4Na OH+aq
4. 3Ca(OH)2+2Na Al(OH)4 +x Na2SiO3 +aq=3CaO·Al2O3·x SiO2 ·(6-2x)H2O+
2(1+x)Na OH+aq
- 含水铝硅酸钠和水化石榴石的形成,C2S表面致密膜破坏;
- 反应(4)中x比反应(3)大许多。
二次反应的影响因素和抑制措施
1. 溶出温度:70~80℃,溶出过程是放热的
2. 溶出的苛性比值:低苛性比值(苛性比值为1.20~1.25)溶出
3. 碳酸钠浓度:适当地提高Na2O C浓度
4. 二氧化硅浓度
5. 溶出时间:熟料中有用成分在15 min左右便已溶出完毕,C2S的分解是在这以后才趋于强烈。
我国采用低苛性比值、高Na2CO3浓度,二段湿磨粉碎溶出工艺。
四、赤泥的分离与洗涤
五、铝酸钠溶液的分解
拜耳法:种分(只需予脱硅即可)
NaAl(OH)4+x Al(OH)3(晶种)→(x+1)Al(OH)3+NaOH
碱石灰烧结法:碳分为主(对硅量指数要求高,有专门的脱硅工序),种分为辅六、母液蒸发
拜耳法:母液蒸发后需苛性化返回配料
碱石灰烧结法:直接蒸发浓缩即可返回配料
七、工艺特点
拜耳法:优点:工艺简单,成本低,建设投资少,操作方便,产品质量好。
缺点:对矿石质量要求高,不能处理低品位矿石。
处理一水硬铝石型矿石时,能耗为15~18 GJ/t Al2O3
碱石灰烧结法:优点:能处理低品位矿石
缺点:流程复杂,能耗高达43 GJ/t Al2O3以上,产品质量差。
